Похожие презентации:
Сера. Строение атома, аллотропия, свойства и применение серы
1. Сера. Строение атома, аллотропия, свойства и применение серы.
МОУ СОШ № 12Город Ноябрьск
Учитель химии
Никитина Л.А.
2. Цель:
Определить положение серы впериодической системе химических
элементов Д.И. Менделеева;
Рассмотреть строение атома серы,
физические и химические свойства,
области применения серы.
3. «В древней магии присутствую при рождении огня, называют серой издавна меня»
4. Сера. Строение атома, аллотропия, свойства и применение серы.
5. Положение серы в периодической системе химических элементов Д.И. Менделеева
?Положение серы в
периодической
системе
химических
элементов Д.И.
Менделеева
6.
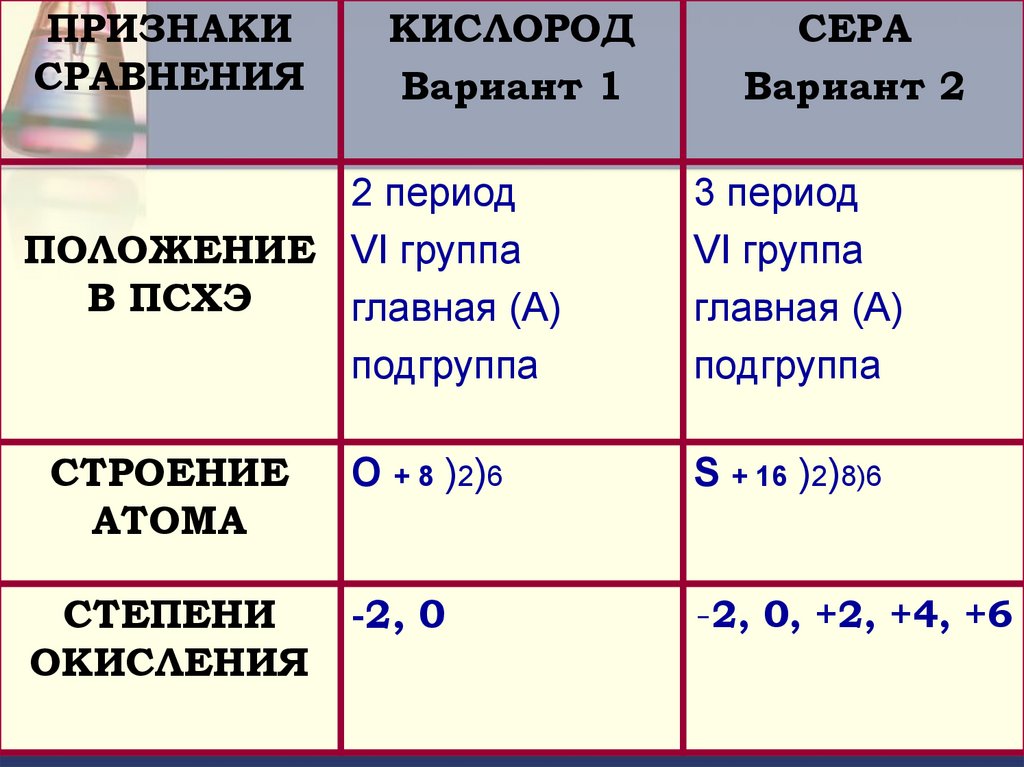
ПРИЗНАКИСРАВНЕНИЯ
КИСЛОРОД
Вариант 1
2 период
ПОЛОЖЕНИЕ VI группа
В ПСХЭ
главная (А)
подгруппа
СТРОЕНИЕ
АТОМА
СТЕПЕНИ
ОКИСЛЕНИЯ
СЕРА
Вариант 2
3 период
VI группа
главная (А)
подгруппа
О + 8 ) 2) 6
S + 16 )2)8)6
-2, 0
-2, 0, +2, +4, +6
7. Валентные состояния атома серы S
Валентность II,ст. окисления -2
3s
3p
3d
↓
↑
Н2S
Валентность IV,
Ст. окисления +4
Валентность VI,
Ст. окисления +6
SО2
Н2SО4
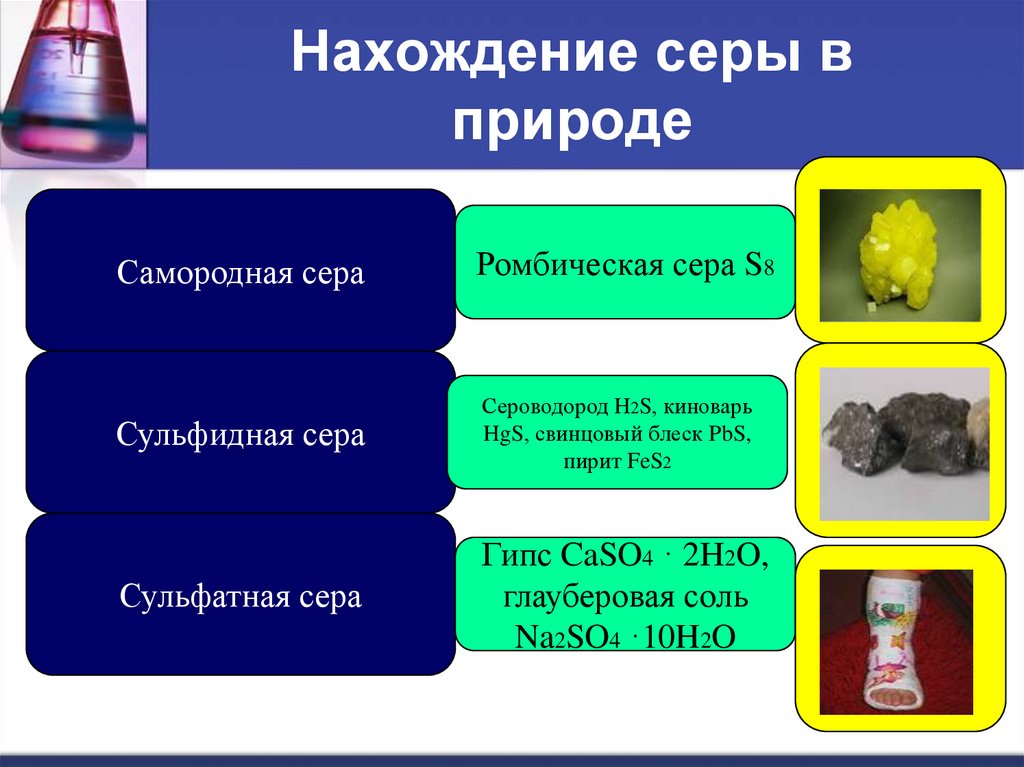
8. Нахождение серы в природе
Самородная сераРомбическая сера S8
Сульфидная сера
Сероводород H2S, киноварь
HgS, свинцовый блеск PbS,
пирит FeS2
Сульфатная сера
Гипс CaSO4 · 2H2O,
глауберовая соль
Na2SO4 ·10H2O
9. Физические свойства серы
Твердоекристаллическое
вещество желтого
цвета,
нерастворима в
воде, водой не
смачивается
(порошок серы в
воде не тонет и
плавает на
поверхности воды)
10.
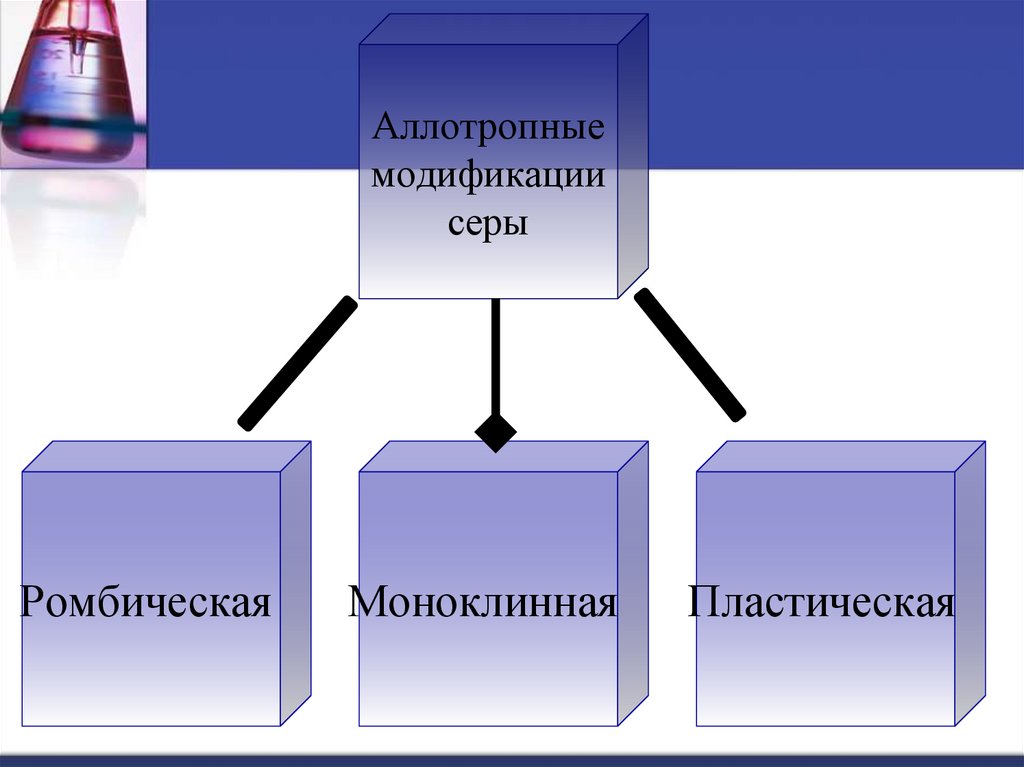
Аллотропныемодификации
серы
Ромбическая
Моноклинная
Пластическая
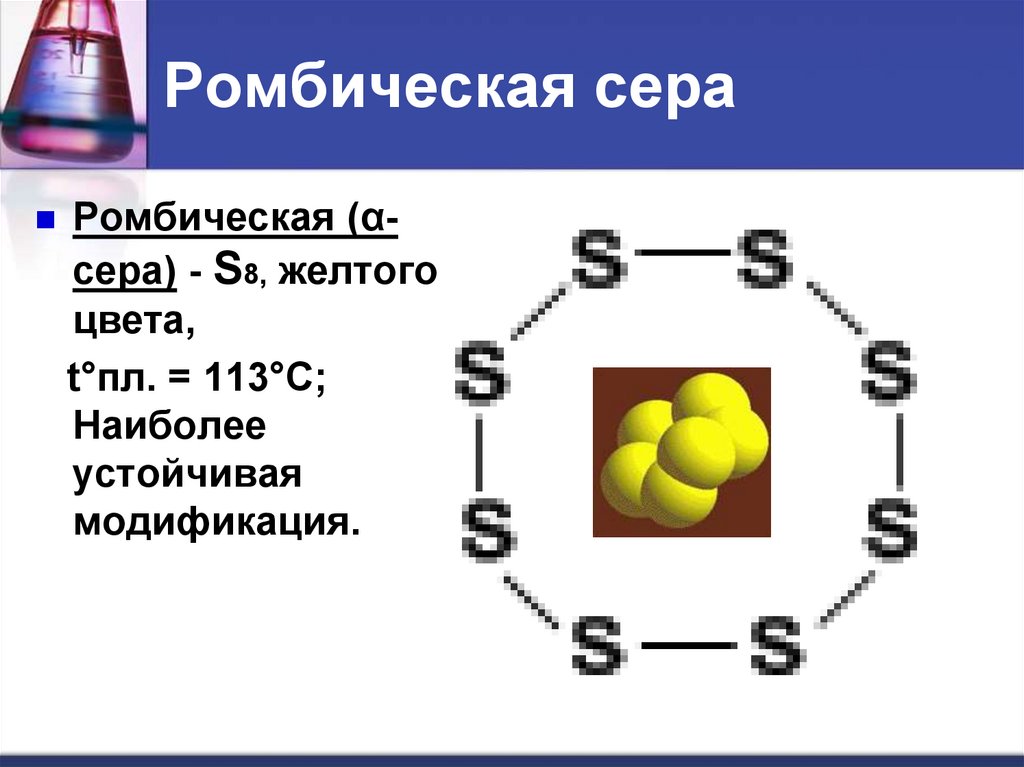
11. Ромбическая сера
Ромбическая (αсера) - S8, желтогоцвета,
t°пл. = 113°C;
Наиболее
устойчивая
модификация.
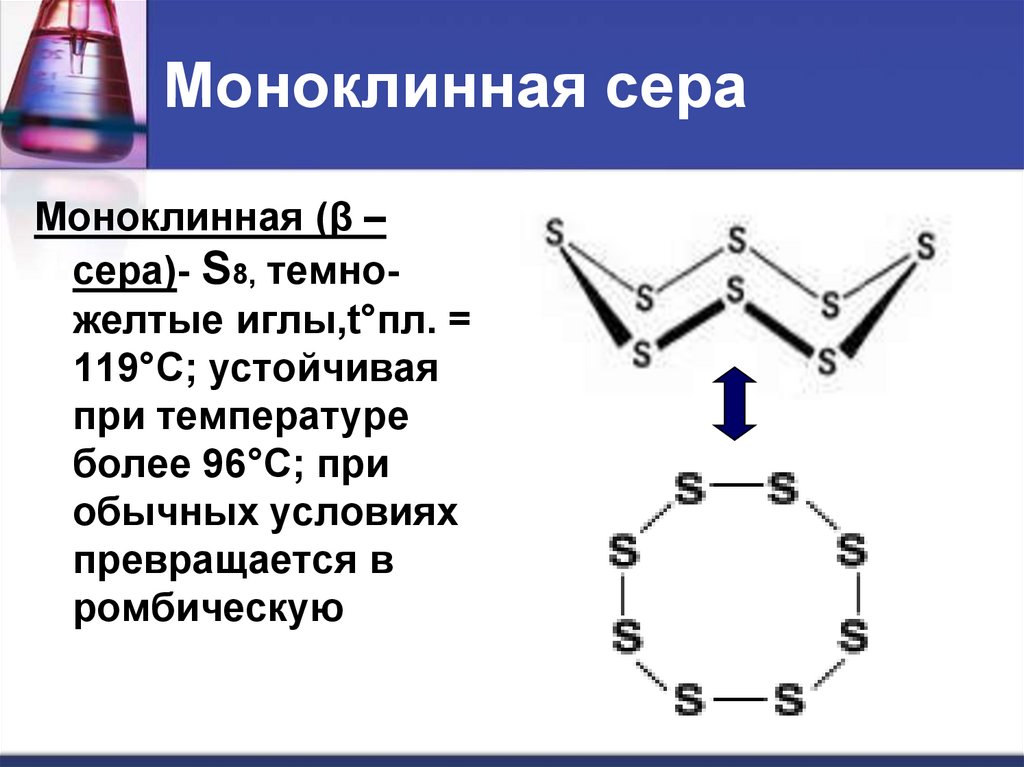
12. Моноклинная сера
Моноклинная (β –сера)- S8, темножелтые иглы,t°пл. =
119°C; устойчивая
при температуре
более 96°С; при
обычных условиях
превращается в
ромбическую
13. Пластическая сера
Пластическая серакоричневаярезиноподобная
(аморфная) масса.
Она неустойчива и
через некоторое
время становится
хрупкой, приобретёт
желтый цвет, т.е
превращается в
ромбическую серу.
14. Химические свойства серы Взаимодействие серы с простыми веществами
Сера реагирует:А) с металлами, образуя сульфиды
Hg + S→ HgS
Б) с неметаллами (водородом,
кислородом, фтором…)
1) H2 + S → H2S
2) S + O2 → SO2
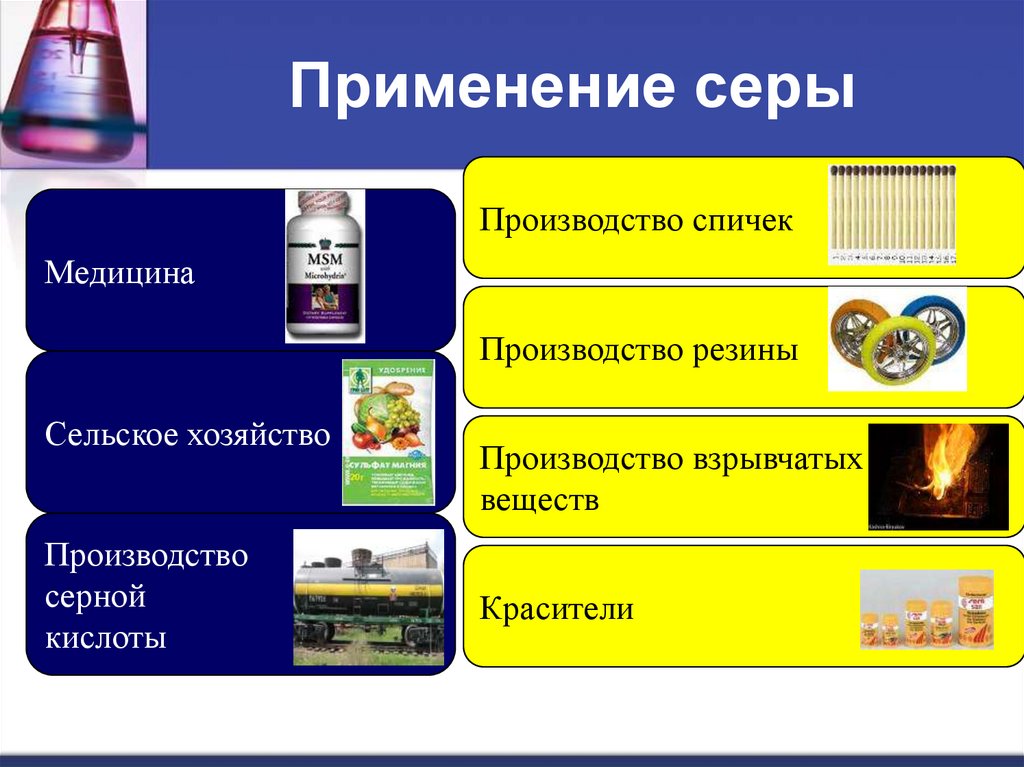
15. Применение серы
Производство спичекМедицина
Производство резины
Сельское хозяйство
Производство
серной
кислоты
Производство взрывчатых
веществ
Красители
16. ОТВЕТЬТЕ НА ВОПРОСЫ:
Охарактеризуйтеположение серы в
периодической системе
химических элементов
Д.И. Менделеева.
17. Выберите правильный ответ:
Вкаком соединении сера
проявляет степень
окисления +4?
А) H2S
Б) H2SO3
В) H2SO4
18. ОТВЕТЬТЕ НА ВОПРОСЫ:
Вкаком виде сера
находится в природе?
19. ОТВЕТЬТЕ НА ВОПРОСЫ:
Охарактеризуйтефизические свойства
серы.
20. Выберите правильный ответ:
Скаким веществом
реагирует сера образуя
сульфид:
А) водой
Б) водородом
В) натрием
21. Домашнее задание
§22, упр. 3















 Химия
Химия








