Похожие презентации:
Практическая работа №7 «Условия протекания химических реакций между растворами электролитов до конца»
1. Практическая работа № 7
«Условия протеканияхимических реакций между
растворами электролитов до
конца»
2. Цель: .
Цель: .Осуществить практически реакции
ионного обмена, выяснить условия
протекания химических реакций
между растворами электролитов до
конца.
3. Оборудование:
пробирки, растворы сульфата меди (II),хлорида калия, сульфата алюминия,
гидроксида натрия, фосфата натрия,
хлорида бария, карбоната натрия,
азотной кислоты, фенолфталеин,
серной и соляной кислот.
4. Ход работы:
Что делали НаблюденияУравнения
реакций. Выводы.
5. Инструкция по технике безопасности:
1. Запрещается использовать посуду,имеющую трещины и отбитые края.
6.
2. Осторожно: кислоты и щёлочи – едкиевещества. Разрушают ткани, раздражают
кожу, слизистые оболочки.
7.
3. После завершения работы тщательнопомыть руки с мылом под проточной водой.
8. Первая помощь
при порезах• Обратиться к лаборанту или учителю (остановить
кровотечение; кожу вокруг раны обработать йодной
настойкой или раствором бриллиантовой зелени;
закрыть стерильной салфеткой, перебинтовать)
при попадании кислоты на кожу рук:
• смыть большим количеством воды
• обработать 2% раствором питьевой соды.
при попадании щёлочи на кожу рук:
• смыть большим количеством воды
• обработать 2% раствором
борной кислоты.
• При необходимости
обратиться в медпункт.
9. Ход работы:
Что делалиНаблюдения
Уравнения реакций.
Выводы.
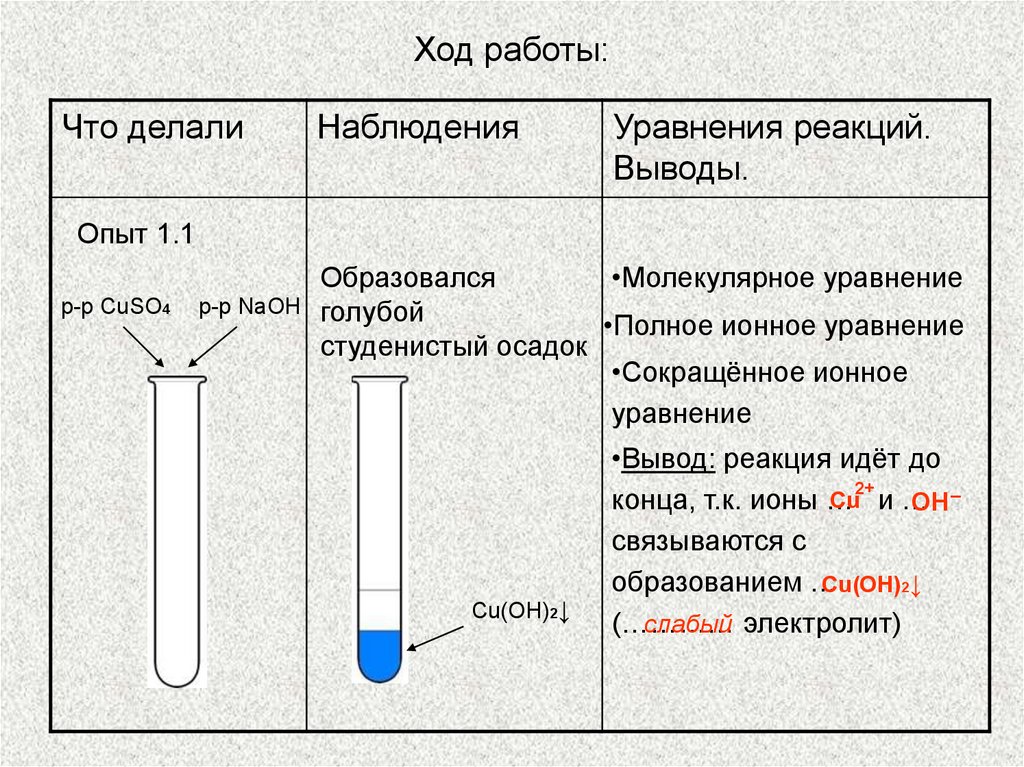
Опыт 1.1
р-р CuSO4
р-р NaOH
Образовался
•Молекулярное уравнение
голубой
•Полное ионное уравнение
студенистый осадок
•Сокращённое ионное
уравнение
Cu(OH)2↓
•Вывод: реакция идёт до
2+
_
Сu и …
конца, т.к. ионы …
ОН
связываются c
образованием …
Cu(OH)2↓
слабый электролит)
(…………
10.
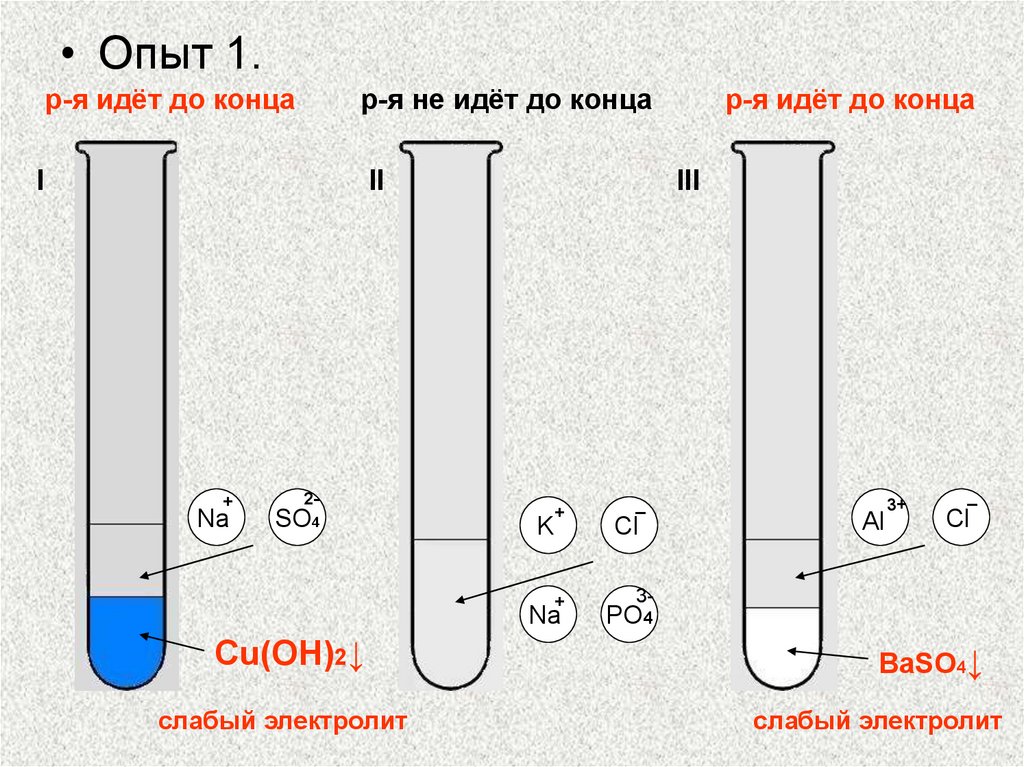
• Опыт 1.р-я идёт до конца
р-я не идёт до конца
I
II
+
Na
III
2-
SO4
K
+
+
Na
Cu(OH)2↓
слабый электролит
р-я идёт до конца
_
Cl
Al
3+
_
Cl
3-
PO4
BaSO4↓
слабый электролит
11. Опыт 2.
р-я идёт до концаCO2↑
+
Na
_
NO3
Н2СО3
H2O
слабый электролит
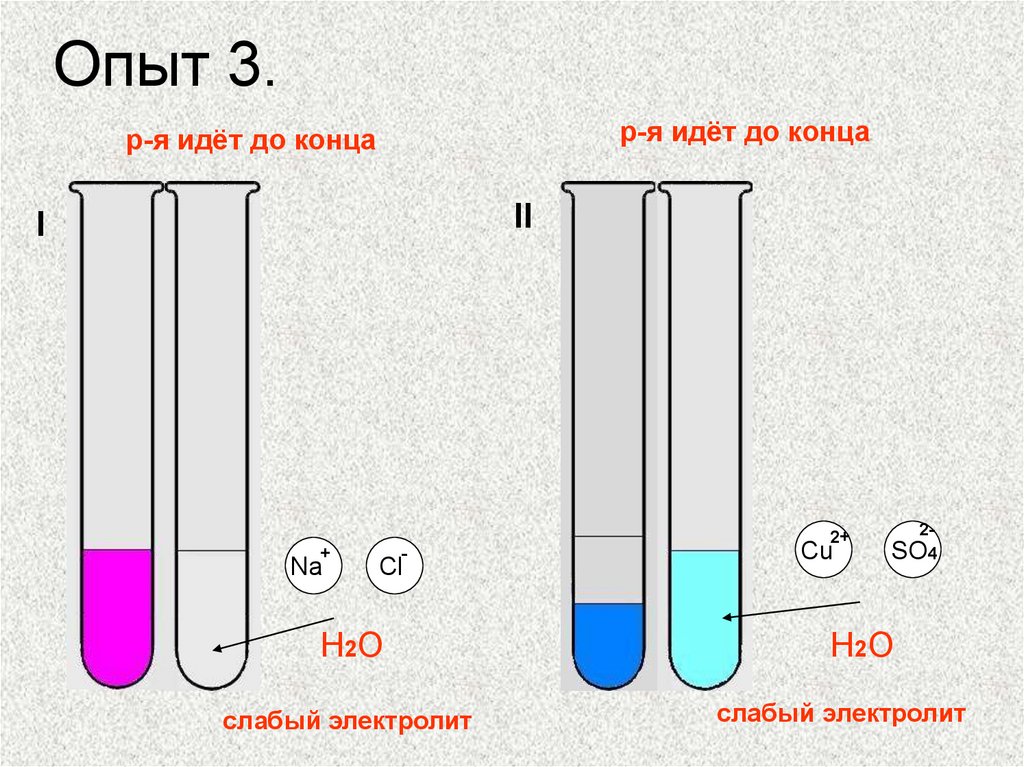
12. Опыт 3.
р-я идёт до концар-я идёт до конца
II
I
2+
+
Na
-
Cl
H2O
слабый электролит
Cu
2SO4
H2O
слабый электролит
13. Вывод:
Реакция ионного обмена протекает доконца при условии, что в растворе
слабого
присутствуют ионы ……….
связываются друг
электролита, которые ……………….
с другом с образованием…
• осадка ↓;
• газа ↑;
• воды.
14. Домашнее задание:
• Повторить §, подготовиться к
проверочной работе.










 Химия
Химия








