Похожие презентации:
Урок-обобщение по теме «Важнейшие классы неорганических соединений»
1. Урок-обобщение по теме «Важнейшие классы неорганических соединений»
2.
Цель урока: закреплениеи углубление изученного
материала, выявление
уровня теоретических
знаний и умений
применять эти знания на
практике.
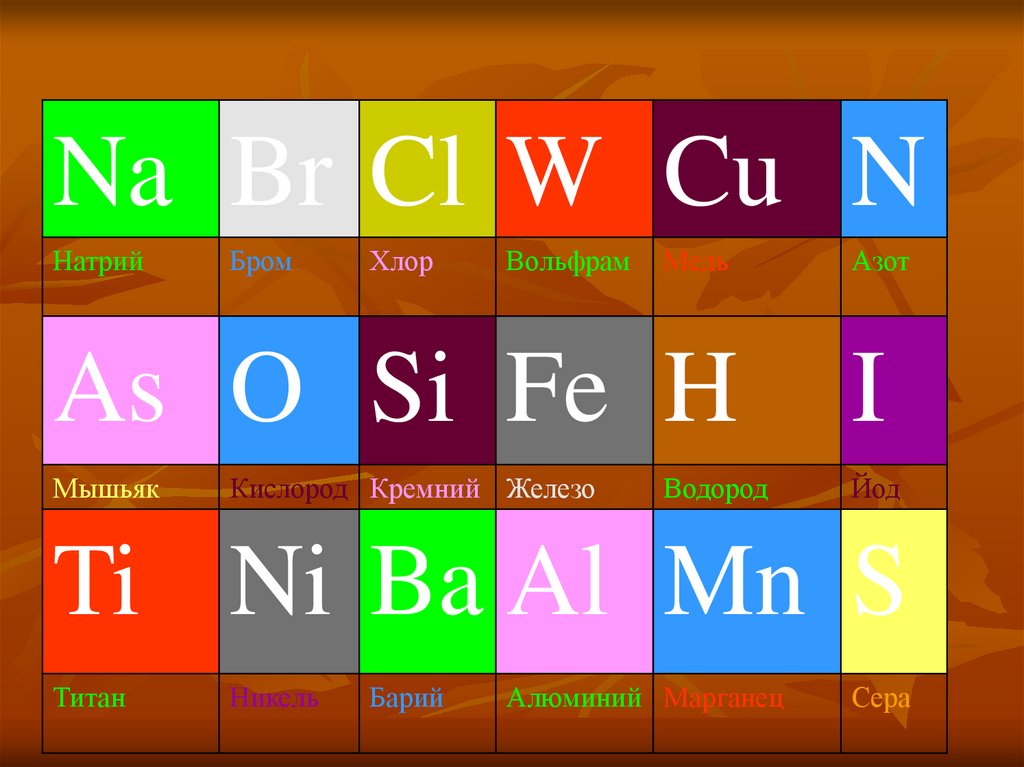
3. I Этап «Химическое лото»
4.
Na Br Cl W Cu NAs O Si Fe H
I
Ti Ni Ba Al Mn S
5.
Na Br Cl W Cu NНатрий
Бром
Хлор
Вольфрам
Медь
Азот
As O Si Fe H
I
Мышьяк
Йод
Кислород Кремний Железо
Водород
Ti Ni Ba Al Mn S
Титан
Никель
Барий
Алюминий Марганец
Сера
6. II Этап «Химическая формула»
Царство формул поразиластрашная болезнь --- раздвоение,
разрушившая формулы на
составные части--- осколки.
Помогите формулам справиться
с этой болезнью, соединив
правильно их осколки.
7.
+3 +4 +1 -2 -1 +2 +3 -2Al2 Ti Na S3 F Ba Al О2
+5 -2 -1 -2 -2 +6 -2 +7
N2 S Cl3 O5 O7 S O3 Mn2
8. Al2O3 TiO2 NaF Al2S3 BaS TiS Mn2O7 AlCl3 N2O5 SO3
Al2O3 TiO2NaF
Al2S3
BaS
TiS Mn2O7
N2O5
SO3
AlCl3
9. IIIЭтап «Классификация веществ»
«В лесу на поляне стояли пять избушек.Хозяевами первой избушки были
металлы, второй ---неметаллы, в
третьей жили оксиды, в четвёртой --кислоты, а по соседству с ними--основания. Пошли вещества в лес
погулять, а когда вернулисьрастерялись, не знают, в какаю избушку
кому заходить. Давайте, ребята,
поможем веществам найти свои дома.»
10.
11.
НеметаллыH2, N2, O2 S
,
12.
Оксиды:CuO, P O ,
CaO , CO
2
5
2
13.
Основания :NaOH, Ca(OH)2,
Cu(OH)2,
KOH
14.
Кислоты :HCl, HNO3,
H2CO3, H2SO4
15.
МеталлыCu, Fe, Zn,
Al
16. IV Этап «Математическая экспертиза»
Решение задач.I вариант.
Какое вещество тяжелее и во сколько раз
CaO, N2?
II вариант.
Какое вещество тяжелее и во сколько раз
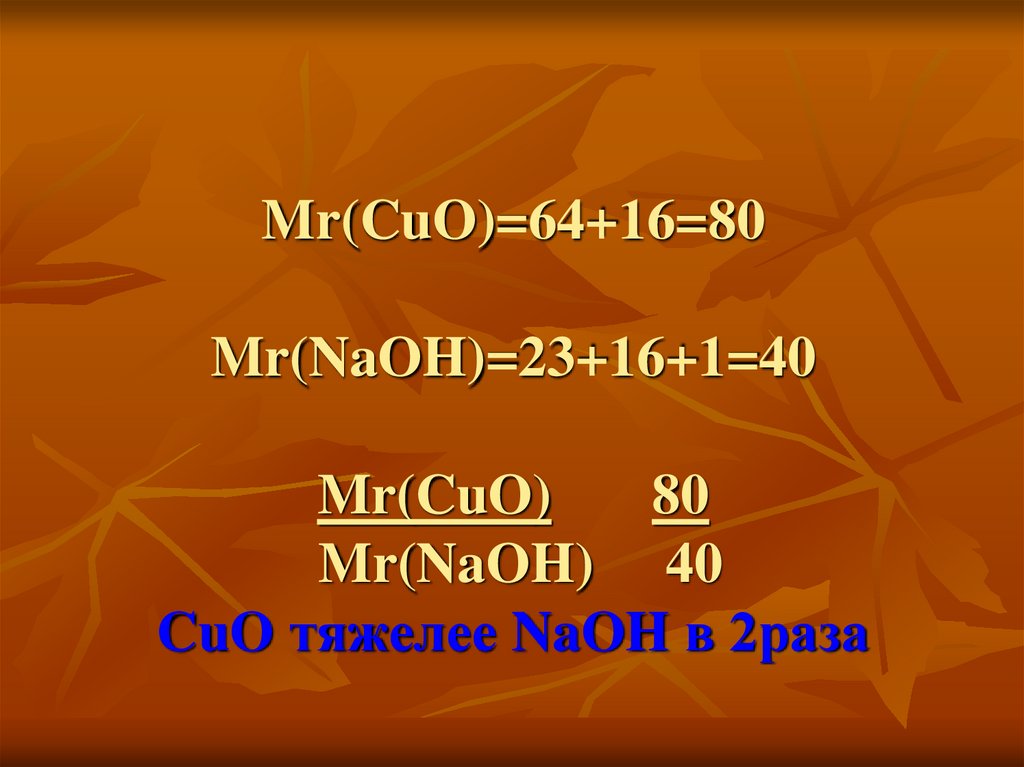
CuO, NaOH ?
17. Mr(CuO)=64+16=80 Mr(NaOH)=23+16+1=40 Mr(CuO) 80 Mr(NaOH) 40 CuO тяжелее NaOH в 2раза
18. Mr (CaO)= 40+16=56 Mr(N2)=28 Mr (CaO) 56 Mr(N2) 28 CaO тяжелее N2 в 2раза.
Mr (CaO)= 40+16=56Mr(N2)=28
Mr (CaO)
Mr(N2)
56
28
CaO тяжелее N2 в 2раза.
19. V Этап «Химическая экспертиза»
Решите экспериментальную задачу:Даны две пробирки с веществами.
Докажите при помощи индикатора, что в
первой пробирке – кислота, а во второй –
щелочь.
20. VI этап «Жизнь моя в опасности без правил безопасности»
«Налив воду в колбу с загрязненной солью, Миша оченьинтенсивно перемешал содержимое стеклянной
палочкой. Затем он поставил колбу на край стола,
приготовил фильтр и вставил его в воронку так, что
фильтр оказался на 1 см. выше края воронки.
Отфильтровал жидкость и весь образовавшийся
прозрачный раствор вылил в чашку для выпаривания.
Затем он зажег спиртовку от соседней спиртовки и
долго нагревал жидкость в нижней части спиртовки.
Как только появились первые кристаллики соли он
поставил зажженную спиртовку на край стола и взял
чашку для выпаривания руками…»
Определите название практической работы и
нарушение правил безопасности, допустимые Мишей.
21.
22.
Cоставила и провела учительхимии Покарева Т.А.
МБОУ «Учхозская средняя
общеобразовательная школа»
Краснослободский район,
Республика Мордовия





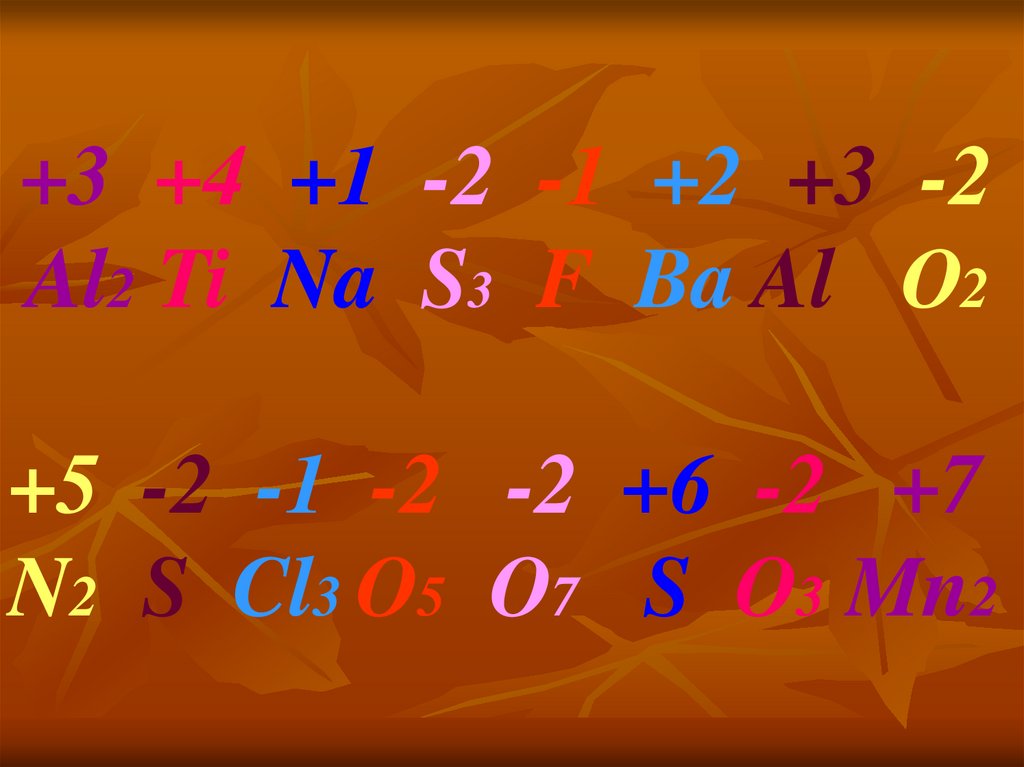














 Химия
Химия








