Похожие презентации:
Игровые технологии на уроках химии в 8-11 классах
1.
Муниципальное бюджетное образовательное учреждение«Средняя общеобразовательная школа № 15»
Презентация
урока
Тема: «ИГРОВЫЕ
ТЕХНОЛОГИИ
НА УРОКАХ ХИМИИ В 8-11 КЛ.»
Подготовила учитель химии
Тлячева Асланхан Беслановна
2. Актуальность введения игровой деятельности в учебный процесс
Побудить интерес к предмету - одна из важных задач каждогоучителя. Экспериментально доказано, что применение разнообразных
форм работы поддерживает активность внимания и снижает
утомляемость. Поэтому различные формы обучения при подаче нового
материала и обобщении знаний учащихся на любой ступени обучения
приобретают все большее значение.
Наиболее интересными являются игровые технологии, которые
опираются на создание в учебном процессе игровых ситуаций.
Познавательные игры - это интерактивный метод, где процесс
образования погружен в процесс общения. При этом активность
обучаемых сравнима или даже превосходит активность преподавателя.
3. Актуальность введения игровой деятельности в учебный процесс
Игра помогает исключить некоторые отрицательные стороны традиционного обучения.Отрицательные стороны традиционного
обучения
Достоинства формы«Элементы игровых
технологий»
Учащиеся изолированы от общения друг с
другом
В работе принимают участие все ученики класса
Пассивность или видимость активности
учащихся
Пассивность невозможна, ученик находится в иной
психологической ситуации ( через интерес
игрового момента выходит на результат)
Слабая речевая деятельность (среднее
время выступления ученика 2 минуты в
день)
При работе с текстом «жужжащее чтение»,
выступление в микрогруппах.
Слабая обратная связь «учитель - ученик»
Работа ученика оценивается непосредственно на
уроке, где делаются замечания по ответам и
даются дополнения ответов; только учитель
отслеживает массу параметров, у него есть свой
набор приёмов, позволяющих чётко
сориентироваться в обстановке
Усреднённый подход учителя к
обучающемуся
Каждый ученик справляется с заданием в меру
своих способностей и знаний
4. Место игрового метода в педагогических технологиях
Слово «технология» происходит от греческих слов techne –искусство, мастерство и logos – учение. Поэтому термин
«педагогическая технология» в буквальном переводе означает
учение о педагогическом искусстве, мастерстве.
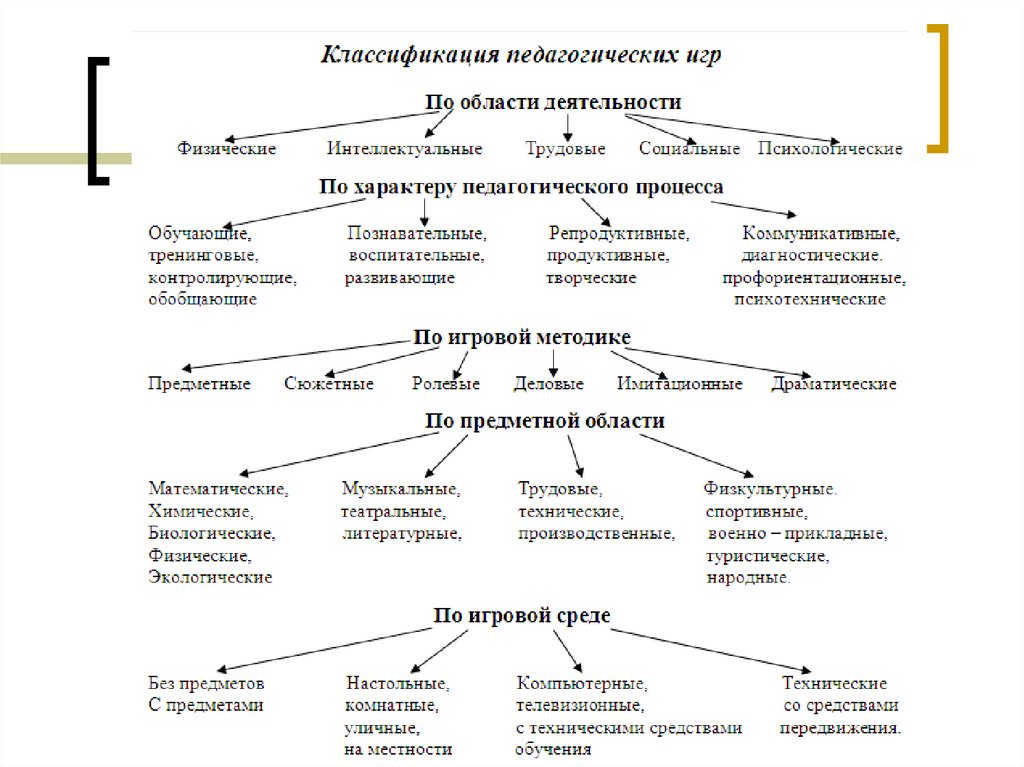
5.
6.
7.
8. Этапы дидактической игры
1. Подготовка к игре, постановка главной задачи,обеспечение учащихся знаниями, необходимыми в игре.
2. Создание игровой ситуации, ознакомление учащихся с
условиями игры, постановка перед ними целей и задач,
которые должны быть решены.
3. Решение учащимися задач в ходе игры. Выводы.
Проверка, коррекция, оценка результатов.
9.
Правила, позволяющие сделать урок увлекательным1. Игра должна приносить радость ученику и учителю.
2. Заинтересованность ученика игрой.
3. Успех вначале работы - обязательное условие.
4. Не переоцениваете уровень развития учащегося.
5. Создайте в игре непринужденную обстановку.
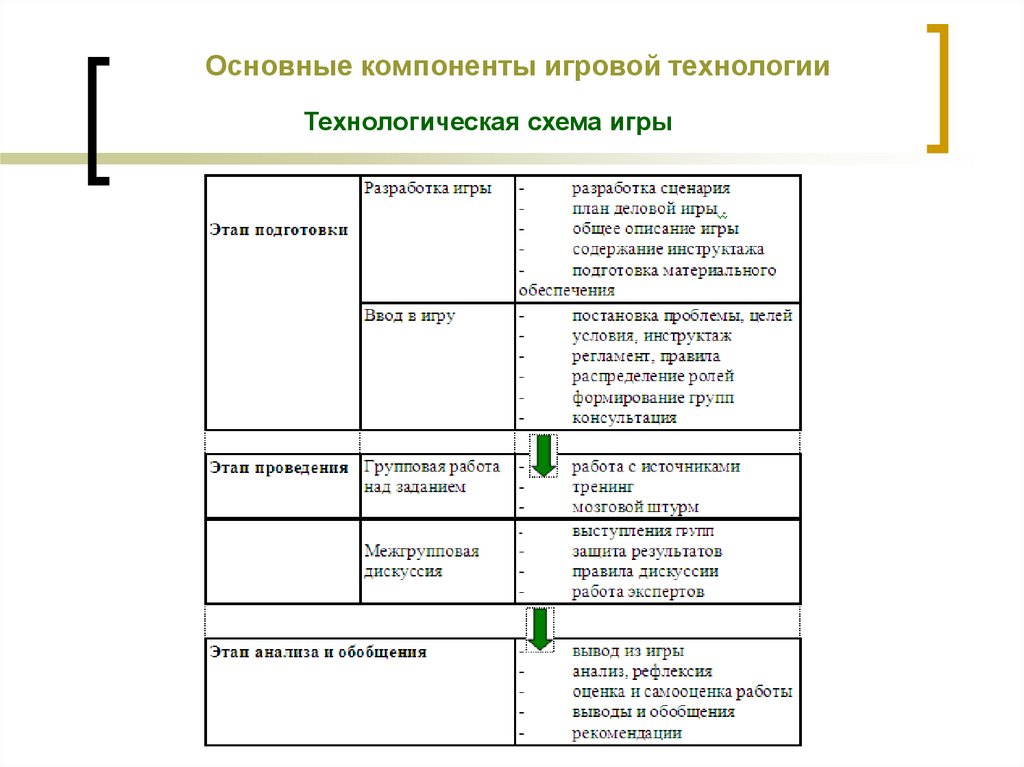
10. Основные компоненты игровой технологии
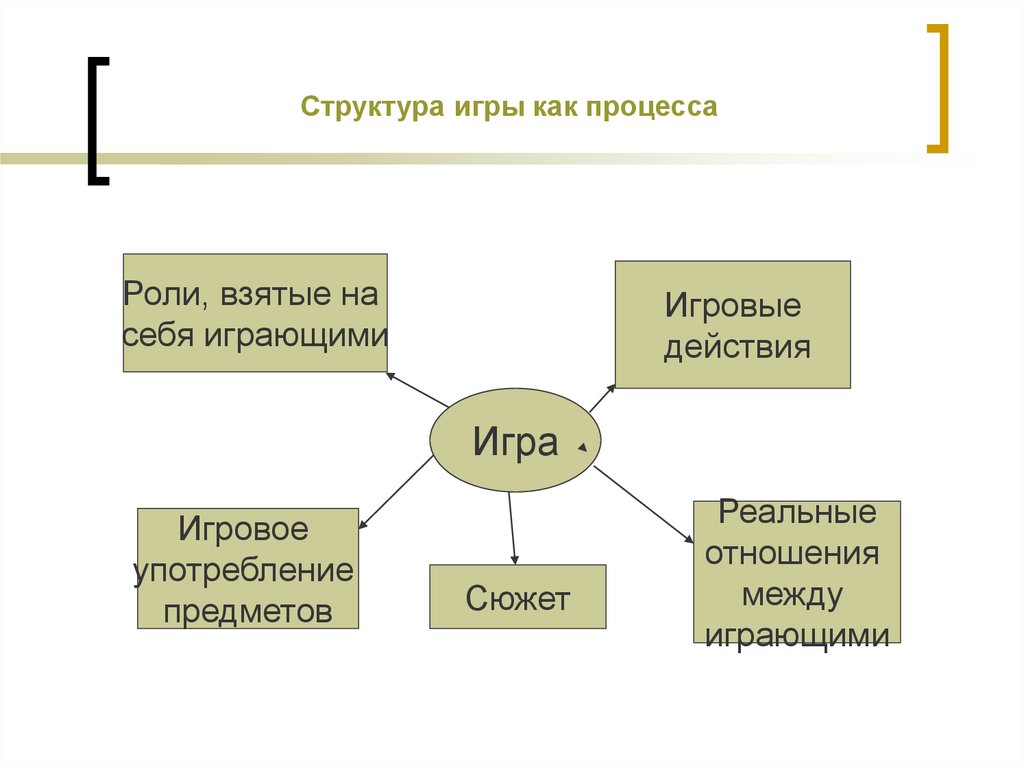
Технологическая схема игры11. Структура игры как процесса
Роли, взятые насебя играющими
Игровые
действия
Игра
Игровое
употребление
предметов
Сюжет
Реальные
отношения
между
играющими
12. Интегрированные игры
Химия и математикаСоставьте формулу оксида алюминия. (25 баллов.) Ответ. Аl20з
Вычислите массовую долю ( в %) кислорода в оксиде серы IV. (50 баллов)
Ответ. 50%
3. Найдите массовые отношения элементов в серной кислоте. (25 баллов)
Ответ. 0,02:4: 0,65
Химия и физика
1. Можно ли заполнить газообразным кислородом полбаллона? (25 баллов)
Ответ. Нет, он распределится по всему баллону.
2. Почему молекулы входящих в состав атмосферы газов, двигаясь во все
стороны, не покидают землю, не улетают в космическое пространство? (50
баллов)
Ответ. Чтобы покинуть Землю, газообразные вещества должны преодолеть
силу земного тяготения. А это возможно лишь в том случае, когда их скорость
будет не менее 11,2 км/с.
3. Подъемная сила водорода больше подъемной силы гелия. Но для
наполнения шаров более удобен гелий. Почему? (25 баллов.)
Ответ. Гелий проще получить.
13. Интегрированные игры
Химия и биология1.С какой целью проводиться рыхление почвы? (25 баллов)
Ответ. В процессе рыхления усиливается доступ кислорода из воздуха
и уменьшается испарение воды из верхнего слоя почвы.
2. Почему под слой почвы в парниках и теплицах закладывают навоз?
(25 баллов)
Ответ. При гниении выделяется теплота, обогревающая почву, и
образуется вещества, необходимые растениям для питания.
3.Почему запрещается пасти скот, собирать грибы и ягоды в зеленой
зоне, прилегающих к автомагистрали? (25 баллов)
Ответ. Автомобильные выхлопы, содержащие оксид углерода (11),
оксиды азота, соединения свинца и другие ядовитые вещества,
накапливаются растениями и могут вызвать отравления человека и
животных.
14. Командные игры
Урок – игра «Русское лото»Условия игры: в игре участвуют пять команд. Каждая команда
получает карточку, в которой указаны номера десяти вопросов. Учитель
или ведущий игры достает из мешка бочонок с номерами. Команда, у
которой в карточке есть этот номер, получает право на ответ. Если ответ
верный, то команда получает бочонок и ставит его на соответствующий
номер в карточке. Если команда не смогла правильно ответить на
вопрос, то бочонок остается у ведущего и право ответа получает другая
команда, которая получает за правильный ответ жетон. За этот жетон
можно выкупить тот бочонок, который был вынут из мешка, но остался у
ведущего. Побеждает та команда, которая первой поставит бочонки на
все номера карточки.
Эту игру можно проводить на уроках обобщающего повторения
или по всему курсу.
15. Игра-лабиринт
16. Ребусы
В этих ребусахзашифрованы
названия химических
элементов
17. Рассказы-загадки
Рассказы-загадки — это задачи и, если хотите, беллетристика. В сюжетрассказа вплетены определенные вопросы, проблемы, ситуации или
задания, которые должен выполнить или решить герой, а вместе с ним и
ученик. Разгадывая рассказ-загадку, следует внимательно читать текст,
так как в нем обычно имеются подсказки, облегчающие выполнение
задания.
Примеры:
1. Дом, который построил М.
2. Чудесная жидкость.
18. Игра-соревнование «Химики - умники и умницы» для учащихся 11-й класс
Игра проводиться по принципу телевизионной игры «Умники и умницы».Всего за мероприятие будет проведено 3 агона (по 3 участника агониста, итого 9), которые выбираются из числа присутствующих теоретиков в ходе викторины.
Теоретики ответившие правильно на максимальное количество вопросов
в предварительной викторине и становятся агонистами.
19.
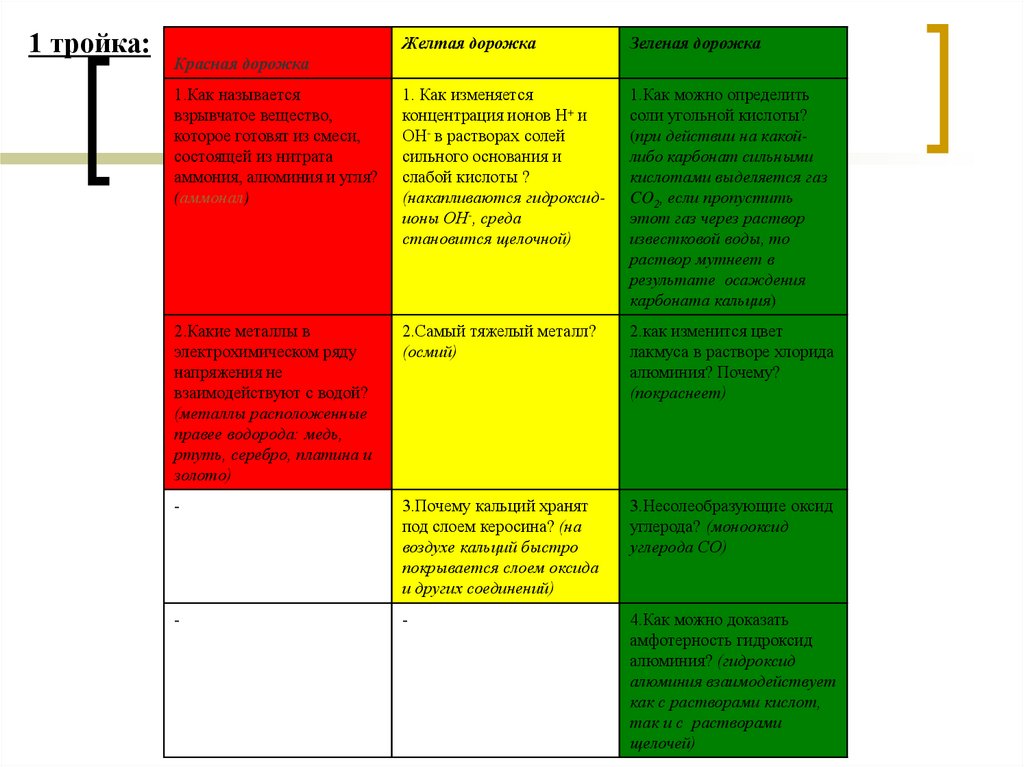
1 тройка:Желтая дорожка
Зеленая дорожка
1.Как называется
взрывчатое вещество,
которое готовят из смеси,
состоящей из нитрата
аммония, алюминия и угля?
(аммонал)
1. Как изменяется
концентрация ионов Н+ и
ОН- в растворах солей
сильного основания и
слабой кислоты ?
(накапливаются гидроксидионы ОН-, среда
становится щелочной)
1.Как можно определить
соли угольной кислоты?
(при действии на какойлибо карбонат сильными
кислотами выделяется газ
CO2, если пропустить
этот газ через раствор
известковой воды, то
раствор мутнеет в
результате осаждения
карбоната кальция)
2.Какие металлы в
электрохимическом ряду
напряжения не
взаимодействуют с водой?
(металлы расположенные
правее водорода: медь,
ртуть, серебро, платина и
золото)
2.Самый тяжелый металл?
(осмий)
2.как изменится цвет
лакмуса в растворе хлорида
алюминия? Почему?
(покраснеет)
-
3.Почему кальций хранят
под слоем керосина? (на
воздухе кальций быстро
покрывается слоем оксида
и других соединений)
3.Несолеобразующие оксид
углерода? (монооксид
углерода СО)
-
-
4.Как можно доказать
амфотерность гидроксид
алюминия? (гидроксид
алюминия взаимодействует
как с растворами кислот,
так и с растворами
щелочей)
Красная дорожка
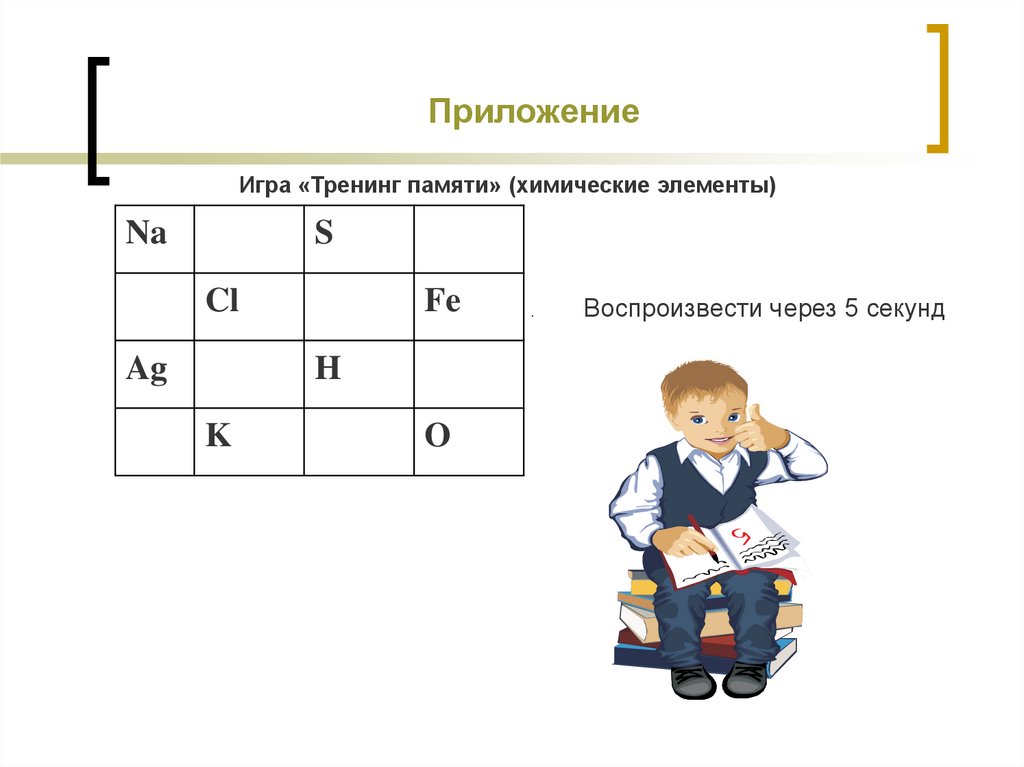
20. Приложение
Игра «Тренинг памяти» (химические элементы)Na
S
Cl
Ag
Fe
H
K
O
.
Воспроизвести через 5 секунд
21. Игра «Крестики - нолики» (8 класс)
При игре в «Крестики - нолики» в горизонтальном, вертикальном илидиагональном направлении следует соединить прямой линией три клетки
по признаку, являющемуся одинаковым для всех веществ, приведённых в
этих клетках. Признак этот указывается в условиях игры.
а) Выигрышный путь – названия металлов
Железо
Кремний
Кальций
Калий
Магний
Углерод
Хлор
Алюминий
Фосфор
б) Выигрышный путь – названия неметаллов
Хлор
Ртуть
Золото
Кремний
Азот
Кислород
Водород
Железо
Никель
22. Игра «Угадай задуманное» (8 класс)
Порядковые номера элементов А, В и С соответственноn , n +2 и n +4. Если химический элемент А – самый лёгкий
галоген, то каким химическим элементом будет В?
Если химический элемент С – благородный газ, а В – металл,
то каким химическим элементом является А?
Могут ли А, В и С в виде простых веществ при обычных
условиях быть газами?
Если химические элементы А и В входят в одну и ту же группу,
то каким химическим элементом является С?
23.
Игра «Третий лишний» (8 класс)Зачеркните лишнее вещество, для двух оставшихся веществ
укажите класс веществ, к которому они относятся.
I Вариант CaO, CO2,KOH | II Вариант HCL, H2SO4, CaO.
Дайте названия всем веществам.
Игра «Химическое домино» (8 класс)
Эту игру использую при изучении составления химических
формул по валентности, а так же при проверке умения
составлять химические формулы по валентности. Играют
по 4-6 человек в группе
24. Игра «Крестики - нолики» (9 класс)
Определить выигрышный путь.а) Реакции, идущие с образование осадка
NaOH + HCL
Na2S + HCL
NaI + AgNO3
Na2SO4 + BaCL2
NaOH + CuCL2
NaCL + AgNO3
MgO + H2O
Cu(OH)2=t
б) Реакции, идущие с образованием газообразного вещества
NaOH + H2SO4
K2SO4 + HCL
CuO + HCL
CaCO3 + H2SO4
AL(OH)3 =t
K2S + HCL
Zn + H2O
ALCL3 + NaOH
Na2SO4 + BaCL2
в) Реакции, идущие с образованием малодиссоциируемого вещества
Cu(OH)2 + HCL
H3PO4 + LiOH
AgNO3 + KCL
H2S + O2
Fe(OH)3 = t
CaO + H2O
CuO + H2SO4
Mg + H2O
KOH + H2SO4
25.
«Пропавшее вещество». Задача на сообразительность.Получая AgCL, лаборант, по несчастью, взял самые неподходящие
реактивы: AgF и MgCL2 (в виде кристаллогидрата MgCL2*6H2O).
Обычно берут AgNO3, но AgF тоже прекрасно растворяется в воде, и
лаборант, по-видимому, это знал. В фильтрате осталась чистая вода.
Почему? (Лаборант не учел, что оба продукта реакции практически не
растворяются в воде).
MgCL2 + 2AgF = MgF2 + 2AgCL
Так как количество взятых веществ точно соответствовало уравнению
реакции , то в фильтрате осталась чистая вода.
26.
ЗаключениеОпыт работы показывает, что в развитии интереса к предмету нельзя
полностью полагаться на содержание изучаемого материала. Сведение
истоков познавательного интереса только к содержательной стороне
материала приводит лишь к ситуативной заинтересованности на уроке.
Если учащиеся не вовлечены в активную деятельность, то любой
содержательный материал вызовет в них созерцательный интерес к
предмету, который не будет являться познавательным интересом.
Желание каждого учителя – привить любовь и интерес к своему
предмету. Каким бы хорошим знанием предмета, высокий эрудицией не
обладал учитель, традиционный урок мало способствует
эмоциональному настроению учащихся на дальнейшее восприятие
учебного материала, активизации их мыслительной деятельности,
развитию и реализации их потенциальных умственных способностей.
Применение системы различных игровых творческих заданий расширяет
горизонт предметного обучения, стимулирует интерес учащихся к
предмету, способствует саморазвитию личности, самоутверждению
подростков. И все это приводит к значительному повышению качества
знаний учащихся
27. Список литературных источников, использованных к уроку
Список использованных литературных источников1. Чернобельская Г.М: Теория и методика обучения химии. М.: Дрофа,
2010.
2. Глинка Н. Л. Общая химия: Учеб. пособие для вузов /Под ред. А.И.
Ермакова. — 30-е изд., испр. — М.: ИНТЕГРАЛ-ПРЕСС, 2005. — 728 с.
3. Колеченко А.К. Энциклопедия педагогических технологий: Пособие
для преподавателей. – СПб.: КАРО, 2008. – 368 с.
4. Штемплер Г.И., Пичугина Г.А. Дидактические игры при обучении химии.
- М.: Дрофа, 2005 г.
5. Белинская Т.В. О развитии познавательного интереса на урокахсоревнованиях // Химия в школе. 2003. № 3. С. 43. .
6. Исаев С.Д. Об использовании дидактических игр // Химия в школе.
2002. № 6. С. 50. .
7. Шукайло А.Д. Тематические игры по химии. Творческий центр
«Сфера», М.: Дрофа, 2003 .
8. Енякова Т.М. Внеклассная работа по химии. – М.:Дрофа, 2004 .
9. Казанцев Ю.Н. Формула успеха, или как увлечь учащихся новым
предметом // Химия в школе. –2009. – № 2. - С. 15-19 .






















 Химия
Химия Педагогика
Педагогика








