Похожие презентации:
Оксидлашу - кайтарылу реакцияләре
1.
Оксидлашу – кайтарылуреакцияләре
Химия, 11 класс
2.
3.
1.CaCO3 → CaO + CO22.KCIO3 + P → P2O5 +KCI
3.H2SO4 +BaCI2 → BaSO4 + HCI
4.
Схема реакции+2 +2 0 0 + -2 + -3 + А) N H4CI +CuO →N2 +Cu +H2O +HCI
0 0
-3 +
Б) N2 +H2 → N H3
+2 -2 0 +4 -2
В) N O +O2 → N O2
+ -2 +
+ +5 -2 ++3 -2
+4 -2
Г) N O2 +NaO H →Na N O3 +NaN O2
А
Б
Степень окисления
1.
+3
2. +2
В
3.
-3
4.
+5
5.
+4
6.
0
Г
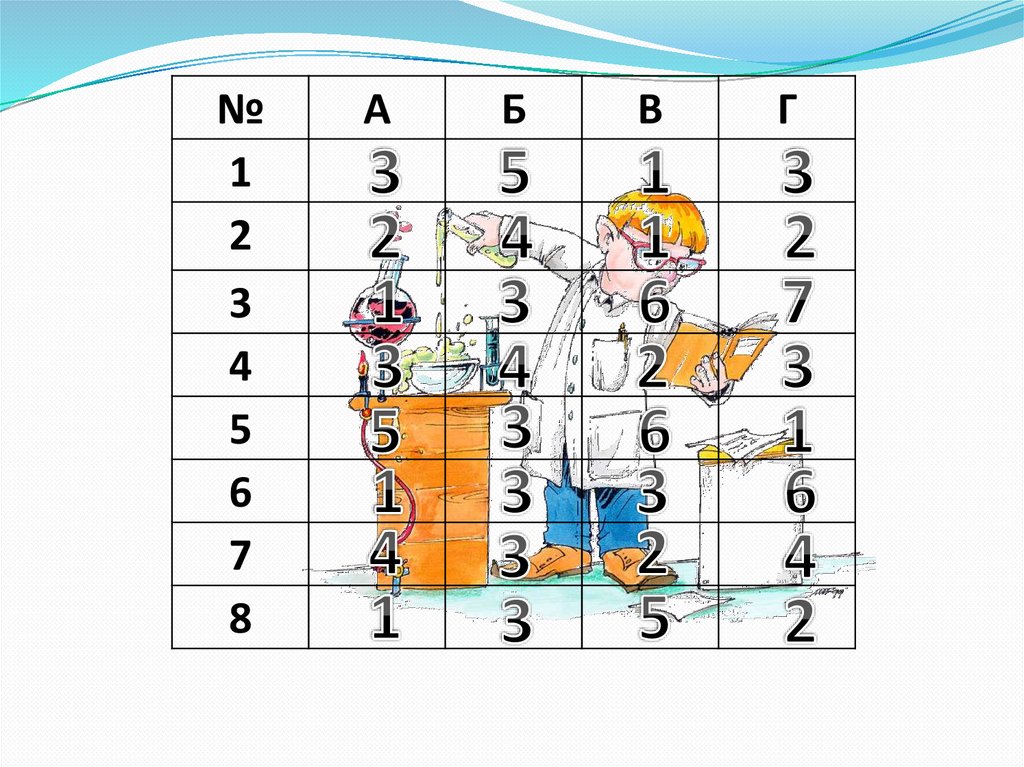
5.
№1
2
3
4
5
6
7
8
A
Б
В
Г
6.
7.
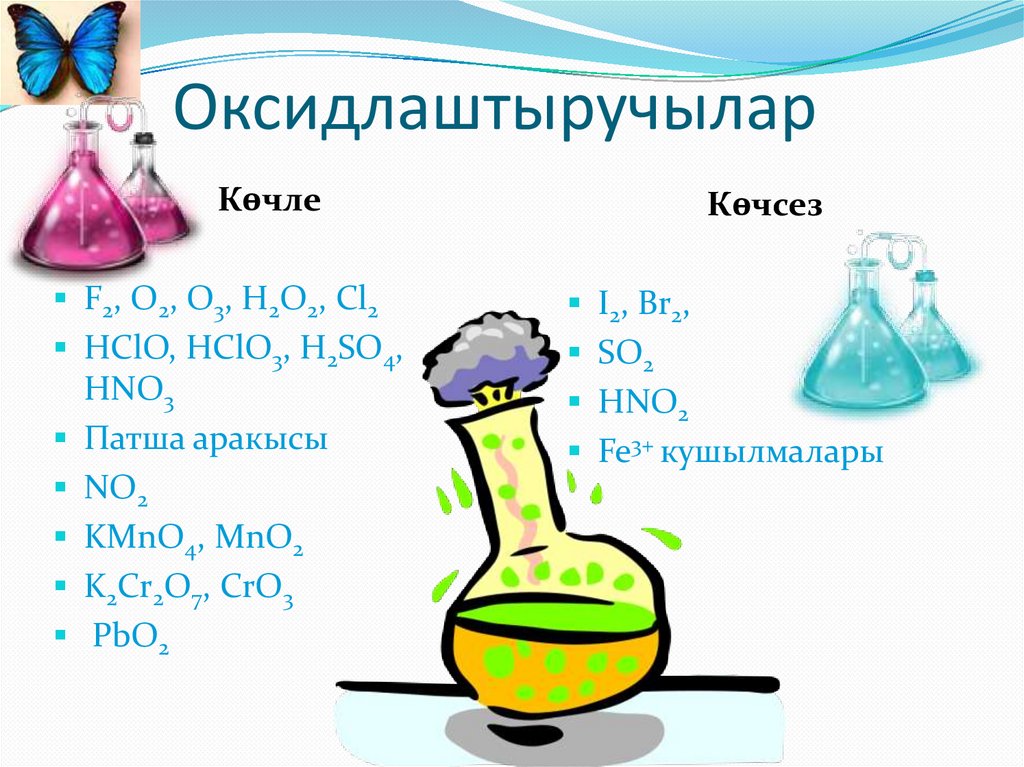
ОксидлаштыручыларКөчле
Көчсез
F2, O2, O3, H2O2, Cl2
I2, Br2,
HClO, HClO3, H2SO4,
SO2
HNO3
Патша аракысы
NO2
KMnO4, MnO2
K2Cr2O7, CrO3
PbO2
HNO2
Fe3+ кушылмалары
8.
КайтаручыларКөчле
Селтеле металлар
Mg, Al, H2
HI и йодидлар
HBr и бромидлар
H2S и сульфидлар
NH3, PH3, H3PO3
C, CO
Fe2+, Cr2+ кушылмалары
Көчсез
Көчсез металлар(Pb, Cu,
Ag, Hg)
HCl
SO2
HNO2
Альдегидлар, спиртлар,
кырмыска кислотасы,
кузгалак кислота,
глюкоза
9.
Оксидлашу – кайтарылу реакцияләретигеләмәләрен төзү
10.
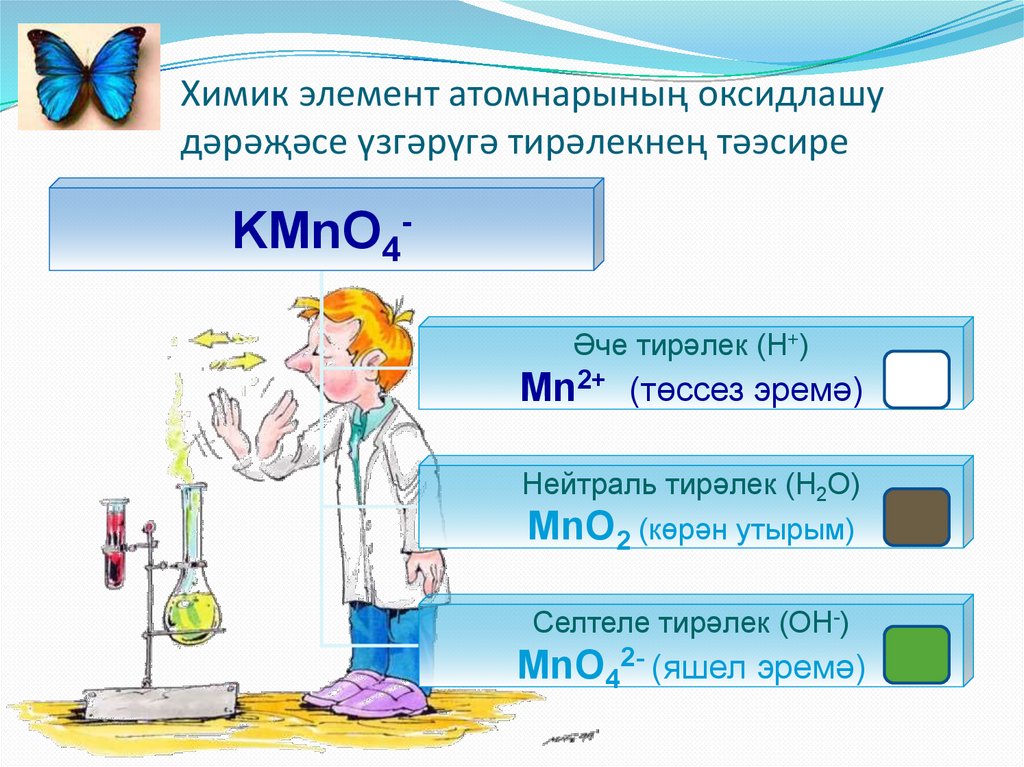
Химик элемент атомнарының оксидлашудәрәҗәсе үзгәрүгә тирәлекнең тәэсире
KMnO4Әче тирәлек (Н+)
Mn2+ (төссез эремә)
Нейтраль тирәлек (Н2О)
MnO2 (көрән утырым)
Селтеле тирәлек (ОН-)
MnO42- (яшел эремә)
11.
Калий перманганатының әче тирәлектә кайтарылуыKMnO4 + KI + H2SO4
Mn+7 + 5e2I-1
- 2e-
MnSO4 + I2 + K2SO4 + H2O
Mn+2 2 кайтарыла оксидлаштыручы
I2 0
5 оксидлаша кайтаручы
Молекуляр тигезләмә:
KMnO4 + KI + H2SO4 = MnSO4 + I2+ K2SO4+ H2O
12.
Калий перманганатының нейтральтирәлектә кайтарылуы
KMnO4 + K2SO3 + H2O
MnO2 + K2SO4 + KOH
Mn+7 + 3e-
Mn+4 2
кайтарыла оксидлаштыручы
S+4 – 2e-
S+6
оксидлаша кайтаручы
3
Молекуляр тигезләмә:
KMnO4 + K2SO3 + H2O = K2SO4 + MnO2 + KOH
13.
Калий перманганатының селтелетирәлектә кайтарылуы
KMnO4 + K2SO3 + KOH
K2MnO4 + K2SO4 +H2O
Mn+7 +1e-
Mn+6 2 кайтарыла оксидлаштыручы
S+4 -2e-
S+6
1 оксидлаша кайтаручы
Молекуляр тигезләмә:
KMnO4 + K2SO3 + KOH = K2MnO4 + K2SO4 + H2O
14.
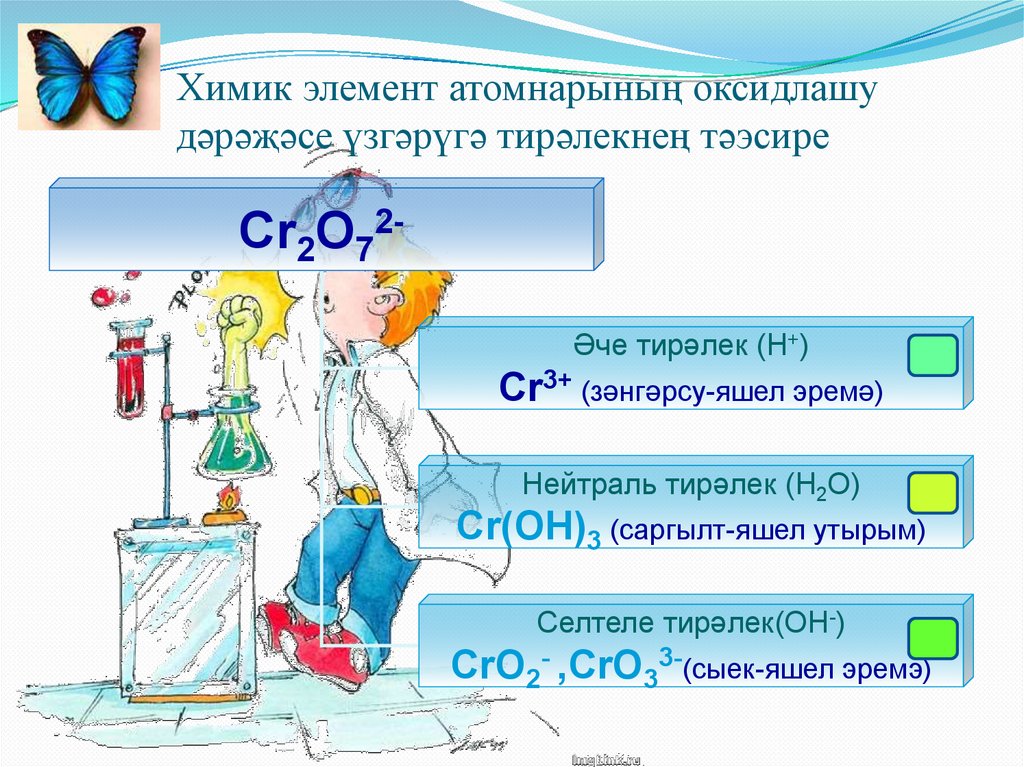
Химик элемент атомнарының оксидлашудәрәҗәсе үзгәрүгә тирәлекнең тәэсире
Cr2O72Әче тирәлек (Н+)
Cr3+ (зәнгәрсу-яшел эремә)
Нейтраль тирәлек (Н2О)
Cr(OH)3 (саргылт-яшел утырым)
Селтеле тирәлек(ОН-)
CrO2- ,CrO33-(сыек-яшел эремэ)
15.
Калий дихроматының әче тирәлектә кайтарылуыK2Cr2O7 + FeSO4 +H2SO4
Fe2(SO4)3 + K2SO4 + Cr2(SO4)3 + H2O
2Cr+6 + 6e
Cr+32 1 кайтарыла
оксидлаштыручы
Fe+2
Fe+3
кайтаручы
-1e
6 оксидлаша
Молекуляр тигезләмә:
K2Cr2O7 + FeSO4+ H2SO4 → Fe2(SO4)3 +K2SO4+Cr2(SO4)3+ H2O
16.
Хром селтеле тирәлектә оксидлашаKCr O2 + Br2 +KOH
Cr+3 -3e
Cr+6
Br02 +2e
2Br-
K2CrO4 + KBr + H2O
2 оксидлаша
3 кайтарыла
кайтаручы
оксидлаштыручы
Молекуляр тигезләмә:
KCrO2 + Br2 + KOH →
K2CrO4 + KBr+ H2O
17.
Калий хроматының нейтраль тирәлектә кайтарылуыK 2CrO4 +H2S +H2O
Cr+6 +3e
S-2
-2e
Cr+3
S0
2
3
Cr(OH)3 +S +KOH
кайтарыла оксидлаштыручы
оксидлаша кайтаручы
Молекуляр тигезләмә:
K2CrO4 + H2S + H2O → Cr(OH)3 + S +
KOH
18.
Галогеннарнын кислородлы кислоталары һәм аларныңтозлары галогеноводородларга яки металл галогенидларына
кадәр кайтарыла.
KCIO3 +KOH +MnO2
CI+5 +6e
Mn+4 -2e
CIMn+6
K2MnO4 + KCI +H2O
1 кайтарыла оксидлаштыручы
3 оксидлаша кайтаручы
Молекуляр тигезләмә:
KCIO3 + KOH+ MnO2 → K2MnO4 + KCI +
H2O
19.
Галогенид – ионнар (CI-,Br-,I-) һәрвакыт кайтаручылар гынабула,һәм алар галогенга кадәр оксидлаша
HBr+H2SO4
2Br- -2e
S+6 +2e
Br02
S+4
Br2 +SO2 + H2O
оксидлаша кайтаручы
кайтарыла оксидлаштыручы
Молекуляр тигезләмә:
HBr +H2SO4 → Br2 +SO2+ H2O
20.
PbS + H2O2 → PbSO4 +H2OS-2
-8e
O2-1 +2e
S+6 1 оксидлаша кайтаручы
2O-2 4 кайтарыла оксидлаштыручы
Молекуляр тигезләмә:
PbS + H2O2 → PbSO4+ H2O
21.
KMn O4 +H2O2 +H2SO4 → Mn SO4 +K2SO4 +O 2 + H2OMn+7
+5e
Mn+2 2 кайтарыла оксидлаштыручы
2O-1
-2e
O02
5 оксидлаша кайтаручы
Молекуляр тигезләмә:
KMnO4 + H2O2 + H2SO4 → MnSO4 +K2SO4 + O2 + H2O
22.
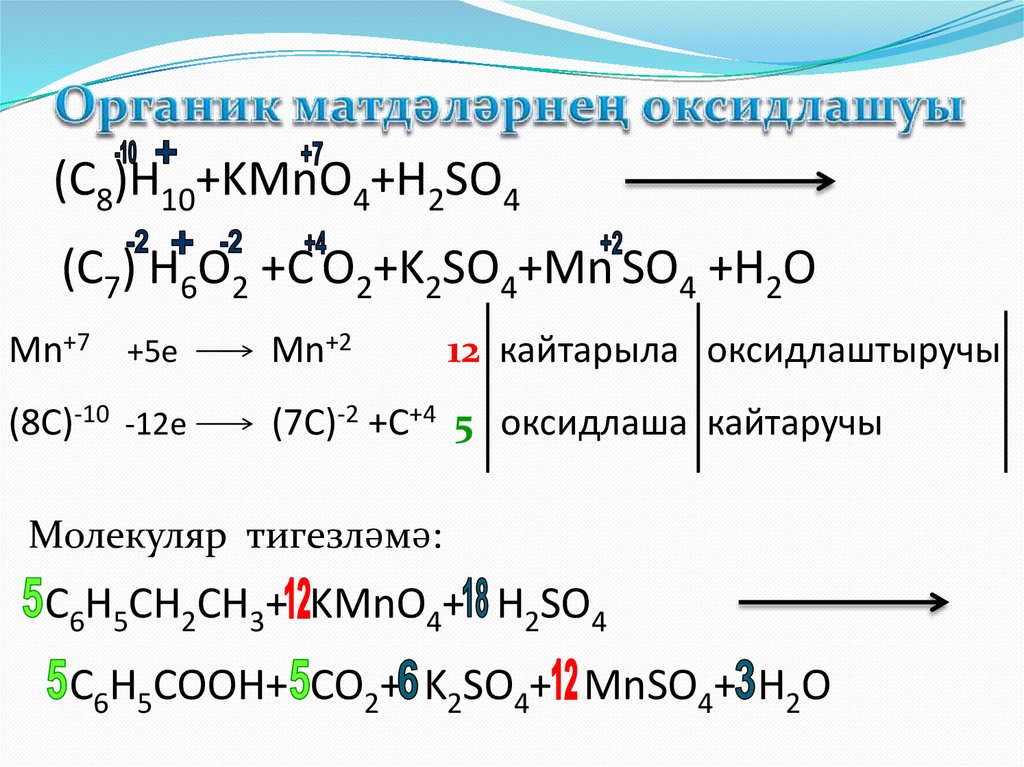
(C8)H10+KMnO4+H2SO4(C7) H6O2 +C O2+K2SO4+Mn SO4 +H2O
Mn+7 +5e
Mn+2
(8C)-10 -12e
(7C)-2 +C+4 5 оксидлаша кайтаручы
12 кайтарыла оксидлаштыручы
Молекуляр тигезләмә:
C6H5CH2CH3+ KMnO4+ H2SO4
C6H5COOH+ CO2+ K2SO4+ MnSO4+ H2O


















 Химия
Химия








