Похожие презентации:
Расчеты по химическим уравнениям
1.
Расчетыпо химическим
уравнениям
Для добавления текста
щёлкните мышью
2.
Расчёты по химическим уравнениям.N – число частиц (атомов или молекул)
n – количество вещества (моль)
М – молярная масса (г/моль)
М = Σ Аr
М (СО2) = Аr(C) + Ar(O) ∙ 2 =
= 12 + 16 ∙ 2 = 44 (г/моль)
m - масса вещества ( г )
m=n∙M
3.
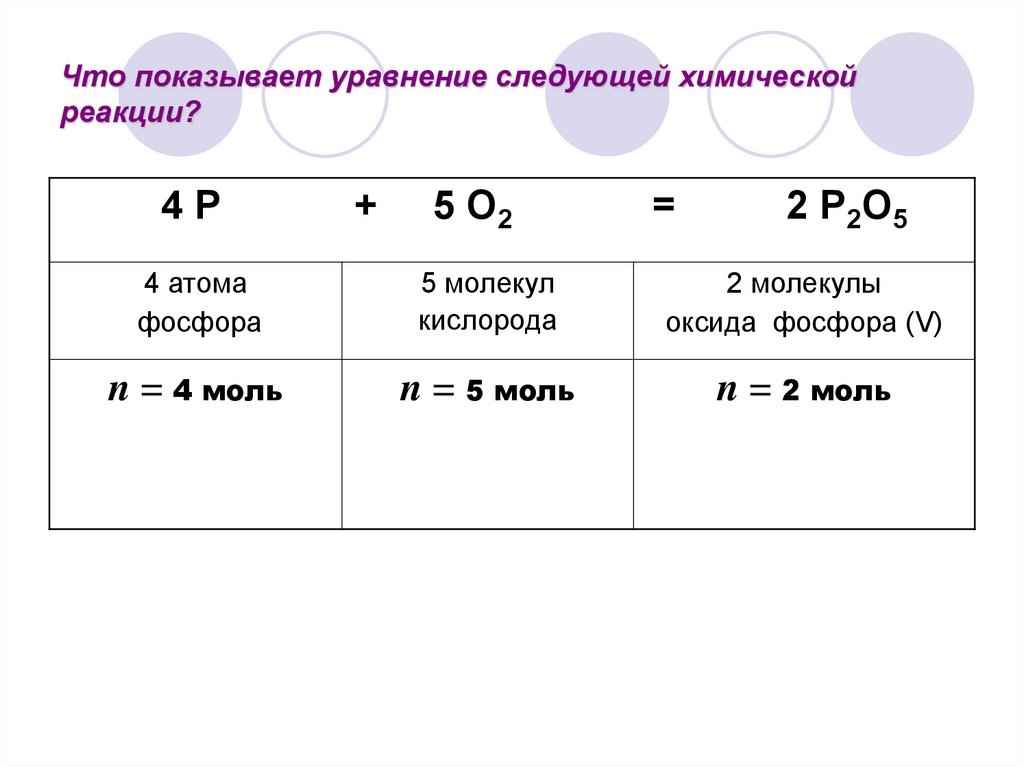
Что показывает уравнение следующей химическойреакции?
4Р
5 О2
=
4 атома
фосфора
5 молекул
кислорода
2 молекулы
оксида фосфора (V)
n = 4 моль
n = 5 моль
n = 2 моль
+
2 Р2О5
4.
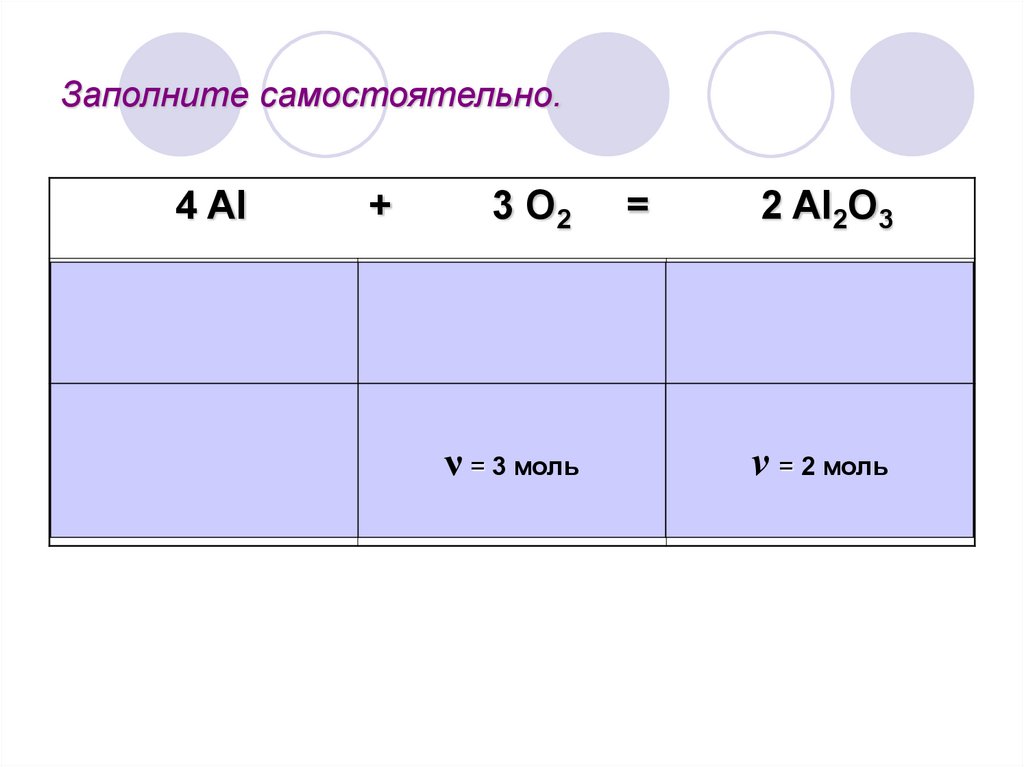
Заполните самостоятельно.4 Al
+
3 О2
ν = 3 моль
=
2 Al2О3
ν = 2 моль
5.
Алгоритм решения задач:1шаг:
Прочитай условие задачи.
2 шаг: Запиши дано задачи, найти,
молярные массы веществ, используя
соответствующие обозначения.
Молярные массы найди с помощью
таблицы Менделеева.
3 шаг: Решение. 1. Составь уравнение
реакции. 2.Подчеркни формулы
веществ, о которых говорится в условии
задачи.
6.
Образец решения задачи поалгоритму:
1шаг:
Прочитай задачу. Определите
массу кислорода, необходимого для
сжигания 8 грамм магния.
2 шаг: Запиши дано задачи, найти,
молярные массы веществ, используя
соответствующие обозначения.
(Молярные массы веществ найдите по
таблице Менделеева).
Дано:
7.
Образец решения задачи поалгоритму:
4 шаг: Под формулами веществ запиши
количество вещества необходимые для
реакции – оно равно коэффициенту
2Мg + 02 = 2 Мg0
2моль 1моль
5 шаг: Найди количество известного
вещества по формуле n = m : М :
ν (Мg)= m (Мg): M(Мg) = 8г : 24г/моль=
8.
Образец решения задачи поалгоритму:
7 шаг: Составь пропорцию и реши ее:
0,33 моль
х моль
2 моль
1 моль
х = (0,33моль• 1моль)/2моль = 0,167
моль
n (02) = 0,167 моль
8 шаг: Найди массу неизвестного
вещества по формуле m = М· n:
9.
Задача 1.Вычислите массу железа, необходимого для
получения 39 г хлорида железа(III).
Схема уравнения реакции следующая:
Fe + Cl2 → FeCl3
10.
Задача 2.Вычислите массу оксида, полученного при
окислении 60 г мышьяка.
Схема уравнения реакции следующая:
As + O2 → As2O5
11.
Домашнее задание:Задача1:
Вычислите массу меди, которая
образуется при восстановлении
избытком водорода 4 г оксида меди
(II).
CuO + H2 = Cu + H2O
Задача 2:
В реакцию с серной кислотой
вступило 20 г гидроксида натрия.
Рассчитайте массу образовавшейся
соли.
2NaOH + H2SO4 = Na2SO4 + 2H2O









 Химия
Химия








