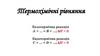Похожие презентации:
Тепловий ефект хімічних реакцій. Екзотермічні ї ендотермічні реакції термохімічні рівняння
1.
2.
3.
Класифікація реакцій затепловим ефектом
Екзотермічні
Відбуваються з виділенням
тепла
Способи запису термохімічного
рівняння
2Mg + O2 → 2MgO + Q
2Mg + O2 → 2MgO + 1205 кДж
2Mg + O2 → 2MgO; ∆ Н ‹ 0
2Mg + O2 → 2MgO; ∆Н = -1205кДж
Ендотермічні
Відбуваються з поглинанням
теплоти
Способи запису термохімічного
рівняння
СаСО3 → СаО +СО2- Q
СаСО3 → СаО +СО2-180кДж
СаСО3 → СаО +СО2; ∆ Н › 0
СаСО3 → СаО +СО2; ∆ Н =180 кДж
4.
Тепловий ефект позначається:а) Q – показує скільки теплоти (кДж)
виділилося або поглинулося під час реакції;
б) ∆ Н – показує різницю між вмістом енергії у
вихідних речовинах і кінцевих продуктах
(ентальпія)
∆Н=-Q
Тепловий ефект вимірюється в Дж або кДж
5.
Тепловийефект реакції
залежить лише від початкового
та кінцевого стану реагуючих
речовин, але не залежить від
проміжних стадій процесу.
6.
СН4+Н2О→СО2+3Н2 ─QСаО + Н2О → Са(ОН)2 + Q
N2 + O2 →2NO; ∆Н›О
СО +Н2О→СО2+Н2 ; ∆Н ‹ О
7.
Рівняння реакцій, в яких указано чисельнезначення теплового ефекту реакції, а також
агрегатний стан речовин, називають
термохімічними.
8.
9.
Завдання 1. У процесі згоряння 12 гвуглецю виділяється 393 кДж тепла.
Запишіть термохімічне рівняння.
C + О2 =CО2 + 393 кДж/моль
або C + О2 = CО2; ΔH = - 393 кДж.
10.
Завдання 2. При утворенні 1 моль хлороводню зпростих речовин виділяється 92,2 кДж. Обчислити
кількість теплоти яка виділиться при утворенні 4
моль хлороводню.
Запам’ятайте: Теплота, що поглинається або
виділяється прямо пропорційна масі, об’єму,
кількості речовини кожної речовини у реакції.
11.
Завдання 3.Обчисліть кількість теплоти, що
виділиться при спалюванні:
а) 4 моль; б) 4г; в) 4л (н.у) карбон
(ІІ) оксиду. Термохімічне рівняння
реакції горіння карбон (ІІ) оксиду
2СО(г) + О2(г)= 2СО2(г), ∆Н = 566кДж
12.
Завдання 4. Укажіть тип хімічнихреакцій (за знаком теплового ефекту):
N2 + O2 = 2NO – 90,4 кДж
CaCO3 = CaO + CO2 – 157 кДж
2NO + O2 = 2NO2 + 116 кДж
2CO + O2 = 2CO2; ∆Н= –566 кДж
2HBr = Н2 + Вr2; ∆Н= +72 кДж












 Химия
Химия