Похожие презентации:
Углеводороды. Алканы
1.
УглеводородыАлканы
2.
Углеводороды – органические соединения,состоящие исключительно из атомов углерода
и
водорода.
Углеводороды
считаются
базовыми соединениями органической химии,
все остальные органические соединения
рассматриваются как их производные.
Поскольку углерод имеет четыре валентных
электрона, а водород – один, простейший
углеводород (природный газ) – метан (СН4)
3.
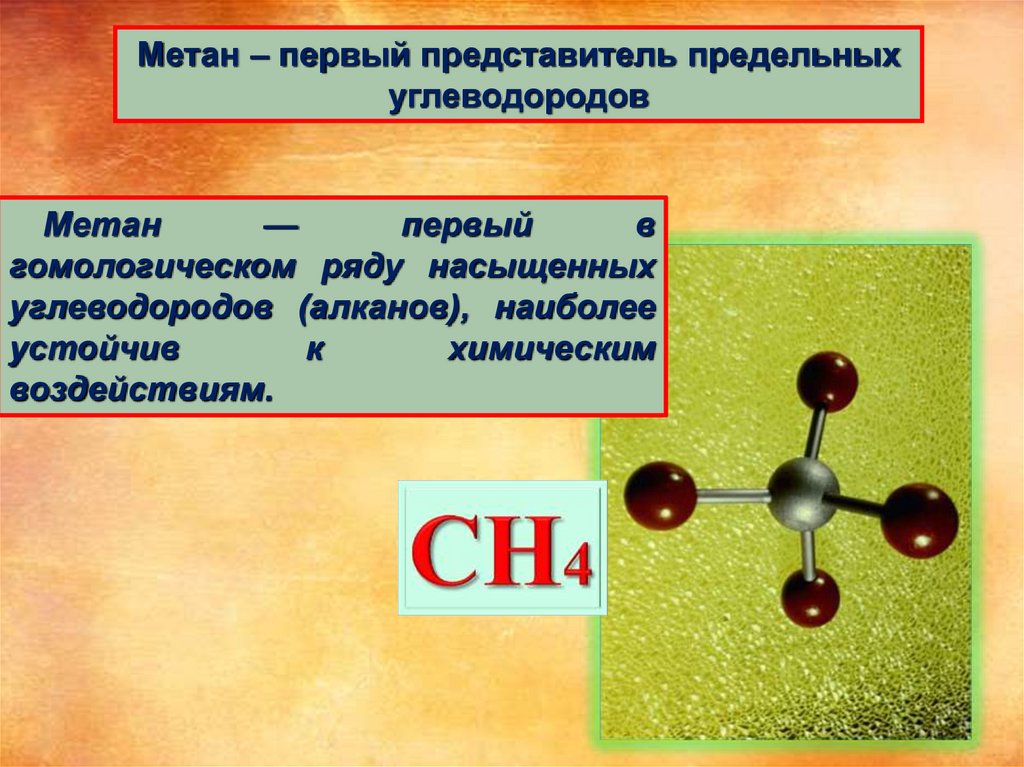
Метан – первый представитель предельныхуглеводородов
Метан
—
первый
в
гомологическом ряду насыщенных
углеводородов (алканов), наиболее
устойчив
к
химическим
воздействиям.
4.
АлканыМетан, этан, пропан, бутан являются первыми
четырьмя членами гомологического ряда
предельных углеводородов – алканов.
Алканы –
это предельные углеводороды, в
молекулах которых все атомы связаны
одинарными связями. Состав их
отражает общая формула
CnH2n + 2
5.
Строение молекулы метанаМолекулярная форма метана:
– электронная формула (ковалентная полярная связь);
– структурная формула (порядок соединения атомов в
молекуле)
.
Но:
6.
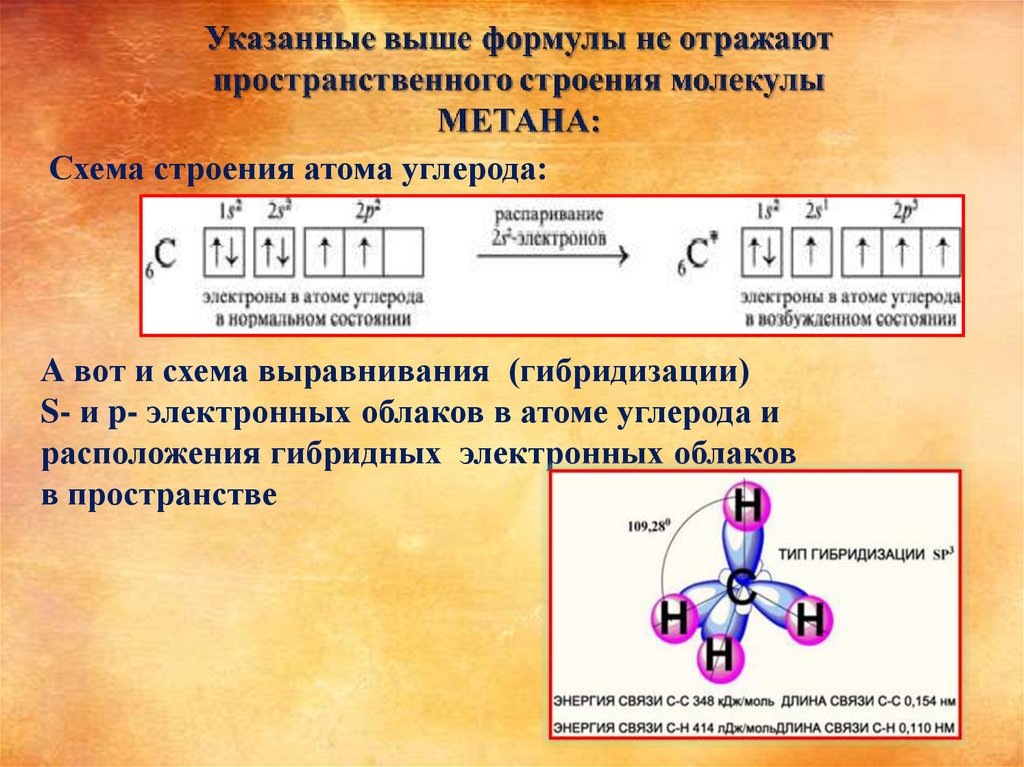
Схема строения атома углерода:А вот и схема выравнивания (гибридизации)
S- и p- электронных облаков в атоме углерода и
расположения гибридных электронных облаков
в пространстве
7.
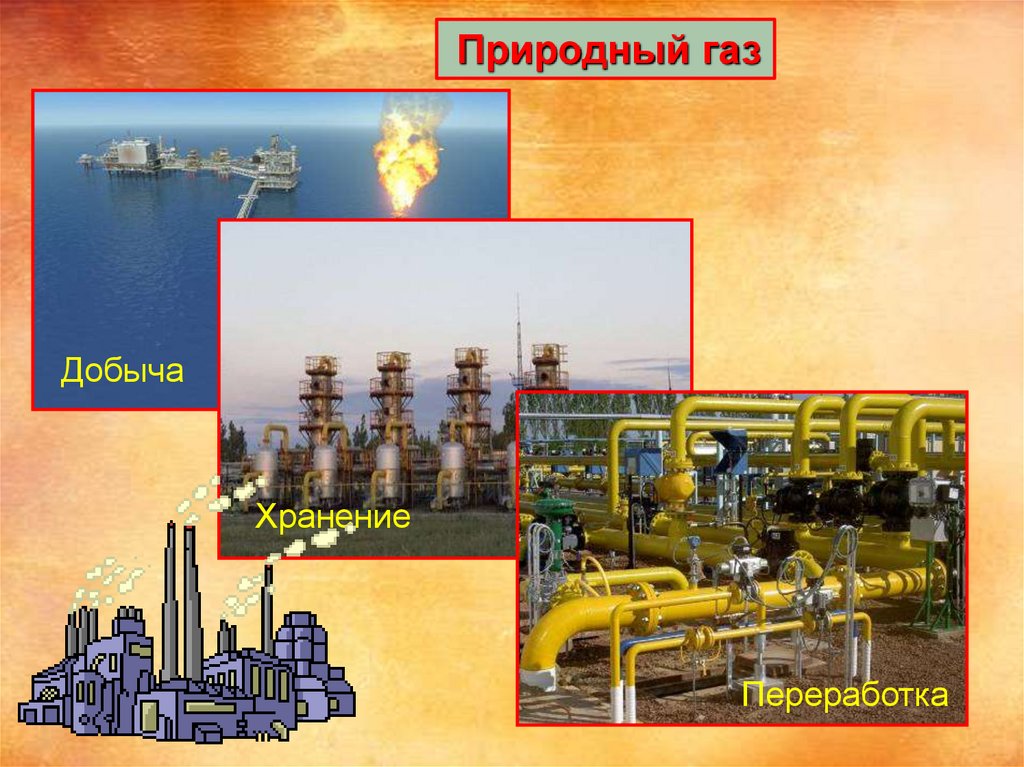
Природный газДобыча
Хранение
Переработка
8.
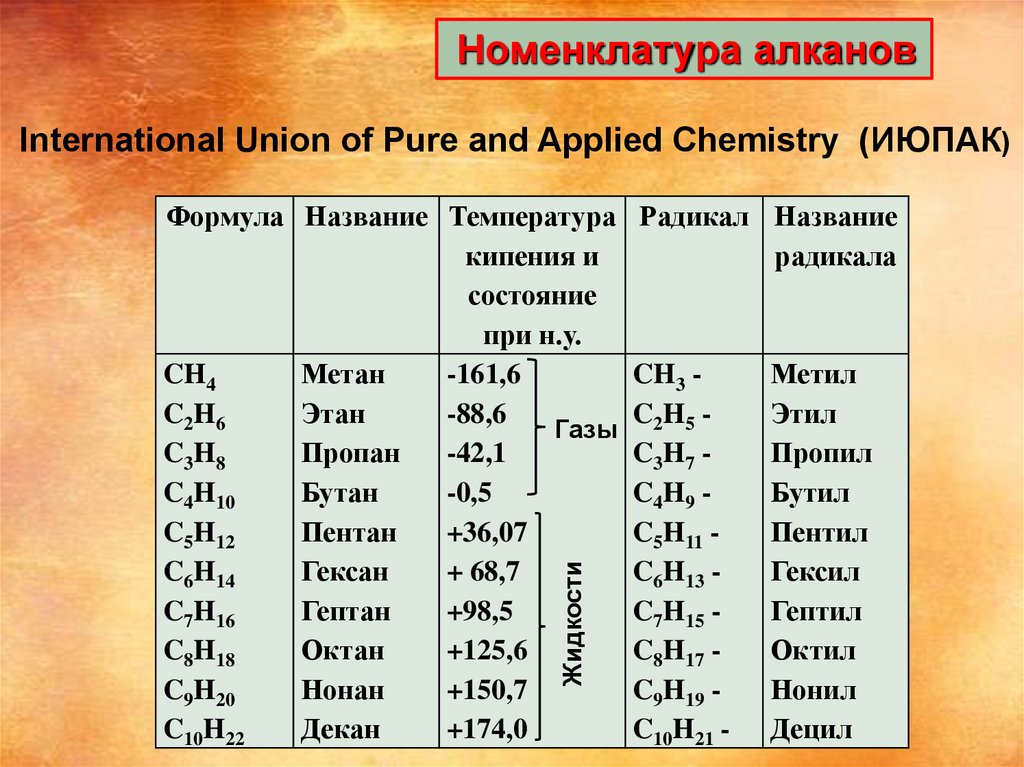
Номенклатура алкановInternational Union of Pure and Applied Chemistry (ИЮПАК)
Жидкости
Формула Название Температура Радикал
кипения и
состояние
при н.у.
CH4
Метан
-161,6
CH3 C 2 H6
Этан
-88,6
CH Газы 2 5
C3H8
Пропан
-42,1
C3H7 C4H10
Бутан
-0,5
C 4 H9 C5H12
Пентан
+36,07
C5H11 C6H14
Гексан
+ 68,7
C6H13 C7H16
Гептан
+98,5
C7H15 C8H18
Октан
+125,6
C8H17 C9H20
Нонан
+150,7
C9H19 C10H22
Декан
+174,0
C10H21 -
Название
радикала
Метил
Этил
Пропил
Бутил
Пентил
Гексил
Гептил
Октил
Нонил
Децил
9.
Номенклатура алкановДля определения названия углеводорода
следует придерживаться следующего порядка:
1. Выбрать в формуле наиболее длинную углеродную цепь и символы
атомов углерода в ней пронумеровать, начиная с того конца цепи, к
которому ближе разветвление:
CH
3
4
3 2│
1
CH3 ─ CH2 ─ C ─ CH3
│
CH3
2. Назвать радикал (начиная с простейшего) и при помощи цифр
указать их место в у нумерованных атомов углерода. Если у
одного и того же атома углерода находятся два одинаковых
радикала, номер повторяют дважды:
2,2-диметил…
3. Полное название данному углеводороду дать по числу атомов
углерода в нумерованной цепи: 2,2-диметилбутан
10.
Физические свойства алкановТемпературы плавления и кипения увеличиваются
с молекулярной массой и длиной главной углеродной
цепи.
При нормальных условиях неразветвлённые
алканы с CH4 до C4H10 — газы; с C5H12 до C13H28 —
жидкости; начиная с C14H30 и далее — твёрдые
вещества.
Температуры плавления и кипения понижаются от
менее разветвленных к более разветвленным. Так,
например,
при
20°C
н-пентан
—
жидкость,
а неопентан — газ.
Газообразные алканы горят бесцветным или
бледно-голубым пламенем с выделением большого
количества тепла.
11.
Химические свойства алканов1. Горение
CH4 + 2O2 → CO2 + 2H2O + Q
2. Замещение (галогенирование) – реакции идут на свету
CH4 + Cl2 → CH3Cl + HCl
xлорметан
CH3Cl + Cl2 → CH2Cl2 + HCl
дихлорметан
CH2Cl2 + Cl2 → CHCl3 + HCl
трихлорметан
CHCl3 + Cl2 → CCl4 + HCl
тетрахлорметан
12.
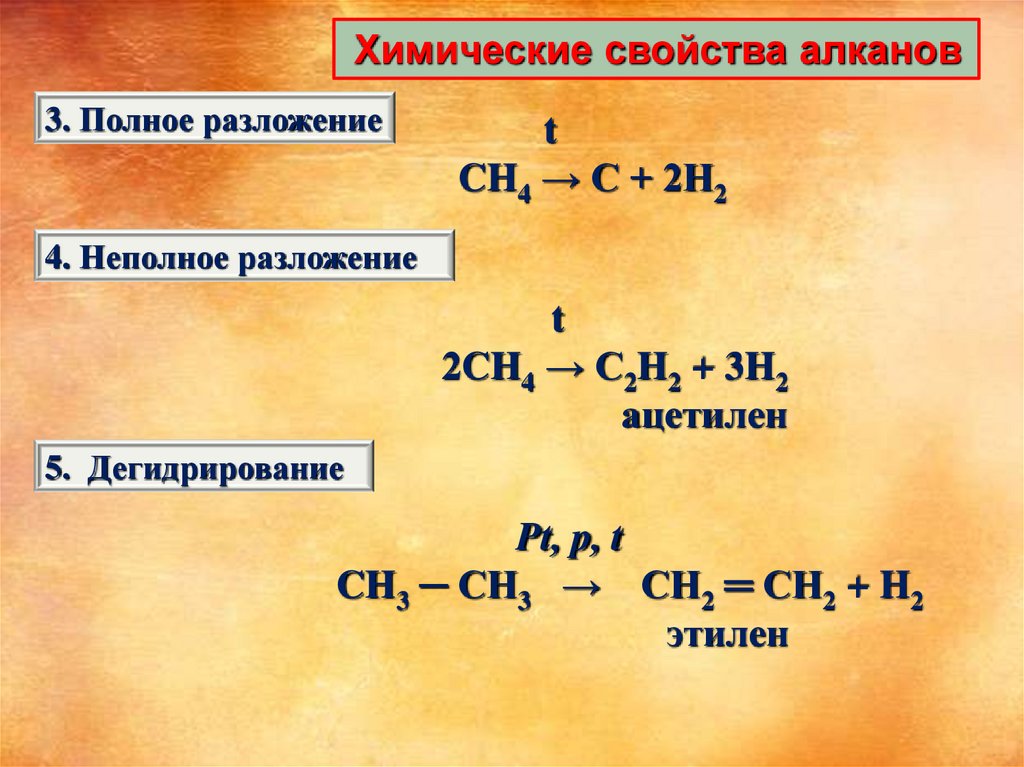
Химические свойства алканов3. Полное разложение
t
CH4 → C + 2H2
4. Неполное разложение
t
2CH4 → C2H2 + 3H2
ацетилен
5. Дегидрирование
Pt, p, t
CH3 ─ CH3 → CH2 ═ CH2 + H2
этилен
13.
Химические свойства алканов6. Изомеризация
Углеводороды
нормального
строения
под
влиянием
катализаторов и при нагревании подвергаются реакциям
изомеризации и превращаются в углеводороды разветвленного
строения.
t,AlCl3
CH3─CH2─CH2─CH2─CH3 → CH3─CH─CH2─CH3
│
CH3
2-метилбутан
14.
Получение алкановВ лаборатории метан получают при нагревании
ацетата натрия с твердым гидроксидом натрия:
t
CH3COONa + NaOH →
CH4↑ + Na2CO3
15.
Получение алкановЭтан и другие предельные углеводороды с более
длинной углеродной цепью можно получить при
взаимодействии однородных галогенопроизводных
предельных
углеводородов
с
металлическим
натрием:
CH3 ─ I
Na
+
CH3 ─ I
Na
иодометан
→ CH3 ─ CH3 + 2NaI
этан
Реакция Вюрца
16.
Применение алканов1. Картриджи.
2. Резина.
3. Типографская краска.
4. Растворители.
5. Хладагенты (фреоны).
6. Метанол.
7. Ацетилен.
17.
Применение алканов18.
Использованные источники1. О.С.Габриелян. Химия. 10 класс. Базовый уровень. М. Дрофа.
2013.
2. 2. Г.Е.Рудзитис, Ф.Г.Фельдман. Химия. 10 класс. М.
Просвещение. 2012.
3. Картинка «получение алканов» слайд 14:
http://dist-tutor.info/mod/book/view.php?id=28450&chapterid=1598
4. Картинка «применение алканов» слайд 16:
http://www.alhimikov.net/organikbook/alcan_01.html
19.
Вопросы1. Что такое алканы?
2. Напиши название этих веществ:
а. СН4 б. С2 Н6 в. С6 Н14 г. С8 Н18
3. Напиши название этих радикалов:
а. CH3 - б.C2H5 - в. C3H7 - г. C4H9 - д. C5H11 4. Опиши физические свойства алканов.
5. Напиши название вещества, используя правлила
составления названий органических веществ.
CH3─CH─CH2─CH3
│
CH3
6. Напиши реакции полного и неполного разложения
алканов














 Химия
Химия








