Похожие презентации:
Алканы. Гомологический ряд предельных углеводородов
1. Алканы
Алканами называютсянасыщенные углеводороды,
молекулы которых состоят из
атомов углерода и водорода,
связанных между собой только σсвязями
СnН2n+2
Насыщенные или метановые
углеводороды, парафины
1
2. Гомологический ряд предельных углеводородов
CH4CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
и т.д.
В гомологическом ряду алканов каждый
последующий член ряда отличается от
предыдущего на группировку атомов СН2,
которая
называется
гомологической
разностью.
2
3. Алканы
НоменклатураЗа первыми четырьмя членами гомологического ряда
оставлены тривиальные названия, далее названия
алканов образуются от греческих и латинских (для
С9Н20) числительных с добавлением суффикса - ан
СН4
метан
С2Н6 этан
С3Н8 пропан
С4Н10 бутан
С5Н12 пентан
С6Н14 гексан
С7Н16 гептан
С8Н18 октан
С9Н20 нонан
С10Н22 декан
С20Н42 эйкозан
С30Н62 триаконтан
С100Н202 гектан
3
4. Алкильные радикалы
НоменклатураCH2CH2CH2CH3 бутил
CH3
метил
CH3CH2CHCH3 вт.бутил
CH2CH3
этил
CH2CHCH3 изобутил
CH2CH2CH3 пропил
CH3
CH3CHCH3
изопропил
CH3
C CH3
трет.бутил
CH3
4
5. Алканы
НоменклатураВыбирается наиболее длинная цепь взаимосвязанных
углеродных атомов.
Цепь нумеруется, начиная с того конца, куда ближе
радикал-заместитель (сумма чисел, обозначающих
местоположение алкилов в цепи должно быть
наименьшим).
Далее составляется название алкана. В названии
перечисляются все алкильные заместители по
старшинству с указанием их положения в главной
цепи. Название завершается названием углеводорода,
которому соответствует наиболее длинная цепь.
Названия одних и тех же радикалов объединяются.
5
6. Алканы
Номенклатура6
5
H3CH2C CH3
4
3
2
1
CH3CH2CH2 C C CH3
H3С
CH3
метилэтилпропил-трет-бутилметан или
2,2,3-триметил-3-этилгексан
6
7. Алканы
ИзомерияВ
предельных
углеводородах,
уже
начиная
с
четвертого члена гомологического ряда, одному и
тому же составу С4Н10 соответствуют разные по
строению соединения
CH3
CH3CH2CH2CH3
н-бутан
CH3CHCH3
изобутан
Соединения, имеющие одинаковый состав, но различное
строение, называются изомерами.
7
8. Алканы
Способы полученияГидрирование алкенов
CH2 CH2
H2
Pt, Pd, Ni
CH3CH3
8
9. Алканы
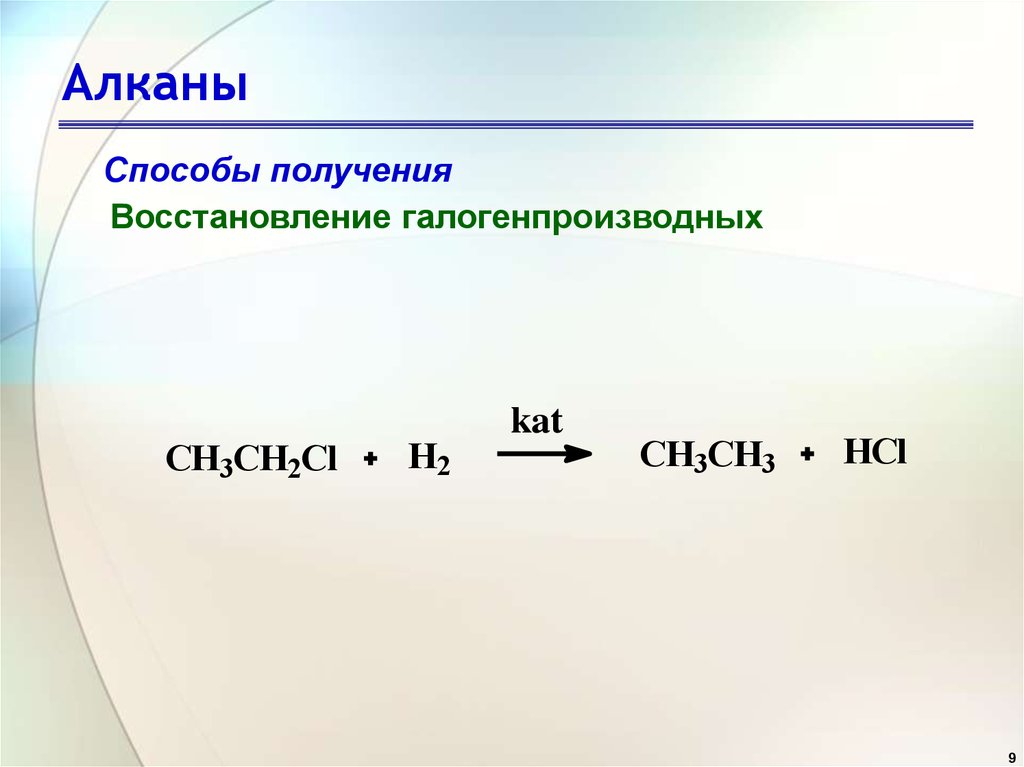
Способы полученияВосстановление галогенпроизводных
CH3CH2Cl
H2
kat
CH3CH3
HCl
9
10. Алканы
Способы полученияКонденсация галогенпроизводных под
действием щелочных металлов (реакция Вюрца)
2CH3CH2Cl
2Na
CH3CH2CH2CH3
2NaCl
10
11. Алканы
Способы полученияПри участии в реакции Вюрца молекул одного
галогенпроизводного
получающийся
алкан
содержит в два раза больше углеродов, чем
исходный галоидный алкил. В случае же
использования
в
реакции
смеси
галогенпроизводных по понятным причинам
получается смесь трех углеводородов
CH3Cl CH3CH2Cl
2Na
- NaCl
CH3CH3
CH3CH2CH3 CH3CH2CH2CH3
11
12. Алканы
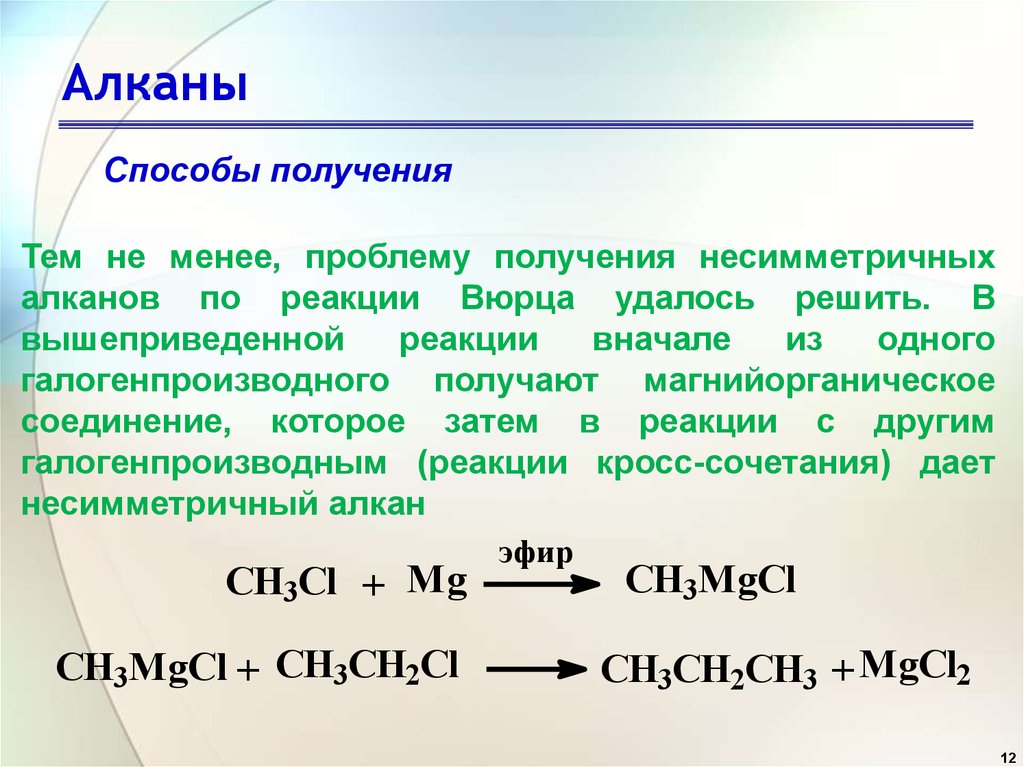
Способы полученияТем не менее, проблему получения несимметричных
алканов по реакции Вюрца удалось решить. В
вышеприведенной
реакции
вначале
из
одного
галогенпроизводного получают магнийорганическое
соединение, которое затем в реакции с другим
галогенпроизводным (реакции кросс-сочетания) дает
несимметричный алкан
эфир
CH3Cl + Mg
CH3MgCl + CH3CH2Cl
CH3MgCl
CH3CH2CH3 + MgCl2
12
13. Алканы
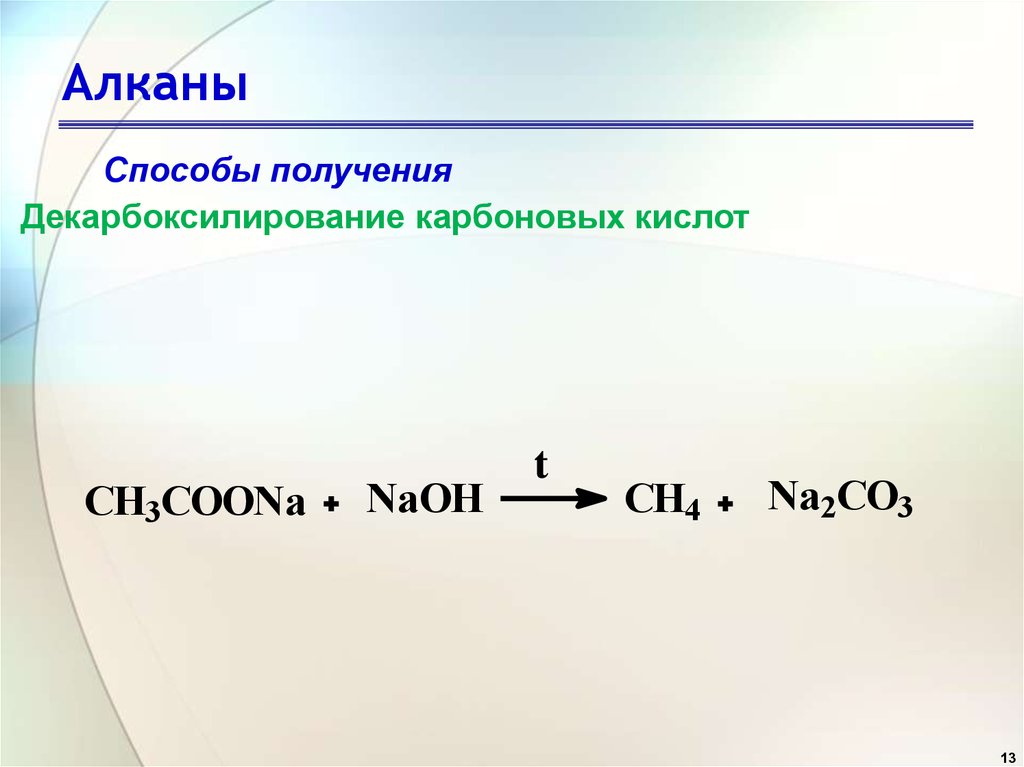
Способы полученияДекарбоксилирование карбоновых кислот
CH3COONa
NaOH
t
CH4
Na2CO3
13
14. Алканы
Способы полученияЭлектролиз карбоновых кислот
RCOONa
e
RCOO
RCOO
RCOO
RCOO
R
R
R R
R
Na
CO2
14
15. Алканы
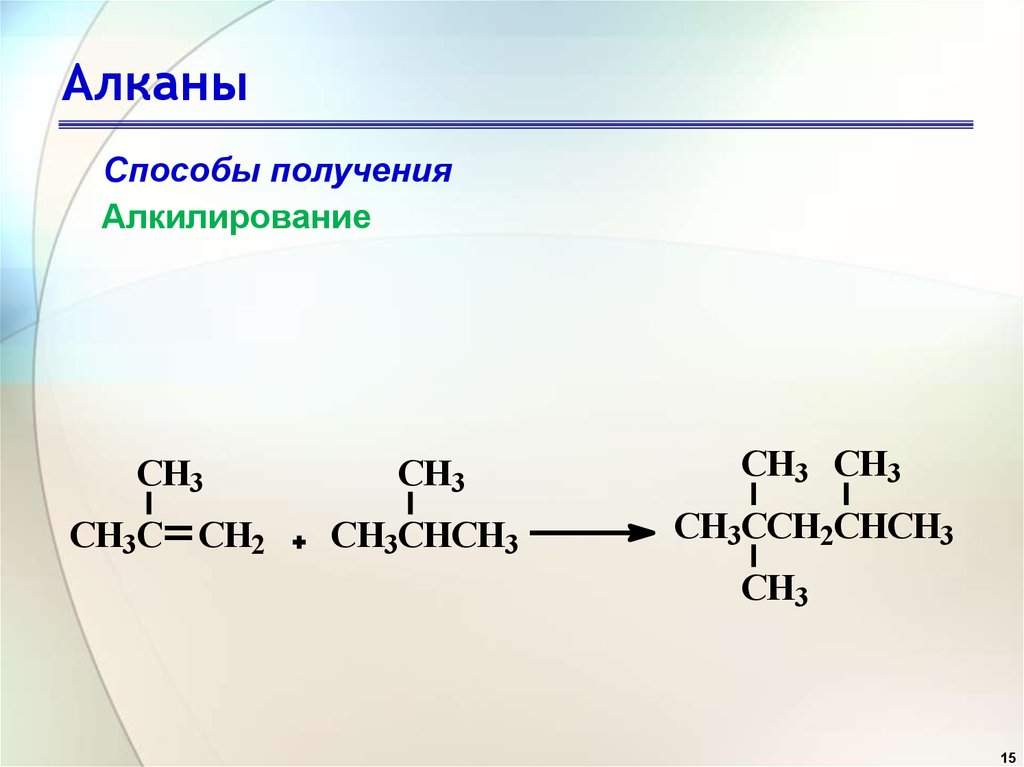
Способы полученияАлкилирование
CH3
CH3
CH3 CH3
CH3C CH2
CH3CHCH3
CH3CCH2CHCH3
CH3
15
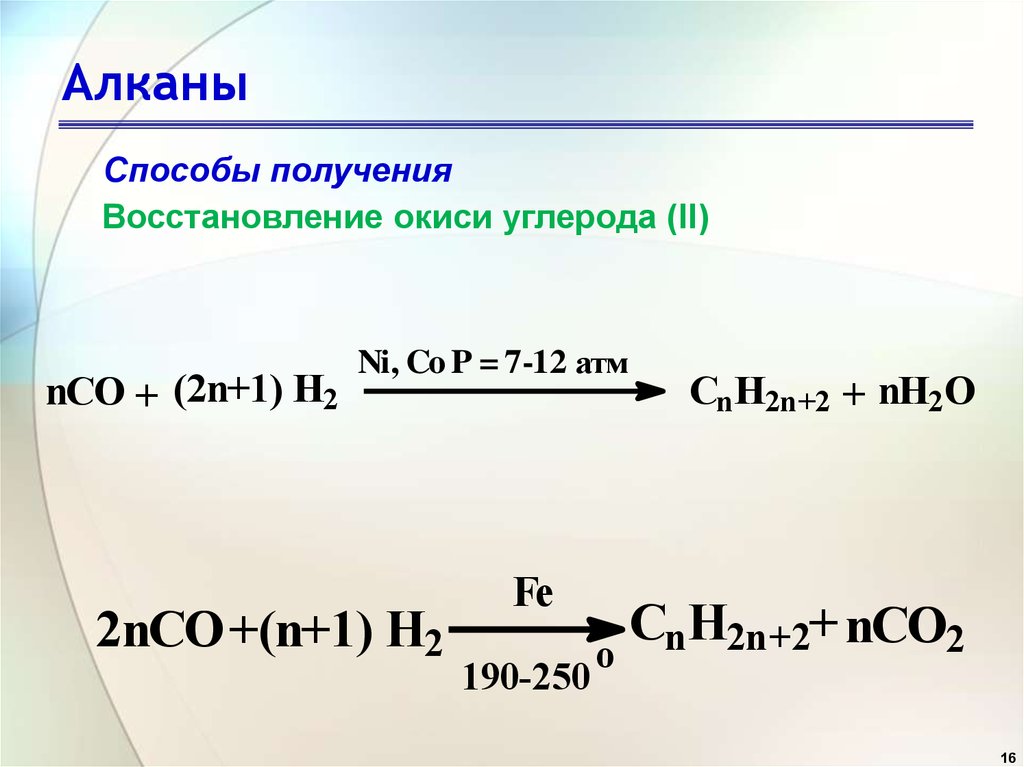
16. Алканы
Способы полученияВосстановление окиси углерода (II)
nCO + (2n+1) H2
Ni, Co P = 7-12 атм
2nCO +(n+1) H2
Fe
190-250
o
CnH2n+2 + nH2O
CnH2n+2+ nCO2
16
17. Алканы
Химические свойстваРеакции радикального замещения
Галогенирование
CH4
+
Cl2
CH3Cl + Cl2
CH2Cl2 +
Cl2
CHCl3 + Cl2
hv, t
hv, t
CH3Cl + HCl
CH2Cl2 + HCl
hv, t
CHCl3 + HCl
hv, t
CCl4 + HCl
17
18. Алканы
Химические свойстваРеакции радикального замещения
Механизм галогенирования алканов
(1)
Cl Cl
h
(2) Cl + СH4
инициирование цепи
2Cl
HCl + CH3
(3) CH3 + Cl Cl
CH3Cl + Cl
(4) Cl+ Cl
Cl2
Cl
CH3Cl
+ CH3
CH3 + CH3
CH3CH3
рост цепи
рост цепи
обрыв цепи
18
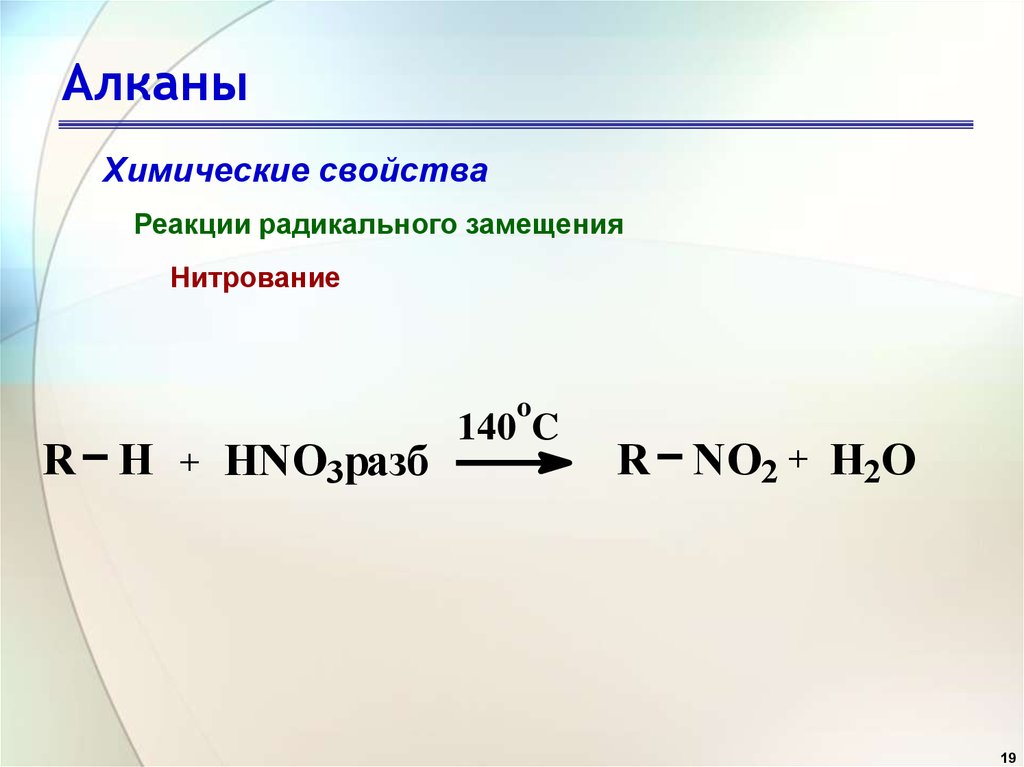
19. Алканы
Химические свойстваРеакции радикального замещения
Нитрование
o
R H
+
HNO3разб
140 C
R NO2 + H2O
19
20. Алканы
Химические свойстваРеакции радикального замещения
Сульфирование
R H
R
H2SO4конц
+
SO3H
+
H2O
Сульфоокисление
2R H
+
2SO2
+
O2
h
2R
SO3H
Сульфохлорирование
R H
+
SO2
+
Cl2
h
2R
SO2Cl
+
HCl
20
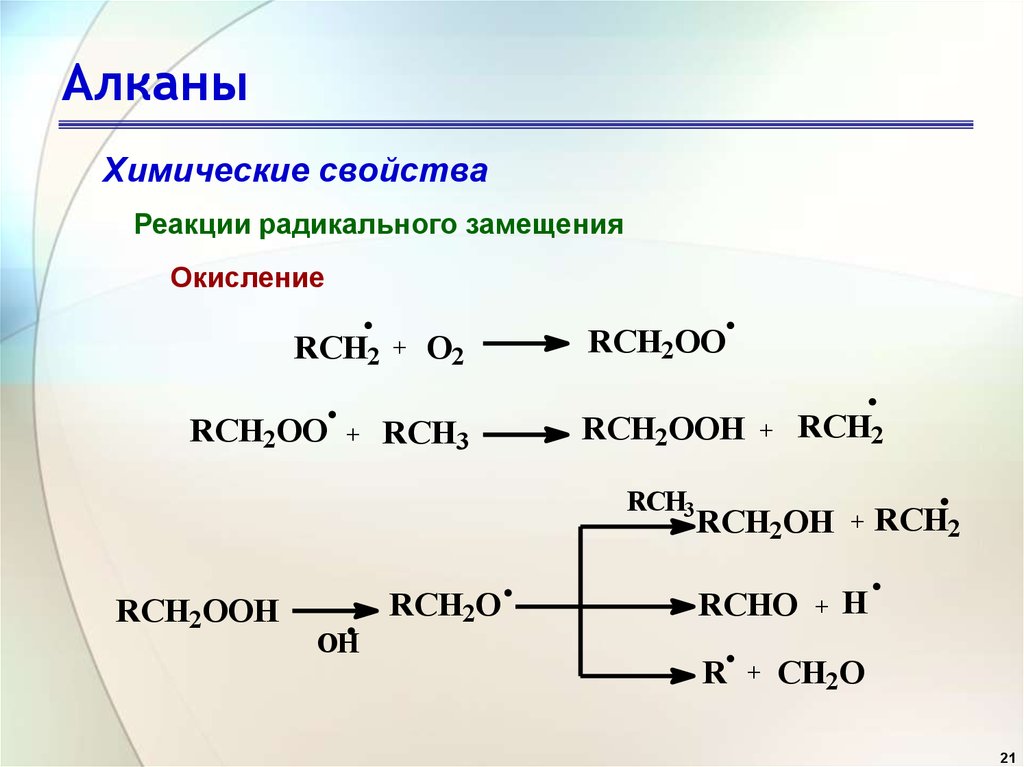
21. Алканы
Химические свойстваРеакции радикального замещения
Окисление
RCH2
RCH2OO
+
+
O2
RCH3
RCH2OO
RCH2OOH
RCH3
RCH2OOH
RCH2O
OH
+
RCH2
RCH2OH
RCHO
R
+
+
+
RCH2
H
CH2O
21
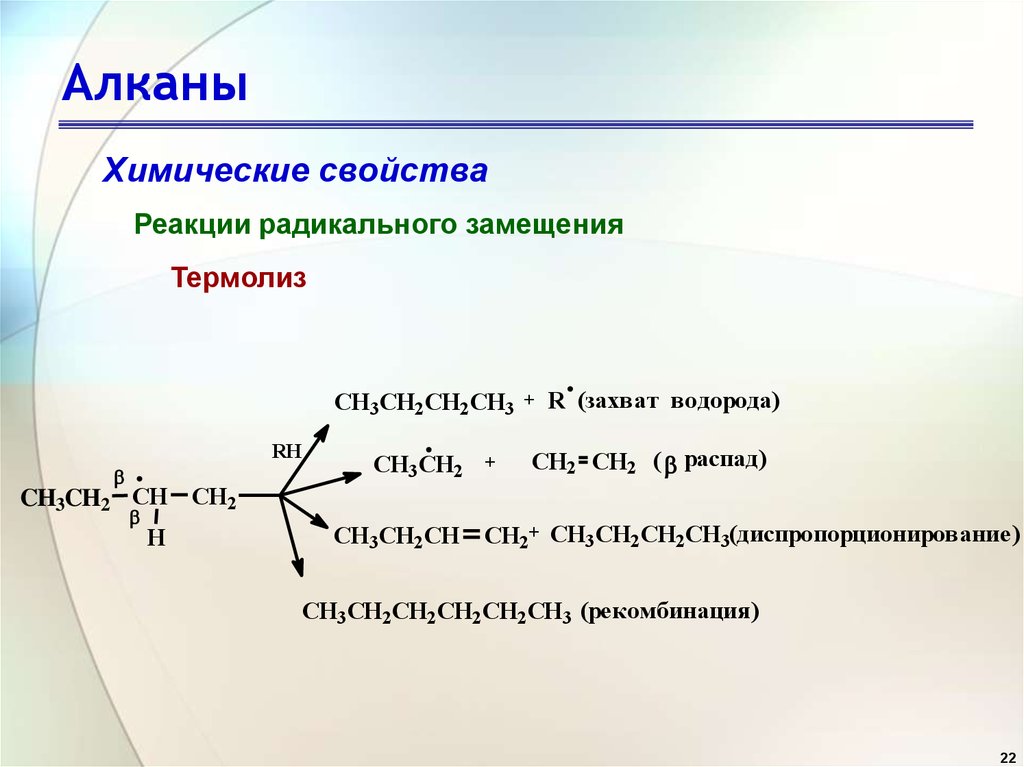
22. Алканы
Химические свойстваРеакции радикального замещения
Термолиз
CH3CH2CH2CH3
RH
CH3CH2
+
+
R (захват водорода)
CH2 CH2 ( распад)
CH3CH2 CH CH2
H
CH3CH2CH CH2+ CH3CH2CH2CH3(диспропорционирование)
CH3CH2CH2CH2CH2CH3 (рекомбинация)
22














 Химия
Химия








