Похожие презентации:
Азот. Характеристика азота, фосфора (9класс)
1.
АЗОТ2. История открытия:
1772 г Д.Резерофорд и К. Шееле (газ неподдерживает дыхание и горение)
1787 г А.Лавуазье(обнаружил в воздухе
газ и назвал его «безжизненный»).
1790 гЖ.Шапталь (рождающий селитру).
3. Характеристика азота
1. Химический знак _______, период ______,группа__________, подгруппа
____________, Ar = _____
2. Состав атома азота: р = ____, е= _____,
n=_____
3. Строение атома азота:
N +7
или 2е,5е
Степени окисления:
-3, +1,+2,+3,+4,+5
4. Характеристика фосфора
1. Химический знак _______, период ______,группа__________, подгруппа
____________, Ar = _____
2. Состав атома фосфора: р = ____, е= _____,
n=_____
3. Строение атома фосфора :
Р +15
или Степени
окисления:-3, +1,+2,+3,+4,+5
5.
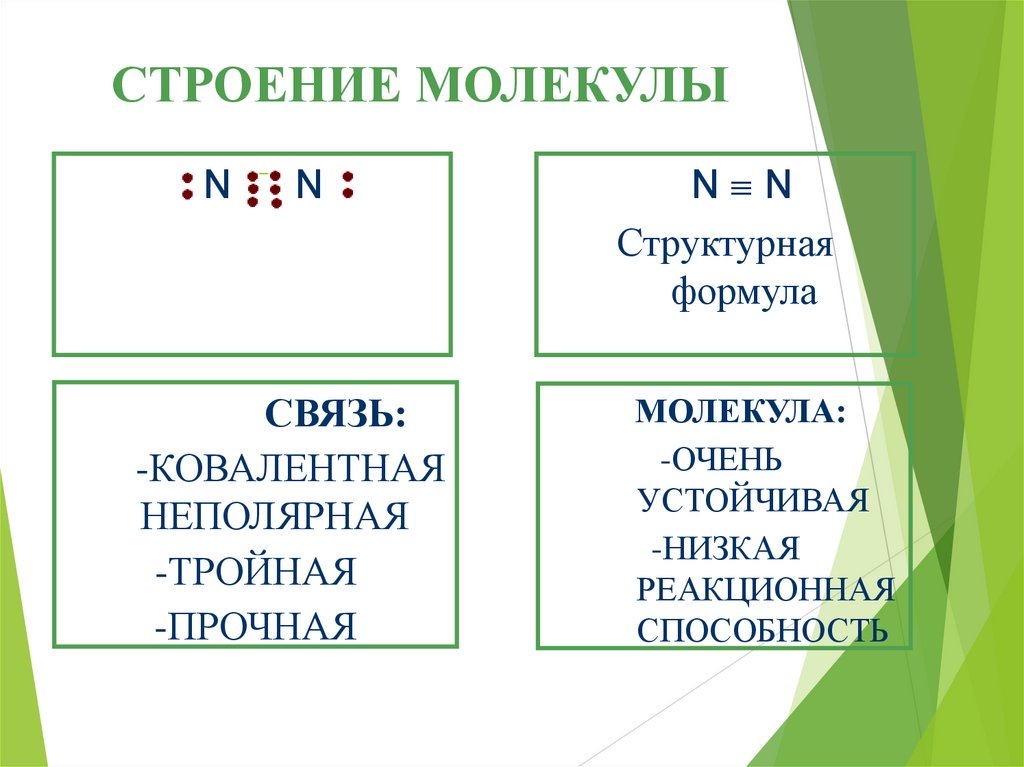
СТРОЕНИЕ МОЛЕКУЛЫN
N
СВЯЗЬ:
-КОВАЛЕНТНАЯ
НЕПОЛЯРНАЯ
-ТРОЙНАЯ
-ПРОЧНАЯ
N N
Структурная
формула
МОЛЕКУЛА:
-ОЧЕНЬ
УСТОЙЧИВАЯ
-НИЗКАЯ
РЕАКЦИОННАЯ
СПОСОБНОСТЬ
6.
ФИЗИЧЕСКИЕ СВОЙСТВА.Газ без цвета, запаха и вкуса
Плохо растворим в воде
Немного легче воздуха
В обычных условиях пассивен
Tºпл.= -210ºС
Tºкип.= -196ºС
7.
Химические свойства:1.При обычных условиях только с литием.
Li + N2 = Li3N (нитрид лития (N -3)
2.С другими металлами только при высоких
температурах.
Ca + N2 = _____
8. 3. При высоких температурах и давлении в присутствии катализатора с водородом с образованием аммиака.
N2 + __H2__N-3H3+Q экзотермическая
аммиак
9. 4.При температуре электрической дуги с кислородом образуя оксид азота (II).
N2 + O2__N+2O-Q эндотермическая
10.
ПРИМЕНЕНИЕ И ПОЛУЧЕНИЕПрименение
Получение аммиака
Создание инертной атмосферы
Создание низких температур
Насыщение поверхности стали
для повышения прочности
Получение
В промышленности – из жидкого
воздуха
В лаборатории – разложением
неустойчивых соединений азота









 Химия
Химия