Похожие презентации:
Водород. Химический знак - H
1.
Водород.
2.
Химический знак – HОтносительная атомная
масса Ar (H) = 1, 008
Химическая формула – H2
Относительная молекулярная
масса Mr (H2) = 2, 016
В соединениях водород одновалентен
3. История открытия
Водород(Hudrogenium)
был открыт в первой
половине XVI века
немецким врачом и
естествоиспытателем
Парацельсом.
4.
В 1766 г.Генри Кавендиш
(Англия)
установил свойства
водорода
и указал его
отличия от других
газов
5.
Французский химикАнтуан Лавуазье
доказал и обратное:
получил «горючий газ»
из воды. Он дал
новому газу и другое
имя – водород
(рождающий воду)
6.
Водородявляется самым
распространенным
химическим элементом
во Вселенной, он
является главной
составной частью
Солнца, а также многих
звезд.
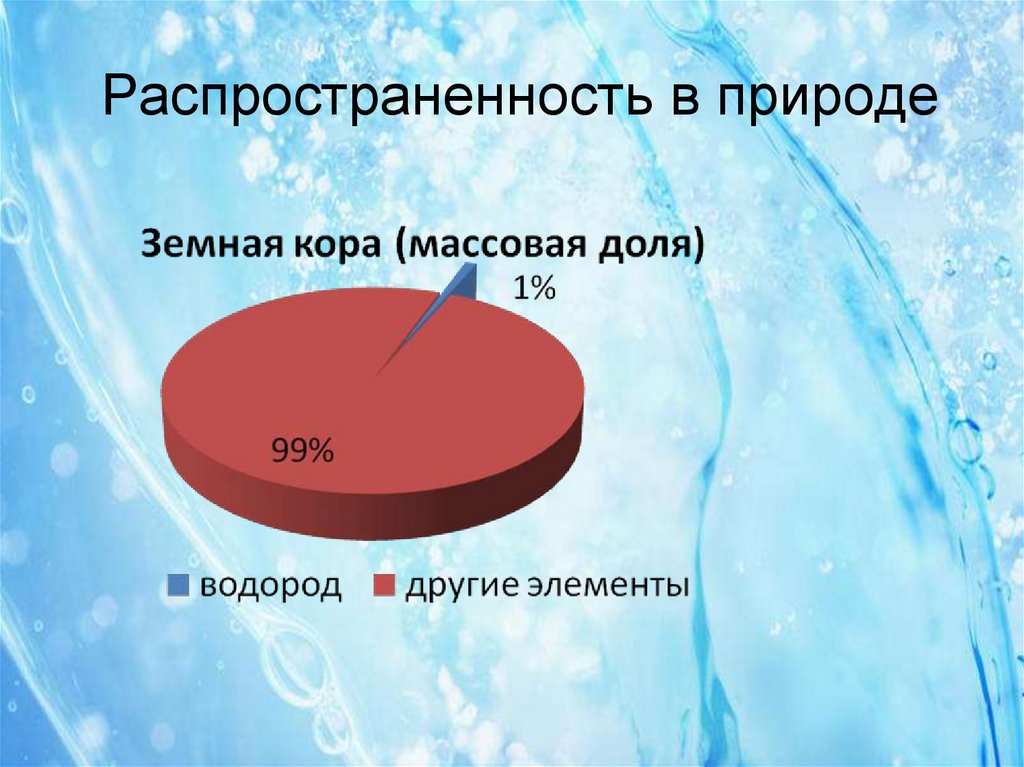
7. Распространенность в природе
8.
Водородзанимает первое место в
периодической системе
химических элементов
Д.И. Менделеева, имеет
простейшее строение
атома: ядро атома
окружено электронным
облаком
9. Получение водорода в промышленности
1. В основном получают из природного газа путемконверсии ( превращения) под действием
водяных паров и катализатора:
CH4 + 2H2O
4H2 + CO2
2. Нагревание:
CH4
2H2 + C
3. Разложение воды под действием электрического
тока:
2H2O
2H2 + O2
4.В промышленности водород получают, пропуская
водяные пары над раскаленным углем:
C + H2O
CO + H2
10. Получение водорода в лаборатории
1.Взаимодействие металлов скислотами:
Zn +2HCl → ZnCl2 +H2↑
2.Взаимодействие активных металлов с
водой:
2Na + 2HOH
2NaOH + H2
3.Разложение воды под действием
постоянного электрического тока:
2H2O
2H2 + O2
11. Способы собирания водорода
Вытеснение водыВытеснение воздуха
12. Физические свойства
1.Бесцветный газ2.Без запаха
3.Без вкуса
4.Легче воздуха в 14,5 раза
5.Плохо растворим в воде
13. Химические свойства
1.Взаимодействие с кислородом2H2 + O2 = 2H2O
2.Взаимодействие с серой
H 2 + S = H 2S
3.Взаимодействие с оксидами
металлов
CuO + H2 = Cu + H2O
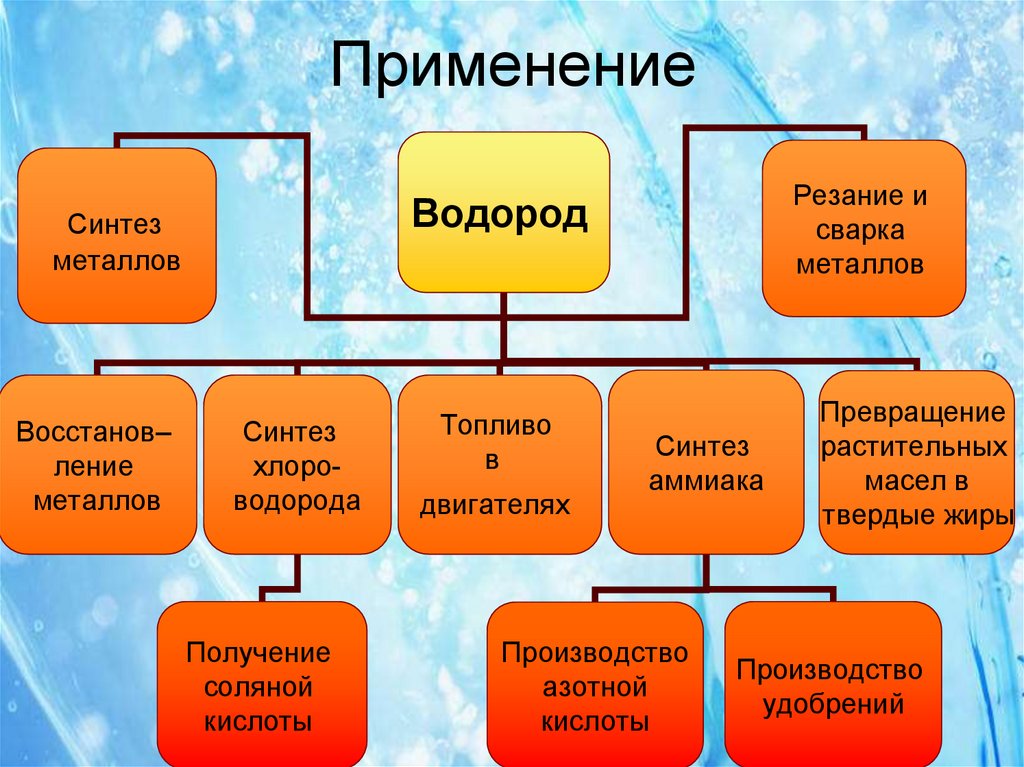
14. Применение
ВодородСинтез
металлов
Восстанов–
ление
металлов
Резание и
сварка
металлов
Синтез
хлороводорода
Получение
соляной
кислоты
Топливо
в
двигателях
Синтез
аммиака
Производство
азотной
кислоты
Превращение
растительных
масел в
твердые жиры
Производство
удобрений
15. Помимо полезных свойств водорода существует еще одно: из водорода можно сделать оружие разрушительной силы. Это оружие
называется водородная бомба. Взрывводородной бомбы сопровождается выбросом
большого количества радиоактивных веществ.
Благодаря своей конструкции и механизму
действия, водородная бомба может быть
сделана какой угодно мощной. При этом она
намного дешевле атомных бомб той же
мощности.
16.
Водородные бомбыиногда
сравнивают с
солнцем. Однако
солнце дарует нам
жизнь, а
водородная бомба
— сулит смерть...
17. Водородная энергетика
В недалеком будущемосновным источником
получения энергии станет
реакция горения
водорода. Водородная
энергетика вытеснит
традиционные источники
получения энергии (уголь,
нефть и др.)
18. Водородные автомобили
В 1979 годукомпания BMW
выпустила первый
автомобиль, вполне
успешно ездивший
на водороде
19. Toyota переходит на водород
20.
H2H2
H2
Я, газ легчайший и бесцветный,
Неядовитый и безвредный.
Соединяясь с кислородом,
Я для питья даю вам воду.
H2
H2
H2
H2
H2

















 Химия
Химия








