Похожие презентации:
Классификация неорганический веществ
1. Классификация неорганический веществ
28.04.20.Классификация
неорганический веществ
Домашнее задание:
1.
Изучите презентацию, Выпишите
химические свойства соединений.
2.
Выполните тест по учебнику на стр.207208 (12 вопросов)
Фото выполненных работ отправляем
учителю milyaycha@mail.ru или WhatsApp
89053742581
2. Вещества
Простые-Сложные-
состоят из атомов
одного химического
элемента.
состоят из атомов
разных элементов
3. Простые вещества
МеталлыNa,
Fe,
Al,
Zn…
Благородные
газы
Неметаллы
O2,
H2,
Cl2,
S,
P,
C…
He,
Ne,
Ar,
Kr,
Xe,
Rn
4. Сложные вещества
ОксидыГидроксиды
Кислоты
Соли
Основания
Амфотерные
5.
Оксиды-2
(ЭхО y )
Несолеобразующие
(СO, NO, N2O)
Солеобразующие
Кислотные
Амфотерные
Основные
6. Кислотные оксиды
Оксидынеметаллов:
SO2
SO3
CO2
P2O5
SiO2
N2O3
N2O5
Оксиды металлов
со степенью
окисления +6, +7
СrO3
Mn2O7
7. Основные оксиды-
оксиды металловсо степенью окисления +1, +2
Na2O
Li2O
K 2O
MgO
CaO
BaO
CrO
FeO
NiO
8. Амфотерные оксиды
ZnOAl2O3
Fe2O3
Cr2O3
CuO
BeO
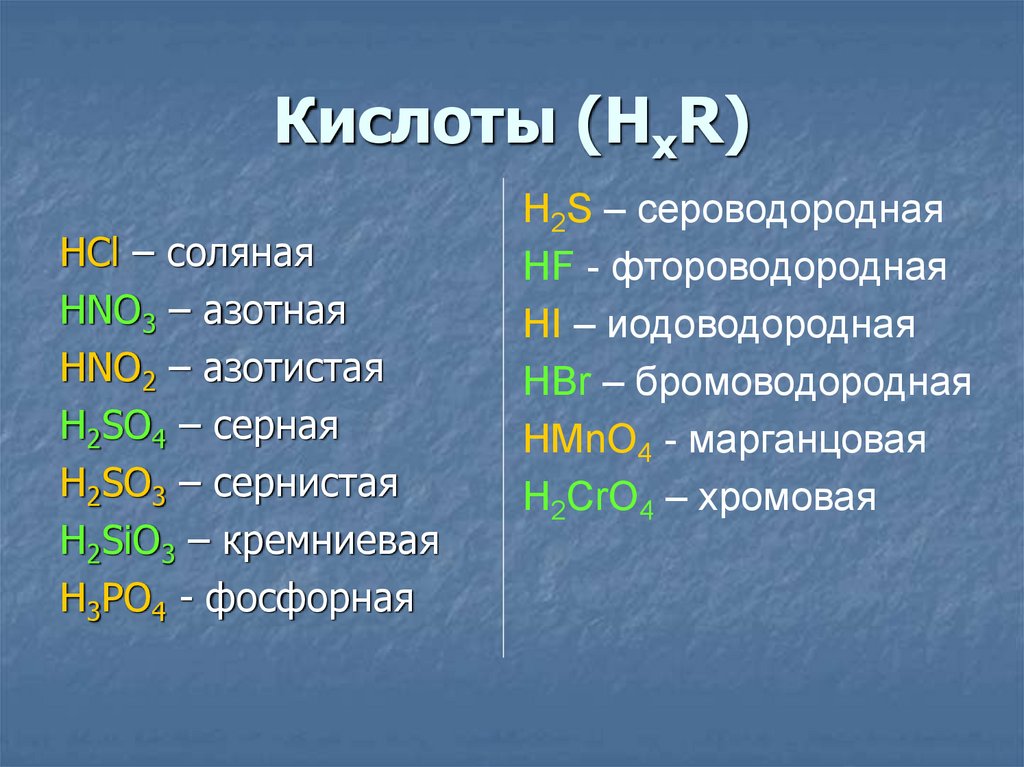
9. Кислоты (НхR)
HCl – солянаяHNO3 – азотная
HNO2 – азотистая
H2SO4 – серная
H2SO3 – сернистая
H2SiO3 – кремниевая
H3PO4 - фосфорная
H2S – сероводородная
HF - фтороводородная
HI – иодоводородная
HBr – бромоводородная
HMnO4 - марганцовая
H2CrO4 – хромовая
10. Кислоты
По содержанию кислородаКислородосодержащие
(H2SO4, HNO3)
Бескислородные
(HCl, HF, H2S)
По основности
Одноосновные
Двухосновные
(HCl, HBr, HNO3)
(H2SO4, H2CO3)
Трехосновные
(H3PO4)
По силе
Сильные
Средние
Слабые
(HBr, HCl, HNO3)
(H3PO4, HNO2)
(H2CO3,H2SiO3)
11. Соответствие кислот и оксидов
SO2 –SO3 –
CO2 –
P2O5 –
SiO2 –
N 2O 3 –
N 2O 5 –
СrO3 –
Mn2O7 –
H2SO3
H2SO4
H2CO3
H3PO4
H2SiO3
HNO2
HNO3
H2CrO4
HMnO4
12. Основания (Ме(ОН)x)
По растворимости в водеРастворимые – щелочи
Нерастворимые
(NaOH, KOH, Ba(OH)2 )
(Fe(OH)2, Ni(OH)2, Mg(OH)2)
По силе
Сильные -
щелочи
Слабые
13. Соответствие оснований и оксидов
Na2O –Li2O –
K2O –
MgO –
CaO –
BaO –
CrO –
FeO –
NaOH
LiOH
KOH
Mg(OH)2
Ca(OH)2
Ba(OH)2
Cr(OH)2
Fe(OH)2
14. Амфотерные гидроксиды
Zn(OH)2H2ZnO2
Al(OH)3
H3AlO3
Cr(OH)3
HCrO2
Метахромистая
кислота
HAlO2
Метаалюминиевая
кислота
15. Соли
Нормальные (средние)NaCl, Na2SO4, Na3PO4
Кислые
NaHSO4, Na2HPO4, NaH2PO4
Основные
MgOHCl, Al(OH)2NO3
Двойные (смешанные)
KAl(SO4)2, Fe(NH4)2(SO4)2
Комплексные
Na2[Zn(OH)4], K3[Fe(CN)6]
16. Химические свойства оксидов
Вспомните, с какими веществами взаимодействуютоксиды?
Основные оксиды
1) С кислотами
2) С водой
3) С кислотными оксидами
Кислотные оксиды
1) С растворимыми основаниями (щелочами)
2) С водой
3) С основными оксидами
17. Химические свойства кислот
Вспомните, с какими веществами взаимодействуюткислоты ?
1) с металлами
2) с основными оксидами
3) с основаниями
4) с солями
5) разлагаются при нагревании
18. Химические свойства оснований
Вспомните, с какими веществами взаимодействуютоснования?
1) с кислотами
2) растворимые основания (щелочи) с солями
3) Растворимые основания (щелочи) с кислотными
оксидами
4) нерастворимые разлагаются при нагревании
19. Химическая свойства солей
Вспомните, с какими веществами взаимодействуютсоли?
1) с металлами
2) с кислотами
3) с растворимыми основаниями (щелочами)
4) с растворами солей
5) нерастворимые при нагревании разлагаются

















 Химия
Химия








