Похожие презентации:
Металлы
1.
12.
Быть символом не каждому дано,Но именем моим не без причины
Назвали руки, дождь, тельца, руно,
Сечение и мнений середину.
И в честь меня был назван даже век,
Когда был очень счастлив человек.
Иду на мелкую монету,
В колоколах люблю звенеть,
Мне ставят памятник за это
И знают: мое имя Из глины я обыкновенной,
Но я на редкость современный.
Я не боюсь электротока,
Бесстрашно в воздухе лечу;
Служу на кухне я без срока Мне все задачи по плечу.
Горжусь я именем своим :
И зовусь я….
2
3. Металлы – химические элементы и простые вещества
34.
План урока1.Хим. элементы металлы (Ме):
а) положение в ПСХЭ Д.И. Менделеева
б) особенности электронного строения атомов.
2.Простые вещества Ме:
а) структура простых веществ, общие физические свойства.
б) общие химические свойства.
4
5.
1. На какие группы можно разделить простые вещества?2. Из приведённых ниже формул веществ назовите
формулы металлов:
Ca, P4, Li, O3, Br2, N2, K, Cl2. Ответ обоснуйте.
Ca, Li, K
5
6.
№ 1.1. Изобразите схемы строения электронных оболочек
атомов магния и алюминия. Укажите признаки сходства и
различия.
2. Какой из химических элементов сильнее проявляет
металлические свойства? Почему?
№ 2.
Дайте характеристику химическому элементу железу по
положению в ПСХЭ и строению атома. Укажите свойства
и возможные значения валентности.
№ 3.
1. В какую частицу превратится атом, отдав или приняв
электроны до завершения внешнего уровня?
Саo – 2 е →
No + 3 е →
6
7.
- Какие химические элементы относят к металлам?- Какое строение атома характерно для элементовметаллов?
- Какое положение в ПСХЭ занимают химические
элементы-металлы? Почему?
- Расположите в ряд по возрастанию числа валентных
электронов металлические элементы: стронций, хром,
рубидий, марганец, олово, галлий, осмий ванадий.
- Как периодически изменяются свойства элементов при
продвижении по периодам (слева направо) и по Агруппам (сверху вниз)?
- Какие значения степеней окисления могут проявлять
металлы?
7
8.
1 группа: Металлическая связь и металлическаякристаллическая решетка.
1.Какой тип кристаллической решётки в металлах?
2.Какую связь называют металлической?
3.Что находится в узлах кристаллической решётки
металлов?
4.Чем связаны узлы кристаллической решетки?
М0 – n е
Мn+
атомы
металла
ионы
металла
•связь в металлах и сплавах между атом-ионами
посредством обобществлённых электронов называют
металлической
8
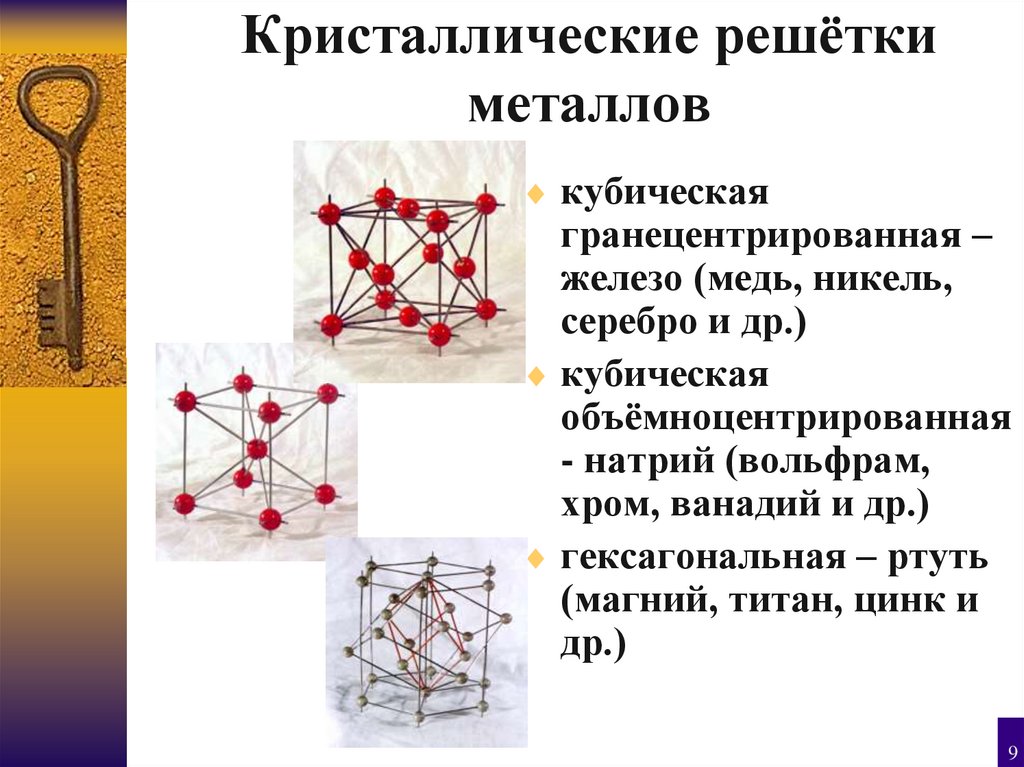
9. Кристаллические решётки металлов
кубическаягранецентрированная –
железо (медь, никель,
серебро и др.)
кубическая
объёмноцентрированная
- натрий (вольфрам,
хром, ванадий и др.)
гексагональная – ртуть
(магний, титан, цинк и
др.)
9
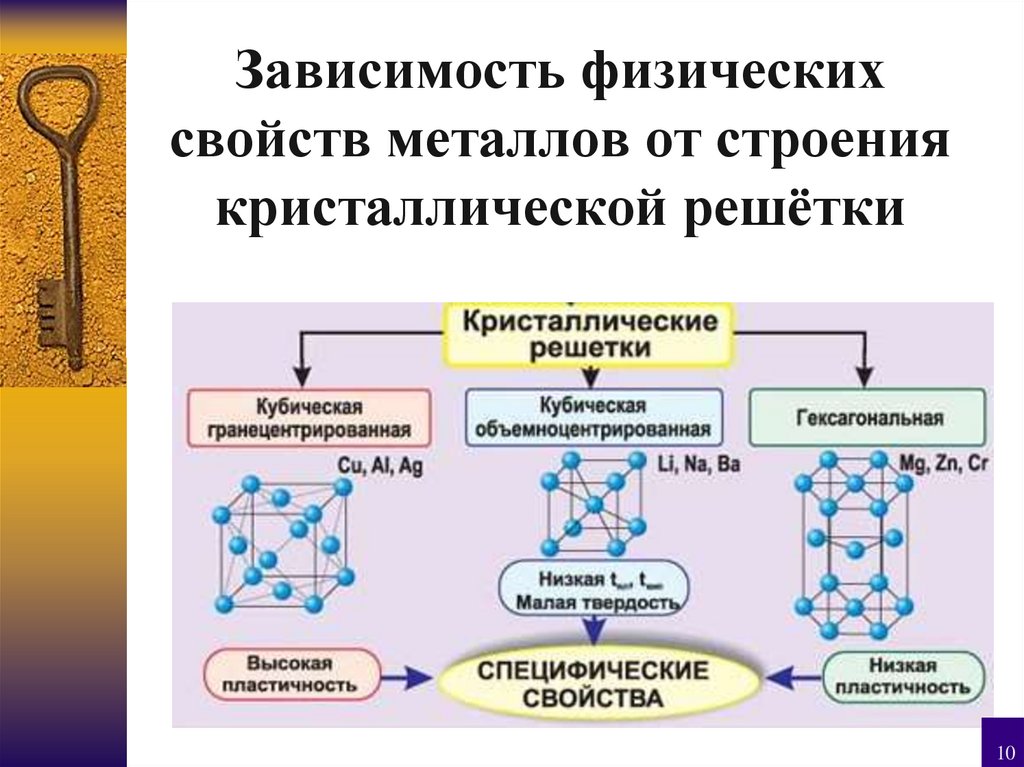
10. Зависимость физических свойств металлов от строения кристаллической решётки
1011.
2 группа: Общие физические свойства и строениеметаллов
- Какие физические свойства характерны для веществ с
металлической кристаллической решёткой?
-Какая существует зависимость между физическими
свойствами и строением кристаллической решетки
металла?
11
12. Металлический блеск
металлическийблеск
–
электроны,
заполняющие
межатомное
пространство
отражают световые лучи, а не пропускают как
стекло.
Поэтому
все
металлы
в
кристаллическом
состоянии
имеют
металлический блеск.
12
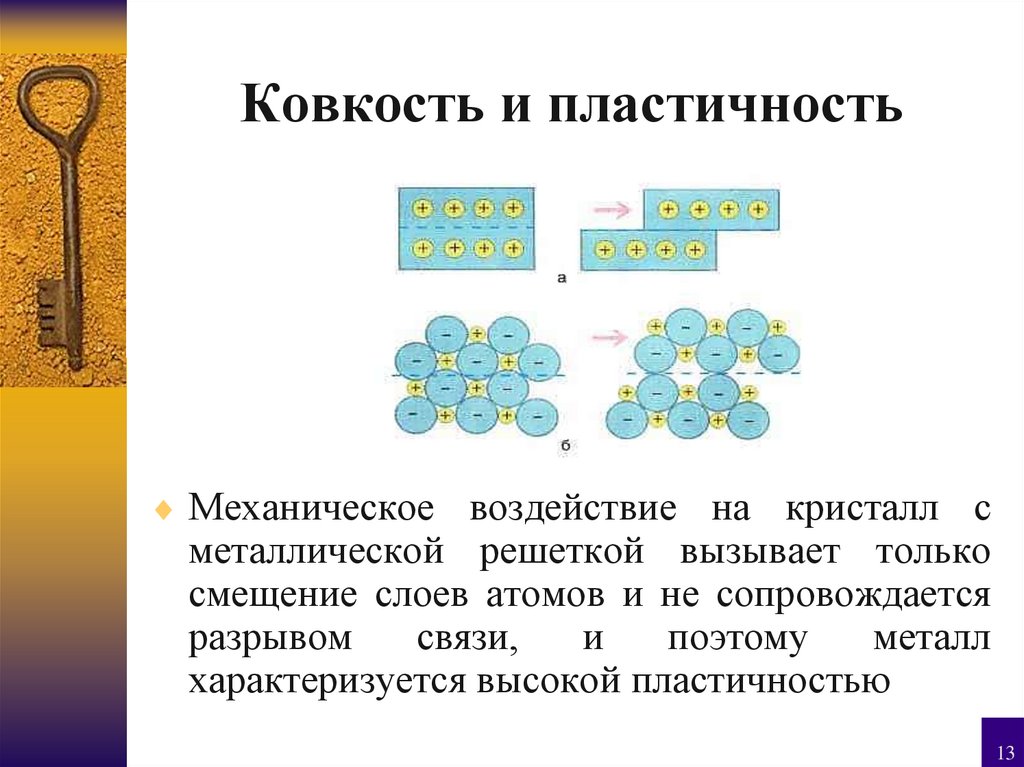
13. Ковкость и пластичность
Механическое воздействие на кристалл сметаллической решеткой вызывает только
смещение слоев атомов и не сопровождается
разрывом
связи,
и
поэтому
металл
характеризуется высокой пластичностью
13
14. Обладают тепло- и электропроводностью
Хаотически движущиеся электроны поддействием
электрического
поля
приобретают направленное движение, в
результате чего возникает электрический
ток.
14
15. Классификация металлов по физическим свойствам
СвойствоКлассификационные группы
Примеры
Электропро
водность
С высокой электропроводностью
Ag, Cu, Au, Al, Mg
С низкой электропроводностью
Mn, Pb, Hg
Температура
плавления
Легкоплавкие
Hg, Ga, Cs, In, Bi
tпл(Hg) =-38,9°С
Тугоплавкие
W, Mo,V,Cr
tпл (W) = 3420 °С
Лёгкие
Li, K, Mg, Na
ρ (Li) =0,53 г/см3
Тяжёлые
Os, Ir, Pb
ρ (Os) =22,6 г/см3
Мягкие
In, Na, K, Rb
(режутся ножом)
Твёрдые
Mo, Cr
(царапают стекло)
Плотность
Твёрдость
15
16. Магнитные свойства металлов
Ферромагнетики– металлы способные
сильно намагничиваться и долго сохранять
это свойство (Fe, Co, Ni).
Парамагнетики – слабо намагничиваются и
не сохраняют это состояние вне магнитного
поля (щелочные, щелочно-земельные и
большая часть переходных металлов).
Диамагнетики – металлы, выталкиваемые
магнитным полем (Cu, Аg, Au, Bi).
16
17. Это интересно…
плотность самоголёгкого металла
лития равна 0,53
г/см3;
литий настолько
лёгок, что плавает в
керосине;
плотность самого
тяжёлого металла
осмия равна 22,6 г/см3
17
18.
3 группа: Химические свойства металлов1. Какие свойства проявляют в химических реакциях
простые вещества металлы?
2. Напишите уравнения реакций:
натрий + вода →?
серебро + вода →?
цинк + раствор сульфата меди (II) →?
серебро + раствор хлорида меди (II) →?
алюминий + раствор карбоната натрия →?
натрий + раствор карбоната алюминия →?
Zn + H2SO4(К) →?
Zn + H2SO4(К) →?
Zn + H2SO4(К) →?
18
19.
Найдите ошибку в синквэйне:1. Металлы
2.Блестящие, ковкие
3.Окисляются, растворяются, замещаются
4.Имеют молекулярную кристаллическую
решетку
5.Восстановители
19
20. Вопросы для самоконтроля
Какое положение в периодической системезанимают металлы и почему?
Какую химическую связь называют
металлической?
Какими общими физическими свойствами
обладают простые вещества металлы? Почему?
Назовите самый тугоплавкий и легкоплавкий
металлы?
Назовите самый лёгкий и тяжёлый металлы?
Какие металлы являются лучшими проводниками
электрического тока?
Как можно использовать общие физические
свойства металлов?
20
21.
Тест1) Электронная формула кальция.
а) 1S² 2S² 2P 3S¹
б) 1S² 2S²2P 3S²
в) 1S² 2S² 2P 3S² 3P 4S¹
г) 1S² 2S² 2P 3S ²3P 4S²
2) Электронную формулу 1S²2S² 2P 3S² 3P 4S² имеет атом:
а)Na
б)Са
в)Cu
г)Zn
3) Электронная формула наиболее активного металла:
а) 1S² 2S²
б) 1S² 2S² 2P 3S²
в) 1S² 2S² 2P 3S² 3P 3d 4S²
г) 1S² 2S² 2P 3S² 3P 4S²
4) Металлы при взаимодействий с неметаллами
проявляют свойства:
а) окислительные;
б) восстановительные;
в) и окислительные, и восстановительные;
г) не участвуют в окислительно-восстановительных реакциях.
5) В периодической системе типичные металлы расположены в:
а) верхней части
б) нижней части
в) правом верхнем углу
г) левом нижнем углу
21
22.
д/з § 19Устно вопросы 1 – 5
Творческое задание на выбор:
А) составить кроссворд по теме урока
Б) найти загадки о металлах
В) написать стихотворение или сказку по теме
урока
22



















 Химия
Химия








