Похожие презентации:
Электролиз. Получение металлов при получении электролиза
1.
Электролиз. Получениеметаллов при получении
электролиза
Выполнил: ученик 11 класса
Напалков Станислав Геннадьевич
2.
ЭлектролизЭлектролизом называется химический процесс при
постоянном токе, заставляющий перемещаться ионы в
требуемом направлении. Этот процесс нашел применение
в многих отраслях промышленности – химической,
металлургической и других. Любой раствор состоит из
частиц, которые имеют положительный и отрицательный
заряды. Такое состояние является нестабильным, так как
противоположные заряды притягиваются. Таким образом
появляется частица с нейтральным зарядом или другими
словами новая молекула другого вещества. В статье будет
описан механизм электролиза, как он происходит,
работает, в каких сферах он нашел применение. Самый
распространенный электролиз которым все пользуются
каждый день.
3.
Применение электролизаЭлектролиз широко применяется для осуществления
следующих процессов:
– Получение веществ в чистом состоянии.Этот процесс
используется для того, чтобы обработать горные породы и
получить чистые вещества. Так образуются алюминий,
двуокись марганца, водород, перекись водорода.
– Очистка сточных вод.В результате помещения в такие
растворы электролитов происходит не только
обеззараживание воды, но и образование взвесей,
которые выпадают в осадок.
– Нанесение тонких покрытий.Под воздействием тока ионы
металла осаждаются на предмете, формируя тонкую
декоративную или защитную плёнку.
4.
Промышленное применение электролизаЭлектролиз широко используется в следующих сферах
промышленности:
• Выделение и очистка металлов.
• Получение алюминия, магния, натрия, кадмия.
• Получение щелочей, хлора, водорода.
• Очистка меди, никеля, свинца.
• Процессы напыления защитных покрытий с целью
защиты металлов от коррозии.
5.
ЭлектрометаллургияЭлектролитическим путём в промышленности получают
многие металлы:
– алюминий
– медь
– магний
– хром
– титан и др.
Например, для получения чистого алюминия в специальную
металлическую ванну вливают расплавленную при 900 °С
руду, содержащую алюминий в химически связанном виде
(обычно в виде оксидов). В ванну опускают угольные
стержни, которые служат анодами, а сама ванна – катодом.
При прохождении тока через расплав на дне ванны
выделяется жидкий алюминий, который сливают через
отверстие внизу ванны.
6.
Рафинирование (очистка) медиМедь, применяемая в электро- и
радиотехнике для изготовления
проводников, должна быть чистой, поскольку
примеси уменьшают электропроводность.
Для очистки меди от примесей в
электролитическую ванну заливают раствор
сульфата меди II (устаревшее название –
медный купорос) и опускают две пластины:
анод – толстую пластину из неочищенной
меди и катод – тонкий лист из чистой меди.
7.
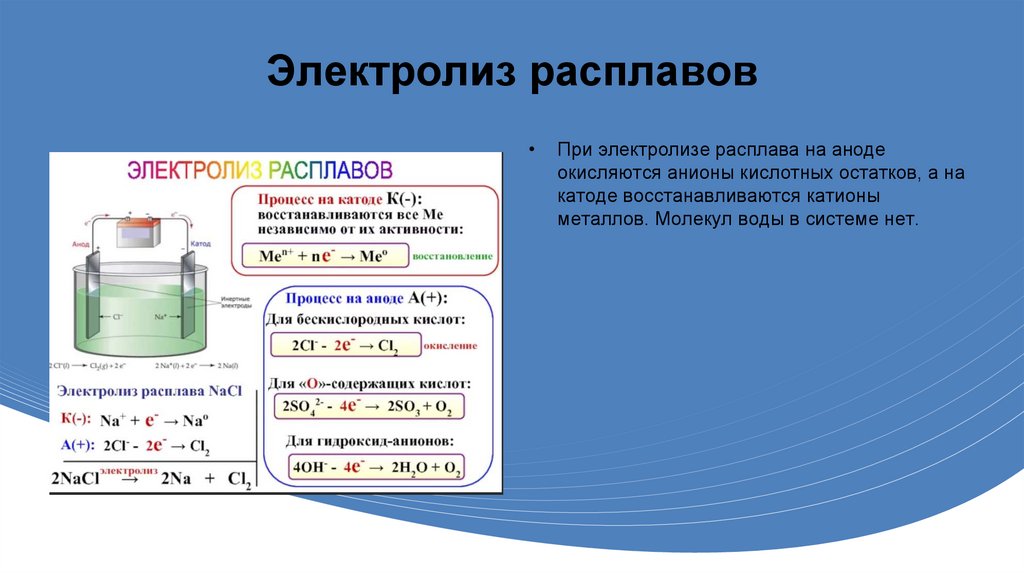
Электролиз расплавовПри электролизе расплава на аноде
окисляются анионы кислотных остатков, а на
катоде восстанавливаются катионы
металлов. Молекул воды в системе нет.
8.
Получение алюминияАлюминий получают электролизом раствора
оксида алюминия в расплаве криолита.
Криолит – Na3[AlF6] плавится при более
низкой температуре (1100оС), чем оксид
алюминия (2050оС). А оксид алюминия
отлично растворяется в расплавленном
криолите.
9.
ГальваностегияДля придания изделиям красивого внешнего
вида, прочности или для предохранения от
коррозии, их покрывают тонким слоем
какого-либо металла: никеля, хрома и др.
Для этого изделие тщательно очищают,
обезжиривают и помещают как катод в
электролитическую ванну, содержащую соль
того металла, которым желают покрыть. Для
более равномерного покрытия полезно
применять две пластины в качестве анода,
помещая изделие между ними.
10.
ГальванопластикаЭто электролитическое осаждение металла на
поверхности какого-либо предмета для
воспроизведения его формы. Для этого с
предмета сначала снимают слепок (из воска
или гипса) и покрывают его токопроводящим
слоем, например, слоем графита.
Подготовленный таким способом предмет
помещают в качестве катода в ванну с
раствором соли соответствующего металла.
При включении тока металл из электролита
оседает на поверхности предмета.
Гальванопластику используют для
изготовления неограниченного числа точных
копий того изделия, с которого был снят слепок.
11.
ГальванополировкаЕсли резное металлическое изделие поместить
в раствор электролита и включить ток, то
наиболее сильное электрическое поле
образуется у микроскопических выступов на
поверхности этого изделия. Если оно
подключено к «+» источника тока, то наиболее
интенсивно ионы металла будут «вырываться»
именно из выступов, и поверхность металла
выровняется.










 Физика
Физика








