Похожие презентации:
Оксиды. Общая характеристика
1.
Оксиды8 класс
2.
Общая характеристика• Оксиды – соединения, состоящие из атомов
двух химических элементов, один из которых
кислород (в степени окисления -2).
• Оксид алюминия
• Оксид натрия
• Оксид серы (VI)
• Оксид меди (II)
• Оксид железа (III)
3.
Получение оксидов• При окислении простых веществ
кислородом воздуха:
S + O2 = SO2
2Cu + O2 = 2CuO
4Al + 3O2 = 2Al2O3
• При разложении нерастворимых в воде
оснований:
Cu(OH)2 = CuO + H2O
• При разложении некоторых солей:
CaCO3 = CaO + CO2
4.
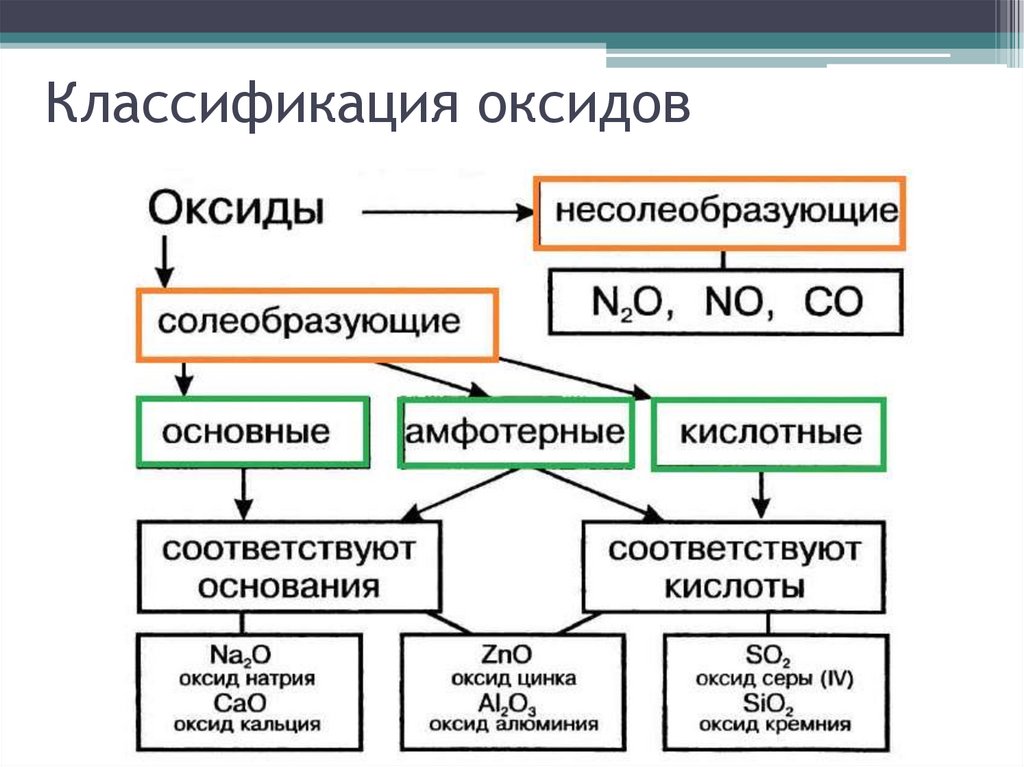
Классификация оксидов5.
Оксиды, образующие соли при взаимодействии с кислотамиили щелочами, называют солеобразующими.
Солеобразующие оксиды бывают основными, кислотными
или амфотерными.
Несолеобразующие оксиды (индифферентные,
безразличные) солей не образуют.
Основным оксидам соответствуют основания.
Обычно это оксиды металлов с валентностью I и II.
Кислотным оксидам (ангидридам кислот) соответствуют
кислоты. Обычно это оксиды неметаллов и металлов,
имеющих валентность выше IV.
Амфотерные оксиды проявляют двойственность (основные
и кислотные свойства, в зависимости от условий).
6.
• Валентность хрома: II, III, VI .• Оксид хрома (II) – основный
• Оксид хрома (III) – амфотерный
• Оксид хрома(VI) - кислотный
7.
8.
Физические свойства оксидовКислотные оксиды:
• Почти все имеют молекулярное строение
• Газы (углекислый газ CO2, сернистый газ SO2)
• Жидкости (серный ангидрид SO3)
• Твердые вещества (фосфорный ангидрид P2O5,
кварц SiO2)
Основные и амфотерные оксиды:
• Твердые вещества немолекулярного строения.
9.
Химические свойства оксидовОсновные оксиды
Кислотные оксиды
1. О. оксид + кислота
= соль + вода
1. К. оксид + щелочь!
= соль + вода
2. Основный оксид + кислотный оксид = соль
3. О. оксид + вода =
3. К. оксид + вода =
основание (щелочь!)
кислота
Реакция протекает только в
том случае, если образуется
растворимое основание
(щелочь).
кроме SiO2 (песок)








 Химия
Химия








