Похожие презентации:
Врожденный иммунитет
1. ВРОЖДЕННЫЙ ИММУНИТЕТ
2. План лекции
Классификация факторовврожденного иммунитета
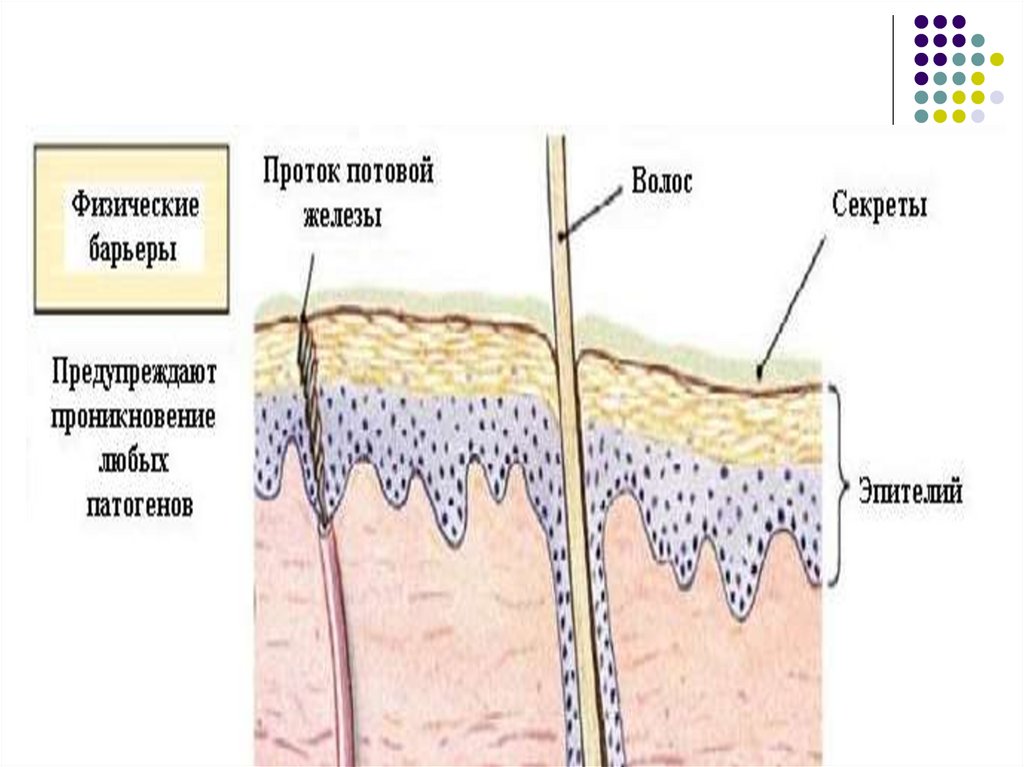
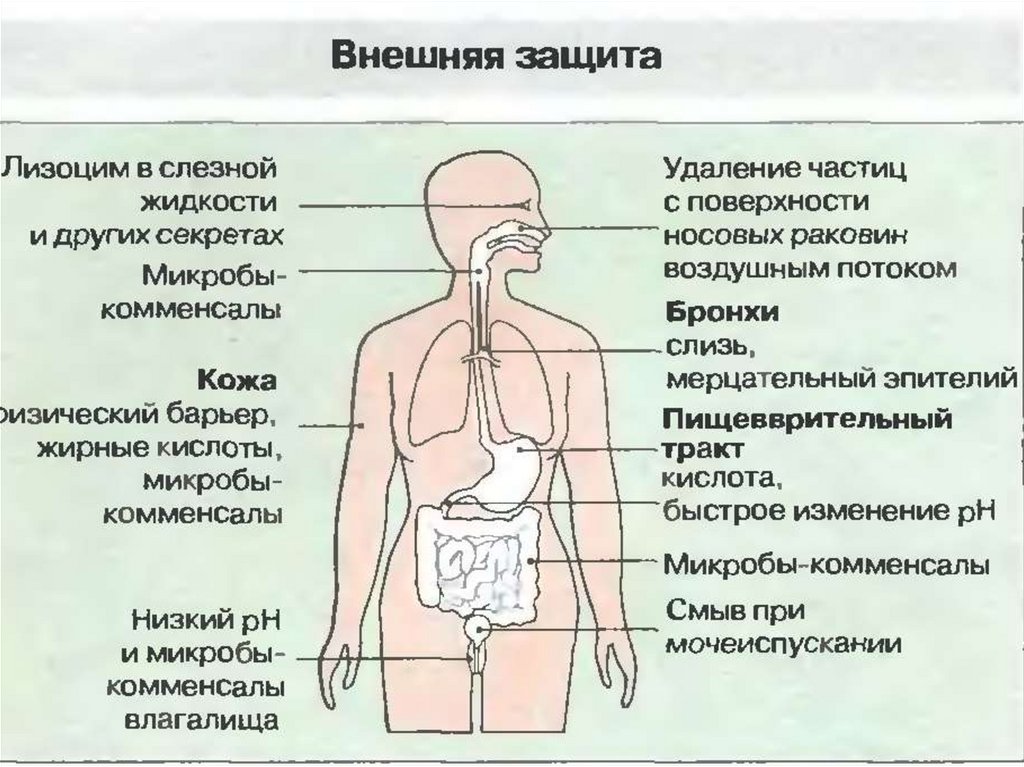
Внешние барьеры
Внутренние барьеры
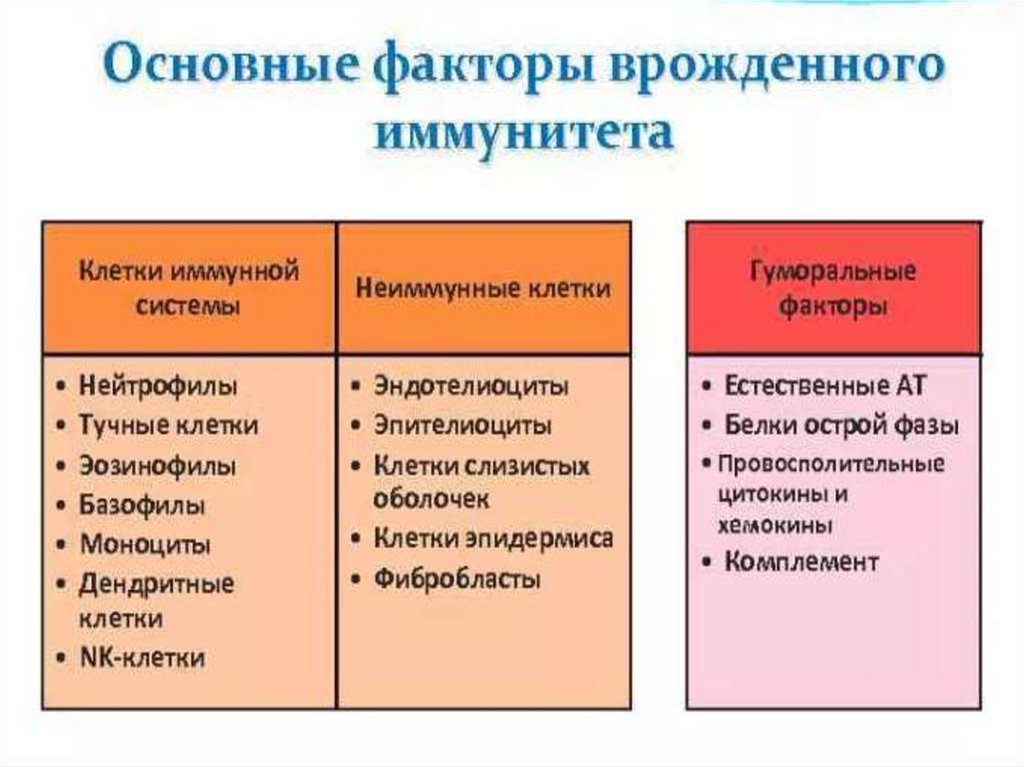
Клеточные факторы
Гуморальные факторы
3.
Эволюционно иммунная системапредназначена для санации (очистки)
организма от инфекций и удаления чужеродных
агентов.
Общую систему иммунитета можно разделить
на две большие подсистемы – врожденный и
приобретенный иммунитет.
Врожденный иммунитет — наследственно
закрепленная система защиты многоклеточных
организмов от любых патогенных и
непатогенных микроорганизмов, а также
эндогенных продуктов тканевой деструкции.
Как самая ранняя форма иммунной защиты
организма, врожденный иммунитет
сформировался на начальных этапах эволюции
многоклеточных организмов.
4.
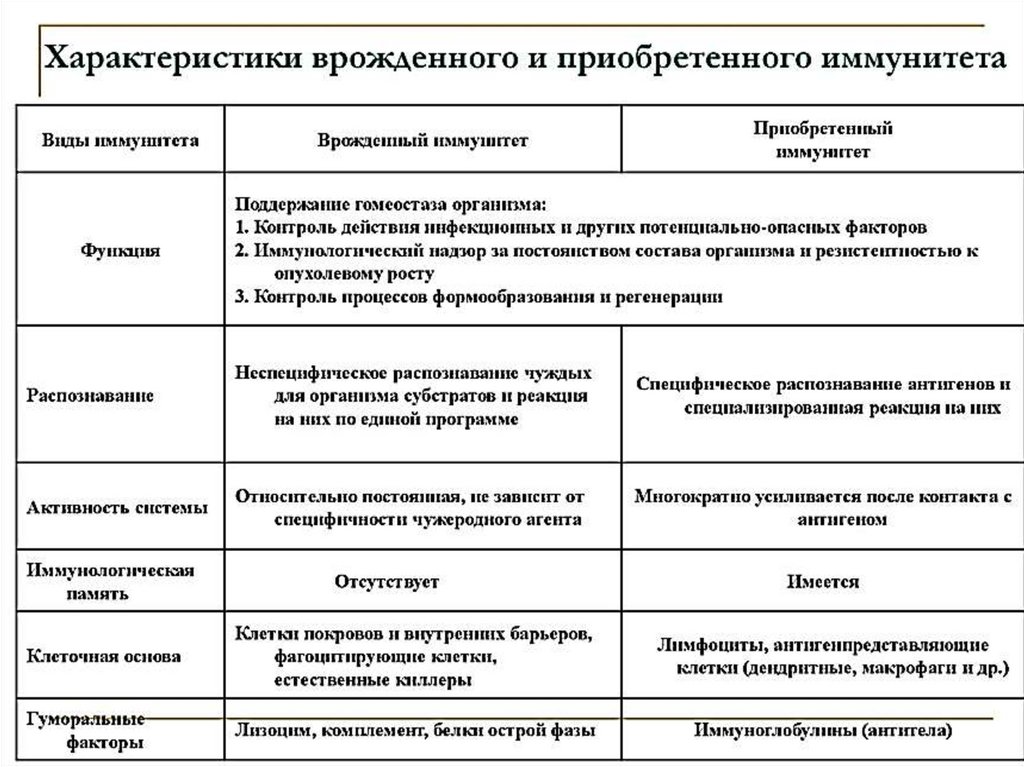
5. Характеристика врожденного и приобретенного (адаптивного) иммунитета
6.
7.
8.
9.
10.
Молекулы –мишени
иммунитета
Образы
патогенности
Стрессорные
молекулы
Антигены
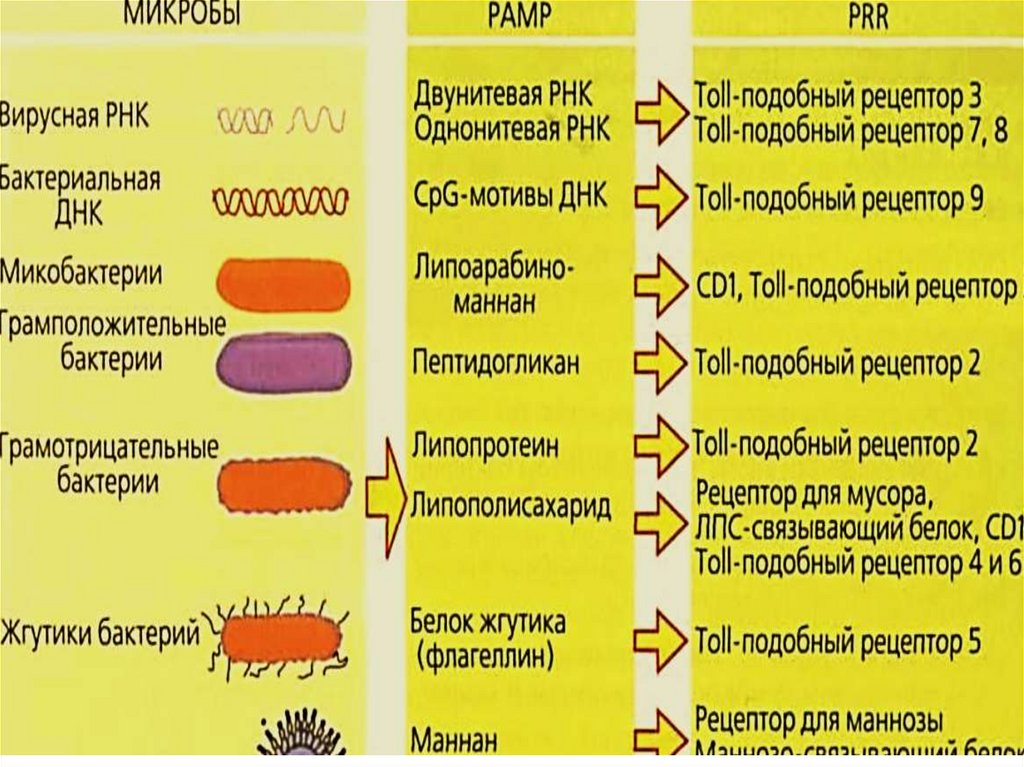
11. Образы патогенности
Образы патогенности или патогенассоциированныемолекулярные паттерны– РАМР (Pathogen-associated molecular
patterns) – группы молекул, как правило, отсутствующие в
организме-хозяине, но характерные для патогенов (вирусов,
бактерий, грибов, простейших, паразитов), они консервативны.
Термин «паттерн» (знак/маркёр опасности) был введен
Р.Меджитовым и Сh. Janeway.
PAMP однозначно связаны с патогенностью и поэтому могут
рассматриваться как знаки опасности, наиболее универсальный
сигнал о проникновении в организм не просто чужеродного, но
биологически агрессивного агента.
Рецепторы для PAMP - PRR (паттернраспознающие рецепторы)
позволяют распознавать все возможные типы патогенов и
представлены у всех многоклеточных организмов (животных,
растений).
Узнавание PAMP — основа распознавания во врожденном
иммунитете, в определенной степени PAMP способны узнавать
и клетки адаптивного иммунитета.
12.
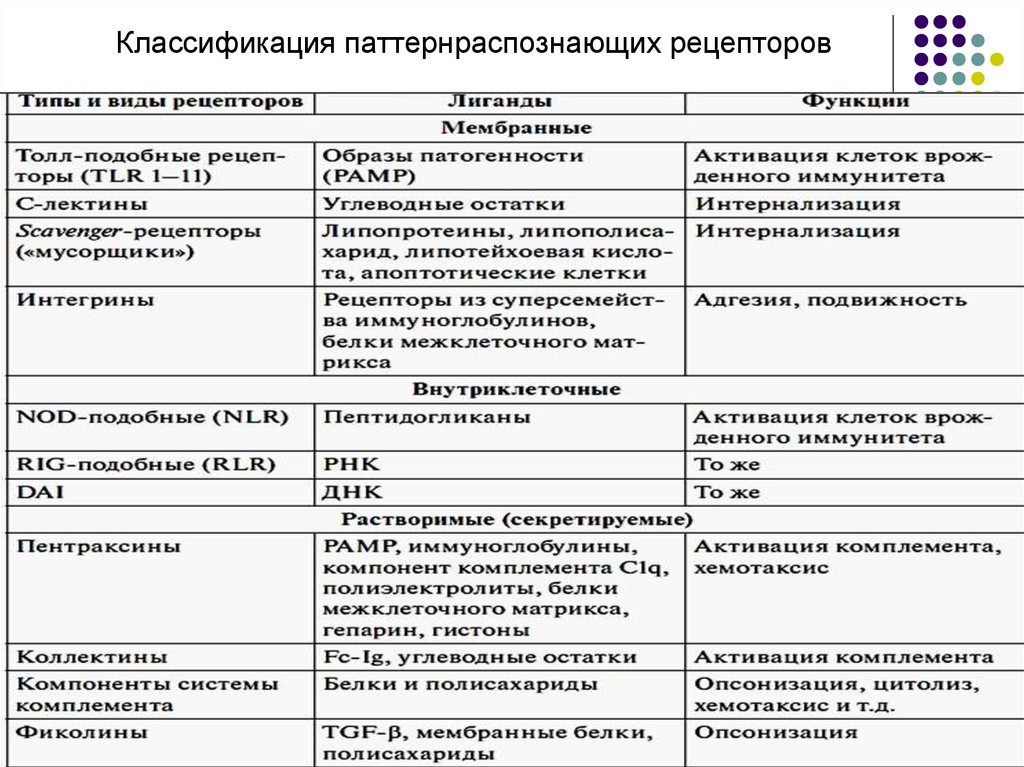
13. Классификация паттернраспознающих рецепторов
14. Стрессорные молекулы
Стрессорные молекулы — собственные молекулыорганизма, экспрессируемые на мембране при клеточном
стрессе и сигнализирующие преимущественно об опасности
эндогенного происхождения. Они распознаются рецепторами
некоторых разновидностей лимфоцитов (например,
естественными киллерами). По своей активности эти
молекулы и их рецепторы занимают промежуточное
положение между врожденным и адаптивным иммунитетом.
Родственную группу молекул образуют образы
опасности (danger-associated molecular patterns) - DAMP —
эндогенные молекулы, сигнализирующие о любом
повреждающем воздействии (температурном, лучевом,
инфекционном и т.д.); эти процессы не полностью
контролируются иммунной системой.
15.
Главную роль в противоинфекционнойзащите играет не иммунитет, а
разнообразные механизмы механического
удаления микроорганизмов (клиренса)
Система иммунитета включается тогда,
когда механизмы клиренса не
справляются.
16. Барьерные функции кожи
17.
18.
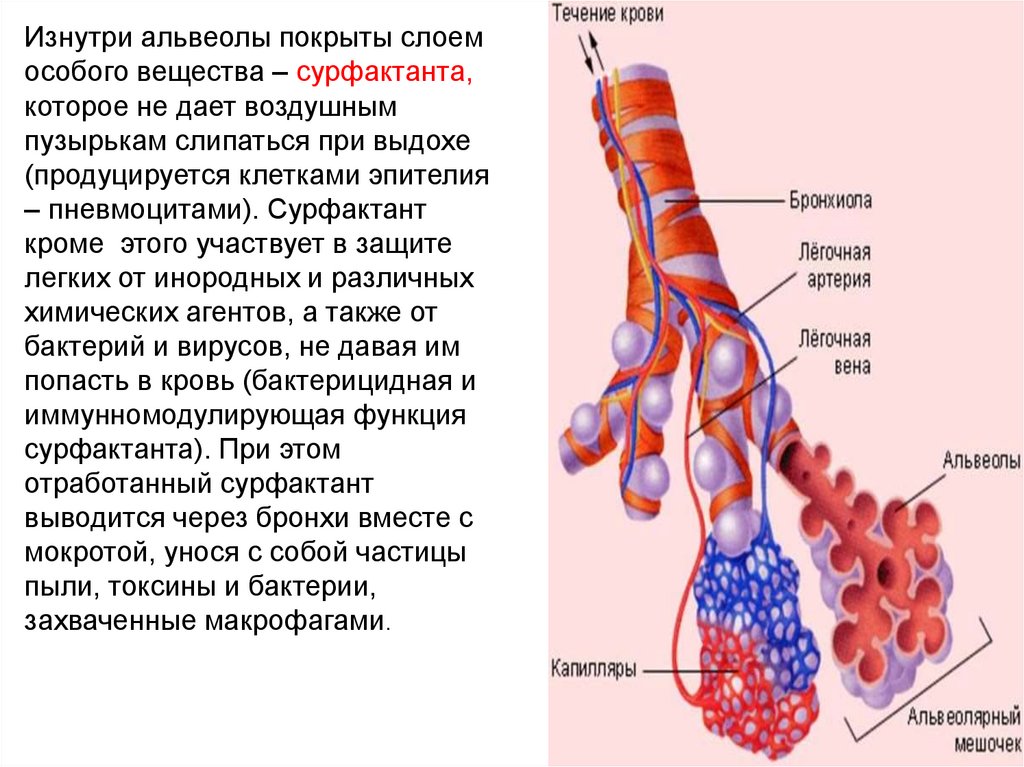
Изнутри альвеолы покрыты слоемособого вещества – сурфактанта,
которое не дает воздушным
пузырькам слипаться при выдохе
(продуцируется клетками эпителия
– пневмоцитами). Сурфактант
кроме этого участвует в защите
легких от инородных и различных
химических агентов, а также от
бактерий и вирусов, не давая им
попасть в кровь (бактерицидная и
иммунномодулирующая функция
сурфактанта). При этом
отработанный сурфактант
выводится через бронхи вместе с
мокротой, унося с собой частицы
пыли, токсины и бактерии,
захваченные макрофагами.
19. ВОСПАЛЕНИЕ
1. Воспаление – это каскад реакций, возникающих как первый(неспецифический) этап защиты организма.
2. Сводится к выходу клеток иммунной системы из кровяного
русла и миграции их в очаг проникновения инфекта.
3. Развитие различных деструктивных эффектов, в результате
чего чужеродные клетки погибают.
4. Основные механизмы подавления инфекта в очаге
воспаления: фагоцитоз (внутриклеточный киллинг),
внеклеточный цитолиз (киллинг), неспецифический
контактный киллинг, гуморальные реакции.
5. Воспалительная реакция служит естественным механизмом
включения реакций специфического иммунитета.
6. Воспаление характеризуется быстротой развития и низкой
специфичность происходящих событий.
20.
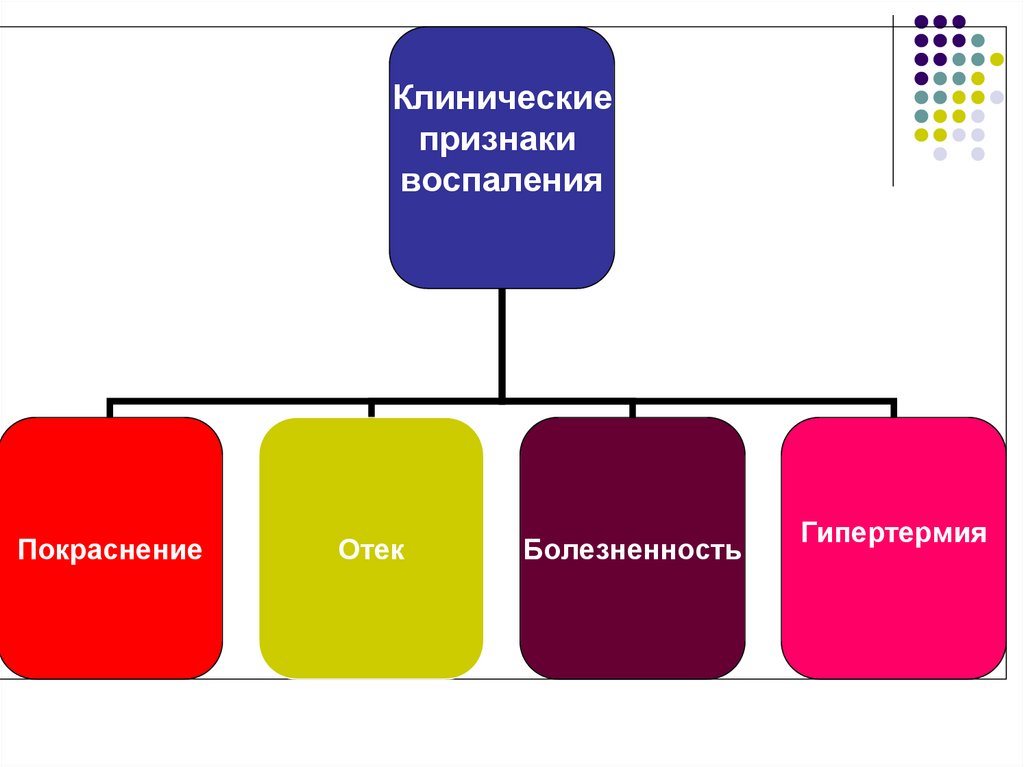
Клиническиепризнаки
воспаления
Покраснение
Отек
Болезненность
Гипертермия
21. Этапы воспаления
1. Сосудистая реакция.2. Миграция лейкоцитов в очаг
воспаления.
3. Нейтрализация и элиминация
возбудителя.
4. Включение механизмов адаптивного
иммунитета.
5. Завершение или хронизация
воспалительного процесса.
22. СОСУДИСТАЯ РЕАКЦИЯ
При проникновении патогена в ответ на воспалительные стимулы(антигены и токсины бактерий, субстрат разрушенных тканей и т.д.)
близлежащие клетки лейкоцитов, эпителия, эндотелия сосудов и других
образований секретируют целый спектр сосудорасширяющих медиаторов
– вазодилататоров (гистамин, брадикинин, простагландин Е2,
простациклин и др.).
Гистамин, брадикинин и некоторые другие медиаторы не только вызывают
расширение сосудов и усиление их кровенаполнения, но изменяют и
состояние клеток эндотелия.
Клетки эндотелия становятся высокими и кубовидными, промежутки между
ними увеличиваются, в результате развивается «протекание сосудов».
«Протекающие сосуды» - это небольшие посткапиллярные венулы.
Сосудистая реакция обеспечивает проникновение в межклеточное
пространство очага воспаления активных белков плазмы (антител,
компонентов комплемента, белков острой фазы и др.)
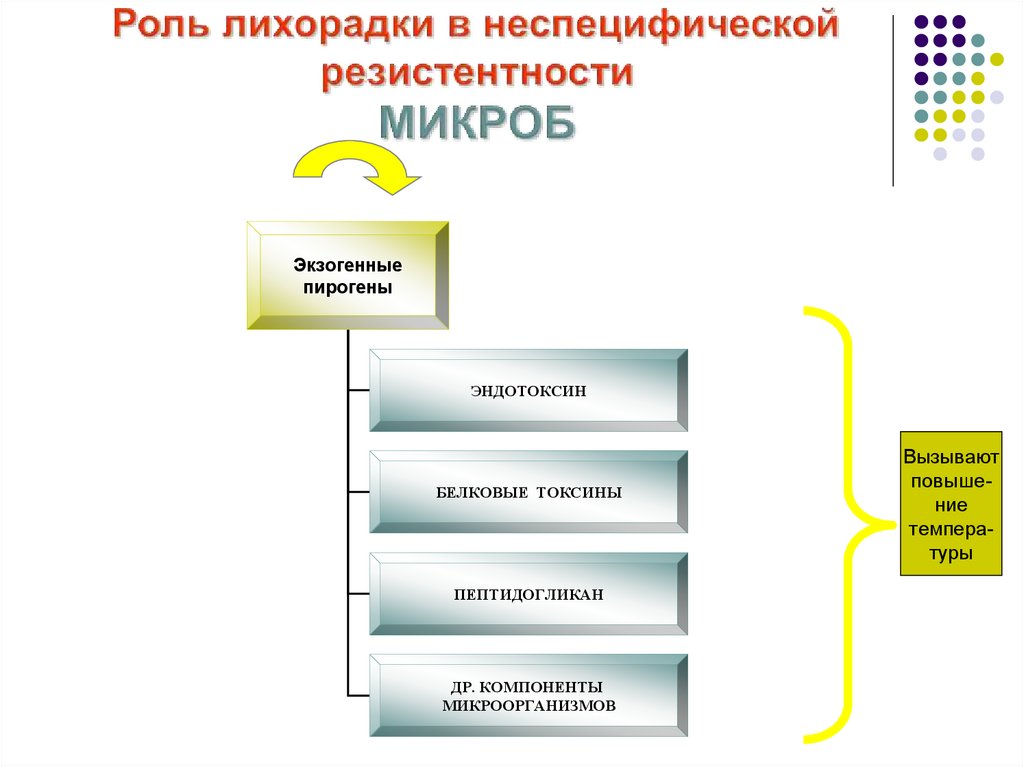
23. Роль лихорадки в неспецифической резистентности МИКРОБ
Экзогенныепирогены
ЭНДОТОКСИН
БЕЛКОВЫЕ ТОКСИНЫ
ПЕПТИДОГЛИКАН
ДР. КОМПОНЕНТЫ
МИКРООРГАНИЗМОВ
Вызывают
повышение
температуры
24.
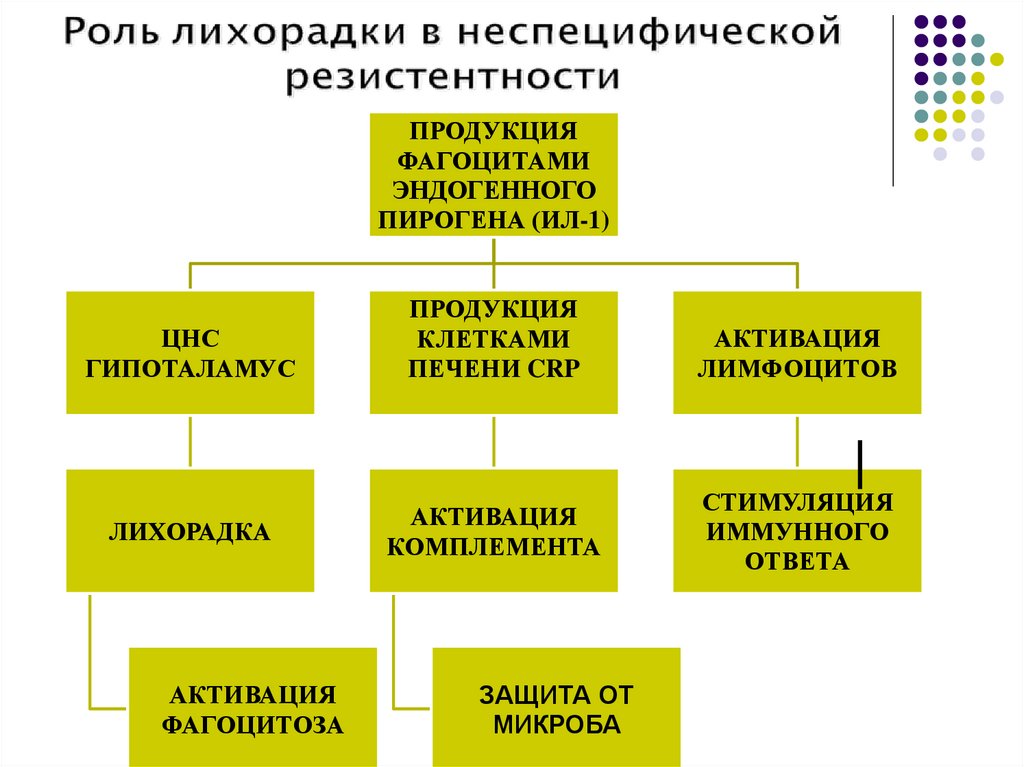
ПРОДУКЦИЯФАГОЦИТАМИ
ЭНДОГЕННОГО
ПИРОГЕНА (ИЛ-1)
ЦНС
ГИПОТАЛАМУС
ЛИХОРАДКА
АКТИВАЦИЯ
ФАГОЦИТОЗА
ПРОДУКЦИЯ
КЛЕТКАМИ
ПЕЧЕНИ CRP
АКТИВАЦИЯ
КОМПЛЕМЕНТА
ЗАЩИТА ОТ
МИКРОБА
АКТИВАЦИЯ
ЛИМФОЦИТОВ
СТИМУЛЯЦИЯ
ИММУННОГО
ОТВЕТА
25. ЭТАПЫ МИГРАЦИИ КЛЕТОК В ОЧАГ ВОСПАЛЕНИЯ
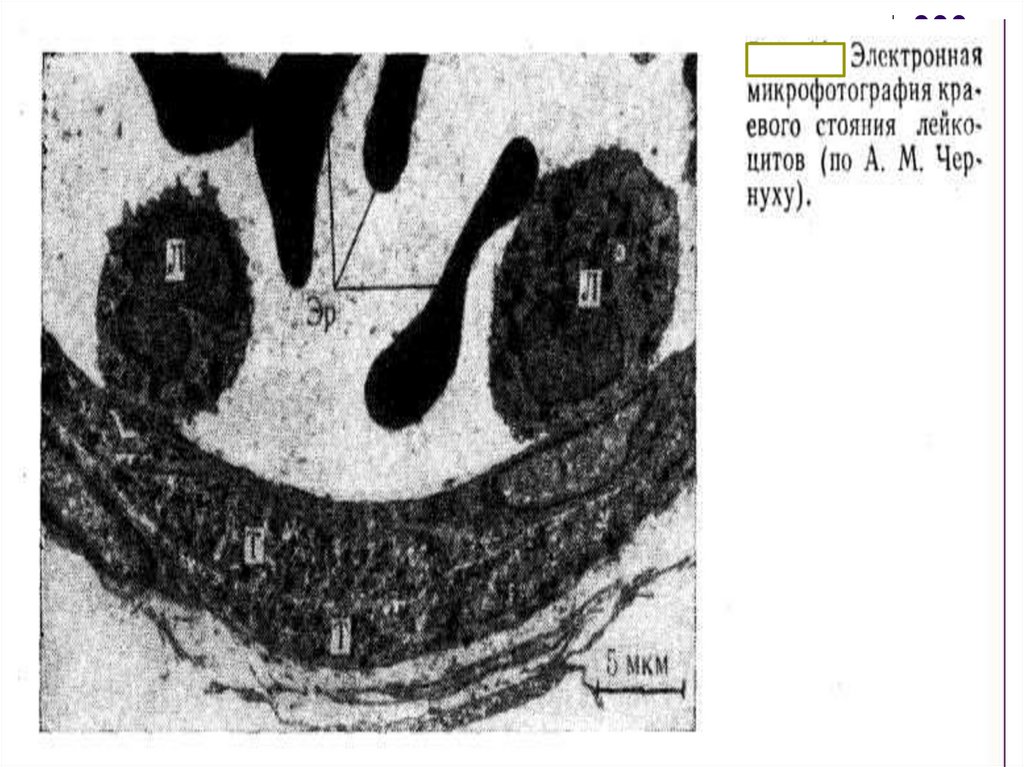
КачениеАдгезия лейкоцитов на эндотелии
Трансэндотелиальная миграция
Хемотаксис – направленная
миграция в очаг воспаления
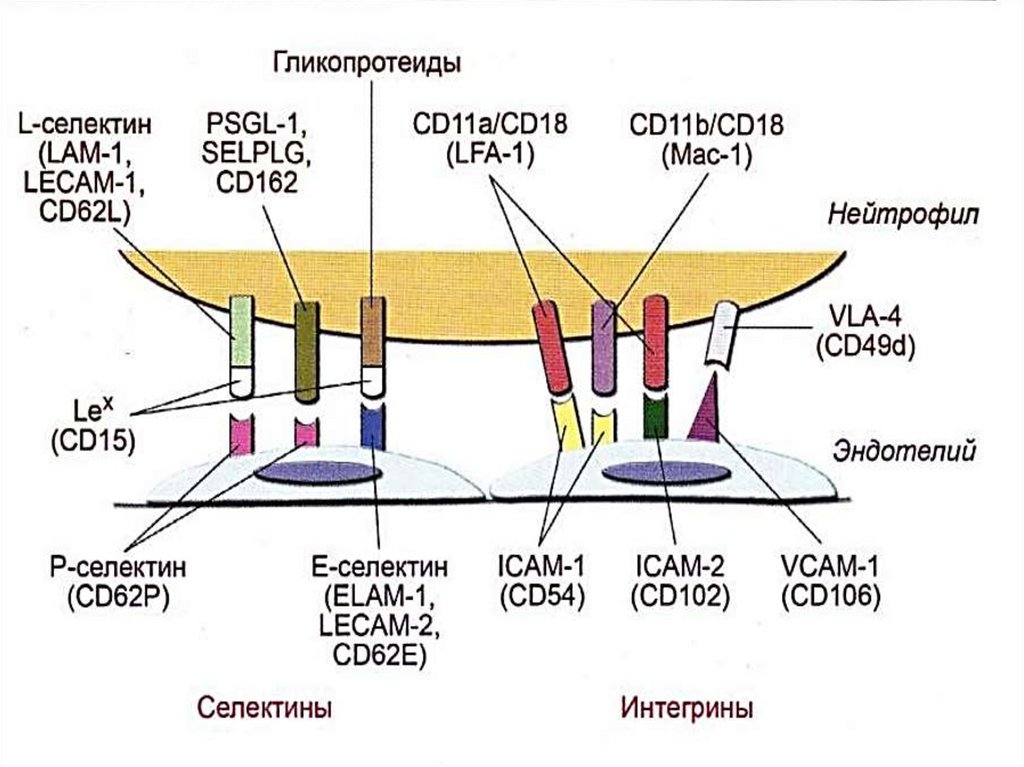
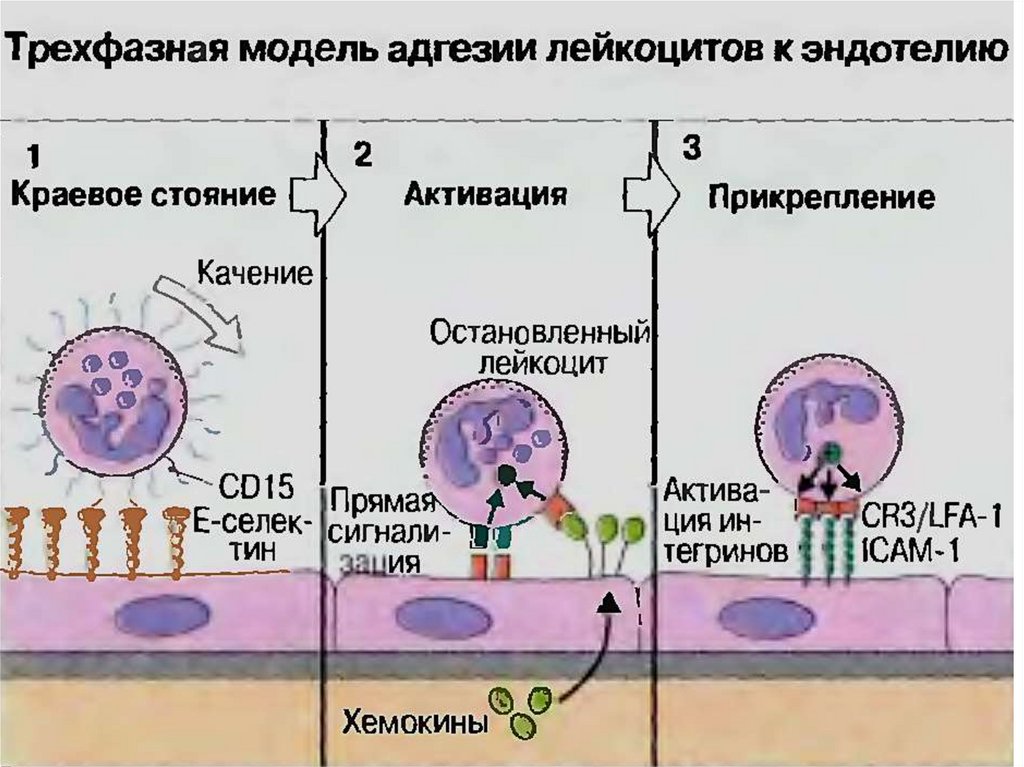
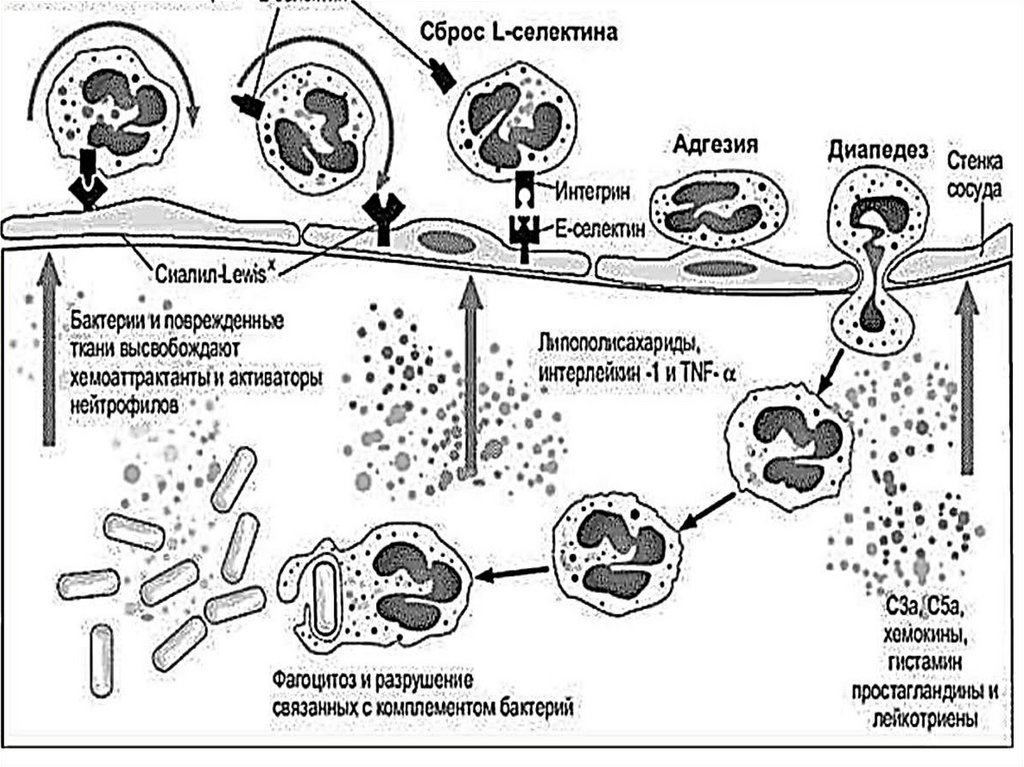
26. ФАЗЫ АДГЕЗИИ ЛЕЙКОЦИТОВ
Первая фаза - движение лейкоцитов в очагевоспаления замедляется, отмечается их «качение»,
что связано с взаимодействием молекул адгезии
(селектинов, углеводных лигандов и др.).
Вторая фаза – активация, при которой лейкоциты
подвергаются действию цитокинов, хемокинов и
других агентов.
Третья фаза – прикрепление, которая
характеризуется полной остановкой движения,
прикреплением к клеткам эндотелия и подготовкой к
проникновению в межэндотелиальное пространство,
этот эффект возникает благодаря взаимодействию
многочисленных молекул адгезии
27.
28.
29.
30.
31. ТРАНСЭНДОТЕЛИАЛЬНАЯ МИГРАЦИЯ
Этот этап характеризуется проникновениемлейкоцитов через стенку сосуда и выходом
во внесосудистое пространство.
В процессе проникновения у лейкоцитов
экспрессируется новый набор адгезинов,
позволяющий им взаимодействовать с
клетками базальной мембраны сосудов,
которую они расплавляют, секретируя
коллагеназу и другие ферменты.
32.
33.
34.
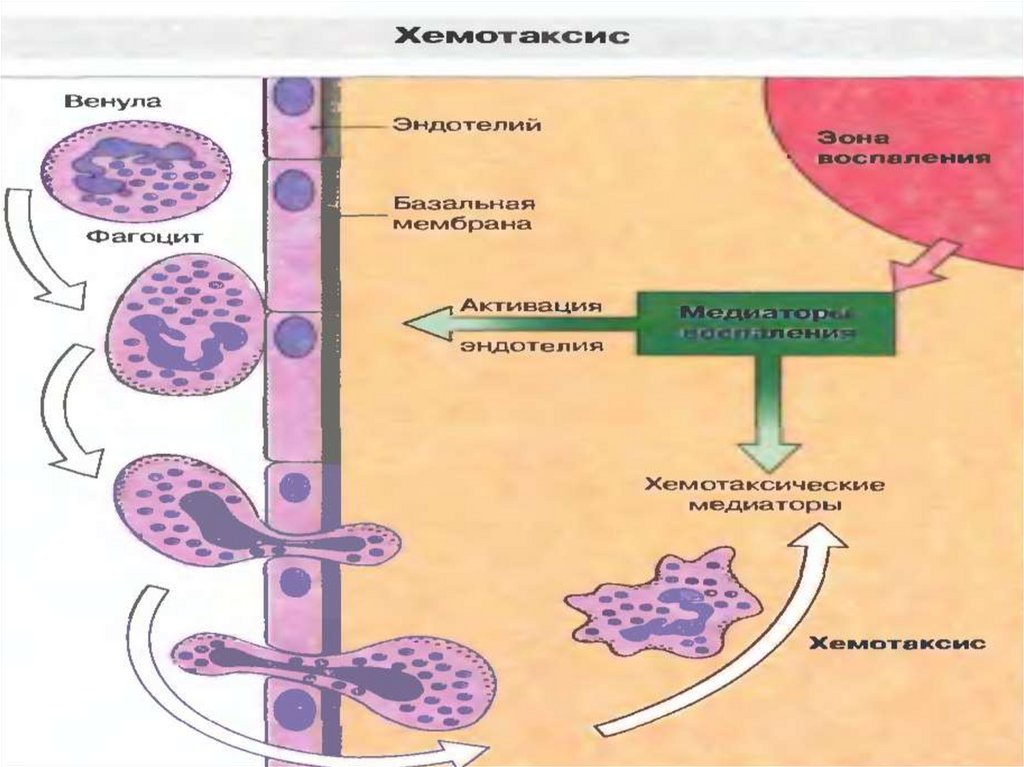
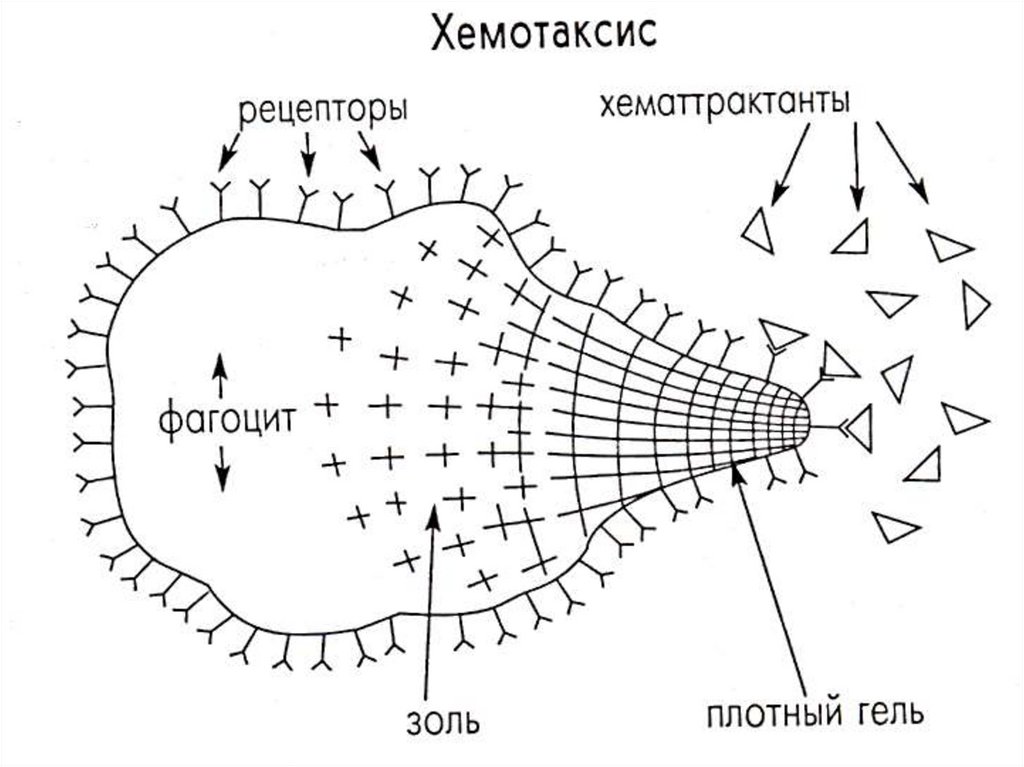
35. ХЕМОТАКСИС
После выхода из кровеносного русла, лейкоцитыосвобождаются от ненужных рецепторов, а на их
поверхности появляются новые рецепторы для
хемотоксических факторов.
Направленность движения лейкоцитов определяется
возрастанием концентрации различных хемотаксических
веществ.
Основные группы хемоаттрактантов:
а) продукты жизнедеятельности микроорганизмов;
б) цитокины, вырабатываемые в очаге воспаления
(ИЛ-1, ФНО-ά, С-реактивный белок (СРБ), гистамин,
лейкотриен В4);
в) компоненты комплемента (С3а, С5а);
г) поврежденные и денатурированные белки;
д) тромбин, фибрин и др.
36.
37. Фагоцит удлиняет полужидкое образование (так называемая ложноножка) в направлении бактерий
38. НЕЙТРАЛИЗАЦИЯ И ЭЛИМИНАЦИЯ ВОЗБУДИТЕЛЯ
Внеклеточный цитолиз (внеклеточныйкиллинг).
Фагоцитоз (внутриклеточный киллинг).
Контактный киллинг.
Нейтрализация и опсонизация
возбудителя гуморальными
факторами врожденного иммунитета.
39.
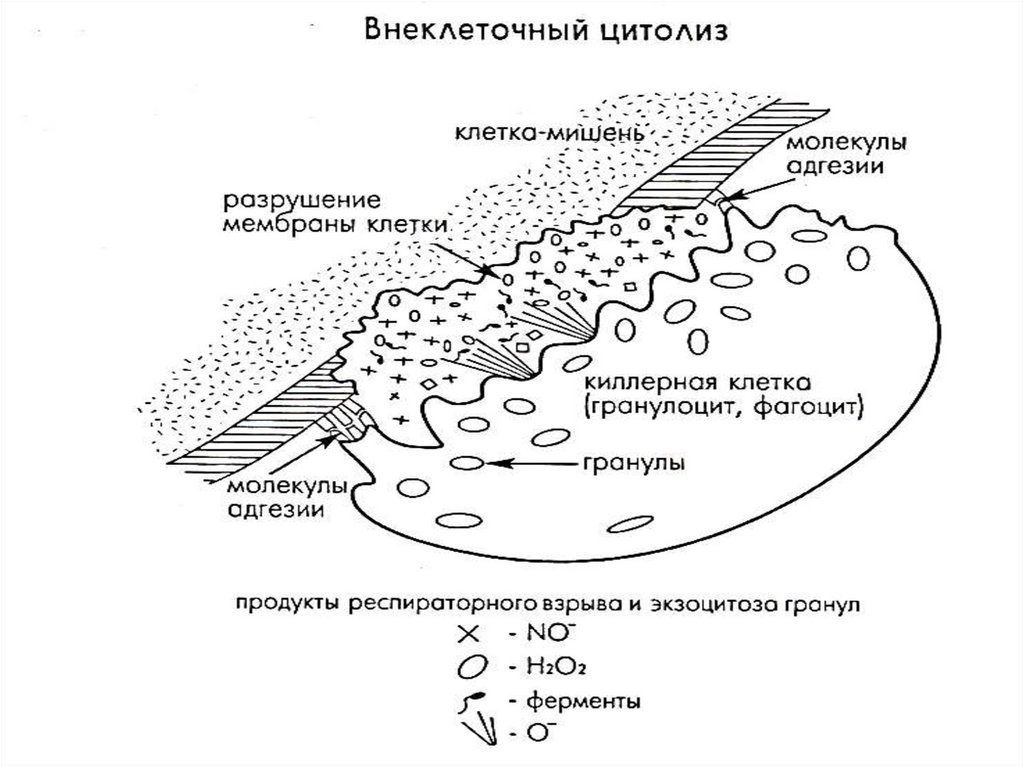
Внеклеточный цитолиз (киллинг) – это процесс убийстваклетки-мишени под действием токсических факторов,
секретируемых во внеклеточную среду клеткойкиллером
Механизмы
внеклеточного
цитолиза
Продукты
респираторного
взрыва
Продукты,
высвобождаемые
из гранул
лейкоцитов
Выделение
окиси азота
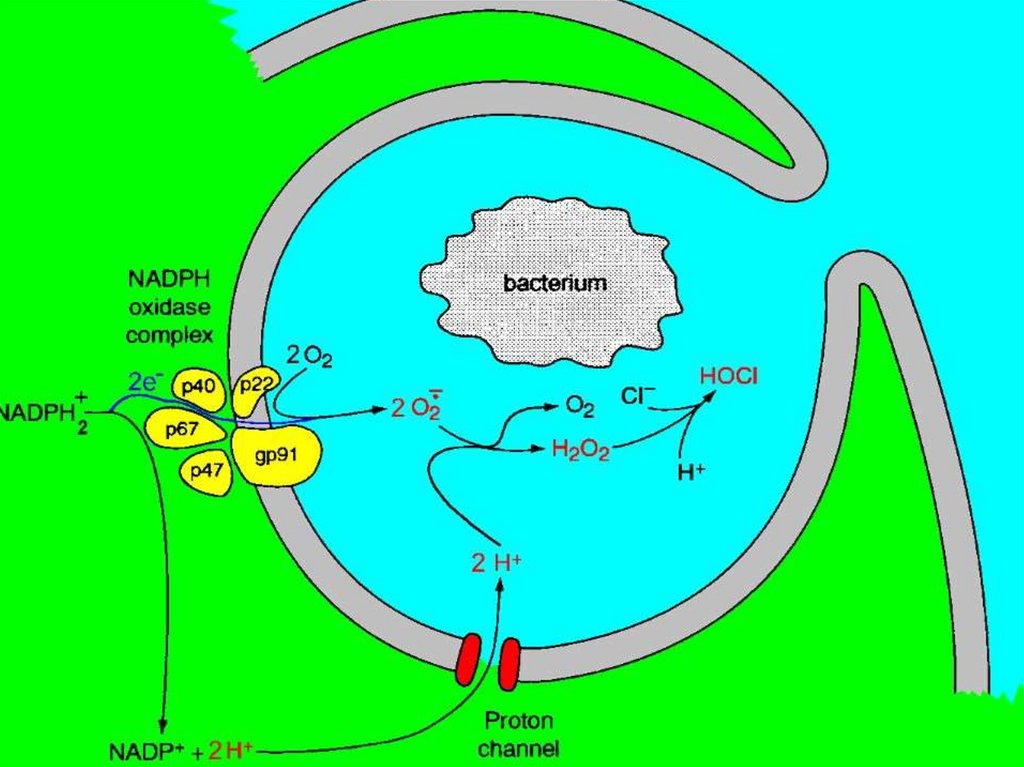
40. Респираторный взрыв
Респираторный взрыв – это каскадреакций, в результате которых образуются
активные формы кислорода
(супероксидный анион, гидроксильные
радикалы, перекись водорода).
Эти продукты воздействуют на
биологический субстрат микроорганизмов,
вызывая его окисление и гибель.
41. Продукция окиси азота
В результате каскада реакций вмакрофагах, нейтрофилах и
некоторых других клетках
происходят реакции метаболизма
аргинина.
В итоге образуется окись азота,
обладающая очень сильным
бактерицидным эффектом.
42. Экзоцитоз (дегрануляция)
Под экзоцитозом понимают процесс высвобождениясодержимого гранул клеток во внеклеточное
пространство.
Этот процесс реализуется клеткой после получения
активирующего сигнала (через рецепторы) и протекает
очень быстро, в течение нескольких часов.
Функции дегрануляции присущи нейтрофилам,
эозинофилам, базофилам, макрофагам, моноцитам.
На сегодняшний день известно более 60 активных
белков и ферментов (миелопероксидаза, катионные
белки, катепсин, лизоцим, лактоферрин и др.).
43.
44. Фагоцитоз (внутриклеточный киллинг))
Под фагоцитозом понимают процесс поглощения объекта клеткойфагоцита с дальнейшим ферментативным разрушением его
структуры.
Фагоцитоз в отдельных своих проявлениях напоминает некоторые
механизмы внеклеточного цитолиза (здесь также огромную роль
играют продукты респираторного взрыва, метаболиты окиси азота и
содержимое гранул).
Отличие от внеклеточного киллинга – процессы происходят внутри
клетки, в замкнутом пространстве фагосомы, куда объект попадает в
результате его захвата псевдоподиями фагоцита.
«Профессиональными фагоцитами» являются: нейтрофилы,
макрофаги, моноциты.
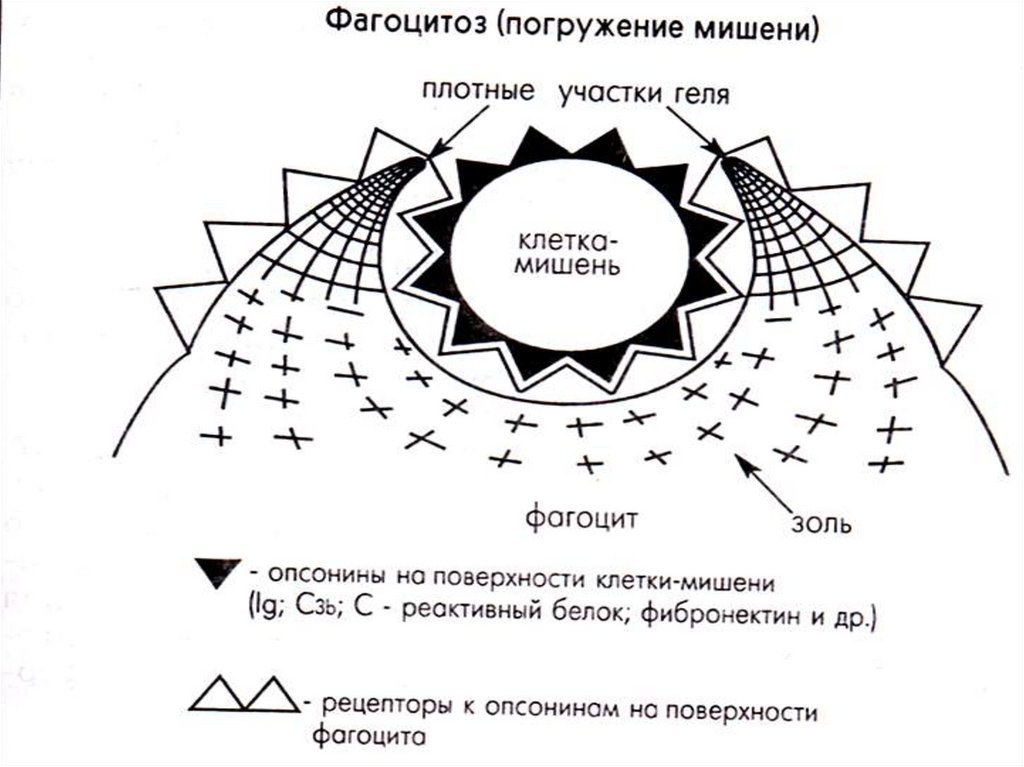
45. Этапы фагоцитоза
Адгезия (или прилипание к объекту).Формирование фагоцитарной чаши
(или погружение).
Слияние фагосом с лизосомами (или
образование фаголизосом).
Гидролиз (переработка)
фагоцитированного материала.
Удаление остатков.
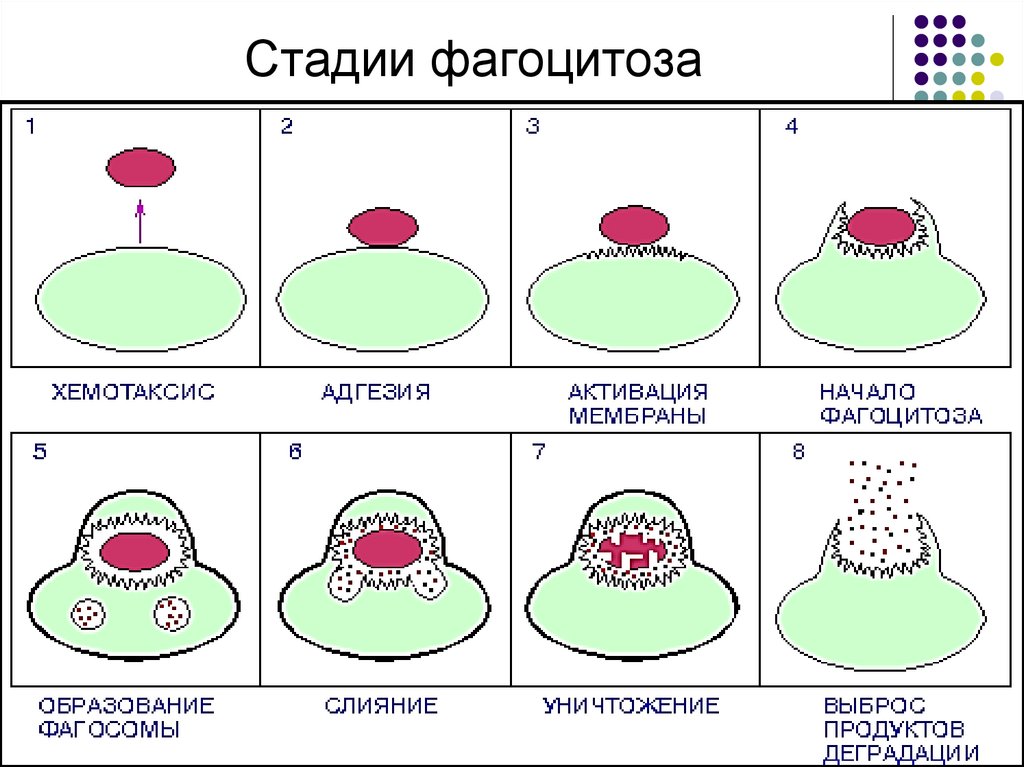
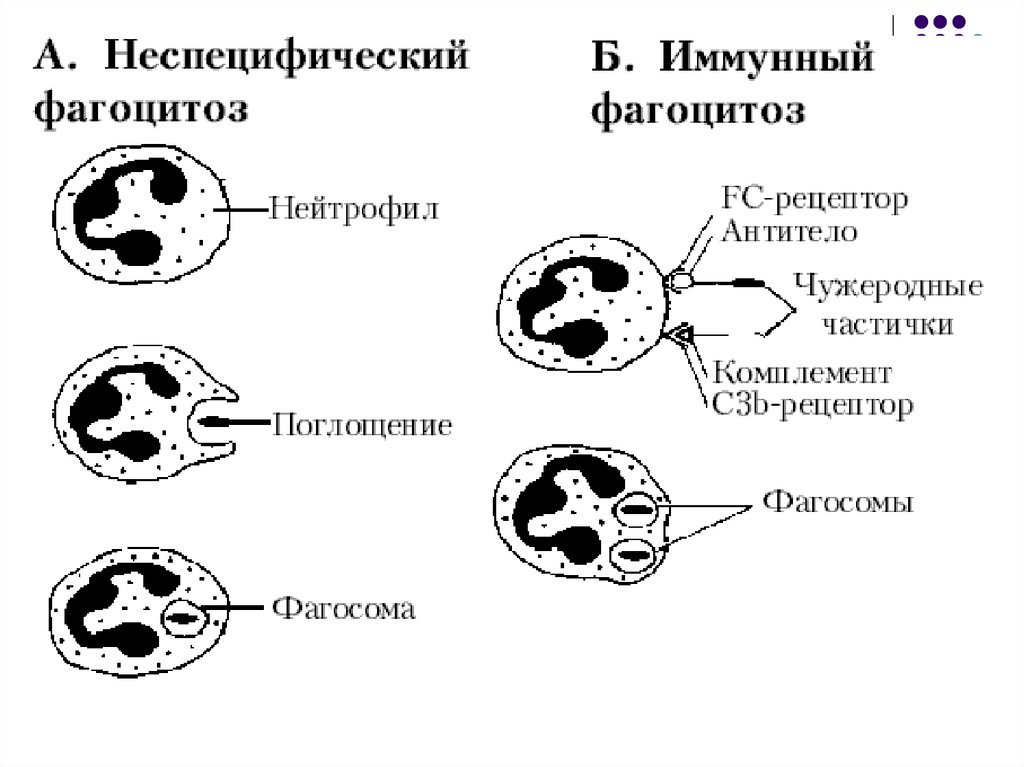
46. Стадии фагоцитоза
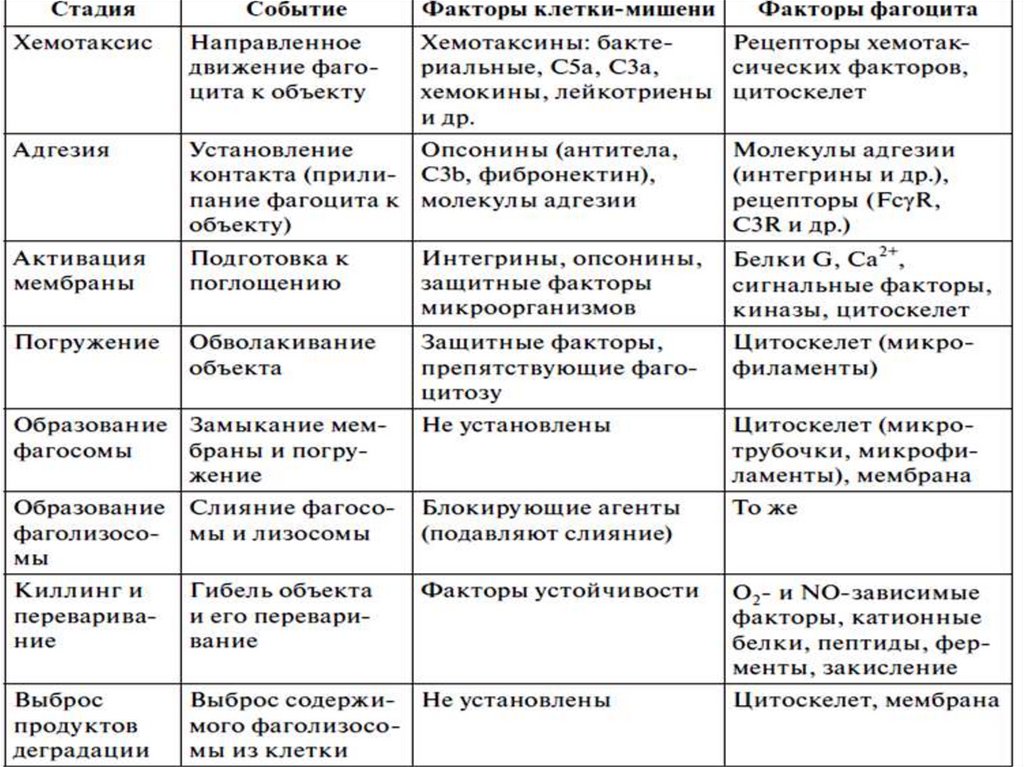
47. Характеристика стадий фагоцитоза
48.
49.
50.
51. Защитные механизмы бактерий
Некоторые бактерии могут выделять репелленты,подавляющие хемотаксис.
Другие виды обладают капсулами или оболочками,
препятствующими связыванию бактерий фагоцитами.
Третьи не препятствуют поглощению, но затем
выделяют факторы, блокирующие запуск
бактерицидных механизмов (например, M. tuberculosis
ингибирует слияние фагосомы с лизосомами).
Многие бактерии выделяют каталазу, разрушающую
перекись водорода.
Некоторые бактерии, например, M. leprae, покрыты
снаружи оболочкой устойчивой к повреждению.
Ряд микроорганизмов могут выходить из фагосомы и
размножаться в цитоплазме фагоцита.
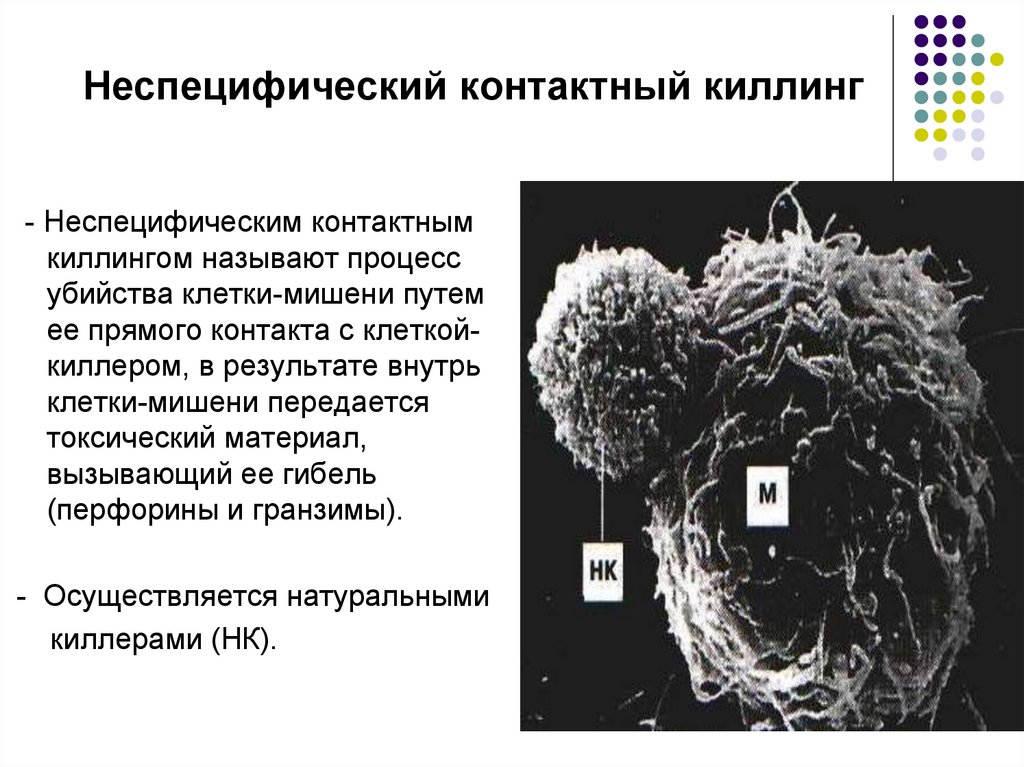
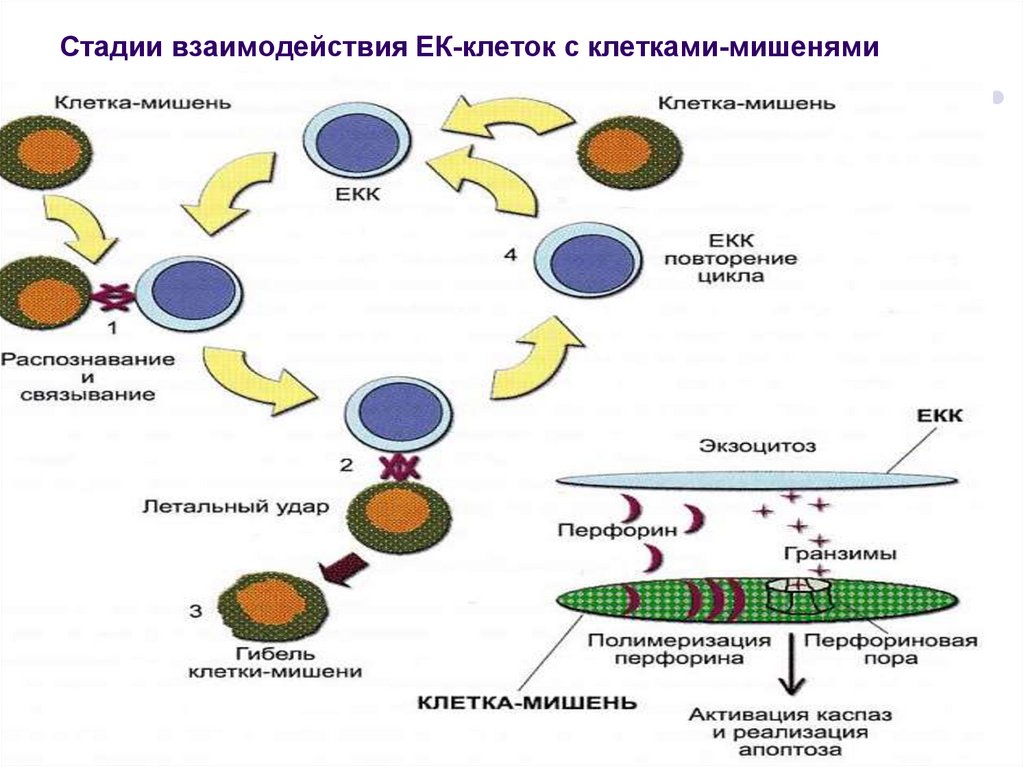
52. Неспецифический контактный киллинг
- Неспецифическим контактнымкиллингом называют процесс
убийства клетки-мишени путем
ее прямого контакта с клеткойкиллером, в результате внутрь
клетки-мишени передается
токсический материал,
вызывающий ее гибель
(перфорины и гранзимы).
- Осуществляется натуральными
киллерами (НК).
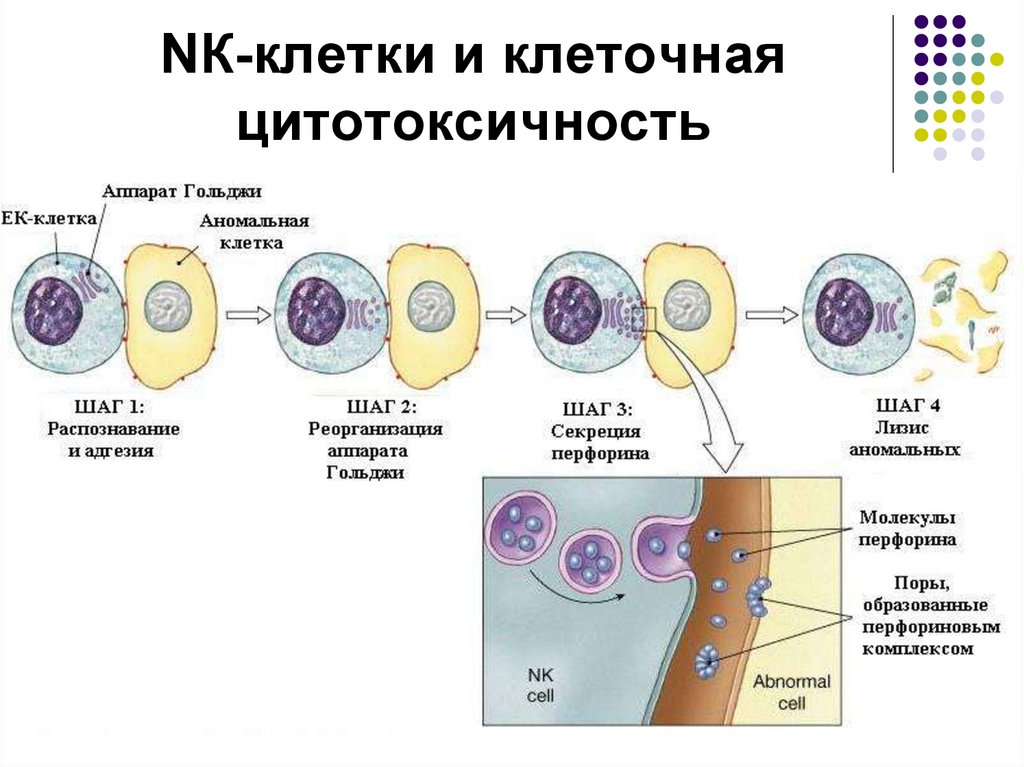
53. Стадии взаимодействия ЕК-клеток с клетками-мишенями
54. Включение механизмов адаптивного иммунитета
Воспалительная реакция является фактором,включающим реакции специфического
иммунитета.
Основные события разворачиваются в
лимфатических узлах и селезенке, куда антиген
доставляется макрофагами или другими
антигенпредставляющими клетками.
Огромную роль в запуске реакций специфического
иммунитета играют воспалительные цитокины
(ИЛ-1, ИЛ-6, ФНО, ИФН и др.)
55. Завершение или хронизация воспалительного процесса
Острый воспалительный процесс может благополучнозавершиться, если индуктор воспаления полностью уничтожен
(в этом случае в очаге начинают преобладать цитокины,
которые ингибируют миграцию новых клеток и препятствуют
распространению воспаления).
Если организм не способен ликвидировать индуктора, то
развивается хронизация воспалительного процесса, в очаге
почти отсутствуют нейтрофилы, но много макрофагов и
лимфоцитов.
В условиях постоянного антигенного раздражения происходит
дифференциация макрофагов в эпителиоидные клетки, которые
секретируют большое количество ФНО-α, иногда они сливаются,
образуя гигантские клетки.
Хронизация воспаления часто завершается образованием
гранулем.
56. Гистологическая картина гранулем
СаркоидозТуберкулез
57. Управление процессом воспаления
Подавление воспалительной реакции можноосуществить при помощи кортикостероидных
препаратов (гидрокортизон) и нестероидных
препаратов (ацетилсалициловой кислоты,
ибупрофена, парацетамола, диклофенака,
индометацина, пироксикама и др.).
Стимуляцию воспалительного процесса можно
провести при помощи вакцин, неспецифических
иммуностимуляторов, воспалительных
цитокинов (ИЛ-1, ИНФ, ФНО-ά).
58.
59.
ПРОФЕССИОНАЛЬНЫЕФАГОЦИТЫ
Нейтрофилы
Моноциты
Макрофаги
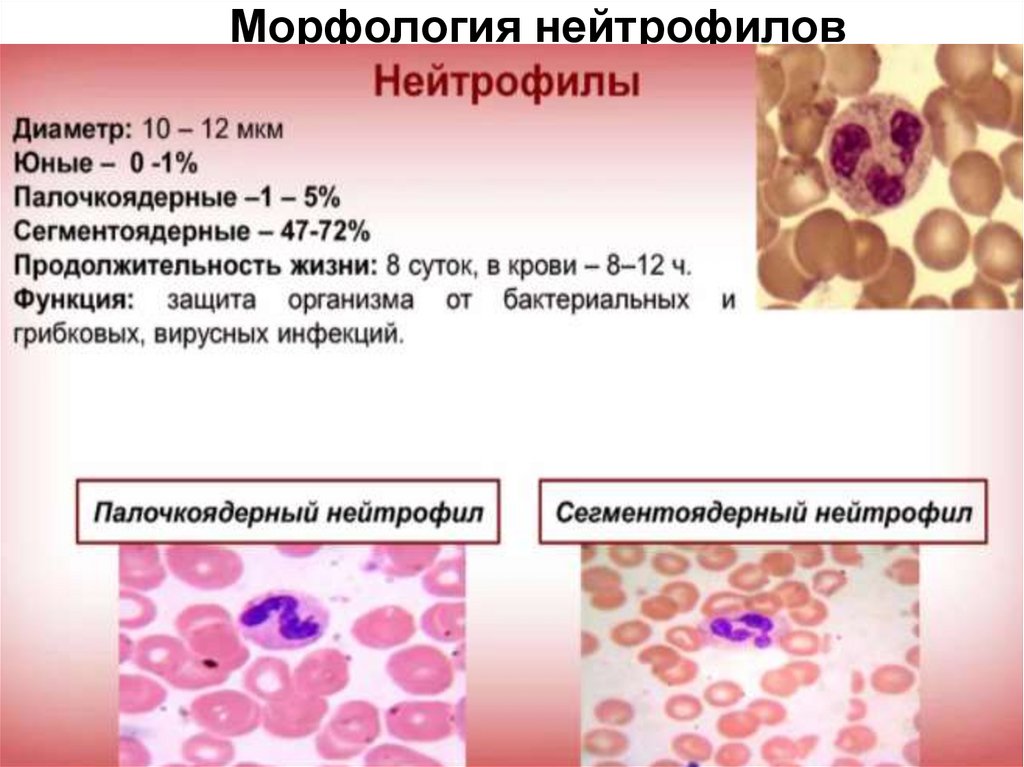
60. Характеристика нейтрофилов
Самая многочисленная популяция, составляет 40 –60 % от всех лейкоцитов.
Происходят из стволовых клеток, проходят стадии
миелобласта, промиелоцита, миелоцита,
палочкоядерного (юного) нейтрофила и становятся
зрелыми на стадии сегментоядерного нейтрофила.
Развитие их контролируется главным цитокином – GCSF (вспомогательные - GM-CSF, ИЛ-3, ИЛ-6).
На стадии палочкоядерного нейтрофила поступают в
кровеносное русло (циркулируют 7-10 часов), а
потом оседают в периферических органах и тканях,
общая продолжительность их жизни -3-5 суток.
61. Морфология нейтрофилов
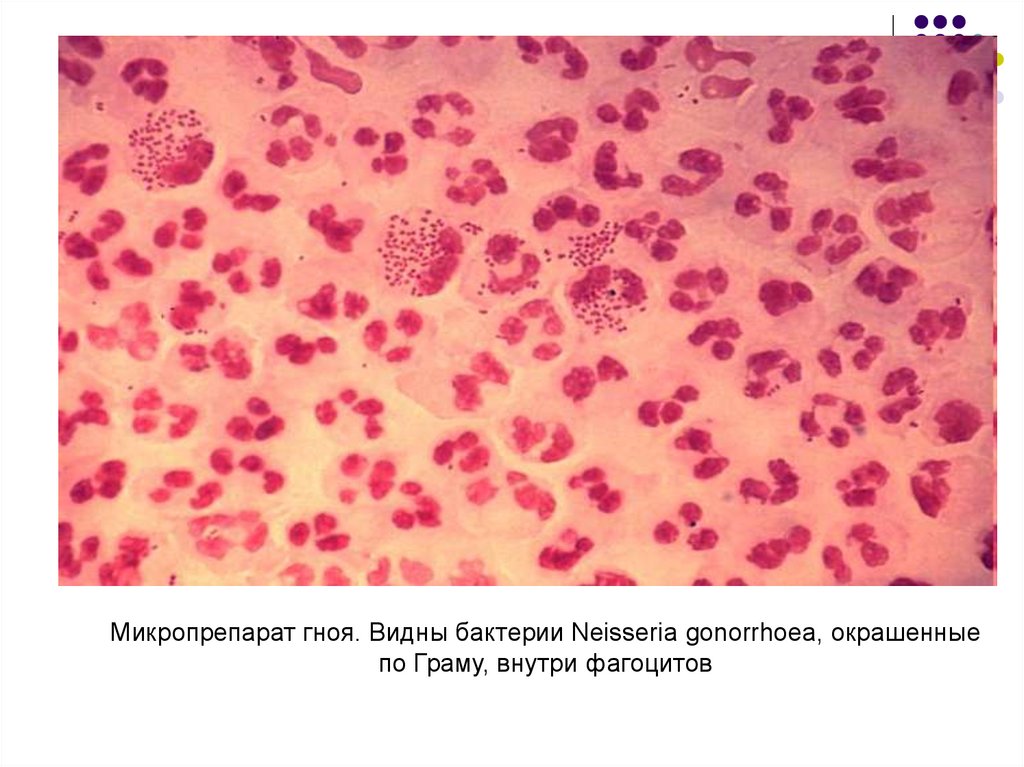
62.
Микропрепарат гноя. Видны бактерии Neisseria gonorrhoea, окрашенныепо Граму, внутри фагоцитов
63. Функции нейтрофилов
Фагоцитоз (внутриклеточный киллинг)Внеклеточный цитолиз (внеклеточный киллинг).
Секреторно-регуляторная функция (образование
продуктов респираторного взрыва, компонентов
комплемента, ИЛ-1, ИЛ-6, ИЛ-8, ФНО-ά,
простагландинов, лейкотриенов, тромбоксанов,
интерферонов и др.).
Инициация воспалительных реакций.
Участие в процессах свертывания.
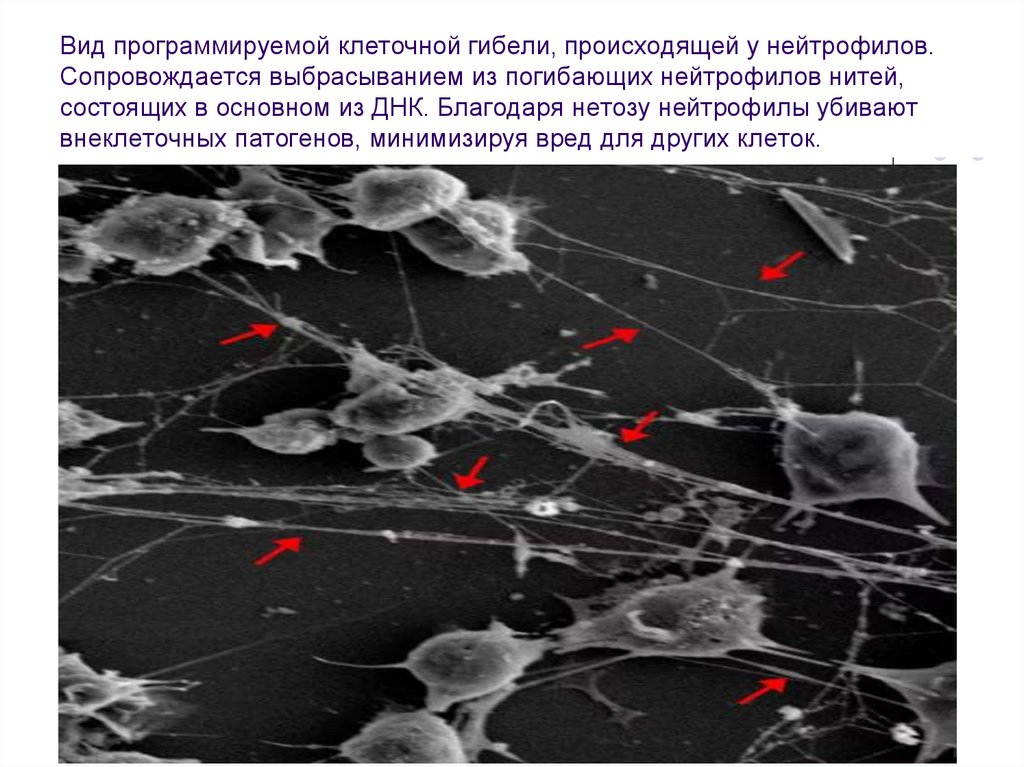
64. Вид программируемой клеточной гибели, происходящей у нейтрофилов. Сопровождается выбрасыванием из погибающих нейтрофилов нитей,
состоящих в основном из ДНК. Благодаря нетозу нейтрофилы убиваютвнеклеточных патогенов, минимизируя вред для других клеток.
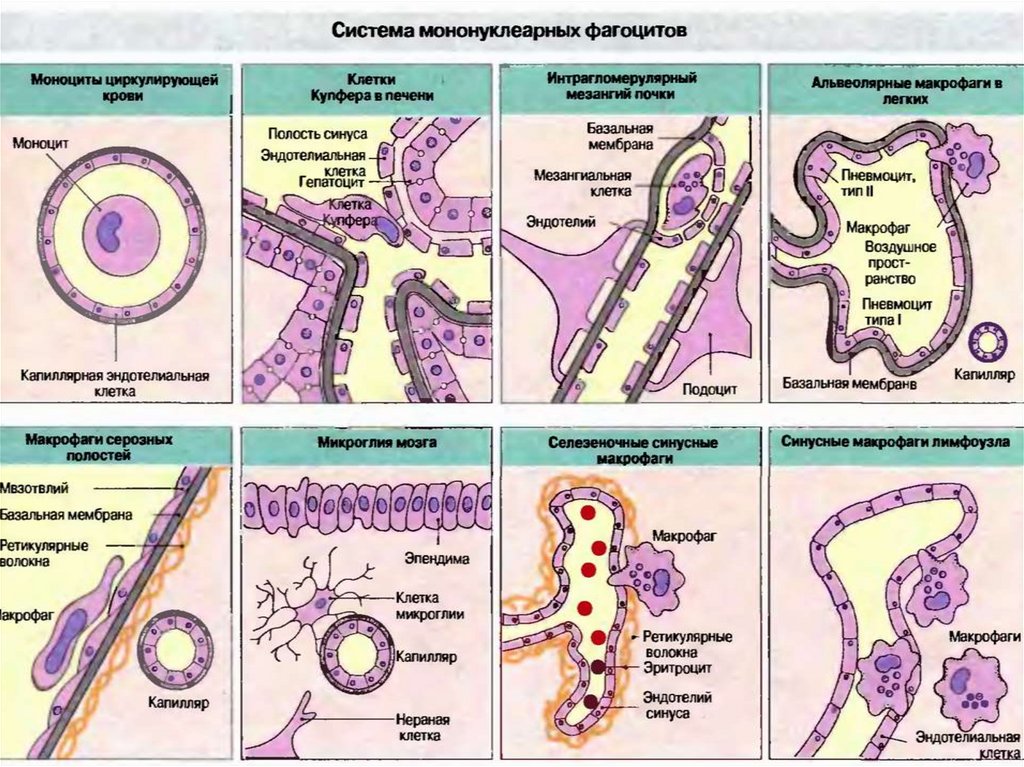
65. Характеристика моноцитов/макрофагов
Моноциты (макрофаги) составляют 4—11% отобщего числа лейкоцитов крови.
Происходят из стволовых клеток, на стадии
моноцита поступают в кровь, где циркулируют 1-2
суток, после чего мигрируют в ткани и органы и
превращаются в макрофаги.
Продолжительность их жизни колеблется от 20
суток до месяцев/лет.
Выстилают и контролируют те места, которые
наиболее вероятны для проникновения инфекта в
организм.
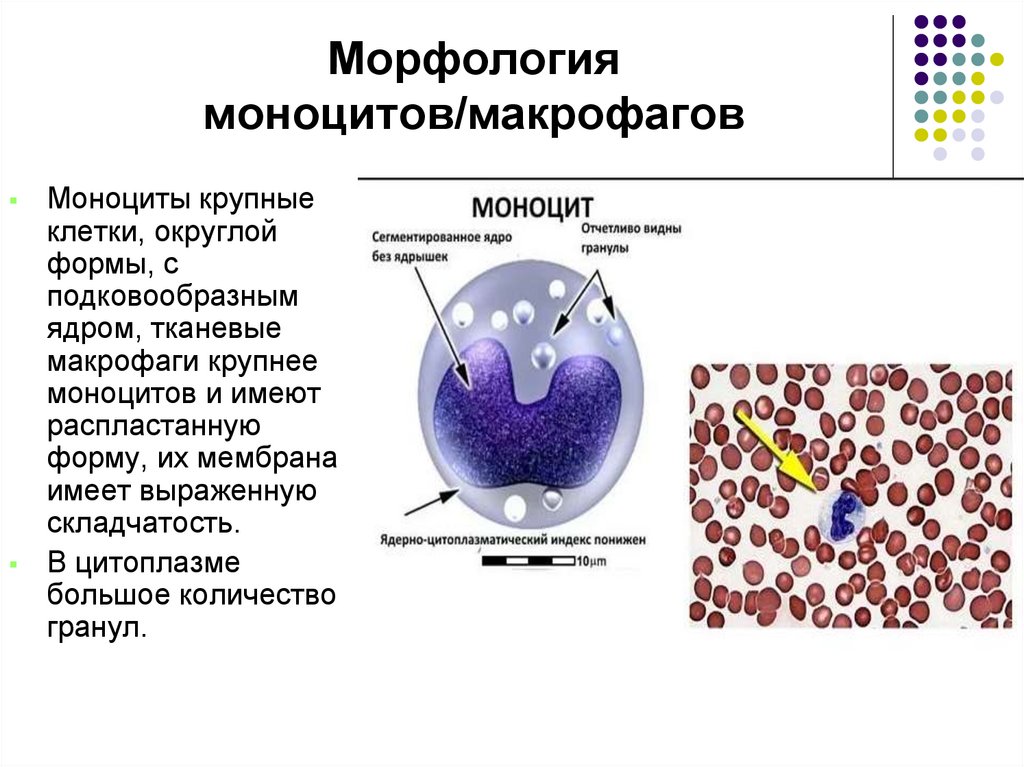
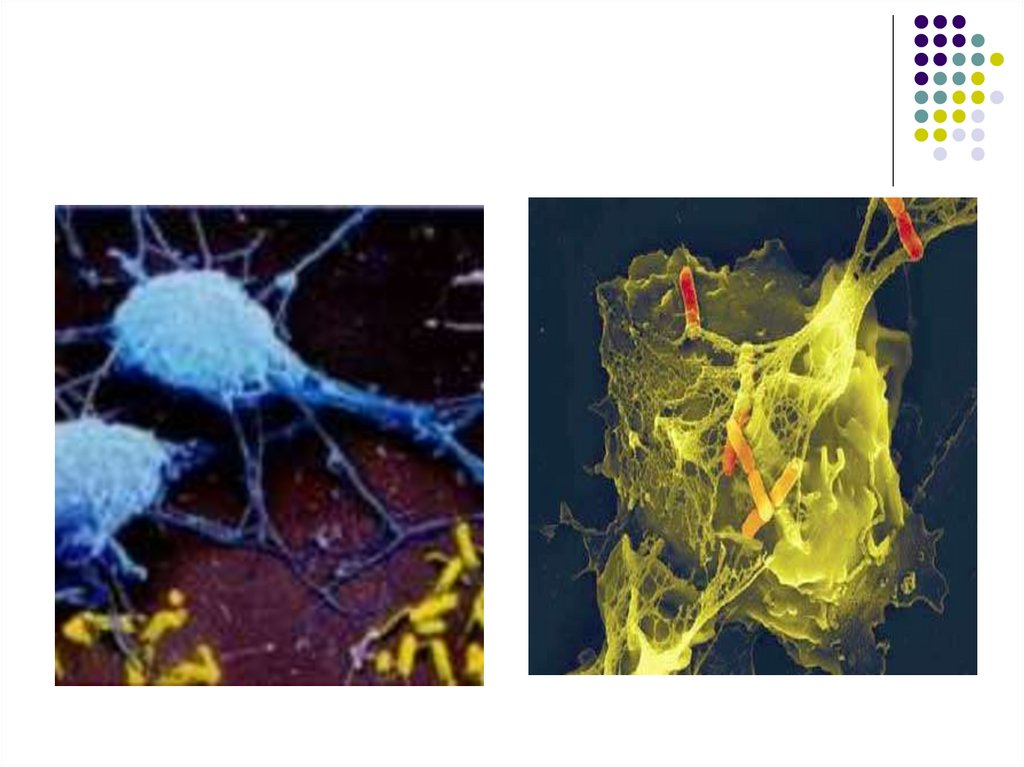
66. Морфология моноцитов/макрофагов
Моноциты крупныеклетки, округлой
формы, с
подковообразным
ядром, тканевые
макрофаги крупнее
моноцитов и имеют
распластанную
форму, их мембрана
имеет выраженную
складчатость.
В цитоплазме
большое количество
гранул.
67.
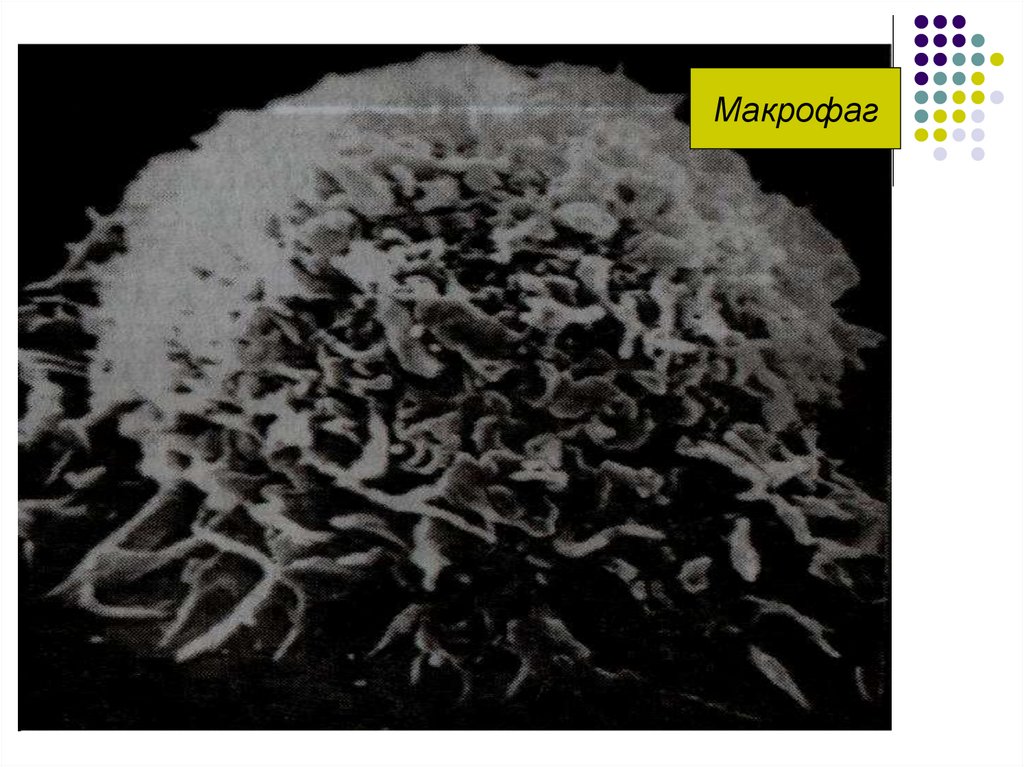
Макрофаг68.
69.
70. Функции макрофагов/моноцитов
Внеклеточный и внутриклеточныйцитолиз.
Антигенпредставляющая функция.
Секреторно-регуляторная функция (синтез
компонентов комплемента, пропердина,
продуков окислительного взрыва, NO,
ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-12, продуктов
метаболизма арахидоновой кислоты,
лизоцима и др.).
Участие в репаративных процессах.
71. Макрофаги при фагоцитозе бактерий кишечной палочки
72.
73. NK-клетки (натуральные, естественные киллеры)
Естественные киллеры — довольно крупные (10–12 мкм вдиаметре) лимфоциты с азурофильной зернистостью в
цитоплазме.
Характеризуются как большие гранулярные лимфоциты.
Главное отличие NK-клеток от других популяций лимфоцитов —
отсутствие на естественных киллерах антигенспецифических
рецепторов.
Основные маркеры NK-клеток у человека — комбинация
молекул CD56 и CD16.
Перфорин, гранзимы — основные компоненты гранул NKклеток, связанные с их цитолитической функцией.
Наиболее важные функции NK-клеток — цитотоксическая
активность в отношении измененных (опухолевых,
инфицированных вирусами, подвергшихся действию стресса)
клеток организма и секреция цитокинов (в первую очередь IFNγ), что играет важную роль в регуляции иммунных процессов..
74. NК-клетки и клеточная цитотоксичность
75. Гуморальные факторы врожденного иммунитета
76. К гуморальным факторам неспецифической защиты относят:
систему комплемента;лизоцим;
пропердин;
интерфероны;
лактоферрин;
белки острой фазы;
катионные белки;
нормальные антитела и др.
77. Пропердин
Белок, открыт в 1954Пиллемером
Принимает участие в разрушении
микробных клеток, особенно Гр-,
нейтрализует вирусы
Активен только при взаимодействии с
комплементом и ионами Mg
Синтезируется моноцитами/макрофагами
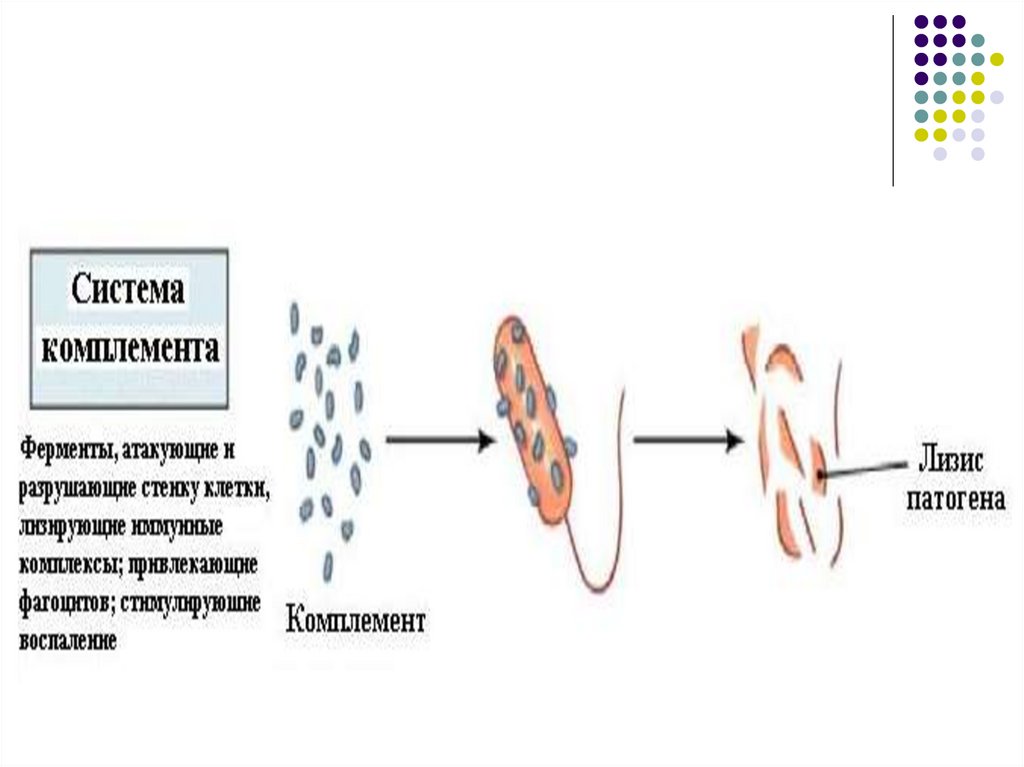
78. Система комплемента
Включает 9 основных компонентов (С1,С2, С3, С4…………С9)
Компоненты комплемента синтезируются
гепатоцитами и моноцитами/макрофагами
Представляет собой систему
действующих пептид-гидролаз
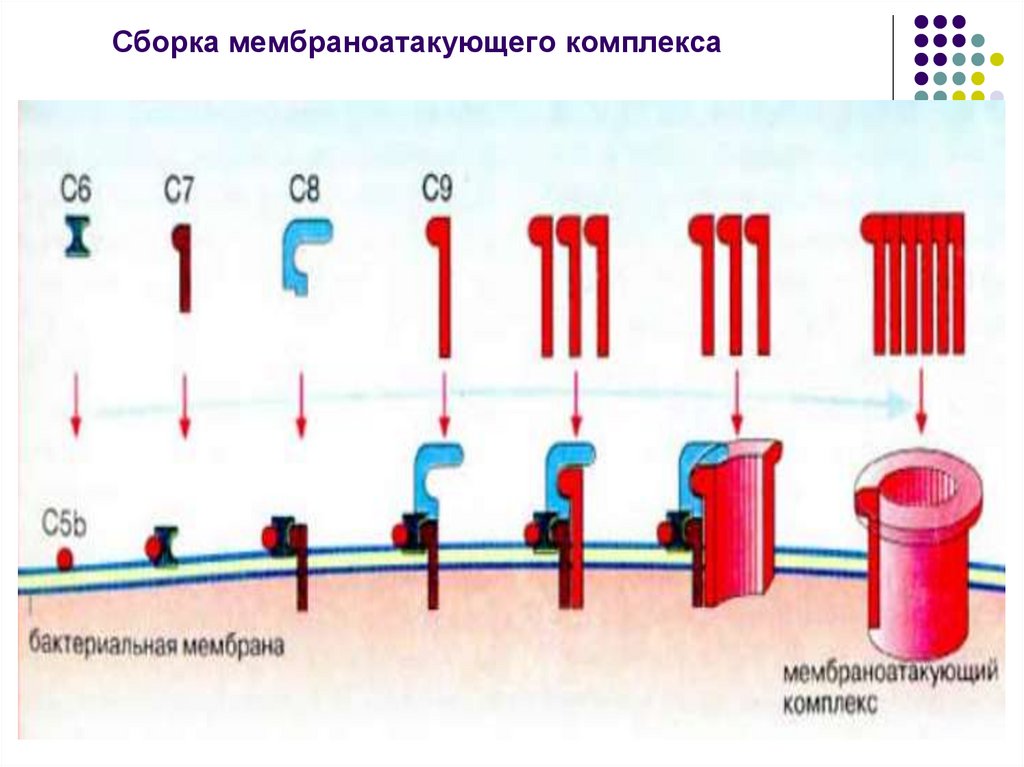
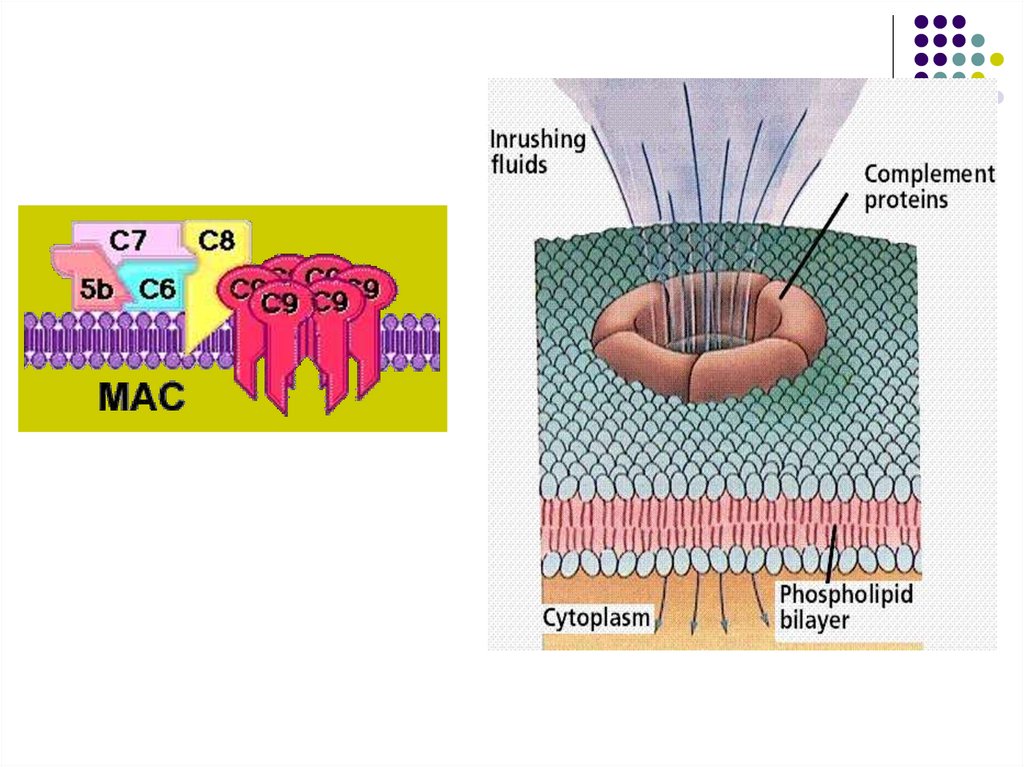
Конечным этапом активации комплемента
является МАК (мембрано-атакующий
комплекс)
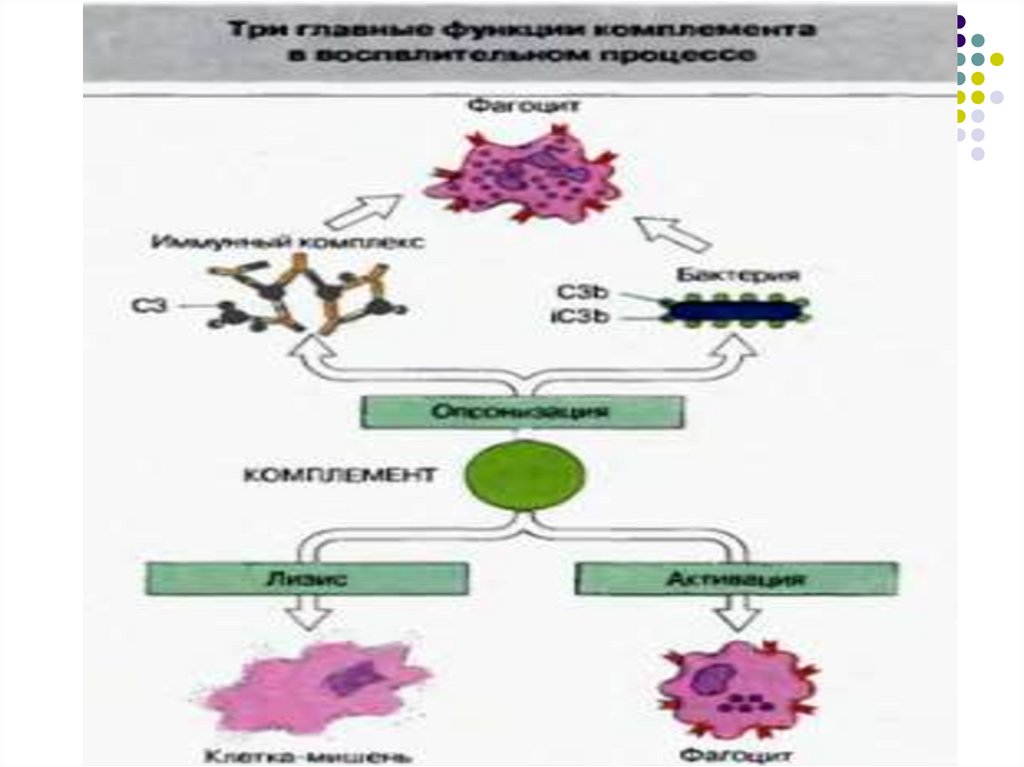
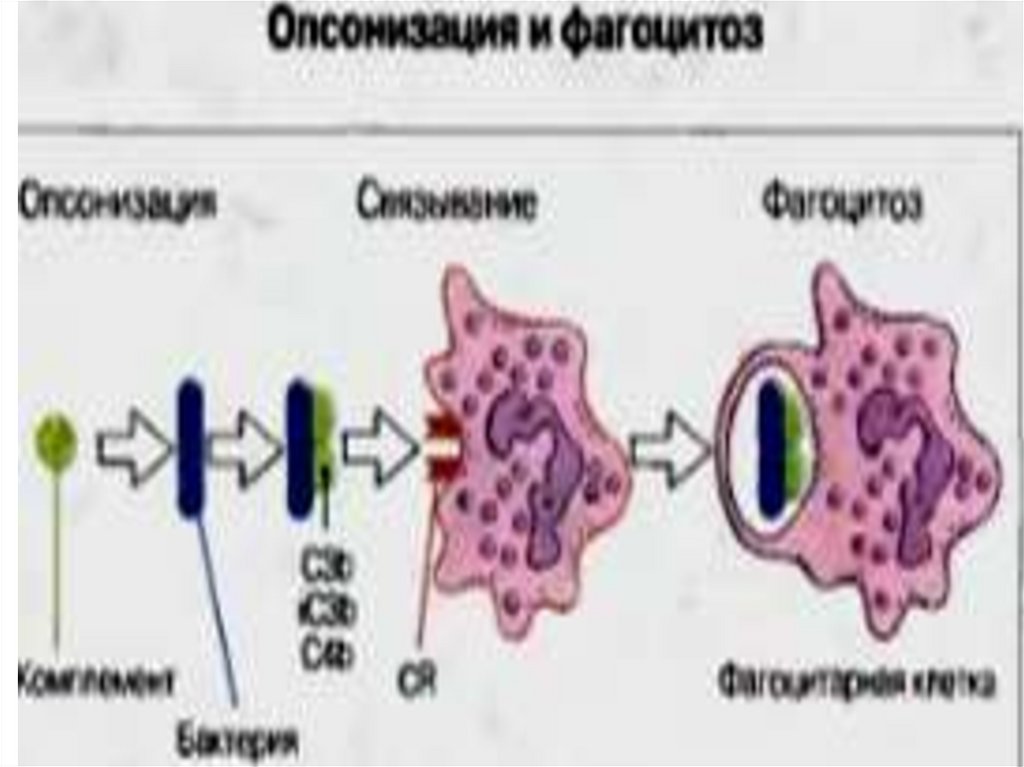
79. Функции комплемента
Опсонизация (связывание компонентовкомплемента с микробными клетками или
иммунными комплексами с целью усиления
фагоцитоза)
Лизис микробных клеток
Лизис иммунных комплексов
Активация воспаления (привлечение в очаг
воспаления нейтрофилов,
моноцитов/макрофагов)
Усиление процессинга антигена
антигенпредставляющими клетками
80.
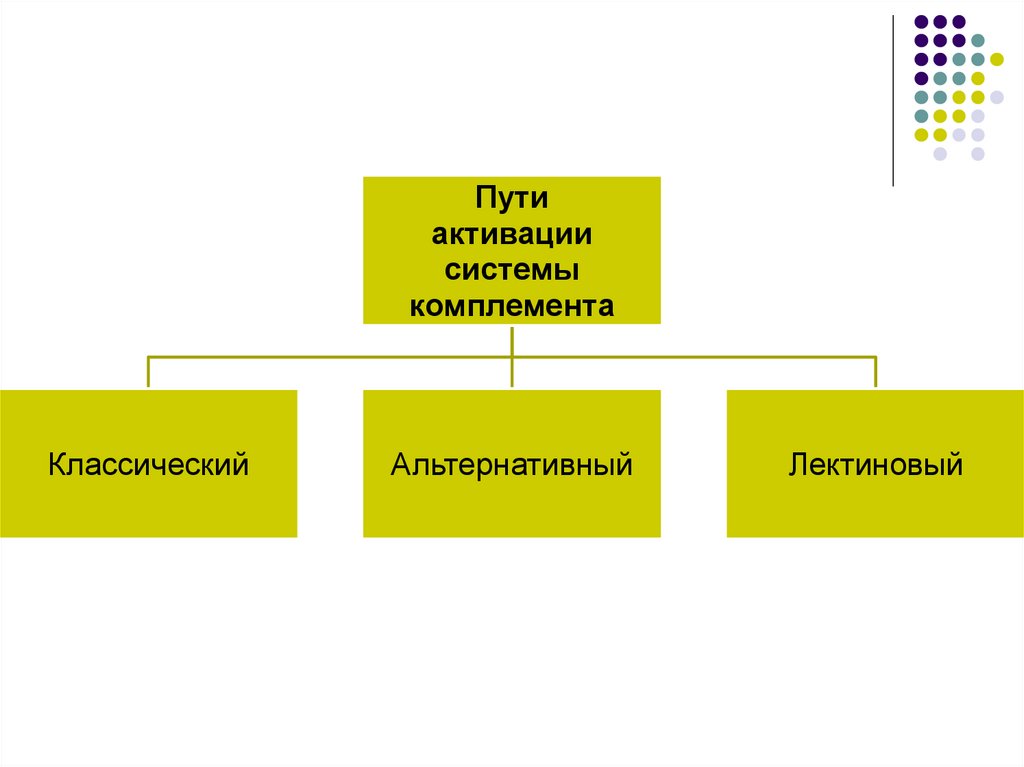
Путиактивации
системы
комплемента
Классический
Альтернативный
Лектиновый
81.
82. Система комплемента
83.
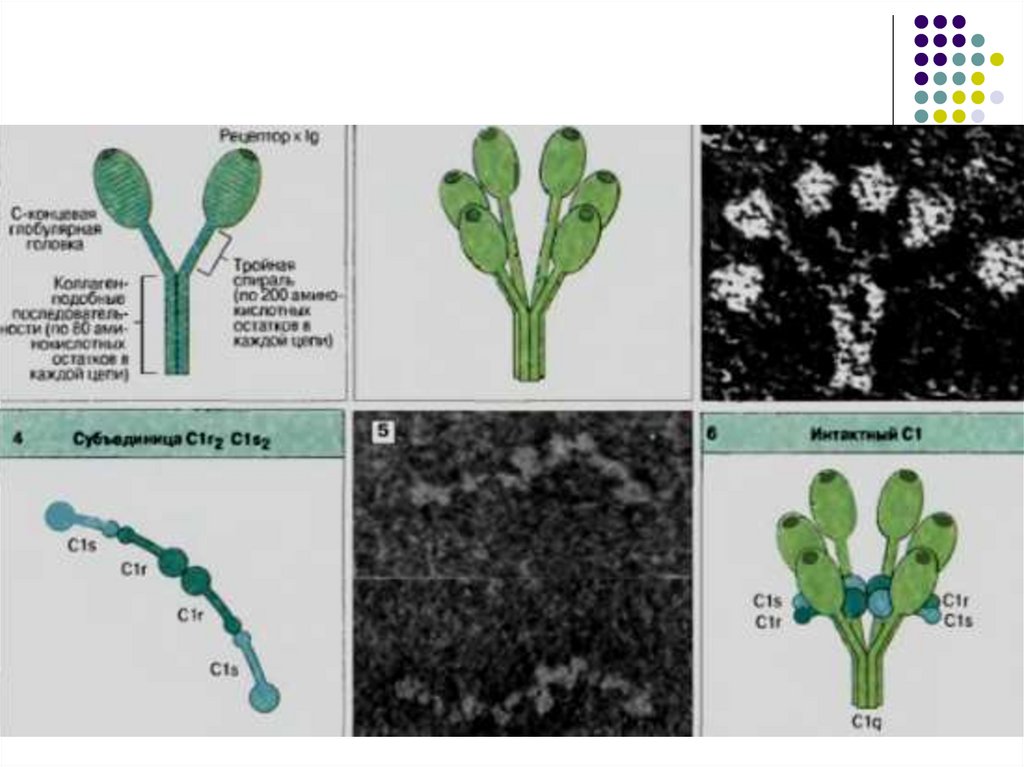
84. Структура С1
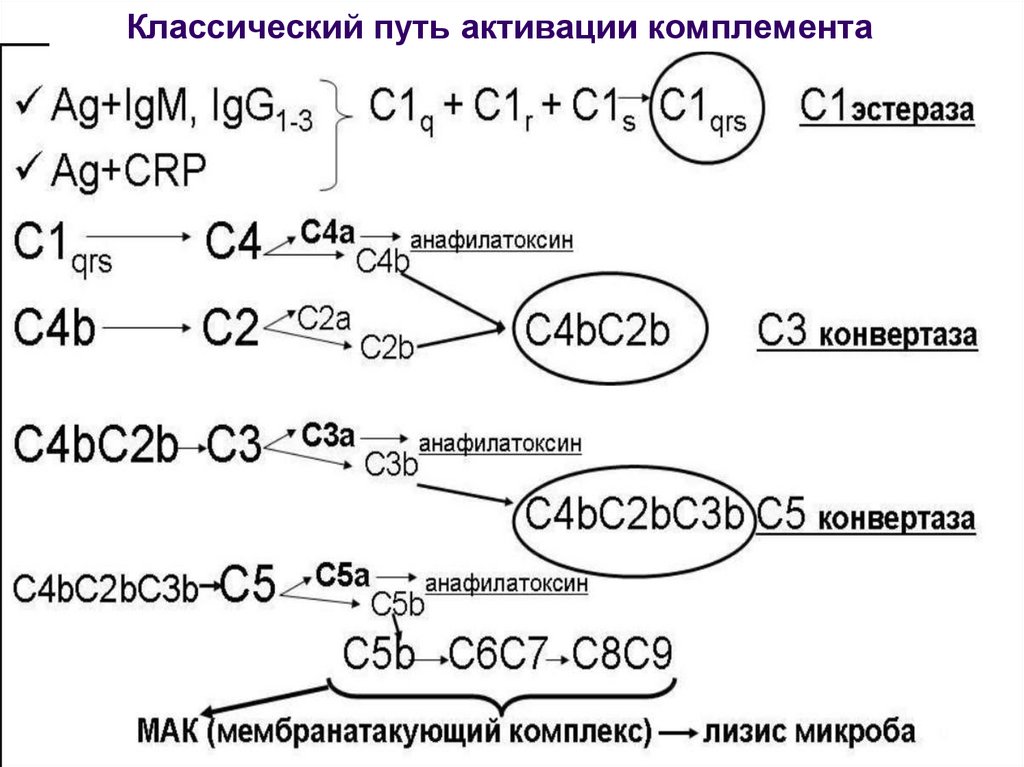
85. Классический путь активации комплемента
86. Сборка мембраноатакующего комплекса
87.
88. Поверхность кишечной палочки, поврежденной МАК
89.
ЛизоцимПротеолитический фермент
Открыт А.Флемингом в 1922 г.
Разрушает клеточную стенку бактерий,
действуя на пептидогликан
Активирует фагоцитоз
Активирует антителообразование
Синтезируется фагоцитами (моноцитами,
макрофагами, нейтрофилами)
Содержится во всех жидкостях организма,
кроме спинномозговой жидкости и передней
камеры глаза
Является показателем резистентности
организма
90.
91. Открыл лизоцим А.Флеминг
92.
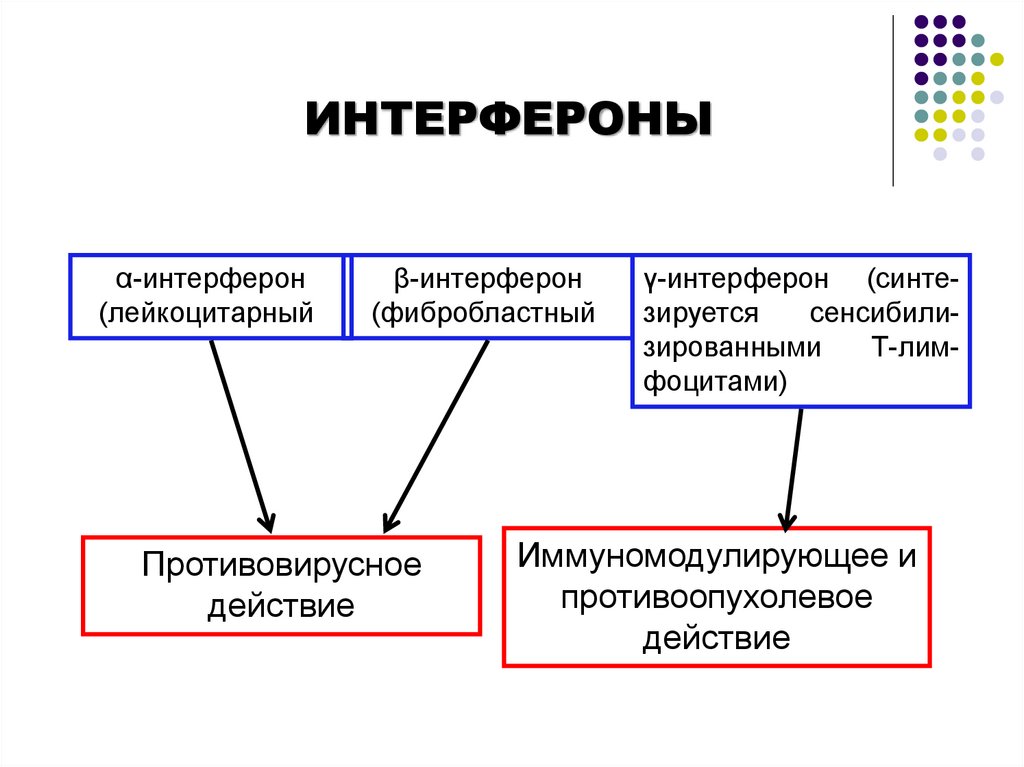
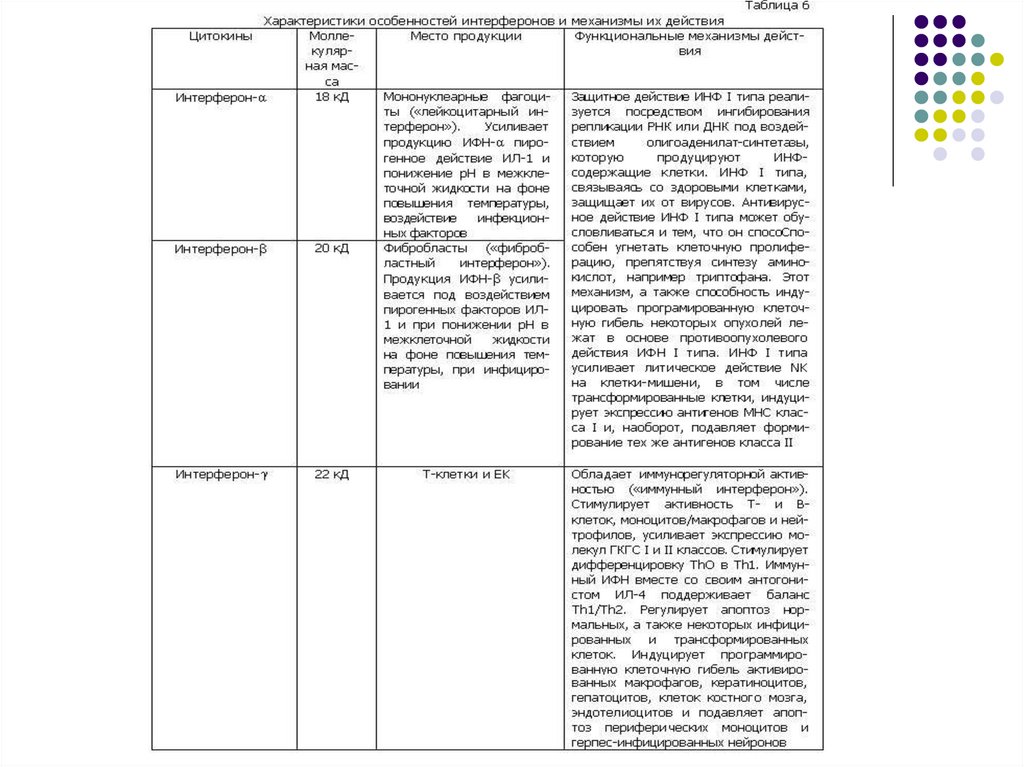
ИНТЕРФЕРОНЫα-интерферон
(лейкоцитарный)
β-интерферон
(фибробластный)
Противовирусное
действие
γ-интерферон (синтезируется
сенсибилизированными
Т-лимфоцитами)
Иммуномодулирующее и
противоопухолевое
действие
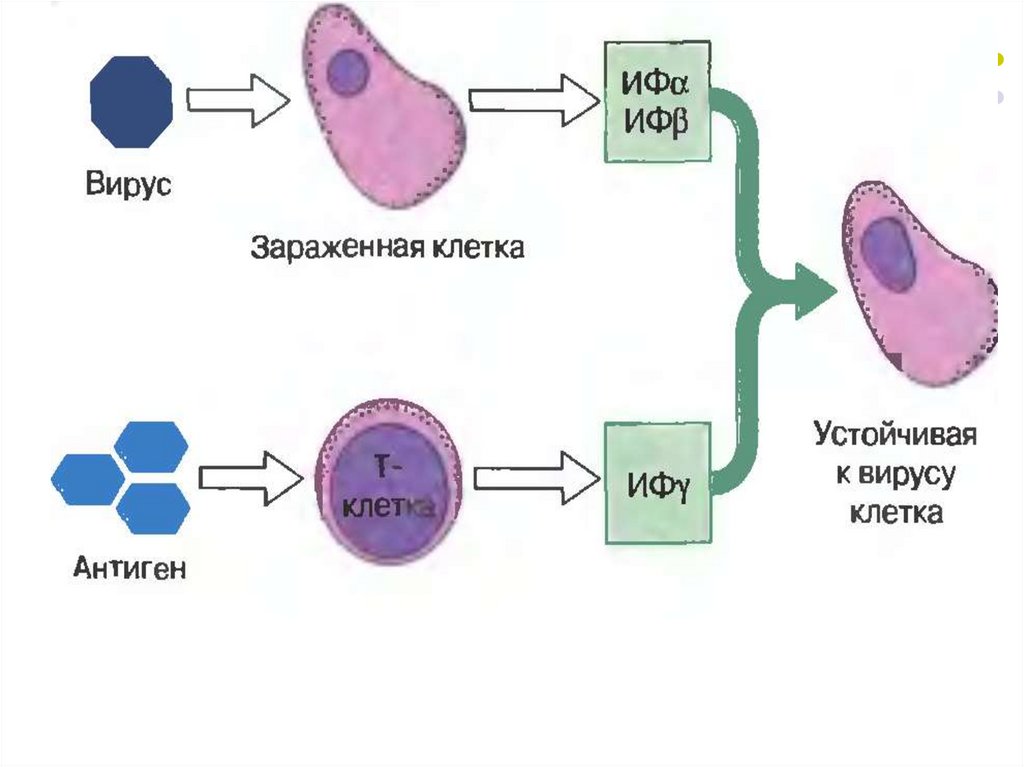
93.
Приобретение клетками устойчивостипосле действия ИФН
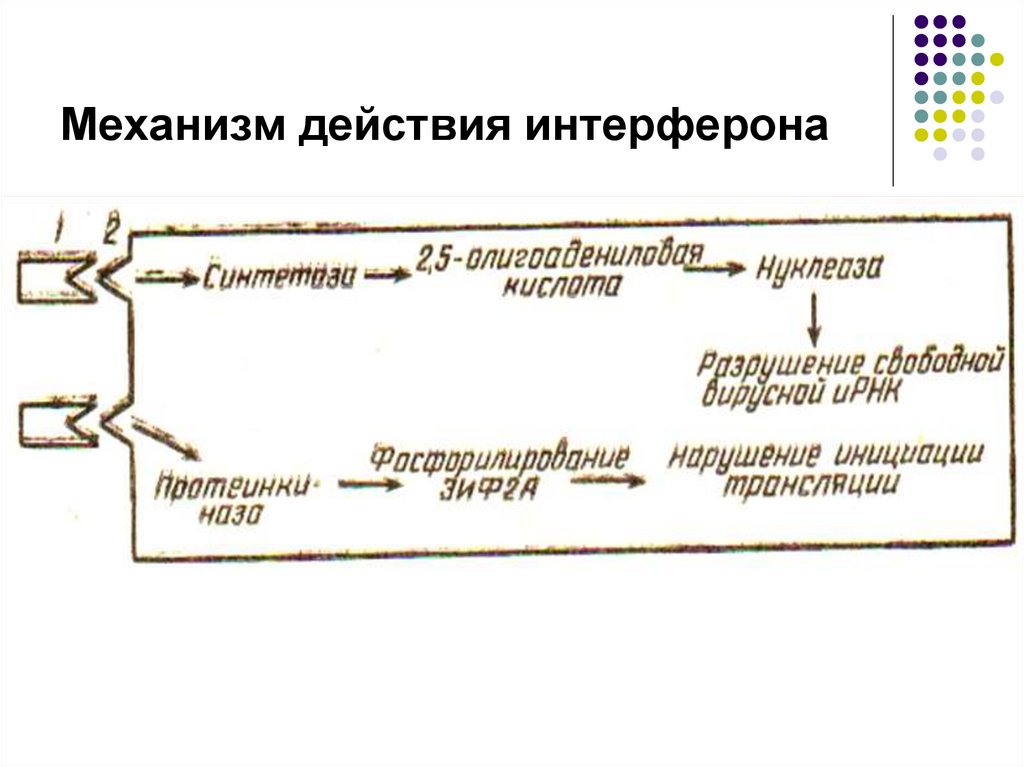
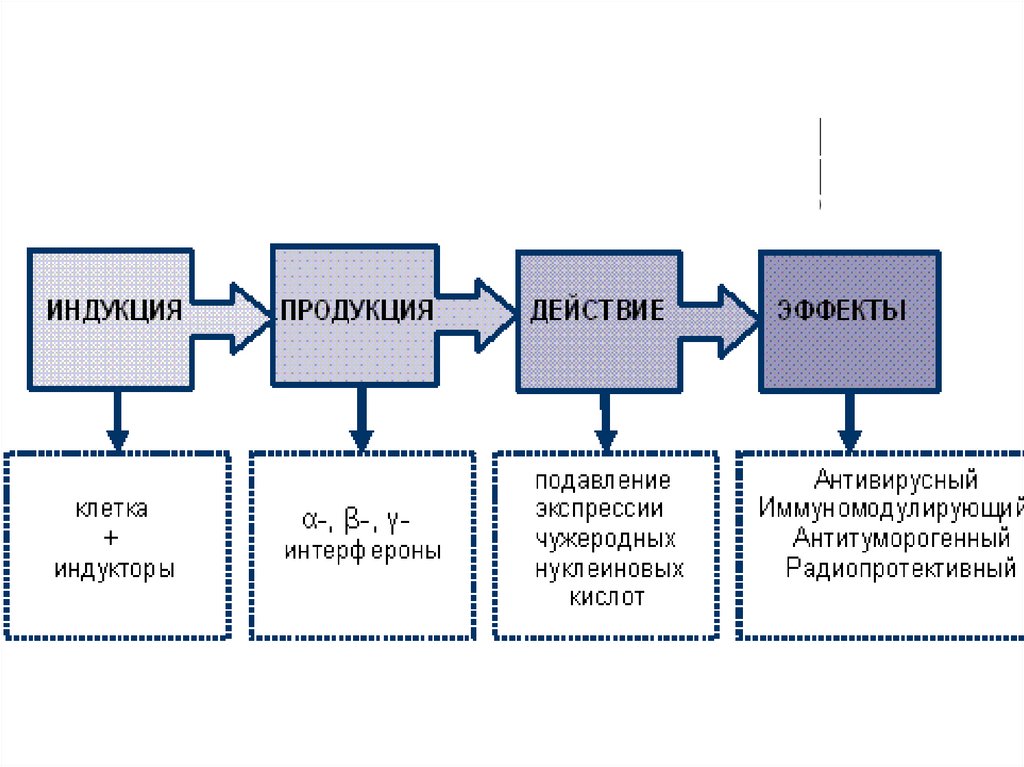
94. Механизм действия интерферона.
1- интерферон; 2 – клеточный рецептор.95.
Функционирование системы ИФНскладывается из строго следующих друг за
другом этапов, представляющих своеобразную
цепную реакцию организма в ответ на
внедрение чужеродной информации.
96.
97.
98.
99.
100.
101.
102.
103.
104. Характеристика лактоферрина
По химической природе - гликопротеидСинтезируется гранулоцитами и гроздевидными
клетками железистого эпителия
Способен связывать 2 атома Fe 3+ , конкурируя в
этом с микроорганизмами
Является компонентом секретов желудочнокишечного, дыхательного, мочеполового трактов,
слюнных, слезных, молочных желез, сыворотки
крови
105.
-ЛИЗИНЫБелки сыворотки крови
Синтезируются тромбоцитами
Повреждают ЦПМ бактерий
(преимущественно грамположительных, спорообразующих )
106.
Белки острой фазы1. Содержатся в сыворотке крови ( в норме – мало, увеличиваются
при тяжелых системных воспалительных процессах, синтезируются
в печени под влиянием цитокинов). Наиболее важные из них:
С-реактивный белок; маннансвязывающий лектин.
2. С-реактивный белок (СРБ) - наиболее важный из белков острой
фазы, связывается с КС ряда бактерий одноклеточных грибов,
опсонизирует, активирует комплемент по классическому пути, его
количество может увеличиваться в 10-100 и даже в 1000 раз
Появляется уже через несколько часов после инфицирования или
травмы. По уровню СРБ можно судить об эффективности
проводимого лечения.
3. Маннозосвязывающий лектин (лектинами называют белки,
способные с высокой прочностью связывать углеводы)
опсонизирует микробную клетку для фагоцитоза моноцитами, а
также вызывает активацию комплемента по лектиновому пути.
107.
108.
Эндогенные пептиды-антибиотики:1) состоят из 13 – 18 аминокислот;
2) убивают бактерии;
3) у эукариотических многоклеточных организмов
их около 400;
4) наиболее изучены - дефензины млекопитающих
(альфа-дефензины содержатся в гранулы
нейтрофилов, бета-дефензины – вырабатывают
клетки эпителия дыхательных путей и ЖКТ)




















































 Медицина
Медицина








