Похожие презентации:
Витамины. Лекция 4 (II семестр)
1. ВИТАМИНЫ
Лекция 4 (II семестр)2. ОПРЕДЕЛЕНИЯ
Витамины (от “vita” и “амин”) – это соединения,обладающие следующими признаками:
- низкомолекулярные органические соединения
- не синтезируются организмом человека
(должны поступать с пищей)
- не входят в структуру тканей
- не используются как источник энергии
- необходимы в малых количествах для
нормального протекания биохимических и
физиологических процессов
И НЕ ОБЯЗАТЕЛЬНО АМИНЫ!
3. Витаминоподобные вещества – вещества, соответствующие признакам витаминов, но
- способны частично синтезироваться ворганизме
- могут входить в структуру тканей
(инозит, липоевая кислота и др.)
Провитамины – прямые предшественники
витаминов
(для вит.А – каротиноиды, для вит. D –
стерины...)
4.
• !!! Признаки недостаточности витаминаспецифичны и позволяют определить,
какого витамина не хватает, а для
витаминоподобных веществ четкой
специфичной картины нет.
5. Авитаминоз – комплекс симптомов, возникающих из-за достаточно длительного и полного или почти полного отсутствия одного из
витаминов.Полиавитаминоз – недостаточность нескольких витаминов
Гиповитаминоз – частичная, но уже проявившаяся
специфическим образом, недостаточность
витамина.
Типы: 1) – экзогенный (пищевой)
2) - эндогенный
3) - дисвитаминоз (несовместимость витаминов)
Гипервитаминоз – комплекс симптомов,
возникающих из-за длительного избыточного
введения витамина в организм. Почти все
случаи - для жирорастворимых витаминов.
6. Примеры эндогенного гиповитаминоза:
1) снижение усвоения витаминов (например, призаболеваниях ЖКТ или после хирургических
вмешательств или нарушения кишечной флоры
при генетических дефектах в генах белков,
необходимых для всасывания – например, нужных
для усвоения вит. В12)
2) влияние гельминтов (например, аскариды)
3) наличие в пище антивитаминов
7.
Вещества, препятствующие проявлениюфункций витаминов – антивитамины
Примеры антивитаминного действия некоторых соединений:
для тиамина (В1):
- рыба, морепродукты (фермент тиаминаза разрушает витамин)
- кофе, чай (ухудшают его всасывание)
для биотина (H):
- авидин (в сыром белке яиц птиц, рептилий, амфибий)
- для вит. С - D-аскорбиновая к-та (человеку нужна L-форма!)
- для вит. К – кумарины и препарат варфарин (ингибиторы циклических
превращений вит. К, нужных для активации факторов свертывания
крови
- для фолиевой к-ты (в форме ТГФК) антагонист - лекарственное соединение
метотрексат (см. “Синтез нуклеотидов”)
8. Синтез дезоксирибонуклеотидов. Синтез тимина
1) Дезоксирибоза возникает только унуклеозидДИфосфатов + нужен НАДФН и
тиоредоксин + рибонуклеотидредуктаза +
тиоредоксинредуктаза
2)
9. Обратить внимание:
• Оптимальные количества (и, следовательно, нормы)потребления витаминов разные при разной массе тела, на
разных стадиях развития и в разных физиологических
состояниях
ПРИМЕР:
ДЛЯ ТИАМИНА (В1)
мг/день
Младенцы до 6 месяцев
– 0,2
Младенцы 7-12 месяцев
– 0,3
Дети 1-3 года
– 0,5
Дети 4-8 лет
– 0,6
Дети 9-13 лет
– 0,9
Мужчины от 14 лет и старше – 1,2
Девушки 14-18 лет
– 1,0
Женщины 19 лет и старше – 1,1
Для КР ориентироваться на цифры, указанные в презентации в разделах по
конкретным витаминам.
10. История открытия витаминов
С 17 векаБолезни обмена:
- Цинга (вит. С)
- Бери-бери (вит В1)
- Куриная слепота (вит А)
11. История открытия
Казимир ФункНиколай Иванович Лунин
Экспериментально доказал
необходимость присутствия витаминов
и минеральных элементов в питании.
1880 год
Поил мышей различными компонентами коровьего молока
(белки и углеводы, но не низкомолекулярные соединения)
Ввел термин «витамины» в
1911-1912 годах
Установил структуру витаминов
В1 и В3
12. Классификация (с 1956г.)
• 1) Водорастворимые• 2) Жирорастворимые
• 3) Витаминоподобные вещества –
обладающие многими, но не всеми
признаками витаминов.
Витамины обозначаются буквами (иногда с индексами),
обычно в соответствии с порядком их открытия.
Некоторые индексы сейчас не используют, так как
выяснили, что обозначаемое вещество – не витамин
13. Витамины и витаминоподобные вещества в составе кофакторов ферментов
14. Инозит – водорастворимое витаминоподобное вещество (ранее – “вит.В8”), 6-атомный спирт
В природе наиболеераспространен
мио-инозит
Его биосинтез – из
глюкозы,
у человека возможен
(3/4 необходимого).
Другие инозиты легко образуются из
миоинозита путем эпимеризации
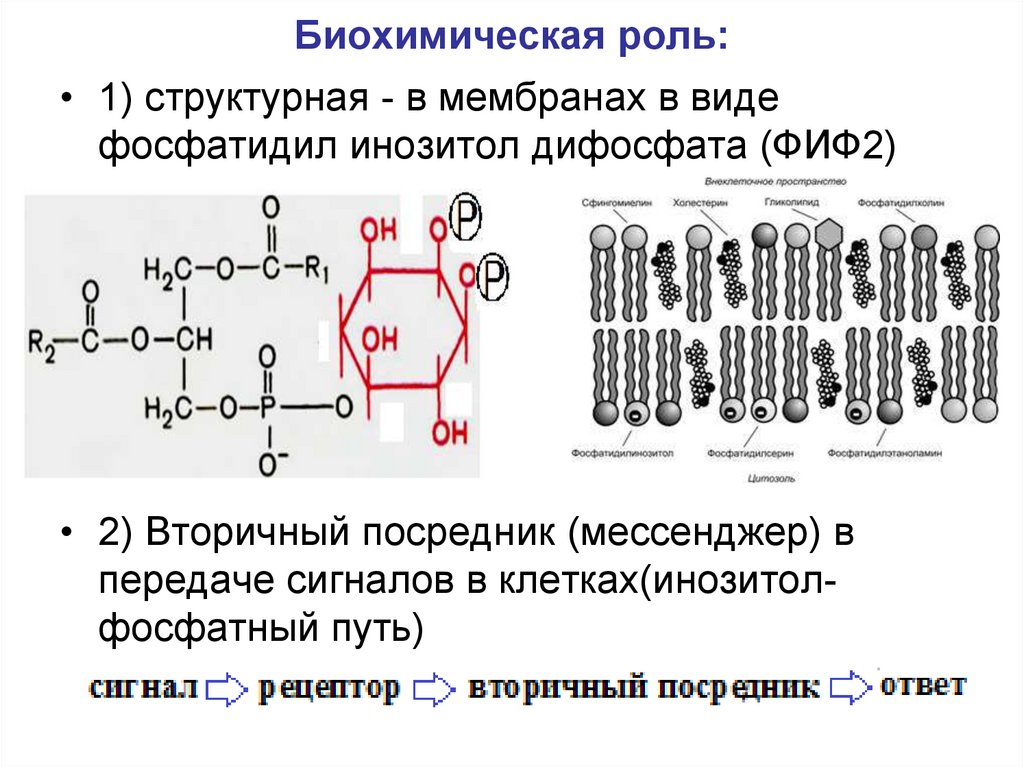
15. Биохимическая роль:
• 1) структурная - в мембранах в видефосфатидил инозитол дифосфата (ФИФ2)
• 2) Вторичный посредник (мессенджер) в
передаче сигналов в клетках(инозитолфосфатный путь)
16. Освобождение инозитолтрифосфата (ИФ3) из фосфолипида (фосфатидил-инозитол-дифосфата) под действием фосфолипазы С
Освобождениеинозитолтрифосфата (ИФ3)
из фосфолипида
(фосфатидил-инозитолдифосфата) под действием
фосфолипазы С
17. Инозитолфосфатный путь регуляции метаболизма
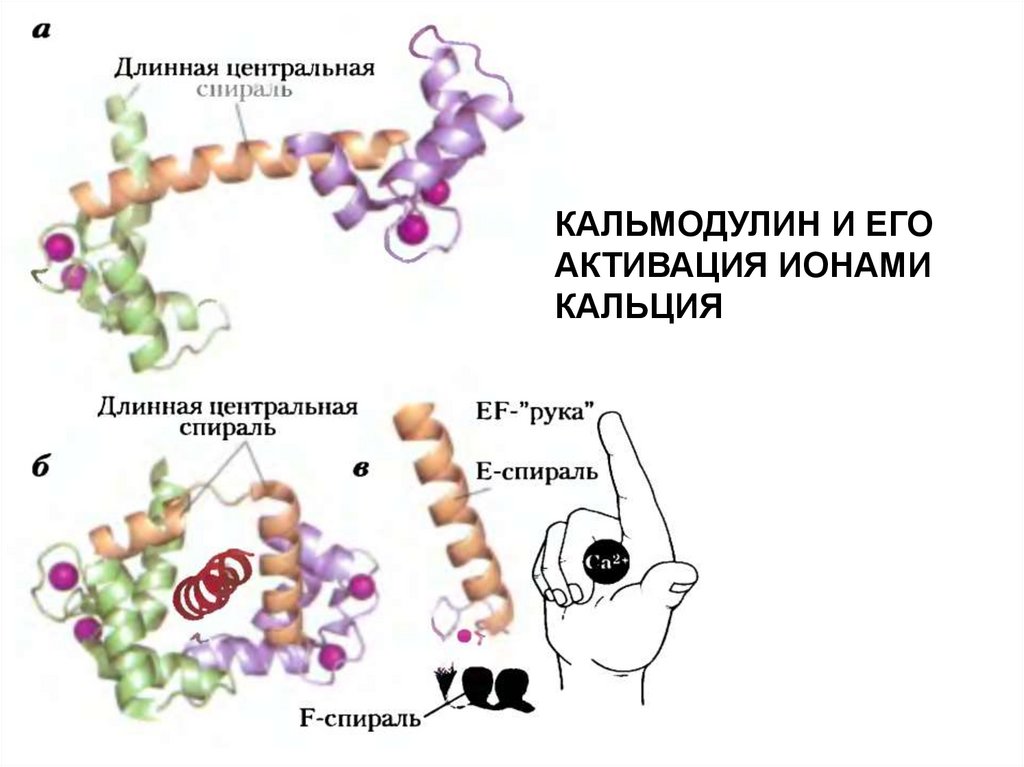
РКС – протеинкиназа С, ФС - фосфатидилсерин18. Кальмодулин – кальцийсвязывающий белок
Связывание 4 ионов Ca2+специальными доменами
обеспечивает смену
конформации молекулы
кальмодулина аналогично
движениям пальцев руки
(см.рис.внизу) и тем самым
переводит его в активное
состояние. Активный
кальмодулин способен, в
свою очередь, активировать
белки-мишени.
E и F - две α-спирали
19.
КАЛЬМОДУЛИН И ЕГОАКТИВАЦИЯ ИОНАМИ
КАЛЬЦИЯ
20. Как остановить сигнал?
• 1) Дефосфорилировать белки (фосфатазами)• 2) Откачать Са2+ наружу или обратно в ЭПР
(Са2+-АТФаза плазматической мембраны,
Na+/Са2+-транслоказа и Н+/Са2+-транслоказы
плазматической мембраны и мембран
органоидов)
• 3) Устранить ИФ3 (дефосфорилировать или
связать в липид) – специальные ферменты
21. Недостаточность инозита, источники
• У человека• Суточная
недостаточность потребность
очень редко. У
• 1 – 1,5 г !!!
животных –
плешивость,
нарушения нервной • Источники: мясо,
бобовые, орехи и др.
системы и работы
желудочнокишечного тракта.
22. Водорастворимые
1) В1 (тиамин)7) В12 (кобаламин)
2) В2 (рибофлавин)
8) H (биотин)
3) В3 (РР, никотинамид,
9) С (аскорбиновая
никотиновая кислота,
кислота)
ниацин)
10) витаминоподобн P
4) В5 (пантотеновая кислота)
(полифенолы,
биофлавоноиды)
5) В6 (пиридоксин,
пиридоксаль, пиридоксамин) 11) витаминоподобн Инозит
6) Вс, реже В9 (фолиевая
кислота)
Жирорастворимые: А, D, E, К,
витаминоподобн липоевая к-та (вит.F. вит.N)
23. Витамин С – аскорбиновая кислота (антицинготный)
Почтовая марка,посвященная
рекомендациям Линда
Нужна именно L-форма!
Выделен из лимона С. Цильва, 1918-1925
Из капусты и др. – А. Сент-Дьёрдьи, 1928-1930
Установлено строение, хим. синтез – Т.Рейхштейн,
Е. Хёрст и. В. Хеуорс …..
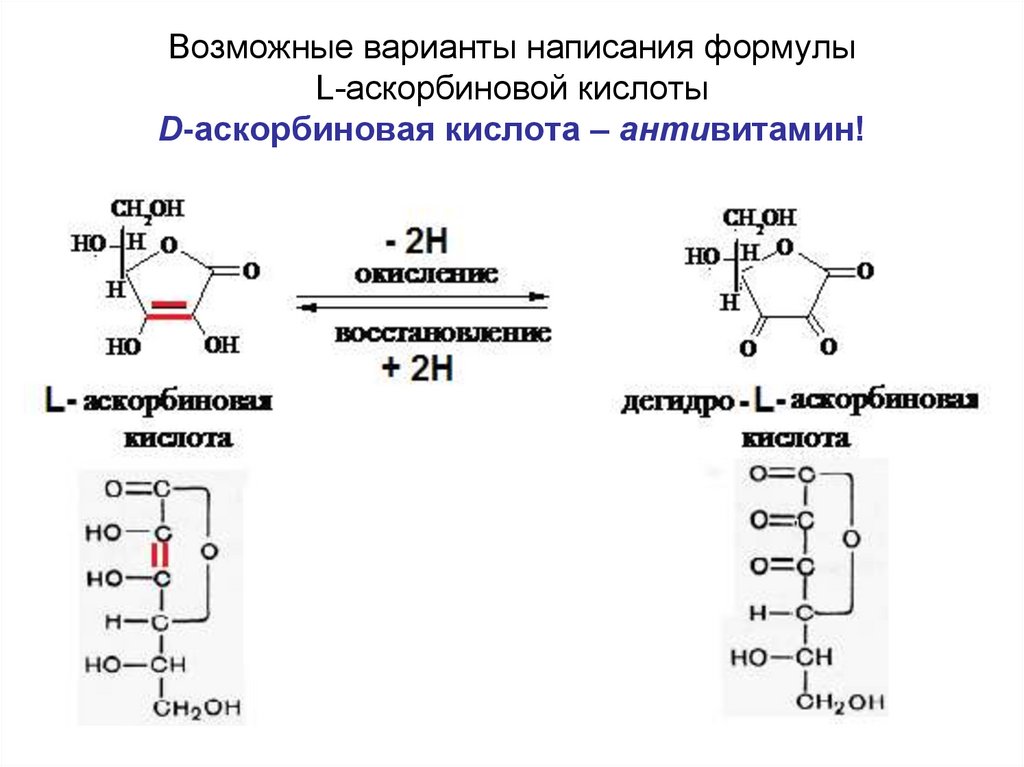
24. Возможные варианты написания формулы L-аскорбиновой кислоты D-аскорбиновая кислота – антивитамин!
25. Недостаточность вит. С
Большинство животных способно к синтезу аскорбиновой кислоты, ачеловек, гориллы, морские свинки, фруктоядные летучие мыши - нет
Недостаточность вит. С
Суточная потребность в витамине С
для человека – 70-120 мг
Симптомы авитаминоза – в основном результат
синтеза дефектного коллагена (пункты 1 и 2 на
следующем слайде)
При цинге на коже видны
кровоизлияния, в
основном вокруг луковиц
волос на ногах
Внутрисуставные
кровоизлияния с
воспалением
суставов
1) Повышенная ломкость
капилляров
2) Болезненность и
разрыхленность десен (вплоть до
выпадения зубов)
3) Общие симптомы повышенной
утомляемости, анемия, похудание
Восприимчивость к инфекциям,
снижение аппетита
Источники: шиповник, черная смородина, картофель,
мясо, др.
26. Биохимическая роль:
- окислительно- восстановительные процессы (витС не кофактор),-кофактор в ферментах (проколлаген-пролин 4-диоксигеназа, проколлагенлизин 5-диоксигеназа и др.)
1) сильный восстановитель,
участвует в окислительновосстановительных процессах,
например – нужен при
функционировании глутатиона.
Снижает уровень окислительного
стресса.
2) синтез норадреналина
3) в синтезе коллагена
4) для превращения кортикостероидов,
работы белка трансферрина (переносящего
Fe)
5) участие в обмене липидов
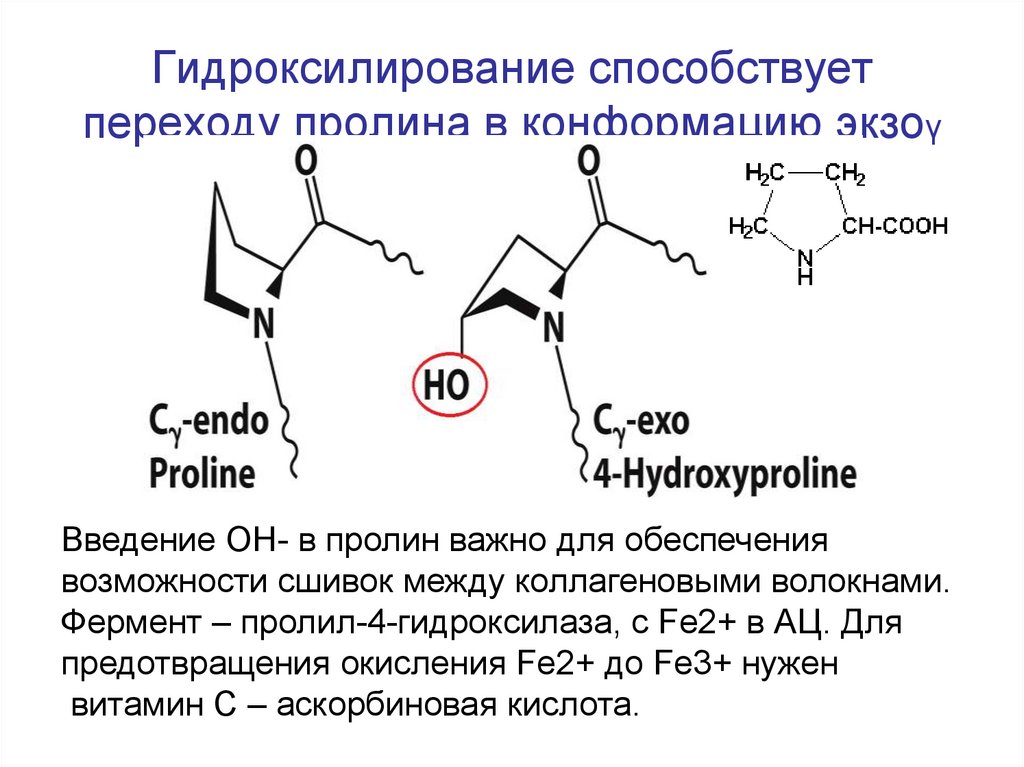
27. Гидроксилирование способствует переходу пролина в конформацию экзоγ
Введение ОН- в пролин важно для обеспечениявозможности сшивок между коллагеновыми волокнами.
Фермент – пролил-4-гидроксилаза, с Fe2+ в АЦ. Для
предотвращения окисления Fe2+ до Fe3+ нужен
витамин С – аскорбиновая кислота.
28. В12 – кобаламин – антианемический (выделен в 1948)
Синтезируетсятолько
микроорганизмами, в том
числе –
кишечной
микрофлорой
(если есть Со)
Дороти Ходжкин расшифровала
структуру (1955) - Нобелевская
премия (1964)
29.
Вверху – коррин, внизу – порфирини соединения на его основе (гем
гемоглобина и
хлорофилл)
Коррин
порфирин
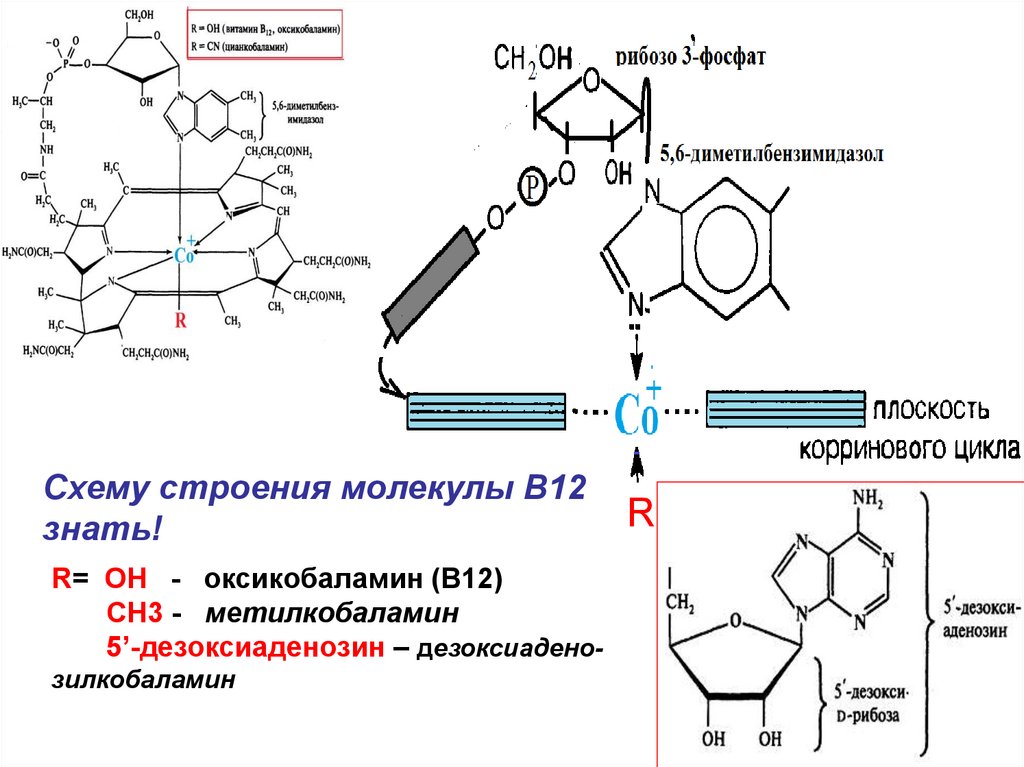
30.
Схему строения молекулы В12знать!
R= ОН - оксикобаламин (В12)
СН3 - метилкобаламин
5’-дезоксиаденозин – дезоксиаденозилкобаламин
R
31. Суточная потребность 0,003мг Недостаточность В12:
• - анемия из-за ухудшения кроветворнойфункции
• - нарушения со стороны НС
• - резкое снижение кислотности желудочного
сока, ацидоз тканей
• ИСТОЧНИКИ: мясо-молочные продукты, сыр,
рыба, яйца.
32. Для усвоения витамина В12 НУЖНЫ БЕЛКИ: ВНУТРЕННИЙ ФАКТОР КАСЛА, ТРАНСКОБАЛАМИНЫ
TCN I такжегаптокоррином
белком
называют
или
R-
33. Биохимическая роль: в виде кобамидных коферментов метилкобаламина и дезоксиаденозилкобаламина
1) Реакции переноса CH3-группы(трансметилирования)
Фермент метионинсинтаза содержит
В12 в форме метилкобаламина и
принадлежит
к классу Трансфераз
2) Внутримолекулярный перенос Н в реакциях изомеризации (важно
для липидного обмена)
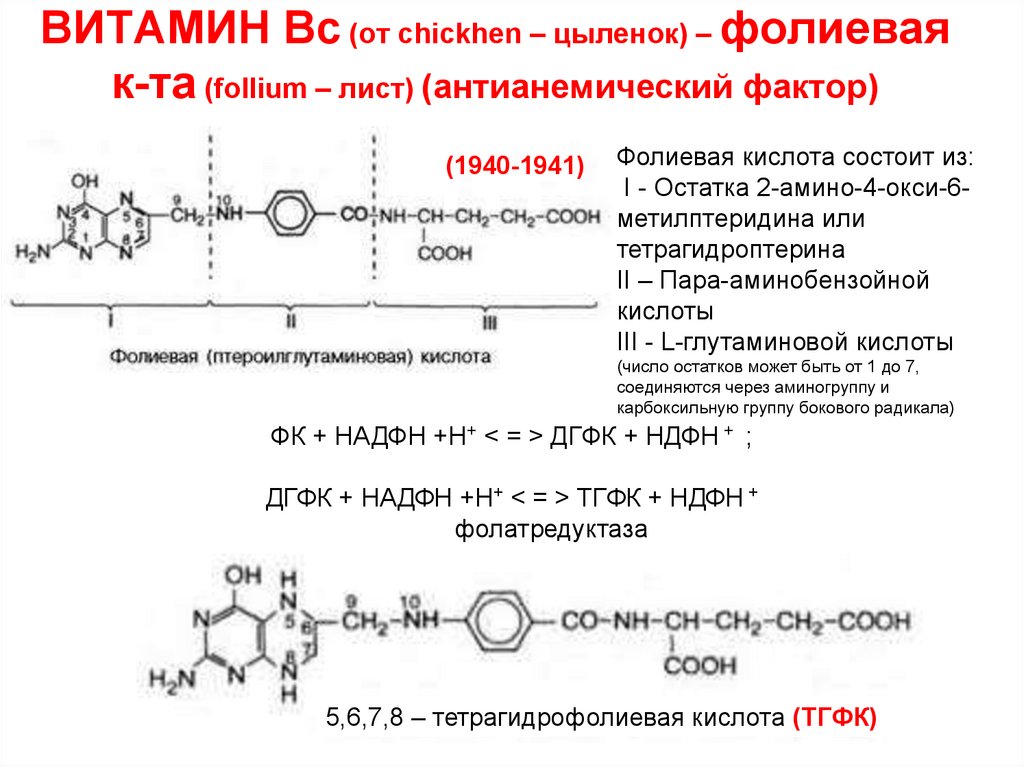
34. ВИТАМИН Вс (от chiсkhen – цыленок) – фолиевая к-та (follium – лист) (антианемический фактор)
(1940-1941)Фолиевая кислота состоит из:
I - Остатка 2-амино-4-окси-6метилптеридина или
тетрагидроптерина
II – Пара-аминобензойной
кислоты
III - L-глутаминовой кислоты
(число остатков может быть от 1 до 7,
соединяются через аминогруппу и
карбоксильную группу бокового радикала)
ФК + НАДФН +Н+ < = > ДГФК + НДФН + ;
ДГФК + НАДФН +Н+ < = > ТГФК + НДФН +
фолатредуктаза
5,6,7,8 – тетрагидрофолиевая кислота (ТГФК)
35. Биохимическая роль фолиевой кислоты – в виде кофермента ТГФК
• Переносит С1-остатки в различных состояниях окисленияв составе С1-трансфераз (КФ 2.1…). С1-фрагменты
присоединяются к N-5 и/или N-10 атомам азота.
Переносимый ТГФК С1-фрагмент нужен в синтезе
пуриновых нуклеотидов, метионина и многих др.
реакциях.
• Участвует в процессах кроветворения и деления клеток
(регулирует эритропоэз, тромбоцитопоэз, лейкопоэз)
АВИТАМИНОЗ: анемия
СУТОЧНАЯ ПОТРЕБНОСТЬ: 0,1 – 0,2 мг
ИСТОЧНИКИ: салат, шпинат и другие овощи;
яичный желток, печень, сыр.
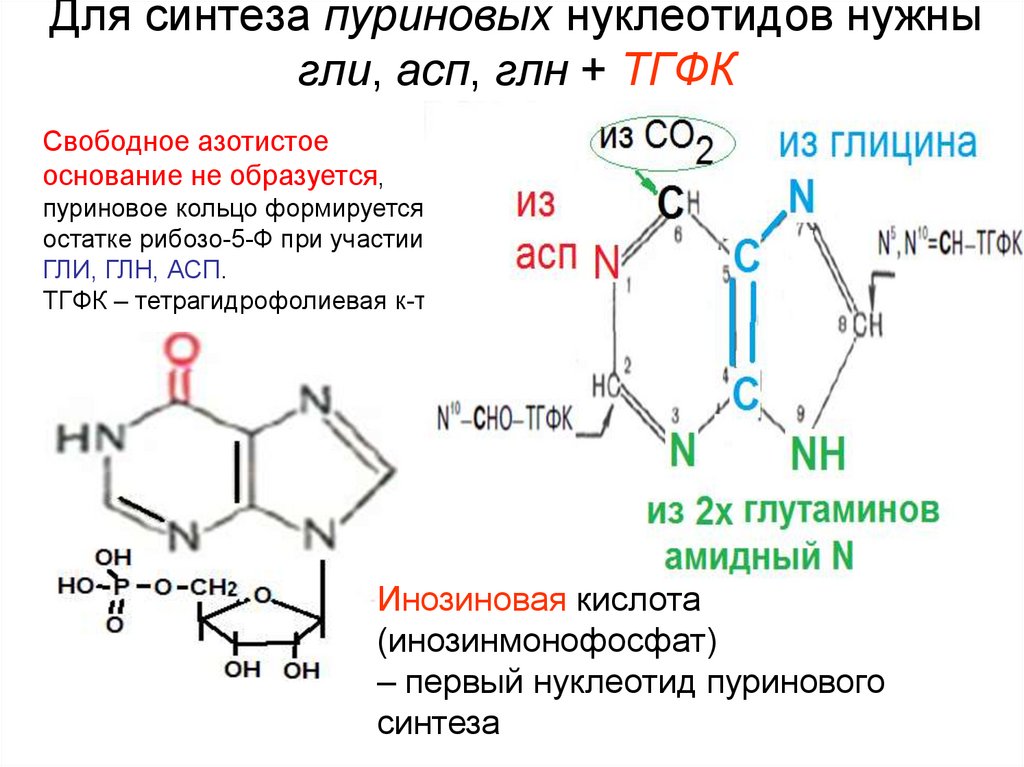
36. Для синтеза пуриновых нуклеотидов нужны гли, асп, глн + ТГФК
Свободное азотистоеоснование не образуется,
пуриновое кольцо формируется на
остатке рибозо-5-Ф при участии
ГЛИ, ГЛН, АСП.
ТГФК – тетрагидрофолиевая к-та
Инозиновая кислота
(инозинмонофосфат)
– первый нуклеотид пуринового
синтеза
37. Синтез дезоксирибонуклеотидов. Синтез тимина
1) Дезоксирибоза возникает только унуклеозидДИфосфатов + нужен НАДФН и
тиоредоксин + рибонуклеотидредуктаза +
тиоредоксинредуктаза
2)
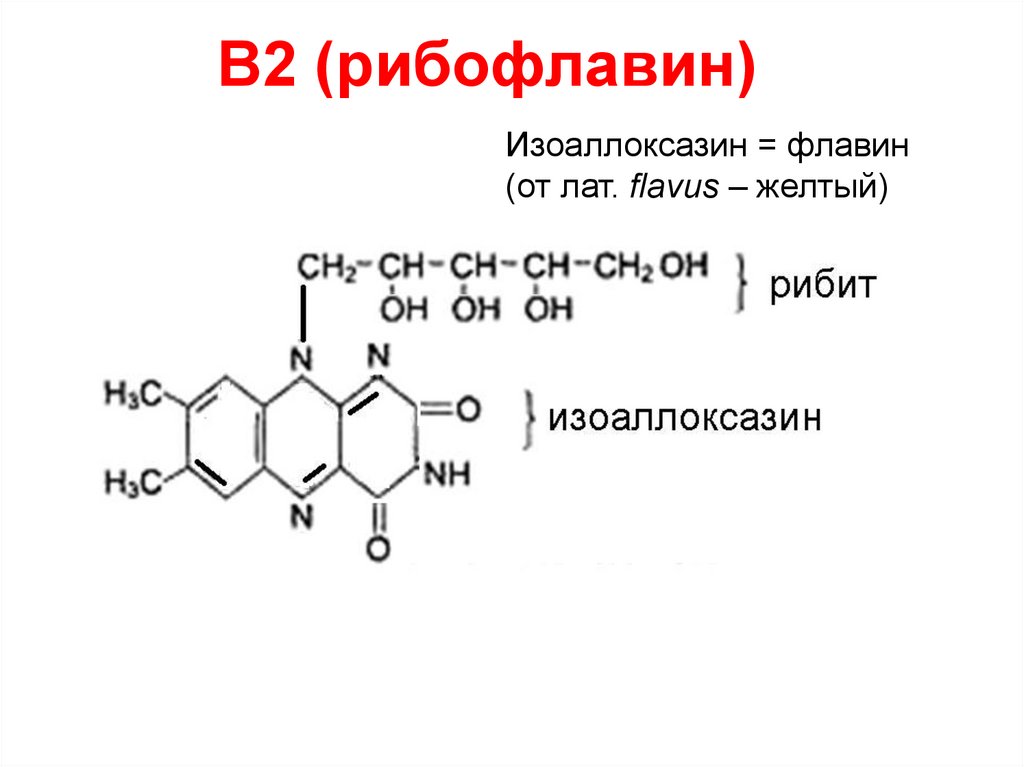
38. В2 (рибофлавин)
Изоаллоксазин = флавин(от лат. flavus – желтый)
39. ФАД
Биохимическая роль В2: в коферментах ФАД и ФМНФМН
ФАД
40. Синтез ФМН и ФАД у животных
АТФАДФ
АТФ
Mg2+
Рибофлавин
рибофлавин
киназа
Mg2+
ФМН
ФАД + 2 Р
ФМН-аденилилтрансфераза
41.
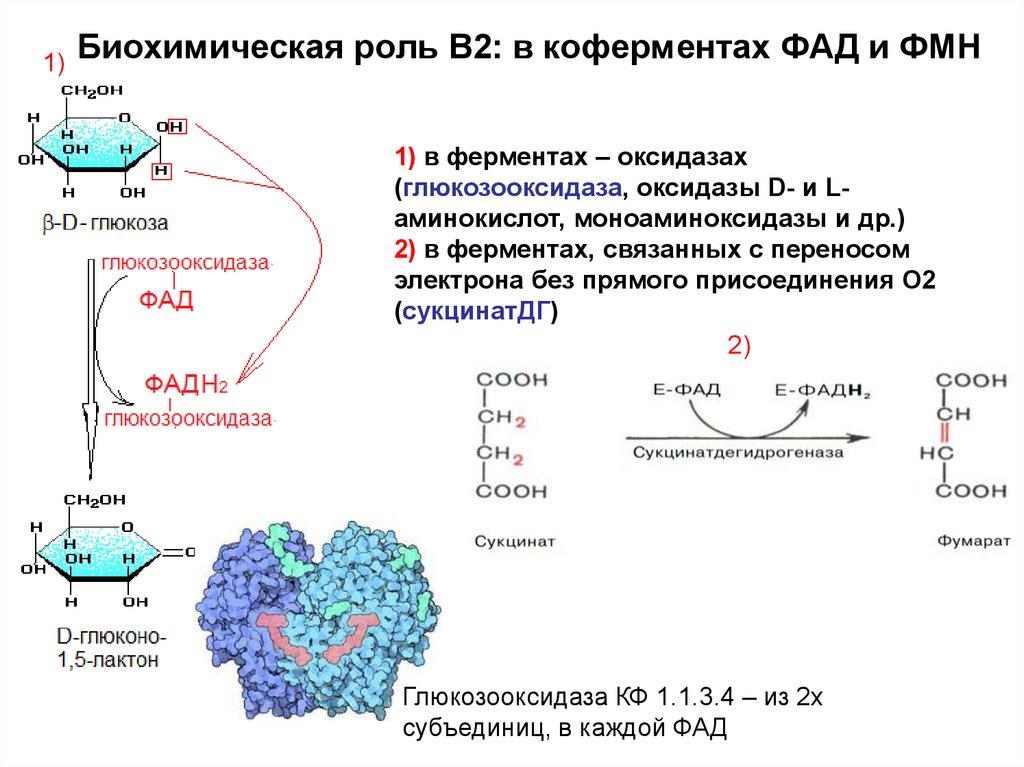
1)Биохимическая роль В2: в коферментах ФАД и ФМН
1) в ферментах – оксидазах
(глюкозооксидаза, оксидазы D- и Lаминокислот, моноаминоксидазы и др.)
2) в ферментах, связанных с переносом
электрона без прямого присоединения О2
(сукцинатДГ)
2)
Глюкозооксидаза КФ 1.1.3.4 – из 2х
субъединиц, в каждой ФАД
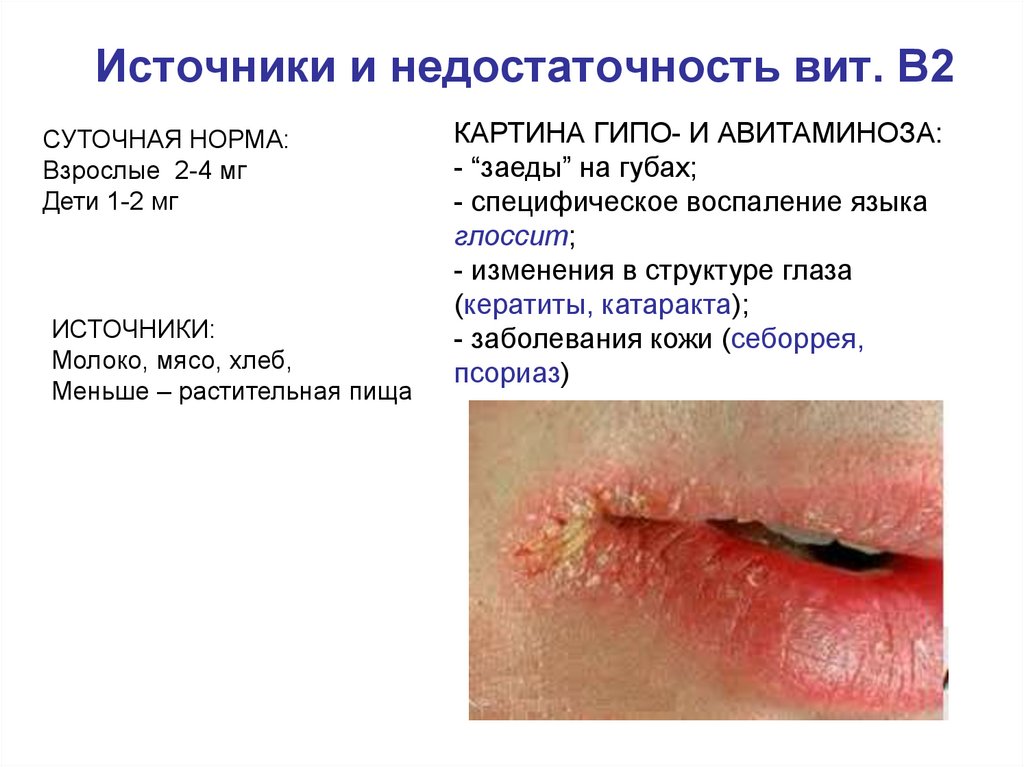
42. Источники и недостаточность вит. В2
СУТОЧНАЯ НОРМА:Взрослые 2-4 мг
Дети 1-2 мг
ИСТОЧНИКИ:
Молоко, мясо, хлеб,
Меньше – растительная пища
КАРТИНА ГИПО- И АВИТАМИНОЗА:
- “заеды” на губах;
- специфическое воспаление языка
глоссит;
- изменения в структуре глаза
(кератиты, катаракта);
- заболевания кожи (себоррея,
псориаз)
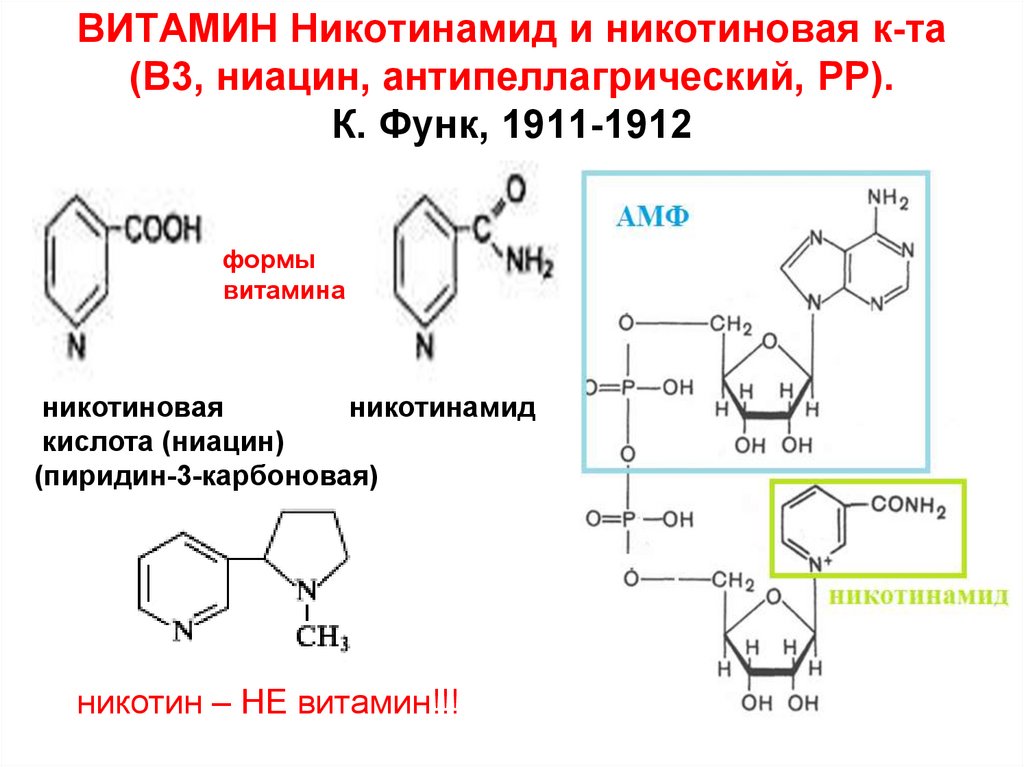
43. ВИТАМИН Никотинамид и никотиновая к-та (В3, ниацин, антипеллагрический, PP). К. Функ, 1911-1912
формывитамина
никотиновая
никотинамид
кислота (ниацин)
(пиридин-3-карбоновая)
никотин – НЕ витамин!!!
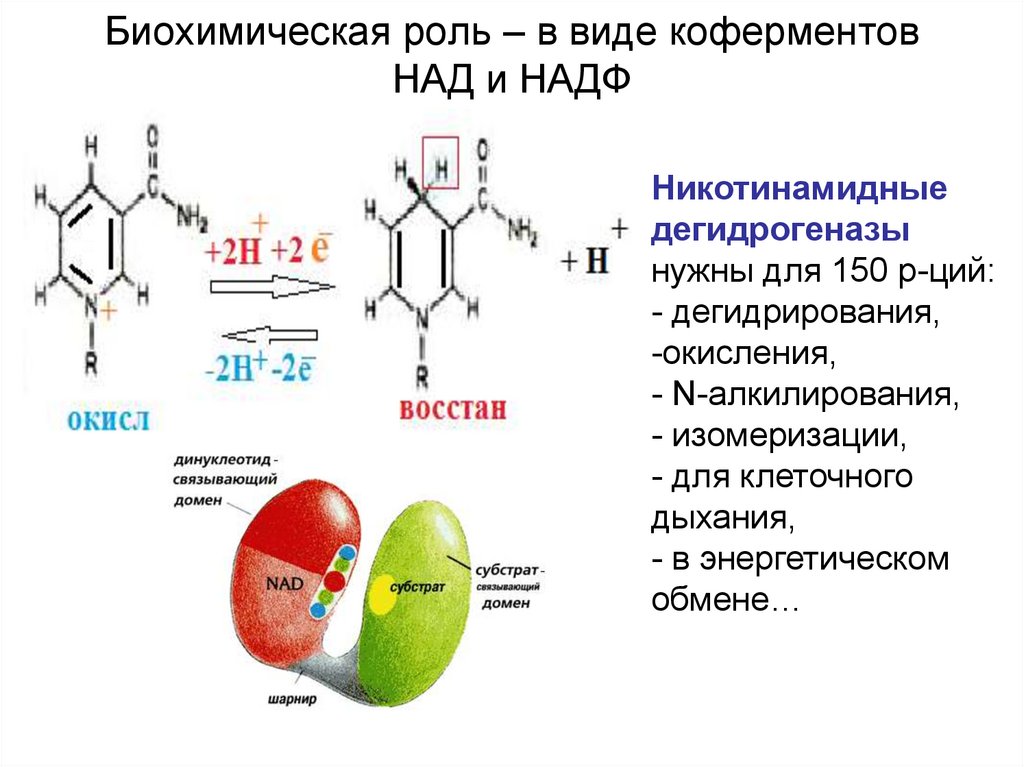
44. Биохимическая роль – в виде коферментов НАД и НАДФ
Никотинамидныедегидрогеназы
нужны для 150 р-ций:
- дегидрирования,
-окисления,
- N-алкилирования,
- изомеризации,
- для клеточного
дыхания,
- в энергетическом
обмене…
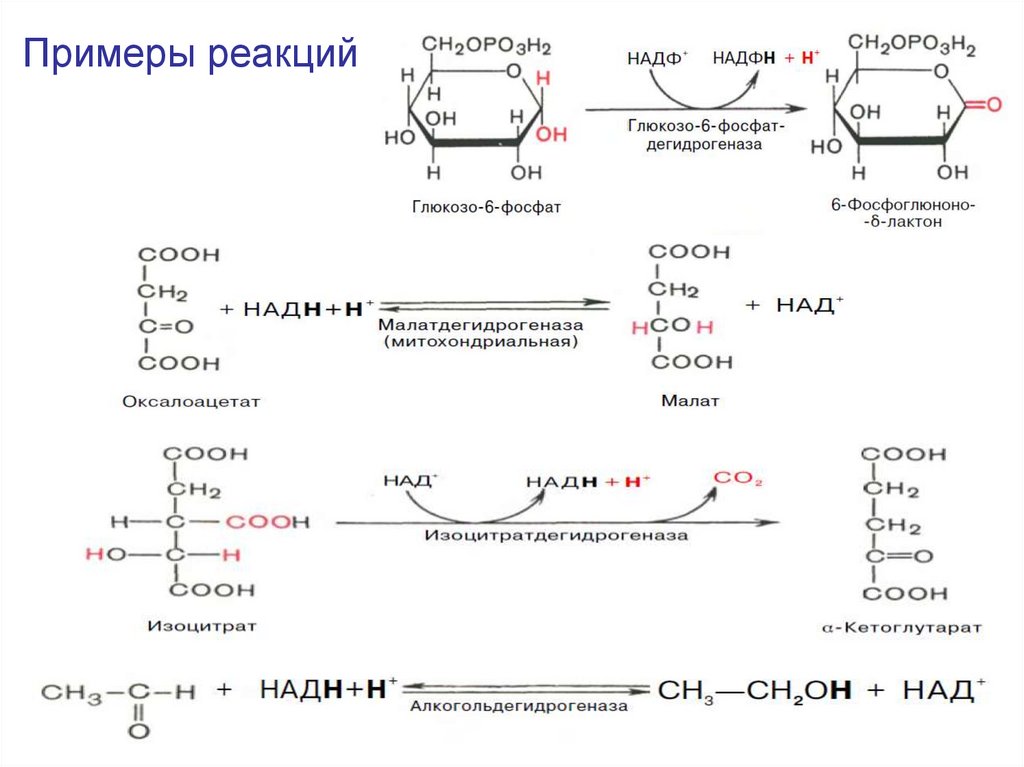
45. Примеры реакций
46. Авитаминоз редок, так как - синтез никотиновой кислоты у животных микрофлорой кишечника или в печени из 60 мг триптофана
получается 1 мг никотиновой кислотыНехватка триптофана
часто возникала из-за
кукурузной монодиеты
(в кукурузе его очень
мало)
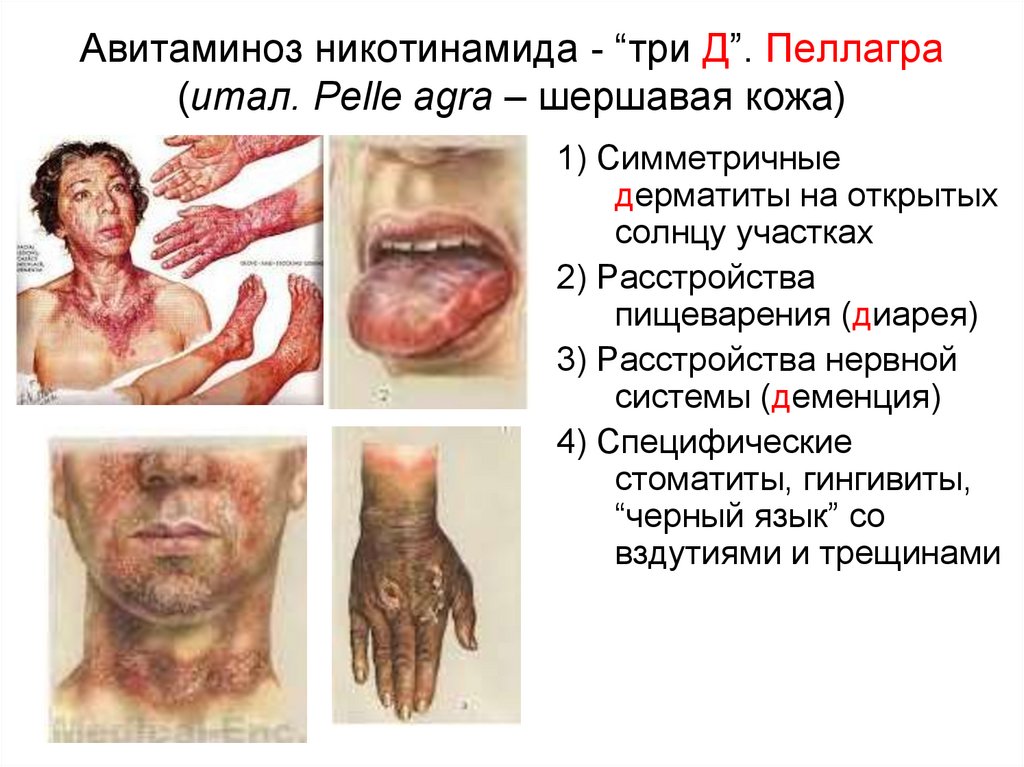
47. Авитаминоз никотинамида - “три Д”. Пеллагра (итал. Pelle agra – шершавая кожа)
1) Симметричныедерматиты на открытых
солнцу участках
2) Расстройства
пищеварения (диарея)
3) Расстройства нервной
системы (деменция)
4) Специфические
стоматиты, гингивиты,
“черный язык” со
вздутиями и трещинами
48. Источники и потребность в никотинамиде или никотиновой кислоте
• Источники: сухие пивные и пекарскиедрожжи, зерновые продукты.
• Потребность 6,5 мг на 1000 ккал пищи
(в среднем 15-22 мг в сут)
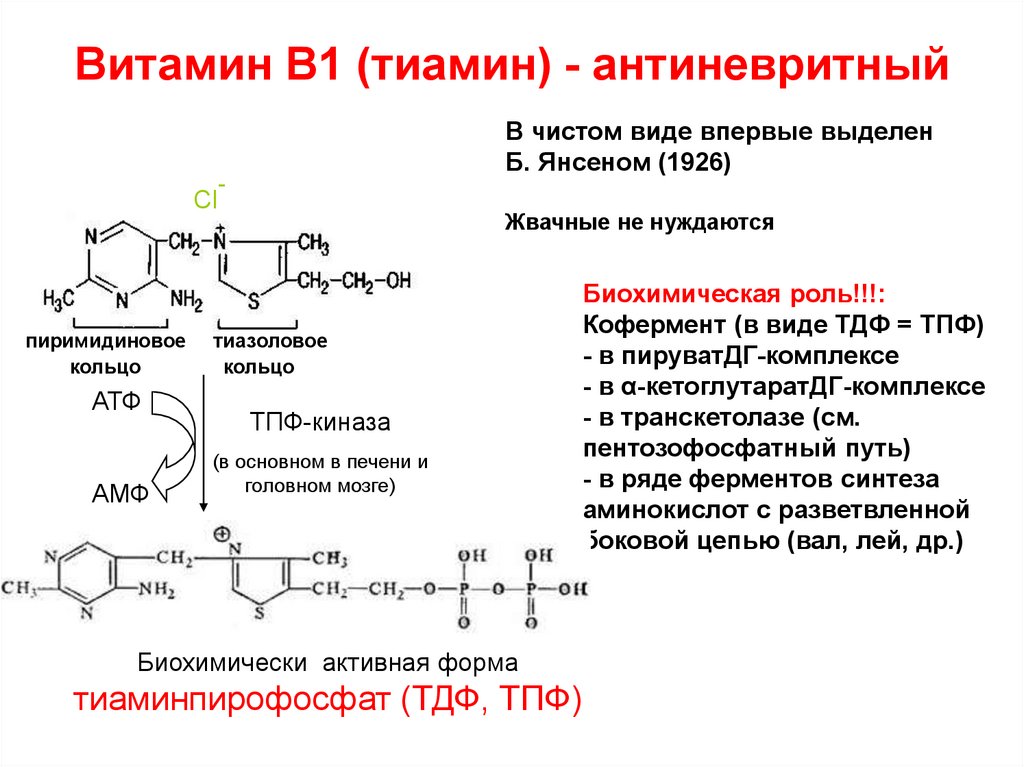
49. Витамин В1 (тиамин) - антиневритный
В чистом виде впервые выделенБ. Янсеном (1926)
-
Cl
пиримидиновое
кольцо
АТФ
АМФ
Жвачные не нуждаются
тиазоловое
кольцо
ТПФ-киназа
(в основном в печени и
головном мозге)
Биохимическая роль!!!:
Кофермент (в виде ТДФ = ТПФ)
- в пируватДГ-комплексе
- в α-кетоглутаратДГ-комплексе
- в транскетолазе (см.
пентозофосфатный путь)
- в ряде ферментов синтеза
аминокислот с разветвленной
боковой цепью (вал, лей, др.)
Биохимически активная форма
тиаминпирофосфат (ТДФ, ТПФ)
50. Авитаминоз Бери-бери (от сингальского beri – слабость, синоним: алиментарный полиневрит) – сухая (поражение головного мозга),
сердечная, острая формыНарушение метаболизма ПВК и накопление ее
в тканях. Блокирование транскетолаз
в пентозофосфатн.пути – снижение синтеза НАДФН
и рибозы
Питание очищенным рисом и при алкоголизме
Слева - голубь при
развившемся авитаминозе В1;
Справа – он же через
3 часа после
введения 4 мг
фракции
из дрожжей,
содержащей B1
51.
Гиповитаминоз начинается если взрослый человекполучает половину нормального количества витамина в
течение 5-6 дней
Основные источники витамина В1
- дрожжи
- рисовые и мучные отруби
- гречиха
- соя
- ржаная мука
- яичный желток
- печень, почки, мозг, свинина, говядина
Суточная потребность
1 – 1,2 мг
-В кислых растворах гораздо устойчивее к нагреванию,
чем в щелочных
52. Витамин Пантотеновая кислота – антидерматитный фактор (В5, 1938, Р. Уильямс)
Пантотеновая кислота =Дигидроксидиметил масляная
кислота (пантоевая) + β -аланин
Пантотеновая кислота
ИСТОЧНИКИ: “вездесущая”,
особенно много
- в пчелином маточном молочке
- в пивных дрожжах. Частично, но
недостаточно, синтезируется
микрофлорой кишечника человека
СУТОЧНАЯ ПОТРЕБНОСТЬ:
10 мг
АВИТАМИНОЗ: дерматиты, выпадение
волос, дегенеративные изменения
миелиновой оболочки спинного мозга.
(Миелин – это комплекс, основная часть
которого – липид галактоцереброзид).
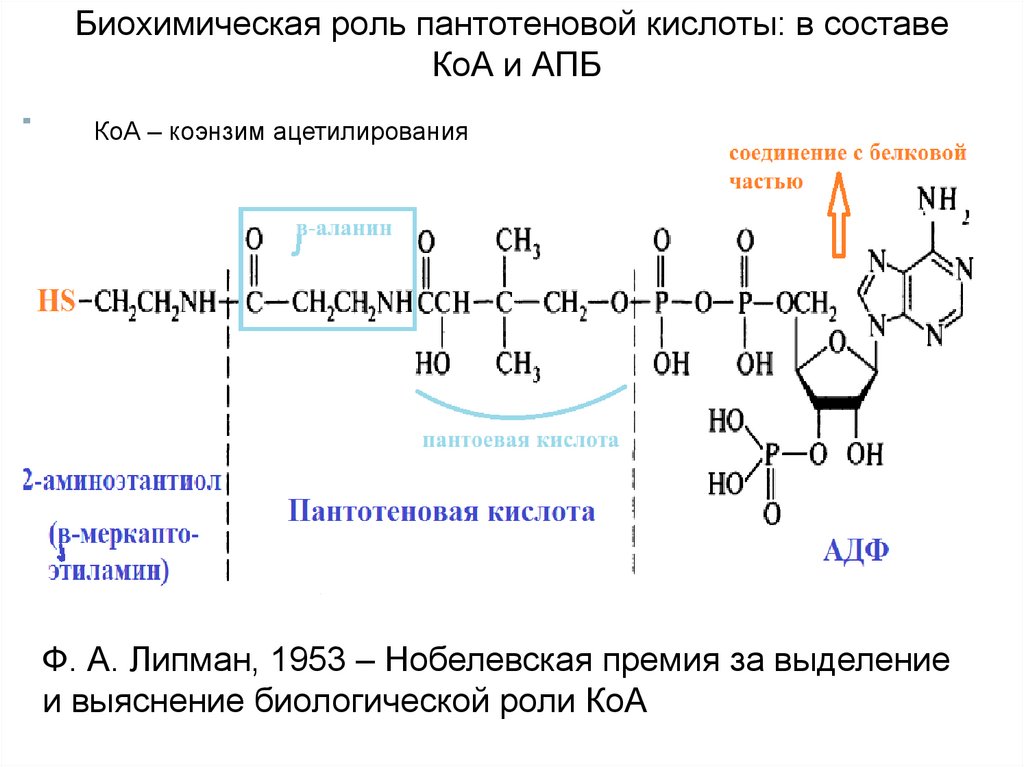
53. Биохимическая роль пантотеновой кислоты: в составе КоА и АПБ
КоА – коэнзим ацетилированияФ. А. Липман, 1953 – Нобелевская премия за выделение
и выяснение биологической роли КоА
54. Витамин В6 Пиридоксаль-5-фосфат (ПЛФ) и пиридоксамин-5-фосфат (ПМФ) – коферментные формы вит. В6 (простетические группы).
Присоединение к белку обычно через лизПиридоксаль + АТФ → пиридоксальфосфат + АДФ,
ферменты - киназы
55. Биохимическая роль В6 – коферменты (в фосфорилированных формах)
Более 20 пиридоксалевых ферментов- Аминотрансферазы (перенос аминогруппы при
переаминировании)
- Декарбоксилазы аминокислот (необратимое отщепление
СО2 от СООН-группы аминокислот с образованием
биогенных аминов)
- Ферменты неокислительного дезаминирования серина и
треонина, окисления триптофана,
- Ферменты превращения серосодержащих аминокислот,
- Взаимопревращение серина и глицина
- Ферменты синтеза ᵟ-аминолевулиновой кислоты –
предшественника синтеза гема
56. Источники и суточная потребность витамина В6
Источники: Бобовые, картофель, мясо, печеньПотребность: 2 мг, но точно не установлено,
т.к. частично синтезируются микрофлорой кишечника.
Авитаминоз:
Угнетение выработки эритроцитов,
воспалительные процессы кожи, замедление
роста, нарушение обмена триптофана и др.
аминокислот
57. Витамин H – биотин (биос II, от bios – жизнь)
Haut (нем.) - кожа1916 – сырой яичный белок токсичен.
Дрожжи и печень в пище – снятие симптомов
1935 – вит.Н выделен как соединение (Ф. Кёгль),
Специфический ростовой фактор для дрожжей и
азотфиксирующих бактерий
1942 – строение (В. Дю Виньо),
1944-1945 – химический синтез
Авидин, связавший биотин. Авидин – гомотетрамер,
поэтому может связать до 4 молекул биотина.
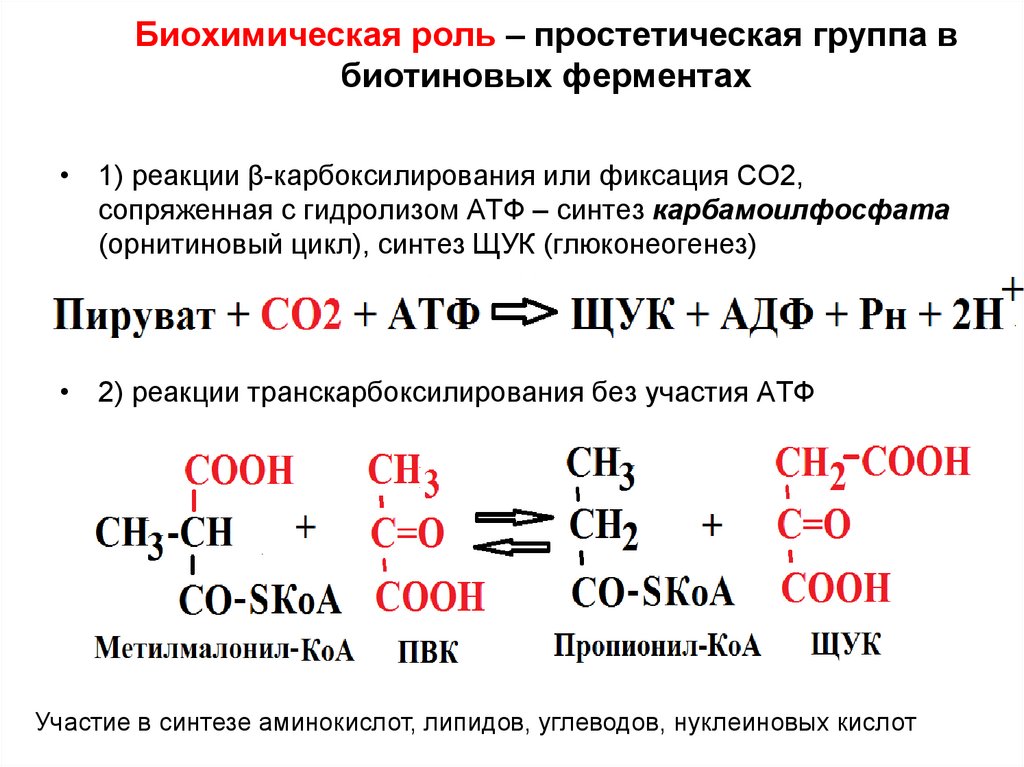
58. Биохимическая роль – простетическая группа в биотиновых ферментах
• 1) реакции β-карбоксилирования или фиксация СО2,сопряженная с гидролизом АТФ – синтез карбамоилфосфата
(орнитиновый цикл), синтез ЩУК (глюконеогенез)
• 2) реакции транскарбоксилирования без участия АТФ
Участие в синтезе аминокислот, липидов, углеводов, нуклеиновых кислот
59. Орнитиновый цикл
60. Недостаточность биотина
СУТОЧНАЯ ПОТРЕБНОСТЬ0,1 – 0,3 мг
Недостаточность биотина
Покраснение и шелушение
кожи
• Выпадение волос (шерсти,
перьев)
• Красные отечные “очки” вокруг
глаз
• Изменения походки и типичная
поза с согнутой спиной
•ИСТОЧНИКИ
- синтез микрофлорой кишечника
(вполне достаточно)
- печень, почки, яичный желток
- рисовые отруби, пшеничная мука
- цветная капуста, бобы
Личинки НАСЕКОМЫХ !
61. “Витамины” P – группа соединений (полифенолы, биофлавоноиды)
Permeability - проницаемостьФлавоны, флаваны, флаваноны,
флаванолы (представитель – рутин),
антоцианы, лейкоантоцианы, катехины…
Суточная потребность - ?
Источники: окрашенные плоды и ягоды (черника,черешня,
черная смородина, темный виноград и др.).
Синтезируются в растениях по ШИКИМАТНОМУ ПУТИ
1) Снижают проницаемость соединительной ткани, сосудов, ингибируя
гиалуронидазу. Блокируют некоторые металлы, чем изменяют активность
некоторых других ферментов
2) Окислительно-восстановительные процессы, совместно с вит.С
(лекарственное средство “Аскорутин”)
3) Способствуют выделению кортикостероидов (предохраняют от окисления
адреналин, он стимулирует гипофиз, гипофиз стимулирует секрецию
кортикостероидов)
62. Жирорастворимые витамины
• 1) А• 2) D
• 3) E
• 4) К
Депо – печень.
Способны накапливаться.
!При передозировке
проявляют токсичность
(вплоть до смертных
случаев)
63. Вит. А – группа веществ (ретиноиды и провитамины А)
Ретинол – циклический спирт с боковойцепью из 2х изопренов и первичной ОНгруппы. Нестабилен, разлагается
кислородом воздуха и на свету, в организме
окисляется до ретиналя и ретиноевой
кислоты.
Ретиноиды (в тканях животных в виде
сложных эфиров – форме,
защищающей от разрушения):
• - ретинол (витамин A1),
• - дегидроретинол (витамин A2),
• - ретиналь (альдегид витамина A1),
• - ретиноевая кислота.
Депо витамина — печень (90%),
почки, жировая ткань, надпочечники.
Открыт в 1913: роль в питании сливочного масла, желтка куриных яиц (на примере мышей, Висконсинский (Э. Макколлум, М. Дэвис) и Йельский (Т. Осборн, Л.
Мендель) ун-тах.
Описана структура в 1931 году (П. Каррер, Нобелевская премия 1937),
кристаллизован в 1937 (Г. Холмс, Р. Корбет), в 1946 - хим. синтез (Д. А. ван Дорп,
Й. Ф. Аренс).
Роль витамина A в зрении открыта биохимиком Дж. Уолдом ( Нобелевская
премия, 1967).
64. Биохимическая роль вит.А
• Ретиналь - компонент зрительного пигмента родопсина.• Ретинол – в составе клеточных мембран, в антиоксидантной
защите организма, необходим для роста, дифференциации и
сохранения функций эпителиальных и костных тканей, для
размножения.
• Ретиноевая кислота в 10 раз активнее ретинола при влиянии на
клеточную дифференциацию, но менее активна при влиянии на
размножение
В крови витамин A соединяется со связывающим белком (БСР),
обеспечивающим растворимость ретинола, защиту от окисления и
транспорт в различные ткани. Витамин, не связанный с белком,
токсичен. Комплекс (витамин A + БСР) соединяется с белком
транстиретином, препятствующим фильтрации витамина в почках. По
мере использования вит. A отсоединяется от этих белков и идет в
ткани. Ретиноевая кислота соединяется с альбумином.
В клетках органов-мишеней есть специальные цитозольные рецепторы,
распознающие и связывающие комплекс вит.А+БСР
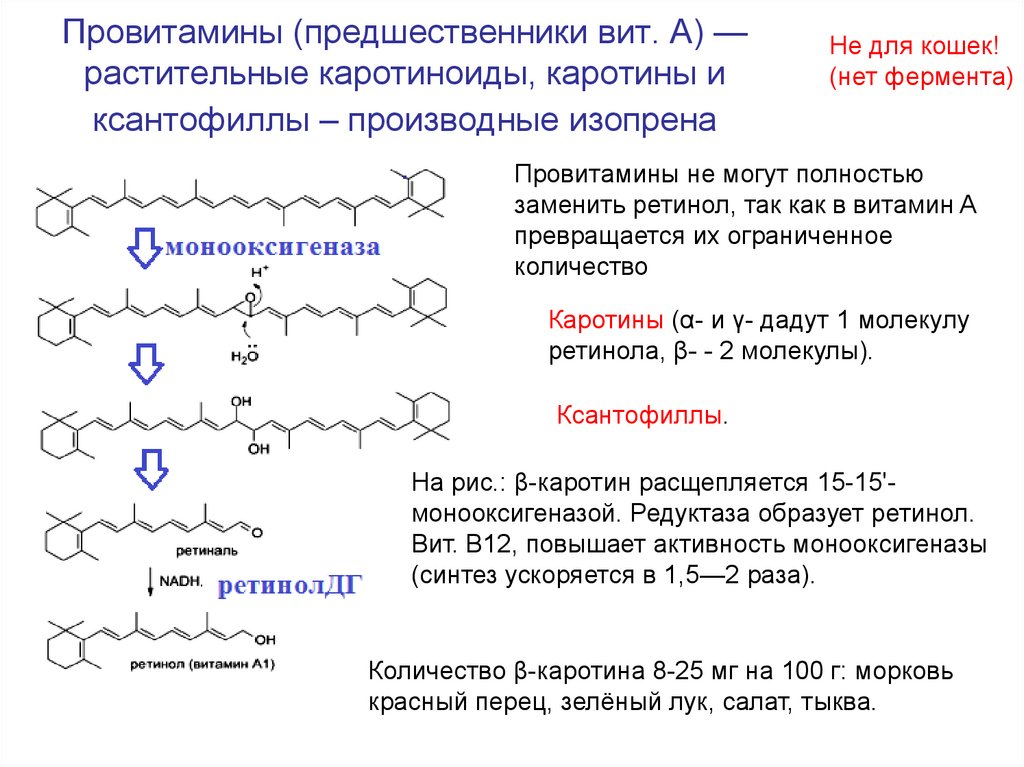
65. Провитамины (предшественники вит. А) — растительные каротиноиды, каротины и ксантофиллы – производные изопрена .
Провитамины (предшественники вит. А) —растительные каротиноиды, каротины и
ксантофиллы – производные изопрена
.
Не для кошек!
(нет фермента)
Провитамины не могут полностью
заменить ретинол, так как в витамин A
превращается их ограниченное
количество
Каротины (α- и γ- дадут 1 молекулу
ретинола, β- - 2 молекулы).
Ксантофиллы.
На рис.: β-каротин расщепляется 15-15'монооксигеназой. Редуктаза образует ретинол.
Вит. B12, повышает активность монооксигеназы
(синтез ускоряется в 1,5—2 раза).
Количество β-каротина 8-25 мг на 100 г: морковь
красный перец, зелёный лук, салат, тыква.
66. Недостаточность вит. A
1 МЕ = 0,3 мкг ретинола, 0,6 мкг β-каротина или1,2 мкг других каротиноидов - провитаминов A.
1 эквивалент ретинола (ЭР) =1 мкг ретинола, 2
мкг растворённого в жире β-каротина… С 2001 г.
– предложен эквивалент активности ретинола
(RAE). 1 RAE = 1 мкг ретинола, 2 мкг
растворённого в жире β-каротина (в виде
фармпрепарата), 12 мкг «пищевого» β-каротина
или 24 мкг иных провитаминов A.
Ксерофтальмия
• - поражения эпителия,
ухудшение зрения,
нарушение смачивания
роговицы, снижение
иммунной функции,
диарея
Мужчине - 0,9 мг/сут,
женщине 0,7 мг/сут.
Передозировка опасна! Для взрослых —
не более 3 мг/cут. Выводится медленно:
за 21 день из организма исчезает всего
34 % введённой дозы, поэтому может
накапливаться.
Печень белого медведя, акулы и др. –
случаи смертельного исхода (1597 года,
плавание Геррита де Веера)
67. Витамин D – антирахитный, группа кальциферолов стероидной природы
1924 – полученпрепарат против
рахита из растительных масел
после УФ
Возможен синтез в коже человека под действием УФ-облучения
68. Биохимическая роль – в основном в виде 1,25-дигидроксивитамина D (1,25-диоксикальциферола)
Биохимическая роль – в основном в виде 1,25дигидроксивитамина D (1,25-диоксикальциферола)Для превращения в
активную форму
важны печень и
почки.
• Транспорт через
мембраны,
распределение,
регуляция Ca и P.
• Может активировать
специальные белки
– факторы,
усиливающие синтез
мРНК белков
гомеостаза Ca и P.
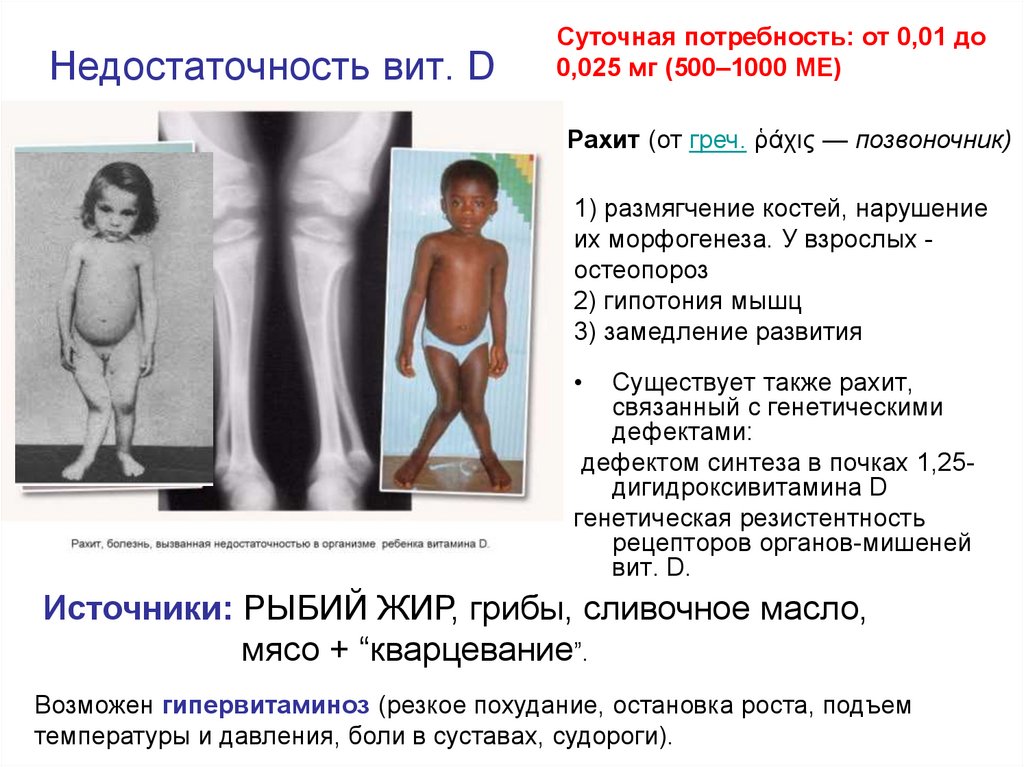
69. Недостаточность вит. D
Суточная потребность: от 0,01 до0,025 мг (500–1000 ME)
Рахит (от греч. ῥάχις — позвоночник)
1) размягчение костей, нарушение
их морфогенеза. У взрослых остеопороз
2) гипотония мышц
3) замедление развития
Существует также рахит,
связанный с генетическими
дефектами:
дефектом синтеза в почках 1,25дигидроксивитамина D
генетическая резистентность
рецепторов органов-мишеней
вит. D.
Источники: РЫБИЙ ЖИР, грибы, сливочное масло,
мясо + “кварцевание”.
Возможен гипервитаминоз (резкое похудание, остановка роста, подъем
температуры и давления, боли в суставах, судороги).
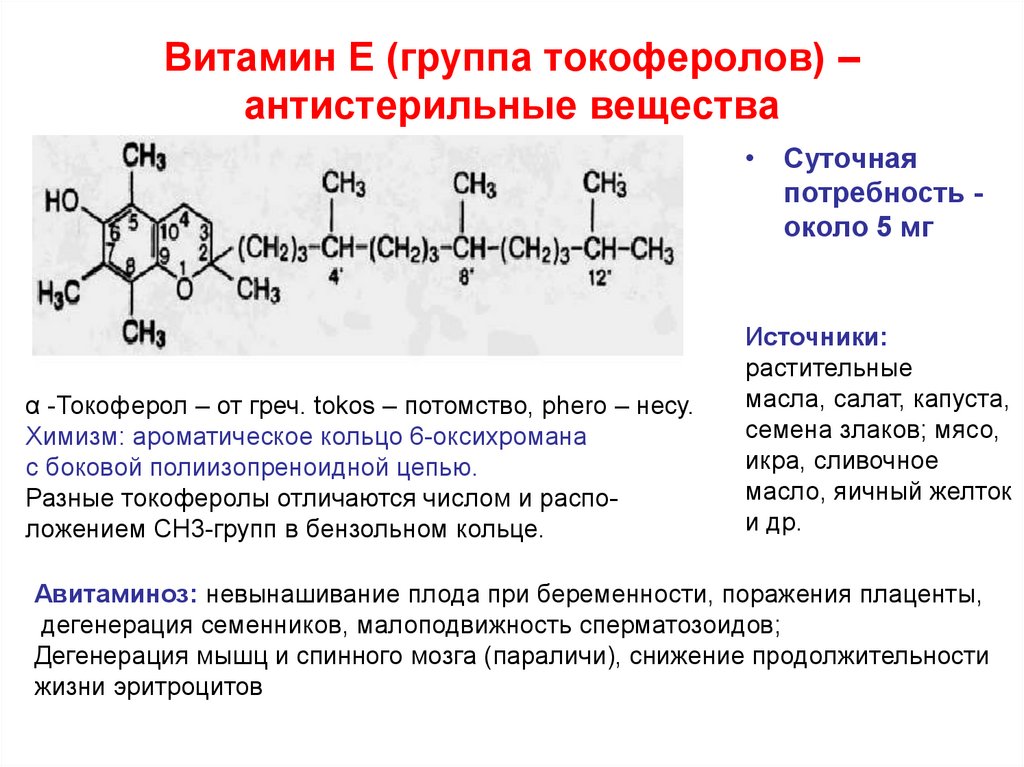
70. Витамин Е (группа токоферолов) – антистерильные вещества
• Суточнаяпотребность около 5 мг
α -Токоферол – от греч. tokos – потомство, phero – несу.
Химизм: ароматическое кольцо 6-оксихромана
с боковой полиизопреноидной цепью.
Разные токоферолы отличаются числом и расположением СН3-групп в бензольном кольце.
Источники:
растительные
масла, салат, капуста,
семена злаков; мясо,
икра, сливочное
масло, яичный желток
и др.
Авитаминоз: невынашивание плода при беременности, поражения плаценты,
дегенерация семенников, малоподвижность сперматозоидов;
Дегенерация мышц и спинного мозга (параличи), снижение продолжительности
жизни эритроцитов
71. Биохимическая роль вит. Е - антиоксидант
• Противостоит окислению липидов,способствует тканевому дыханию
• Участвует в обмене селена (входящего в
глутатионпероксидазу и др. важные
селенопротеины)
• Роль в метаболизме убихинонов
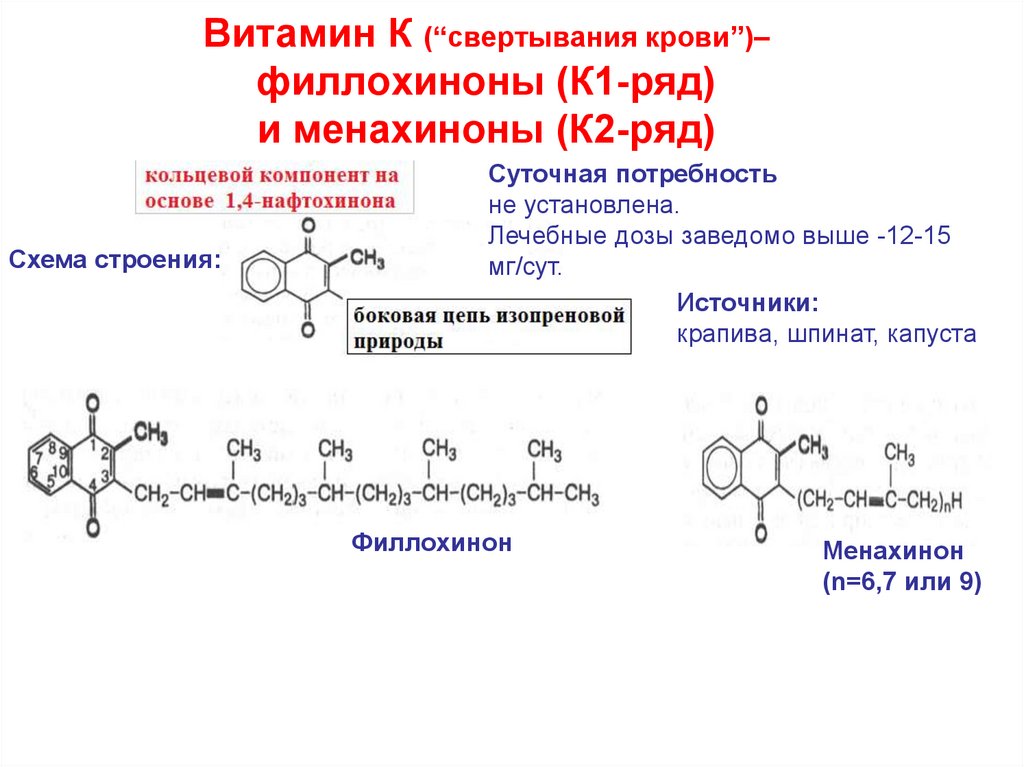
72. Витамин К (“свертывания крови”)– филлохиноны (К1-ряд) и менахиноны (К2-ряд)
Схема строения:Суточная потребность
не установлена.
Лечебные дозы заведомо выше -12-15
мг/сут.
Источники:
крапива, шпинат, капуста
Филлохинон
Менахинон
(n=6,7 или 9)
73.
• Витамин К, воздействуя на фермент γ-глутамилкарбоксилазу ,у человека стимулирует биосинтез не менее 14 белков, для
работы которых необходима ɣ-карбоксиглутаминовая к-та,
таких как ряд факторов свертывания крови и
остеокальцин (Gla-белок кости).
Антагонист витамина К -
варфарин (крысиный яд
и лекарство против тромбов) –
антикоагулянт крови.
74. Роль вит.К
1. В нормализации процессов свертывания крови2. В образовании костной ткани
3. У бактерий – участие в анаэробном и аэробном дыхании как
переносчик электронов
Авитаминоз вит. К у взрослых почти не встречается.





















































 Биология
Биология








