Похожие презентации:
Химическая кинетика
1. «Химическая кинетика» – это раздел химии, занимающийся изучением скоростей химических реакций
02.04.2017ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
1
2. Кинетика «обратимая» ,«необратимая» и «последовательная
02.04.2017ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
2
3. Закон «действующих масс»
02.04.2017ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
3
4. «Скорость» элементарной хим. реакции
Кинетическое уравнениехимической реакции
02.04.2017
ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
4
5.
«Скорость» сложной хим. реакцииКинетическое уравнение
химической реакции
02.04.2017
ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
5
6. Значения n1, n2, n3
Кинетическое уравнение химической реакции, порядок и константу скорости определяютэкспериментально, его нельзя предсказать по виду химического уравнения реакции
02.04.2017
ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
6
7. «Зависимость» константы скорости от температуры
Кинетическое уравнениехимической реакции
После интегрирования (при условии что E=const) уравнение приводится к виду:
Здесь B – константа интегрирования, A – предэкспоненциальный множитель (lnA=B)
02.04.2017
ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
7
8. «Графическая интерпретация» уравнения Аррениуса
Получаютэкспериментально
02.04.2017
Если экспериментальные данные
подчиняются уравнению (закону)
Аррениуса, зависимость окажется
линейной!
ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
8
9. Пример «экспериментальных данных»
02.04.2017ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
9
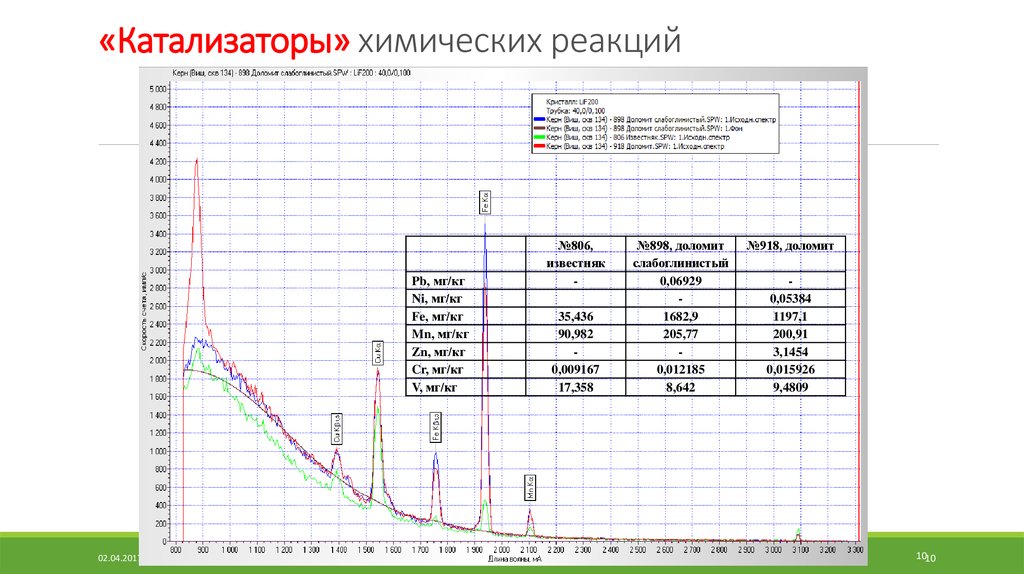
10. «Катализаторы» химических реакций
Pb, мг/кгNi, мг/кг
Fe, мг/кг
Mn, мг/кг
Zn, мг/кг
Cr, мг/кг
V, мг/кг
02.04.2017
№806,
известняк
35,436
90,982
0,009167
17,358
№898, доломит
слабоглинистый
0,06929
1682,9
205,77
0,012185
8,642
ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
№918, доломит
0,05384
1197,1
200,91
3,1454
0,015926
9,4809
1010
11. «Аппарат» формальной кинетики позволяет
02.04.2017ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
11
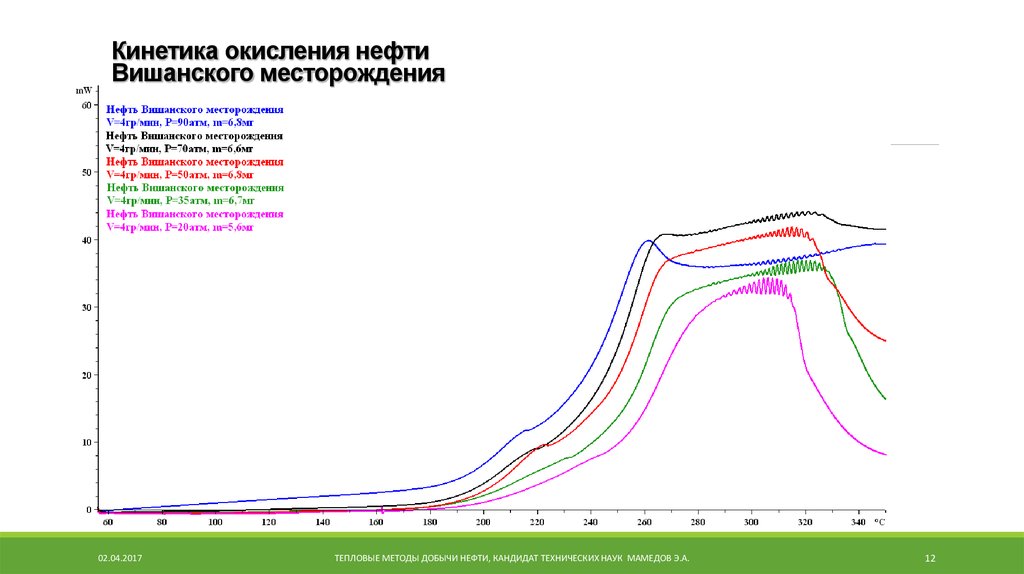
12.
Кинетика окисления нефтиВишанского месторождения
02.04.2017
ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
12
13. Оценка времени самовосламенения нефти при закачке в пласт воздуха (Задача №5)
ПараметрМолекулярная масса кислорода
Плотность кислорода
Количество теплоты по кислороду
1 ккал
Нефтенасыщенность
Пористость
Уд. объемная теплоемкость пласта, Сн
Температура пласта, Tо
Плотность нефти,
Температура активации, Е
Теплота реакции по кислороду, r0
Концентрация нефти в пласте, Zt
Скорость реакции, W0
Скорость реакции
Энергия активации, Е
Время инициирования
PO2
Источник
справочные данные
справочные данные
[2]
справочные данные
данные по Вишанскому месторождению
данные по Вишанскому месторождению
данные по Вишанскому месторождению
К
данные по Вишанскому месторождению
кг/м3
данные по Вишанскому месторождению
К
[3]
кДж/нм3
[2]
кг/м3
данные по Вишанскому месторождению
нм3/м3*сут
[3]
кг/(кг*с)
71200 Дж/моль
[3]
[3]
1935,7 МПа-1 с-1
5,5 MПа
8,3145 Дж/моль К
[3]
данные по Вишанскому месторождению
справочные данные
329
844
8569,3
13745,78
71,74
0,8981
1,67E-08
o
Константа Аррениуса, Аr
Парциальное давление кислорода,
Газовая постоянная,
R
0,032 кг/моль
1,42 кг/м3
74 ккал/моль
4,186 кДж
0,85
0,1
2540 кДж/(м 3 о С)
30,58
t
*
c р н Tо
2
ro Wo zt E
сут
1. Патент РФ №2139421. Способ разработки нефтяного месторождения / Антониади Д.Г., Батурин Ю.Е., Бернштейн А.М., Боксерман А.А., Кашик А.С., Малышев А.Г, Сонич В.П. Заявл. 09.09.1998.
2. О.М. Айзикович, М.Г. Булыгин, Л.И. Кораблев. Тепловой эффект реакций окисления в процессе влажного внутрипластового горения. Нефтепромысловое дело и транспорт нефти. 1985, №11.
3. В. В. Бондаренко. Окисление нефтей кислородом воздуха при начальных пластовых условиях. Нефтепромысловое дело. 1982, №9.
13
14. Формула Гаделя
tignгде
-
tign
( c)r M O2 -
Tr
E
R
ko
o
So
PO2
n
H O2
02.04.2017
2 RTr
2
( c) r M O2 Tr 1
E
E
exp
E
RT
n
ko o So ( PO2 ) H O2
R
время возгорания, сут,
удельная объемная теплоемкость пласта, kJ/(m3.K,),
молекулярная масса кислорода, 32.0 kg/kmol,
-
начальная температура пласта, K,
энергия активации, kJ/kmol
универсальная газовая постоянная, 8.3145 kJ/(kmol.K),
константа Аррениуса, сут-1кPa-n,
пористость, доля единицы,
плотность нефти, kg/m3
-
начальная нефтенасыщенность, доля единицы,
- парциальное давление закачиваемого кислорода, кPa,
- порядок реакции по кислороду,
= выделяемое тепло на kmol кислорода, ~ (330-440) x103 KJ/kmol O2.
ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
14
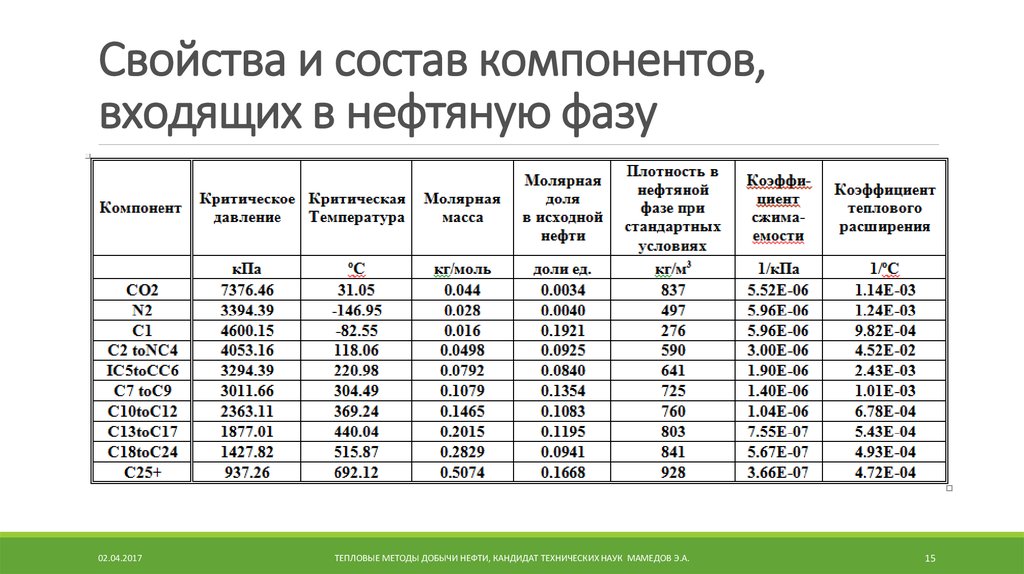
15. Свойства и состав компонентов, входящих в нефтяную фазу
02.04.2017ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
15
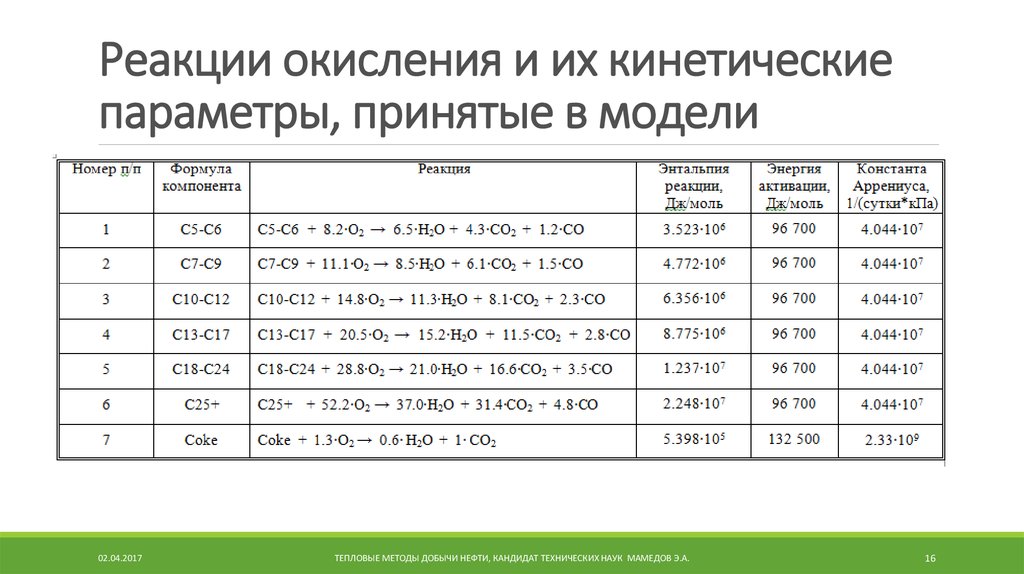
16. Реакции окисления и их кинетические параметры, принятые в модели
02.04.2017ТЕПЛОВЫЕ МЕТОДЫ ДОБЫЧИ НЕФТИ, КАНДИДАТ ТЕХНИЧЕСКИХ НАУК МАМЕДОВ Э.А.
16














 Химия
Химия








