Похожие презентации:
Химические свойства металлов (9 класс)
1. «ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ»
Урок химии9 класс
«МОБУ СОШ №1 с. Бураево»
2.
Металлов много есть, но дело не в количестве:В команде работящей металлической
Такие мастера, такие личности!
Преуменьшать нам вовсе не пристало
Заслуги безусловные металлов
Пред египтянином, китайцем, древним греком
И каждым современным человеком.
3. Повторение
1.2.
3.
4.
5.
История металлов.
Распространение в природе.
Положение металлов в ПСХЭ.
Строение атомов металлов и веществ
металлов.
Взаимосвязь строения металлов и
физических свойств.
4. История металлов.
С глубокой древности человеку былиизвестны 7 металлов:
Au, Ag, Cu, Sn, Pb, Fe, Hg.
5.
Часы истории человечества сталиотсчитывать время быстрее, когда в его
жизнь вошли металлы и сплавы…
6.
Бронза – сплав меди и олова;Латунь – сплав меди и цинка;
Мельхиор – сплав меди и никеля;
Дюралюминий – сплав алюминия,
меди и магния;
Железные
сталь.
сплавы – чугун и
7.
История человечества – этоистория металлов
Каменный век
Бронзовый век
Медный век
Железный век
8. Железный век продолжается …
90% всегоколичества
металлов и
металлических
сплавов
приходится на
железные
сплавы.
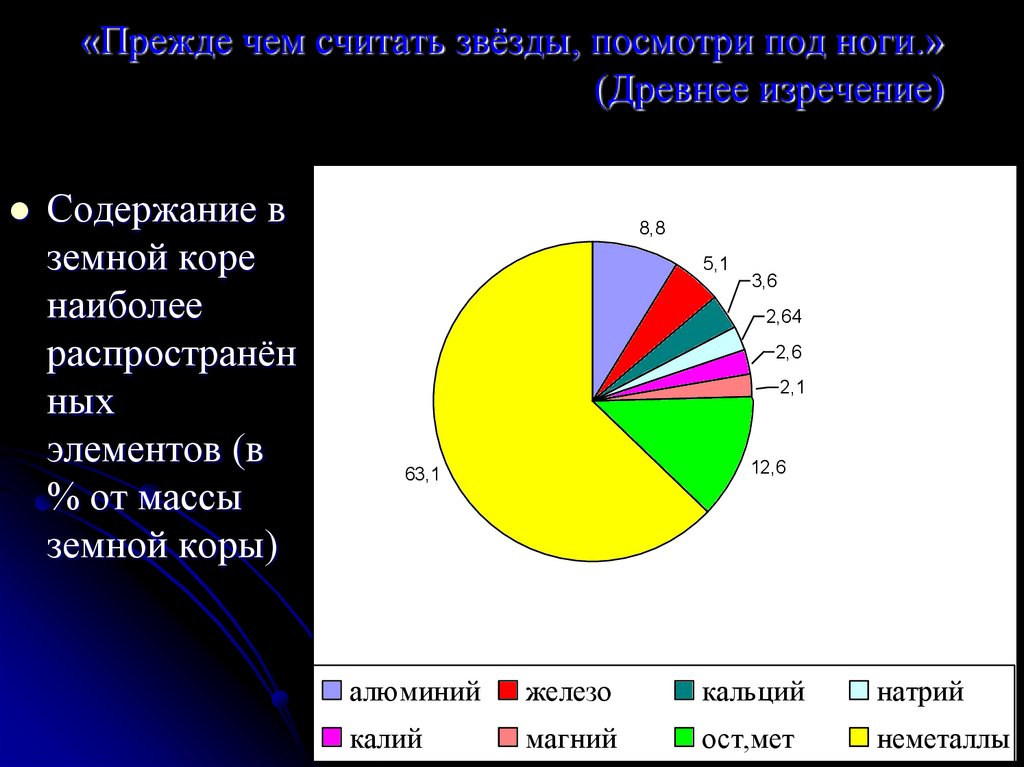
9. «Прежде чем считать звёзды, посмотри под ноги.» (Древнее изречение)
Содержание вземной коре
наиболее
распространён
ных
элементов (в
% от массы
земной коры)
8,8
5,1
3,6
2,64
2,6
2,1
12,6
63,1
алюминий
железо
кальций
натрий
калий
магний
ост,мет
неметаллы
10.
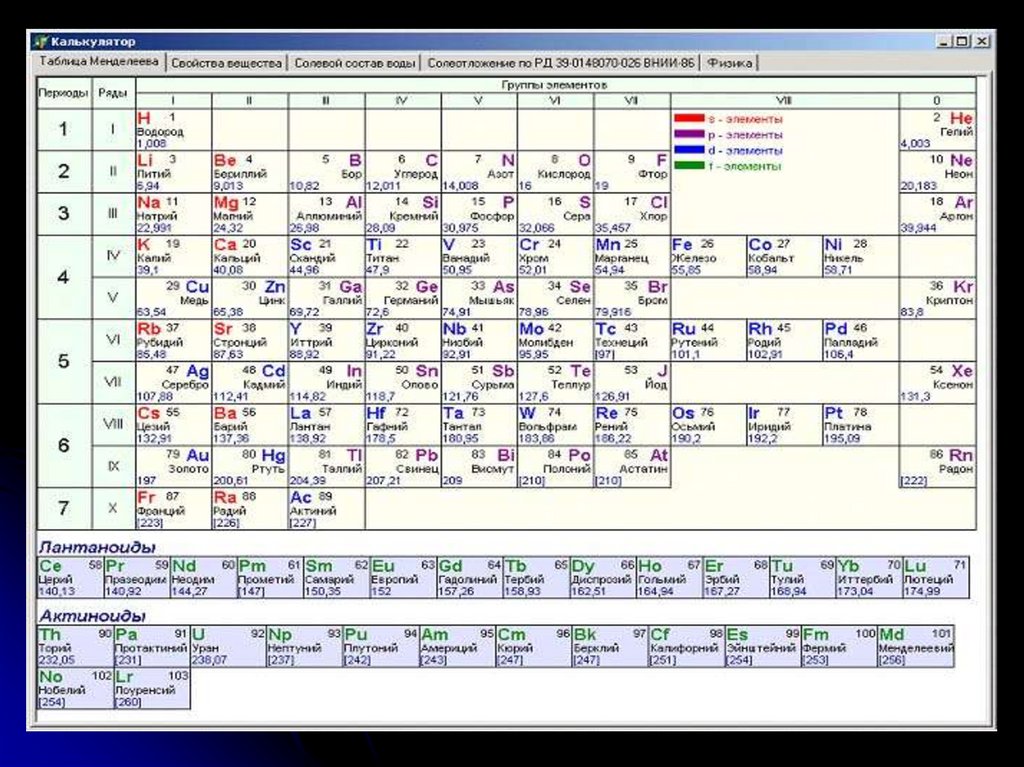
Из 110 изученных химическихэлементов к металлам относятся 88.
Все наиболее распространённые
элементы располагаются в верхней
части менделеевской таблицы.
Где же находятся металлы?
11.
12. Строение атомов металлов и веществ металлов.
Из положения в ПСХЭ:1. Атомы металлов на последнем
энергетическом уровне имеют 1 – 3 ē
Исключения:
Ge, Sn, Pb - 4ē
Sb, Bi - 5ē
Po - 6ē
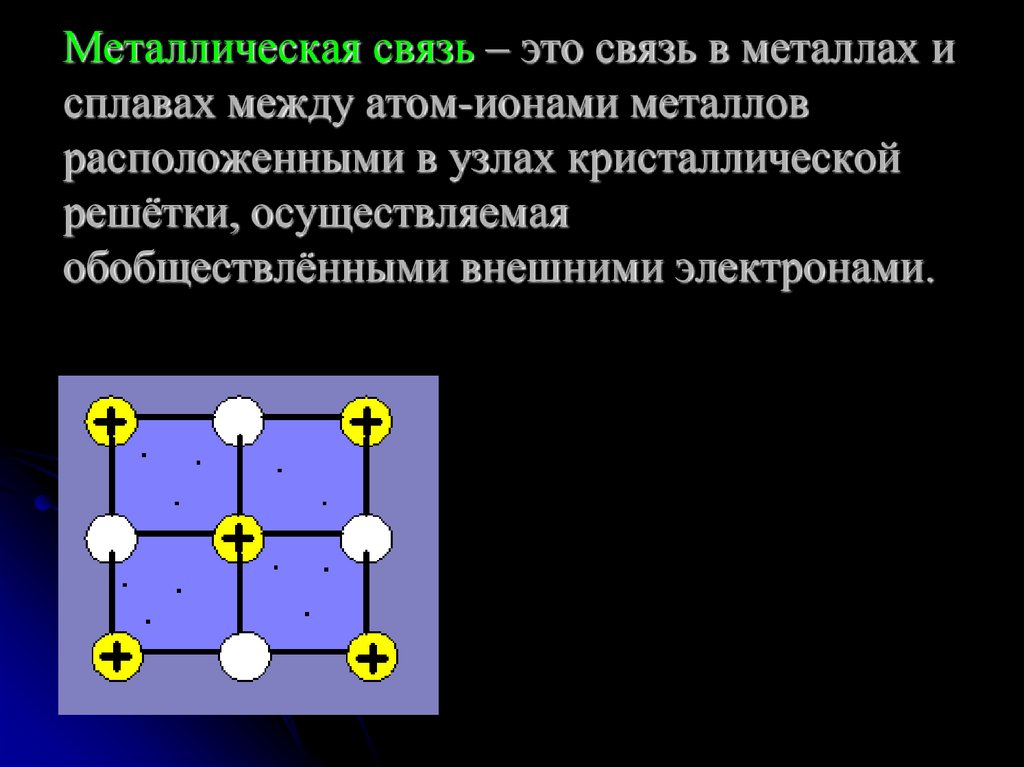
13. Металлическая связь – это связь в металлах и сплавах между атом-ионами металлов расположенными в узлах кристаллической решётки,
осуществляемаяобобществлёнными внешними электронами.
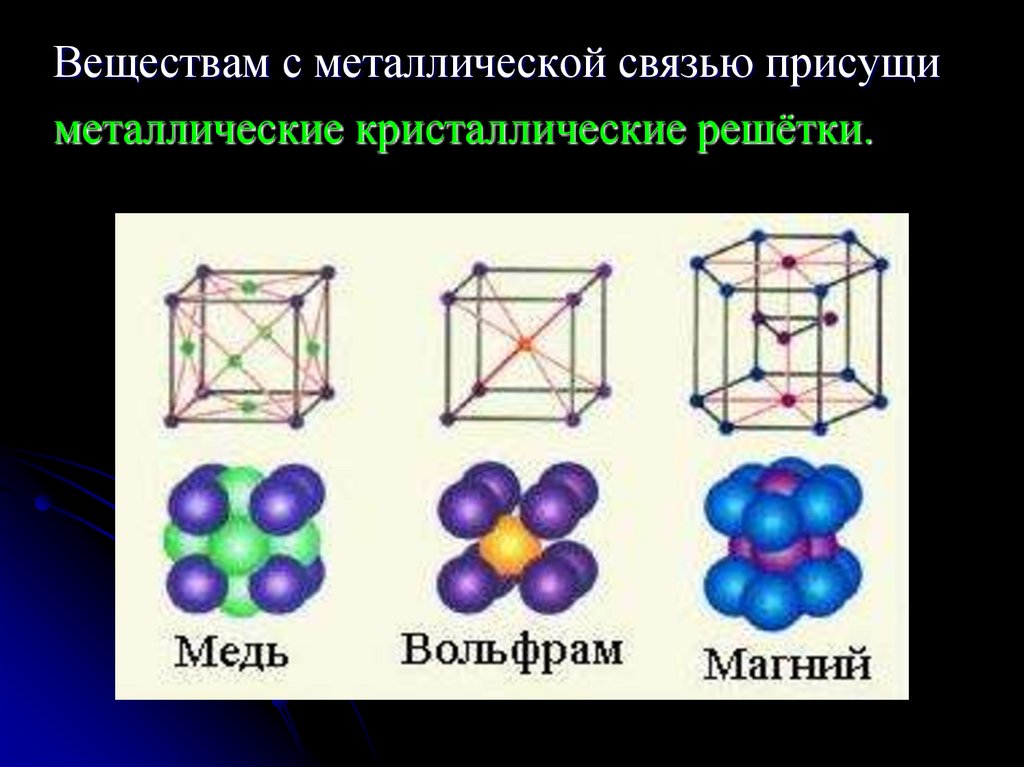
14.
Веществам с металлической связью присущиметаллические кристаллические решётки.
15. Внимание
16. Физические свойства металлов
Физические свойства металлов определяютсяих строением.
Твёрдость
Плотность
Плавкость
Электро- и теплопроводность
Металлический блеск
Пластичность
17. Твёрдость
Видеоопыт18. Видеоопыт
Плавление алюминия19. Плотность
Тема:Общие химические
свойства металлов
20. Плавкость
Цель:Систематизировать
сведения о
химических свойствах металлов
Осознать
химическую функцию
металлов как восстановителей
21. Плавление алюминия
Задачи:Знать отношение металлов к
неметаллам.
Взаимодействие с водой, кислотами,
солями.
Научиться применять знания.
Формирование познавательного
интереса.
Дом. зад.§ 8, выполнить письменно
упражнения с. 37 № №1,3-5
22.
У атомов металлов большие размерыатомных радиусов. Поэтому металлы
легко отдают внешние электроны.
На пример:
Na0 - 1ē → Na+1
n
0
+3
Al - 3ē → Al
M
23. Пластичность -
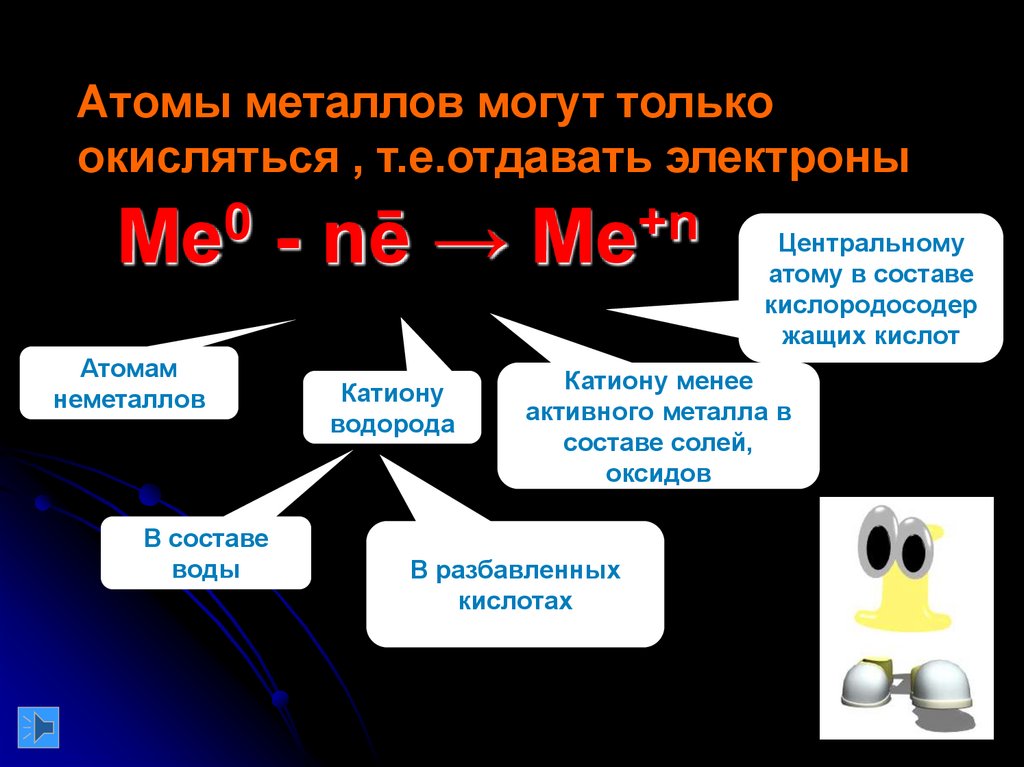
Атомы металлов могут толькоокисляться , т.е.отдавать электроны
0
Me
Атомам
неметаллов
В составе
воды
- nē →
Катиону
водорода
+n
Me
Центральному
атому в составе
кислородосодер
жащих кислот
Катиону менее
активного металла в
составе солей,
оксидов
В разбавленных
кислотах
24. Тема:
Все металлы на основании их восстановительнойспособности по отношению к ионам металлов
в водных растворах расположены в
электрохимический ряд напряжений
металлов:
Li K Ca Na Mg Al Zn Cr Fe Ni Pb H2 Cu Hg Ag
Увеличение
восстановительных свойств
25. Цель:
1.Взаимодействиеметаллов с водой
Li K Ca Na Mg Al || Zn Cr Fe Ni Pb || (H2) Cu Hg Ag
Взаимодействуют
с водой при
обычных
условиях
Me + H2O → H2 +
основание
t0
При нагревании
Me + H2O → H2 +
оксид
Me + H2O ≠>
26. Задачи:
Видеоопыт27. У атомов металлов большие размеры атомных радиусов. Поэтому металлы легко отдают внешние электроны.
З а п о м н и!!!С водой взаимодействует
только
амальгамированный
алюминий
(лишенный оксидной
пленки)
28. Me0 - nē → Me+n
Алюминий с водой29.
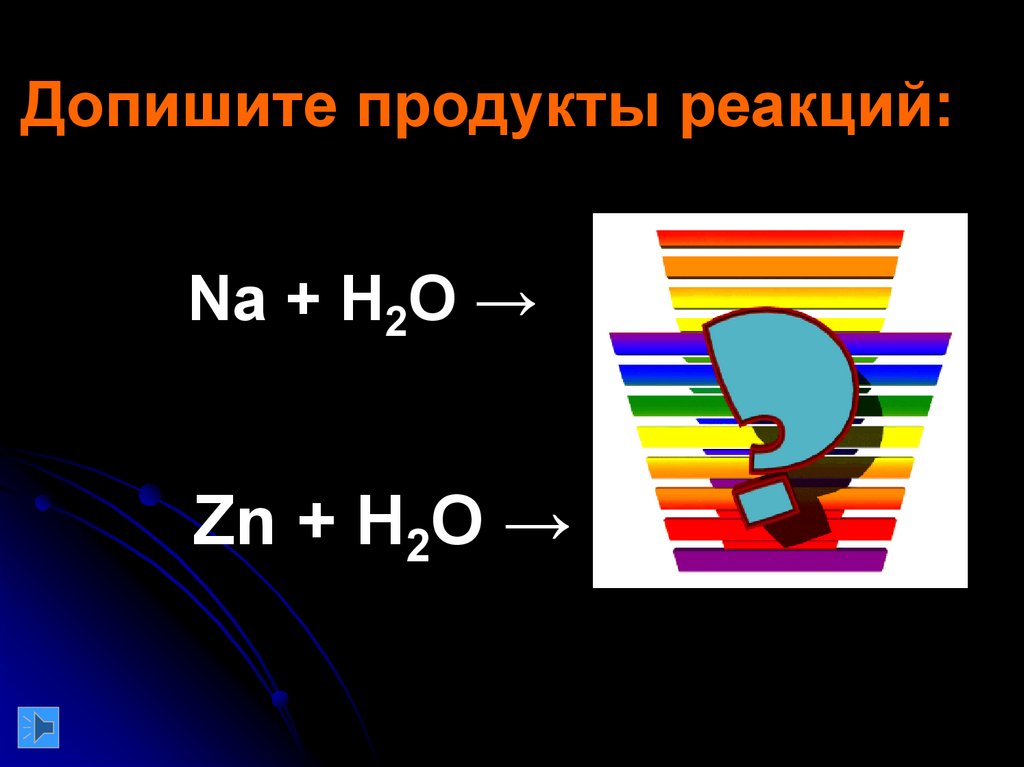
Допишите продукты реакций:Na + H2O →
Zn + H2O →
30. 1.Взаимодействие металлов с водой
Li K Ca Na Mg Al || Zn Cr Fe Ni Pb || (H2) Cu Hg AgВытесняют H2↑ из растворов
кислот (кроме HNO3)
Не вытесняют
H2↑ из
растворов
кислот
Zn + 2HCl → ZnCl2 + H2 ↑
31. Видеоопыт
2. Металлы с кислотами5 Ме с соляной ряд активности.avi
32. З а п о м н и!!!
3.Металлы с солями менееактивных металлов
33. Алюминий с водой
Металлы могут восстанавливать катионы менееактивных металлов из растворов их солей
Zn0 +Cu+2Cl2 → Cu0 + Zn+2 Cl2
34.
4. Окисление металлов неметаллами(Кислород, сера, галогены…)
35.
36. 2. Металлы с кислотами
С кислородом воздуха легковзаимодействуют щелочные и
щелочно-земельные металлы.
4 Li0 + O20 → 2 LI+120-2
37. 3.Металлы с солями менее активных металлов
Магний с кислородом38.
Железо, цинк, медь окисляютсятолько при нагревании
3Fe + 2O2 → Fe3O4
to
39.
Внимание !A u + O2 ≠>
Pt
+
O2 ≠>
40.
Металлы с неметалламиобразуют бинарные
соединения
Бромиды – AlBr3
Сульфиды – PbS
Фосфиды – Na3 Р
41.
Алюминий с бромом42. Магний с кислородом
5.Окрашивание пламени ионами металлов:А) калия
43.
Б) натрия44. A u + O2 ≠> P t + O2 ≠>
В) лития45. Металлы с неметаллами образуют бинарные соединения
В) меди46. Алюминий с бромом
А теперь ты должен закрепитьприобретенные знания, выполнив
упражнение
УДАЧИ ТЕБЕ!!!
47. 5.Окрашивание пламени ионами металлов: А) калия
Допишите практически осуществимыереакции:
1.
2.
3.
4.
Ca + HOH →
Al + HCl →
Hg + HCl →
Fe + CuSO4→
5. Au +
6. Zn +
7. Fe +
8. Li +
O2 →
O2 →
S →
N2 →
48. Б) натрия
Проверь себя!!!2ē
Ca + 2HOH →Ca(OH)2 + H2
6ē
2Al + 6HCl →2AlCl3 + H2
2ē
Fe + CuSO4 → FeSO4 +Cu
Ag + CuCl2 → не происходит
Au + O2 → не происходит
4ē
2Zn + O2 → 2ZnO
2ē
Fe + S → FeS
6ē
6Li + N2 → 2Li3N
49. В) лития
Дома обязательнопоработай с учебником!
§8
Выполнить письменно упражнения:с. 37
№ №1,3-5










































 Химия
Химия








