Похожие презентации:
Антиоксиданты. Два вида порчи жира гидролитическая и окислительная
1.
АНТИОКСИДАНТЫ2.
Различают два вида порчи жира гидролитическая и окислительная1. Гидролитическая порча - распад
жира под действием тканевых и
микробиальных липаз до глицерина
и жирных кислот. Скорость и глубина
гидролиза зависят от температуры,
влажности продукта и воздуха ,
присутствия ионов металлов,
являющихся активаторами липазы (
Fe, Cu,Sn, Pb) .
3.
Поэтому быстрая гидролитическаяпорча будет идти при оптимальных
условиях действия липазы: 37 0С,
высокая влажность воздуха или
продукта, наличие окислов
металлов, состояния жира (скорость
возрастает в эмульгированном жире)
4.
Продукты гидролиза - глицерин ивысшие жирные кислоты не
изменяют вкуса и запаха
Этот вид порчи трудно выявить
органолептически
Можно заметить порчу в жирах,
содержащих низкомолекулярные ЖК:
капроновую, масляную (молочный
жир, кокосовое, пальмовое масло
которые летучи и имеют неприятный
запах и вкус
5.
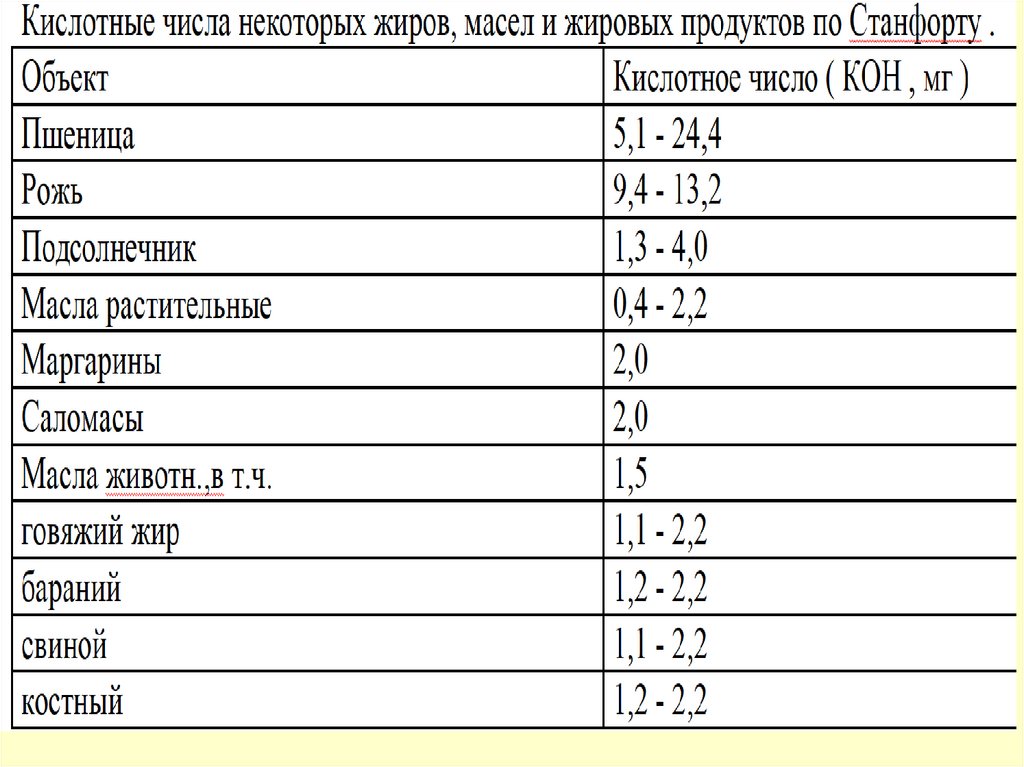
О гидролитической порче судят покислотному числу - К.Ч. количество мг едкого кали , идущего
на нейтрализацию свободных
жирных кислот , содержащихся в 1 г
жира
6.
7.
8.
9.
10.
11.
12.
2. Окислительная порча - болееглубокие изменения жиров,
протекающие при низких
температурах, но в присутствии
кислорода
Это так называемое
неферментативное окисление,
протекающее по цепному механизму
Семенова Н.Н.
13.
1. Молекула жира, поглощая квант света,возбуждается :
RH + h RH*
жир
возбужденная молекула жира
Возбужденная молекула жира непрочна и
распадается на радикалы - частицы,
имеющие свободную валентность:
RH* R + H
Эти радикалы очень активны в химическом
отношении, и взаимодействуя с кислородом,
дают перекисные радикалы
R + О2 R-O-O
H + О2 H-O-O
14.
Возникший перекисный радикалреагирует с новыми молекулами
окисленного вещества, давая гидроокись
и новый свободный радикал:
R-O-O + R1-H R-O- O-H + R1
Радикал H-O-O малоактивен , но с
увеличением концентрации возможно их
столкновение и рекомбинация ; в
результате - распад сложной перекиси .
H-O-O + O-O-H H-O-O - O-O-H О2 + H-O-O-H
сложный пероксид
перекись
водорода
15.
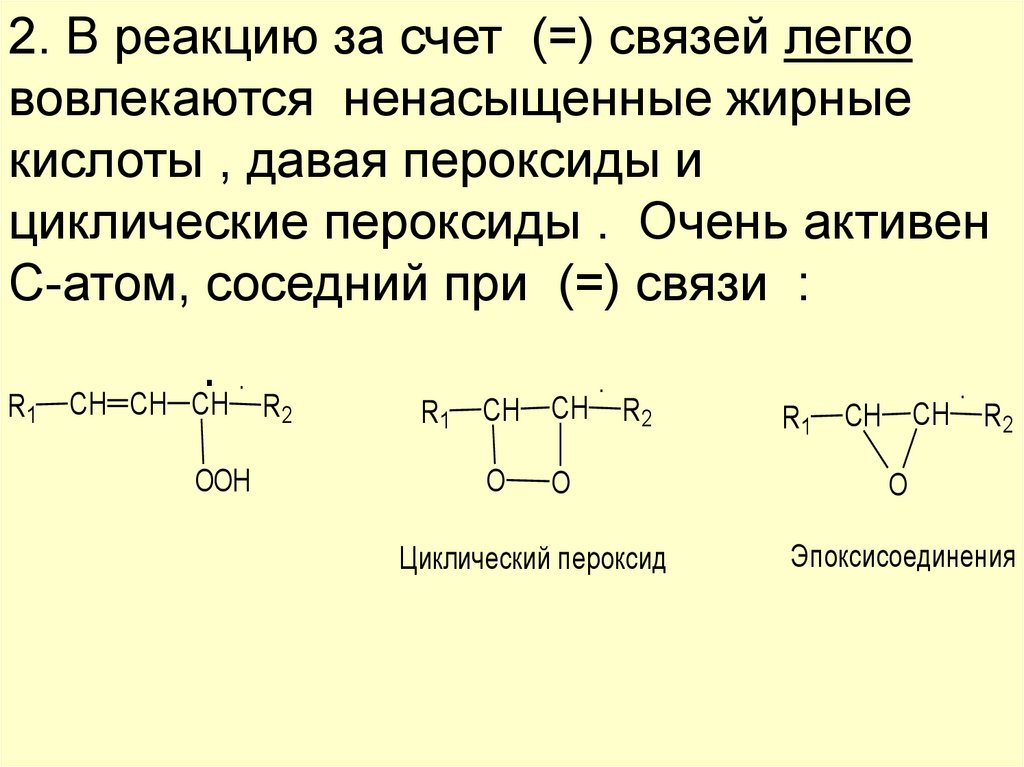
2. В реакцию за счет (=) связей легкововлекаются ненасыщенные жирные
кислоты , давая пероксиды и
циклические пероксиды . Очень активен
С-атом, соседний при (=) связи :
.
.
R CH CH CH R
1
OOH
2
R1
CH CH
O
.
R2
O
Циклический пероксид
R1
CH CH
.
R2
O
Эпоксисоединения
16.
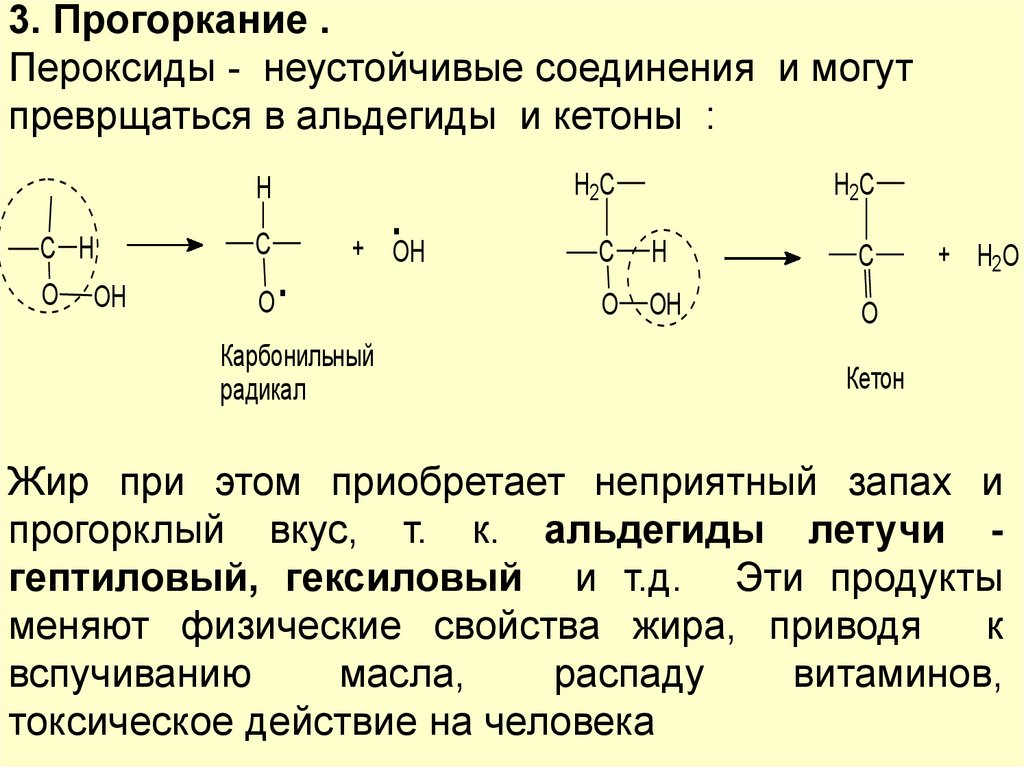
3. Прогоркание .Пероксиды - неустойчивые соединения и могут
преврщаться в альдегиды и кетоны :
H
C H
C
O
O
OH
.
.
+ OH
Карбонильный
радикал
H2C
H2C
C
H
C
O
OH
O
+ H2O
Кетон
Жир при этом приобретает неприятный запах и
прогорклый вкус, т. к. альдегиды летучи гептиловый, гексиловый и т.д. Эти продукты
меняют физические свойства жира, приводя
к
вспучиванию
масла,
распаду
витаминов,
токсическое действие на человека
17.
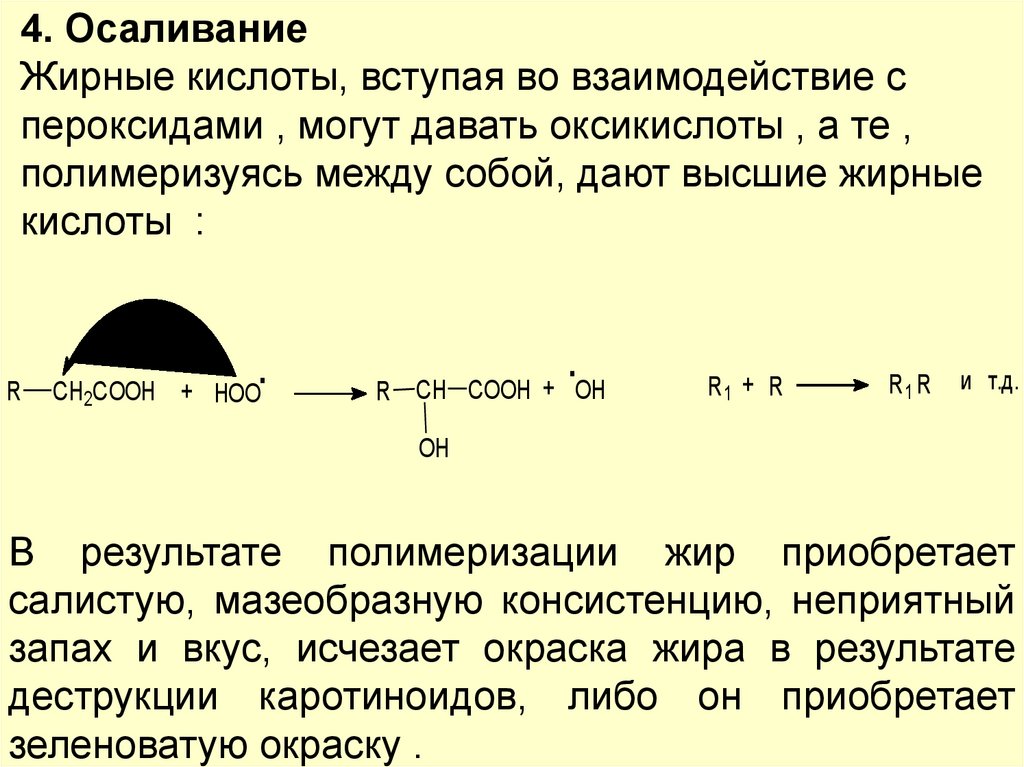
4. ОсаливаниеЖирные кислоты, вступая во взаимодействие с
пероксидами , могут давать оксикислоты , а те ,
полимеризуясь между собой, дают высшие жирные
кислоты :
.
R CH COOH + HOO
2
.
R CH COOH + OH
R1 + R
R1 R
и т.д.
OH
В результате полимеризации жир приобретает
салистую, мазеобразную консистенцию, неприятный
запах и вкус, исчезает окраска жира в результате
деструкции каротиноидов, либо он приобретает
зеленоватую окраску .
18.
Методы определения окислительной порчижира
1. По перекисному числу [ п.ч. ] - основан на
окислении иода кислородом пероксида
[ П.ч.] - это число граммов иода, выделяемого
в кислой среде из иодистого калия при
действии перекисей, содержащихся в 100 г
жира
[ П.ч.] выражают в % J2 или мл раствора
тиосульфата, иногда - в милимолях или
милиэквивалентах активного кислорода
пероксида .
19.
Свежий жир - [ п.ч. ]=0,03 ;испорченный - 0,1 и более
В свежем жире пероксидов
практически нет (не более 0,03 % J2
), т.к. там действуют естественные
антиокислители - витамины А и Е ,
каротиноиды, лецитин, которые в
начале хранения сами
взаимодействуют с О2
20.
R + h RR + A(антиоксидант ) R + А
R передает энергию антиокислителю
и выходит из цепной реакции ) .
А + О2 АО2
Активированный А в результате
взаимодействия с О2 теряет энергию
, переходя в неактивный окисленный
продукт
21.
При наличии в смеси 2-х типовантиоксидантов возникает
синергизм
Период, в течение которого не
происходит взаимодействия жира с
кислородом , называют
индукционным
Продолжительность его зависит от
концентрации антиоксидантов
22.
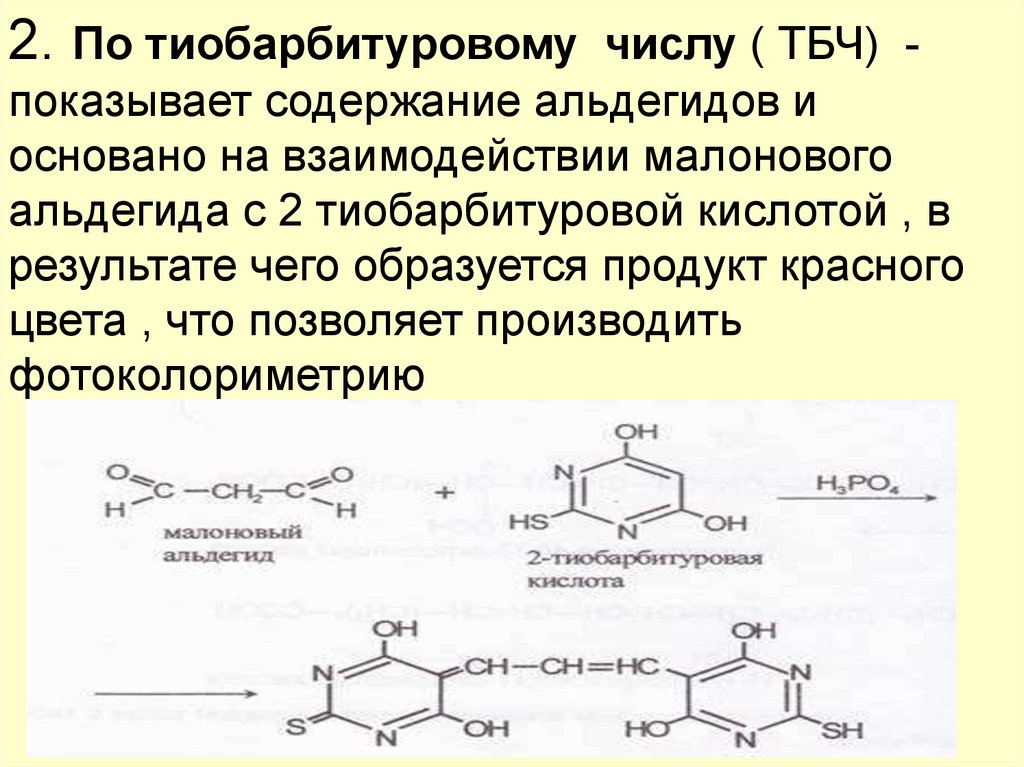
2. По тиобарбитуровому числу ( ТБЧ) показывает содержание альдегидов иосновано на взаимодействии малонового
альдегида с 2 тиобарбитуровой кислотой , в
результате чего образуется продукт красного
цвета , что позволяет производить
фотоколориметрию
23.
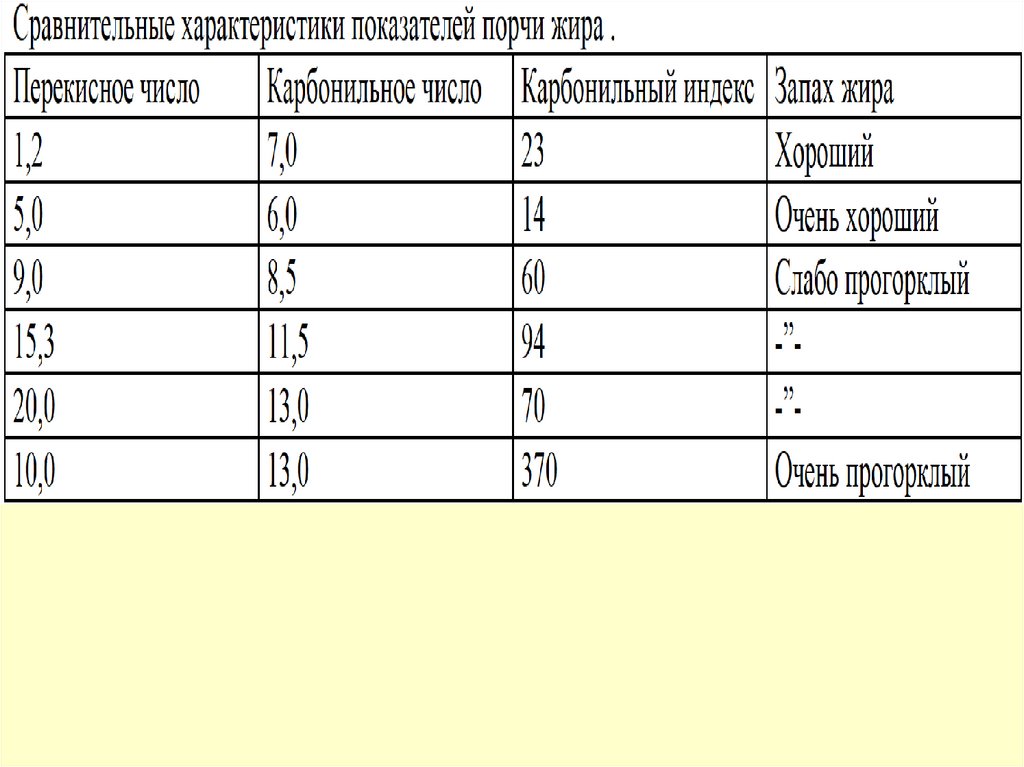
3. По карбонильному числу и индексуОба определения основаны на
интенсивности поглощения света
продуктами взаимодействия между
карбонильными соединениями и 2,4
динитрофенилгидразином
Карбонильное число - обозначает общее
содержание карбонильных соединений в
мкм на 1 кг жира , а индекс - содержание
летучих карбонильных соединений в
0,0001 ммоль карбонила на 1 кг жира .
24.
25.
26.
Предохранение жиров от порчи .1. Гидролитическую порчу жиров
предупреждают : вытапливанием
жиров ; очисткой (рафинированием )
от примесей ; выделением и
хранением жиров на холоду ;
снижением влажности продукта
(специальная упаковка) ; хранение
при низких температурах
эти способы - на инактивацию липаз
27.
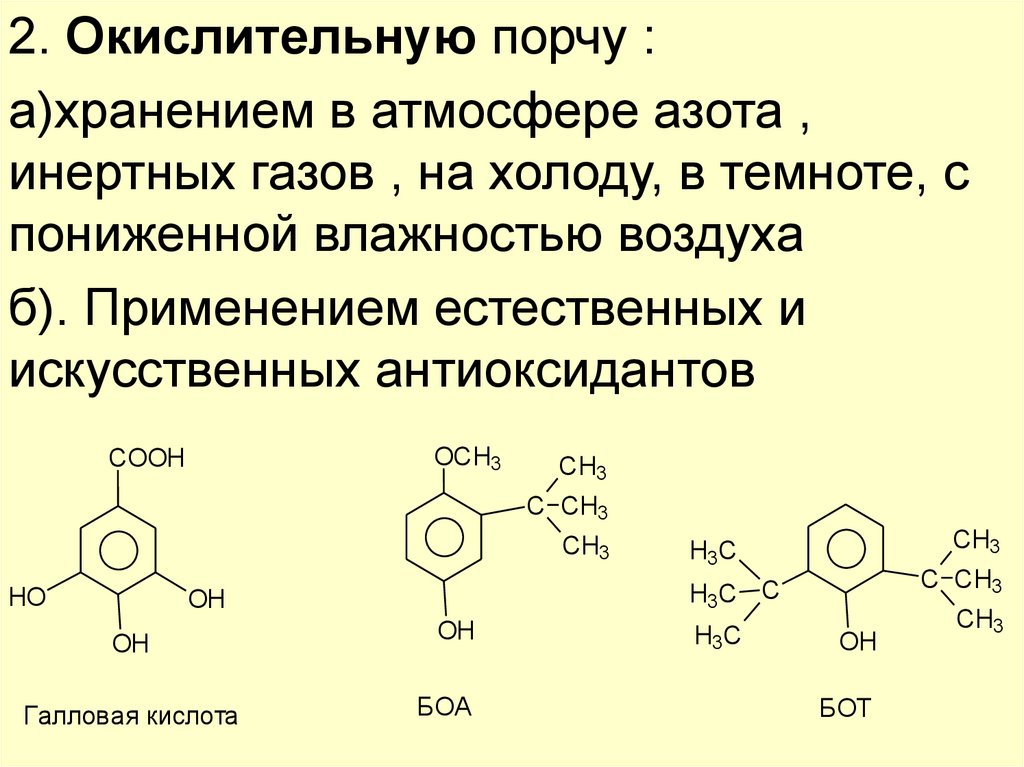
2. Окислительную порчу :а)хранением в атмосфере азота ,
инертных газов , на холоду, в темноте, с
пониженной влажностью воздуха
б). Применением естественных и
искусственных антиоксидантов
OCH3
COOH
CH3
C CH3
CH3
HO
CH3
C CH3
H3C
H3C C
OH
OH
OH
Галловая кислота
БОА
H3C
OH
БОТ
CH3
28.
Естественные : Витамины А, Е ;каротиноиды, лецитин, флавоноиды,
кофейная кислота , аскорбиновая
кислота, лимонная , малоновая ,
фумаровая, щавелевая,фосфорная
Искусственные : производные
галловой кислоты, бутилгидрооксианизол
(БОА), бутилгидроокситолуол (БОТ)
нордигидрогваяретовая кислота ( НДГК),
ионол (2,6 -дибутил -4 метилфенол)
29.
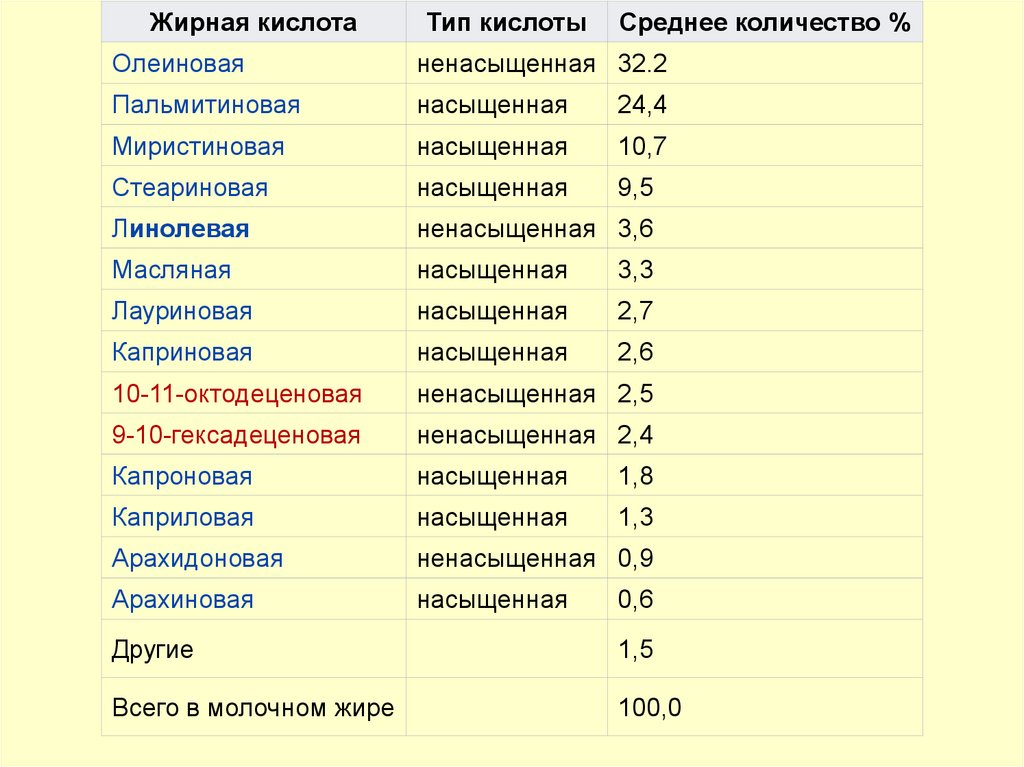
Жирная кислотаТип кислоты
Среднее количество %
Олеиновая
ненасыщенная 32.2
Пальмитиновая
насыщенная
24,4
Миристиновая
насыщенная
10,7
Стеариновая
насыщенная
9,5
Линолевая
ненасыщенная 3,6
Масляная
насыщенная
3,3
Лауриновая
насыщенная
2,7
Каприновая
насыщенная
2,6
10-11-октодеценовая
ненасыщенная 2,5
9-10-гексадеценовая
ненасыщенная 2,4
Капроновая
насыщенная
1,8
Каприловая
насыщенная
1,3
Арахидоновая
ненасыщенная 0,9
Арахиновая
насыщенная
0,6
Другие
1,5
Всего в молочном жире
100,0
30.
При хранении - гидролизтриглицеридов и содержание
свободных жирных кислот
увеличивается
Масляная кислота дает запах
“прогорклости “ молочных продуктов
Содержание жирных кислот в
нормальном стандартном молоке —
составляет менее 1 м-экв/100г жира
При более 2 м-экв /100 г жира в
молоке появляется прогорклый вкус
31.
При нагревании наблюдается частичныйпереход фосфолипидов в плазму
При созревании сыров ( не 15 0С )
происходит под действием
липолитических ферментов молочных
бактерий активный гидролиз
триглицеридов
Содержание жирных кислот + О2 +
микроэлементы сыра альдегиды +
кетоны , участвующие в образовании
аромата и вкуса сыра . У сыров в
основном насыщенные жирные кислоты
32.
Полиненасыщенные жирные кислотылегко окисляются с образованием
насыщенных и мононенасыщенных
жирных кислот. Масляная и
валериановая кислоты вызывают
неприятный запах
Гидроперекиси взаимодействуют с
белками, вызывая их денатурацию
33.
АНТИОКСИДАНТЫ34.
Антиоксиданты (АО) – вещества,которые обладают способностью
вступать во взаимодействие с
различными реактогенными
окислителями, активными формами
кислорода (АФК), другими свободными радикалами и приводить их к
частичной или полной инактивации.
35.
Свободнорадикальное окисление –процесс превращений кислорода,
липидов, нуклеиновых кислот, белков и
других соединений под действием
свободных радикалов, а перекисное
окисление липидов (ПОЛ) – одно из его
последствий
Свободные радикалами (СР)
представляют собой соединения,
имеющие неспаренный электрон на
наружной орбите и обладающие высокой
реакционной способностью.
36.
первичные СР - супероксидный анионрадикал, окись азота, а вторичные СРявляются гидроксильный радикал,
синклетный кислород, перекись
водорода, пероксинитрит
Образование СР тесно связано, с одной
стороны, с появлением свободных
электронов при нарушениях процессов
окисления в дыхательной цепи,
превращении ксантина, синтезе
лейкотриенов и простогландинов.
37.
Эти реакции зависят от активностиксантиноксидазы, альдегидоксидазы
дегидроротатдегидрогеназы,
холестериноксидазы, цитохрома Р-450.
Перекиси - нестойкие и быстро разрушаются.
В липиде появляются "ОН"-группы или
кетогруппы
В тканях человека и животных - два
фермента перекисного окисления:
ЦИКЛООКСИГЕНАЗА и ЛИПООКСИГЕНАЗА.
При окислении с участием циклооксигеназы
одновременно с окислением происходит
циклизация, при действии липооксигеназы
окисление идет без циклизации
38.
39.
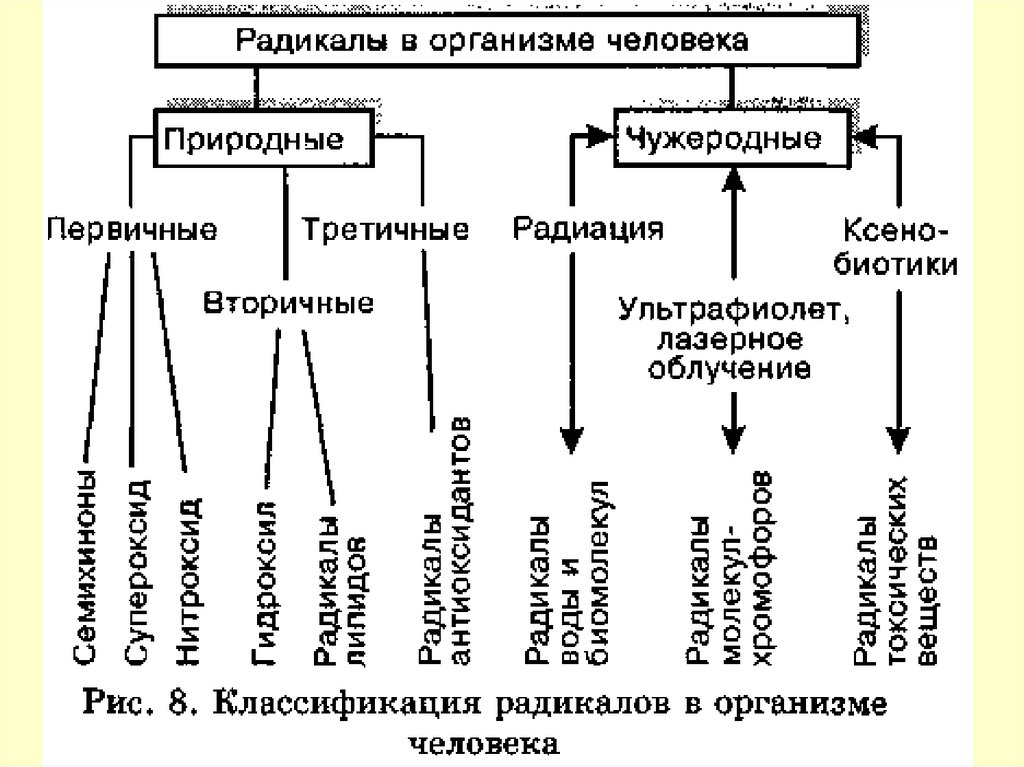
Первичные радикалы - радикалы,образование которых осуществляется
при участии определенных ферментных
систем
Прежде всего - радикалы (семихиноны),
образующиеся в реакциях таких
переносчиков электронов, как коэнзим Q
(обозначим радикал как Q) и
флавопротеины. Два других радикала супероксид (00 ) и монооксид азота (N0)
также выполняют полезные для
организма функции
40.
Из первичного радикала - супероксида, идругих реакций в организме образуются
активные молекулярные соединения:
перекись водорода, гипохлорит и
гидроперекиси липидов
Под действием ионов металлов
переменной валентности (Fe 2+) из этих
веществ образуются вторичные
радикалы (радикал гидроксила и
радикалы липидов), которые оказывают
разрушительное действие на клеточные
структуры
41.
Для защиты от повреждающего действиявторичных радикалов в организме - большая
группа веществ, называемых
антиоксидантами, к числу которых
принадлежат ловушки, или перехватчики
свободных радикалов
Примером последних служат альфатокоферол, тироксин, восстановленный
убихинон (QH2) , женские стероидные гормоны
Реагируя с липидными радикалами, эти
вещества сами превращаются в радикалы
антиоксидантов, которые можно
рассматривать как третичные радикалы
42.
Наряду с радикалами, постояннообразующимися в клетках, есть
радикалы после ионизирующего
излучения, УФО, интенсивный видимый
свет ( лазер), также радикалы, из
попавших в организм ксенобиотиков,
многие из которых оказывают
токсическое действие именно благодаря
свободным радикалам, образующимся
при метаболизме этих соединений
Такие радикалы - чужеродные
43.
Радикалы кислородаКлетки-фагоциты (гранулоциты и
моноциты крови и макрофаги),
соприкасаясь с поверхностью клеток,
бактерий, энергично выделют
супероксид: радикалы, образующиеся в
результате переноса электрона от
НАДФН-оксидазного ферментного
комплекса, встроенного в мембрану
клеток и внутриклеточных везикулфагосом, на растворенный
молекулярный кислород
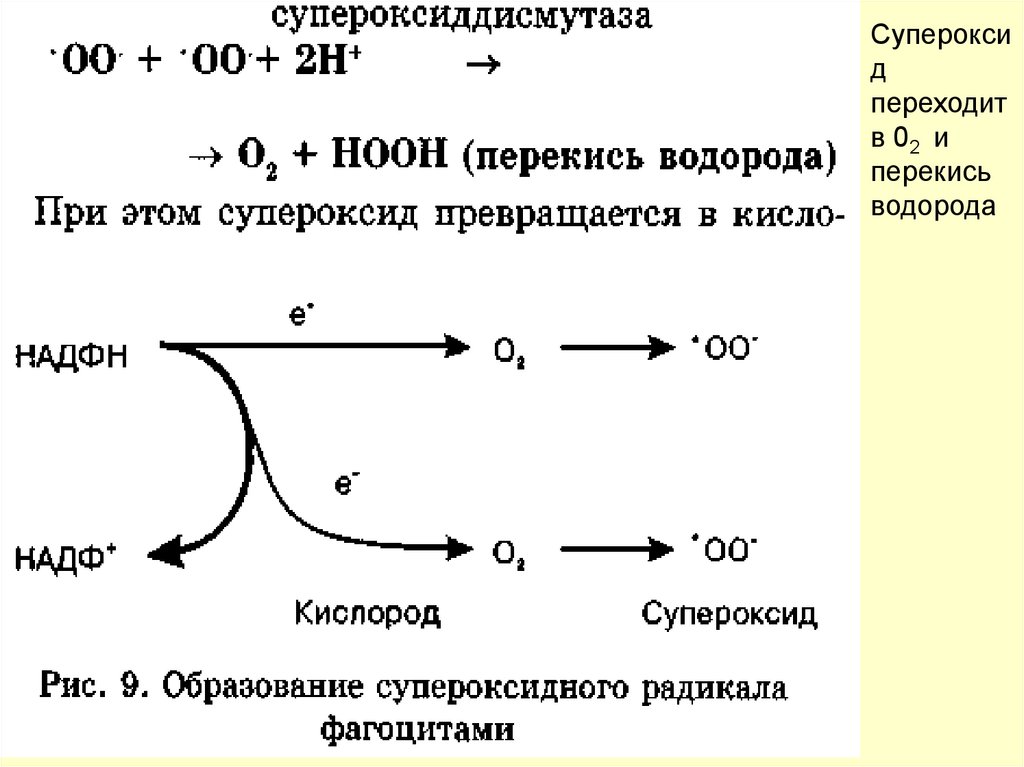
44.
При этом каждая молекула НАДФН,окисляясь, отдает два электрона в цепь
переноса электронов, а каждый из этих
электронов присоединяется к молекуле
кислорода, в результате чего образуется
супероксид анион-радикал
45.
Супероксидные радикалы могут нанестивред самим фагоцитам, другим клеткам
крови и микробам
Эти клетки стараются избавиться от
супероксид-радикалов, для чего они
вырабатывают ферменты, называемые
супероксиддисмутазами
Различаясь по строению активного
центра и структуре полипептидной цепи,
СОД катализируют одну и ту же реакцию
дисмутации супероксидного радикала:
46.
Супероксид
переходит
в 02 и
перекись
водорода
47.
• В норме фагоциты используют перекисьводорода для синтеза гипохлорита,
выделяя миелопероксидазу (МП).
Миелопероксидаза катализирует реакцию
48.
Гипохлоритразрушает стенку бактериальной клетки и тем
самым убивает бактерии. Перекись водорода
диффундирует в клетки, но там разрушается в
результате активности ферментов каталазы и
глутатионпероксидазы (GSH-пероксидазы), которые
катализируют соответственно такие реакции:
49.
В присутствии ионов двухвалентного железаперекись водорода разлагается с
образованием гидроксильного радикала (НО):
50.
Эта реакция (реакция Фентон)приводит к тяжелым последствиям
для окружающих клеток
Радикал гидроксила чрезвычайно
активен химически и разрушает
почти любую встретившуюся ему
молекулу
Действуя на SH-группы,
гистидиновые и другие АО белков,
НО' вызывает денатурацию и
инактивирует ферменты
51.
В нуклеиновых кислотах НО' разрушаетуглеводные мостики между
нуклеотидами и таким образом
разрывает цепи ДНК и РНК, в результате
чего происходят мутации и гибель клеток
Внедряясь в липидный слой клеточных
мембран, гидроксильный радикал
запускает (инициирует) реакции цепного
окисления липидов, что приводит к
повреждению мембран, нарушению их
функций и гибели клеток
52.
53.
Гидроксильный радикал образуется не тольков реакции Фентон, но и при взаимодействии
ионов железа (Fe2+) с гипохлоритом
(реакция Осипова):
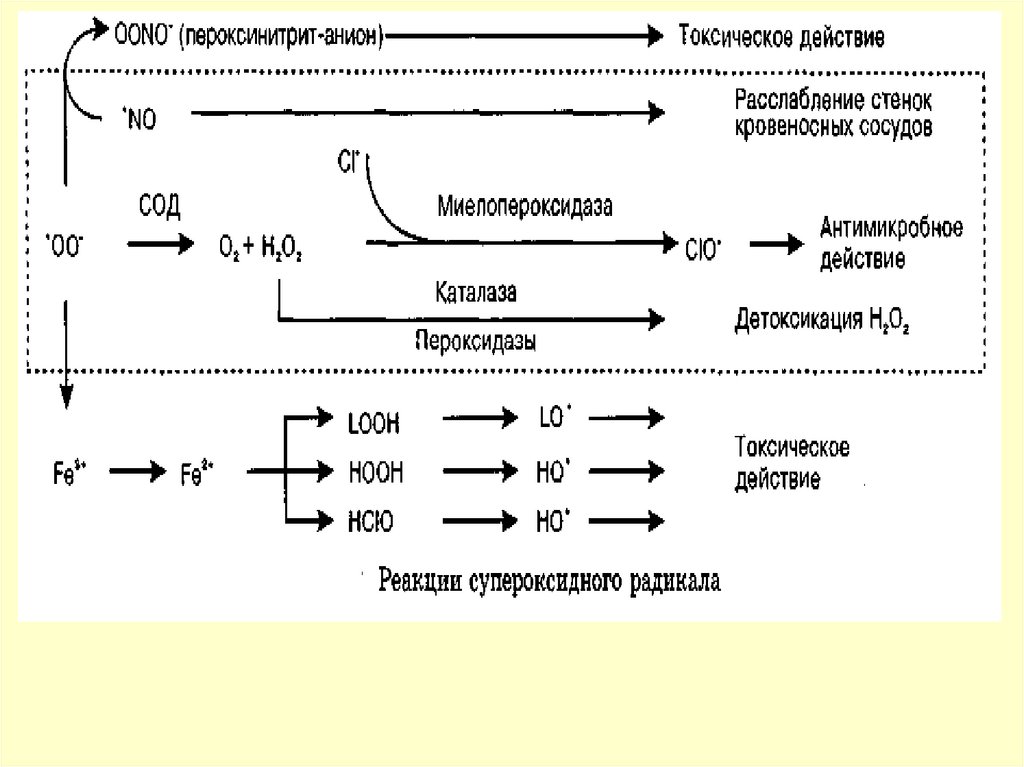
Супероксидный радикал (00 )и продукты его
метаболизма (Н202, НО‘, ClO)
называют активными формами кислорода
54.
Окись азота - радикал, синтезируемыйклетками - монооксид азота ' N0 ( нитроксид )
N0 образуется клетками эндотелия
кровеносных сосудов; эта реакция
катализируется гемсодержащим ферментом
N0-синтазой
'NO - ключевая роль в регуляции тонуса
сосудов : недостаток - к гипертензии, избыток к гипотензии
' N0 выделяется также клетками-фагоцитами и
вместе с супероксид-радикалами
используется для борьбы с микробами
(преимущественно грибковой природы)
55.
Цитотоксическое действие ' N0 обусловлено егореакцией с супероксидом
Пероксинитрит, образующийся в этой реакции, может
разлагаться с образованием 'ОН:
О = N - О - ОН -> О = N - О + ОН (радикал гидроксила)
Образование пероксинитрита и радикала гидроксила
приводит к повреждению клеток.
одна из функций супероксиддисмутазы состоит в
предотвращении образования пероксинитрита за
счет удаления супероксида из зоны образования
окиси азота
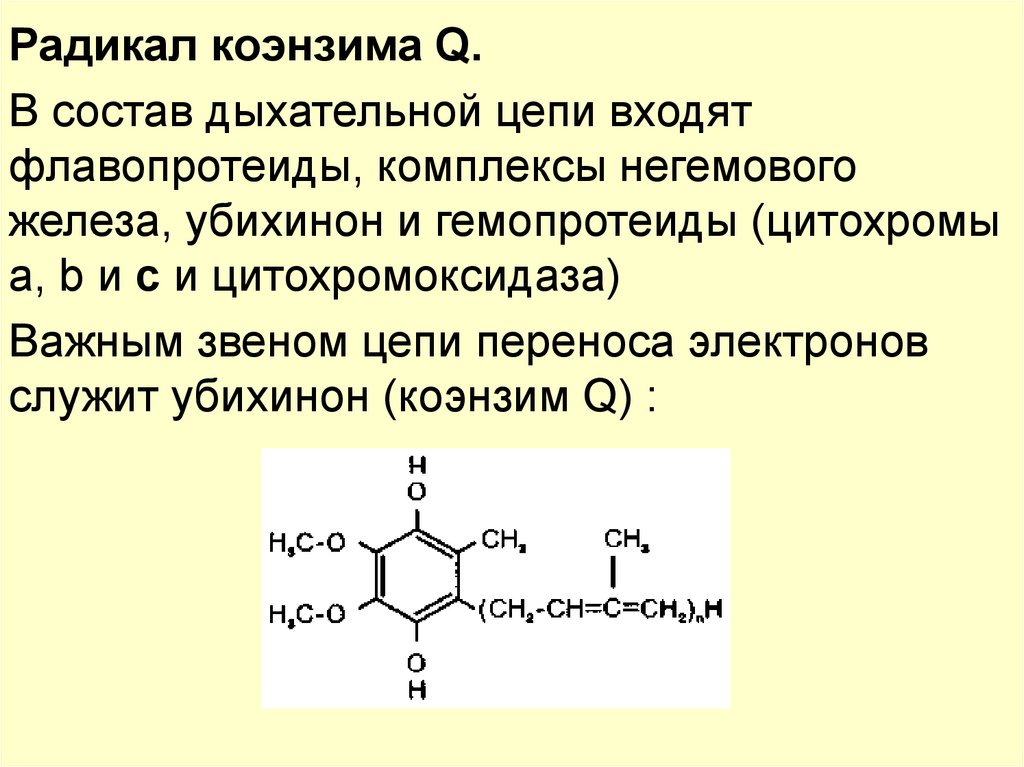
56.
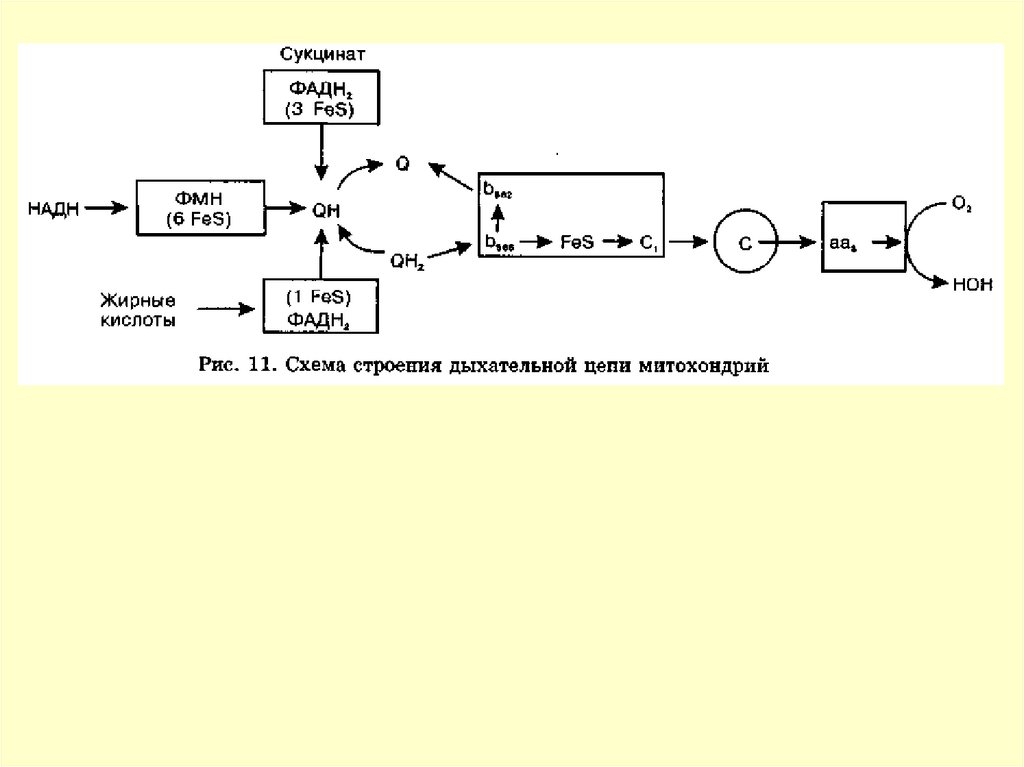
Радикал коэнзима Q.В состав дыхательной цепи входят
флавопротеиды, комплексы негемового
железа, убихинон и гемопротеиды (цитохромы
a, b и с и цитохромоксидаза)
Важным звеном цепи переноса электронов
служит убихинон (коэнзим Q) :
57.
58.
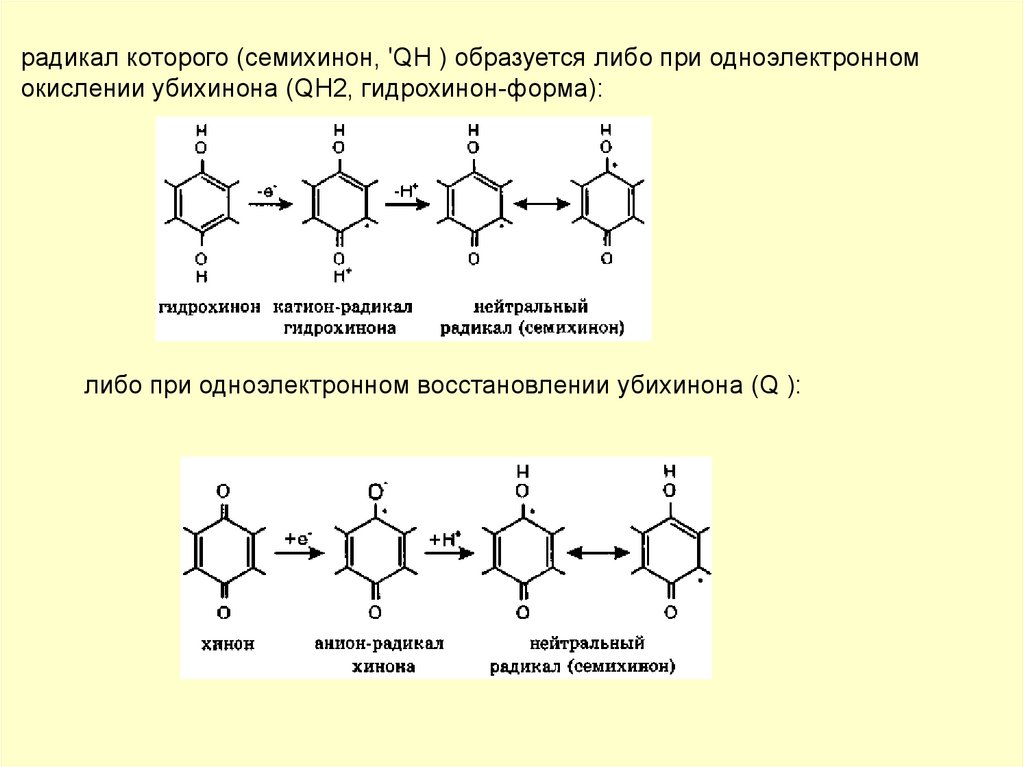
радикал которого (семихинон, 'QH ) образуется либо при одноэлектронномокислении убихинона (QH2, гидрохинон-форма):
либо при одноэлектронном восстановлении убихинона (Q ):
59.
В норме этот радикал является рядовымучастником процесса переноса электронов, но
при нарушении работы дыхательной цепи он
может стать источником других, менее
безобидных радикалов, в первую очередь
радикалов кислорода.
60.
Антиоксидантная система организмаНеферментативные антиоксиданты
Антиоксидантные ферменты
61.
Антиоксидантная система (АОС) - системазащиты биополимеров от деструкции.
Различают:
ферментативное звено АОС,
неферментативное звено АОС.
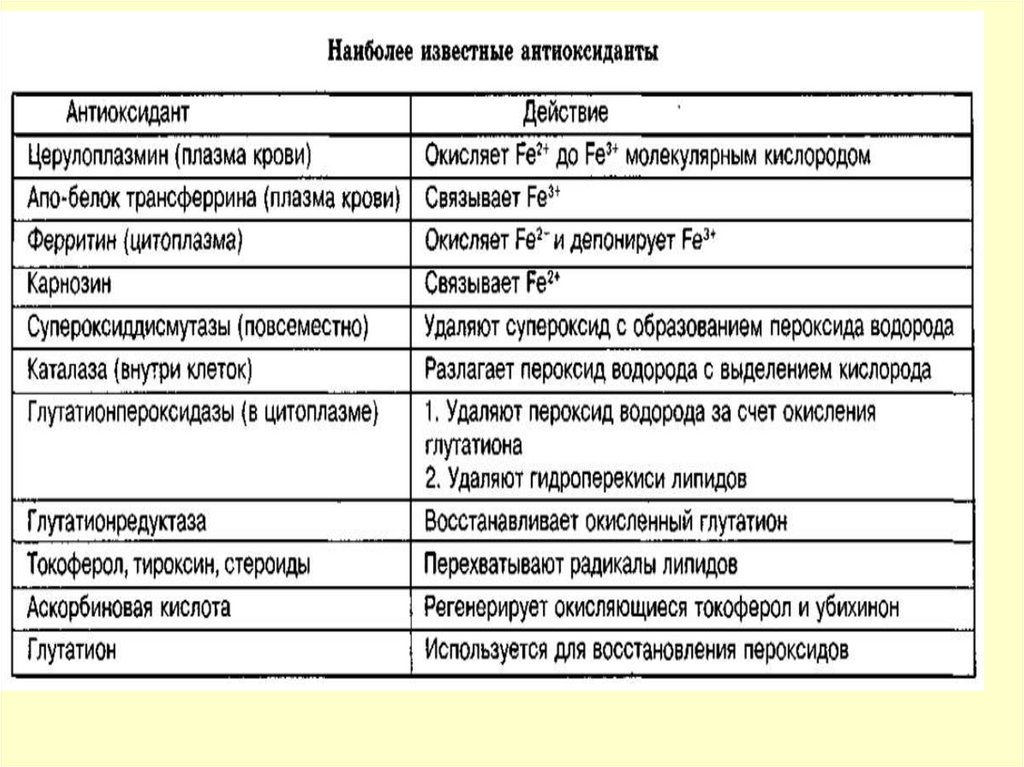
Ферменты АО:
супероксиддисмутаза,
каталаза,
пероксидаза,
глутатионпероксидаза,
глутатионредуктаза,
церулоплазмин
62.
Супероксиддисмутаза СОДО2 + О2 + 2Н+ (СОД)→ Н2О2 + О2
Ионы меди и цинка – кофакторы
СОД,
СОД осуществляет удаление
образовавшегося в клетке
супероксидрадикала,
для лечения пневмонии, инфаркта
миокарда, ожогов глаз.
63.
Супероксиддисмутаза человека:Cu, Zn – содержащие СОД
Cu – в активном центре, Zn – как кофактор,
стабилизирующий конформацию.
СОД1 (цитозольная)
СОД2 (митохондриальная) – относится к Mnсодержащей
СОД3 (внеклеточная)_
СОД (в активном цетре)
64.
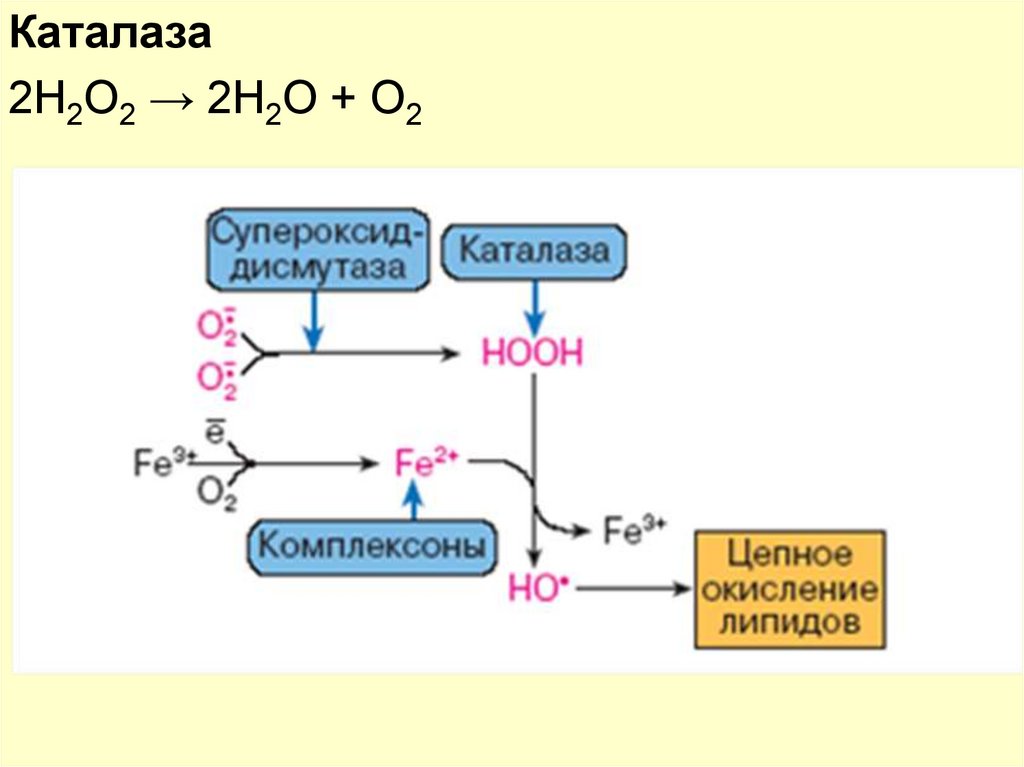
Каталаза2Н2О2 → 2Н2О + О2
65.
ПероксидазаН2О2 + АН2 (пероксидаза)→ 2Н2О + А
АН2 - донор протонов (аскорбиновая кислота,
фенолы)
Глутатионпероксидаза ГПО:
селеносодержащий фермент,
состоит из четырёх субъединиц, в активном центре
каждой содержится селен,
катализирует восстановление гидропероксида или
перекиси водорода с помощью глутатиона.
ROOH +2GSH → ROH + Н2О+ GSSG
Н2О2 +2GSH → 2Н2О+ GSSG
В отличие от каталазы более активна при малых
концентрациях перекиси водорода
66.
Церулоплазмин -основной антиоксидант плазмы крови,«перехватчик» супероксидрадикалов,
обладает ферментативными свойствами,
осуществляет окисление Fe 2+ в Fe 3+
Церулоплазмин человека, благодаря входящим в его состав
ионам меди, имеет голубой цвет. Средняя молекулярная
масса колеблется в диапазоне 150 000—160 000 г/моль. На
одну молекулу приходится 6-7 ионов меди (Cu+2)
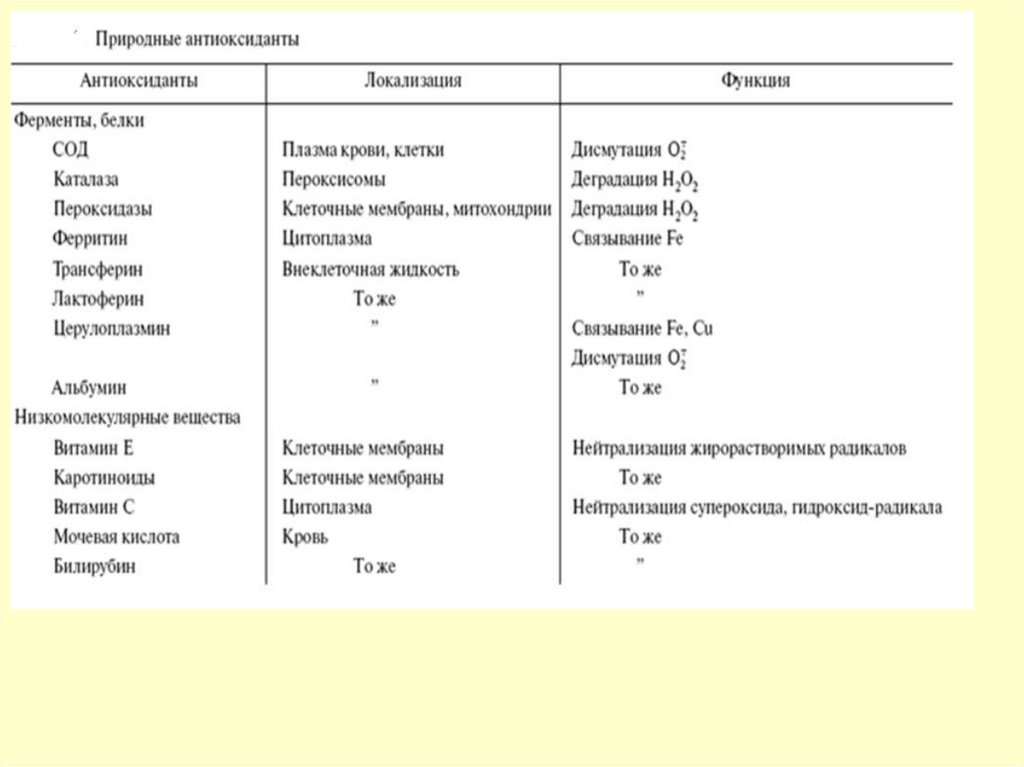
67.
Неферментативные антиоксиданты:Антирадикальные ингибиторы отдают подвижный
водород свободному радикалу.
InH +ROO· → In + ROOH
витамины: С, α-токоферол, β-каротин, К, Р,
белки: церулоплазмин, лактоферрин, трансферин,
альбумин,
минеральные вещества: Se, Zn, Co, Fe, Cu,
гормоны: эстрогены, тироксин,
биогенные амины: серотонин, гистамин,
аминокислоты: фен, тир, три, мет, цис,
пигмент меланин,
мочевая кислота,
карнозин, ансерин,
глутатион,
таурин
68.
Белковые АО плазмы крови:церулоплазмин,
(α +β – глобулины плазмы крови) неспецифические адаптогены,
Слабыми антиоксидантными свойствами
обладают:
альбумины,
трансферин,
лактоферрин
Они связывают ионы железа или меди и тем
самым предотвращают образование
свободных радикалов из перекиси водорода
69.
Антиоксиданты по локализацииделятся:
внутриклеточные: ГПО, СОД, каталаза,
не расходуются в процессе разрушения
свободных радикалов,
встроены в мембраны: α-токоферол, βкаротин, убихинон, расходуются в
процессе разрушения свободных
радикалов,
во внеклеточных жидкостях:
флавоноиды, полифенолы
70.
Идентифицируют 3 класса АО:Первичные АО: ГПО, СОД, церулоплазмин,
ферритин, трансферин,
предупреждают образование новых
свободных радикалов.
Вторичные АО: витамин Е, С, β-каротин, МК,
билирубин, альбумин,
удаляют образованные радикалы.
Третичные АО: ДНК-репарирующие
ферменты, метионинсульфоксидредуктаза,
восстанавливают клеточные структуры,
повреждённые свободными радикалами.
71.
АО могут действовать как прооксиданты:Это зависит от их редокс-потенциала и дозы
потребления.
Приём β-каротина в дозе 20 мг в день
повышает частоту возникновения рака
лёгкого у курильщиков.
72.
Синтетические АО:Синтетические аналоги витаминов:
водорастворимое производное витамина Е –
динатриевая соль токоферолфосфата.
Ароматические фенолы и полифенолы:
дибунол, порбукол.
Гетероароматические фенолы.
Азотистые гетероциклы.
Органические кислоты и их производные:
мочевая кислота,
цистеин, глутатион, фитиновая кислота
способны угнетать формирование
гидроксилрадикалов.



























































 Химия
Химия








