Похожие презентации:
Производство исходного сырья для процессов органического синтеза
1.
ПРОИЗВОДСТВОИСХОДНОГО СЫРЬЯ
ДЛЯ ПРОЦЕССОВ
ОРГАНИЧЕСКОГО
СИНТЕЗА
Преподаватель:
к.т.н., доцент кафедры ХТТ
Черниговская
Марина Алексеевна
2.
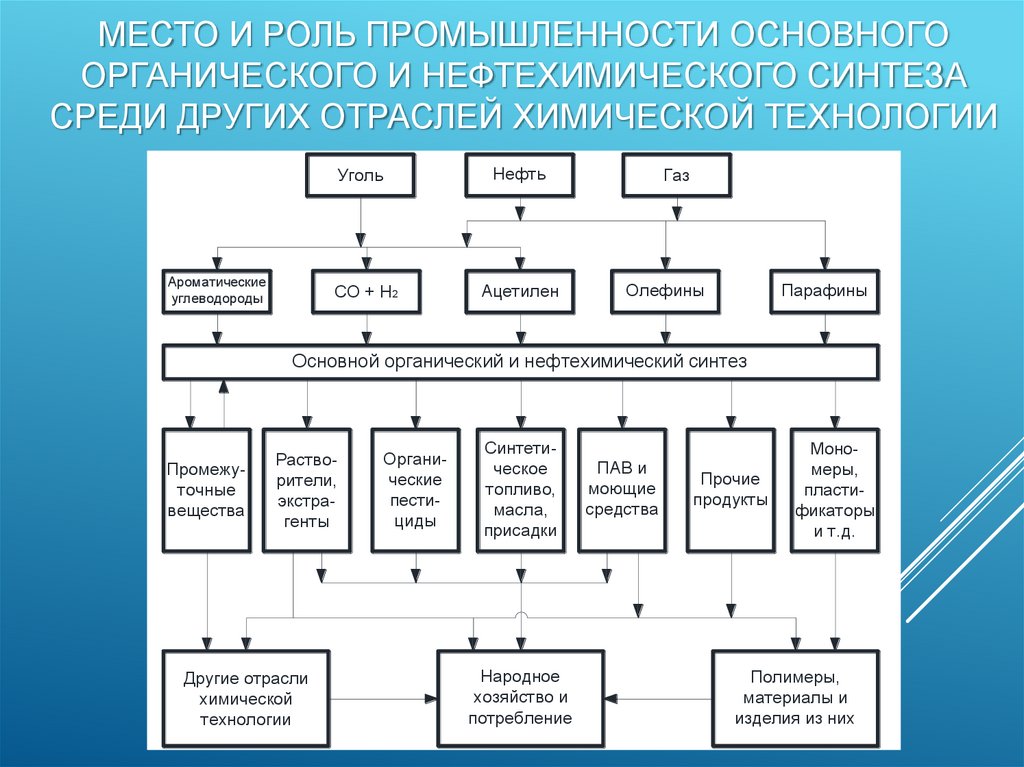
МЕСТО И РОЛЬ ПРОМЫШЛЕННОСТИ ОСНОВНОГООРГАНИЧЕСКОГО И НЕФТЕХИМИЧЕСКОГО СИНТЕЗА
СРЕДИ ДРУГИХ ОТРАСЛЕЙ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ
Ароматические
углеводороды
Уголь
Нефть
Газ
СО + Н2
Ацетилен
Олефины
Парафины
Основной органический и нефтехимический синтез
Промежуточные
вещества
Растворители,
экстрагенты
Другие отрасли
химической
технологии
Органические
пестициды
Синтетическое
топливо,
масла,
присадки
Народное
хозяйство и
потребление
ПАВ и
моющие
средства
Прочие
продукты
Мономеры,
пластификаторы
и т.д.
Полимеры,
материалы и
изделия из них
3.
ПУТИ СОЗДАНИЯ НОВЫХ И СОВЕРШЕНСТВОВАНИЯСУЩЕСТВУЮЩИХ ПРОИЗВОДСТВ
- Экономия материальных ресурсов;
- Повышение селективности процесса;
- Снижение потерь сырья и продуктов путем
утилизации побочных продуктов и
интенсификации производства;
- Экономия энергии;
- Охрана окружающей среды.
4.
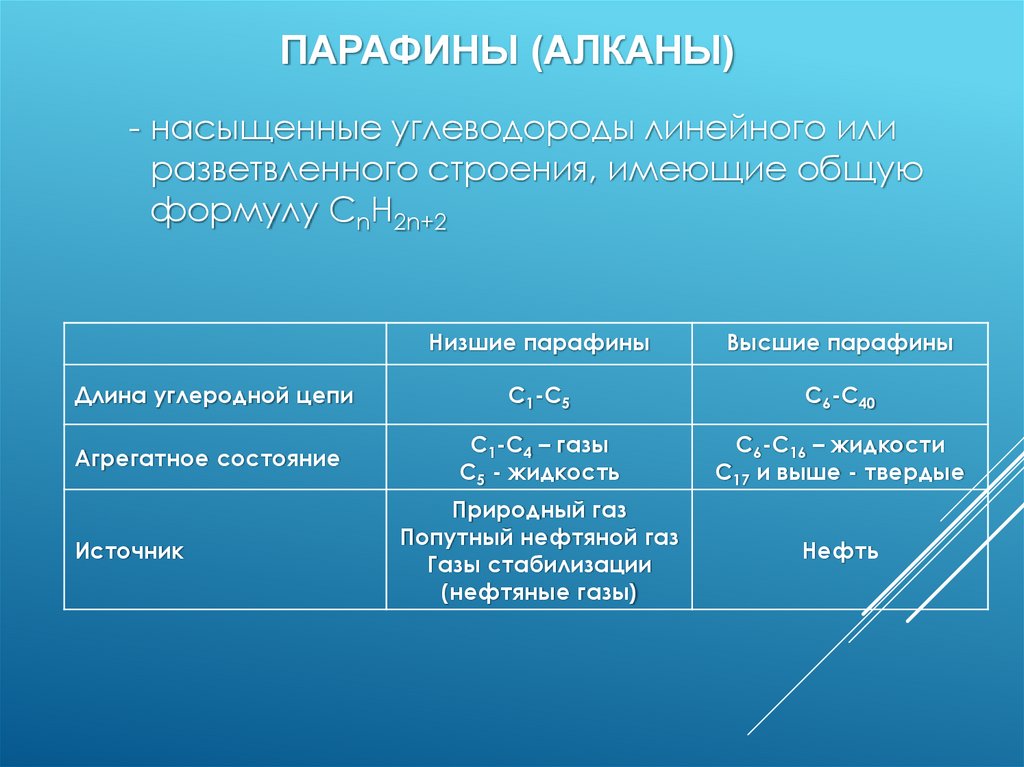
ПАРАФИНЫ (АЛКАНЫ)- насыщенные углеводороды линейного или
разветвленного строения, имеющие общую
формулу СnH2n+2
Низшие парафины
Высшие парафины
Длина углеродной цепи
С1-С5
С6-С40
Агрегатное состояние
С1-С4 – газы
С5 - жидкость
С6-С16 – жидкости
С17 и выше - твердые
Природный газ
Попутный нефтяной газ
Газы стабилизации
(нефтяные газы)
Нефть
Источник
5.
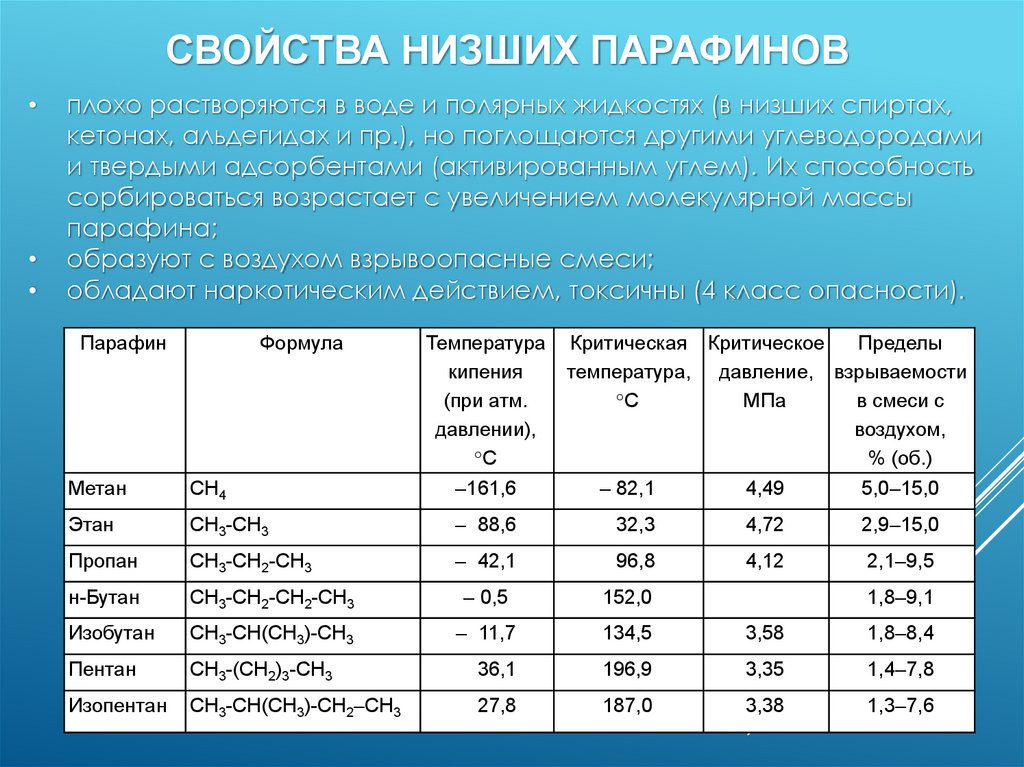
СВОЙСТВА НИЗШИХ ПАРАФИНОВплохо растворяются в воде и полярных жидкостях (в низших спиртах,
кетонах, альдегидах и пр.), но поглощаются другими углеводородами
и твердыми адсорбентами (активированным углем). Их способность
сорбироваться возрастает с увеличением молекулярной массы
парафина;
образуют с воздухом взрывоопасные смеси;
обладают наркотическим действием, токсичны (4 класс опасности).
Парафин
Формула
Температура
кипения
(при атм.
давлении),
°С
–161,6
Критическая Критическое
Пределы
температура, давление, взрываемости
°С
МПа
в смеси с
воздухом,
% (об.)
– 82,1
4,49
5,0–15,0
Метан
СН4
Этан
СН3-СН3
– 88,6
32,3
4,72
2,9–15,0
Пропан
СН3-СН2-СН3
– 42,1
96,8
4,12
2,1–9,5
н-Бутан
СН3-СН2-СН2-СН3
– 0,5
152,0
Изобутан
СН3-СН(СН3)-СН3
– 11,7
134,5
3,58
1,8–8,4
Пентан
СН3-(СН2)3-СН3
36,1
196,9
3,35
1,4–7,8
Изопентан
СН3-СН(СН3)-СН2–СН3
27,8
187,0
3,38
1,3–7,6
1,8–9,1
6.
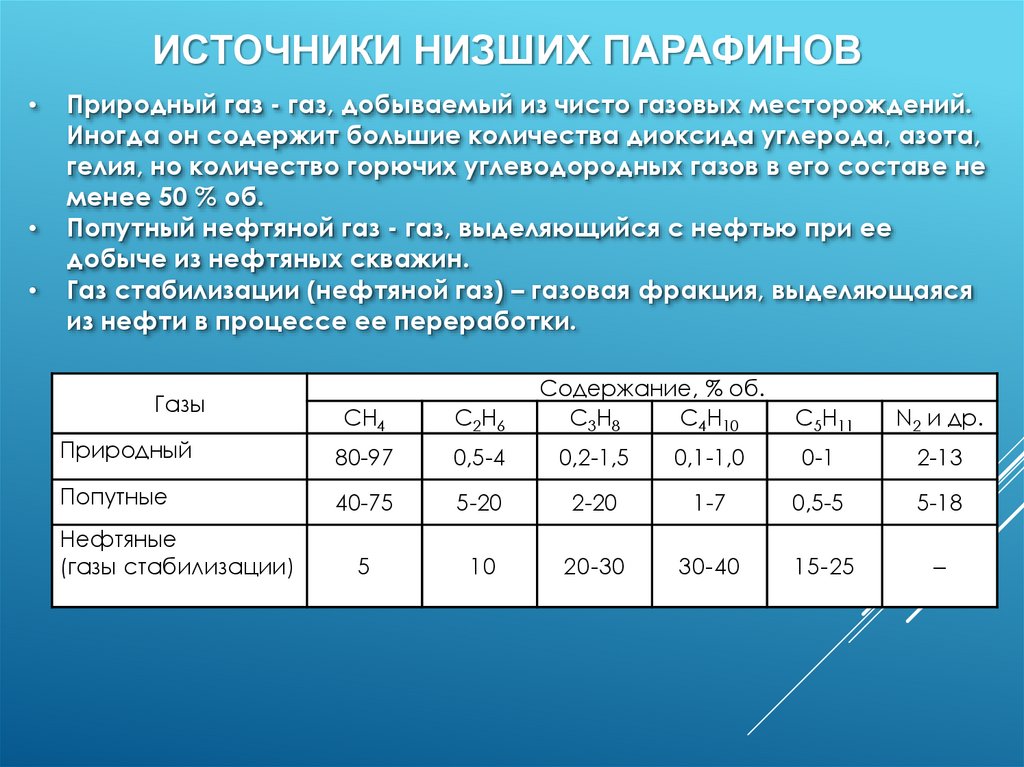
ИСТОЧНИКИ НИЗШИХ ПАРАФИНОВПриродный газ - газ, добываемый из чисто газовых месторождений.
Иногда он содержит большие количества диоксида углерода, азота,
гелия, но количество горючих углеводородных газов в его составе не
менее 50 % об.
Попутный нефтяной газ - газ, выделяющийся с нефтью при ее
добыче из нефтяных скважин.
Газ стабилизации (нефтяной газ) – газовая фракция, выделяющаяся
из нефти в процессе ее переработки.
Газы
Содержание, % об.
С3Н8
С4Н10
СН4
С2Н6
Природный
80-97
0,5-4
0,2-1,5
Попутные
40-75
5-20
5
10
Нефтяные
(газы стабилизации)
С5Н11
N2 и др.
0,1-1,0
0-1
2-13
2-20
1-7
0,5-5
5-18
20-30
30-40
15-25
–
7.
СПОСОБЫ ВЫДЕЛЕНИЯ УГЛЕВОДОРОДОВ С3-С5ИЗ ПОПУТНЫХ НЕФТЯНЫХ ГАЗОВ
Конденсационно-ректификационный (низкотемпературная
ректификация);
Адсорбционно-ректификационный (гиперсорбция
активированным углем с последующей десорбцией и
ректификацией);
Абсорбционно-ректификационный (поглощение
углеводородов С3-С5 с последующей десорбцией и
ректификацией).
8.
АБСОРБЦИОННОЕ РАЗДЕЛЕНИЕ ПОПУТНОГО ГАЗА1 – компрессор; 2, 12 – холодильники; 3 – сепаратор; 4 – абсорбционно-отпарная колонна;
5 – теплообменник; 6, 9 – десорберы; 7, 10 – конденсаторы; 8 – сборник пропан-бутановой
фракции; 11 – сборник газового бензина; 13 – дроссели; 14 - насосы.
9.
СПОСОБЫ ВЫДЕЛЕНИЯ ВЫСШИХ ПАРАФИНОВИЗ НЕФТИ И НЕФТЯНЫХ ФРАКЦИЙ
Ректификация (первичная перегонка нефти с многократным
испарением и конденсацией);
Кристаллизация с растворителем и без (отделение
парафинов в виде твердой фазы после охлаждения);
Карбамидная депарафинизация (отделение линейных
парафинов в виде кристаллических аддуктов мочевины);
Сорбция на цеолитах (выделение линейных парафинов путем
адсорбции на цеолитах).
10.
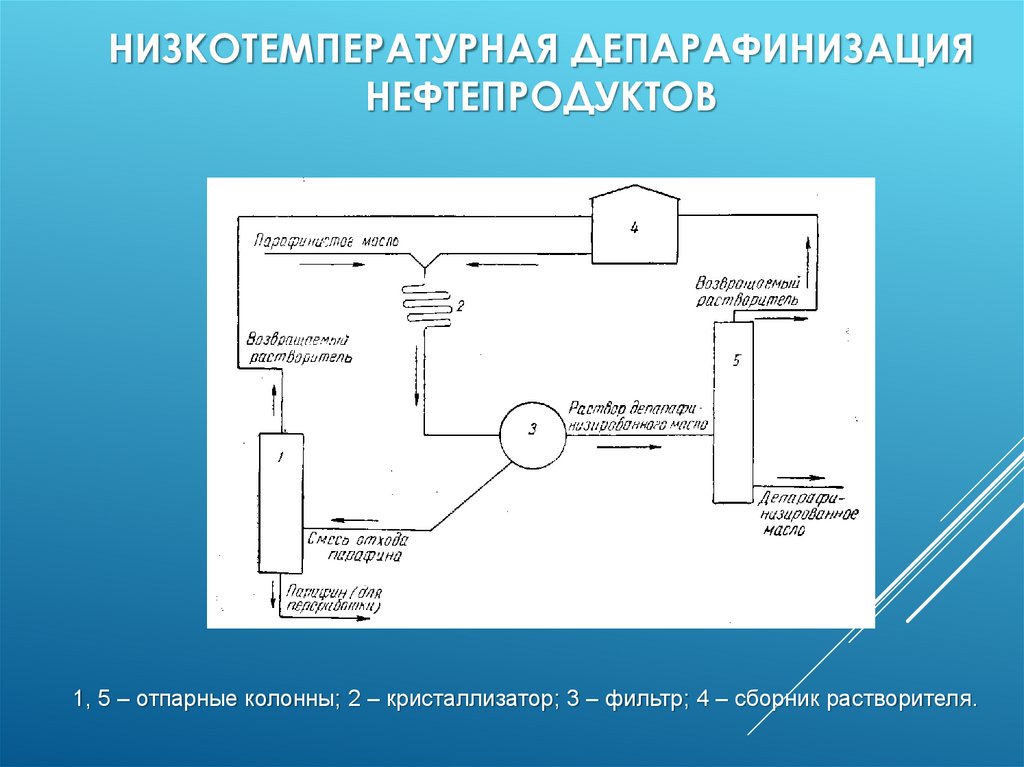
НИЗКОТЕМПЕРАТУРНАЯ ДЕПАРАФИНИЗАЦИЯНЕФТЕПРОДУКТОВ
1, 5 – отпарные колонны; 2 – кристаллизатор; 3 – фильтр; 4 – сборник растворителя.
11.
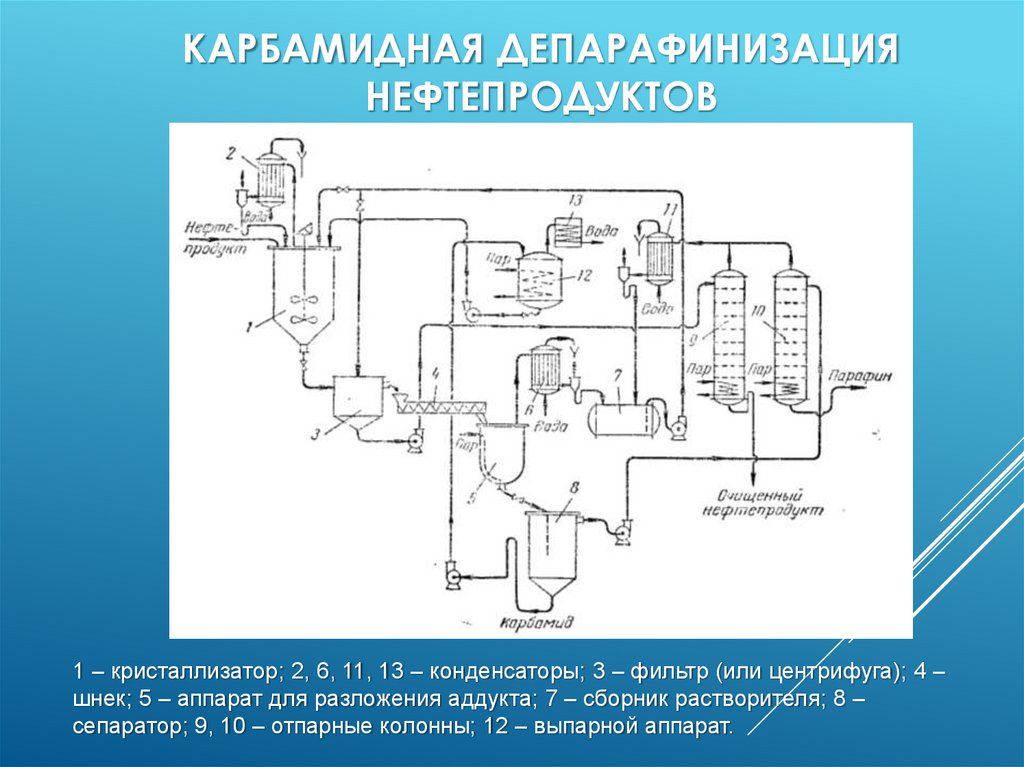
КАРБАМИДНАЯ ДЕПАРАФИНИЗАЦИЯНЕФТЕПРОДУКТОВ
1 – кристаллизатор; 2, 6, 11, 13 – конденсаторы; 3 – фильтр (или центрифуга); 4 –
шнек; 5 – аппарат для разложения аддукта; 7 – сборник растворителя; 8 –
сепаратор; 9, 10 – отпарные колонны; 12 – выпарной аппарат.
12.
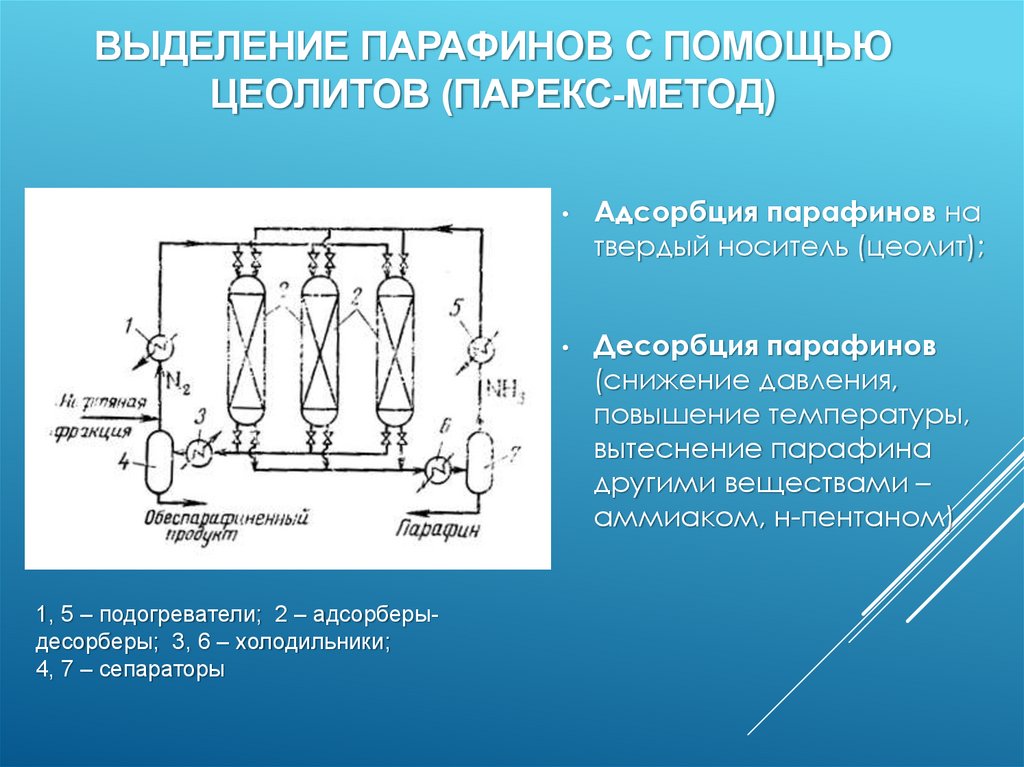
ВЫДЕЛЕНИЕ ПАРАФИНОВ С ПОМОЩЬЮЦЕОЛИТОВ (ПАРЕКС-МЕТОД)
1, 5 – подогреватели; 2 – адсорберыдесорберы; 3, 6 – холодильники;
4, 7 – сепараторы
Адсорбция парафинов на
твердый носитель (цеолит);
Десорбция парафинов
(снижение давления,
повышение температуры,
вытеснение парафина
другими веществами –
аммиаком, н-пентаном)
13.
ИЗОМЕРИЗАЦИЯ ПАРАФИНОВ-
Это процесс изменения структуры парафина без изменения
его брутто-формулы.
Катализатор процесса: хлорид алюминия или бифункциональный
контакт (металлы платиновой группы на носителе кислотного типа
(оксид алюминия, алюмосиликат, цеолит)).
14.
ОЛЕФИНЫ (АЛКЕНЫ)- ненасыщенные углеводороды линейного или
разветвленного строения, содержащие в своей
структуре одну двойную связь и имеющие общую
формулу СnH2n
Низшие олефины
Высшие олефины
Длина углеродной цепи
С2-С5
С6-С18
Агрегатное состояние
С2-С4 – газы
С5 - жидкость
С6-С18 – жидкости
15.
ПОЛУЧЕНИЕ ОЛЕФИНОВ- Термические методы – направлены на получение
олефинов (пиролиз и термический крекинг парафина);
- Каталитические методы – направлены на получение
бензинов, а олефины являются побочным продуктом
(каталитический крекинг);
- Дегидрирование парафинов;
- Реакции взаимного превращения олефинов
(олигомеризация и диспропорционирование).
16.
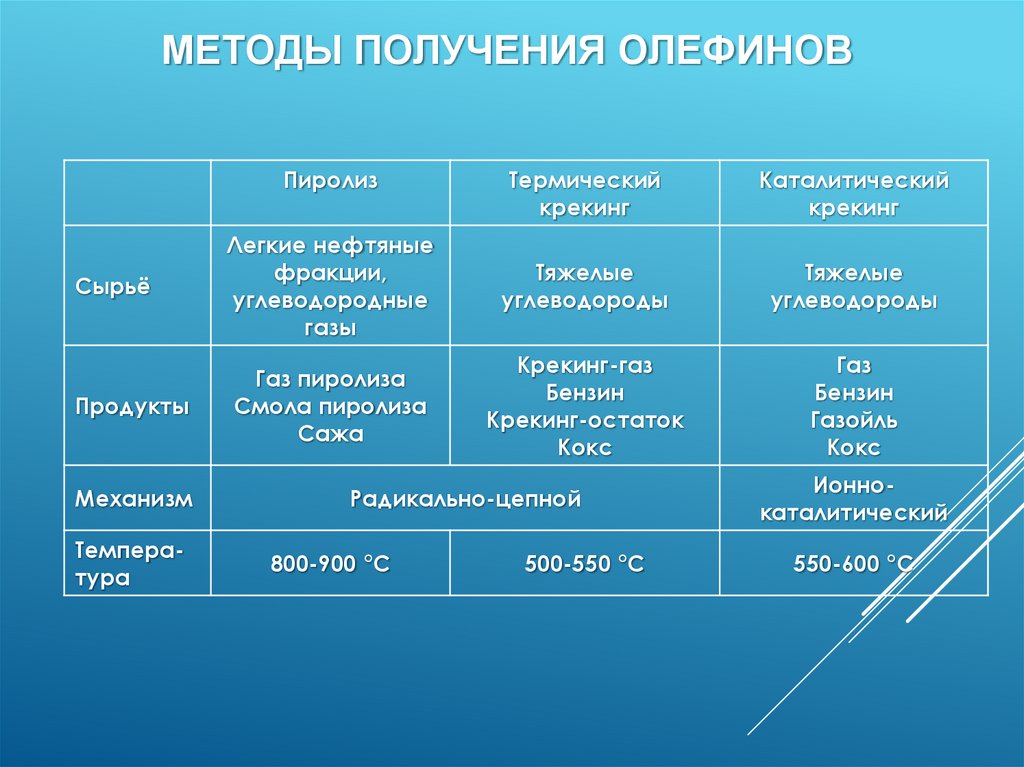
МЕТОДЫ ПОЛУЧЕНИЯ ОЛЕФИНОВПиролиз
Термический
крекинг
Каталитический
крекинг
Сырьё
Легкие нефтяные
фракции,
углеводородные
газы
Тяжелые
углеводороды
Тяжелые
углеводороды
Продукты
Газ пиролиза
Смола пиролиза
Сажа
Крекинг-газ
Бензин
Крекинг-остаток
Кокс
Газ
Бензин
Газойль
Кокс
Механизм
Температура
Радикально-цепной
800-900 °С
500-550 °С
Ионнокаталитический
550-600 °С
17.
ТЕРМИЧЕСКИЕ ПРОЦЕССЫ (ПИРОЛИЗ И КРЕКИНГ)-
это процессы переработки углеводородов под воздействием
высоких температур без доступа воздуха.
Сырье: легкие нефтяные фракции (например, бензиновая), узкие
фракции парафиновых углеводородов.
Получаемые продукты:
- Газообразные (крекинг-газ или газ пиролиза);
- Жидкие (бензин и крекинг-остаток или смола пиролиза);
- Твердые (кокс или сажа).
18.
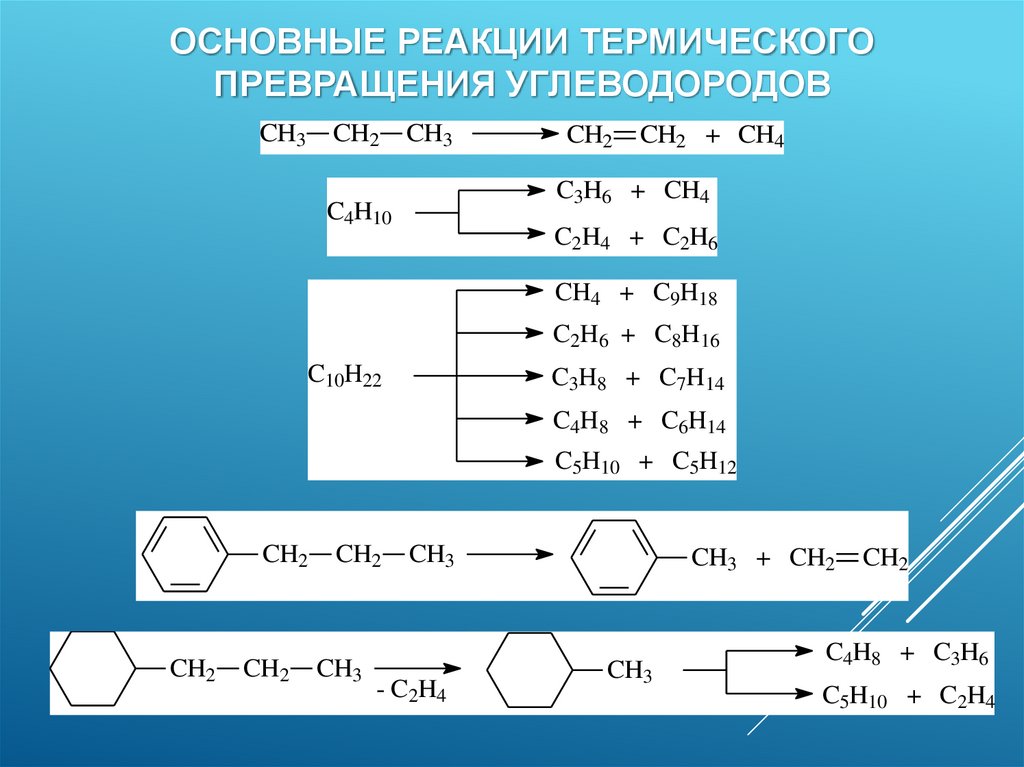
ОСНОВНЫЕ РЕАКЦИИ ТЕРМИЧЕСКОГОПРЕВРАЩЕНИЯ УГЛЕВОДОРОДОВ
CH3
CH2
CH3
CH2
CH2 + CH4
C3H6 + CH4
C4H10
C2H4 + C2H6
CH4 + C9H18
C2H6 + C8H16
C10H22
C3H8 + C7H14
C4H8 + C6H14
C5H10 + C5H12
CH2
CH2
CH2
CH2
CH3
CH3
- C2H4
CH3 + CH2
CH3
CH2
C4H8 + C3H6
C5H10 + C2H4
19.
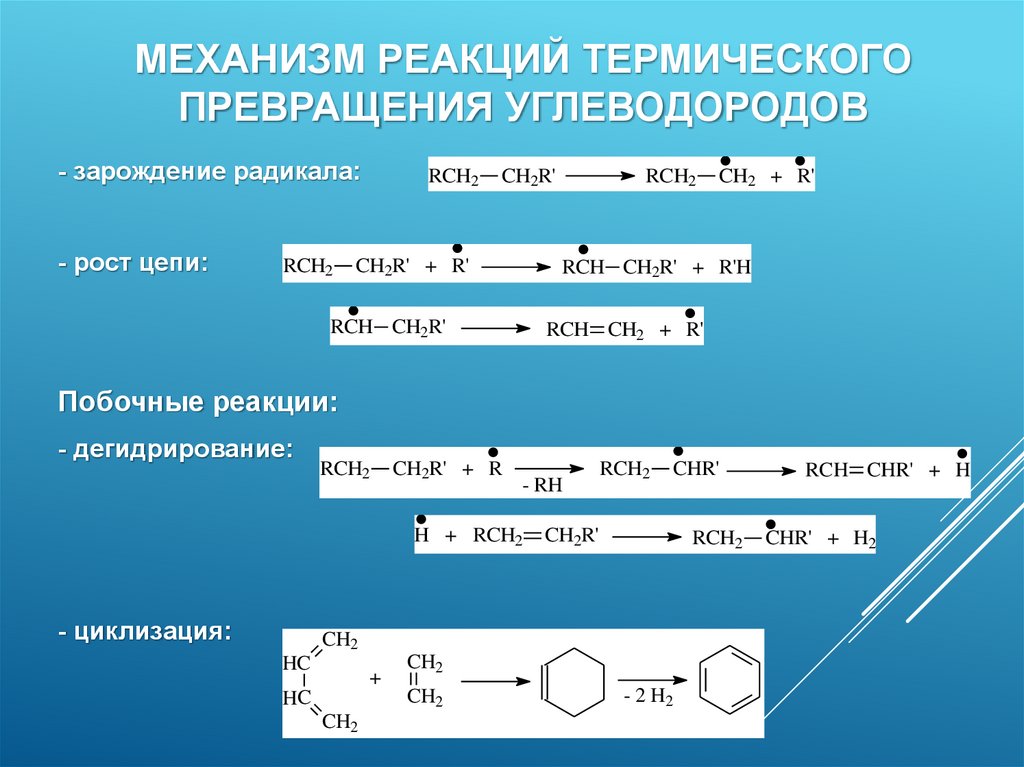
МЕХАНИЗМ РЕАКЦИЙ ТЕРМИЧЕСКОГОПРЕВРАЩЕНИЯ УГЛЕВОДОРОДОВ
- зарождение радикала:
- рост цепи:
RCH2
RCH2
CH2R'
CH2R' + R'
RCH2
CH2 + R'
RCH CH2R' + R'H
RCH CH2R'
RCH CH2 + R'
Побочные реакции:
- дегидрирование:
RCH2
CH2R' + R
- RH
H + RCH2
- циклизация:
RCH2
CHR'
CH2R'
RCH2
CH2
HC
+
CH2
CH2
HC
CH2
- 2 H2
RCH CHR' + H
CHR' + H2
20.
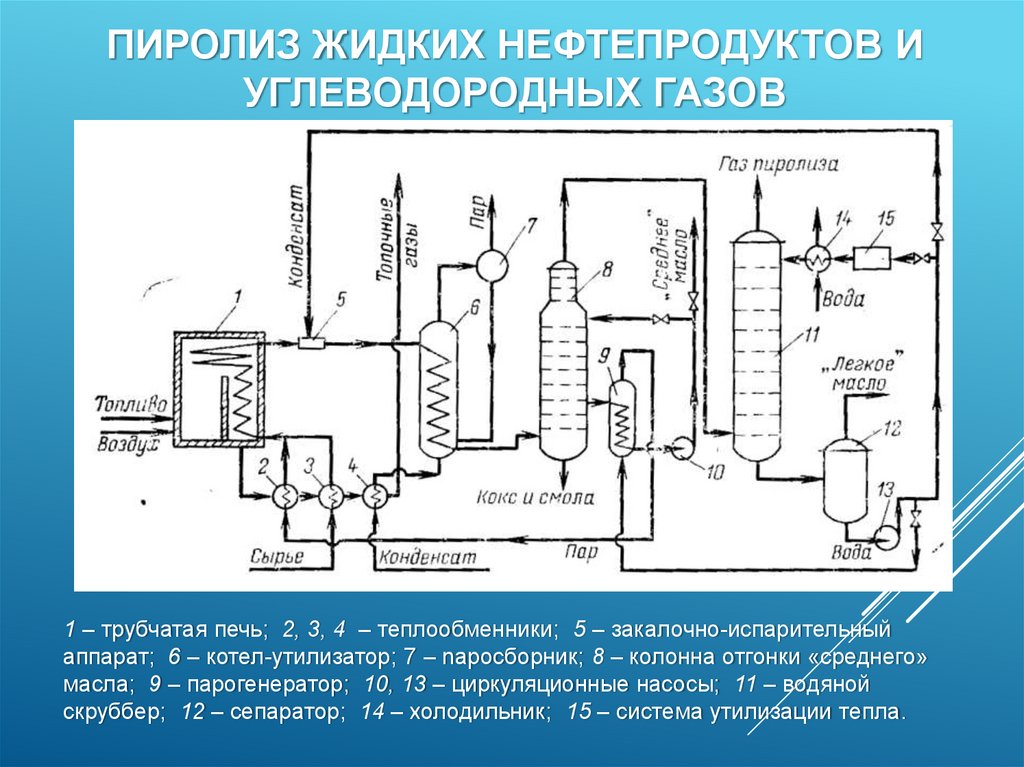
ПИРОЛИЗ ЖИДКИХ НЕФТЕПРОДУКТОВ ИУГЛЕВОДОРОДНЫХ ГАЗОВ
Условия процесса:
Температура: 800-900 °С;
Время контакта: 0,2-0,5 с.
Расход водного конденсата
0,3-0,6 кг/кг углеводородов
Печь пиролиза бензина:
1 – топочная камера;
2 – беспламенная панельная горелка;
3 – трубы радиантной секции;
4 – корпус;
5 – конвекционная камера.
21.
ПИРОЛИЗ ЖИДКИХ НЕФТЕПРОДУКТОВ ИУГЛЕВОДОРОДНЫХ ГАЗОВ
1 – трубчатая печь; 2, 3, 4 – теплообменники; 5 – закалочно-испарительный
аппарат; 6 – котел-утилизатор; 7 – napocбopник; 8 – колонна отгонки «среднего»
масла; 9 – парогенератор; 10, 13 – циркуляционные насосы; 11 – водяной
скруббер; 12 – сепаратор; 14 – холодильник; 15 – система утилизации тепла.
22.
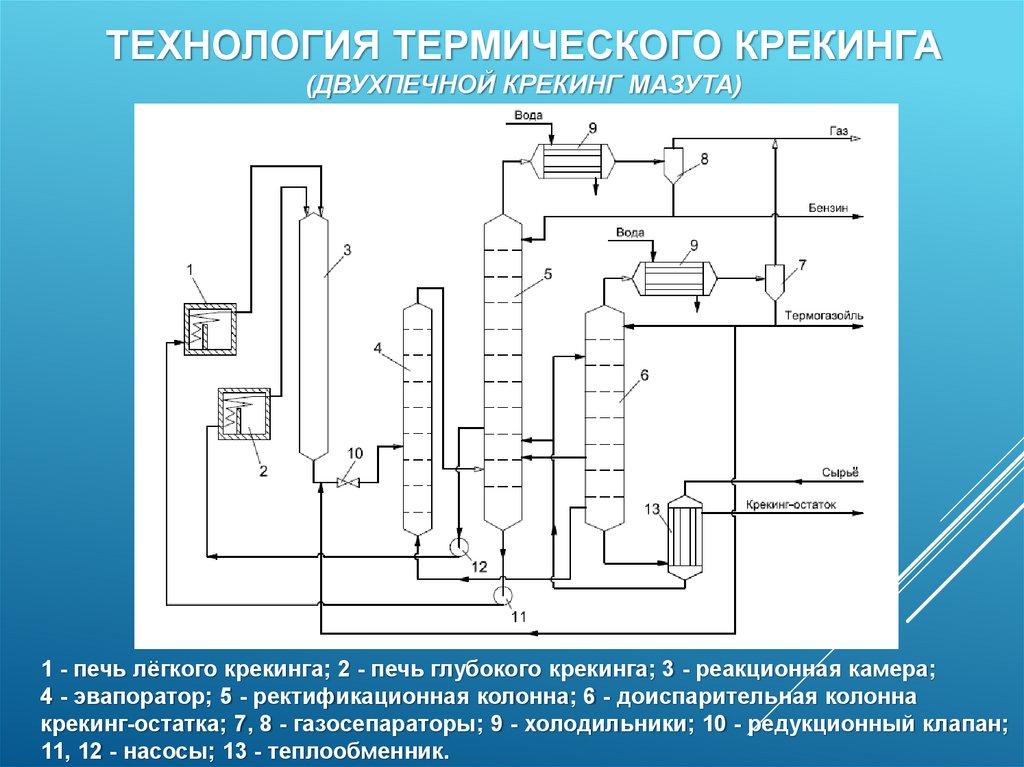
ТЕХНОЛОГИЯ ТЕРМИЧЕСКОГО КРЕКИНГА(ДВУХПЕЧНОЙ КРЕКИНГ МАЗУТА)
1 - печь лёгкого крекинга; 2 - печь глубокого крекинга; 3 - реакционная камера;
4 - эвапоратор; 5 - ректификационная колонна; 6 - доиспарительная колонна
крекинг-остатка; 7, 8 - газосепараторы; 9 - холодильники; 10 - редукционный клапан;
11, 12 - насосы; 13 - теплообменник.
23.
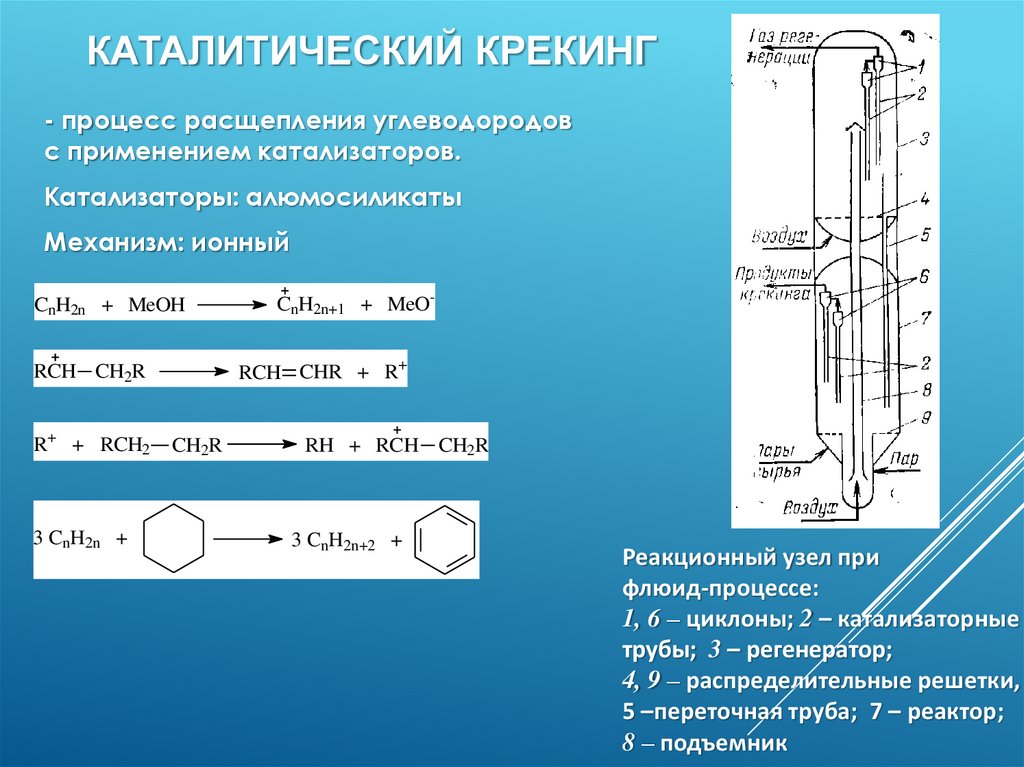
КАТАЛИТИЧЕСКИЙ КРЕКИНГ- процесс расщепления углеводородов
с применением катализаторов.
Катализаторы: алюмосиликаты
Механизм: ионный
CnH2n + MeOH
RCH CHR + R+
RCH CH2R
R+ + RCH2
3 CnH2n +
CnH2n+1 + MeO-
CH2R
RH + RCH CH2R
3 CnH2n+2 +
Реакционный узел при
флюид-процессе:
1, 6 – циклоны; 2 – катализаторные
трубы; 3 – регенератор;
4, 9 – распределительные решетки,
5 –переточная труба; 7 – реактор;
8 – подъемник
24.
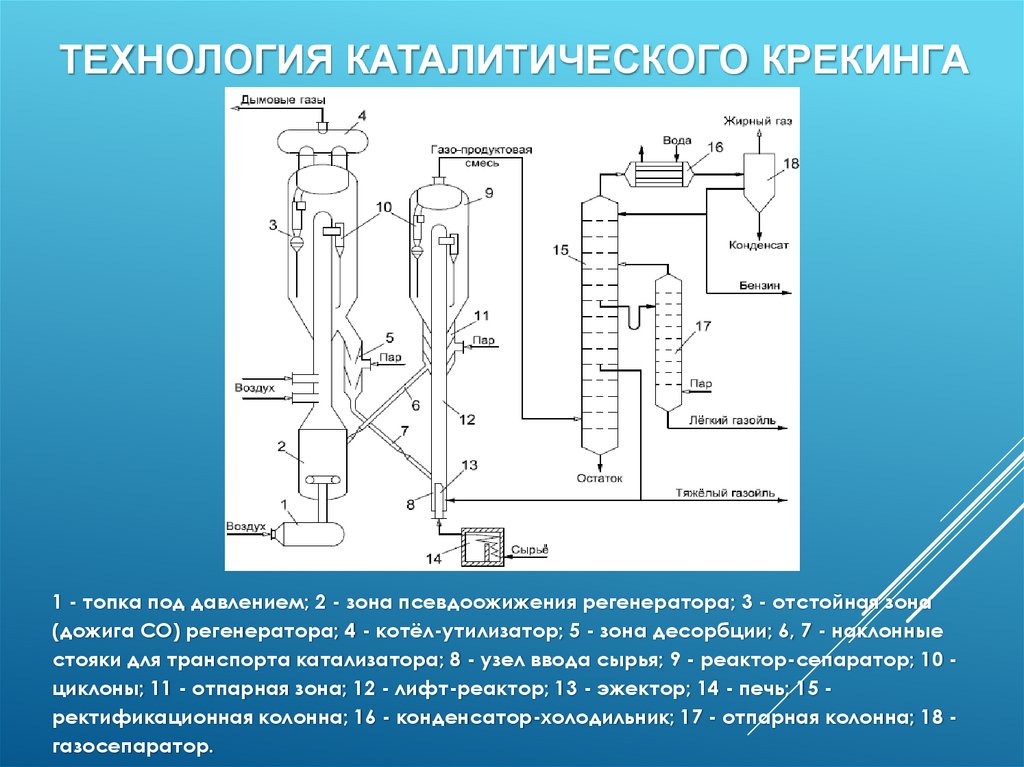
ТЕХНОЛОГИЯ КАТАЛИТИЧЕСКОГО КРЕКИНГА1 - топка под давлением; 2 - зона псевдоожижения регенератора; 3 - отстойная зона
(дожига СО) регенератора; 4 - котёл-утилизатор; 5 - зона десорбции; 6, 7 - наклонные
стояки для транспорта катализатора; 8 - узел ввода сырья; 9 - реактор-сепаратор; 10 циклоны; 11 - отпарная зона; 12 - лифт-реактор; 13 - эжектор; 14 - печь; 15 ректификационная колонна; 16 - конденсатор-холодильник; 17 - отпарная колонна; 18 газосепаратор.
25.
ВЫДЕЛЕНИЕ И КОНЦЕНТРИРОВАНИЕОЛЕФИНОВ
* Газ пиролиза газообразных углеводородов (этилен, пропилен)
* Газ пиролиза жидких нефтепродуктов (этилен, пропилен, бутилены)
* Газы термического и каталитического крекинга (пропилен, бутилены)
Стадии разделения олефинов:
-
Подготовка газа к разделению (очистка от H2S, СО2, Н2О,
выделение жидких углеводородов)
-
Выделение узких фракций углеводородов
-
Выделение индивидуальных веществ из фракций
26.
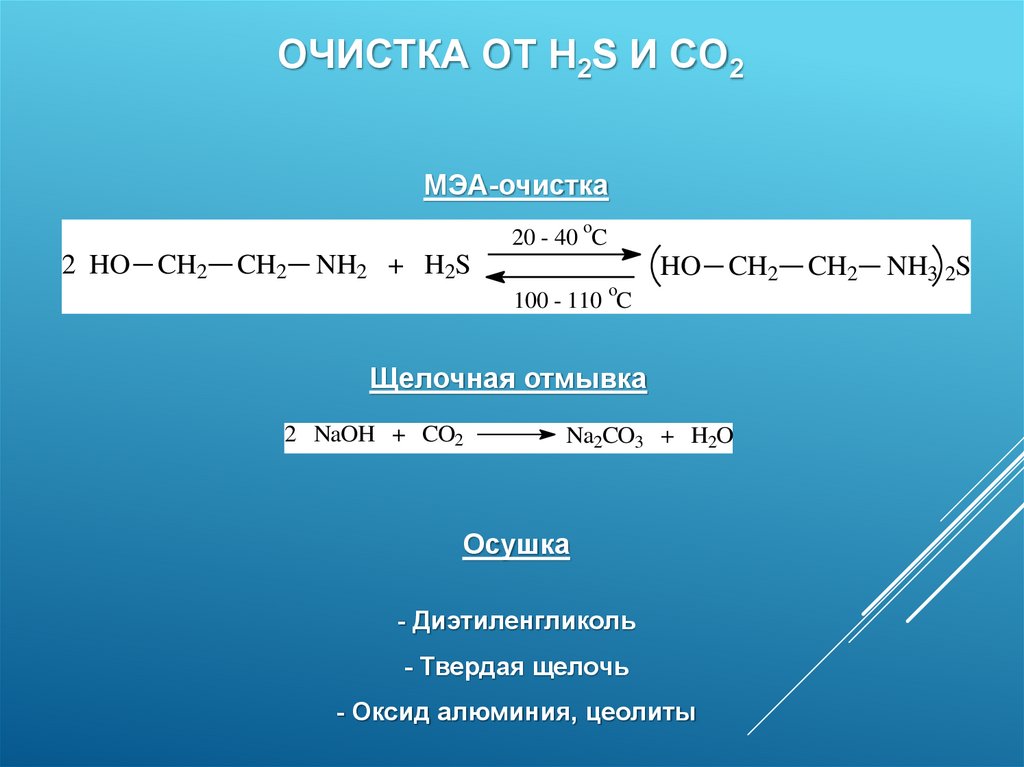
ОЧИСТКА ОТ H2S И CO2МЭА-очистка
o
20 - 40 C
2 HO CH2
CH2
NH2 + H2S
o
HO CH2
100 - 110 C
Щелочная отмывка
2 NaOH + CO2
Na2CO3 + H2O
Осушка
- Диэтиленгликоль
- Твердая щелочь
- Оксид алюминия, цеолиты
CH2
NH3 2S
27.
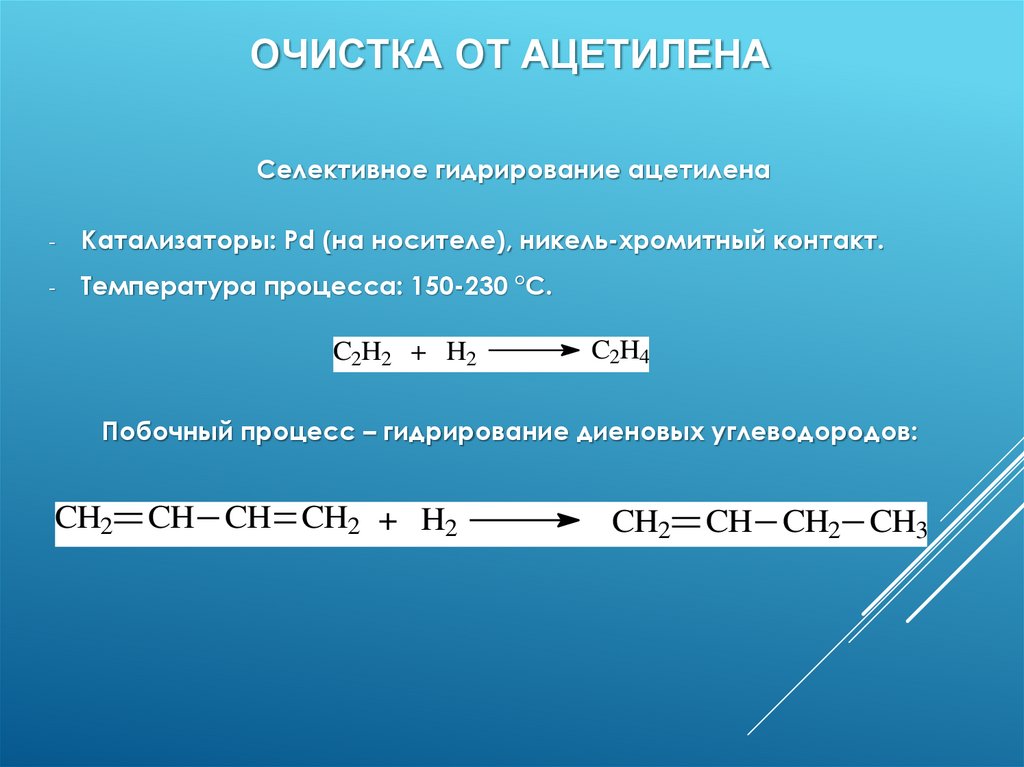
ОЧИСТКА ОТ АЦЕТИЛЕНАСелективное гидрирование ацетилена
-
Катализаторы: Pd (на носителе), никель-хромитный контакт.
-
Температура процесса: 150-230 °С.
C2H2 + H2
C2H4
Побочный процесс – гидрирование диеновых углеводородов:
CH2
CH CH CH2 + H2
CH2
CH CH2 CH3
28.
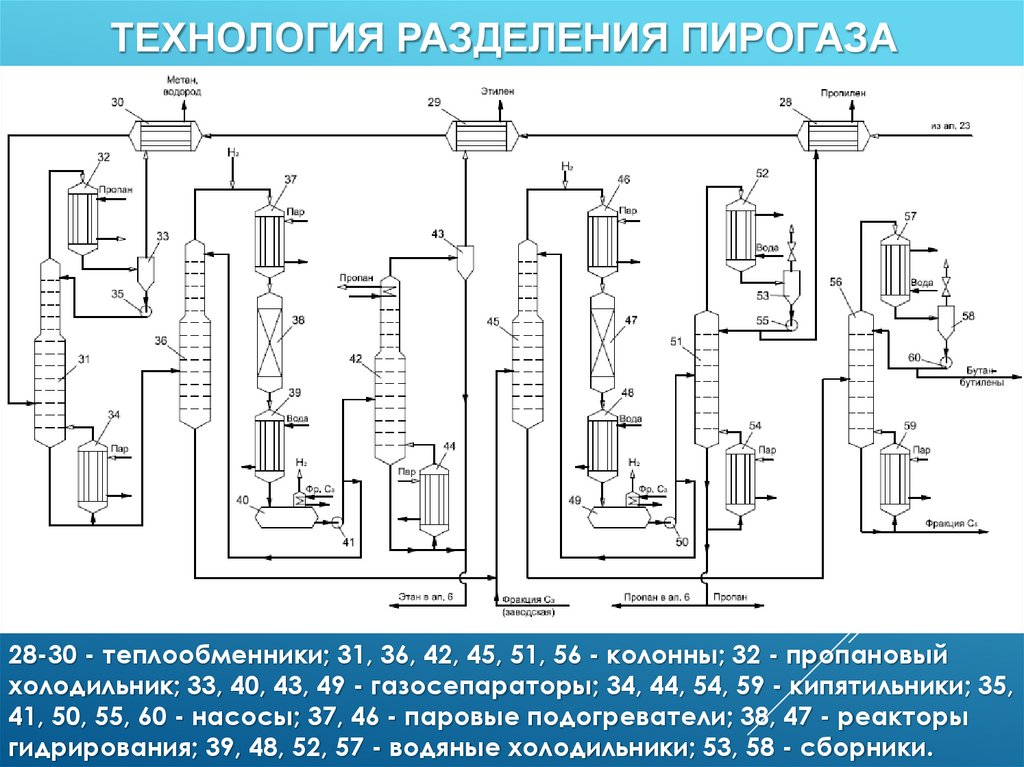
ТЕХНОЛОГИЯ РАЗДЕЛЕНИЯ ПИРОГАЗА28-30 - теплообменники; 31, 36, 42, 45, 51, 56 - колонны; 32 - пропановый
холодильник; 33, 40, 43, 49 - газосепараторы; 34, 44, 54, 59 - кипятильники; 35,
41, 50, 55, 60 - насосы; 37, 46 - паровые подогреватели; 38, 47 - реакторы
гидрирования; 39, 48, 52, 57 - водяные холодильники; 53, 58 - сборники.
29.
ВЫДЕЛЕНИЕ И КОНЦЕНТРИРОВАНИЕФРАКЦИЙ ОЛЕФИНОВ
Фракция
Этиленовая
Способ выделения отдельных компонентов
Ректификация – водород, метан, этан;
Селективное гидрирование – ацетилен.
Пропиленовая Ректификация - пропан
Бутиленовая
Хемосорбция водными растворами аммиачных
комплексов ацетата меди (I) – бутадиен-1,3;
Экстрактивная дистилляция фурфуролом,
ацетонитрилом и N-метилпирролидоном – бутадиен-1,3;
Хемосорбция серной кислотой – изобутилен
Амиленовая
Димеризация с последующей ректификацией –
циклопентадиен;
Экстрактивная дистилляция - изопрен
30.
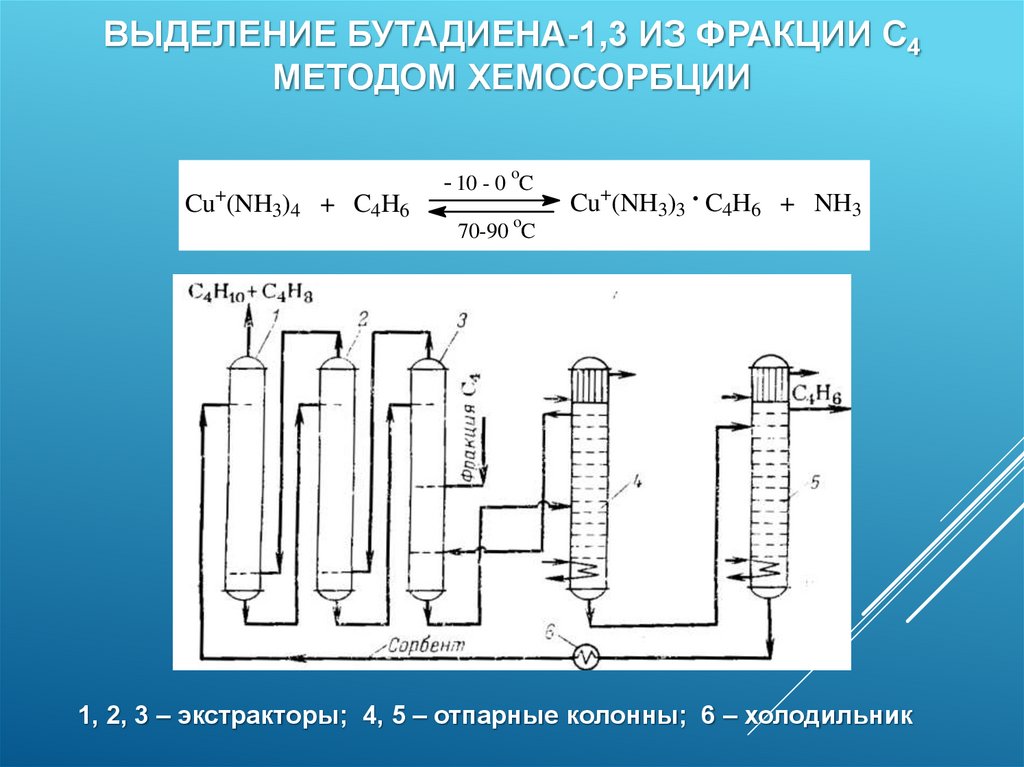
ВЫДЕЛЕНИЕ БУТАДИЕНА-1,3 ИЗ ФРАКЦИИ С4МЕТОДОМ ХЕМОСОРБЦИИ
Cu+(NH3)4 + C4H6
- 10 - 0 oC
o
Cu+(NH3)3 . C4H6 + NH3
70-90 C
1, 2, 3 – экстракторы; 4, 5 – отпарные колонны; 6 – холодильник
31.
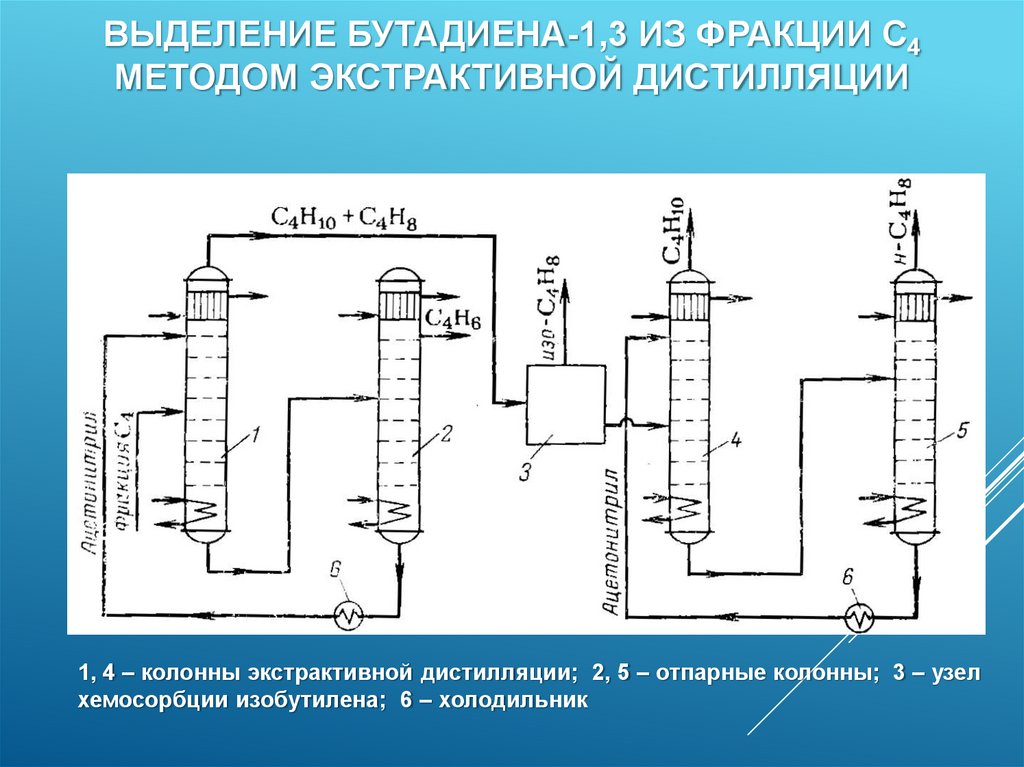
ВЫДЕЛЕНИЕ БУТАДИЕНА-1,3 ИЗ ФРАКЦИИ С4МЕТОДОМ ЭКСТРАКТИВНОЙ ДИСТИЛЛЯЦИИ
1, 4 – колонны экстрактивной дистилляции; 2, 5 – отпарные колонны; 3 – узел
хемосорбции изобутилена; 6 – холодильник
32.
КИСЛОТНАЯ ОЛИГОМЕРИЗАЦИЯ ОЛЕФИНОВ- процесс полимеризации олефинов с получением продуктов
олигомерного характера (низкая степень полимеризации).
Катализаторы – кислотного типа (ортофосфорная кислота)
1) Образование карбокатиона
2) Димеризация
изобутилена
3) Изомеризация
вторичных
карбокатионов
(побочный процесс)
33.
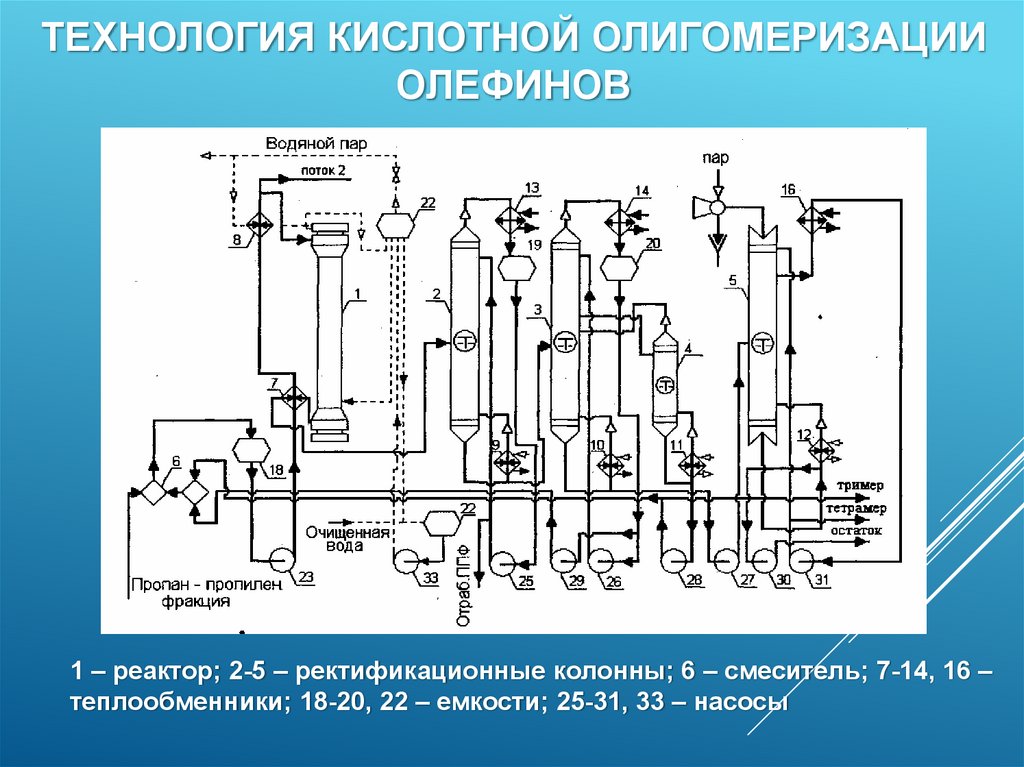
ТЕХНОЛОГИЯ КИСЛОТНОЙ ОЛИГОМЕРИЗАЦИИОЛЕФИНОВ
1 – реактор; 2-5 – ректификационные колонны; 6 – смеситель; 7-14, 16 –
теплообменники; 18-20, 22 – емкости; 25-31, 33 – насосы
34.
ДИСПРОПОРЦИОНИРОВАНИЕ ОЛЕФИНОВДиспропорционирование пропилена в этилен и н-бутилен
Диспропорционирование пропилена и изобутилена
в этилен и 2-метилбутен-2
Основные параметры процесса:
Катализаторы
–
оксиды молибдена и вольфрама на Al2O3 или SiO2
Температура
–
150-400 °С
Давление
–
1-4 МПа
Степень конверсии –
40-55 %
Селективность
95-97 %
–
35.
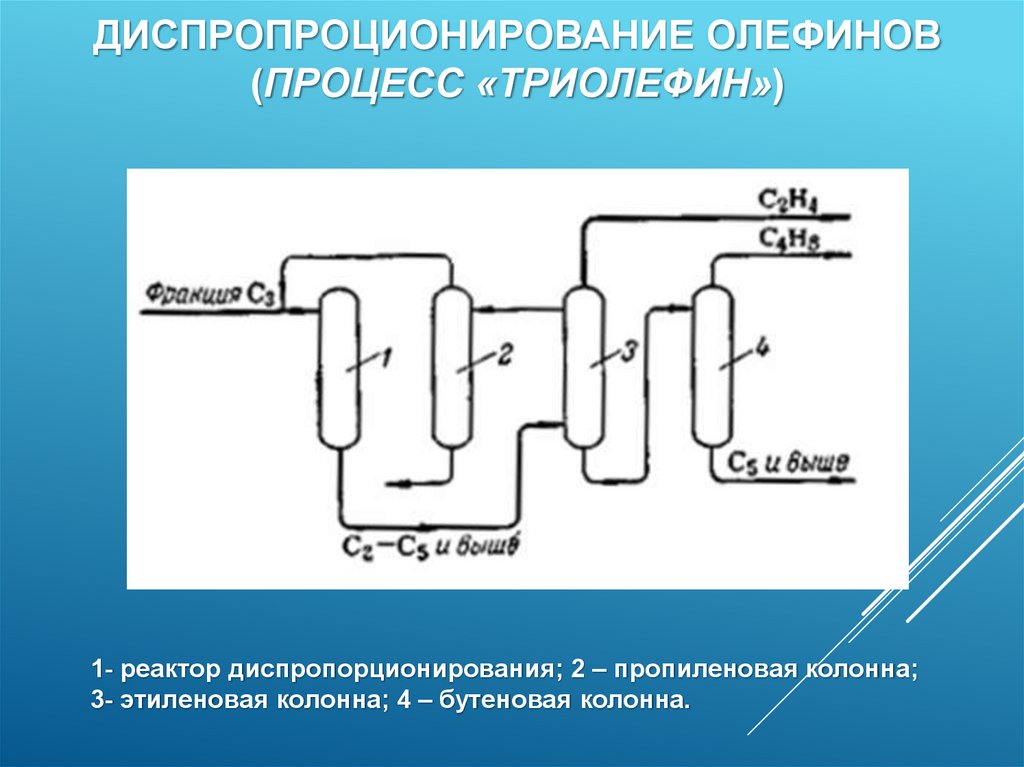
ДИСПРОПРОЦИОНИРОВАНИЕ ОЛЕФИНОВ(ПРОЦЕСС «ТРИОЛЕФИН»)
1- реактор диспропорционирования; 2 – пропиленовая колонна;
3- этиленовая колонна; 4 – бутеновая колонна.
36.
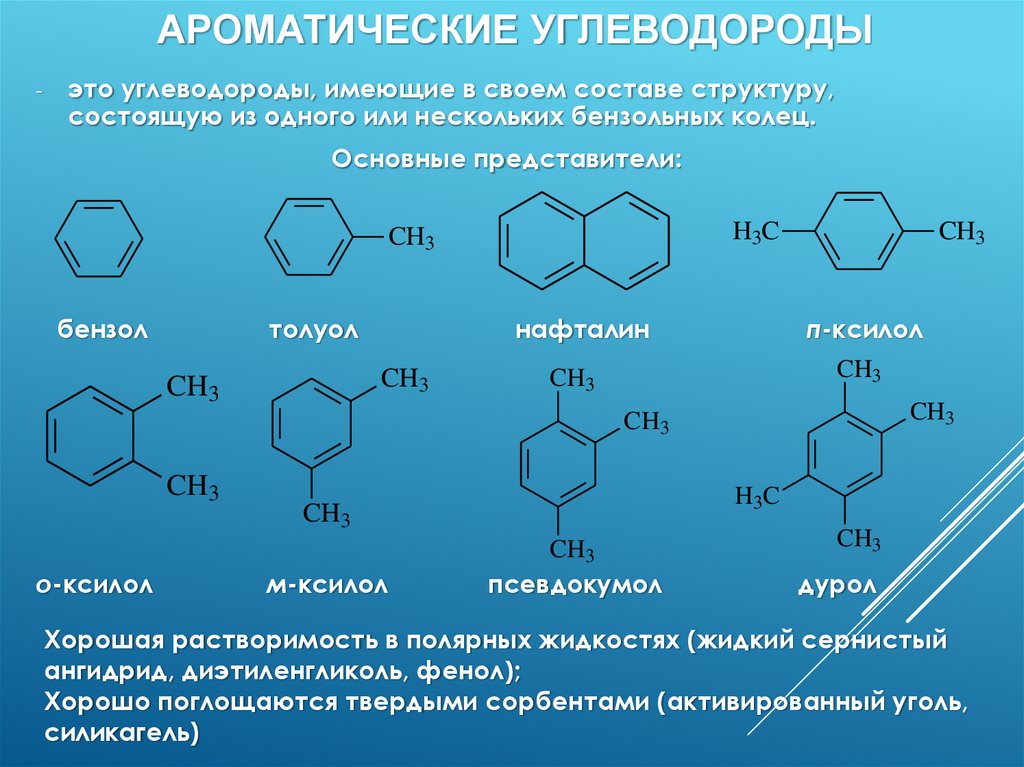
АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ-
это углеводороды, имеющие в своем составе структуру,
состоящую из одного или нескольких бензольных колец.
Основные представители:
H3C
CH3
бензол
толуол
CH3
CH3
CH3
нафталин
п-ксилол
CH3
CH3
CH3
CH3
CH3
о-ксилол
H3C
CH3
м-ксилол
CH3
псевдокумол
CH3
дурол
Хорошая растворимость в полярных жидкостях (жидкий сернистый
ангидрид, диэтиленгликоль, фенол);
Хорошо поглощаются твердыми сорбентами (активированный уголь,
силикагель)
37.
АРОМАТИЗАЦИЯ НЕФТЕПРОДУКТОВОсновные виды процессов:
-
Пиролиз нефтепродуктов (ароматизация
углеводородов с прямой цепью) – бензол,
толуол, ксилолы
-
Каталитический риформинг нефтепродуктов
-
Коксование каменного угля
38.
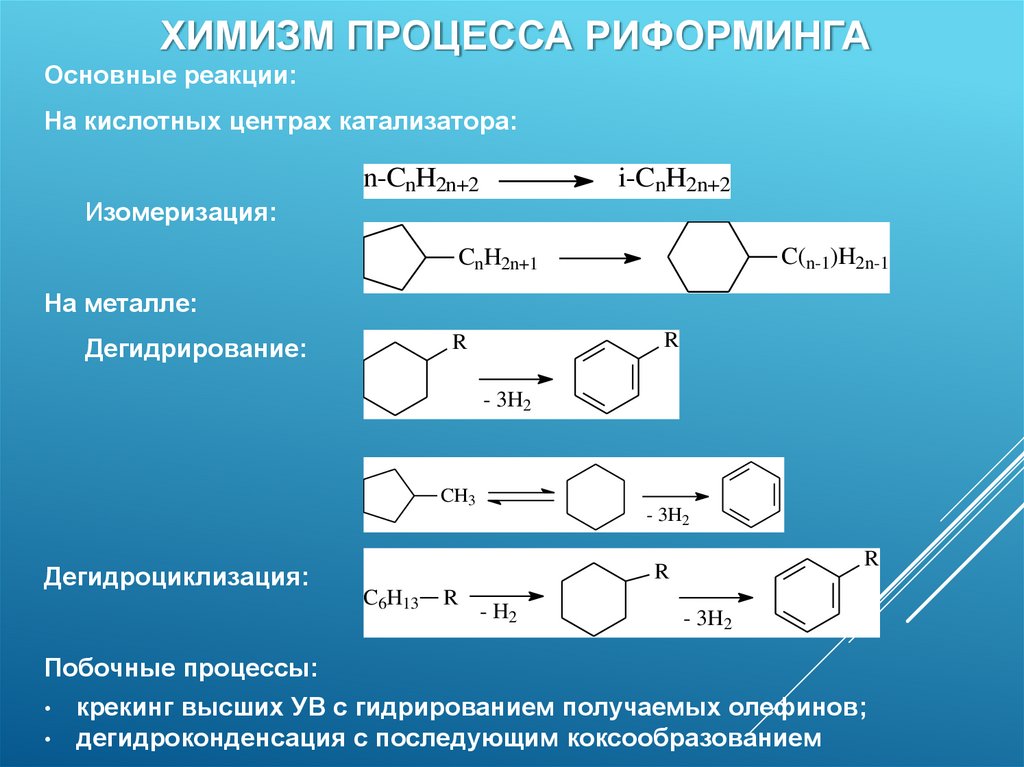
ХИМИЗМ ПРОЦЕССА РИФОРМИНГАОсновные реакции:
На кислотных центрах катализатора:
n-CnH2n+2
i-CnH2n+2
Изомеризация:
C(n-1)H2n-1
CnH2n+1
На металле:
R
R
Дегидрирование:
- 3H2
CH3
Дегидроциклизация:
- 3H2
R
R
C6H13
R
- H2
- 3H2
Побочные процессы:
крекинг высших УВ с гидрированием получаемых олефинов;
дегидроконденсация с последующим коксообразованием
39.
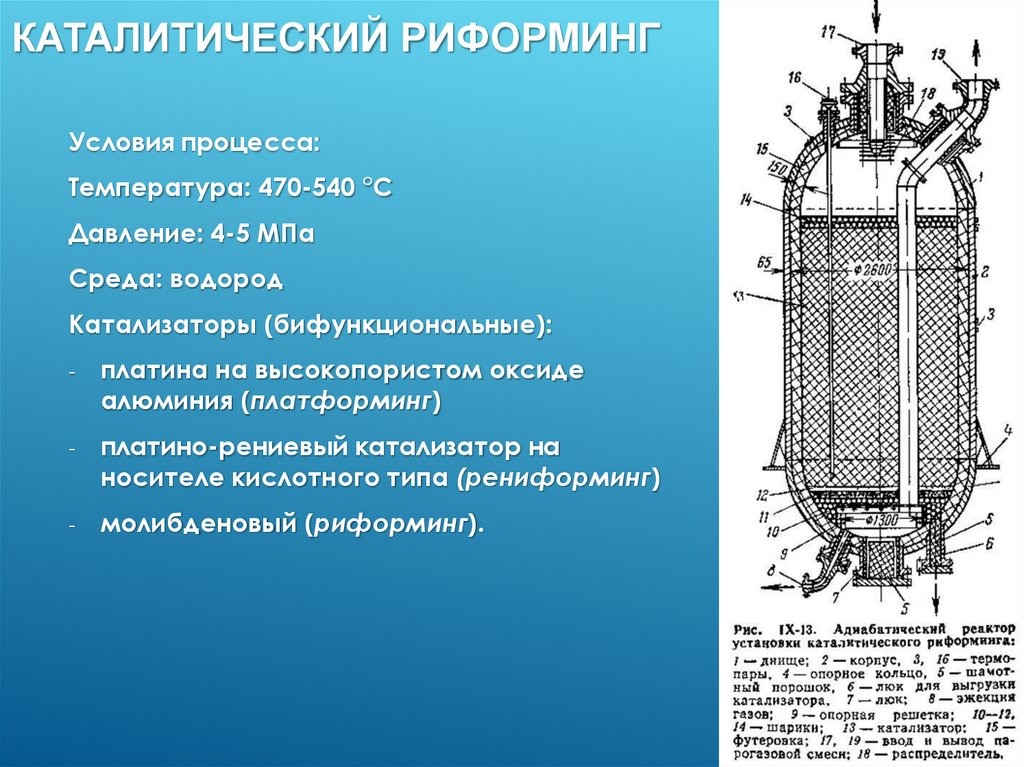
КАТАЛИТИЧЕСКИЙ РИФОРМИНГУсловия процесса:
Температура: 470-540 °С
Давление: 4-5 МПа
Среда: водород
Катализаторы (бифункциональные):
-
платина на высокопористом оксиде
алюминия (платформинг)
-
платино-рениевый катализатор на
носителе кислотного типа (рениформинг)
-
молибденовый (риформинг).
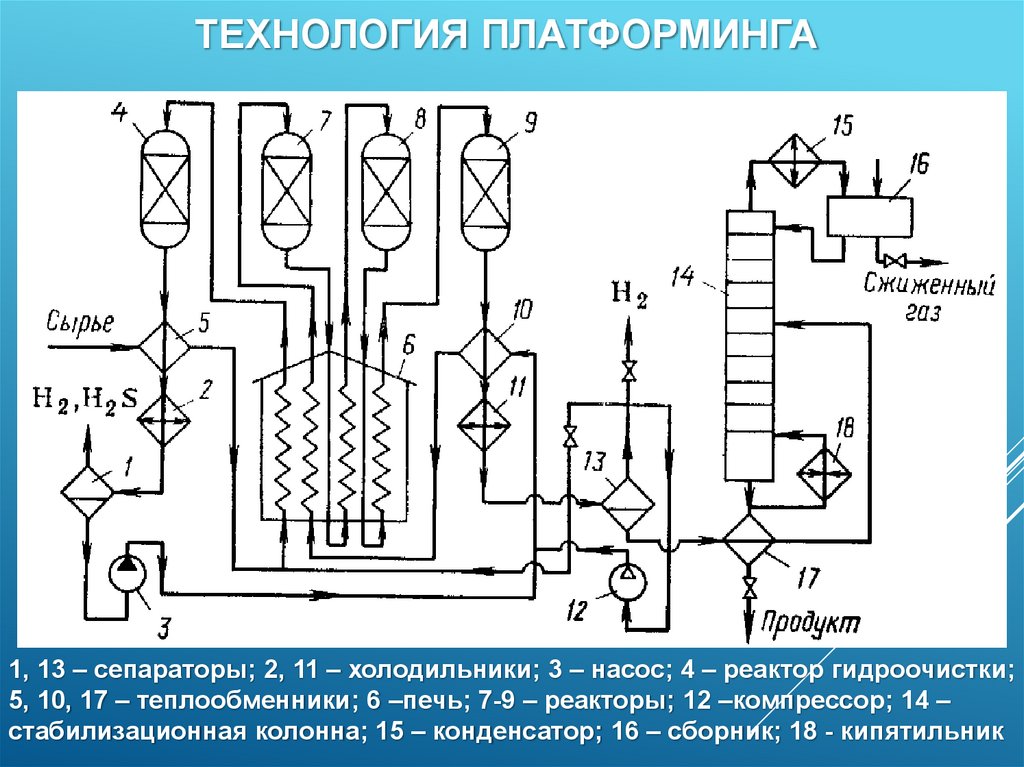
40.
ТЕХНОЛОГИЯ ПЛАТФОРМИНГА1, 13 – сепараторы; 2, 11 – холодильники; 3 – насос; 4 – реактор гидроочистки;
5, 10, 17 – теплообменники; 6 –печь; 7-9 – реакторы; 12 –компрессор; 14 –
стабилизационная колонна; 15 – конденсатор; 16 – сборник; 18 - кипятильник
41.
КОКСОВАНИЕ-
процесс переработки твердых горючих
ископаемых при температуре около 1000 °С
без доступа воздуха.
В основе процесса лежат реакции пиролиза и
ароматизации углеводородов органической
массы угля.
Продукты коксования:
- кокс (75-80 %),
- жидкие продукты коксования – смола и сырой
бензол (4-5 %),
- газ коксования (15-20 %).
Коксовая печь:
1 – перекидные
каналы;
2 – стояки;
3 – коксовые камеры;
4 – обогревательные
простенки;
5 - регенераторы
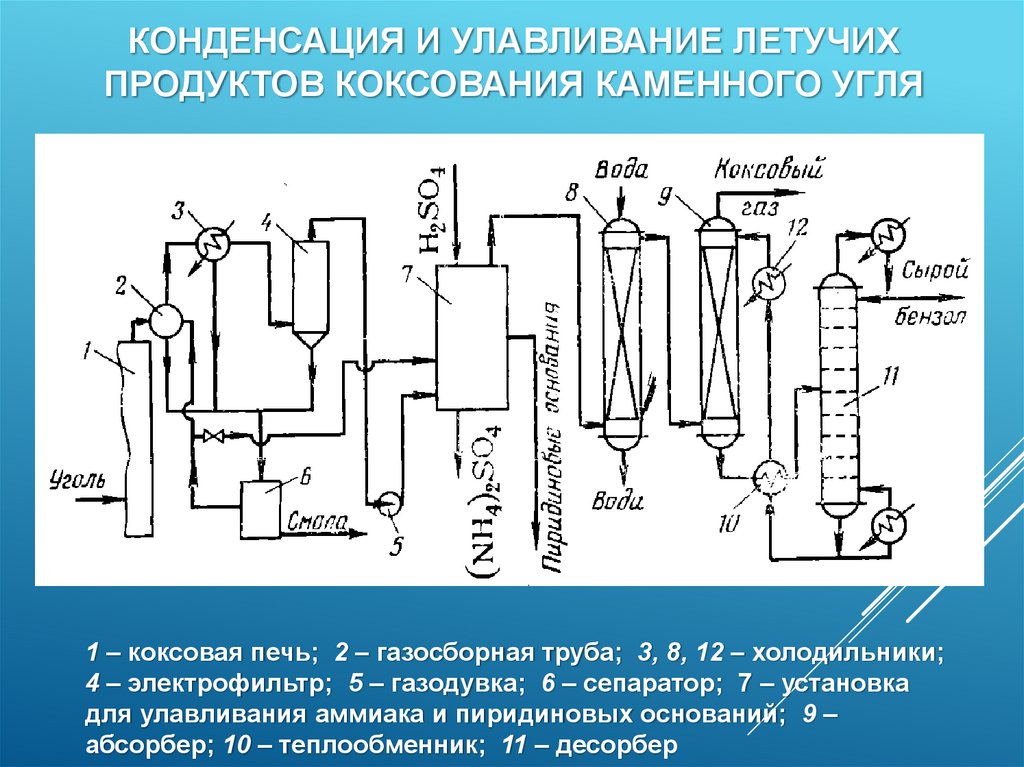
42.
КОНДЕНСАЦИЯ И УЛАВЛИВАНИЕ ЛЕТУЧИХПРОДУКТОВ КОКСОВАНИЯ КАМЕННОГО УГЛЯ
1 – коксовая печь; 2 – газосборная труба; 3, 8, 12 – холодильники;
4 – электрофильтр; 5 – газодувка; 6 – сепаратор; 7 – установка
для улавливания аммиака и пиридиновых оснований; 9 –
абсорбер; 10 – теплообменник; 11 – десорбер
43.
ВЫДЕЛЕНИЕ И ОЧИСТКА АРОМАТИЧЕСКИХУГЛЕВОДОРОДОВ
Очистка от фенолов (коксохимический метод получения фенолов):
Очистка от олефинов (сернокислотный метод):
Очистка от парафинов – экстракция высокоселективными
растворителями (ди-, три- и тетраэтиленгликоль,
диметилсульфоксид).
Выделение ароматических углеводородов с конденсированными
циклами – кристаллизация.
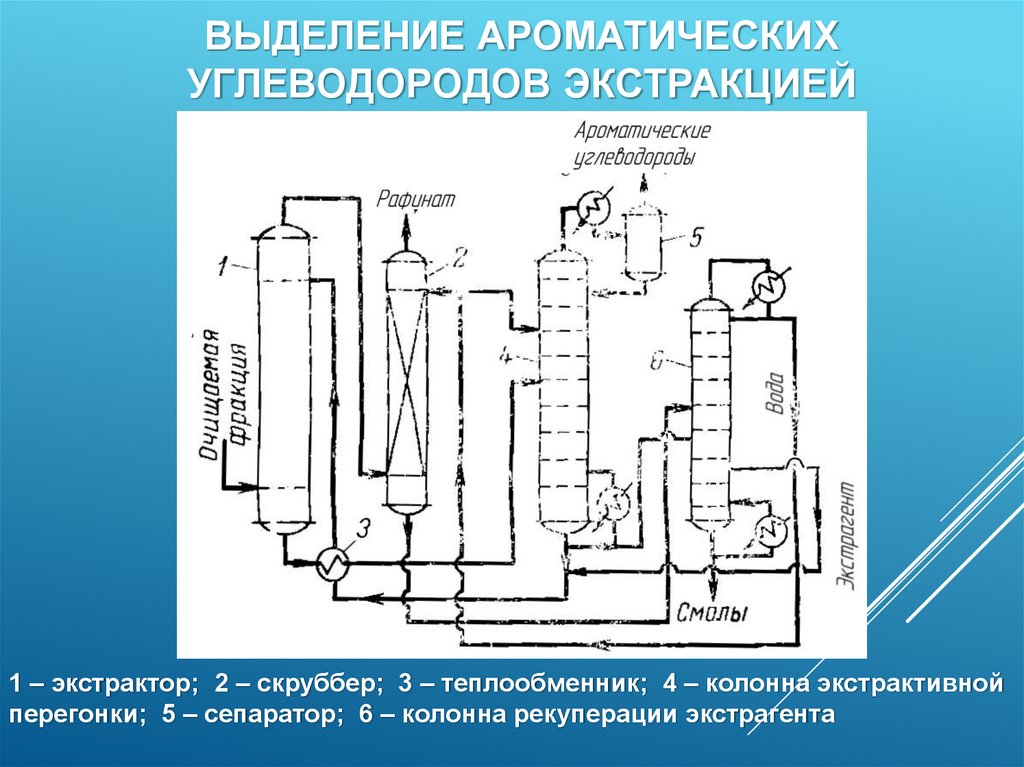
44.
ВЫДЕЛЕНИЕ АРОМАТИЧЕСКИХУГЛЕВОДОРОДОВ ЭКСТРАКЦИЕЙ
1 – экстрактор; 2 – скруббер; 3 – теплообменник; 4 – колонна экстрактивной
перегонки; 5 – сепаратор; 6 – колонна рекуперации экстрагента
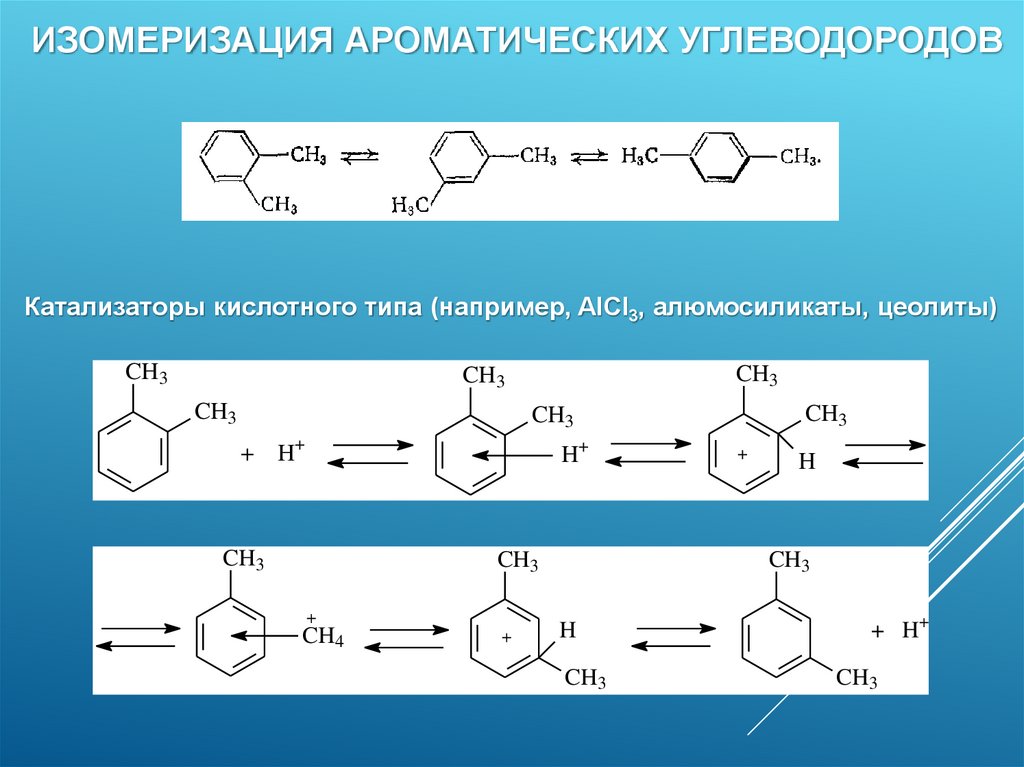
45.
ИЗОМЕРИЗАЦИЯ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВКатализаторы кислотного типа (например, AlCl3, алюмосиликаты, цеолиты)
CH3
CH3
CH3
CH3
CH3
CH3
+ H+
H+
CH3
CH3
+
CH4
+
+
H
CH3
H
CH3
+ H+
CH3
46.
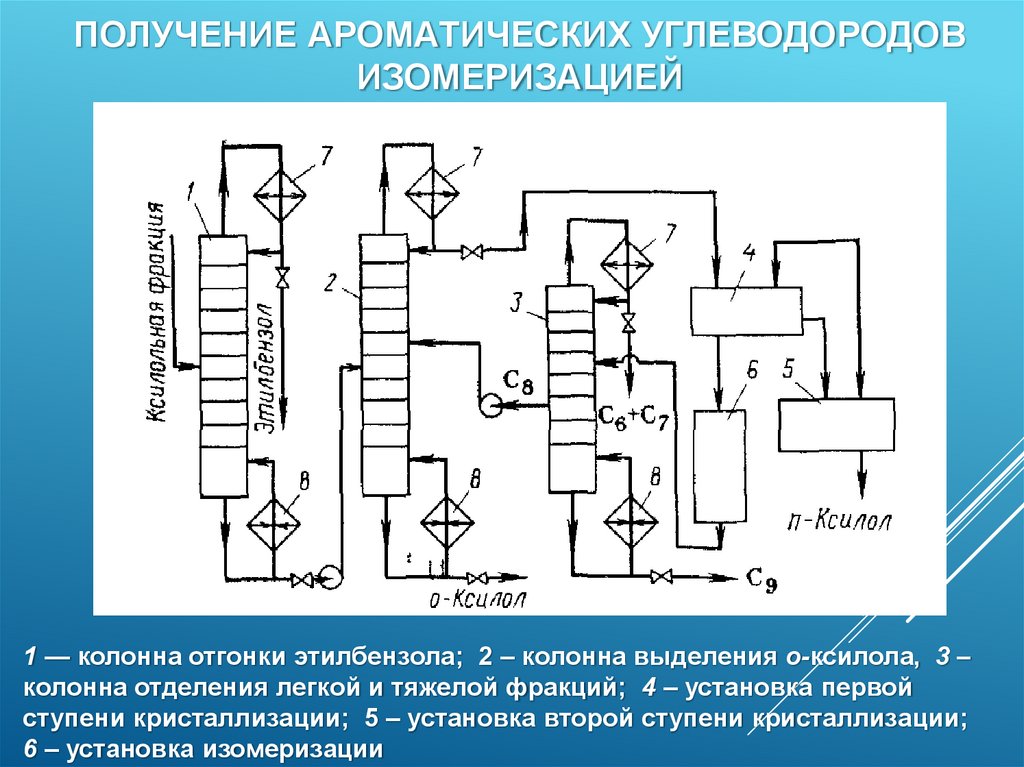
ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВИЗОМЕРИЗАЦИЕЙ
1 — колонна отгонки этилбензола; 2 – колонна выделения о-ксилола, 3 –
колонна отделения легкой и тяжелой фракций; 4 – установка первой
ступени кристаллизации; 5 – установка второй ступени кристаллизации;
6 – установка изомеризации
47.
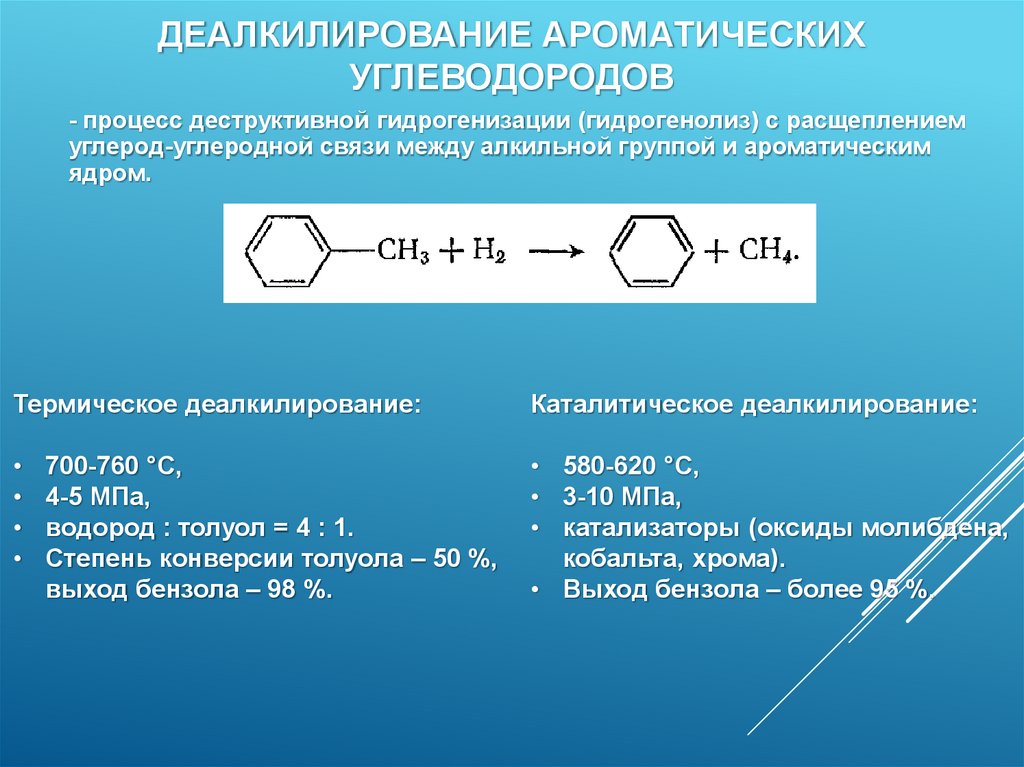
ДЕАЛКИЛИРОВАНИЕ АРОМАТИЧЕСКИХУГЛЕВОДОРОДОВ
- процесс деструктивной гидрогенизации (гидрогенолиз) с расщеплением
углерод-углеродной связи между алкильной группой и ароматическим
ядром.
Термическое деалкилирование:
Каталитическое деалкилирование:
• 580-620 °С,
• 3-10 МПа,
• катализаторы (оксиды молибдена,
кобальта, хрома).
• Выход бензола – более 95 %.
700-760 °С,
4-5 МПа,
водород : толуол = 4 : 1.
Степень конверсии толуола – 50 %,
выход бензола – 98 %.
48.
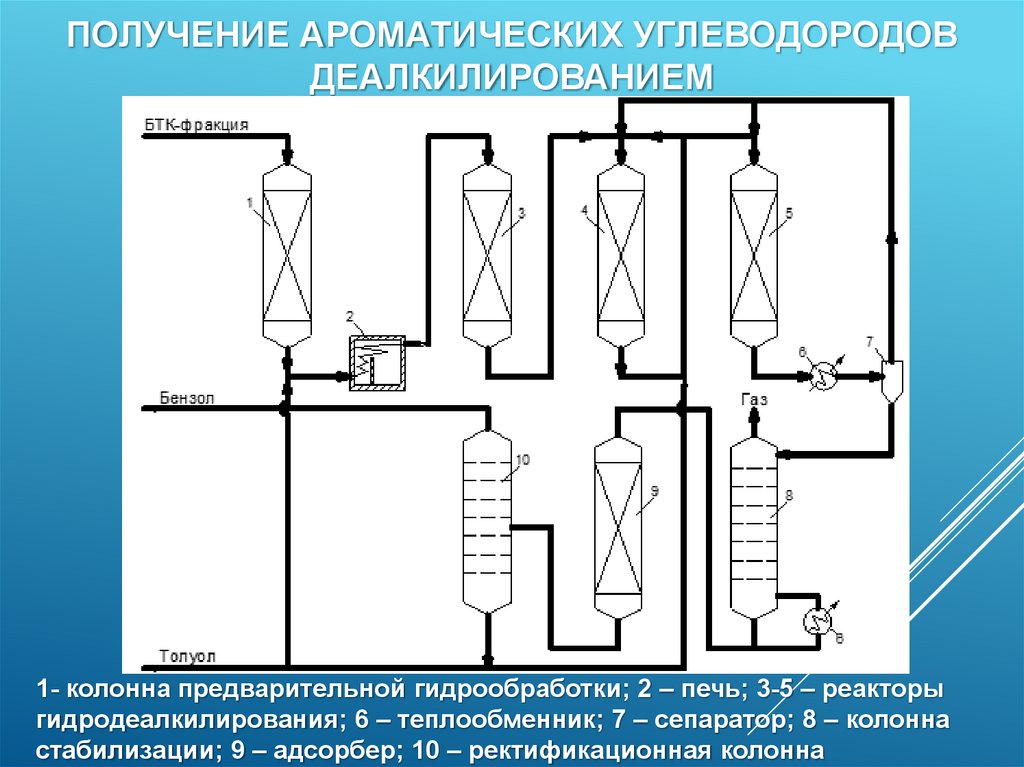
ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВДЕАЛКИЛИРОВАНИЕМ
1- колонна предварительной гидрообработки; 2 – печь; 3-5 – реакторы
гидродеалкилирования; 6 – теплообменник; 7 – сепаратор; 8 – колонна
стабилизации; 9 – адсорбер; 10 – ректификационная колонна
49.
АЦЕТИЛЕН-
бесцветный газ со слабым эфирным запахом.
Взрывоопасен (широкие пределы взрываемости, реакция разложения
сильно экзотермична):
C2H2
2 C + H2
Н 0298 226,7 кДж / моль (54,2 ккал / моль)
Хорошо растворяется в воде, органических жидкостях
(объем/объем растворителя):
- метанол
– 11,2
- ацетон
– 23
- диметилформамид
– 32
- N-винилпирролидон – 37
50.
ПРОИЗВОДСТВО АЦЕТИЛЕНА ИЗКАРБИДА КАЛЬЦИЯ
Получение карбида кальция:
CaO + 3 C
CaC2 + CO
Получение ацетилена:
CaC2 + 2 H2O
C2H2 + H2O
Н 0298 127,1 кДж / моль (30,4 ккал / моль)
1 кг технического карбида – 230-280 л ацетилена.
Теоретический выход ацетилена – 380 л.
51.
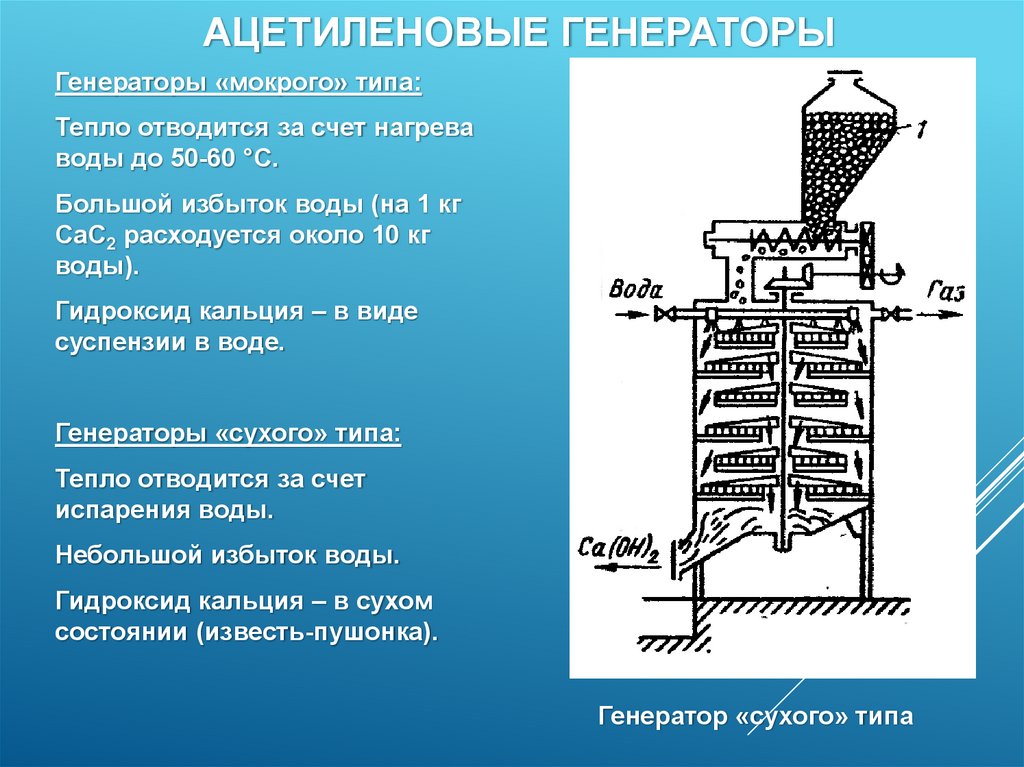
АЦЕТИЛЕНОВЫЕ ГЕНЕРАТОРЫГенераторы «мокрого» типа:
Тепло отводится за счет нагрева
воды до 50-60 °С.
Большой избыток воды (на 1 кг
СаС2 расходуется около 10 кг
воды).
Гидроксид кальция – в виде
суспензии в воде.
Генераторы «сухого» типа:
Тепло отводится за счет
испарения воды.
Небольшой избыток воды.
Гидроксид кальция – в сухом
состоянии (известь-пушонка).
Генератор «сухого» типа
52.
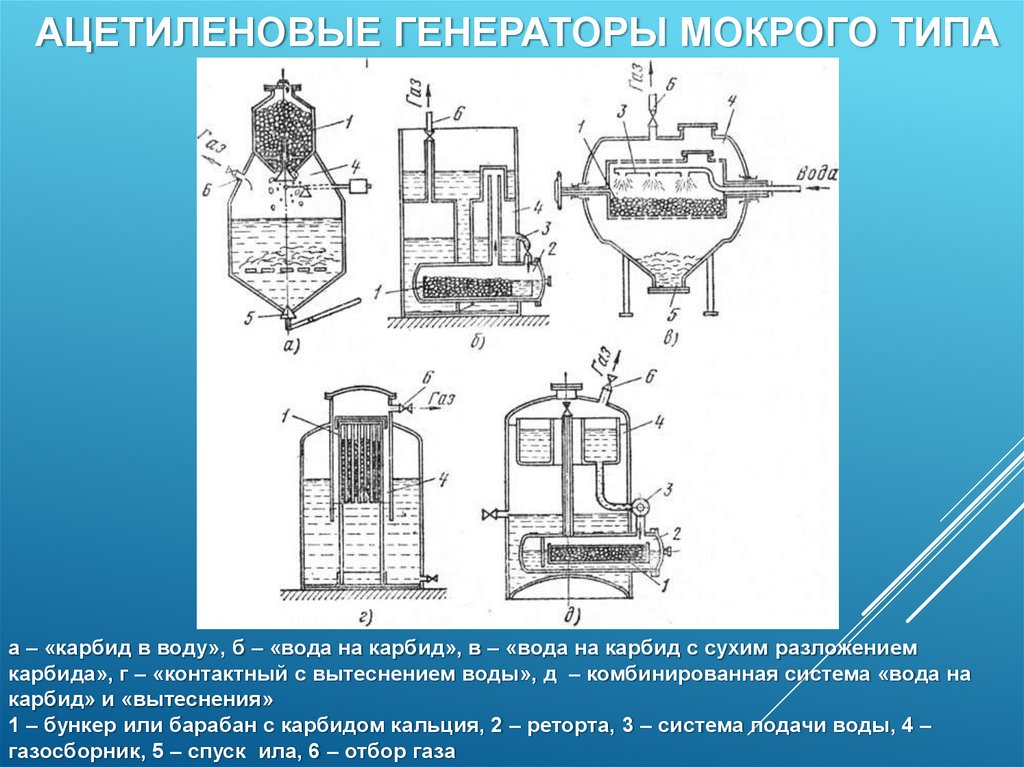
АЦЕТИЛЕНОВЫЕ ГЕНЕРАТОРЫ МОКРОГО ТИПАа – «карбид в воду», б – «вода на карбид», в – «вода на карбид с сухим разложением
карбида», г – «контактный с вытеснением воды», д – комбинированная система «вода на
карбид» и «вытеснения»
1 – бункер или барабан с карбидом кальция, 2 – реторта, 3 – система подачи воды, 4 –
газосборник, 5 – спуск ила, 6 – отбор газа
53.
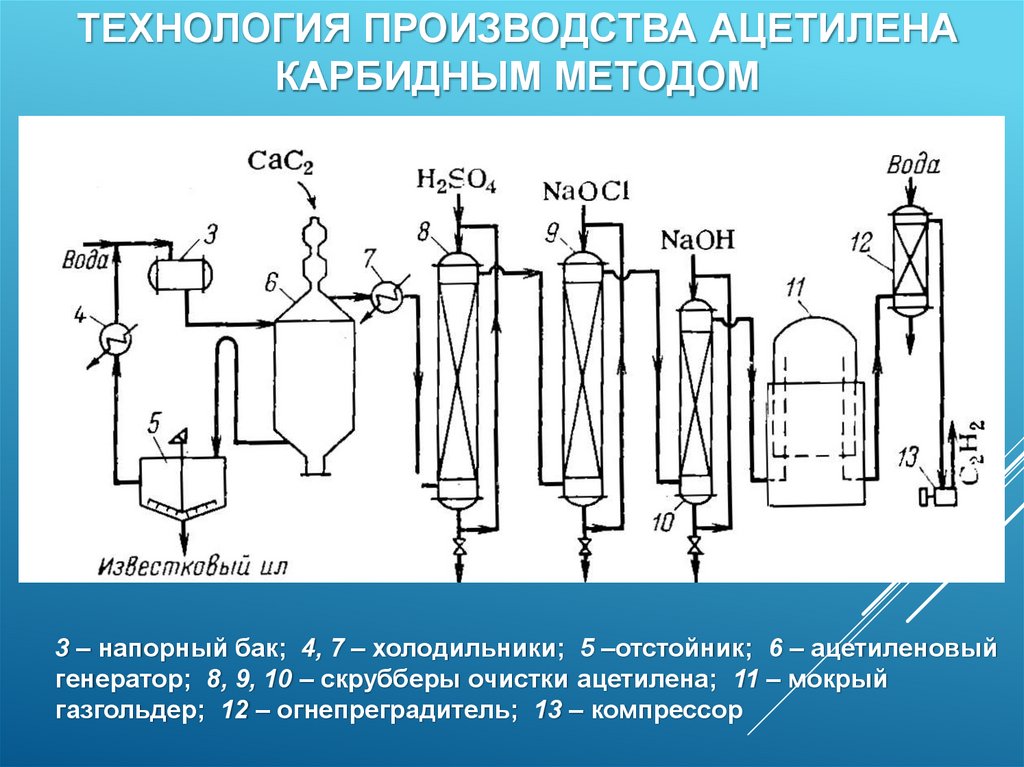
ТЕХНОЛОГИЯ ПРОИЗВОДСТВА АЦЕТИЛЕНАКАРБИДНЫМ МЕТОДОМ
3 – напорный бак; 4, 7 – холодильники; 5 –отстойник; 6 – ацетиленовый
генератор; 8, 9, 10 – скрубберы очистки ацетилена; 11 – мокрый
газгольдер; 12 – огнепреградитель; 13 – компрессор
54.
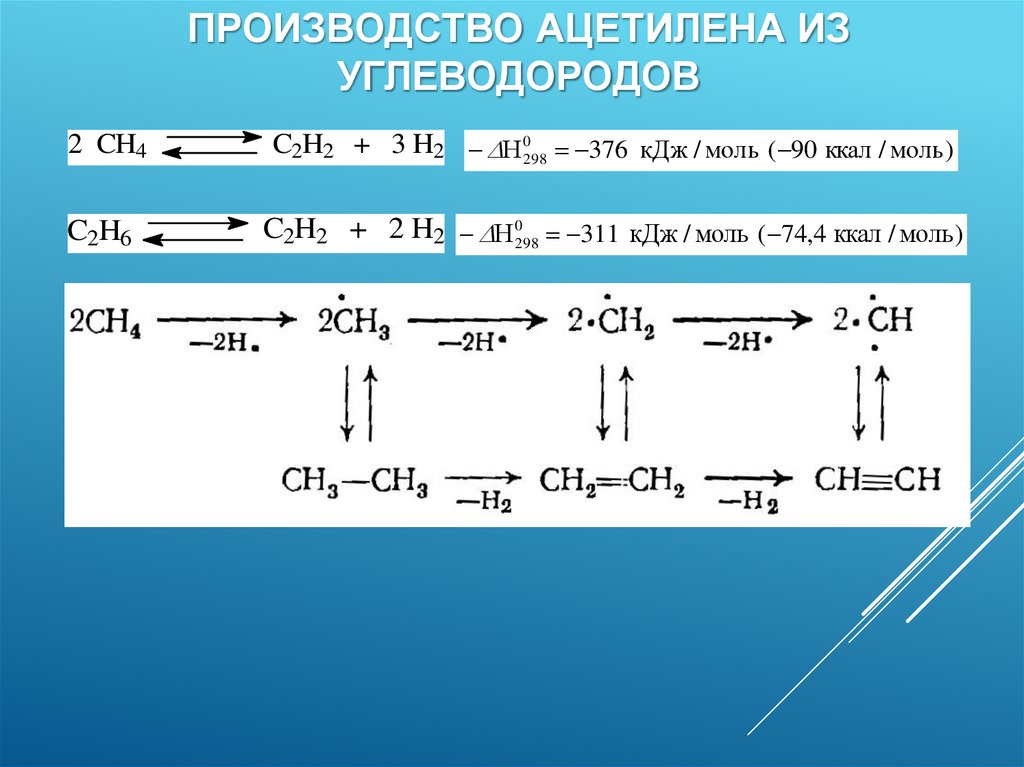
ПРОИЗВОДСТВО АЦЕТИЛЕНА ИЗУГЛЕВОДОРОДОВ
2 CH4
C2H2 + 3 H2 Н 0298 376 кДж / моль ( 90 ккал / моль)
C2H6
C2H2 + 2 H2 Н 0298 311 кДж / моль ( 74,4 ккал / моль)
55.
МЕТОДЫ ПРОИЗВОДСТВААЦЕТИЛЕНА ИЗ УГЛЕВОДОРОДОВ
Электрокрекинг осуществляется при помощи вольтовой дуги, когда
углеводородное сырье подвергают пиролизу в электродуговых печах
при напряжении между электродами около 1000 В. Затраты
электроэнергии доходят до 13 000 кВт ∙ ч на 1 т ацетилена.
Регенеративный пиролиз проводится в печах с огнеупорной насадкой; ее
сперва разогревают топочными газами, а затем через раскаленную
насадку пропускают пиролизуемое сырье. Эти периоды чередуются.
Гомогенный пиролиз, при котором сырье вводят в поток горячего
топочного газа, полученного сжиганием метана в кислороде и имеющего
температуру около 2000 °С.
Окислительный пиролиз, при котором экзотермическая реакция горения
углеводородов и эндотермический процесс пиролиза совмещены в
одном аппарате.
56.
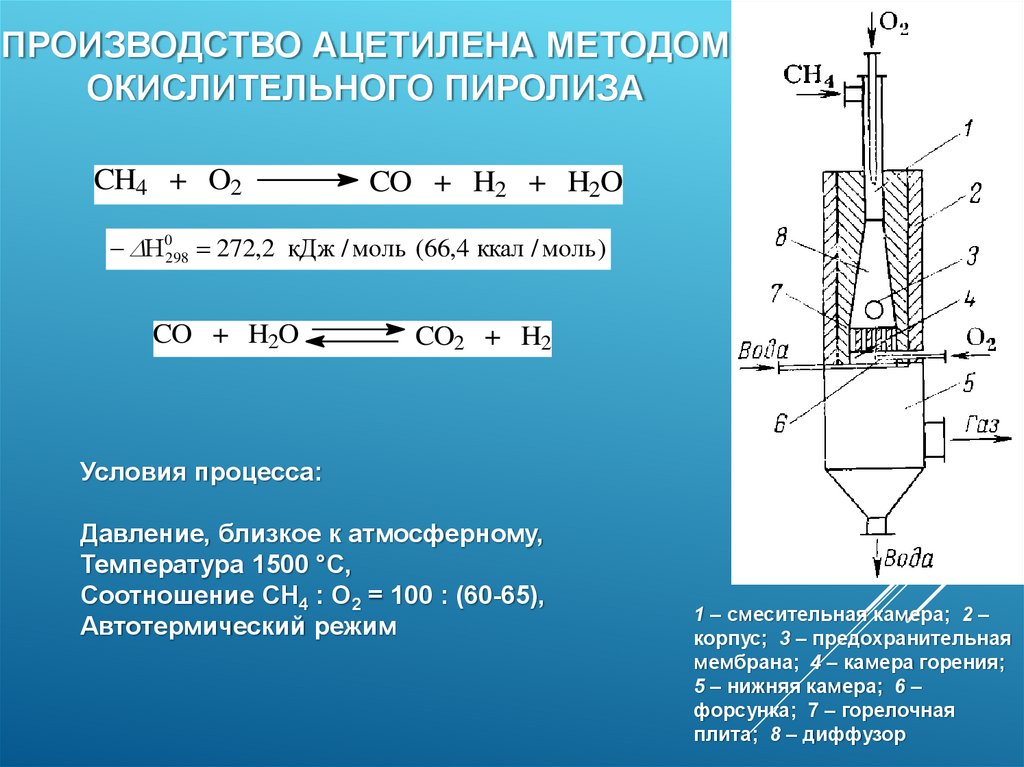
ПРОИЗВОДСТВО АЦЕТИЛЕНА МЕТОДОМОКИСЛИТЕЛЬНОГО ПИРОЛИЗА
CH4 + O2
CO + H2 + H2O
Н 0298 272,2 кДж / моль (66,4 ккал / моль)
CO + H2O
CO2 + H2
Условия процесса:
Давление, близкое к атмосферному,
Температура 1500 °С,
Соотношение СН4 : О2 = 100 : (60-65),
Автотермический режим
1 – смесительная камера; 2 –
корпус; 3 – предохранительная
мембрана; 4 – камера горения;
5 – нижняя камера; 6 –
форсунка; 7 – горелочная
плита; 8 – диффузор
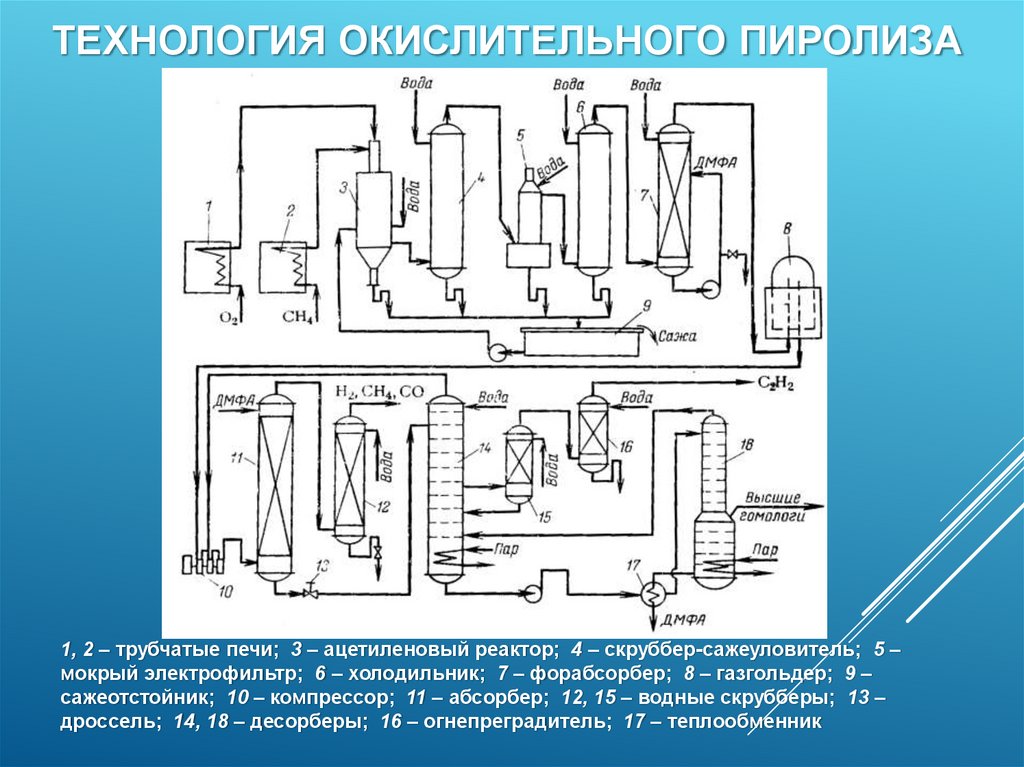
57.
ТЕХНОЛОГИЯ ОКИСЛИТЕЛЬНОГО ПИРОЛИЗА1, 2 – трубчатые печи; 3 – ацетиленовый реактор; 4 – скруббер-сажеуловитель; 5 –
мокрый электрофильтр; 6 – холодильник; 7 – форабсорбер; 8 – газгольдер; 9 –
сажеотстойник; 10 – компрессор; 11 – абсорбер; 12, 15 – водные скрубберы; 13 –
дроссель; 14, 18 – десорберы; 16 – огнепреградитель; 17 – теплообменник
58.
СРАВНЕНИЕ МЕТОДОВ ПОЛУЧЕНИЯ АЦЕТИЛЕНАКарбидный метод
Достоинства:
Получение концентрированного
ацетилена
Очистка от небольшого
количества примесей
Доступность исходного сырья
(каменный уголь, мел)
Недостатки:
Большой расход
электроэнергии,
Многостадийность
Металлоемкость производства
Углеводородный метод
Достоинства:
Одностадийность
Сравнительно невысокие
затраты энергии и материалов
Недостатки:
Невысокий выход ацетилена
Сложность стадии выделения и
очистки ацетилена
59.
СИНТЕЗ-ГАЗ-
смесь оксида углерода и водорода, чаще всего
применяется в объемном отношении от 1 : 1 до
(2-2,3) : 1
Основные способы получения:
1.
Газификация твердых топлив (каменный уголь)
2.
Паровая конверсия – высокотемпературная и
каталитическая (метан, природный и попутный
газы, газы переработки нефти, жидкие фракции
нефти)
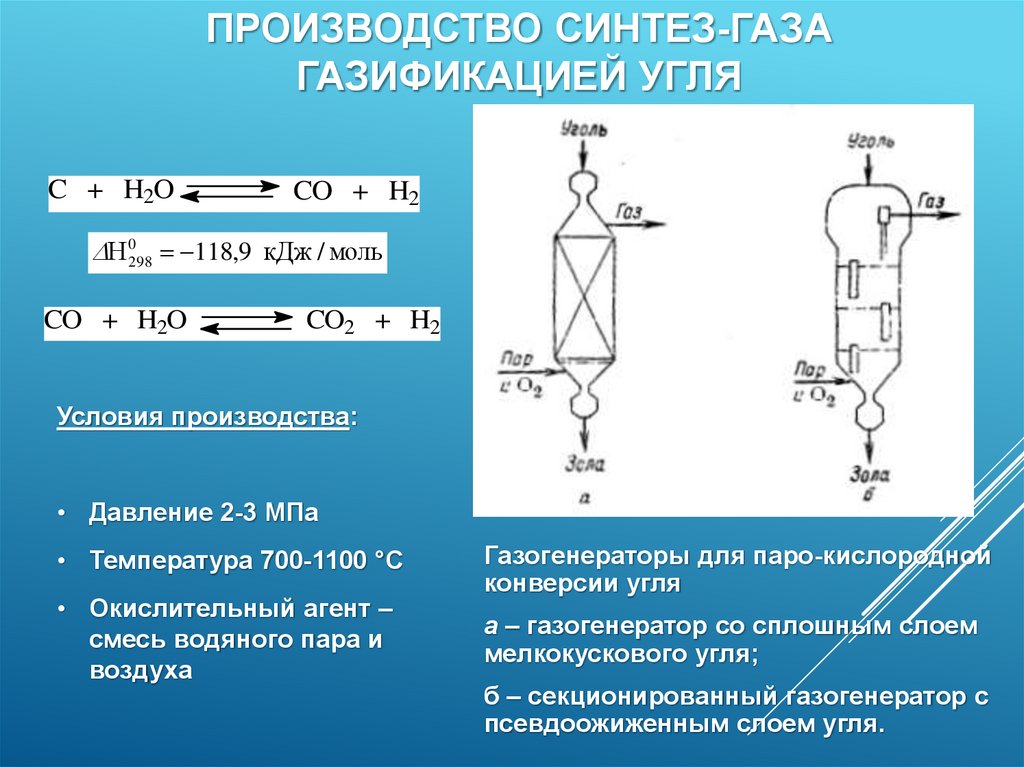
60.
ПРОИЗВОДСТВО СИНТЕЗ-ГАЗАГАЗИФИКАЦИЕЙ УГЛЯ
C + H2O
CO + H2
Н 0298 118,9 кДж / моль
CO + H2O
CO2 + H2
Условия производства:
• Давление 2-3 МПа
• Температура 700-1100 °С
• Окислительный агент –
смесь водяного пара и
воздуха
Газогенераторы для паро-кислородной
конверсии угля
а – газогенератор со сплошным слоем
мелкокускового угля;
б – секционированный газогенератор с
псевдоожиженным слоем угля.
61.
ПРОИЗВОДСТВО СИНТЕЗ-ГАЗАКАТАЛИТИЧЕСКОЙ КОНВЕРСИЕЙ
CH4 + H2O
CO + 3 H2
Н 0298 206 кДж / моль ( 49,3 ккал / моль)
CO + H2O
CO2 + H2
Н 0298 41 кДж / моль (9,8 ккал / моль)
CH4 + CO2
2 CO + 2 H2
Н 0298 247 кДж / моль ( 59,2 ккал / моль)
Температура 800-900 °С
Катализатор: никель на оксиде алюминия
Избыток водяного пара
(при 0,1 МПа – 2:1, при повышении давления – 4:1)
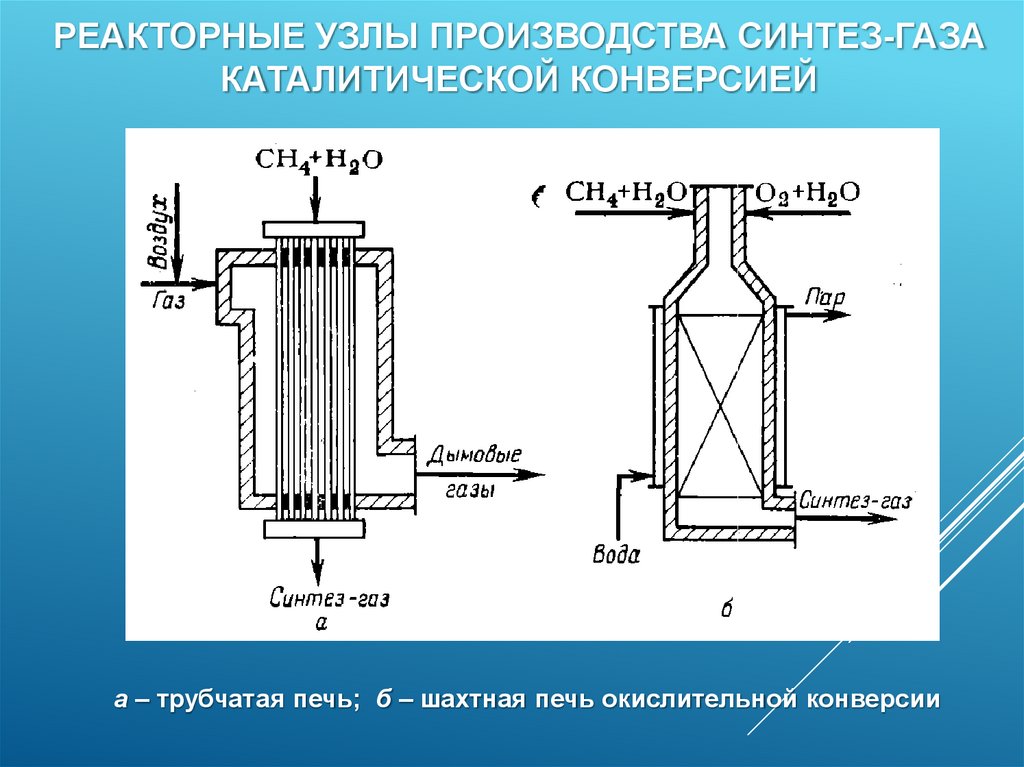
62.
РЕАКТОРНЫЕ УЗЛЫ ПРОИЗВОДСТВА СИНТЕЗ-ГАЗАКАТАЛИТИЧЕСКОЙ КОНВЕРСИЕЙ
а – трубчатая печь; б – шахтная печь окислительной конверсии
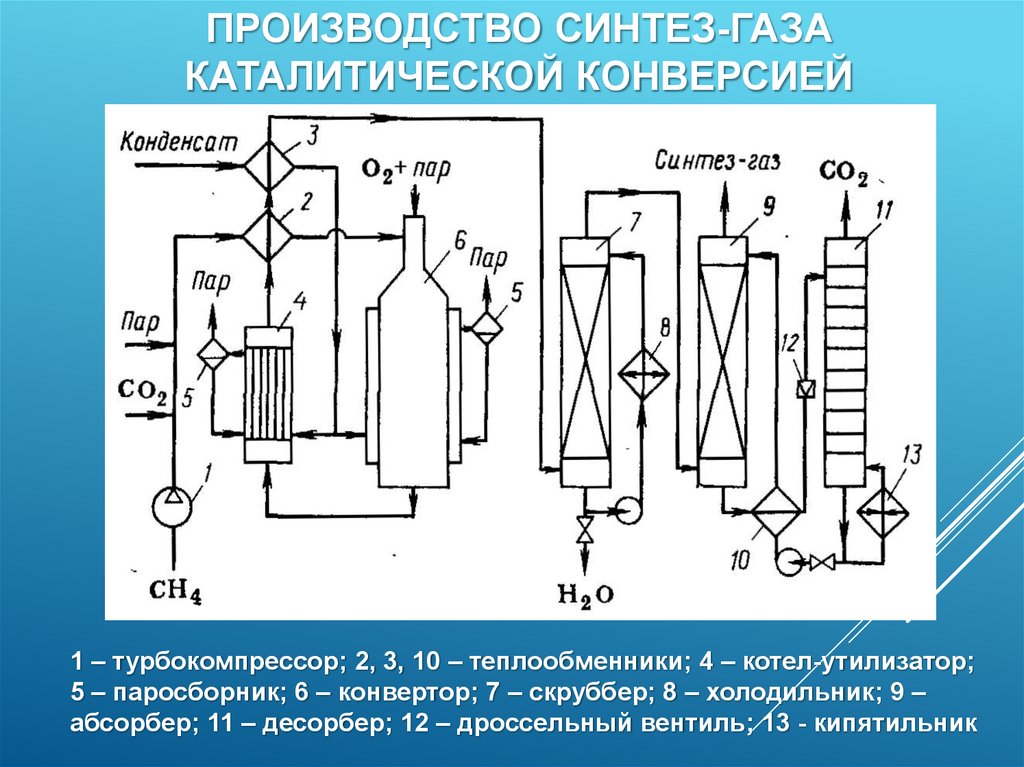
63.
ПРОИЗВОДСТВО СИНТЕЗ-ГАЗАКАТАЛИТИЧЕСКОЙ КОНВЕРСИЕЙ
1 – турбокомпрессор; 2, 3, 10 – теплообменники; 4 – котел-утилизатор;
5 – паросборник; 6 – конвертор; 7 – скруббер; 8 – холодильник; 9 –
абсорбер; 11 – десорбер; 12 – дроссельный вентиль; 13 - кипятильник
64.
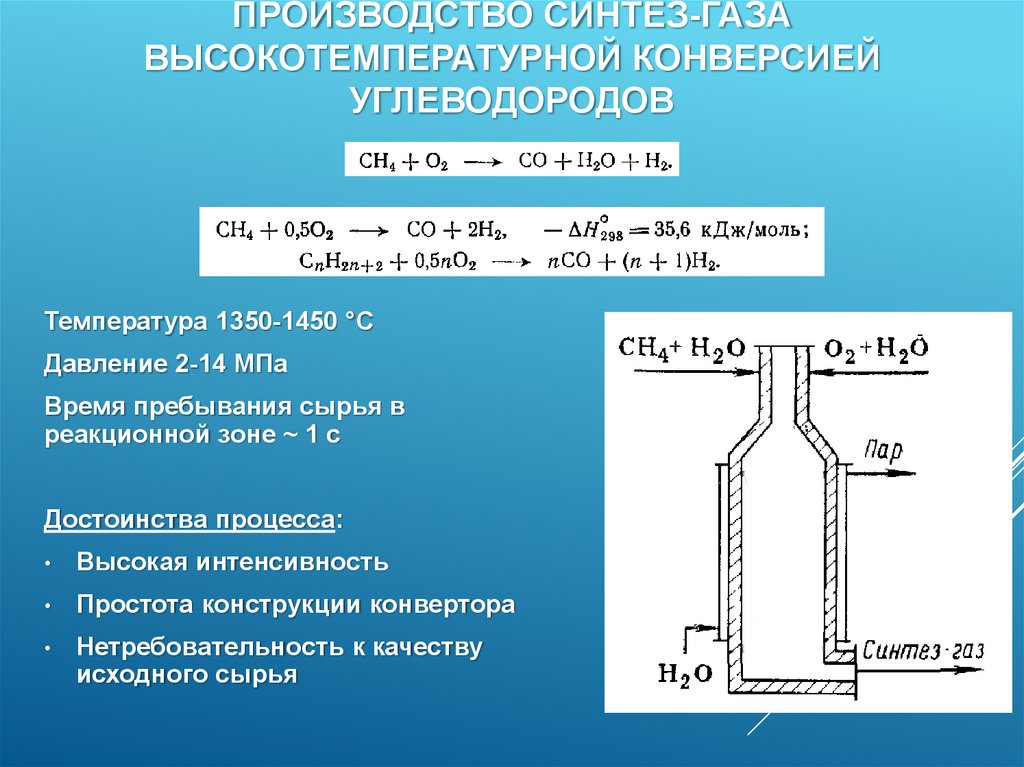
ПРОИЗВОДСТВО СИНТЕЗ-ГАЗАВЫСОКОТЕМПЕРАТУРНОЙ КОНВЕРСИЕЙ
УГЛЕВОДОРОДОВ
Температура 1350-1450 °С
Давление 2-14 МПа
Время пребывания сырья в
реакционной зоне ~ 1 c
Достоинства процесса:
Высокая интенсивность
Простота конструкции конвертора
Нетребовательность к качеству
исходного сырья
65.
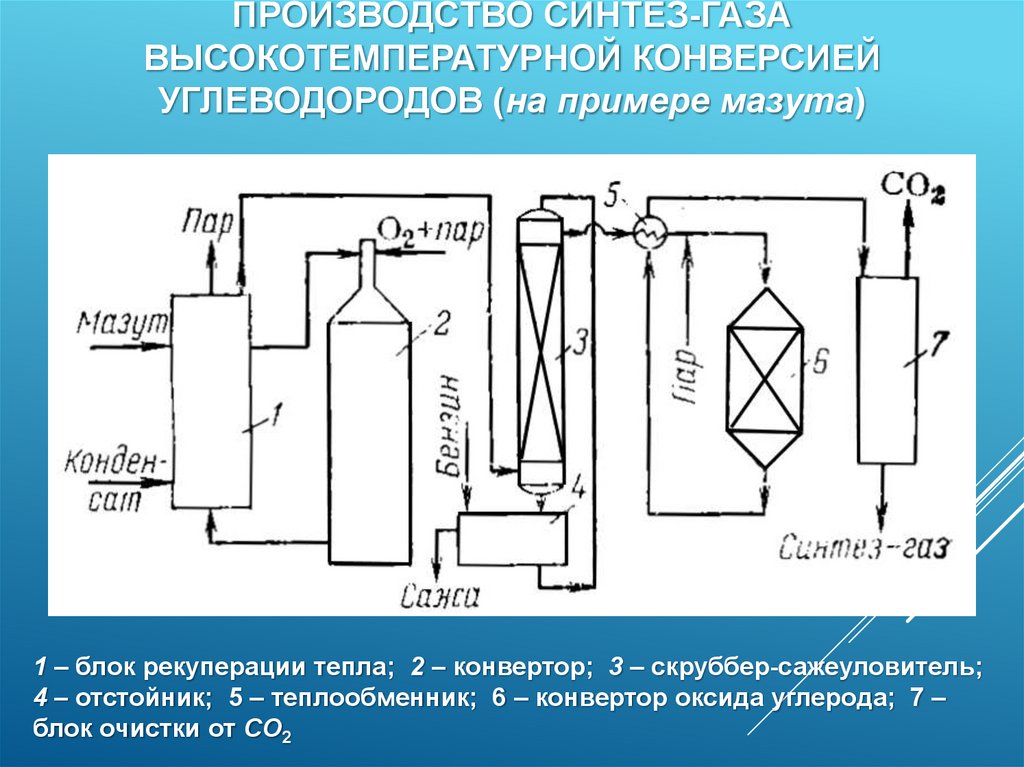
ПРОИЗВОДСТВО СИНТЕЗ-ГАЗАВЫСОКОТЕМПЕРАТУРНОЙ КОНВЕРСИЕЙ
УГЛЕВОДОРОДОВ (на примере мазута)
1 – блок рекуперации тепла; 2 – конвертор; 3 – скруббер-сажеуловитель;
4 – отстойник; 5 – теплообменник; 6 – конвертор оксида углерода; 7 –
блок очистки от СО2























 Химия
Химия Промышленность
Промышленность








