Похожие презентации:
Классификация двойных систем (лекция 6)
1.
12.
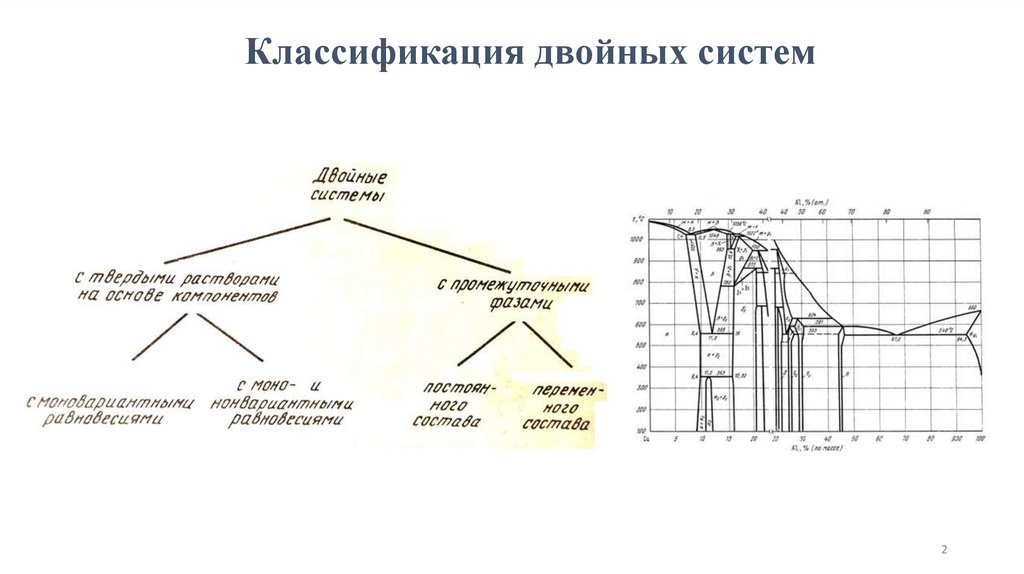
Классификация двойных систем2
3.
Двойные системы с моновариантными двухфазными равновесиямиC=k-f+1
L↔α
f= 2
α↔β
α1↔ α2
α ↔α’
3
4.
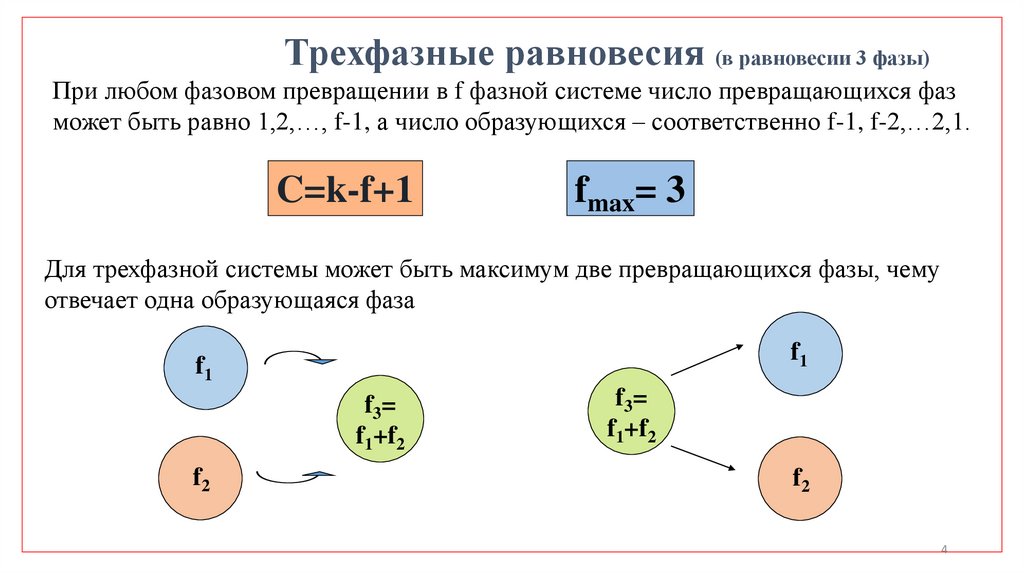
Трехфазные равновесия (в равновесии 3 фазы)При любом фазовом превращении в f фазной системе число превращающихся фаз
может быть равно 1,2,…, f-1, а число образующихся – соответственно f-1, f-2,…2,1.
C=k-f+1
fmax= 3
Для трехфазной системы может быть максимум две превращающихся фазы, чему
отвечает одна образующаяся фаза
f1
f1
f3=
f1+f2
f2
f3=
f1+f2
f2
4
5.
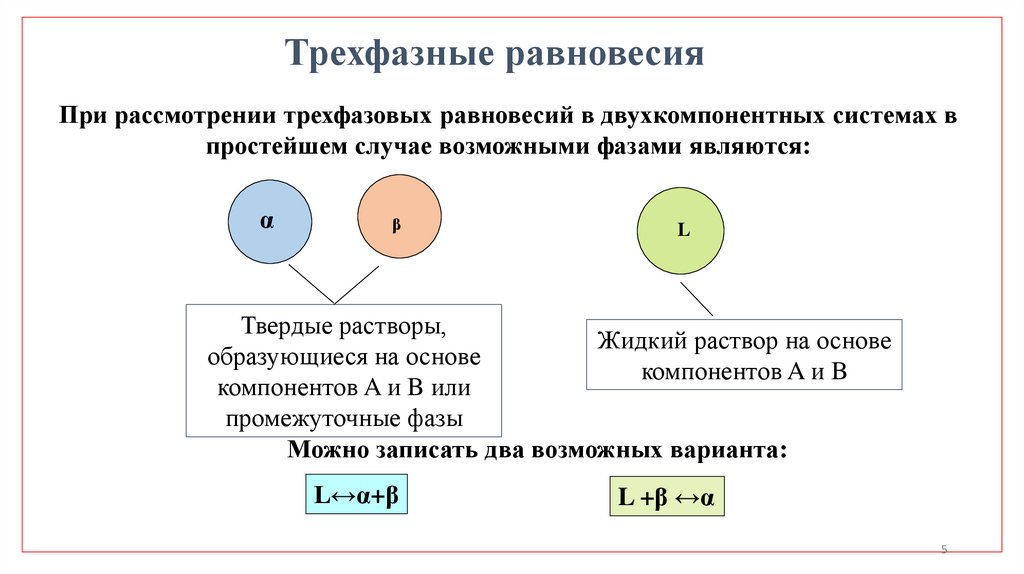
Трехфазные равновесияПри рассмотрении трехфазовых равновесий в двухкомпонентных системах в
простейшем случае возможными фазами являются:
α
β
L
Твердые растворы,
Жидкий раствор на основе
образующиеся на основе
компонентов A и B
компонентов A и B или
промежуточные фазы
Можно записать два возможных варианта:
L↔α+β
L +β ↔α
5
6.
Трехфазные равновесияL↔α+β
L +β ↔α
Эвтектическое равновесие
Перитектическое равновесие
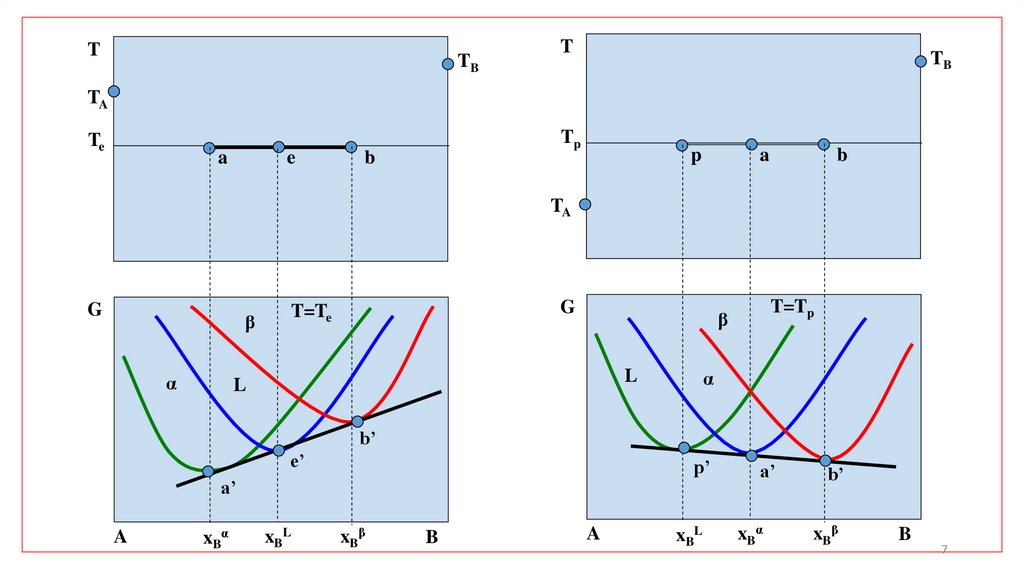
Из общего условия фазового равновесия для эвтектического и перитектического
превращений в системе A-B имеем:
A A
L
A
B B
L
B
Если взаимодействие атомов одного сорта в твердом растворе сильнее вз-я атомов
разного сорта, то непрерывный ряд твердых растворов существовать не может,
система относится к эвтектическому или перитектическому типу
6
7.
TTB
T
TB
TA
Te
a
e
Tp
b
p
a
b
TA
G
β
α
G
T=Te
T=Tp
β
α
L
L
b’
e’
a’
A
xBα
xBL
xBβ
B
A
p’
a’
b’
xBL
xBα
xBβ
B
7
8.
Трехфазное эвтектическое равновесие является сочетанием трехдвухфазных равновесий
L↔α
L↔β
α↔β
Эвтектическую горизонталь можно рассматривать как совокупность
трех конод, символизирующих наличие трех указанных двухфазных
равновесий
8
9.
Трехфазная реакция, в которой участвуют три фазы, всегда протекает припостоянной температуре и постоянном составе фаз. Возможны только два варианта:
- одна фаза распадается на две другие фазы крайних на горизонтали составов – это
реакция эвтектического типа;
F1↔F2+F3
К эвтектическому типу относятся следующие
реакции:
- эвтектическая L↔α+β;
- эвтектоидная γ↔α+β;
- монотектическая L1↔L2+α;
- монотектоидная γ1↔γ2+α;
- метатектическая (кататектическая) γ↔α+L;
9
10.
- при взаимодействии двух крайних на горизонтали фаз образуется третья,промежуточная по составу фаза – это реакция перитектического типа.
F1 +F2 ↔F3
К перитектическому типу относятся следующие
реакции:
- перитектическая α+ L↔β;
- перитектоидная γ + α ↔β;
- синтектическая L1 + L2↔α.
Любое из приведенных трехфазных равновесий может рассматриваться как сочетание
двухфазных равновесий: F1↔F2; F1↔F3; F2↔F3
10
11.
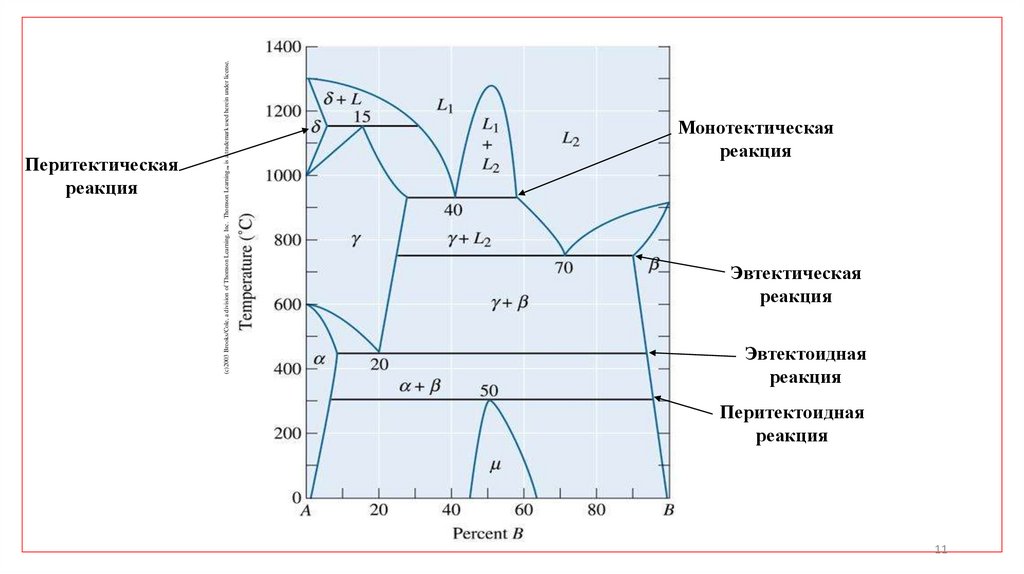
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein under license.Перитектическая
реакция
Монотектическая
реакция
Эвтектическая
реакция
Эвтектоидная
реакция
Перитектоидная
реакция
11
12.
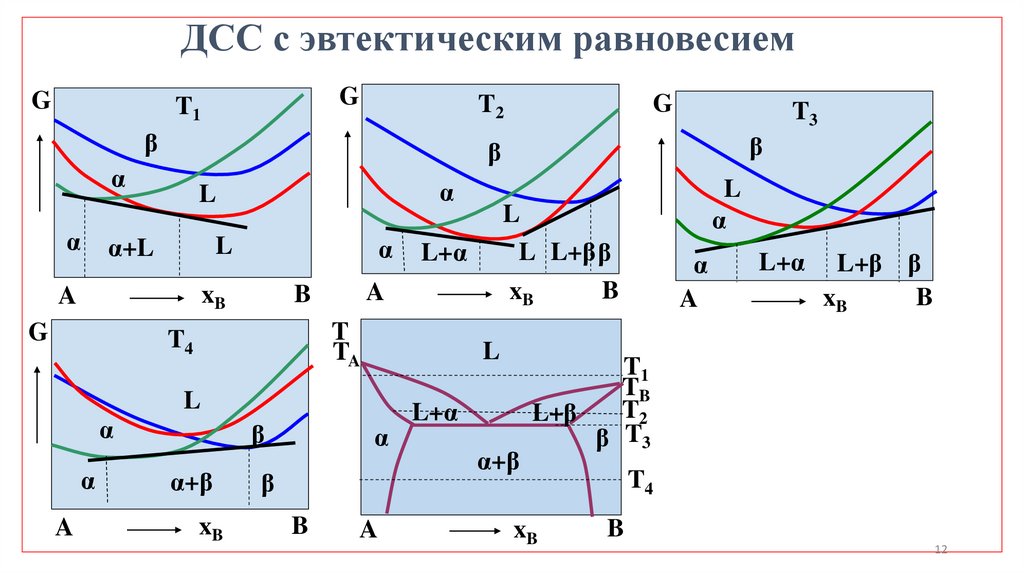
ДСС с эвтектическим равновесиемG
G
T1
β
α
L
α+L
α
L
xB
L
L
α
A
L+α
T
TA
T4
α
β
β
α+β
xB
α
β
B
A
L
α
L
L L+β β
A
B
xB
A
G
T3
β
α
α
G
T2
L+α
α+β
α
A
B
L+α
L+β β
B
xB
T1
TB
T2
L+β
β T3
xB
T4
B
12
13.
ДСС с эвтектическим равновесиемT
TA
k
a
TB
L
L+A
m
L+B
n
e
b
A+B
p
g
A
xB
B
Структурные составляющие это те структурно однородные
элементы, из которых состоит
сплав.
Рассмотрим диаграмму состояния сплава с
эвтектическим равновесием.
Сплав обладает полной взаимной растворимостью
в жидком состоянии.
В твердом состоянии растворимость отсутствует.
L↔A+B
Следует запомнить, что:
1. Состав эвтектики всегда постоянен.
2. Выше линии эвтектики состав жидкой фазы
определяется линией ликвидуса, а состав
твердой фазы постоянен.
3. Есть отличие между понятиями «фаза» и
«структурная составляющая».
13
14.
ДСС с эвтектическим равновесиемT
TA
k
a
0
1
L+A
m
2
p
L
n
e
A+B
h
A
3
xB
В точке 2 в равновесии находится 3 фазы: L, A, B
В интервале 2-3 в равновесии находится 2 фазы: А и B
L
0-1 охлаждение жидкого сплава
1-2 начало кристаллизации с
L+B
b выделением кристаллов A
Точка m. Каков вес жидкой и твердой фаз?
L
km
количество фазы L в точке m Lm
g
kn
mn
A
Am
B
т. 2 трехфазное равновесие L→A+B
жидкость перешла в мелкодисперсную фазу
A+B
2-3 охлаждение твердого сплава
В т. 3 фазы A и B
структурные составляющие A и эвт(А+B)
kn
a2
эвт( A B) 2
ae
2e
A2
ae
количество
структурной
составляющей
эвтектики
14
15.
Диаграмма состояния эвтектического типаСОЛЬВУС – [solvus] — графическое изображение (линия, поверхность)
на диаграмме состояния зависимости температуры растворимости элемента
в твердом растворе от химического состава
Доэвтектические сплавы – сплавы, имеющие в своем составе эвтектику,
любой сплав, чей состав имеет избыток основного металла по сравнению с
составом эвтектики и чья равновесная микроструктура содержит некоторое
количество эвтектической структуры.
Заэвтектический сплав - сплав, имеющий в своем составе эвтектику,
любой сплав, состав которого имеет избыток легирующего элемента по
сравнению с составом эвтектики и чья равновесная микроструктура
содержит некоторое количество эвтектической структуры.
16.
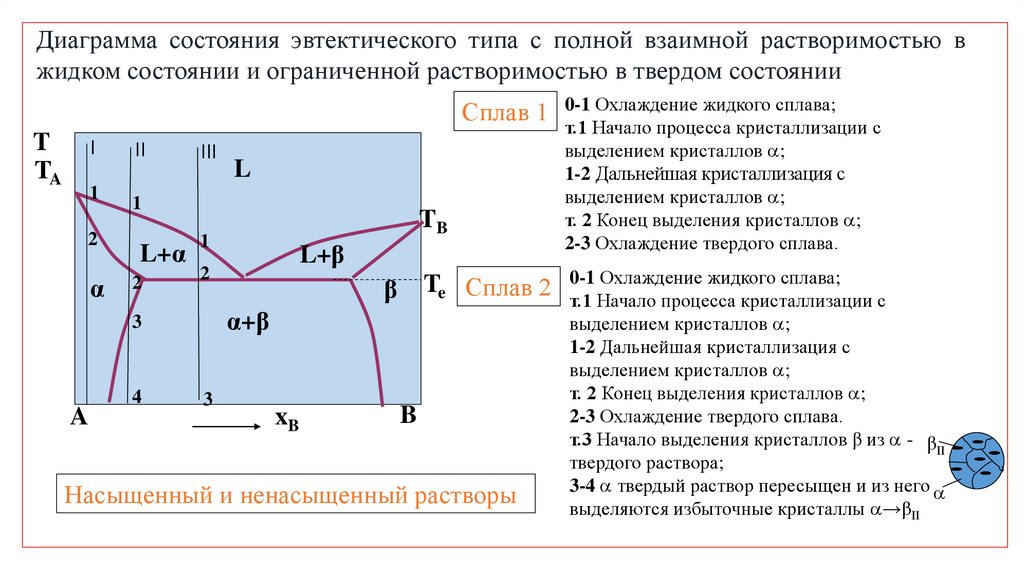
Диаграмма состояния эвтектического типа с полной взаимной растворимостью вжидком состоянии и ограниченной растворимостью в твердом состоянии
Сплав 1 0-1 Охлаждение жидкого сплава;
T
TA
I
1
2
α
II
III
1
L+α
2
4
TB
1
L+β
2
β Te Сплав 2
α+β
3
A
L
3
xB
B
Насыщенный и ненасыщенный растворы
т.1 Начало процесса кристаллизации с
выделением кристаллов ;
1-2 Дальнейшая кристаллизация с
выделением кристаллов ;
т. 2 Конец выделения кристаллов ;
2-3 Охлаждение твердого сплава.
0-1 Охлаждение жидкого сплава;
т.1 Начало процесса кристаллизации с
выделением кристаллов ;
1-2 Дальнейшая кристаллизация с
выделением кристаллов ;
т. 2 Конец выделения кристаллов ;
2-3 Охлаждение твердого сплава.
т.3 Начало выделения кристаллов β из - βII
твердого раствора;
3-4 твердый раствор пересыщен и из него
выделяются избыточные кристаллы →βII
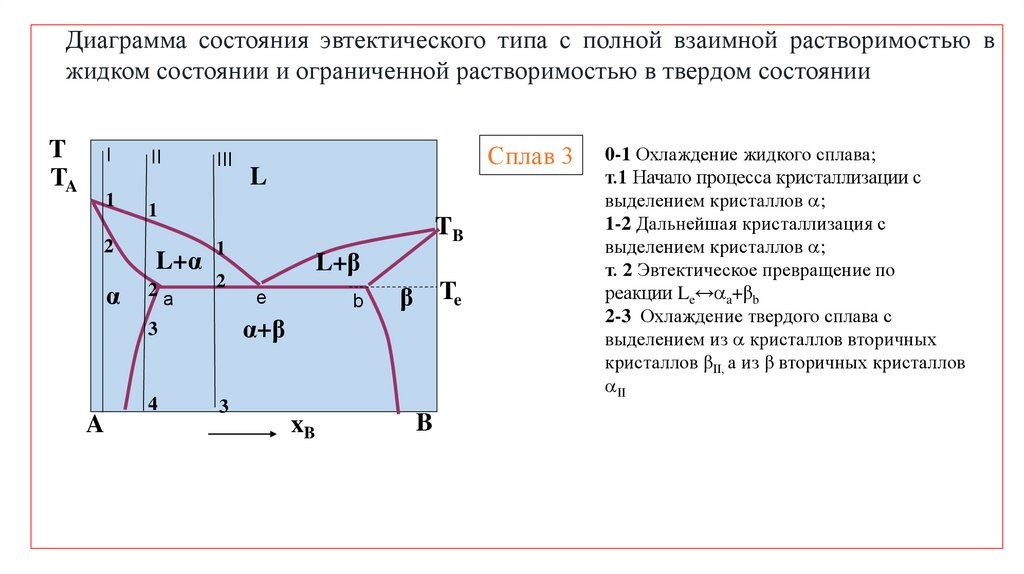
17.
Диаграмма состояния эвтектического типа с полной взаимной растворимостью вжидком состоянии и ограниченной растворимостью в твердом состоянии
T
TA
I
1
2
α
II
III
L
1
L+α
2a
4
TB
1
2
L+β
e
b
β Te
α+β
3
A
Сплав 3
3
xB
B
0-1 Охлаждение жидкого сплава;
т.1 Начало процесса кристаллизации с
выделением кристаллов ;
1-2 Дальнейшая кристаллизация с
выделением кристаллов ;
т. 2 Эвтектическое превращение по
реакции Le↔ a+βb
2-3 Охлаждение твердого сплава с
выделением из кристаллов вторичных
кристаллов βII, а из β вторичных кристаллов
II
18.
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein under license.19.
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein underlicense.
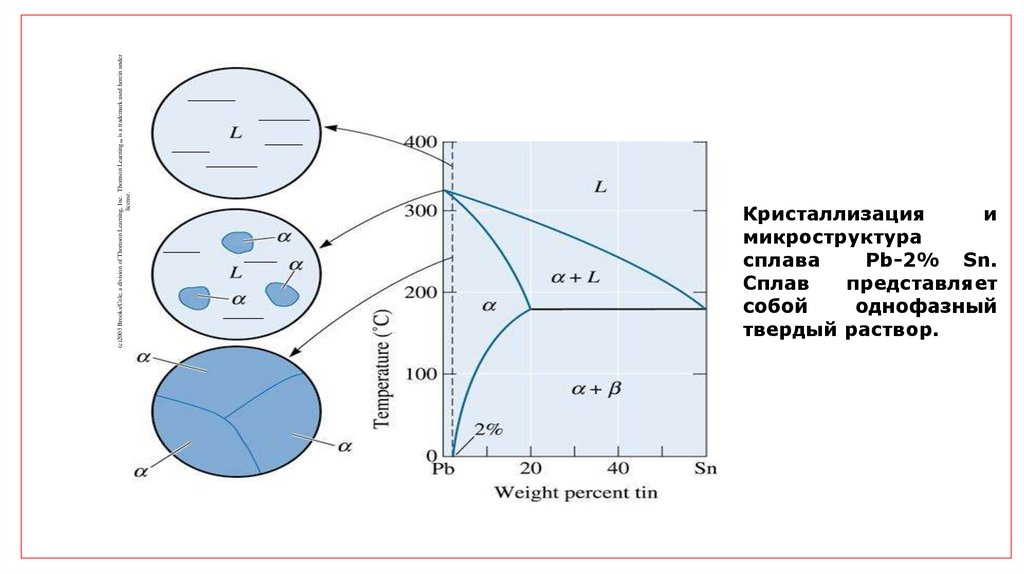
Кристаллизация
и
микроструктура
сплава
Pb-2% Sn.
Сплав
представляет
собой
однофазный
твердый раствор.
20.
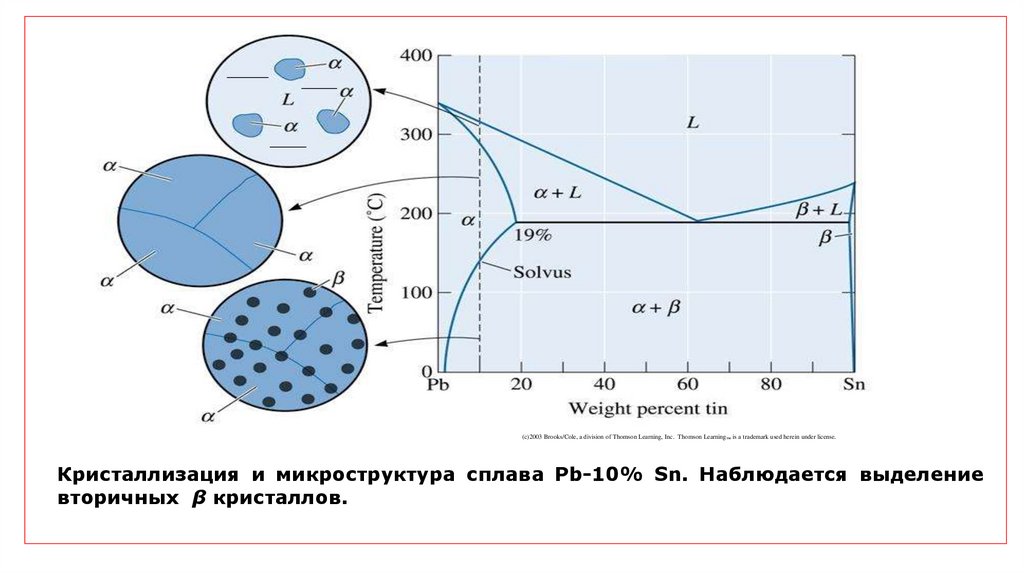
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein under license.Кристаллизация и микроструктура сплава Pb-10% Sn. Наблюдается выделение
вторичных β кристаллов.
21.
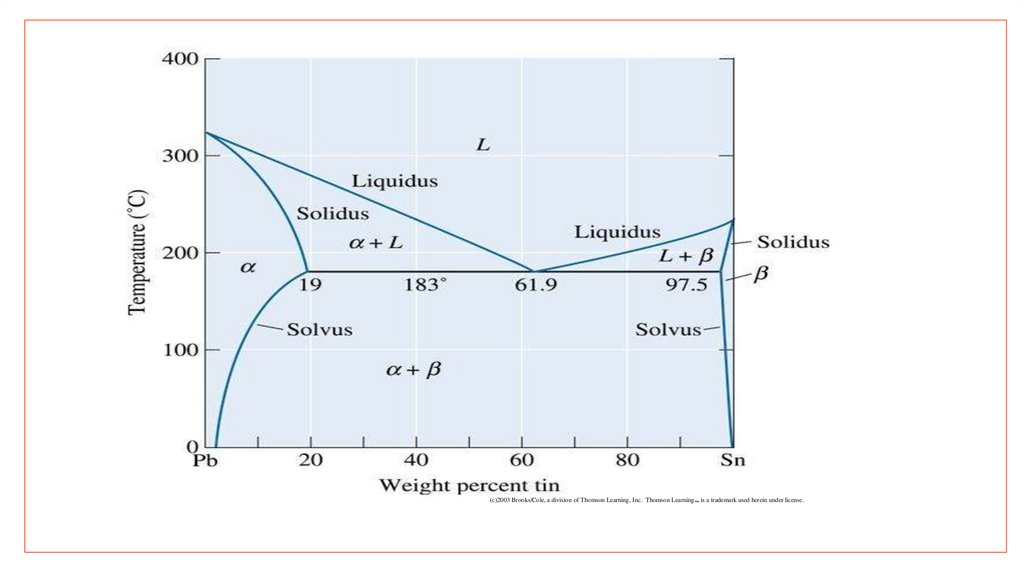
Задача 1Фазовая диаграмма Pb-Sn
Определить : (a) растворимость олова в твердом свинце при 100oC, (b)
максимальную растворимость свинца в твердом олове, (c) количество
бета фазы, которая формируется если сплав Pb-10% Sn охлаждается до
0o C, (d) массу олова, содержащегося в α и β фазе.
Предполагается, что общая масса сплава Pb-10% Sn - 100 грамм.
22.
Решение поставленной задачи:a) При температуре 100oC линия сольвуса пересекается при 5% Sn. Следовательно,
растворимость олова (Sn) в свинце (Pb) при 100oC составляет 5%.
b) Максимальная растворимость свинца (Pb) в олове (Sn), которая определяется по
стороне фазовой диаграммы богатой оловом, наблюдается при эвтектической
температуре 183oC и составляет 97,5% Sn и соответственно 2,5%Pb.
(c) При температуре 0oC, сплав с 10% олова находится в двухфазной области α+β
фазовой диаграммы. Если нарисовать коноду при 0оС и применить правило рычага, мы
можем найти, что:
% 10 - 2 100 8.2%
100 - 2
23.
Продолжение решения(d) масса Sn в -фазе = 2% Sn х 91.8 г -фазы = 0.02 х91.8 г = 1,836 г. Поскольку олово
(Sn) появляется в обеих фазах и β, масса Sn в β-фазе будет = (10 – 1,836) г = 8,164 г.
Масса свинца (Pb) в -фазе = 98% Sn 91,8 г -фазы = 0,98 91,8 г = 89,964 г
Масса свинца (Pb) в β –фазе = 90 – 89,964 = 0.036 г.
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein under license.
24.
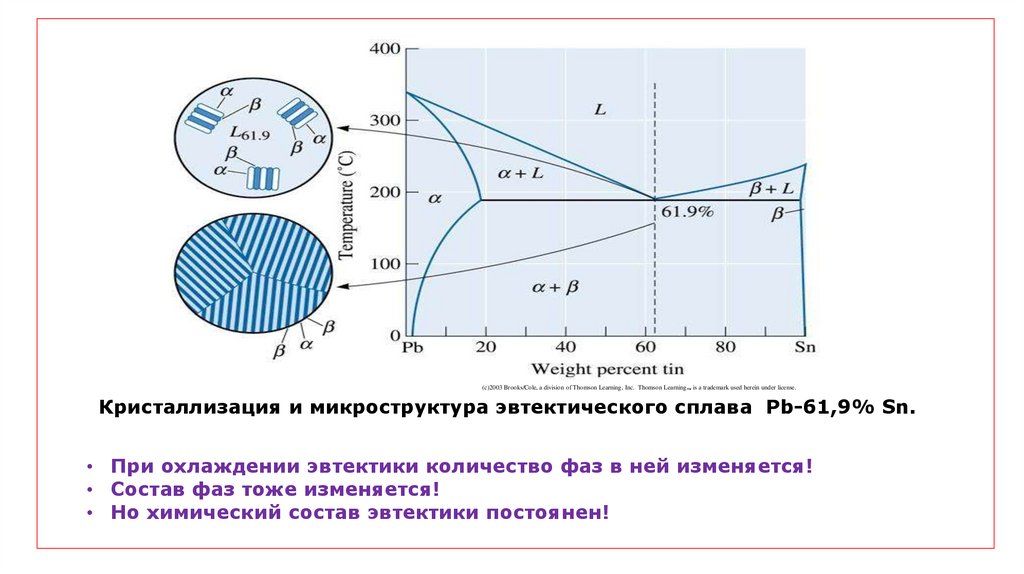
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein under license.Кристаллизация и микроструктура эвтектического сплава Pb-61,9% Sn.
• При охлаждении эвтектики количество фаз в ней изменяется!
• Состав фаз тоже изменяется!
• Но химический состав эвтектики постоянен!
25.
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used hereinunder license.
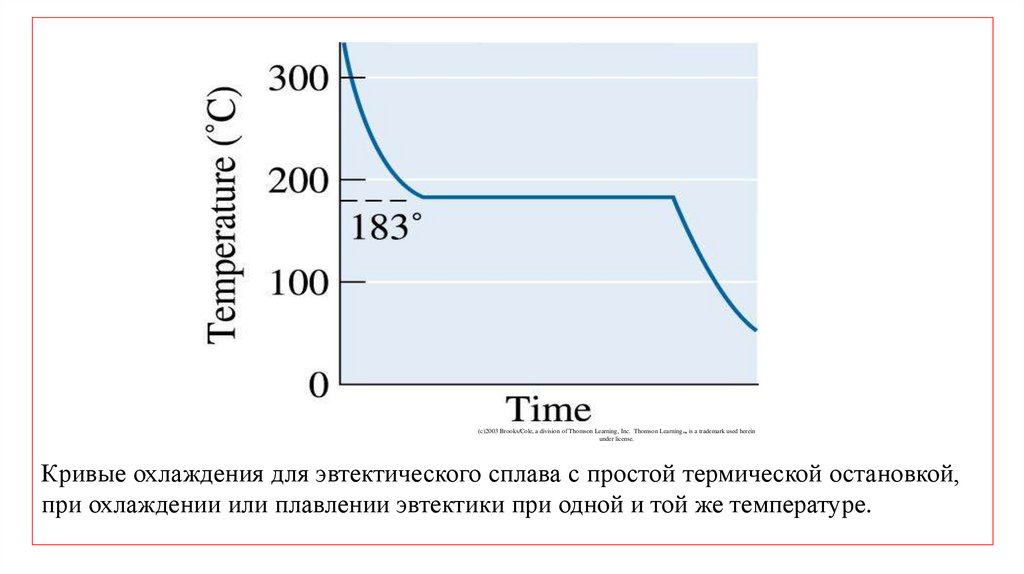
Кривые охлаждения для эвтектического сплава с простой термической остановкой,
при охлаждении или плавлении эвтектики при одной и той же температуре.
26.
Жидкость(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein under license.
(a) Перераспределение атомов в ходе роста пластин эвтектики свинец-олово. Атомы
олова из жидкости, предпочтительно диффундируют к площадке β-фазы, а атомы
свинца диффундируют к площадке -фазы. (b). Микрофотография структуры
эвтектики свинец-олово (x400).
27.
Рост эвтектики – совместный кооперативныйрост двух взаимопереплетенных кристаллов
разных фаз
1. Эвтектическая колония – это взаимно проросшие, сильно разветвленные
кристаллы разных фаз. Каждая колония представляет собой двухфазный
бикристалл, то есть сросток двух разветвленных кристаллов разных фаз.
2. Каждая колония растет из своего центра.
3. Зарождение колонии инициирует базовая фаза, характеризуемая большей долей
направленных межатомных связей. Вторая фаза растет на базовой как на
подкладке.
В жидкости перед растущим бикристаллом очень быстро протекает
разделительная диффузия: перемещение атомов к разным фазам.
28.
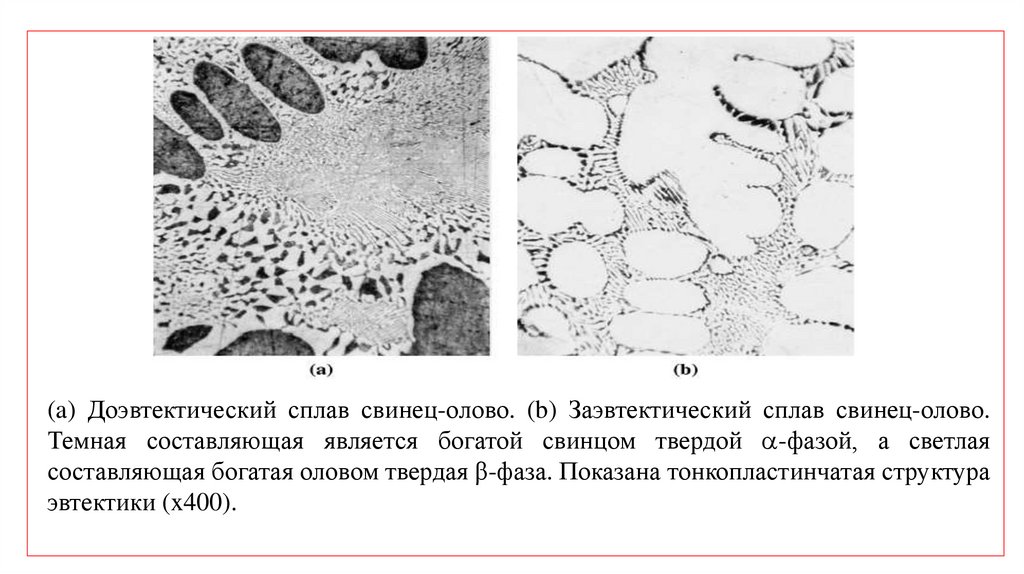
(a) Доэвтектический сплав свинец-олово. (b) Заэвтектический сплав свинец-олово.Темная составляющая является богатой свинцом твердой -фазой, а светлая
составляющая богатая оловом твердая β-фаза. Показана тонкопластинчатая структура
эвтектики (x400).
29.
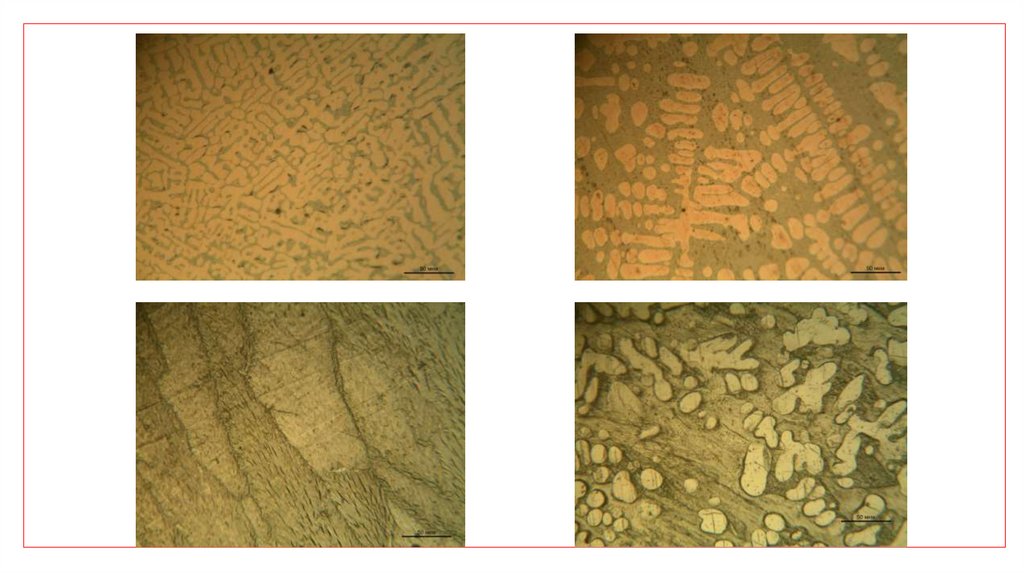
ПластинчатаяЗернистая
Скелетная
Игольчатая
Шлиф – это произвольное плоское сечение объемной структуры. Нужно делать осторожно выводы о
реальной пространственной структуре эвтектики по единичным сечениям!
30.
3031.
32.
33.
34.
Задача 2.Определение количества фаз в эвтектическом сплаве
(a) Определите количество и состав каждой фазы в сплаве свинец-олово
эвтектического состава. (b) Рассчитайте массу фаз.
(c) Рассчитайте количество свинца и олова в каждой фазе, предполагая, что у вас есть
по 200 г сплава.
35.
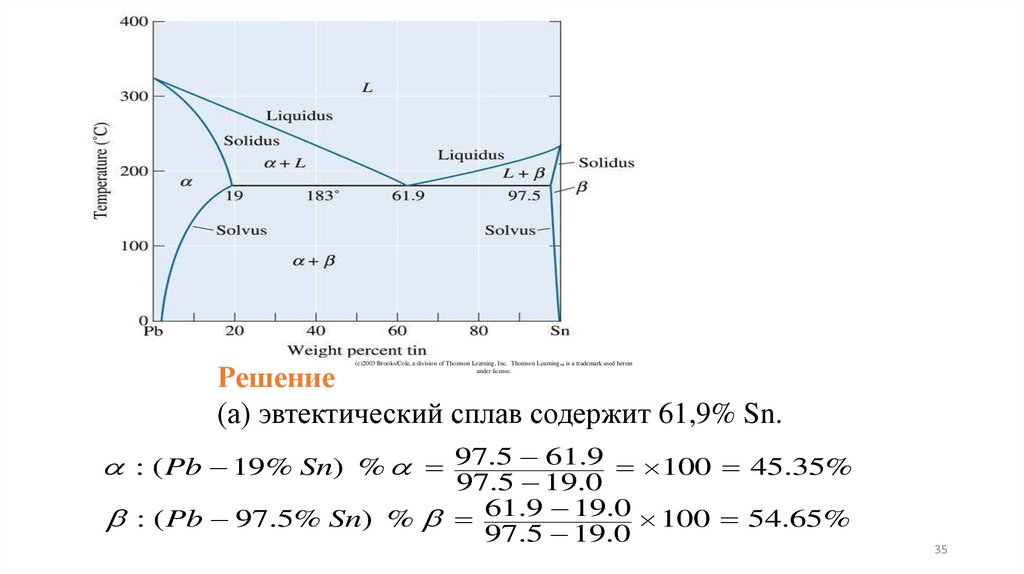
Решение(а) эвтектический сплав содержит 61,9% Sn.
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein
under license.
: ( Pb 19% Sn) % 97.5 61.9 100 45.35%
97.5 19.0
: ( Pb 97.5% Sn) % 61.9 19.0 100 54.65%
97.5 19.0
35
36.
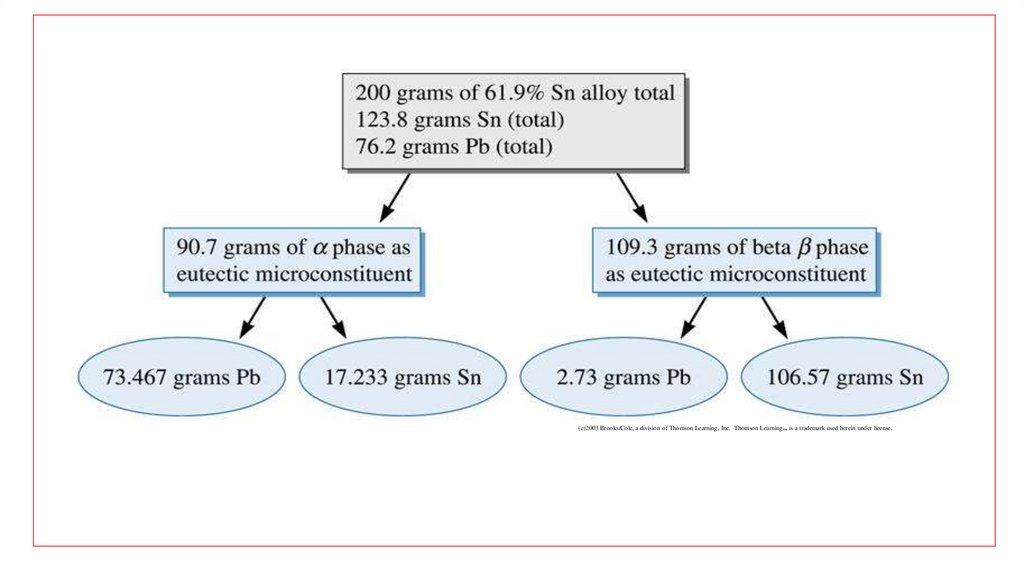
Продолжение решения(b) При температуре чуть ниже эвтектической:
Масса -фазы в 200 г сплава
= масса сплава х часть фазы = 200 г х 0,4535 = 90,7 г
Количество β-фазы в 200 г сплава (масса сплава х масса фазы) =
200,0 г х 90,7 г = 109,3 г
(c) Масса Pb в α фазе = масса фазы в 200 г (концентрация Pb в α) = (90,7 г) (1 –
0,190) = 73,467 г
Масса Sn в α фазе = масса фазы – масса Pb в фазе = (90,7 – 73,467 г) = 17,233 г
Масса Pb в β фазе = масса β фазы в 200 г (весовое количество Pb в β) = (109,3 г)
(1 – 0,975) = 2.73 г
Масса Sn в β фазе = полная масса Sn – масса Sn в α фазе = 123,8 г – 17,233 г =
106,57 г
37.
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein under license.38.
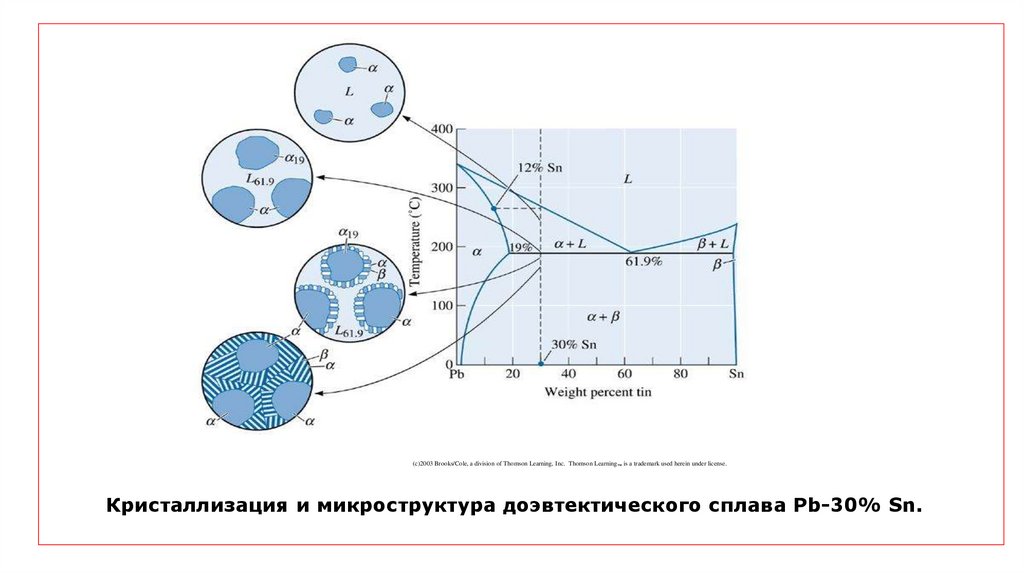
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein under license.Кристаллизация и микроструктура доэвтектического сплава Pb-30% Sn.
39.
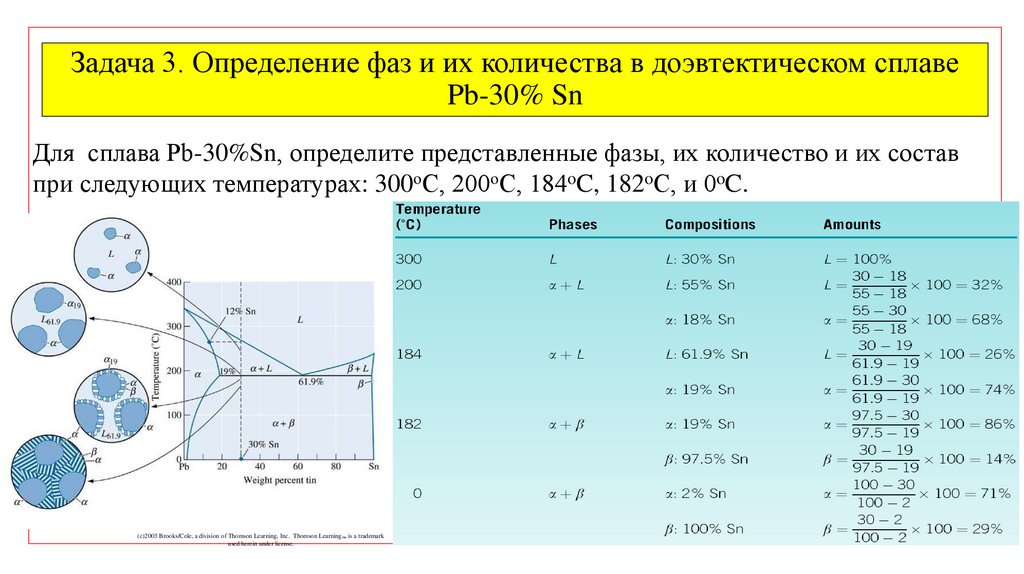
Задача 3. Определение фаз и их количества в доэвтектическом сплавеPb-30% Sn
Для сплава Pb-30%Sn, определите представленные фазы, их количество и их состав
при следующих температурах: 300оС, 200оС, 184oC, 182oC, и 0oC.
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark
used herein under license.
40.
Задача 4. Определение количества микрокомпонентов и их состава длядоэвтектоидного сплава
Определить количество и состав каждого микрокомпонента в сплаве Pb-30% Sn до
того, как была завершена эвтектическая реакция.
Решение
При температуре чуть выше эвтектической 184oC - количество и состав двух фаз:
% 61.9 30 100 74% % первичные
61.9 19
L : 61.9% Sn % L 30 19 100 26% % эвтектика при 182o C
61.9 19
:19% Sn
41.
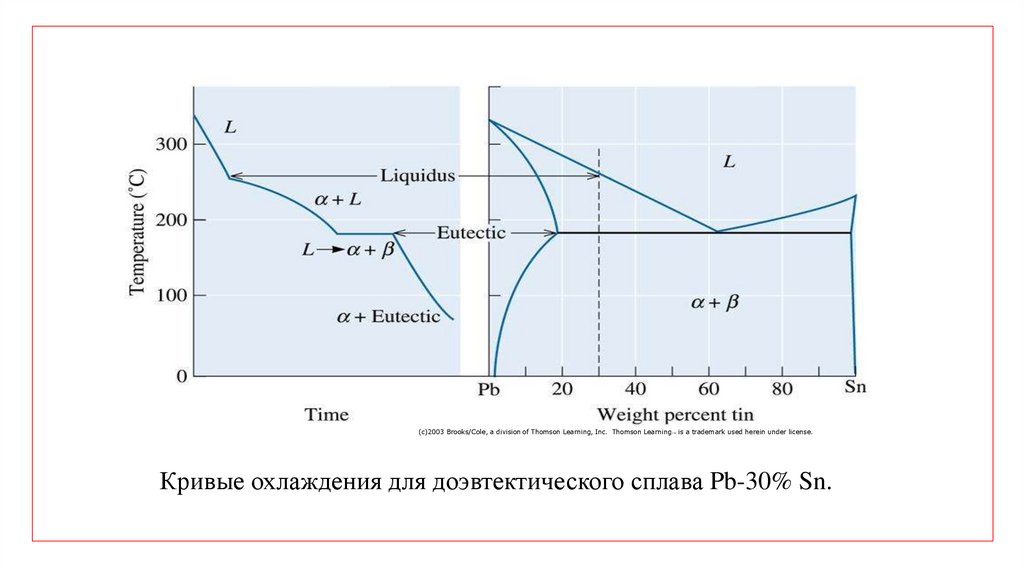
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning ™ is a trademark used herein under license.Кривые охлаждения для доэвтектического сплава Pb-30% Sn.
42.
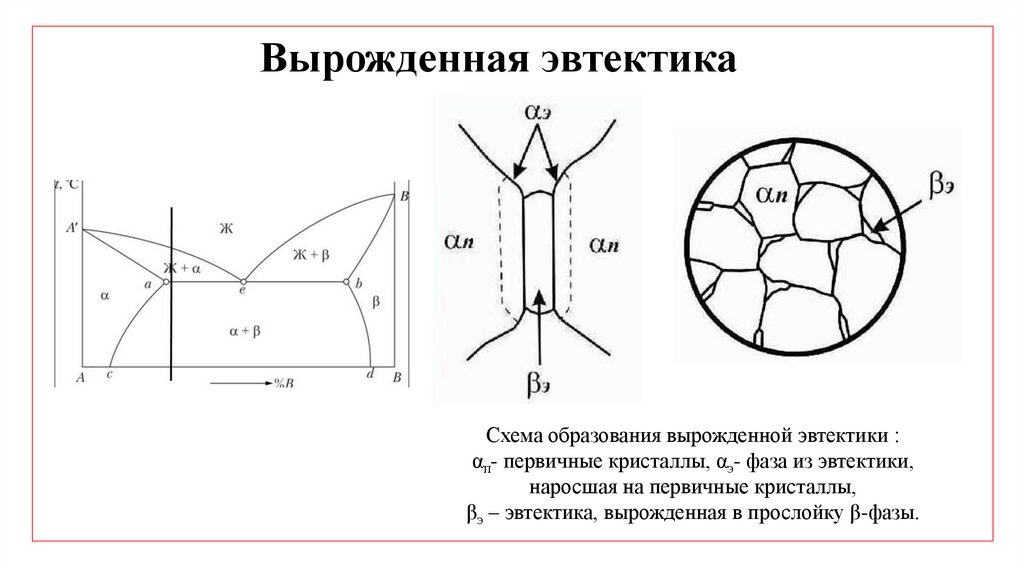
Вырожденная эвтектикаСхема образования вырожденной эвтектики :
αп- первичные кристаллы, αэ- фаза из эвтектики,
наросшая на первичные кристаллы,
βэ – эвтектика, вырожденная в прослойку β-фазы.
43.
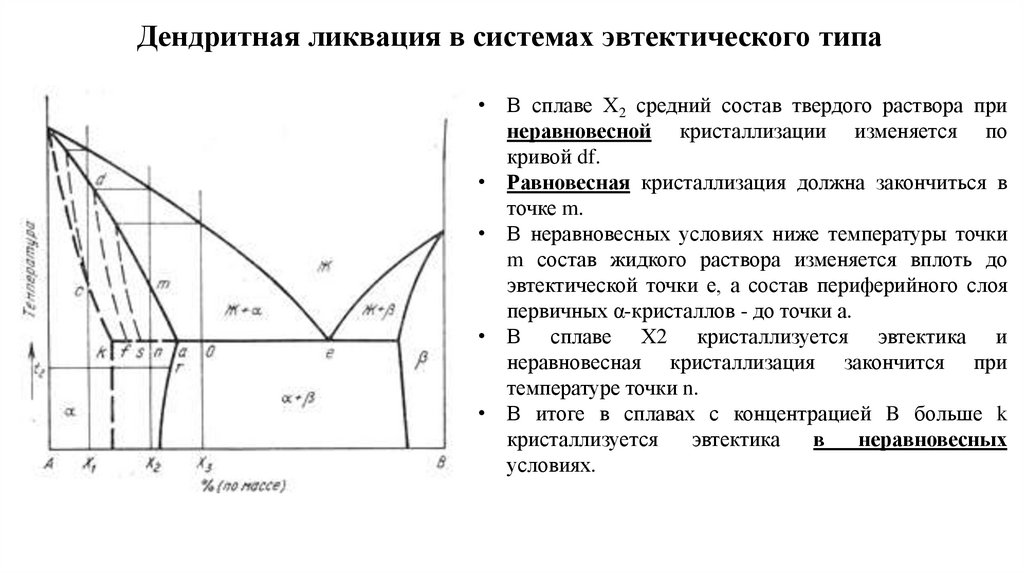
Дендритная ликвация в системах эвтектического типа• В сплаве Х2 средний состав твердого раствора при
неравновесной кристаллизации изменяется по
кривой df.
• Равновесная кристаллизация должна закончиться в
точке m.
• В неравновесных условиях ниже температуры точки
m состав жидкого раствора изменяется вплоть до
эвтектической точки е, а состав периферийного слоя
первичных α-кристаллов - до точки а.
• В сплаве Х2 кристаллизуется эвтектика и
неравновесная кристаллизация закончится при
температуре точки n.
• В итоге в сплавах с концентрацией B больше k
кристаллизуется
эвтектика
в
неравновесных
условиях.
44.
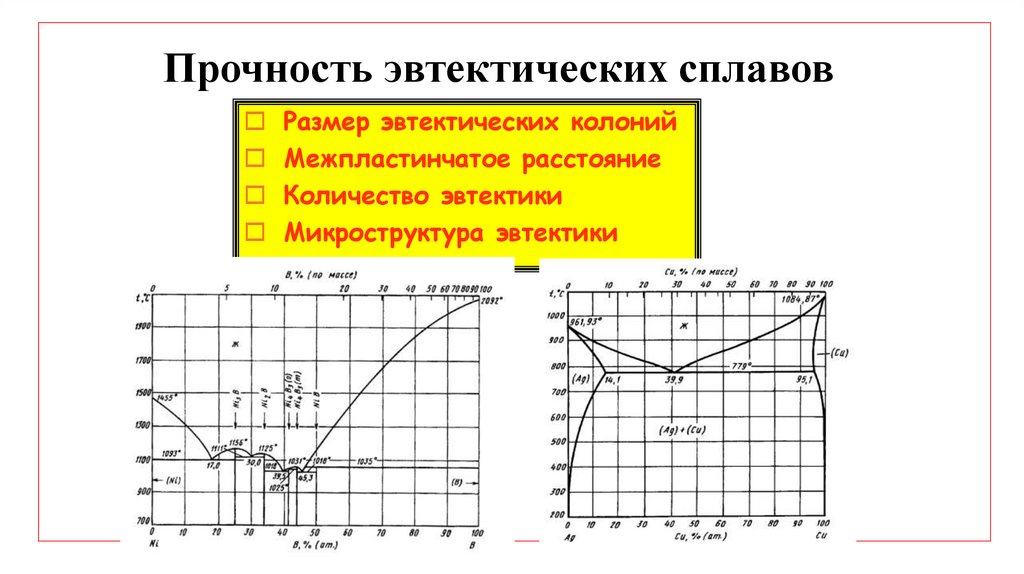
Прочность эвтектических сплавовРазмер эвтектических колоний
Межпластинчатое расстояние
Количество эвтектики
Микроструктура эвтектики
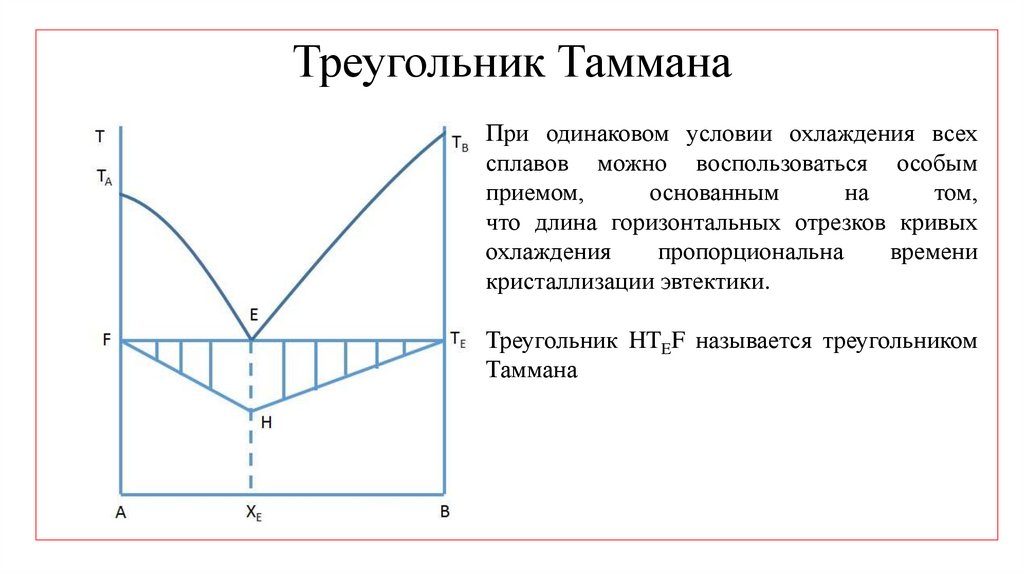
45. Треугольник Таммана
При одинаковом условии охлаждения всехсплавов можно воспользоваться особым
приемом,
основанным
на
том,
что длина горизонтальных отрезков кривых
охлаждения
пропорциональна
времени
кристаллизации эвтектики.
Треугольник HTEF называется треугольником
Таммана
46.
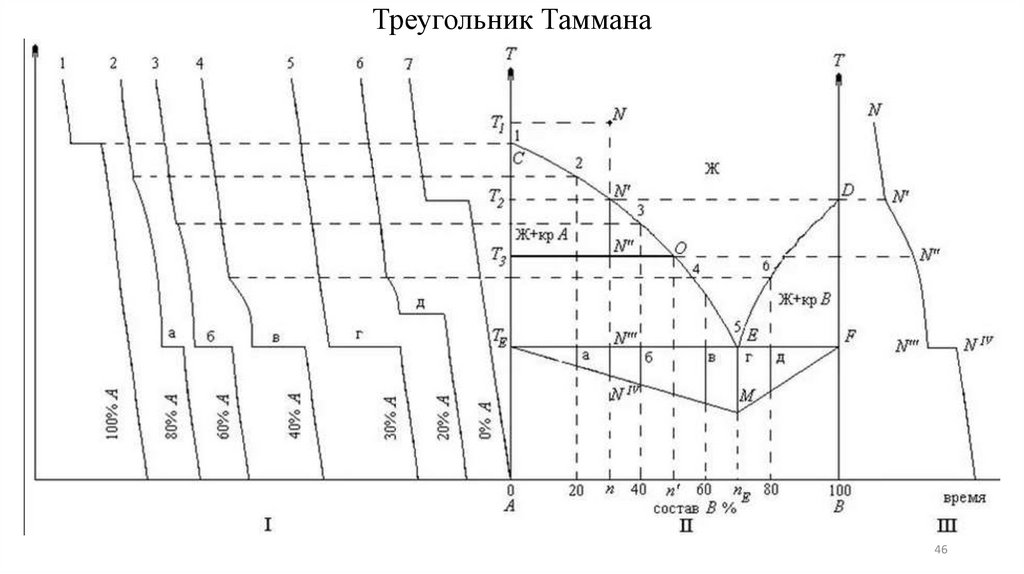
Треугольник Таммана46
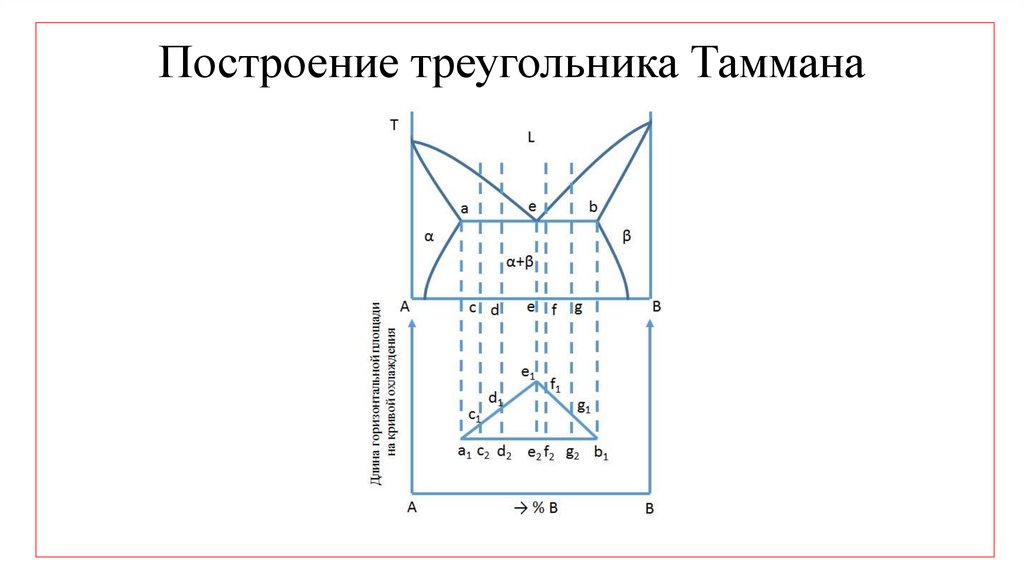
47. Построение треугольника Таммана
48. Для чего нужен треугольник Таммана?
Построение этого треугольника можноиспользовать для ускоренного определения
положения эвтектической точки e
на горизонтали ab и концов горизонтали a и b.
Точность построения зависит прежде
всего от количества исследованных
сплавов и аппаратурных условий
снятия их кривых охлаждения.
49.
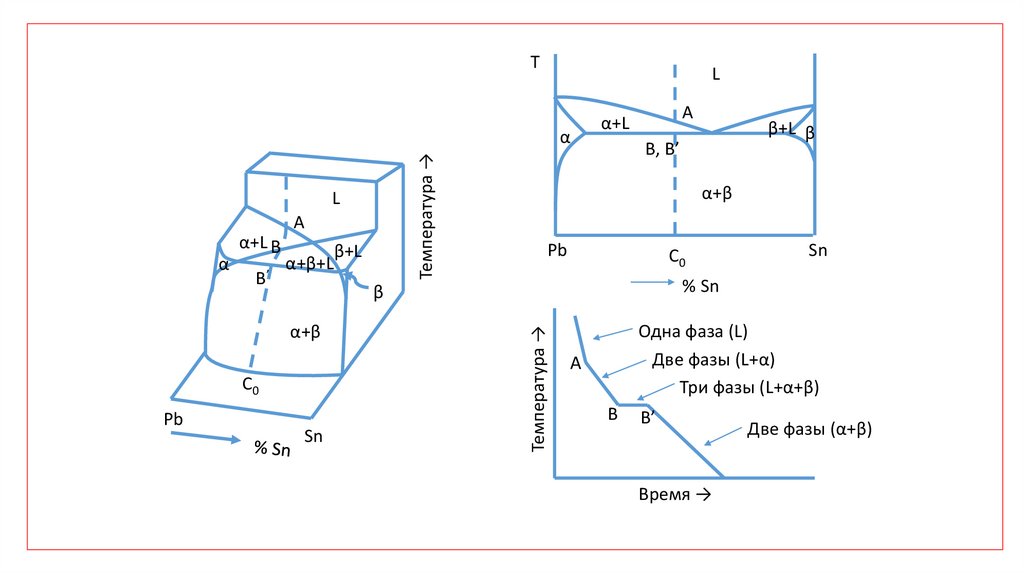
TL
Температура →
α
L
A
B’
β+L
α+β+L
C0
Pb
B, B’
Pb
C0
Sn
Sn
% Sn
β
α+β
β+L β
α+β
Температура →
α
α+L B
A
α+L
Одна фаза (L)
Две фазы (L+α)
Три фазы (L+α+β)
A
B
B’
Время →
Две фазы (α+β)
50.
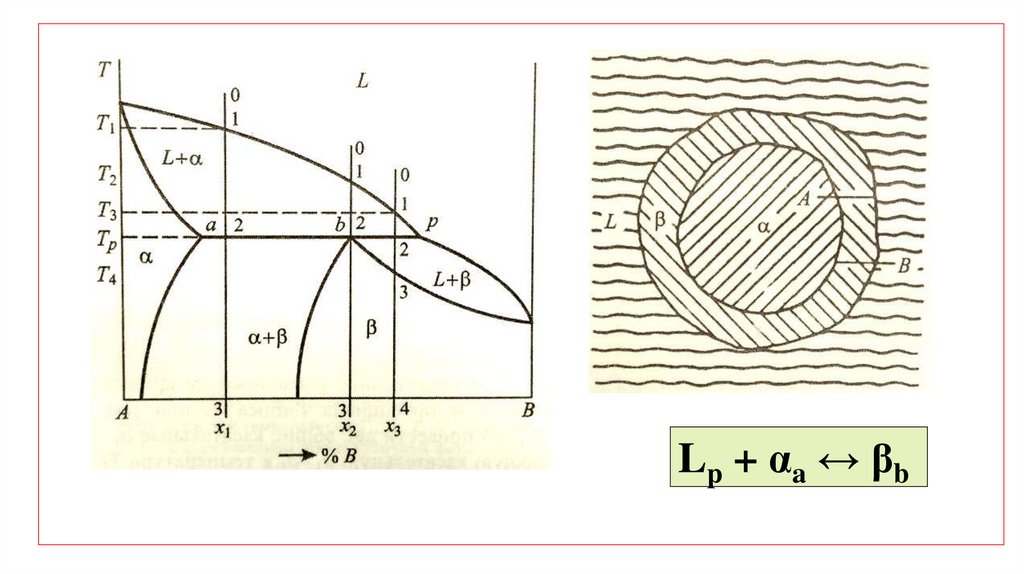
Lp + αa ↔ βb51.
5152.
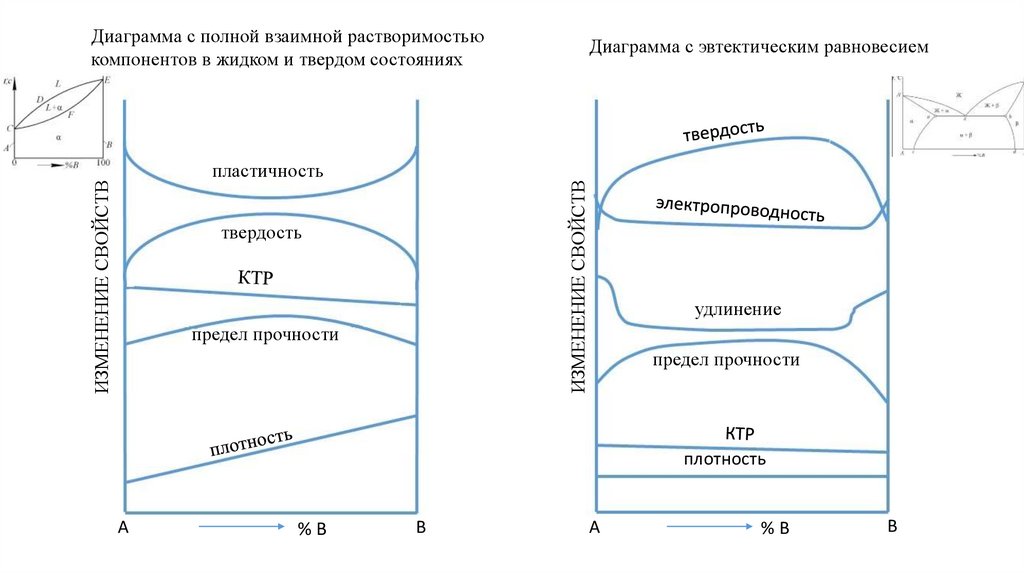
Диаграмма с полной взаимной растворимостьюкомпонентов в жидком и твердом состояниях
ИЗМЕНЕНИЕ СВОЙСТВ
ИЗМЕНЕНИЕ СВОЙСТВ
пластичность
Диаграмма с эвтектическим равновесием
твердость
предел прочности
удлинение
предел прочности
плотность
A
%B
B
A
%B
B
53.
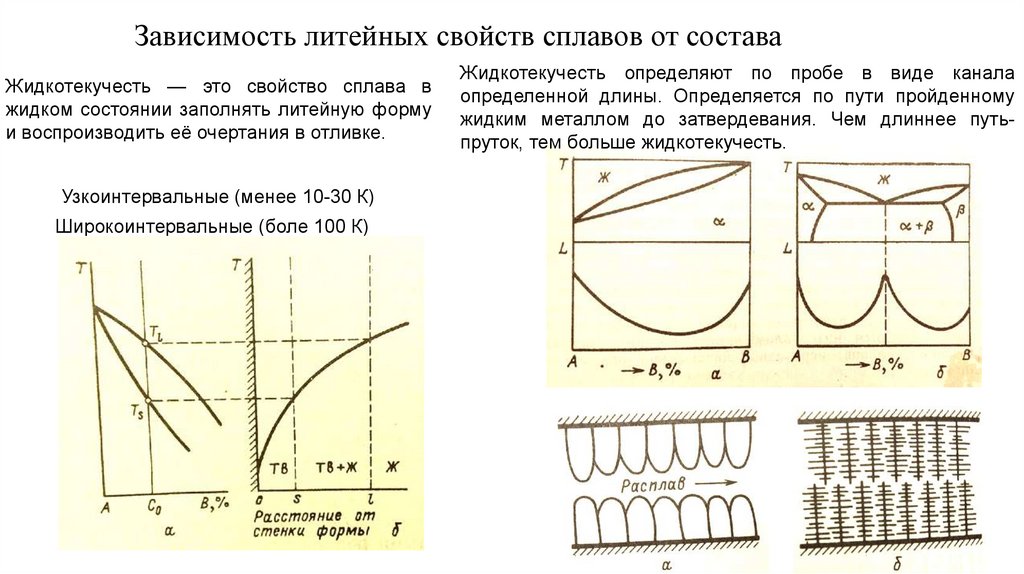
Зависимость литейных свойств сплавов от составаЖидкотекучесть — это свойство сплава в
жидком состоянии заполнять литейную форму
и воспроизводить её очертания в отливке.
Узкоинтервальные (менее 10-30 К)
Широкоинтервальные (боле 100 К)
Жидкотекучесть определяют по пробе в виде канала
определенной длины. Определяется по пути пройденному
жидким металлом до затвердевания. Чем длиннее путьпруток, тем больше жидкотекучесть.
54. ДСС с промежуточными фазами
Промежуточными фазами называют все твердые фазы, которые образуются в интервале концентрациймежду граничными твердыми растворами на основе компонентов А и В.
Если между компонентами А и В образуется химическое соединение AmBn, то оно обладает своей
кристаллической решеткой. То есть соединение можно рассматривать как самостоятельный
компонент, разделяющий данную систему на две подсистемы. В кристаллической решетке
промежуточной фазы можно выделить две подрешетки, каждая из которых образована атомами одного
сорта.
Промежуточные фазы могут иметь постоянный и переменный состав.
Промежуточные фазы постоянного состава имеют очень узкие области гомогенности (области
существования однородного твердого раствора на основе данного химического соединения) или их
отсутствие. Изображаются такие промежуточные фазы вертикальными линиями.
Промежуточные фазы переменного состава имеют широкую область гомогенности. Эти фазы
представляют твердые растворы на основе соединений.
55.
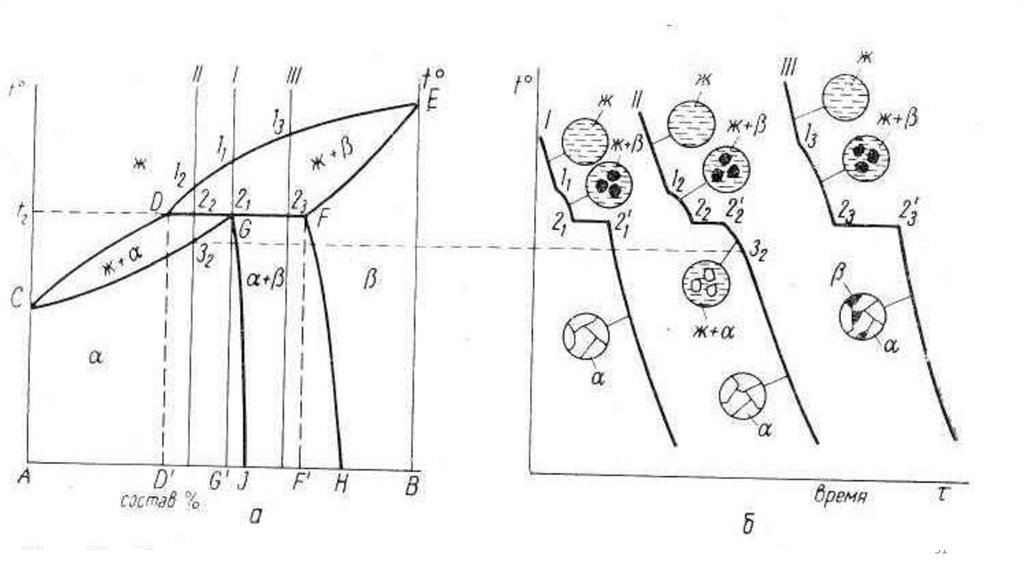
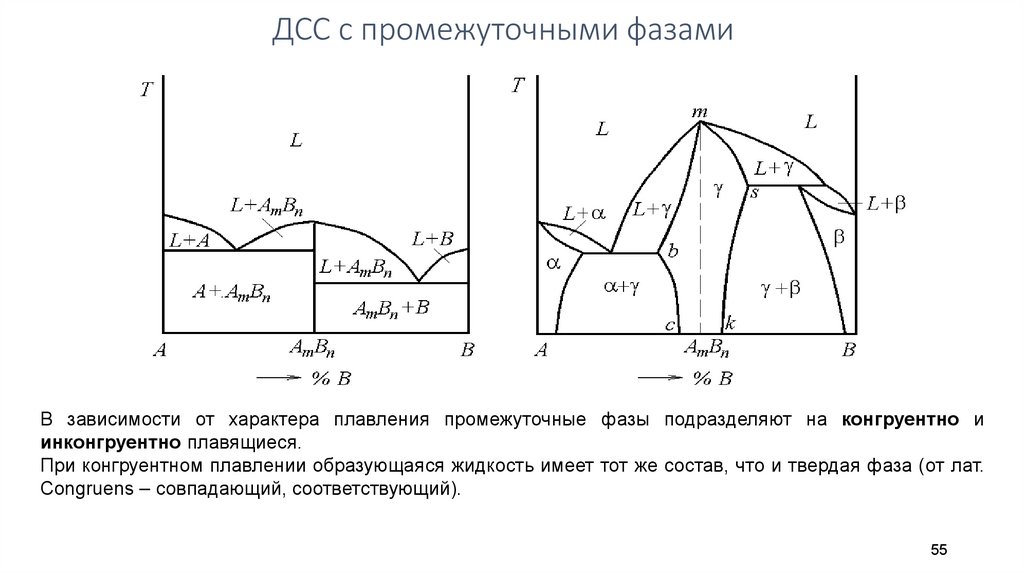
ДСС с промежуточными фазамиВ зависимости от характера плавления промежуточные фазы подразделяют на конгруентно и
инконгруентно плавящиеся.
При конгруентном плавлении образующаяся жидкость имеет тот же состав, что и твердая фаза (от лат.
Congruens – совпадающий, соответствующий).
55
56.
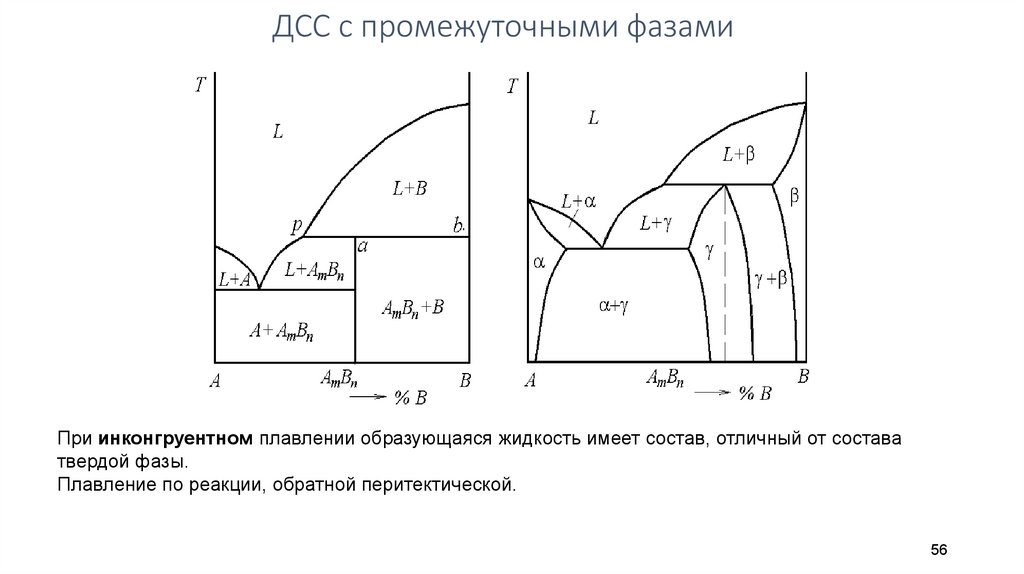
ДСС с промежуточными фазамиПри инконгруентном плавлении образующаяся жидкость имеет состав, отличный от состава
твердой фазы.
Плавление по реакции, обратной перитектической.
56
57.
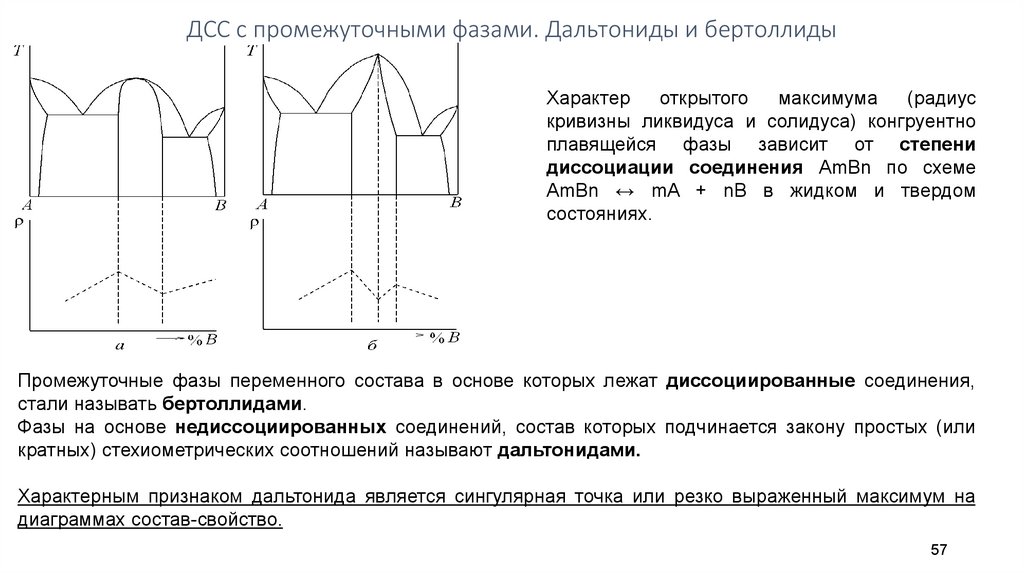
ДСС с промежуточными фазами. Дальтониды и бертоллидыХарактер
открытого
максимума
(радиус
кривизны ликвидуса и солидуса) конгруентно
плавящейся фазы зависит от степени
диссоциации соединения AmBn по схеме
AmBn ↔ mA + nB в жидком и твердом
состояниях.
Промежуточные фазы переменного состава в основе которых лежат диссоциированные соединения,
стали называть бертоллидами.
Фазы на основе недиссоциированных соединений, состав которых подчинается закону простых (или
кратных) стехиометрических соотношений называют дальтонидами.
Характерным признаком дальтонида является сингулярная точка или резко выраженный максимум на
диаграммах состав-свойство.
57
58.
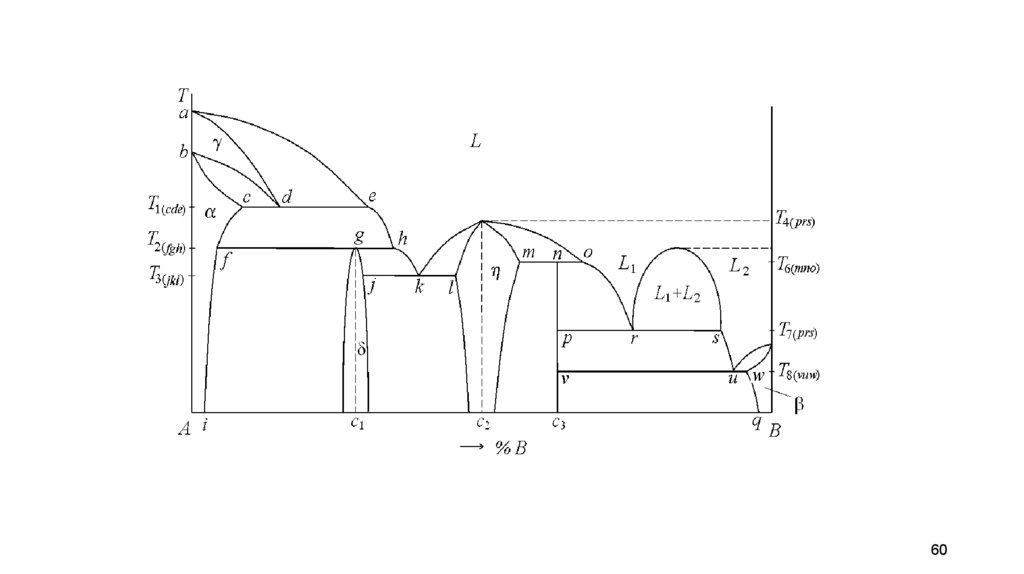
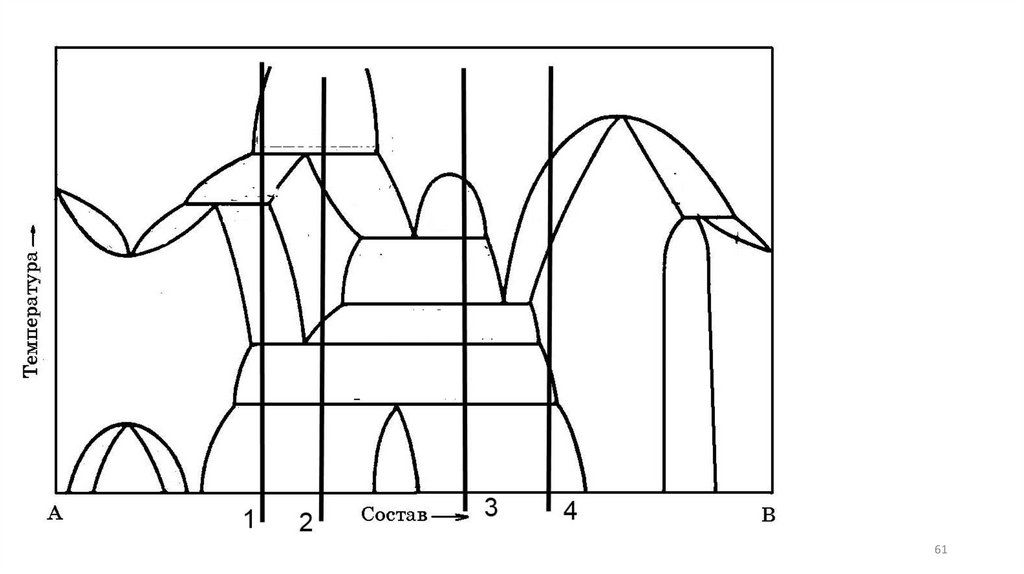
Охарактеризуйте диаграмму состояния по следующим пунктам:Растворимость компонентов в жидком состоянии.
Полиморфизм компонентов, если это имеет место.
Растворимость компонентов в твердом состоянии, ее максимальное значение.
Наличие каких-либо реакций на горизонтальных линиях на диаграмме с записью этих реакций.
Если на диаграмме имеются промежуточные фазы, дать им развернутую характеристику: их состав,
наличие или отсутствие области гомогенности, конгруэнтно или инконгруэнтно плавящиеся.
Дать характеристику состояния заданного сплава:
• Определить химический состав сплава.
• Построить кривую охлаждения сплава с указанием всех превращений, протекающих в нем.
• Определить химический состав фаз при комнатной температуре.
• Определить количество фаз при комнатной температуре.
• Нарисовать микроструктуру сплава при комнатной температуре.
58























 Химия
Химия








