Похожие презентации:
Классификация неорганических веществ (9 класс)
1.
2. Цели урока:
O Повторить классификациюнеорганических веществ
O Обобщить и систематизировать знания
учащихся о классах неорганических
веществ
O Показать значение неорганических
веществ в повседневной жизни
3.
O ВеществаO Простые вещества
O Сложные вещества
O Оксиды
O Основания
O Кислоты
O Соли
4.
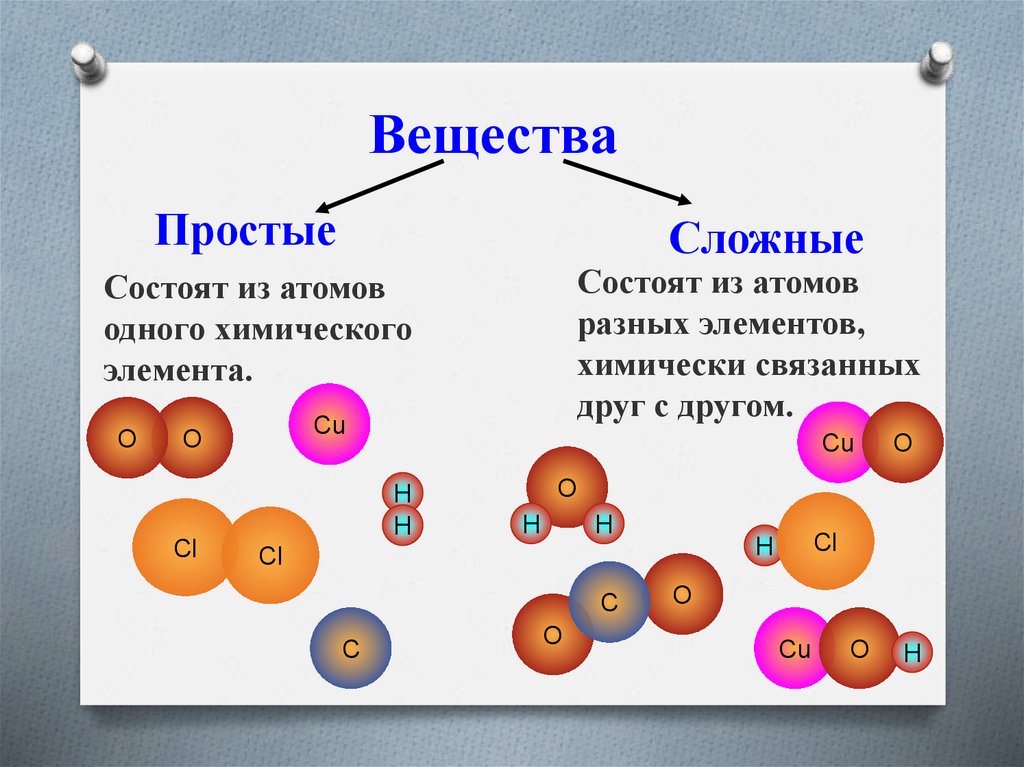
ВеществаПростые
Сложные
Состоят из атомов
разных элементов,
химически связанных
друг с другом.
Состоят из атомов
одного химического
элемента.
О
Cu
О
Cl
Cu
Н
Н
О
Н
Н
Н
Cl
C
C
О
О
Cl
О
Cu
О
Н
5.
Простые веществаМеталлы
Na
Cu
Fe
Неметаллы
S
Благородные газы
Cl2
He
O2
Ne
Rn
6. На классы вещества разбиты Состав их сложен. Надо знать: «Оксиды», «Соли», «Гидроксиды». Посмотрим, как их различать…
7.
Сложные веществаОксиды
ЭxOy
Основания
Me(OH)n
Кислоты
Соли
HxKO
Mex(KO)y
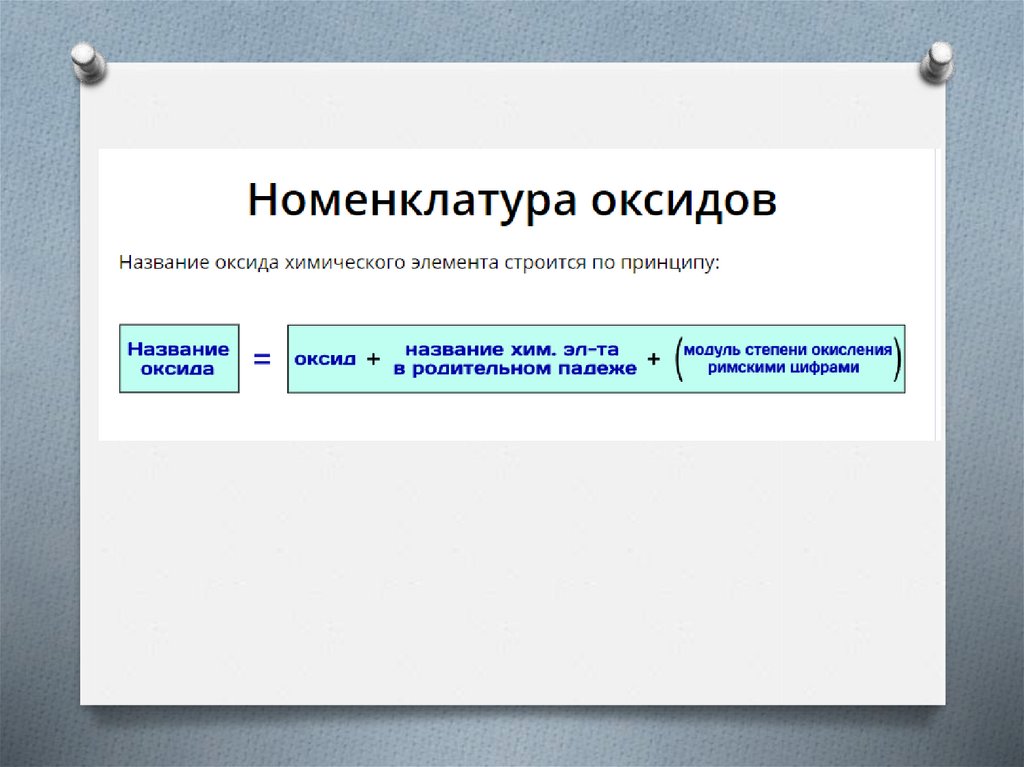
8. В оксидах разберись однажды В самом составе вещества: Есть кислород в оксиде каждом, А элементов только два.
9.
Оксиды – это сложные вещества, состоящиеиз двух химических элементов, один из которых –
кислород со степенью окисления (-2).
Оксиды
Солеобразующие
Амфотерные
Кислотные BeO
Основные
SO2
ZnO
Na2O
P2O5
Al2O3
CuO
Mn2O7
MgO
Несолеобразующие
CO
NO
N2O
SiO
10.
11. Самый известный оксид – вода, занимающий большую часть поверхности Земли.
O Оксид кремния(IV),Оксид алюминия
образует минерал
корунд, а также
входит в состав
рубинов и сапфиров.
Корунд.
входящий в состав
огромного количества
минералов.
O Горный хрусталь.
12. Глина, используемая в силикатной промышленности для производства керамики, в ее составе оксиды кремния, алюминия и вода.
КерамикаФарфор
13. Определим класс «оснований» Классическим обоснованием Ведем научный репортаж: «Металлы связаны с «ОН»!
14.
Основания – это сложные вещества,состоящие из атомов металла и одной или
нескольких гидроксогрупп (-OH).
Основания
Растворимые в воде
(щелочи)
Нерастворимые в воде
NaOH
Cu(OH)2
KOH
Al(OH)3
Ba(OH)2
Fe(OH)2
15.
16. В любой аптечке можно найти нашатырный спирт – гидроксид аммония.
O Гидроксид натрия(едкий натр,
каустическая сода)
применяется для
очистки
нефтепродуктов, в
производстве мыла.
O Гидроксид кальция –
гашеную известь
используют в
строительстве.
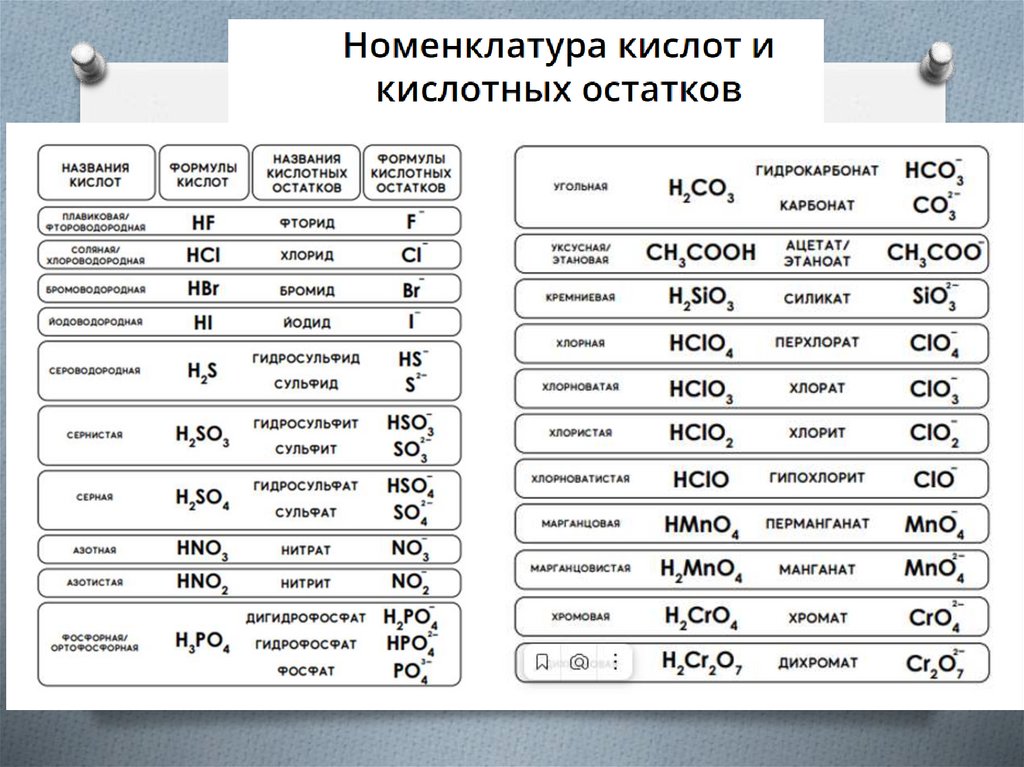
17. Давайте вдумаемся вместе, Каков состав любых кислот. В их формулах на первом месте- Одновалентный водород!
Давайте вдумаемся вместе,Каков состав любых кислот.
В их формулах на первом местеОдновалентный водород!
18.
Кислоты – это сложные вещества,состоящие из атомов водорода, способных
замещаться на атомы металла, и кислотных
остатков.
Кислоты
Бескислородные
Кислородсодержащие
HCl
HNO3
HF
H2SO4
H2S
H3PO4
19.
20.
21. Кислоты (используют в производстве)
лекарстваКислоты
удобрения
(используют в производстве)
красители
взрывчатые вещества
22. Состав солей уже известен Пример используем любой- Металл стоит на первом месте, Остаток от кислот – второй.
Состав солей уже известенПример используем любойМеталл стоит на первом месте,
Остаток от кислот – второй.
23.
Соли – это сложные вещества, состоящие изатомов металла и кислотных остатков.
Соли
Средние
CuSO4
NaCl
KNO3
Кислые
KHCO3
NaHSO4
KH2PO4
Основные
FeOHCl
CuOHNO3
AlOHCl2
Комплексные
Na[Al(OH)4]
K4[Fe(CN)6]
[Cu(H2O)4]SO4•H2O
24.
25.
26. Соли
пищевая содаСоли
гипс
марганцовка
поваренная соль
мрамор
27.
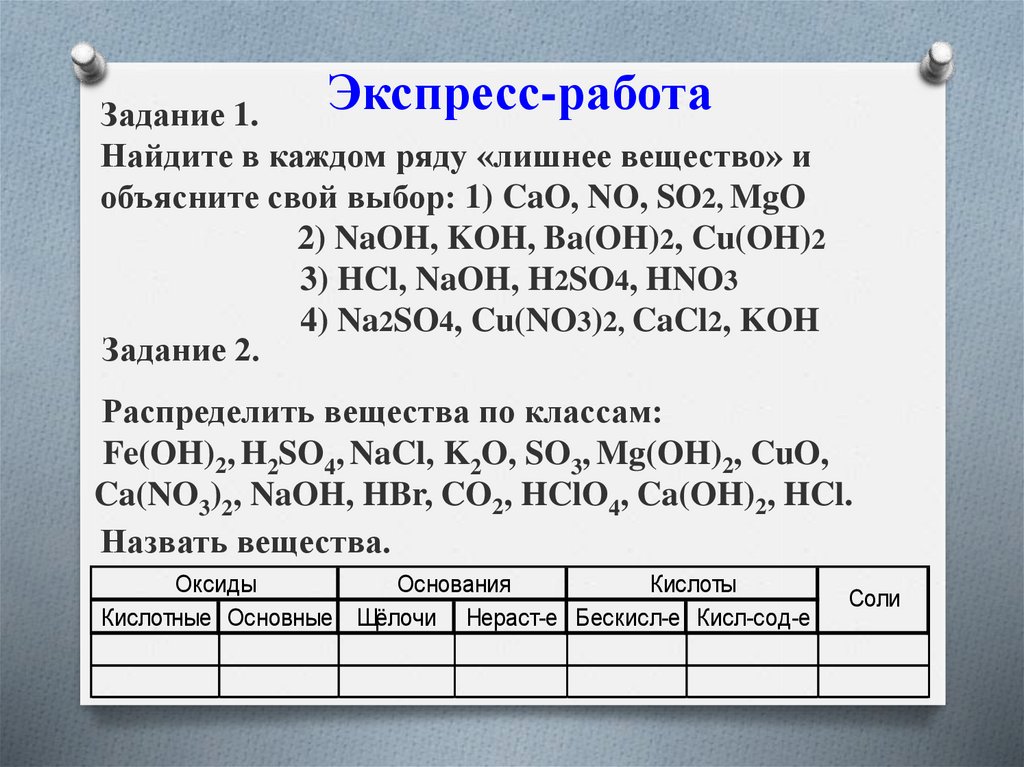
Экспресс-работаЗадание 1.
Найдите в каждом ряду «лишнее вещество» и
объясните свой выбор: 1) CaO, NO, SO2, MgO
2) NaOH, KOH, Ba(OH)2, Cu(OH)2
3) HCl, NaOH, H2SO4, HNO3
4) Na2SO4, Cu(NO3)2, CaCl2, KOH
Задание 2.
Распределить вещества по классам:
Fe(OH)2, H2SO4, NaCl, K2O, SO3, Mg(OH)2, CuO,
Ca(NO3)2, NaOH, HBr, CO2, HClO4, Ca(OH)2, HCl.
Назвать вещества.
Оксиды
Основания
Кислоты
Кислотные Основные Щёлочи Нераст-е Бескисл-е Кисл-сод-е
Соли
28.
Проверим:Задание1: 1)NO
2)Cu(OH)2
3) NaOH
4) KOH
Задание2:
Оксиды
Основания
Кислоты
Соли
Кислотные Основные Щёлочи Нераст-е Бескисл-е Кисл-сод-е
SO3
K2O
NaOH
Fe(OH)2
HBr
H2SO4
NaCl
CO2
CuO
Ca(OH)2 Mg(OH)2
HCl
HClO4
Ca(NO3)2



























 Химия
Химия








