Похожие презентации:
Коллоидные растворы. Молекулярно- кинетические и оптические свойства. Строение коллоидных частиц
1.
"Коллоидные растворы.Молекулярно-кинетические
и оптические свойства.
Строение коллоидных частиц."
1
2. Коллоидная химия
• Коллоидная химия - раздел физической химии,занимающийся изучением дисперсных систем
и их поверхностных явлений.
20.12 .1805 г. – 11.09 1869 г.
Томас Грэм– английский
химик, один из
основоположников
коллоидной химии
Вопросы коллоидной
химии
должно считать
передовыми и
могущими иметь
значение во всей
физике и химии."
Д.И. Менделеев.
"Основы химии". 1871 г
2
3.
Коллоидная химия изучает физико- химическиесвойства высокодисперсных гетерогенных
систем и гомогенных (разбавленных) растворов
ВМС
Дисперсные системы –
гетерогенные системы,
состоящие из
дисперсионной среды,
дисперсной фазы и
стабилизатора.
3
4.
Дисперсная фаза –мелкораздробленныечастицы, равномерно распределённые в
дисперсной системе.
Дисперсионная среда –однородная
непрерывная фаза, в которой распределены
частицы дисперсной фазы.
Стабилизатор – необходим, чтобы система была
устойчивой.
Можно сказать, что весь человек – это ходячий
коллоид, а все органы и системы организма дисперсные системы
4
5.
Кости – это коллаген, насыщенный кальцием ифосфором, мигрирующими в присутствии
витамина Д.
Кровь – это дисперсная система, в которой
ферментные элементы эритроциты, тромбоциты,
лейкоциты являются фазой, а плазма –
дисперсионной средой.
Из коллоидов, богатых белками соединительной
ткани (аминокислоты пролин и глицин), состоят
кожа, мышцы, ногти, волосы, кровеносные
сосуды, легкие, весь желудочно-кишечный тракт и
многое другое, без чего немыслима сама жизнь.
5
6.
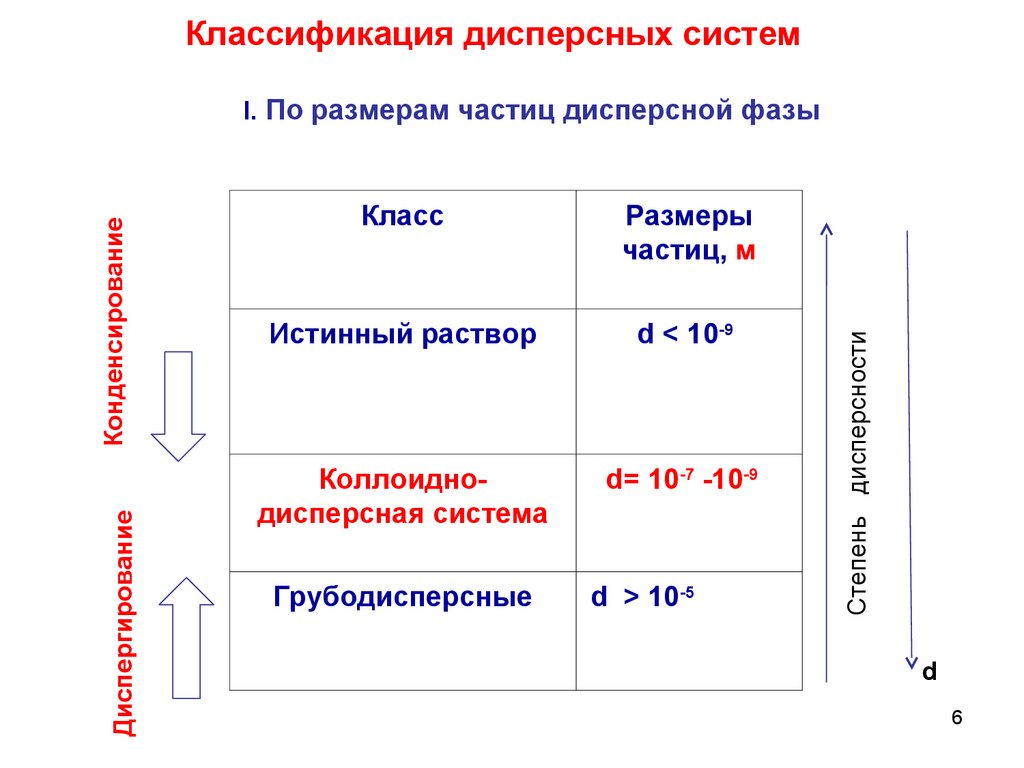
Классификация дисперсных системКласс
Размеры
частиц, м
Истинный раствор
d < 10-9
Коллоиднодисперсная система
d= 10-7 -10-9
Грубодисперсные
d > 10-5
Степень дисперсности
Диспергирование
Конденсирование
I. По размерам частиц дисперсной фазы
d
6
7.
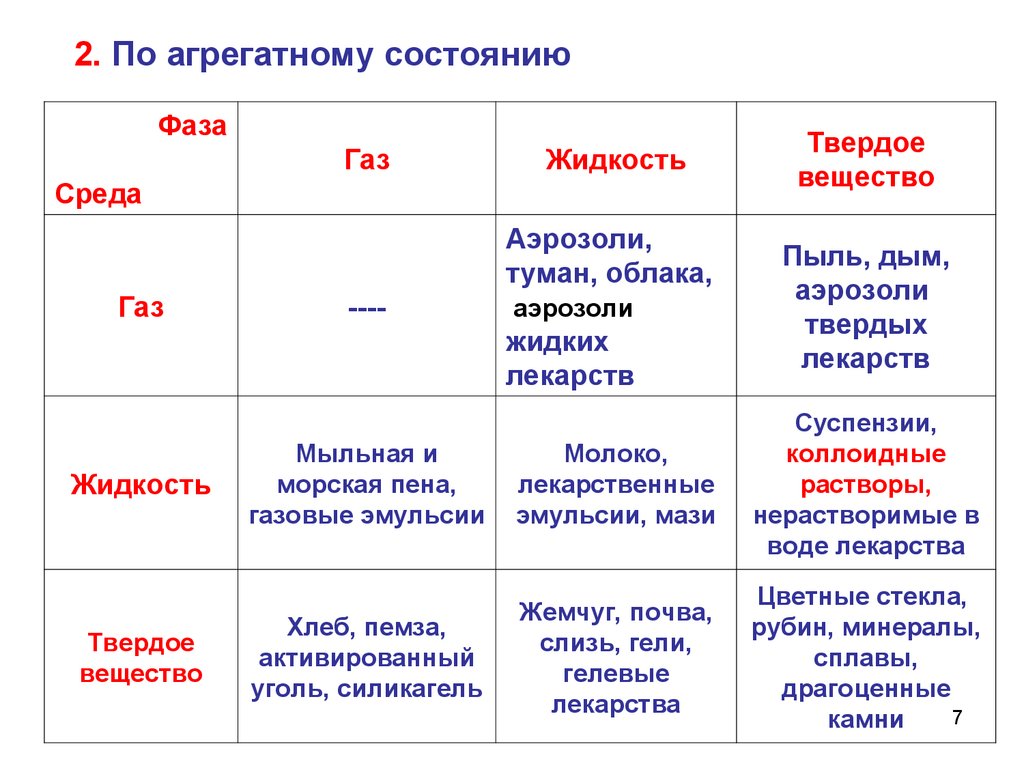
2. По агрегатному состояниюФаза
Среда
Газ
Жидкость
Твердое
вещество
Газ
----
Жидкость
Аэрозоли,
туман, облака,
аэрозоли
жидких
лекарств
Твердое
вещество
Пыль, дым,
аэрозоли
твердых
лекарств
Мыльная и
морская пена,
газовые эмульсии
Молоко,
лекарственные
эмульсии, мази
Суспензии,
коллоидные
растворы,
нерастворимые в
воде лекарства
Хлеб, пемза,
активированный
уголь, силикагель
Жемчуг, почва,
слизь, гели,
гелевые
лекарства
Цветные стекла,
рубин, минералы,
сплавы,
драгоценные
7
камни
8.
Среда - газ, фаза –твердая Среда - газ, фаза – жидкаядым
облака
Среда - твердая, фаза –
твердая рубин, сапфир
Среда – твердая,фаза –
жидкая жемчуг
8
9.
Среда - твердая,фаза – газ
хлеб, пемза
Среда – жидкая, фаза – твердая
суспензии, коллоидные
растворы
Среда – жидкая, фаза –
жидкая
Эмульсии, молоко, сливки
9
10.
3. По характеру взаимодействия дисперсной фазыс дисперсионной средой:
Лиофобные системы:
коллоидные растворы
со стабилизатором
(золи), суспензии,
эмульсии, пены,
аэрозоли (протаргол,
преднизолон, красители,
Лиофильные системы:
растворы ВМС (белки,
мыла, глины, крахмал),
коллоидные растворы
ПАВ
Слабое взаимодействие
между дисперсной
фазой и дисперсионной
средой (гидратная
оболочка -тонкая)
Сильное
взаимодействие между
дисперсной фазой и
дисперсионной средой
(большая гидратная
оболочка)
10
11.
4. По структурно-механическим свойствамСвободнодисперсные
системы,
обладают свойством
текучести:
лиозоли, суспензии,
эмульсии, кровь,
биологические мембраны,
аэрозоли - туманы, дым,
пыль
Связнодисперсные
системы,
потеря текучести:
лиогели, студни,
волокнистые
и пористые капиллярные
системы (костная ткань,
биологические мембраны,
студни)
Дисперсная фаза подвижна.
Дисперсная фаза практически
неподвижна, так как образует
сплошную структуру
5. По природе дисперсионной среды
Жидкая - лиозоли
11
12.
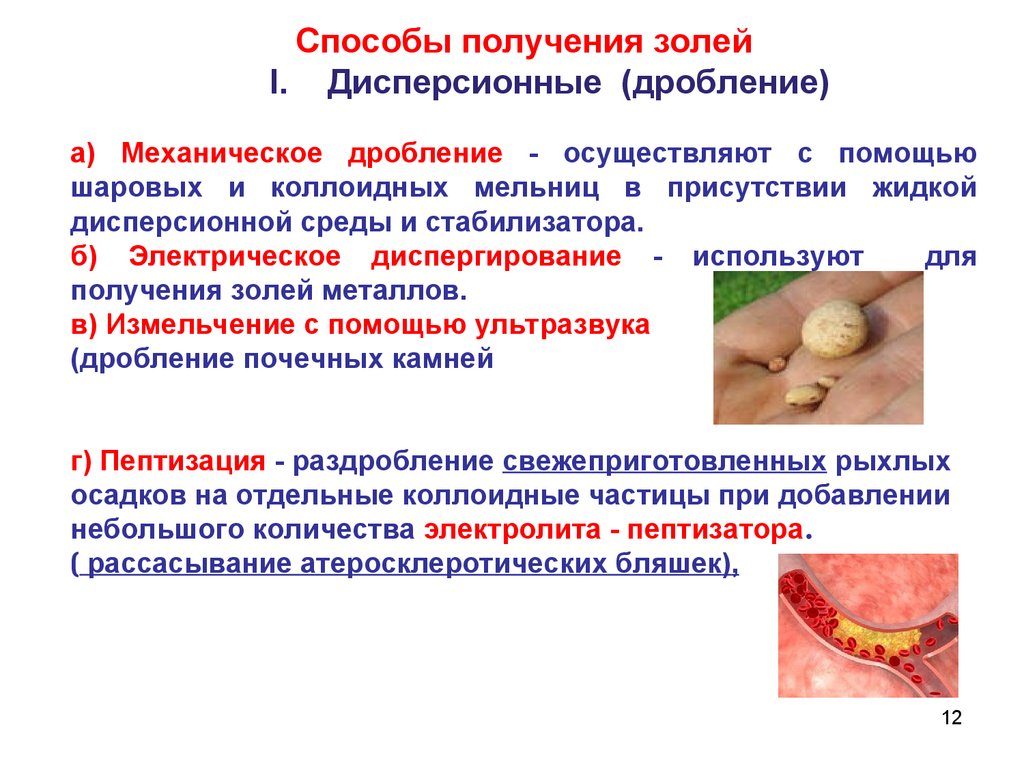
Способы получения золейI. Дисперсионные (дробление)
a) Механическое дробление - осуществляют с помощью
шаровых и коллоидных мельниц в присутствии жидкой
дисперсионной среды и стабилизатора.
б) Электрическое диспергирование - используют
для
получения золей металлов.
в) Измельчение с помощью ультразвука
(дробление почечных камней
г) Пептизация - раздробление свежеприготовленных рыхлых
осадков на отдельные коллоидные частицы при добавлении
небольшого количества электролита - пептизатора.
( рассасывание атеросклеротических бляшек),
12
13.
II. Конденсационные– из истинных растворов (укрупнение).
а ) Физические - метод замены растворителя.
Раствор вещества прибавляют к жидкости, в которой
растворенное вещество мало растворимо и выделяется в
виде высокодисперсной фазы. Золи серы, холестерина и
канифоли получают добавлением спиртовых растворов
этих веществ к воде.
б) Химические
1) Реакции восстановления
2KAuO2 3HCHO K 2 CO 3 2Au 3HCOOK KHCO3 H 2 O
m[Au]nAuO (n x)K xK .
2
x
Формула мицеллы золя золота
13
14.
Реакции восстановления8KMnO 4 Na 2S2 O 3 H 2 O 8MnO 2 3K 2SO 4 3Na 2SO 4 2KOH
m[MnO ]nMnO (n x)K xK
x
2
4
мицелла
MnO2
2) Реакции обмена
Ba ( NO 3 ) 2 K 2SO 4 BaSO 4 2KNO 3
избыток
m[BaSO ]nBa 2(n x)NO 2xNO
4
2x
2
3
3
мицелла
BaSO4
3) Реакции гидролиза
FeCl3 3H 2O Fe(OH )3 3HCl
FeOCl FeO Cl
мицелла
Fe(OH)3
m[Fe(OH ) ]nFeO (n x)Cl xCl .
3
x
-
14
15.
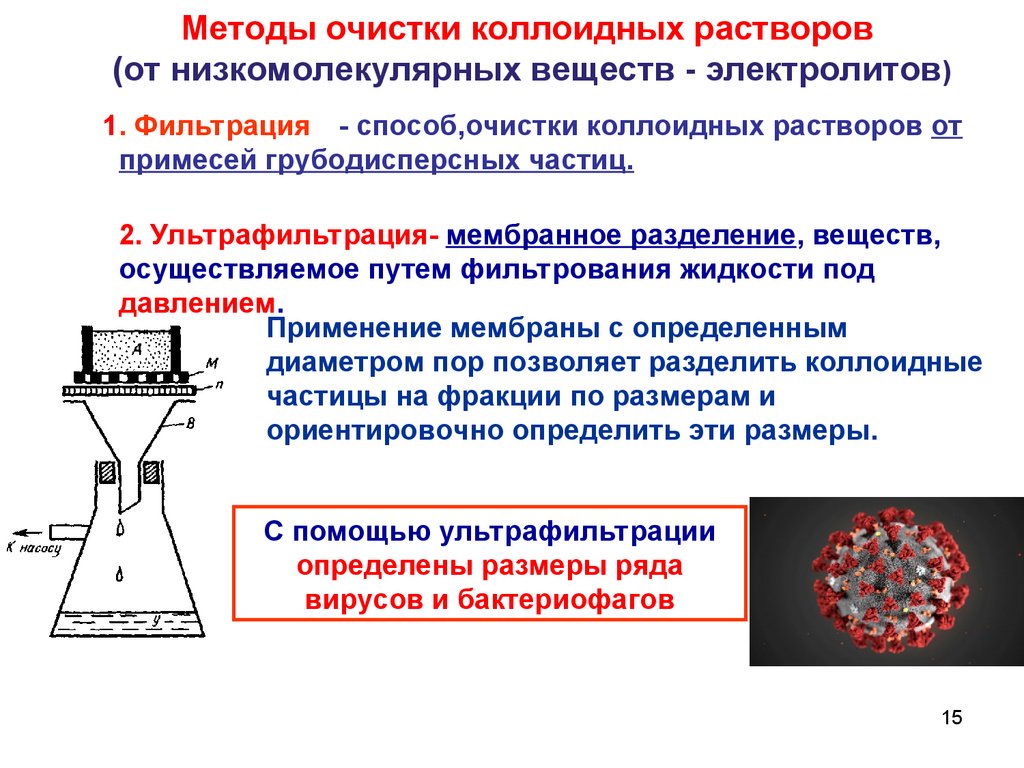
Методы очистки коллоидных растворов(от низкомолекулярных веществ - электролитов)
1. Фильтрация - способ,очистки коллоидных растворов от
примесей грубодисперсных частиц.
2. Ультрафильтрация- мембранное разделение, веществ,
осуществляемое путем фильтрования жидкости под
давлением.
Применение мембраны с определенным
диаметром пор позволяет разделить коллоидные
частицы на фракции по размерам и
ориентировочно определить эти размеры.
С помощью ультрафильтрации
определены размеры ряда
вирусов и бактериофагов
15
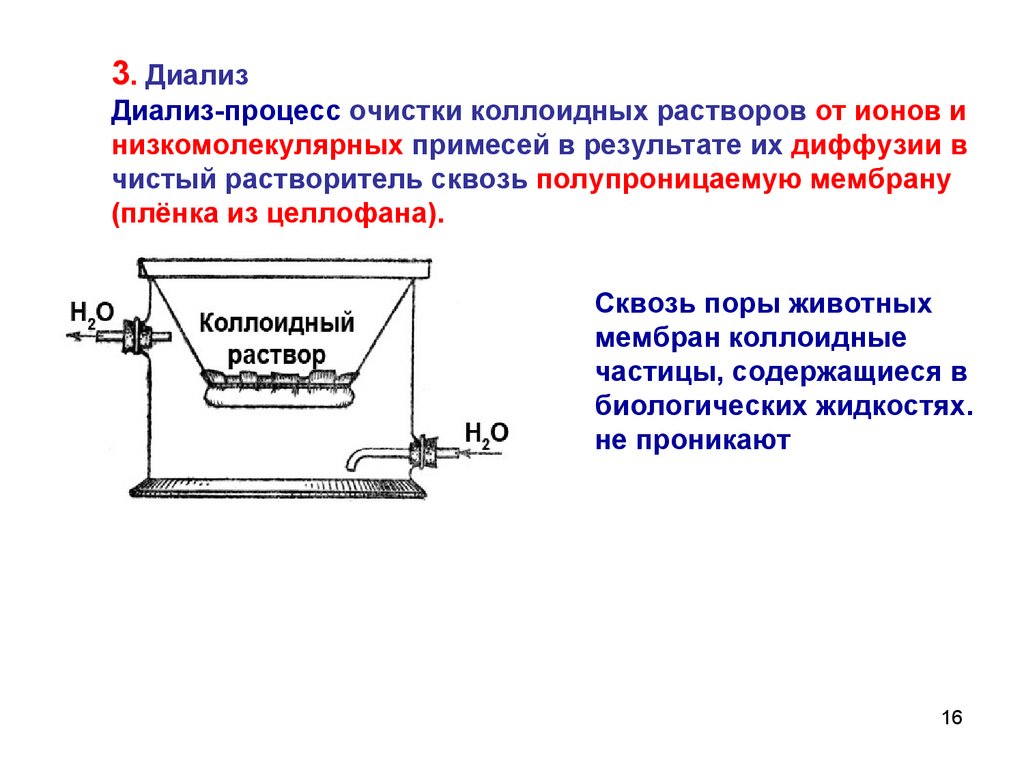
16.
3. ДиализДиализ-процесс очистки коллоидных растворов от ионов и
низкомолекулярных примесей в результате их диффузии в
чистый растворитель сквозь полупроницаемую мембрану
(плёнка из целлофана).
Сквозь поры животных
мембран коллоидные
частицы, содержащиеся в
биологических жидкостях.
не проникают
16
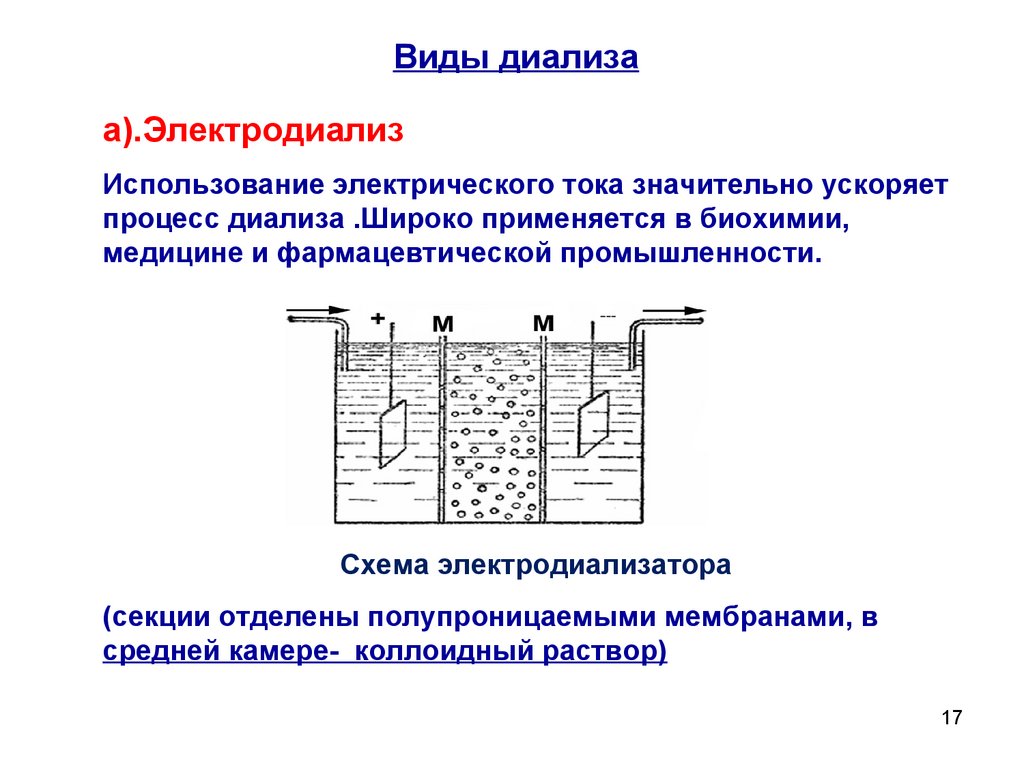
17.
Виды диализаа).Электродиализ
Использование электрического тока значительно ускоряет
процесс диализа .Широко применяется в биохимии,
медицине и фармацевтической промышленности.
Схема электродиализатора
(секции отделены полупроницаемыми мембранами, в
средней камере- коллоидный раствор)
17
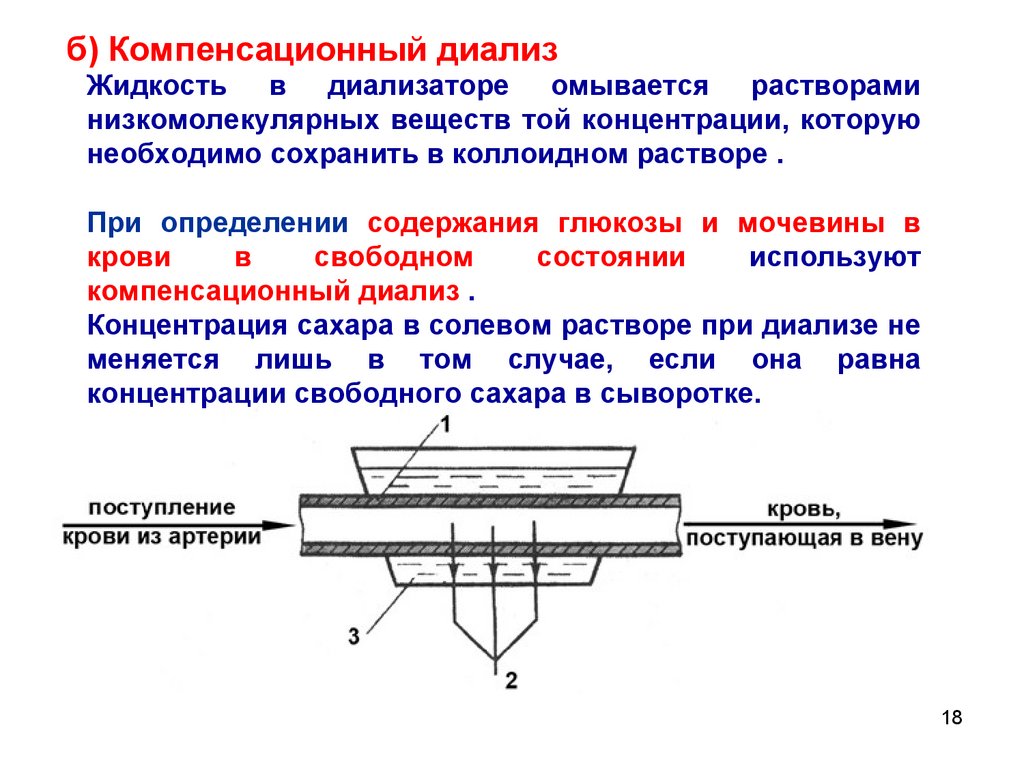
18.
б) Компенсационный диализЖидкость в диализаторе омывается растворами
низкомолекулярных веществ той концентрации, которую
необходимо сохранить в коллоидном растворе .
При определении содержания глюкозы и мочевины в
крови
в
свободном
состоянии
используют
компенсационный диализ .
Концентрация сахара в солевом растворе при диализе не
меняется лишь в том случае, если она равна
концентрации свободного сахара в сыворотке.
18
19.
в). ВивидиализЭто метод извлечения низкомолекулярных веществ из
физиологических жидкостей с целью очистки или
анализа. При этом биологическая жидкость проходит
через аппарат для диализа и возвращается в живой
организм.
По принципу вивидиализа работает аппарат
« искусственная почка». Гемодиализ (очистка
крови)
применяется при острой почечной
недостаточности.
Схема аппарата
для вивидиализа
19
20.
Аппарат подключают к системе кровообращениябольного. Кровь под давлением ,которое создаёт
пульсирующий насос, подаётся в капилляры,
изготовленные из полупроницаемого материала.
диализатор
Капилляры омываются извне диализирущим раствором.
Диализирующий раствор содержит одинаковые с кровью
концентрации веществ, которые необходимо сохранить в
крови.
Продукты обмена и распада
тканей (мочевина, креатинин,
ионы калия) удаляются из
крови за 3-4 часа благодаря
большой рабочей площади
мембран (до 1.5 м2).
диализатор
20
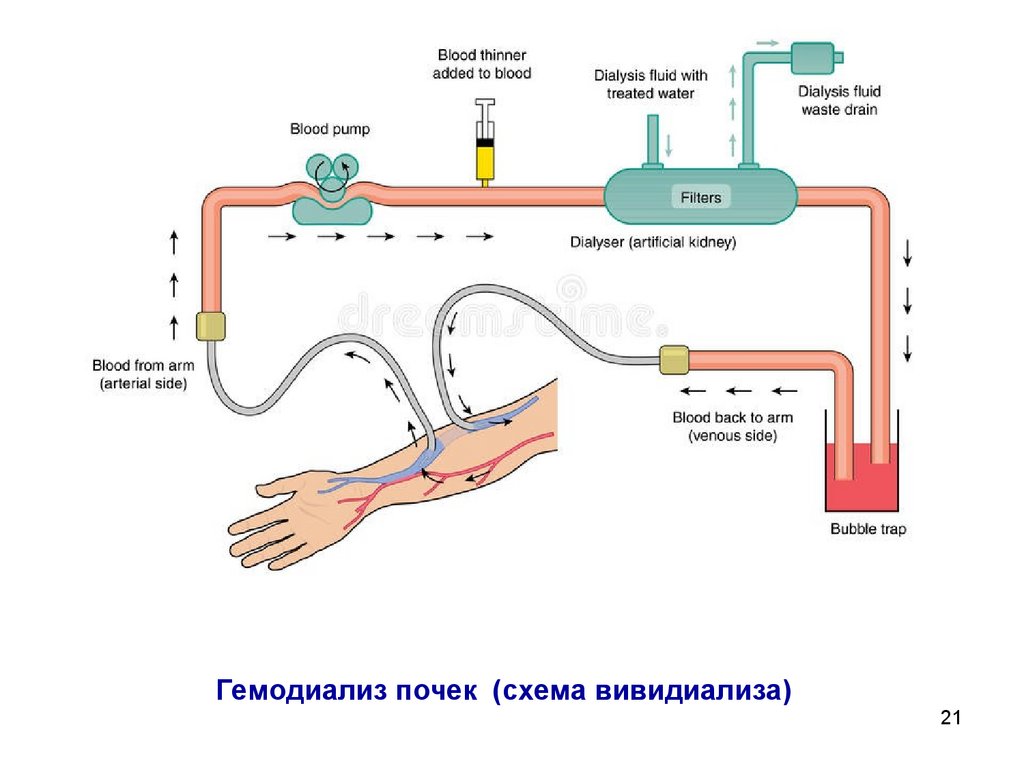
21.
Гемодиализ почек (схема вивидиализа)21
22.
Свойства дисперсных систем1.Молекулярно-кинетические свойства –
обусловлены хаотическим тепловым
движением частиц.
а)Броуновское движение
б) Диффузия
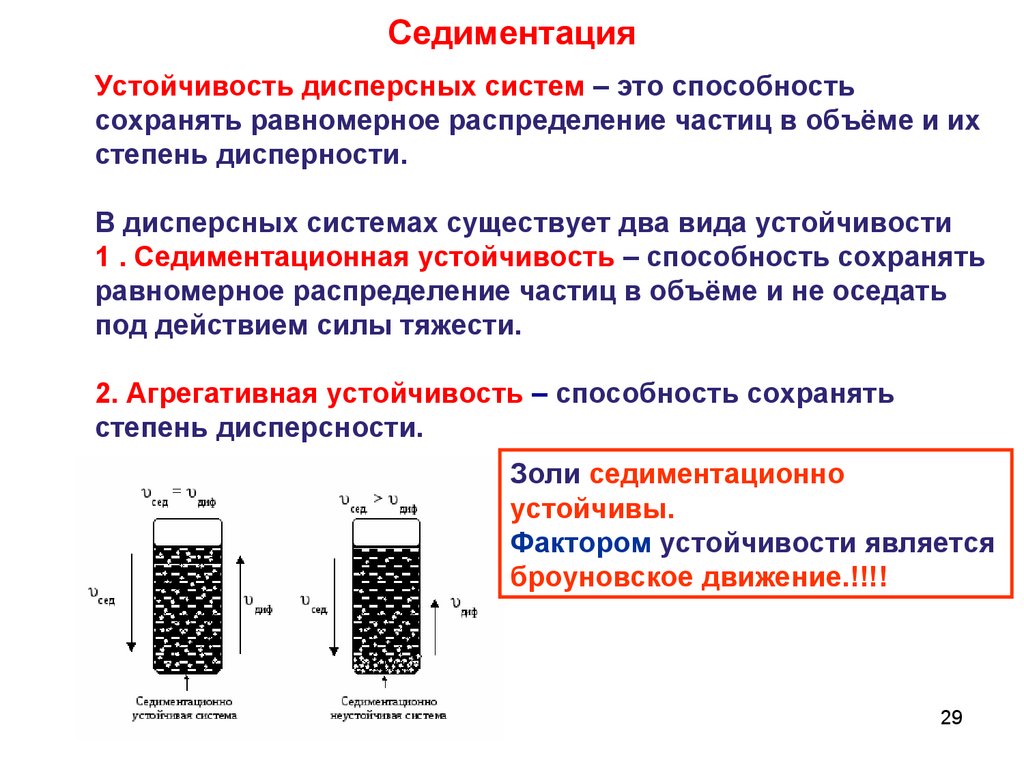
в) Седиментация
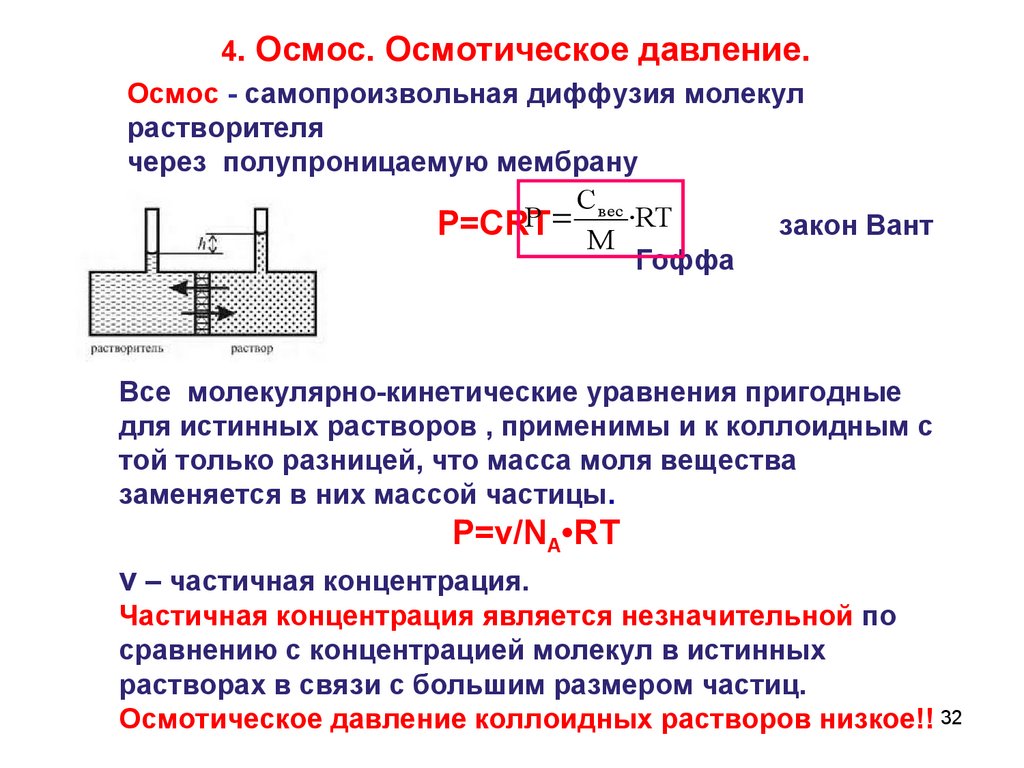
г) Осмотическое давление
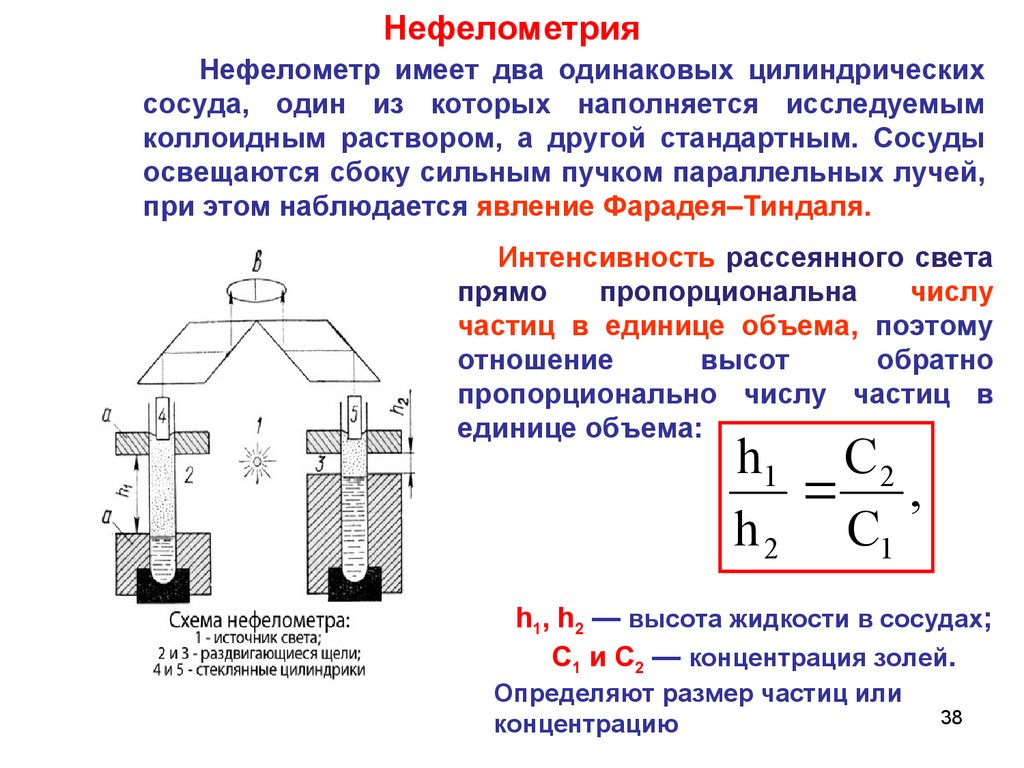
2. Оптические свойства.
3. Электрокинетические свойства
4. Поверхностные явления .Адсорбция
22
23.
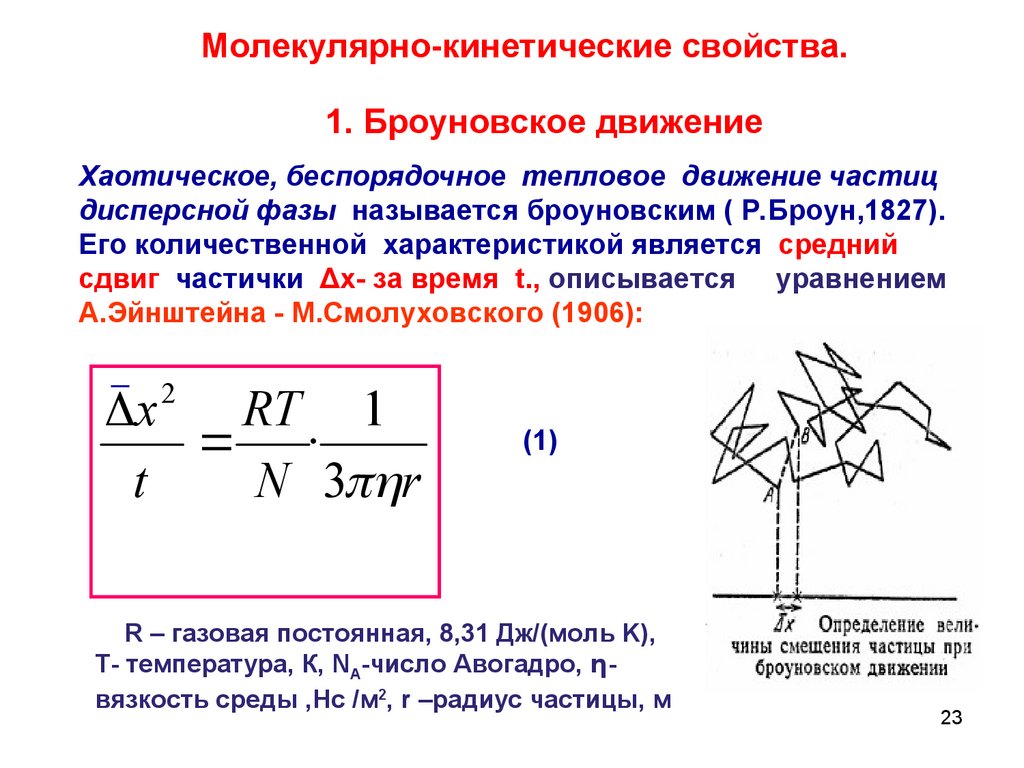
Молекулярно-кинетические свойства.1. Броуновское движение
Хаотическое, беспорядочное тепловое движение частиц
дисперсной фазы называется броуновским ( Р.Броун,1827).
Его количественной характеристикой является средний
сдвиг частички Δх- за время t., описывается уравнением
А.Эйнштейна - М.Смолуховского (1906):
─
2
x
RT 1
·
t
N 3 r
(1)
R – газовая постоянная, 8,31 Дж/(моль K),
T- температура, К, NA-число Авогадро,


























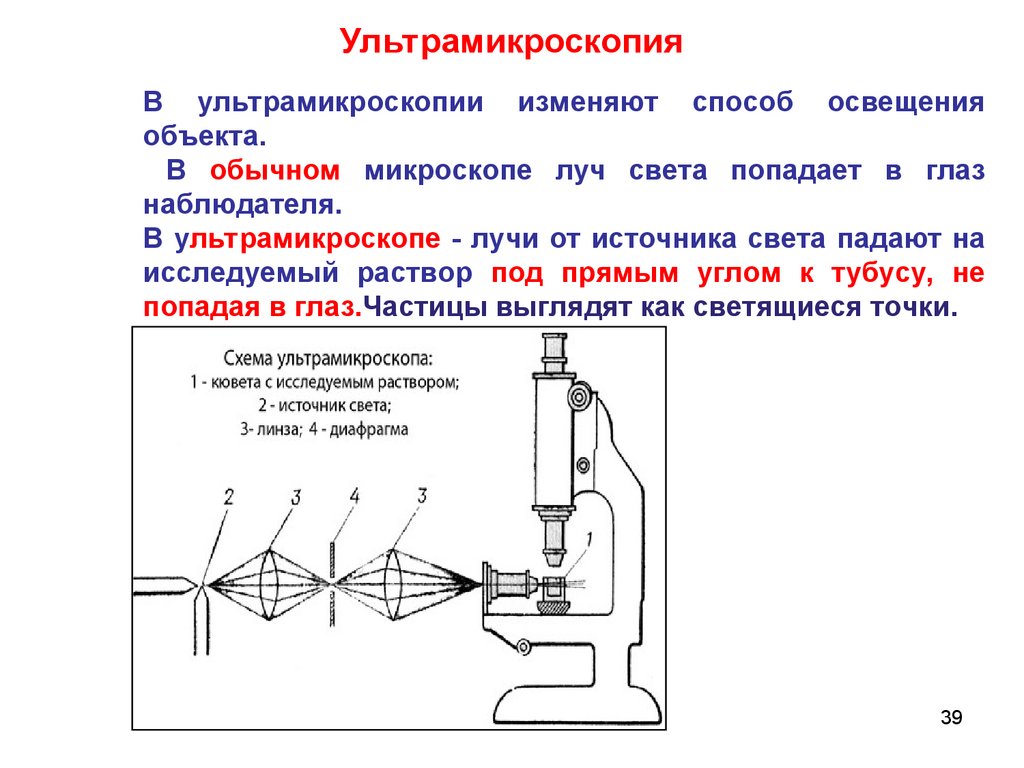
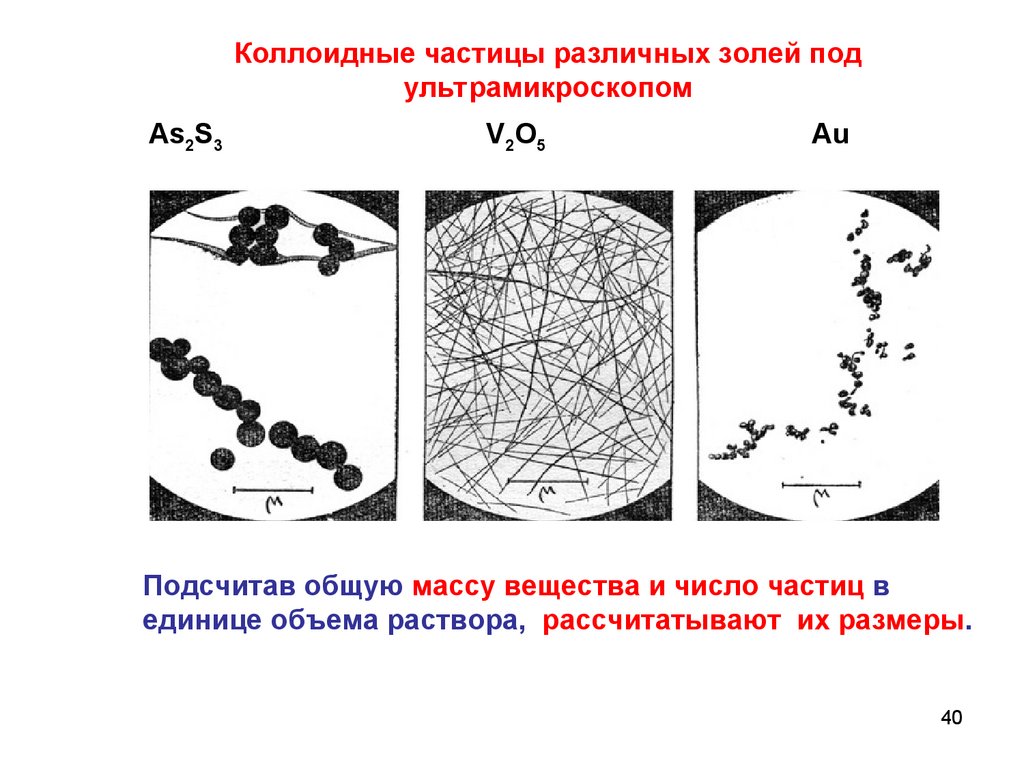

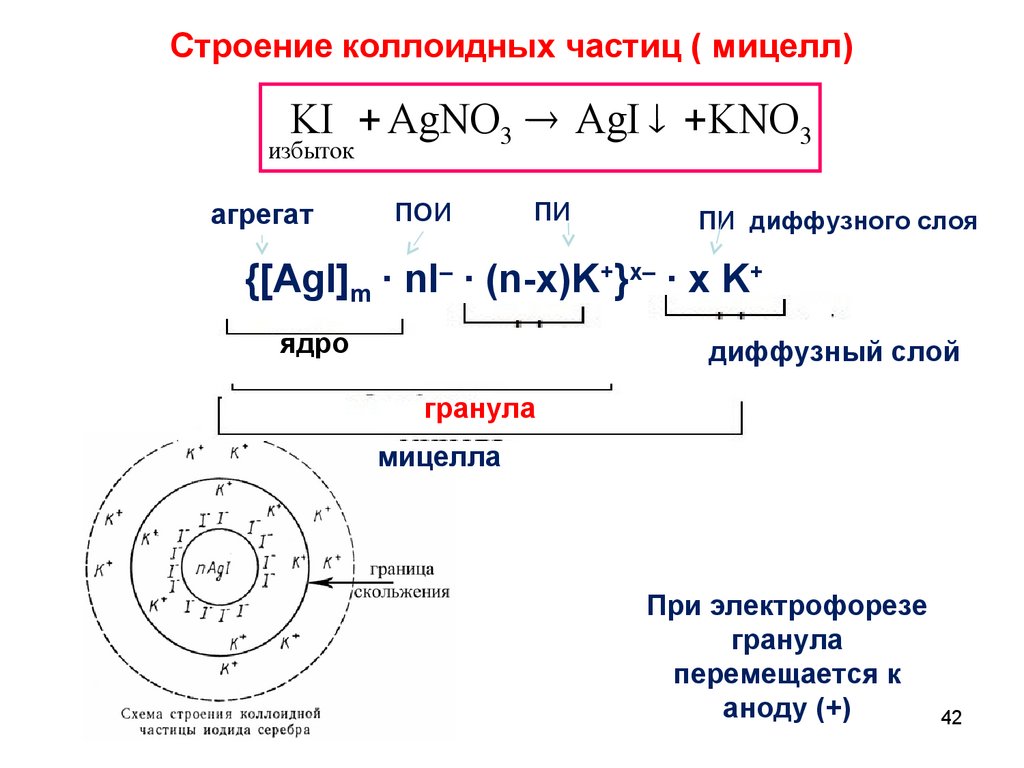
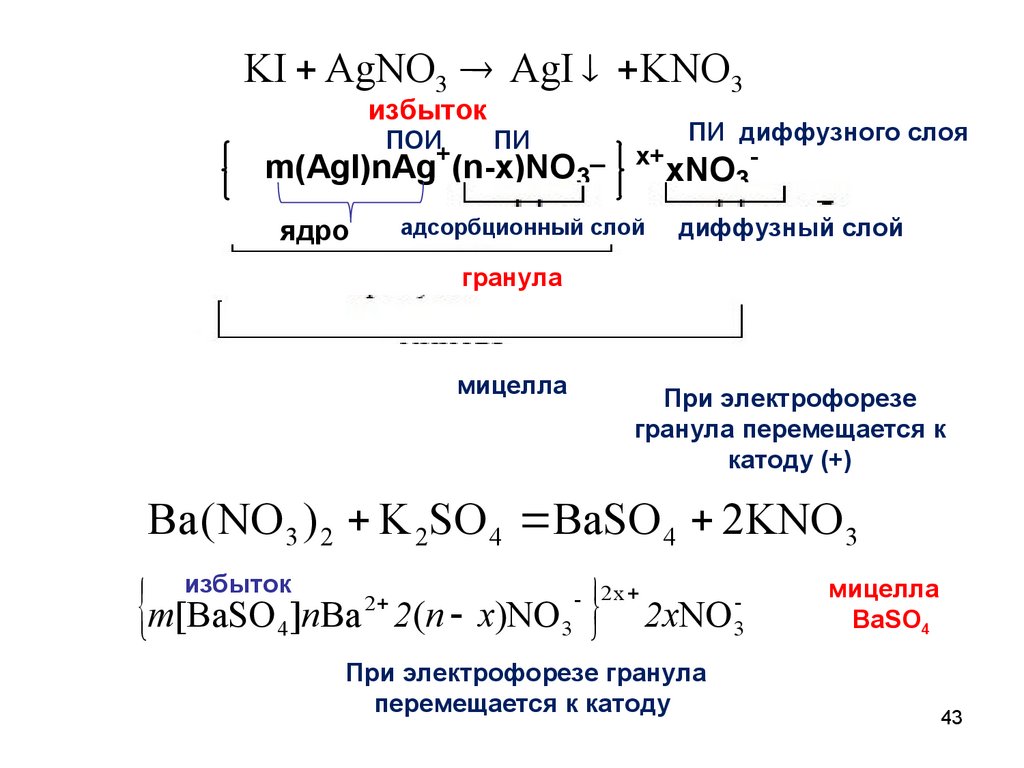



 Химия
Химия








