Похожие презентации:
Спектроскопические методы анализа. Атомная спектроскопия
1. Аналитическая химия II. Физические и физико-химические методы анализа
Аналитическая химия II.Физические и физикохимические методы анализа
Лекция 6. Спектроскопические методы анализа.
Атомная спектроскопия
лекция6
Аналитическая химия 2. ФХМА
1
2.
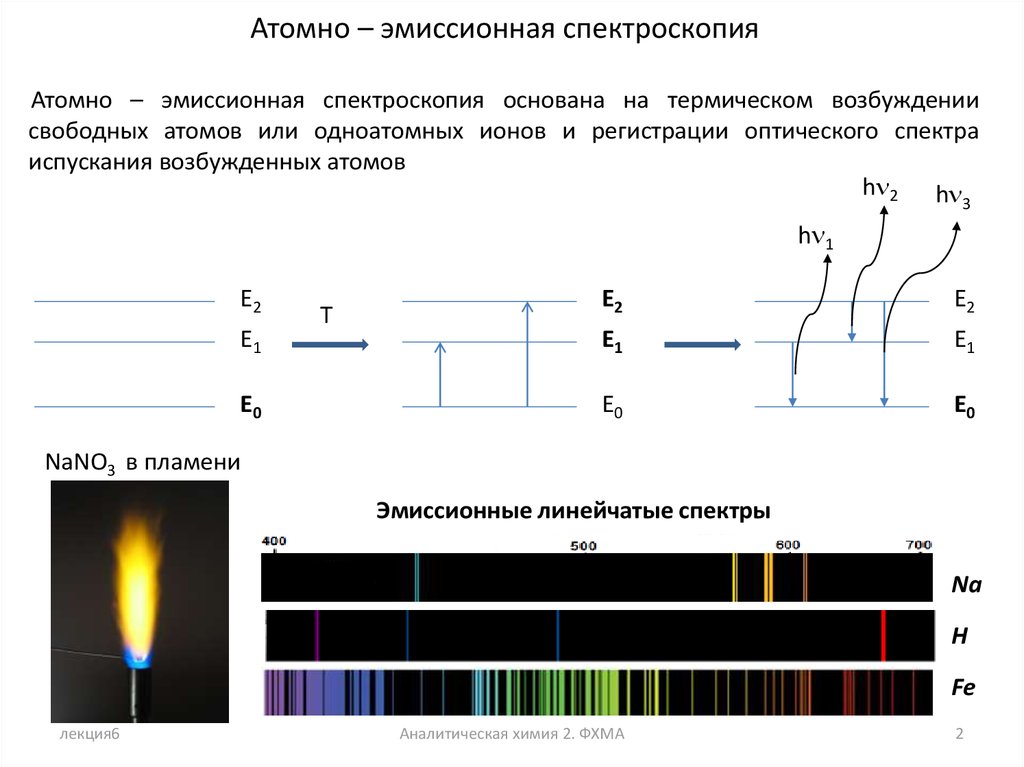
Атомно – эмиссионная спектроскопияАтомно – эмиссионная спектроскопия основана на термическом возбуждении
свободных атомов или одноатомных ионов и регистрации оптического спектра
испускания возбужденных атомов
hn2 hn
3
hn1
E2
E1
E0
T
E2
E2
E1
E1
E0
E0
NaNO3 в пламени
Эмиссионные линейчатые спектры
Na
H
Fe
лекция6
Аналитическая химия 2. ФХМА
2
3.
Возбужденные и невозбужденные атомы находятся между собой в термодинамическомравновесии, которое описывается законом распределения Больцмана:
Ne ge
e
No go
E
kT
где Ne и No – число возбужденных и невозбужденных атомов при температуре Т (Ne << No),
ge и go - статистические веса возбужденного и невозбужденного состояний,
k – постоянная Больцмана, Е – энергия возбуждения.
I A Ne hn
E
g e kT
I A N 0 hn e
g0
Уравнение Ломакина – Шайбе:
I=acb
лекция6
Аналитическая химия 2. ФХМА
3
4.
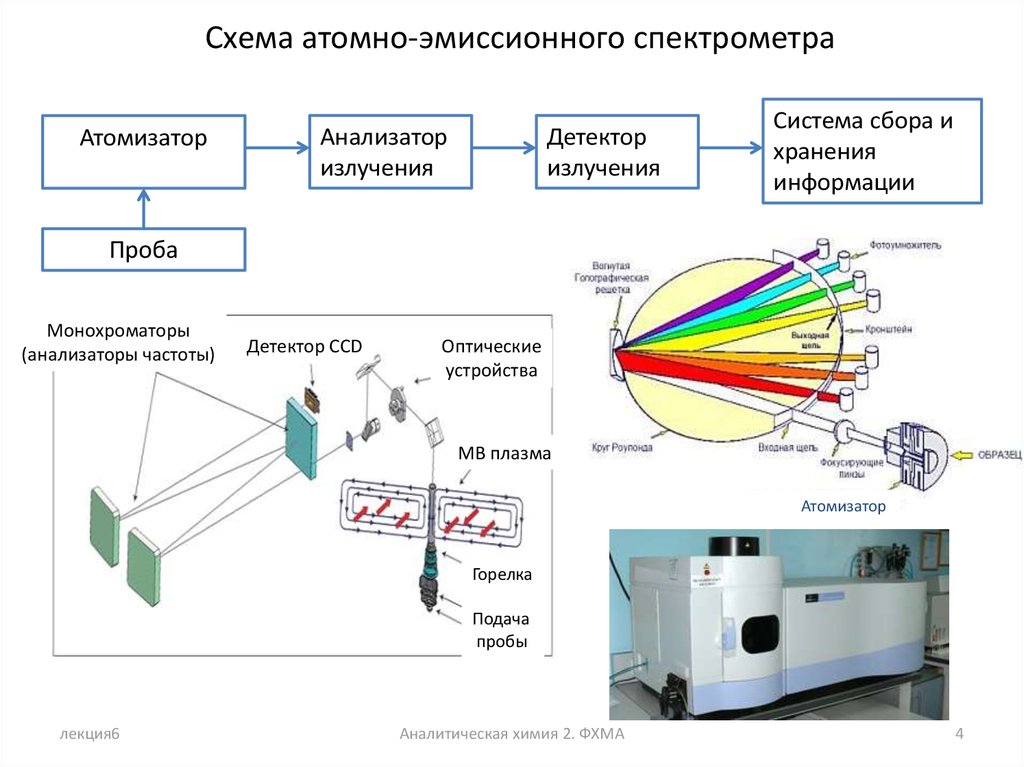
Схема атомно-эмиссионного спектрометраАтомизатор
Анализатор
излучения
Детектор
излучения
Система сбора и
хранения
информации
Проба
Монохроматоры
(анализаторы частоты)
Детектор CCD
Оптические
устройства
МВ плазма
Атомизатор
Горелка
Подача
пробы
лекция6
Аналитическая химия 2. ФХМА
4
5.
ПламяЭмиссионная фотометрия пламени – атомно-эмиссионная спектроскопия с
атомизацией в пламени
Горелка Бекмана (турбулентное пламя)
Внешний конус
Окислительная зона
Вход
окислителя
Внутренний конус
Восстановительная
зона
Капилярная
инжекторная
трубка
Вход
горючего
Ввод пробы
в форме раствора
горелка Бунзена
(ламинарное пламя)
лекция6
Аналитическая химия 2. ФХМА
5
6.
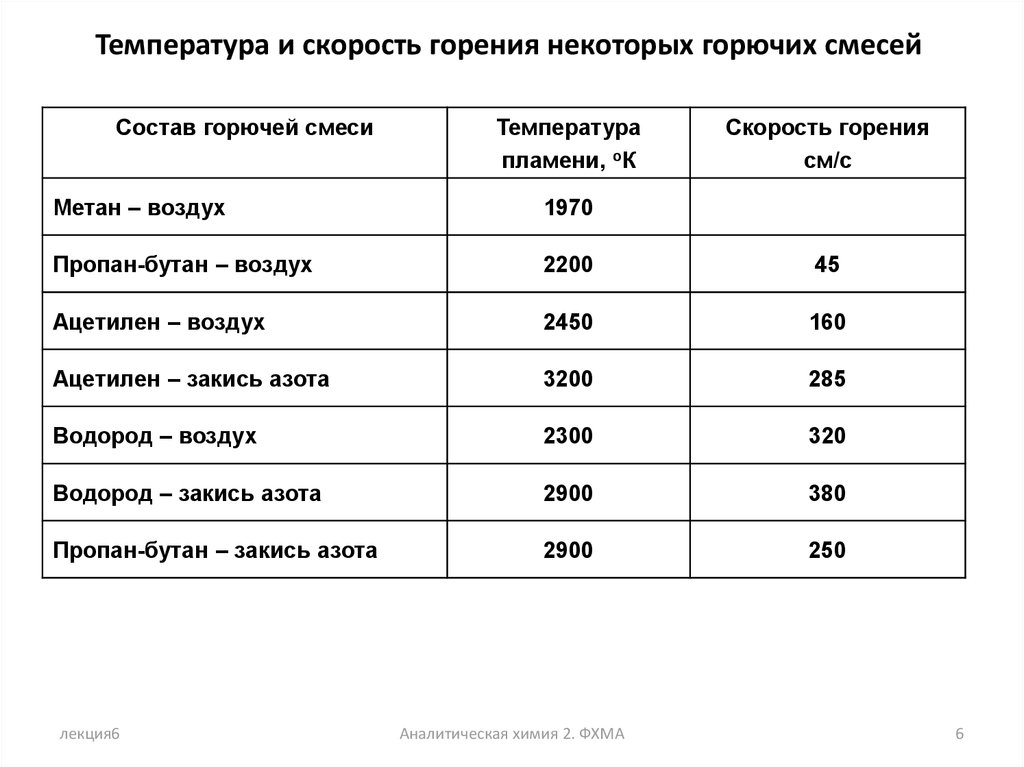
Температура и скорость горения некоторых горючих смесейСостав горючей смеси
Температура
пламени, оК
Скорость горения
см/с
Метан – воздух
1970
Пропан-бутан – воздух
2200
45
Ацетилен – воздух
2450
160
Ацетилен – закись азота
3200
285
Водород – воздух
2300
320
Водород – закись азота
2900
380
Пропан-бутан – закись азота
2900
250
лекция6
Аналитическая химия 2. ФХМА
6
7.
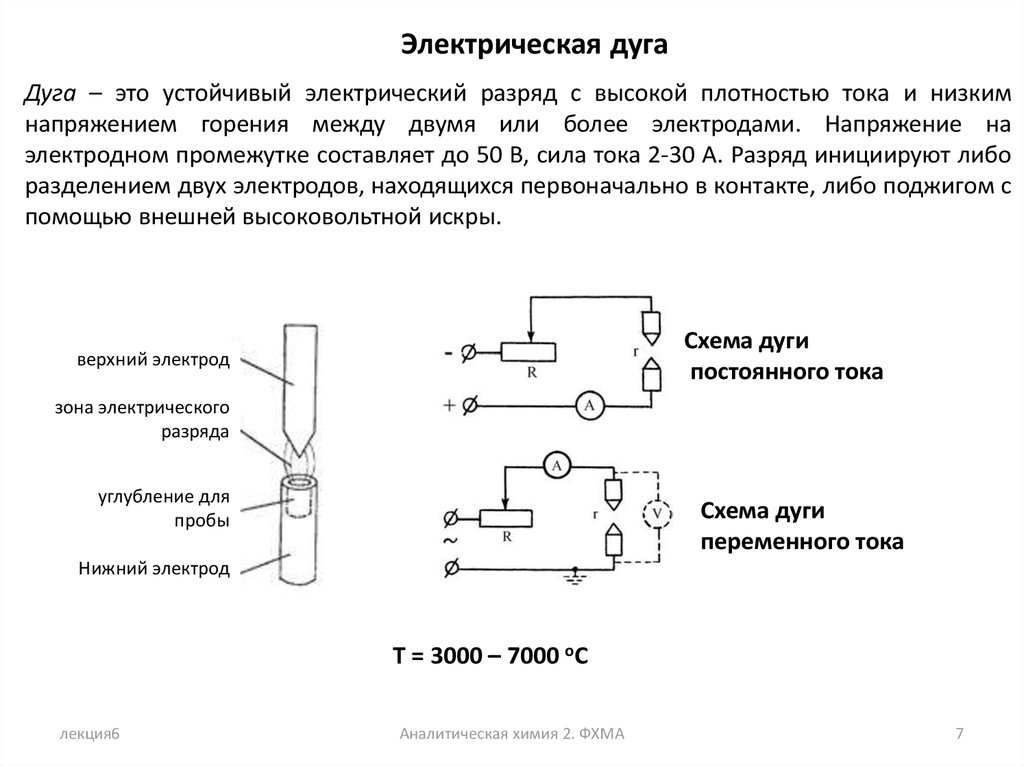
Электрическая дугаДуга – это устойчивый электрический разряд с высокой плотностью тока и низким
напряжением горения между двумя или более электродами. Напряжение на
электродном промежутке составляет до 50 В, сила тока 2-30 А. Разряд инициируют либо
разделением двух электродов, находящихся первоначально в контакте, либо поджигом с
помощью внешней высоковольтной искры.
Схема дуги
постоянного тока
верхний электрод
зона электрического
разряда
углубление для
пробы
Схема дуги
переменного тока
Нижний электрод
T = 3000 – 7000 oC
лекция6
Аналитическая химия 2. ФХМА
7
8.
Электрическая искраИскра представляет пульсирующий электрический разряд высокого напряжения и
относительно низкой средней силы тока между двумя электродами.
Длительность искры – несколько микросекунд. Частота – 50-100 Гц.
Пространство между электродами 3 -6 мм.
Искра может быть классифицирована в соответствии с приложенным напряжением:
-искра высокого напряжения (10-20 кВ),
-искра среднего напряжения (500 – 1500 В)
-искра низкого напряжения (300 – 500 В)
Контакт
Проводящая проба
(электрод)
Зона искрового
разряда
Противоэлектрод
T = 10000 oC
лекция6
Аналитическая химия 2. ФХМА
8
9.
ПЛАЗМАПлазма – это ионизированный газ, который макроскопически нейтрален, т.е. имеет
одно и то же число положительных частиц (ионов) и отрицательных частиц
(электронов). Отличительной чертой плазмы является высокая плотность носителей
заряда.
В отличие от пламени для ионизации газа и поддержания плазмы необходим подвод
внешней энергии в виде электрического поля. Плазма в свою очередь передает часть
энергии пробе, что приводит к атомизации и возбуждению последней.
Плазму можно классифицировать в соответствии с типом электрического поля,
используемого для создания и поддержания плазмы:
- плазма постоянного тока (ППТ) образуется при наложении на электроды
постоянного потенциала;
- индуктивно-связанная плазма (ИСП - ICP) образуется при возбуждении
высокочастотного поля в катушке;
- микроволновая плазма (МП) образуется при наложении микроволнового поля на
кювету.
лекция6
Аналитическая химия 2. ФХМА
9
10.
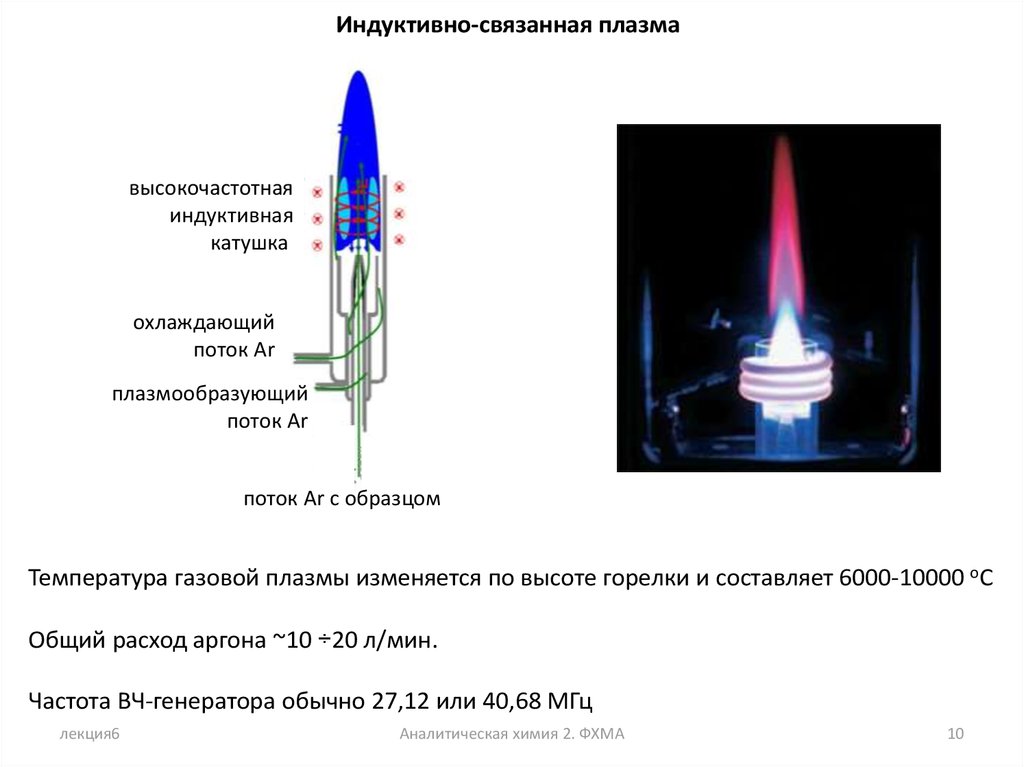
Индуктивно-связанная плазмавысокочастотная
индуктивная
катушка
охлаждающий
поток Ar
плазмообразующий
поток Ar
поток Ar с образцом
Температура газовой плазмы изменяется по высоте горелки и составляет 6000-10000 оС
Общий расход аргона ~10 ÷20 л/мин.
Частота ВЧ-генератора обычно 27,12 или 40,68 МГц
лекция6
Аналитическая химия 2. ФХМА
10
11.
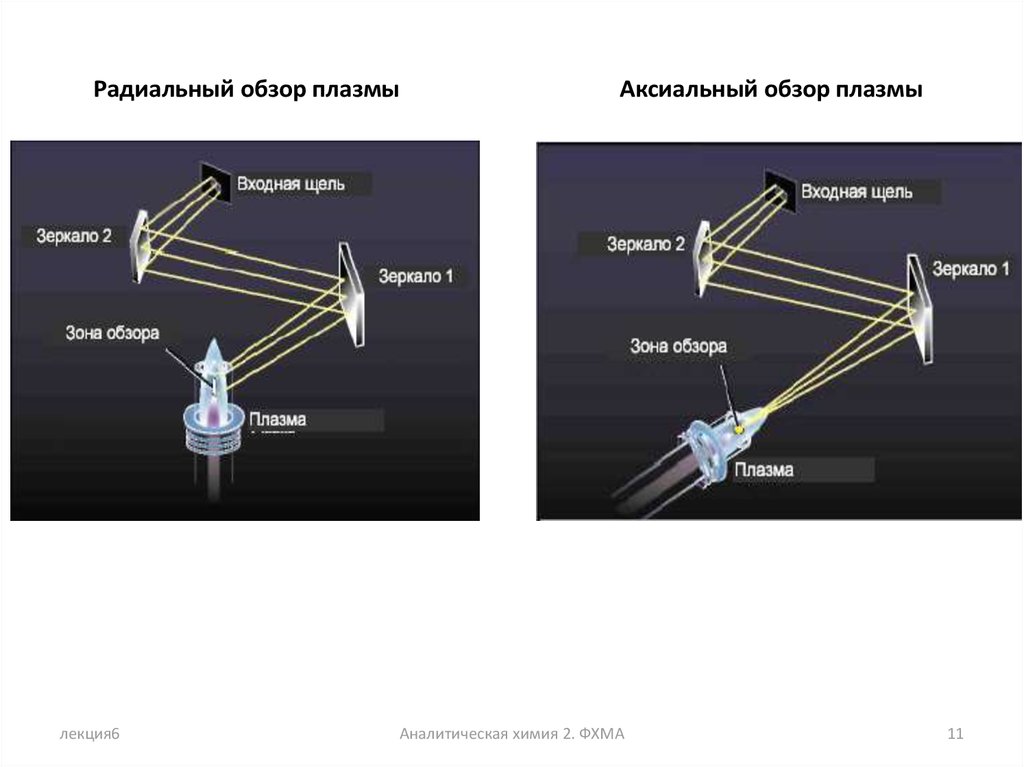
Радиальный обзор плазмылекция6
Аксиальный обзор плазмы
Аналитическая химия 2. ФХМА
11
12.
Схема процессов, протекающих в атомизаторе1 – испарение
2 – атомизация
3,5 – возбуждение
4,6 – ионизация
Физико-химические помехи
-Полнота испарения и атомизация пробы
-Ионизация: M = M++ e
-Изменение температуры плазмы
лекция6
Аналитическая химия 2. ФХМА
12
13.
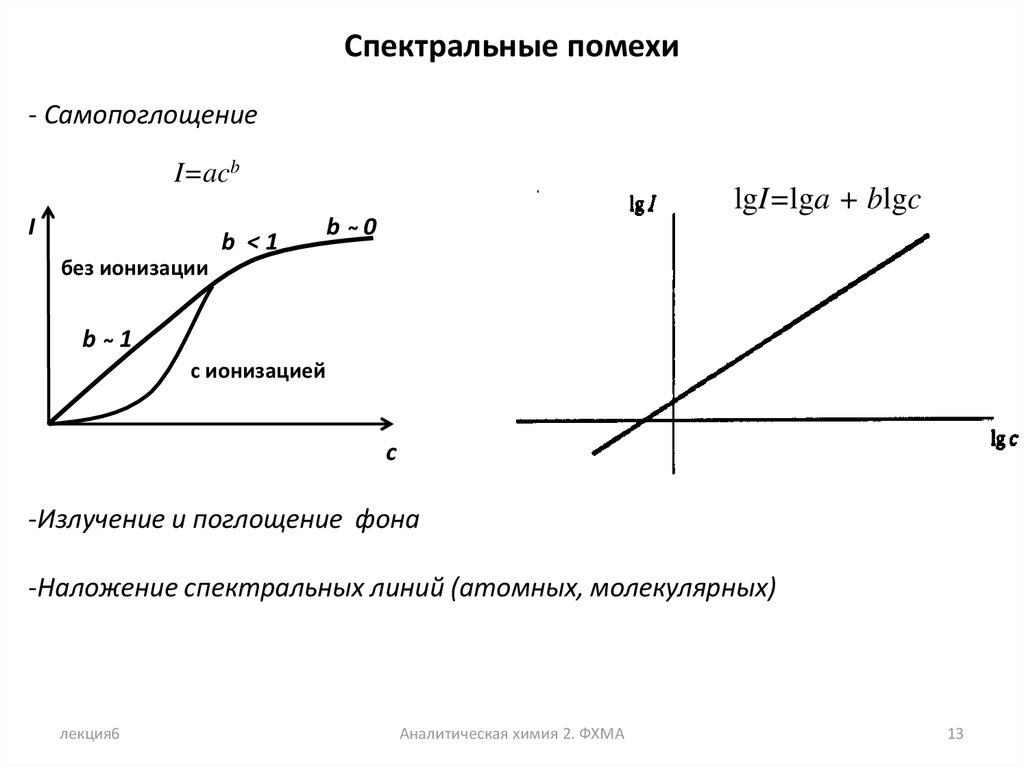
Спектральные помехи- Самопоглощение
I=acb
I
b <1
lgI=lga + blgc
b ̴0
без ионизации
b ̴1
с ионизацией
c
-Излучение и поглощение фона
-Наложение спектральных линий (атомных, молекулярных)
лекция6
Аналитическая химия 2. ФХМА
13
14.
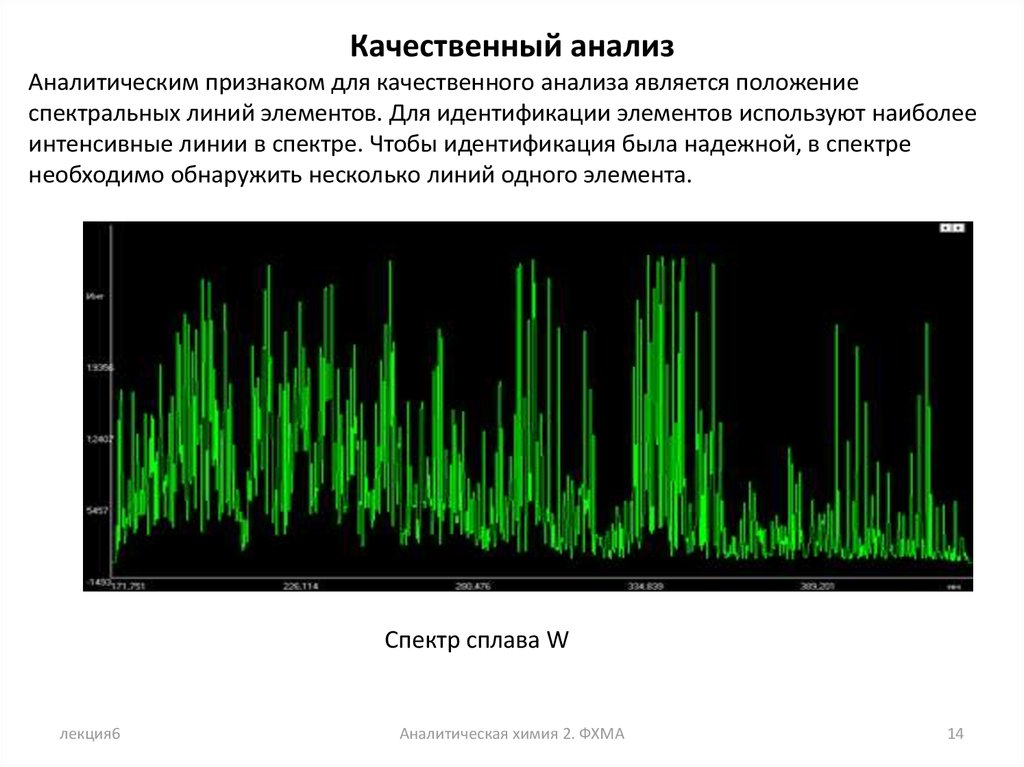
Качественный анализАналитическим признаком для качественного анализа является положение
спектральных линий элементов. Для идентификации элементов используют наиболее
интенсивные линии в спектре. Чтобы идентификация была надежной, в спектре
необходимо обнаружить несколько линий одного элемента.
Спектр сплава W
лекция6
Аналитическая химия 2. ФХМА
14
15.
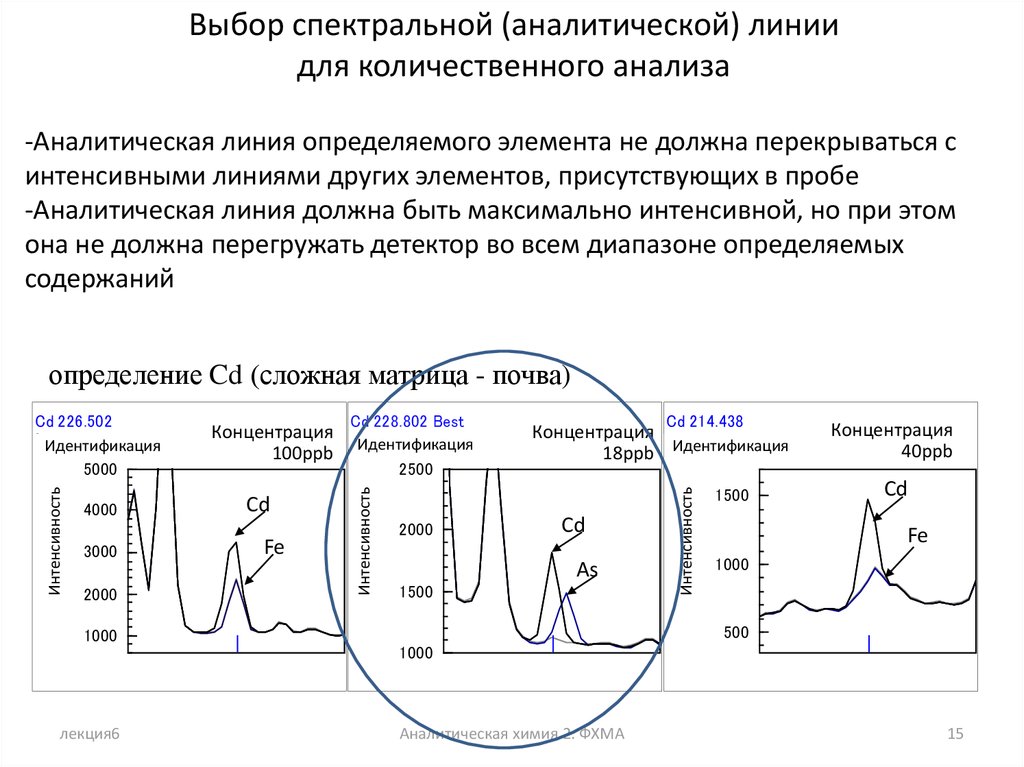
Выбор спектральной (аналитической) линиидля количественного анализа
-Аналитическая линия определяемого элемента не должна перекрываться с
интенсивными линиями других элементов, присутствующих в пробе
-Аналитическая линия должна быть максимально интенсивной, но при этом
она не должна перегружать детектор во всем диапазоне определяемых
содержаний
определение Cd (сложная матрица - почва)
3000
2000
2500
Cd
Fe
2000
Cd 214.438
Концентрация Џ р
ЊЏ
1
18ppb Идентификация
Cd
As
1500
Intensity
Интенсивность
4000
Cd 228.802 Best
Концентрация ’ и
ђ «
100ppb Идентификация
Интенсивность
Intensity
Intensity
Интенсивность
Cd 226.502
’ Идентификация
ђ «
и
5000
1500
Концентрация
40ppb
Cd
Fe
1000
500
1000
1000
лекция6
Аналитическая химия 2. ФХМА
15
16.
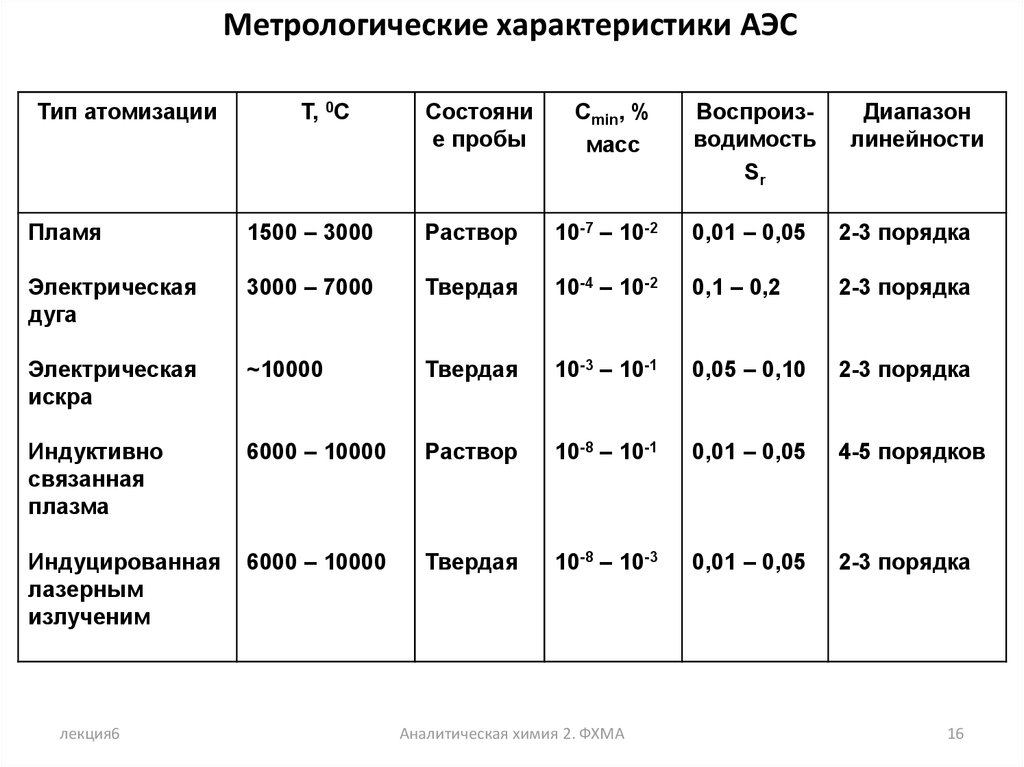
Метрологические характеристики АЭСТип атомизации
Т, 0С
Состояни
е пробы
Сmin, %
масс
Воспроизводимость
Sr
Диапазон
линейности
Пламя
1500 – 3000
Раствор
10-7 – 10-2
0,01 – 0,05
2-3 порядка
Электрическая
дуга
3000 – 7000
Твердая
10-4 – 10-2
0,1 – 0,2
2-3 порядка
Электрическая
искра
~10000
Твердая
10-3 – 10-1
0,05 – 0,10
2-3 порядка
Индуктивно
связанная
плазма
6000 – 10000
Раствор
10-8 – 10-1
0,01 – 0,05
4-5 порядков
Индуцированная
лазерным
излученим
6000 – 10000
Твердая
10-8 – 10-3
0,01 – 0,05
2-3 порядка
лекция6
Аналитическая химия 2. ФХМА
16
17.
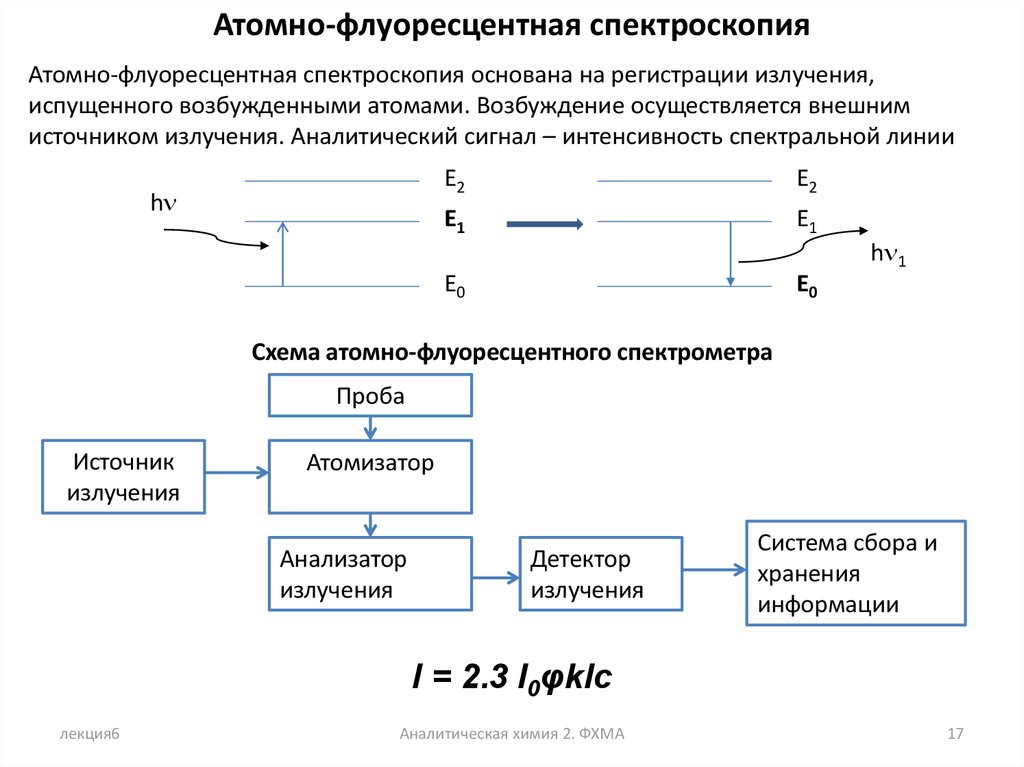
Атомно-флуоресцентная спектроскопияАтомно-флуоресцентная спектроскопия основана на регистрации излучения,
испущенного возбужденными атомами. Возбуждение осуществляется внешним
источником излучения. Аналитический сигнал – интенсивность спектральной линии
hn
E2
E2
E1
E1
hn1
E0
E0
Схема атомно-флуоресцентного спектрометра
Проба
Источник
излучения
Атомизатор
Анализатор
излучения
Детектор
излучения
Система сбора и
хранения
информации
I = 2.3 I0φklc
лекция6
Аналитическая химия 2. ФХМА
17
18.
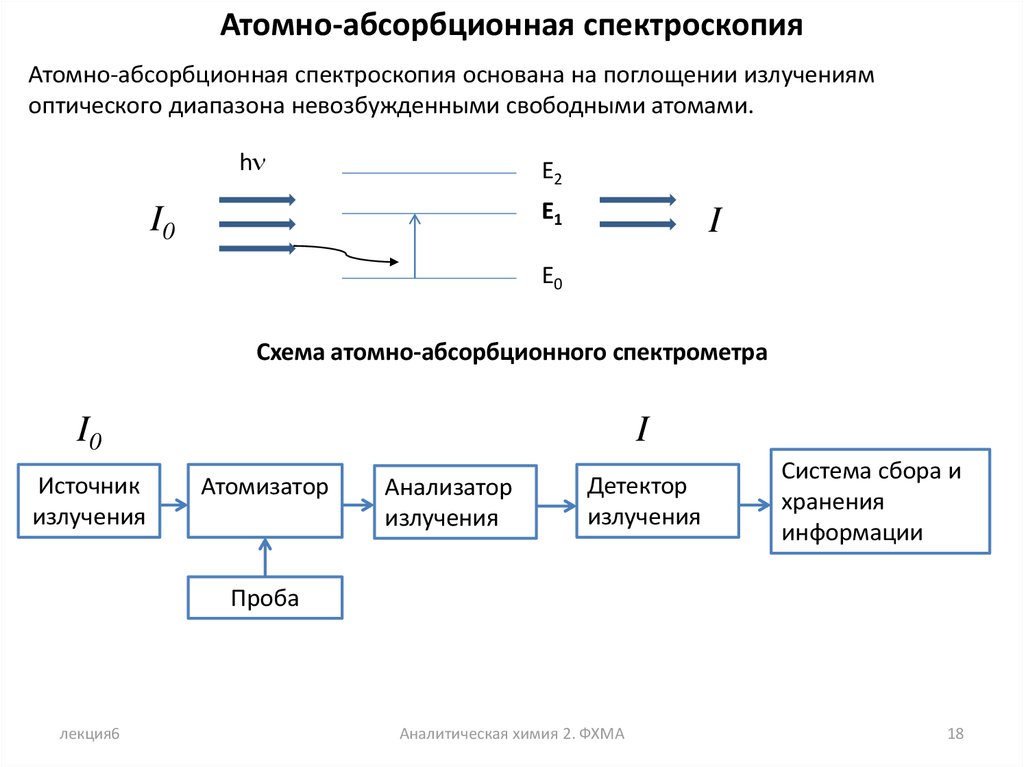
Атомно-абсорбционная спектроскопияАтомно-абсорбционная спектроскопия основана на поглощении излучениям
оптического диапазона невозбужденными свободными атомами.
hn
E2
E1
I0
I
E0
Схема атомно-абсорбционного спектрометра
I0
Источник
излучения
I
Атомизатор
Анализатор
излучения
Детектор
излучения
Система сбора и
хранения
информации
Проба
лекция6
Аналитическая химия 2. ФХМА
18
19.
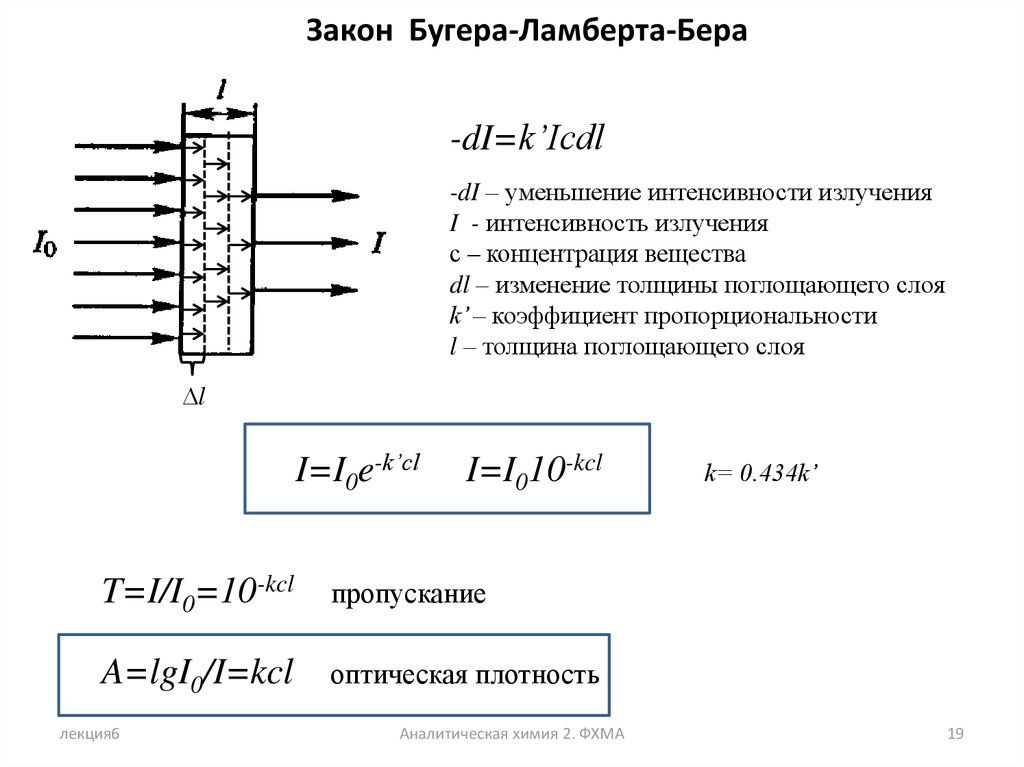
Закон Бугера-Ламберта-Бера-dI=k’Icdl
-dI – уменьшение интенсивности излучения
I - интенсивность излучения
с – концентрация вещества
dl – изменение толщины поглощающего слоя
k’ – коэффициент пропорциональности
l – толщина поглощающего слоя
Dl
I=I0e-k’cl
I=I010-kcl
T=I/I0=10-kcl
пропускание
A=lgI0/I=kcl
оптическая плотность
лекция6
Аналитическая химия 2. ФХМА
k= 0.434k’
19
20.
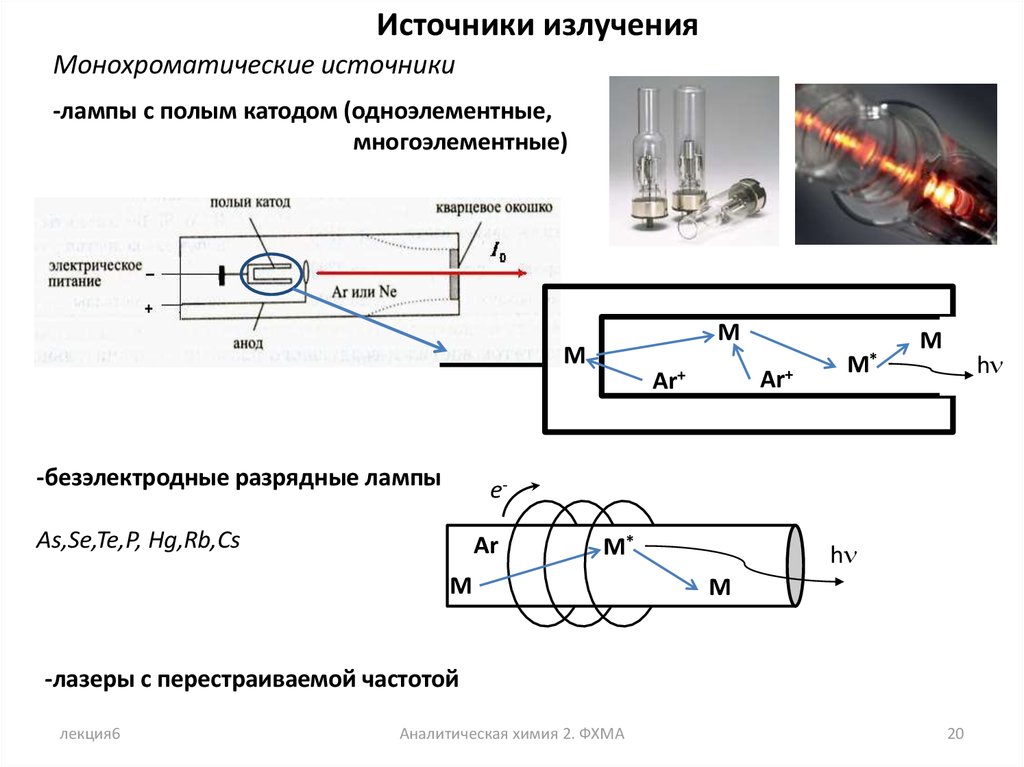
Источники излученияМонохроматические источники
-лампы с полым катодом (одноэлементные,
многоэлементные)
M
M
-безэлектродные разрядные лампы
Ar+
Ar+
M*
M
hn
e-
As,Se,Te,P, Hg,Rb,Cs
Ar
M*
M
hn
M
-лазеры с перестраиваемой частотой
лекция6
Аналитическая химия 2. ФХМА
20
21.
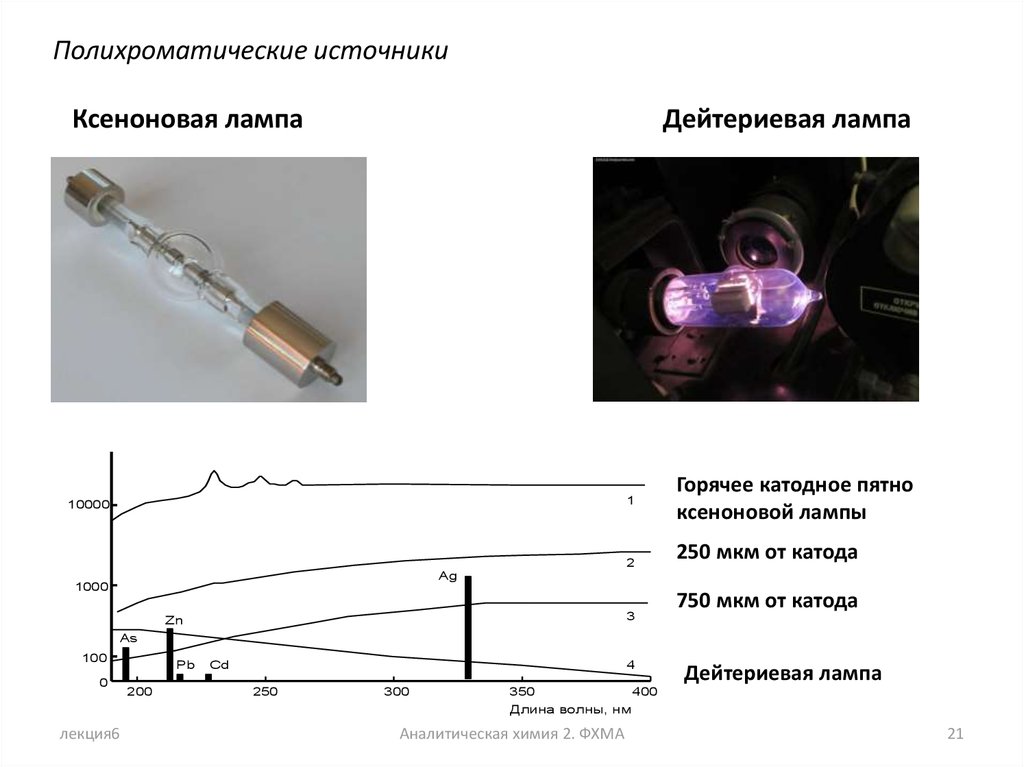
Полихроматические источникиКсеноновая лампа
Дейтериевая лампа
Мощность излучения, мВт см-2стерадиан-1нм-1
1
10000
2
Горячее катодное пятно
ксеноновой лампы
250 мкм от катода
Ag
1000
3
Zn
750 мкм от катода
As
100
0
Pb
200
Cd
4
250
300
350
Дейтериевая лампа
400
Длина волны, нм
лекция6
Аналитическая химия 2. ФХМА
21
22.
Способы атомизации- пламя (смеси различных горючих газов)
Атомизация пламенем
- электротермический (в графитовой печи)
- техника гидридных соединений
-холодного пара
Электротермическая атомизация
графитовая
трубка
температурная программа
электротермического атомизатора
о
Ат
ввод
пробы
металлические контакты
для подвода напряжения
Температура
Ar,Xe
2500
я
облако
атомного
пара
M
I
Отжиг
ци
I0
за
ми
3000
2000
1500
Пиролиз
1000
500
Сушка
0
Время
лекция6
Аналитическая химия 2. ФХМА
22
23.
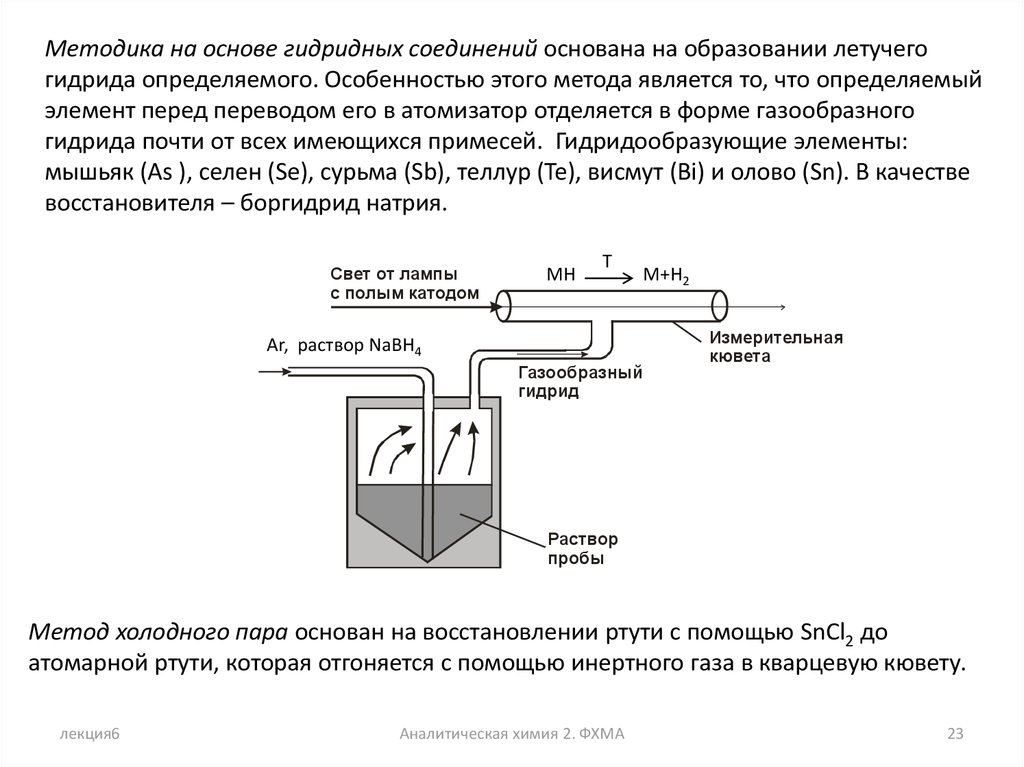
Методика на основе гидридных соединений основана на образовании летучегогидрида определяемого. Особенностью этого метода является то, что определяемый
элемент перед переводом его в атомизатор отделяется в форме газообразного
гидрида почти от всех имеющихся примесей. Гидридообразующие элементы:
мышьяк (As ), селен (Se), сурьма (Sb), теллур (Te), висмут (Bi) и олово (Sn). В качестве
восстановителя – боргидрид натрия.
Свет от лампы
с полым катодом
MH
T
Ar,Раствор
растворNaBH
NaBH4 4
Газообразный
гидрид
M+H2
Измерительная
кювета
Раствор
пробы
Метод холодного пара основан на восстановлении ртути с помощью SnCl2 до
атомарной ртути, которая отгоняется с помощью инертного газа в кварцевую кювету.
лекция6
Аналитическая химия 2. ФХМА
23
24. Сравнение метрологических характеристик различных способов атомизации
Пламенная атомизацияЭлектротермическая
атомизация
Гидридная техника и метод
холодного пара
лекция6
- высокая точность
- высокая скорость
- предел обнаружения в области миллионных
долей (0.01 – 1 ppm; 10-6 -10-4 масс.%)
- предел обнаружения в области миллиардных
долей (0.01- 1 ppb, 10-9 - 10-7 масс.%)
- малые объемы пробы (5-50мкл)
- возможность анализа твердых образцов
- наилучшие пределы обнаружения
для Hg, As, Bi, Sb, Se, Sn, Te
- малое влияние матричных эффектов
Аналитическая химия 2. ФХМА
24
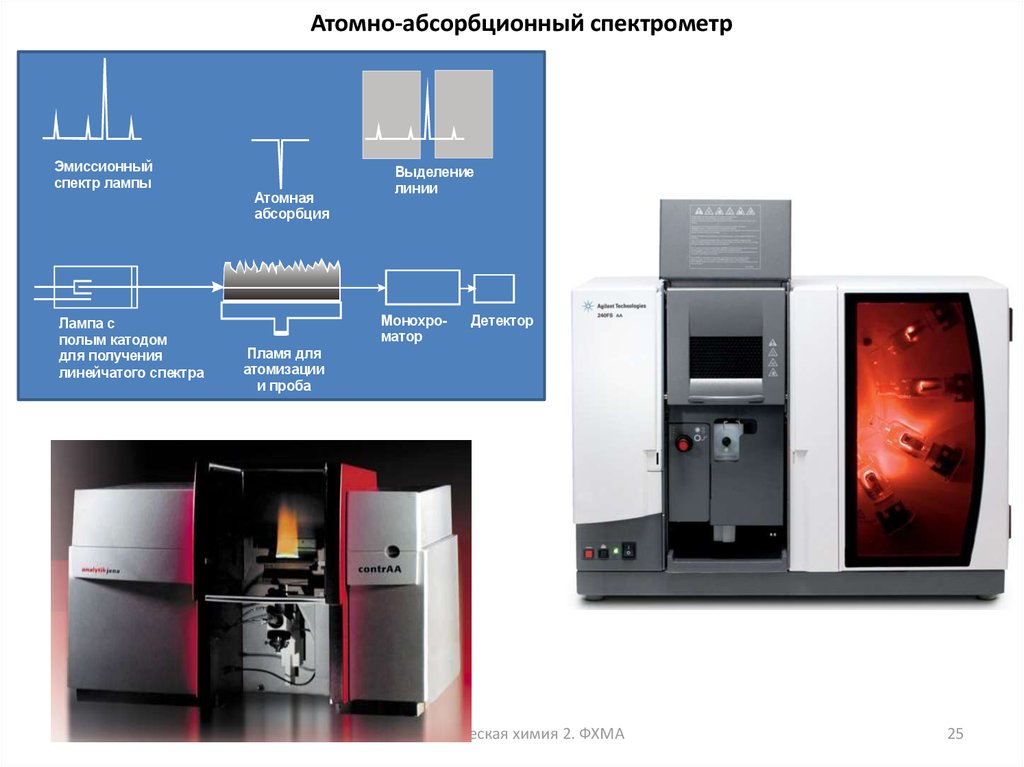
25.
Атомно-абсорбционный спектрометрЭмиссионный
спектр лампы
Лампа с
полым катодом
для получения
линейчатого спектра
лекция6
Атомная
абсорбция
Выделение
линии
Монохроматор
Детектор
Пламя для
атомизации
и проба
Аналитическая химия 2. ФХМА
25
26.
Спектральные помехи-излучение фона
-поглощение фона
дейтериевая коррекция
зеемановская коррекция
лампа с
полым
катодом
Дейтериевая
лампа
Поляризатор
атомизатор
в маг.
анализатор
поле
частоты
Детектор и регистрирующее
устройство
Монохроматор
Делитель
пучка
Лампа
с полым
катодом
Физико-химические помехи
-полнота испарения и атомизация пробы
-ионизация
лекция6
Аналитическая химия 2. ФХМА
26
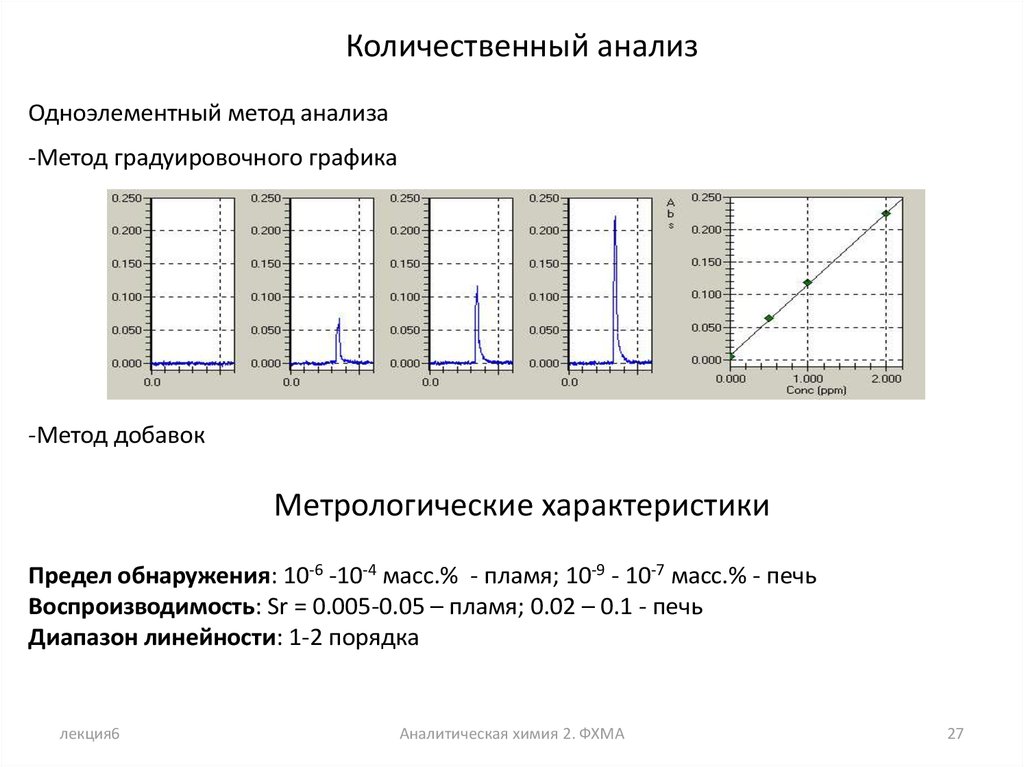
27.
Количественный анализОдноэлементный метод анализа
-Метод градуировочного графика
-Метод добавок
Метрологические характеристики
Предел обнаружения: 10-6 -10-4 масс.% - пламя; 10-9 - 10-7 масс.% - печь
Воспроизводимость: Sr = 0.005-0.05 – пламя; 0.02 – 0.1 - печь
Диапазон линейности: 1-2 порядка
лекция6
Аналитическая химия 2. ФХМА
27









 Физика
Физика








