Похожие презентации:
Предпосылки возникновения геномики. Основные положения классической генетики. Вклад генетики микроорганизмов
1. ОСНОВЫ ГЕНОМИКИ И ПРОТЕОМИКИ
Тема 1. Предпосылки возникновения геномики. Основные положенияклассической генетики. Вклад генетики микроорганизмов. Молекулярная
генетика. Центральная догма молекулярной биологии. Биоинформатика.
Развитие аналитических методов. Технологии рекомбинантных ДНК.
Проект «Геном человека».
2.
ОПРЕДЕЛЕНИЯГено́мика — раздел молекулярной генетики, посвященный изучению
генома и генов живых организмов (Википедия).
Геномика — направление современной молекулярной биологии,
основными задачами которого являются секвенирование геномов (т.е.
определение нуклеотидной последовательности суммарного набора
молекул ДНК клетки какого-либо организма), их картирование (т.е.
идентификация генов и локализация места их расположения на
хромосоме) и сравнительный анализ структур геномов разных
организмов.
Геномика — комплексная наука, изучающая геномы.
Геномика — раздел молекулярной генетики, посвященный
изучению общих принципов построения геномов и их
структурно-функциональной организации, путем
секвенирования, картирования и идентификации функций
генов и внегенных элементов.
Геномика — наука о геномах всех живых существ.
3.
ГЕНОМ- это наследственный аппарат клетки,
содержащий весь объем информации,
необходимой для:
•развития организма,
•его существования в определенных
условиях среды,
•эволюции и
•передачи всех наследственных
свойств в ряду поколений.
ПРОТЕОМ
- совокупность белковых структур
организма, определяемых геномом.
PROTEOME: entire PROTEin complement expressed by genOME
4.
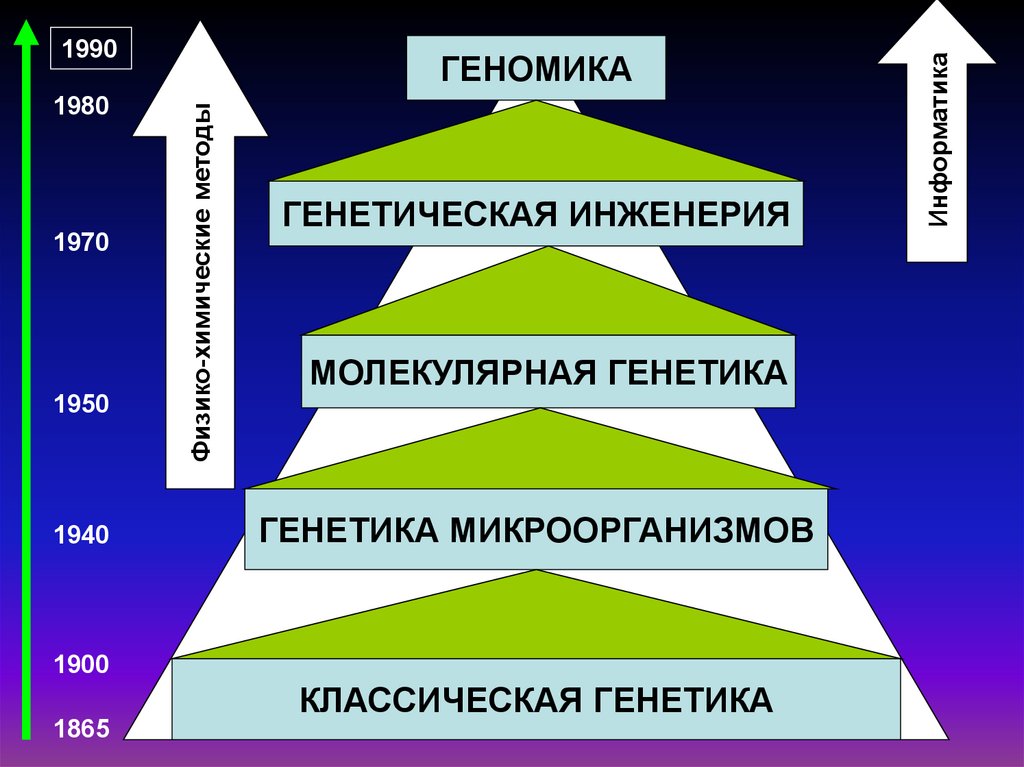
19701950
1940
Физико-химические методы
1980
ГЕНОМИКА
ГЕНЕТИЧЕСКАЯ ИНЖЕНЕРИЯ
МОЛЕКУЛЯРНАЯ ГЕНЕТИКА
ГЕНЕТИКА МИКРООРГАНИЗМОВ
1900
1865
КЛАССИЧЕСКАЯ ГЕНЕТИКА
Информатика
1990
5.
Геномика направлена на анализ структуры генома как целого изанимается изучением всей совокупности происходящих процессов
и обеспечивающих их механизмов.
Поэтому само возникновение геномики как отрасли научного знания
было вызвано возможностью получения огромных объемов данных
о нуклеотидных последовательностях и необходимостью быстрого и
качественного анализа получаемой информации.
6.
Научные и технологические условия 1980-х годов сталикатализатором дискуссий по секвенированию геномов
некоторых видов живых организмов:
Выделение ДНК;
Электрофорез;
Рестрикция;
Лигирование;
Гибридизация;
ПЦР;
Клонирование больших фрагментов ДНК;
Методы секвенирования;
Применение компьютерных технологий в
генетике.
7.
Технологии ДНК-секвенирования появились благодаря работам ученыхВ. Гилберта и А. Максама (Maxam, Gilbert, 1977), Ф. Сэнгера и А.
Коулсона (Sanger, Coulson, 1975).
В 1973 г. Вальтером Гилбертом и Алленом Максамом получена
последовательность участка гена лактозного оперона длиной в 24
нуклеотида:
5'—TGGAATTGTGAGCGGATAACAATT 3'
3'—ACCTTAACACTCGCCTATTGTTAA 5'
Метод химической модификации
2
1
4
3
8.
Прорыв в области секвенирования ДНК случился, когда английскийбиохимик Фред Сэнгер в 1975 г. предложил для чтения
последовательностей ДНК метод терминации цепи.
Химико-ферментативный метод
(дидезоксисеквенирование).
1
ДНК-полимераза;
дНТФ;
меченые ддНТФ
2
3
9.
Самым первым был прочтен ген белка оболочкибактериофага MS2 (РНК-вируса) в лаборатории
Валтера Файерса (Walter Fiers) в 1972 г.
В 1976 г. секвенирован его полный геном. Он состоит из 3569
нуклеотидов оцРНК и содержит 4 гена (mat, cp, lys, rep),
которые кодируют только 4 белка: белок созревания (A-белок),
белок оболочки, белок лизиса и репликазу, соответственно.
10.
В 1977 г. был полностью секвенирован геномбактериофага Ø-X174; кольцевая дцДНК,
длиной 5 386 нуклеотидов, содержащая 11
генов.
Проект осуществлялся под руководством
Фреда Сэнгера.
В 1985 г. метод Сэнгера был существенно улучшен в лаборатории Лероя Худа,
где радиоактивную метку заменили светящейся флуоресцентной меткой.
Каждый отрезок ДНК теперь был окрашен разными цветами в зависимости от
того, на каком нуклеотиде обрывалась цепь. Это дало возможность создать
первый автоматический секвенатор. Фрагменты разделялись на геле по
размерам, и машина автоматически считывала спектр свечения поступающих
полос, выдавая результаты на компьютер.
11.
Стандартное ДНК секвенирование98% точность в определении основания
капилляры 50 см
2,5 часа при 500 С
650 н
24 час - 23400 оснований
Prober JM et al. A system for rapid DNA sequencing with fluorescent chainterminating dideoxynucleotides //Science, 1987. - Vol. 238, no. 4825. - pp. 336-341
12.
В июне 1985 года в Университете Калифорниив Санта-Крус началось совещание, направленное
на изложение практических задач секвенирования
генома человека.
Сама идея прочитать геном человека родилась
в 1986 г. по инициативе Департамента Энергии
США, который впоследствии финансировал
проект.
13.
В 1988 г. начато создание проектапо инициативе лауреата Нобелевской премии,
отца двойной спирали Джеймса Уотсона.
• В 1988 г. Национальный институт здоровья (US National Institutes
of Health - NIH) создал Объединенный комитет для разработки
плана этого проекта (В 1997 г. название изменено на
Национальный институт исследований человеческого генома - NHGRI).
В 1990 г. проект «Геном человека» (HGP — human genome project)
был запущен официально, благодаря государственному
финансированию лабораторий США : US National Institutes of
Health (NIH) и Department of Energy.
Главой проекта «Геном Человека» был назначен Дж.
Уотсон в NIH (1994 г. - Фрэнсис Коллинз).
Стартовый объем годового финансирования составил
в США 30, а в России 10 млн долларов.
14.
В 1989 г. к проекту присоединилась Россия по инициативеакадемика Александра Александровича Баева.
Координатор – Институт молекулярной биологии им.
В.А. Энгельгардта РАН. По проекту работало
около 100 групп, исследовали 3-, 13- и 19-ю хромосомы.
Далее присоединились лаборатории институтов
стран: Франции, Великобритании, Германии, Японии,
Китая, Бразилии, (>50).
1903-1994 гг
В выполнении проекта было задействовано
несколько тысяч ученых, специализирующихся в
биологии, химии, математике, физике и технике, даже
таких малых стран, как Швеция, Дания, Нидерланды.
15.
В 1990-х Э. Ландер основал новый центрГеномных исследований Уайтхед и MIT (WICGR).
Новый центр стал одним из основных партнеров
национального института здравоохранения и
других научно-исследовательских лабораторий
в выполнении международного проекта «геном
человека» (HGP).
Whitehead Institute for
Biomedical Research, Center for
Genome Research,
Кембридж, Массачусетс, США
Broad Institute - 2003
(MIT, Harvard, the Whitehead
institute and affiliated hospitals)
16.
В 1999 г. создана международная организация по изучениюгенома человека: The Human Genome Organization (HUGO),
г. Бетесда (США), вице-президентом которой несколько лет был
академик А.Д. Мирзабеков.
1937-2003 гг
Далее членом Всемирного совета по исследованию
генома человека от нашей страны был проф. Н.К.
Янковский - заведующий лаборатории анализа
генома Института общей генетики им. Н.И. Вавилова,
г. Москва.
17. Проект «ГЕНОМ ЧЕЛОВЕКА»
Основная цель проекта HGP –определить последовательность
всех оснований ДНК, составляющих
гаплоидный набор генома человека
и установить локализацию всех генов,
что помогло бы выяснить причины
наследственных заболеваний и этим
открыть пути к их лечению.
2n=46
9
Геном человека — это около 3,2 млрд нуклеотидных звеньев, 3.2х10 п.н.
распределенных между 23 парами хромосом в ядре; всего
около двух метров ДНК в каждой клетке.
Проект «Геном человека» планировал определить
последовательность в общей сложности 12 раз.
18. ДЛЯ РЕШЕНИЯ ПРОБЛЕМЫ БЫЛО СФОРМУЛИРОВАНО ПЯТЬ ОСНОВНЫХ ЗАДАЧ:
1.составление детальной генетической карты каждой хромосомы
– разрешение 2 Мб;
2.
составление полных физических карт низкого разрешения
каждой хромосомы – разрешение 0,1 Мб;
3.
составление физической карты высокого разрешения всего
генома в виде охарактеризованных по отдельности клонов –
разрешение 5 Кб;
4.
полное секвенирование ДНК – разрешение 1 н.;
завершить к 2004 году;
5.
нанести на полностью завершенную секвенсовую карту все
гены человека и определить их функциональное значение к
2005 году.
(95%-ный охват генома человека за 15 лет):
Ожидали, что, когда все указанные цели будут достигнуты, исследователи
определят все функции генов и разработают методы биологического и
медицинского применения полученных данных.
19. В ходе работ планировали секвенировать геномы других организмов:
Е. coli (4.6 Мб)D. melanogaster (180 Мб)
S. cerevisiae (12.1 Мб)
М. musculus (2700 Мб)
С. elegans (97 Мб)
A. thaliana (125 Мб)
20.
По научной значимости для биологии проект HGPсравнивают со значением открытия периодической системы
для химии.
21.
Н.К. Янковский:«Число букв в гаплоидном наборе человека
примерно равно числу букв в подшивке газеты
«Известия» за тридцать лет».
3,2 млрд п.н. +
3,2 млрд п.н.
1014 клеток у взрослого
Длина всей ДНК клетки
около 2 м
Длина ДНК в каждом из Вас превышает в тысячу раз расстояние от Земли до
Солнца.
22.
Сидней Бреннер: «… Секвенированием должнызаниматься заключенные!»
Самая маленькая хромосома (Y)
Самая большая (1)
Весь геном
50 Мб;
250 Мб;
3200 Мб
При методах первого поколения:
самый большой участок ДНК, выделяемый препаративно
из хромосом
0,35 Мб,
на самом лучшем оборудовании
можно было секвенировать
Стоимость
ок. 0,001 Мб/день
от 0,05 до 0,1 Мб/год
1-2 $ за 1 основание
30 тыс. дней непрерывной работы при стоимости только секвенирования
(без учета всех остальных операций)
3 млрд долларов
1 млн п.н. = 1 Мб (мегабаза); 1 тыс. п. н. = = 1 кб (килобаза)
23.
Стоимостьсеквенирования
генома человека
1988
3 МЛРД $
1990
1991
США
1992-1995
60 млн $
135 млн $
Один из самых дорогостоящих научных проектов
в истории цивилизации
165 до 187 млн $
1996
1997
1998
200 млн $
225 млн $
253 млн $
2001
Done it!
2009
100’000 $
(4 000 $)
2014
1’000 $
Соотношение финансирования в 1990 г. Россия:США – 1:1000.
24.
БиоинформатикаЭкспериментальные
лаборатории
Сервера NCBI,
EMBL, DDJB
Электронные
базы данных в
Internet
• GenBank
• UniGene
• TIGR
• TRANSFAC
• SWISS-PROT
• Pubmed
• MedLine
Любой специалист в мире может практически беспрепятственно
войти в эти банки данных и воспользоваться для
исследовательских целей собранной там информацией.
25.
Необходимо решение этических,юридических и социальных аспектов
проекта HGP:
Программа ЭЮСА или англ. ELSI (The Ethical, Legal
and Social Implications Research Program):
(1) Защита частной жизни и устранение дискриминации
при использовании и интерпретации генетической информации;
(2) Проблема переноса и применения генетических знаний,
полученных в исследовательских лабораториях,
в клиническую практику;
(3) Информированное согласие участников генетических
исследований;
(4) Общественное просвещение и профессиональное образование.
26.
Временная шкала, отражающая началои выполнение работ по геномным проектам
27.
Прочтение первого миллиарда пар нуклеотидов заняло у мировогонаучного сообщества 4 года, следующий миллиард был прочтен за 4
месяца.
Июнь 2000 г.
Lander e.a., Nature (2001), v.409, p.860
28.
Крег Вентер, The Institute for Genome Research (TIGR)В сентябре 1999 г. в частной компании
Celera были начаты исследования
по проекту «Геном человека».
В июне 2000 г. расшифровка
последовательности генома была
завершена.
Сиквенс генома человека занял 9 месяцев 10 дней и
200 млн долларов за 2000 год, что составило 60% от
средств, затраченных госбюджетом США на эту
программу за тот же период.
29.
30. Первый черновой вариант генома человека – 2001 г.
•последовательность не соответствовала ни одному конкретномучеловеку: 2 европейца, 1 африканец, 1 китаец, 1 мексиканец (2
женщины, 3 мужчин);
•геном был прочтен с точностью в 10 раз ниже необходимой
(заданная точность — не более одной ошибки на 10000
нуклеотидов, с такой точностью было прочтено лишь 25%
последовательностей;
•прочтено только 3 раза;
•50 тыс. пробелов в последовательности ДНК, суммарный размер
которых был около 150 Мб;
•не расшифрованы 15% генома, которые представлены
гетерохроматином;
частично описаны выявленные в нуклеотидном тексте гены и
регуляторные последовательности.
31.
«Чистовую версию» (с уровнем ошибок не выше 1 на 10 000нуклеотидов) закончили к 2003 г., т. е. к пятидесятилетнему юбилею
открытия двойной спирали ДНК.
Выполненный с максимально возможным в реальности качеством
проект «Геном человека» дал в результате секвенирования только
92,3 % от всей геномной последовательности. Неизвестными
остались не только центромерные и теломерные районы хромосом,
протяженные зоны высокоповторяющихся последовательностей, но
и большие кластеры мультигенных семейств, например генов
иммуноглобулинов.
32.
В течение последних лет исследования проводились в следующихнаправлениях:
Компьютерный анализ полного генома человека и его частей на основе
информации в открытых базах данных. Разработка принципиально новых
подходов к хранению, обработке и получению структурной информации из баз
данных на основе вновь созданного программного обеспечения.
Идентификация новых генов на основе физического, хромосомного и
функционального картирования, клонирования и секвенирования. Структурный
и функциональный анализ вновь найденных генов и регуляции их активности.
Установление cause-and-effect генетических отношений между генами и
предрасположенностью к широко распространенным заболеваниям различной
природы. Выявление роли индивидуальных генов и их мутаций в этиологии и
развитии некоторых заболеваний человека.
Развитие методов генной и геномной диагностики заболеваний человека на
основе знания физической карты и последовательностей нуклеотидов.
Разработка методов генной терапии моногенных заболеваний на основе знаний
о молекулярно-генетических механизмах их возникновения и развития.
Разработка открытых юридических, этических, законодательных, правовых,
социальных и других аспектов исследований генома и использования
информации о структуре и свойствах геномов отдельных людей. Предсказания
путей развития медицины и здравоохранения на основе нового уровня знаний
о геноме человека и формулирование соответствующих практических
предложений.
33.
В начале 2003 г. Конгресс США принялрезолюцию, в соответствии с которой
малоизвестный Международный День
ДНК, отмечаемый 25 апреля, был
объявлен Национальным Днём ДНК.
34.
К 2011 г. полностью секвенированныгеномы: 11326
42 ЭУКАРИОТ (1014 в работе, 36,8%
близки к завершению), 2033
среди них 10 простейших;
6 животных; 19 грибов; 6 растений.
1431 ПРОКАРИОТ 31700
Caenorhabditis elegans - 1998 г.
Arabidopsis thaliana Columbia-O – 2000 г.
Oryza sativa Japonica – 2002 г.
Pan troglodytes verus – 2006 г.
Drosophila virilis 1.25535 – 2009 г.
Zea mays B73 - 2970 Мб – 2009 г.
Sus scrofa Duroc – 2009 г.
Mus musculus – 2010 г.
2970 Мб
Плазмиды – 5681, органеллы - 6416
2559 ВИРУСОВ и
41 ВИРОИДОВ
(4459)
35.
2015 г.36.
NCBI – The National Center for BiotechnologyInformation
37.
38.
39.
Microbial Genome Growthhttp://www.ncbi.nlm.nih.gov/genome/browse/
40.
2007 г.$2 млн
Знать последовательность своей ДНК
не менее важно, чем иметь автомобиль.
2 месяца
454 Life
Sciences
Геномы К.Вентера и Дж.Уотсона
Джеймс Уотсон
Пущино, 20 февраля 2011 г.
41.
Секвенирование – заводской процесс на ABI Prizm 3700at the Whitehead Institute, Center for Genome Research.
Цикл непрерывный при 15 мин труда оператора в сутки
Celera – секвенирует более 1,5 млрд п.н. в месяц.
42.
Приборы для секвенирования ДНК в Объединенном институте генома(Joint Genome Institute), Калифорния, США. Здесь ДНК разрезается на
фрагменты и каждое основание помечается различными
флуоресцентными красителями, так что их может различить детектор.
(Фото: sciencephoto.com, C011/6490)
43.
Приборной основой современной геномики являютсявысокопроизводительные секвенаторы второго поколения.
Методы NGS
(HT-NGS, high-throughput next generation
sequencing)
• Секвенирование синтезом
– Пиросеквенирование
– Полупроводниковое
секвенирование
– Синтез с обратимой терминацией
– Секвенирование в реальном
времени
• Секвенирование лигированием
44.
Френсис Коллинс, директор Национального института геномныхисследований США, выделяет ряд приоритетных задач, решаемых
сегодня с помощью постгеномных технологий:
• генотипирование 2 тыс. человек (по 400 тыс.
однонуклеотидных замен у каждого) по цене 10 тыс. долл. за
генотип (или меньше);
• разработка и внедрение методики секвенирования ДНК на 4-5
порядков более дешевой, чем существующие, то есть геном
человека должен стоить ~1000 долл.;
• создание технологий синтеза молекул ДНК (синтетические
гены, геномы) по цене до 10 центов за основание, то есть
стоимость синтеза одного гена должная быть от 10 до 10 тыс.
долл.;
• разработка методов определения метилирования ДНК в
одной клетке;
• создание технологий, позволяющих проводить
одномоментный мониторинг всех белков в клетке.
45.
46.
•Структурная геномика – последовательностьнуклеотидов в геноме, строение генов и негенных
элементов (повторяющейся ДНК, промоторов,
энхансеров и т.д.), физические, генетические,
транскрипционные карты.
•Антропогеномика – особенности генома человека.
•Функциональная геномика – выявление функций
генов/участков генома, их функциональных
взаимодействий в клеточной системе.
•Сравнительная геномика – организация геномов
разных видов, общие закономерности строения и
функционирования геномов.
Эволюционная геномика – эволюция геномов, происхождение наследственного
разнообразия.
Этногеномика – генетическое разнообразие популяций человека, генетика
происхождения человека как вида, рас, народов.
47.
Практическая геномикаМедицинская геномика (геномная медицина) – применение знаний и
технологий геномики к вопросам клинической и профилактической
медицины (ДНК-диагностика, генотерапия).
Фармакогеномика – определяет влияние генетической информации,
полученной от родителей, на способность реагировать на
лекарственные средства.
Клиническая геномика – геномика и протеомика наследственной
патологии.
Нейрогеномика – изучить протеом и транскриптом тканей, сыворотки
крови и спинномозговой жидкости в норме и при нейропатологиях.
•Компьютерная геномика (Биоинформатика) – создание алгоритмов для
поиска генов, поиска регуляторных сигналов в ДНК, предсказания
структуры и функций белка, его локализации в клетке, для
реконструкции метаболизма.
48. …ОМИКи
• Транскриптомика – выявление функций генов/участковгенома, их функциональных взаимодействий в
клеточной системе.
• РНомика – идентификация некодирующих РНК,
определение количества каждой нкРНК, определение
закономерностей экспрессии всех нкРНК.
• Протеомика – изучение белковых ансамблей в клетке.
• Метаболомика – идентификация и количественное
определение всех метаболитов, синтезируемых (или
находящихся) в данных клетках, тканях, органах и в
биологических жидкостях.
















































 Биология
Биология








