Похожие презентации:
Ионная связь
1. Тема: Ионная связь
2. Вопрос на засыпку:
Какую особенность в строении имеютатомы инертных газов (He, Ne, Ar)?
Атомы этих элементов практически не
образуют соединений с другими
атомами. С чем это может быть
связано?
3. Какие разные элементы!
А это кто?Имеют завершенные уровни,
не взаимодействуют с
другими атомами
Кто это?
Все остальные элементы
Имеют незавершенные уровни,
взаимодействуют с другими
атомами, чтобы завершить
свои энергетические уровни
4. Атомы элементов - металлов
Если мало электронов на внешнемуровне – атом стремится их отдать
Na +11 )2)8)1
атом натрия
Na+ +11 )2)8
Ион (катион) натрия
Атомы элементов – металлов в ПС учебника обозначены
черным, а также зеленым цветом
5. Атомы элементов - неметаллов
Если внешний уровень близок к завершению(т.е. содержит 7, 6, или 5 электронов), атом
стремится принять недостающие до 8 электроны
Cl +17 )2)8)7
атом хлора
Сl- +17 )2)8)8
Ион (анион) хлора
Атомы элементов – неметаллов в ПС обозначены красным цветом
6. Итак…
Атомы металлов имеют тенденцию котдаче электронов с внешнего уровня
Атомы неметаллов имеют тенденцию к
принятию недостающих до завершения
внешнего уровня электронов.
7. В периодах: стр.63
NaMg
Al
Si
P
S
Cl
Металлические свойства ослабевают,
а неметаллические усиливаются, так как:
А) увеличиваются заряды атомных ядер;
Б) увеличивается число электронов на внешнем уровне;
В) число энергетических уровней постоянно;
Г) радиус атома уменьшается;
Д) способность к отдаче электронов ослабевает, а
способность к принятию недостающих электронов
возрастает.
8. В группах (главных подгруппах): стр.63
LiNa
K
щ
е
л
о
ч
н
ы
е
Rb м
Cs
Fr
е
т
а
л
л
ы
Самый
Сильный
Металлические свойства усиливаются,
Неметалл!
а неметаллические ослабевают, так как:
А) увеличиваются заряды атомных ядер;
Б) число электронов на внешнем уровне
постоянно;
В) увеличивается число энергетических
уровней;
Г) увеличивается радиус атома;
Д) способность к отдаче электронов
возрастает, а способность к принятию
недостающих электронов ослабевает.
Самый
Сильный
Металл!
F
г
а
л
о
г
е
н
ы
Cl
Br
I
At
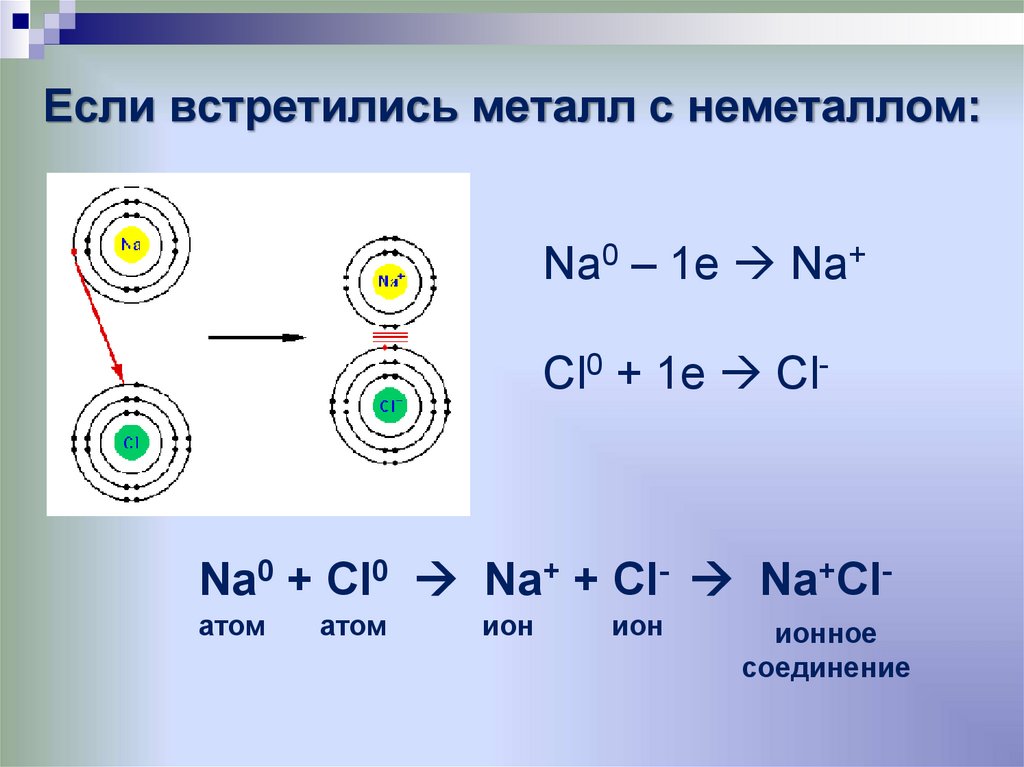
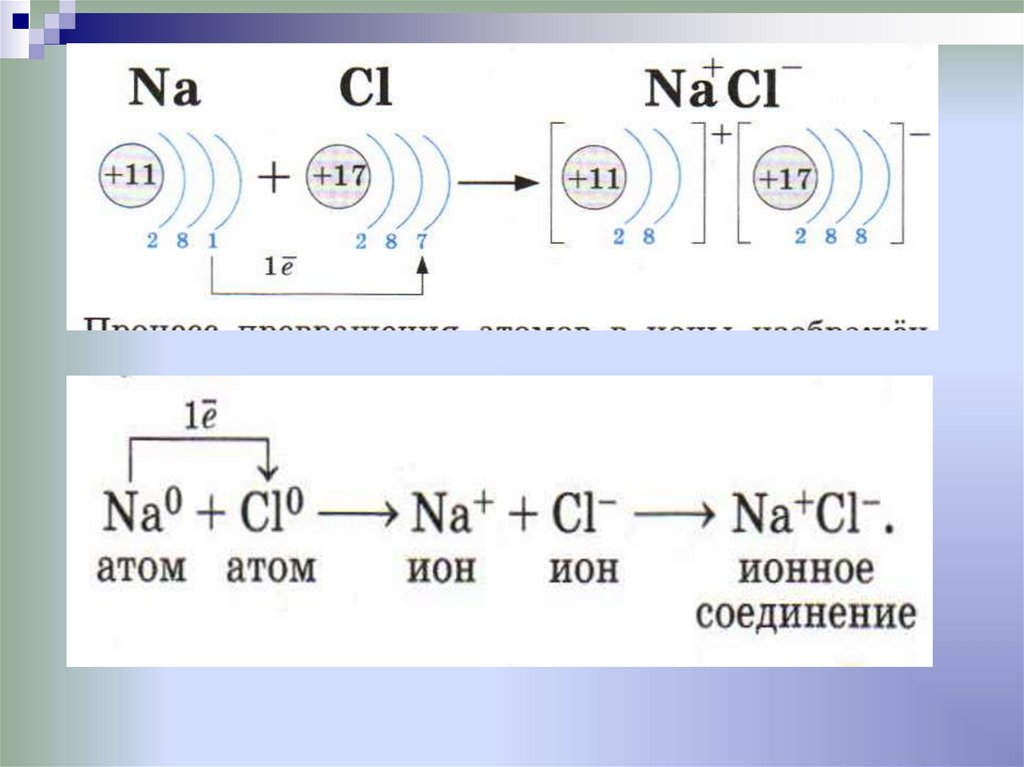
9. Если встретились металл с неметаллом:
Na0 – 1e Na+Cl0 + 1e Cl-
Na0 + Cl0 Na+ + Cl- Na+Clатом
атом
ион
ион
ионное
соединение
10.
11.
12. Ионная химическая связь
это связь, образующаяся междуположительно и отрицательно
заряженными ионами.
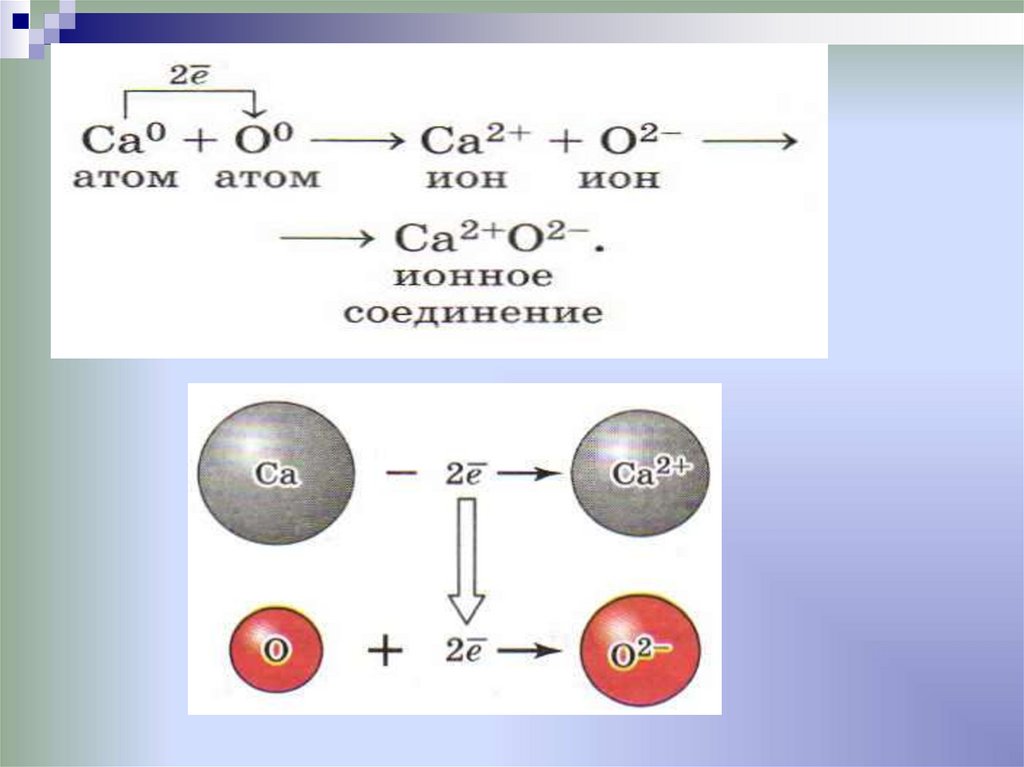
13. Алгоритм составления схемы образования ионной связи.
Разберите алгоритм составленияионной связи на стр.65 §10 учебника.
Пользуясь алгоритмом, составьте
схемы образования ионной связи при
взаимодействии: а) калия и кислорода;
б) лития и хлора; в) магния и фтора.
14. Подведем итоги:
1. Какие группы элементов мы выделили с точкизрения строения внешнего уровня их атомов?
2. Каким образом атомы металлов завершают
свои уровни? А атомы неметаллов?
3. Как называются частицы, в которые
превращаются атомы элементов, принимая или
отдавая электроны?
4. Что такое ионная химическая связь,
в каком случае она образуется?
15. Домашнее задание:
§10, составьте схемы образованияионной связи для элементов с
порядковыми номерами:
а)Na и F б) K и Cl в) Li и O
СПАСИБО ЗА РАБОТУ!












 Химия
Химия








