Похожие презентации:
Синтез ТАГ и ФЛ. Липотропные факторы. Синтез и экскреция холестерина. Транспортные липопротеины крови. Биохимия атеросклероза
1. Синтез ТАГ и ФЛ. Липотропные факторы. Синтез и экскреция холестерина. Транспортные липопротеины крови. Биохимия атеросклероза.
Лекция № 10 для специальности 31.05.01 Лечебное делоподготовлена доцентом ИФОИТ ТГМУ Артюковой О.А.
2020–2021 учебный год
2. Основные вопросы лекции:
Синтез и распад триацилглицеролов и глицерофосфолипидов:последовательность реакций.
Различия синтеза ТАГ в печени и жировой ткани. Ожирение.
Взаимопревращение глицерофосфолипидов.
Жировое перерождение печени. Липотропные факторы.
Синтез холестерола; реакции образования мевалоновой кислоты.
Регуляция активности ГМГ-КоА-редуктазы. Экскреция холестерола.
Желчные кислоты (первичные и вторичные).
Транспортные липопротеины: строение, образование, функции.
Апобелки. Роль липопротеинлипазы и лецитин-холестерин-ацилтрансферазы
(ЛХАТ).
Метаболизм плазменных липопротеинов.
Атеросклероз. Коэффициент атерогенности.
3. Жиры (ТАГ) - наиболее компактная форма запасания энергетического материала в адипоцитах.
Депонирование жиров в жировой ткани происходитв абсорбтивный период, когда увеличивается
соотношение инсулин / глюкагон.
ТАГ в организме в 30 раз больше, чем гликогена.
ТАГ по калорийности превосходят углеводы.
Резерв гликогена (печень) расходуется за 24 час.
ТАГ в жировой ткани могут и не расходоваться
или их хватит на несколько недель.
Важной особенностью ТАГ является то,
что при их гидролизе образуется
2 различных продукта - ЖК и глицерол.
Глицерол используется для глюконеогенеза
и участвует в обеспечении глюкозой клеток
мозга при голодании, а окисление ЖК
является источником АТФ для многих
тканей, прежде всего, мышц.
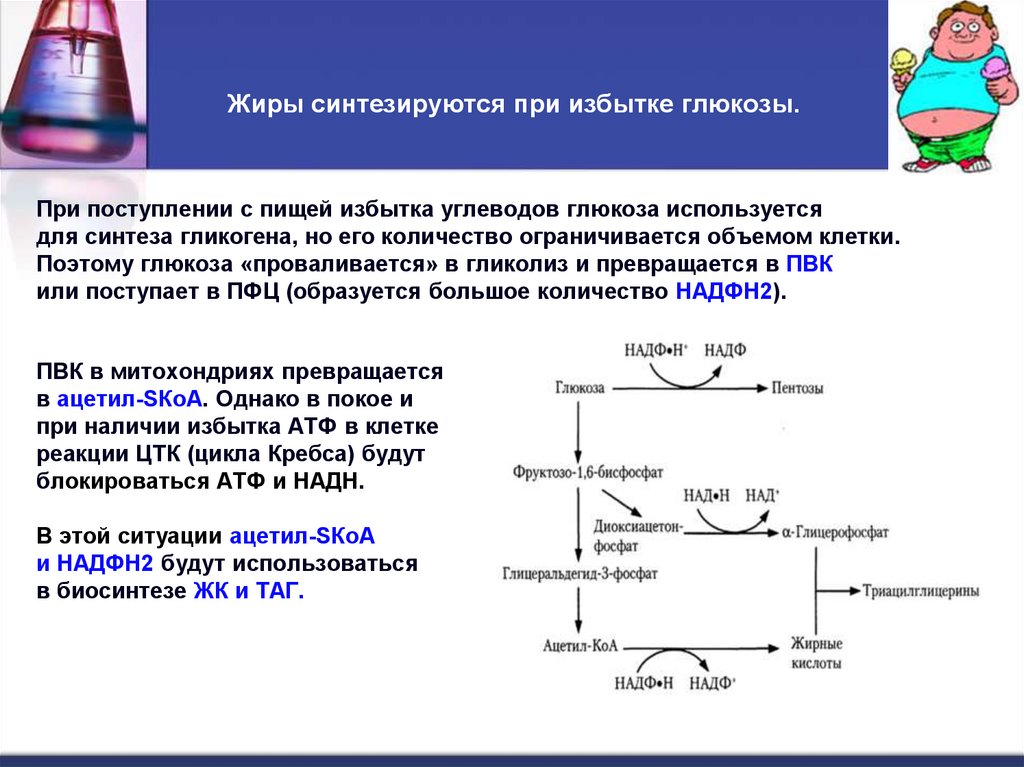
4. Жиры синтезируются при избытке глюкозы.
При поступлении с пищей избытка углеводов глюкоза используетсядля синтеза гликогена, но его количество ограничивается объемом клетки.
Поэтому глюкоза «проваливается» в гликолиз и превращается в ПВК
или поступает в ПФЦ (образуется большое количество НАДФН2).
ПВК в митохондриях превращается
в ацетил-SКоА. Однако в покое и
при наличии избытка АТФ в клетке
реакции ЦТК (цикла Кребса) будут
блокироваться АТФ и НАДН.
В этой ситуации ацетил-SКоА
и НАДФН2 будут использоваться
в биосинтезе ЖК и ТАГ.
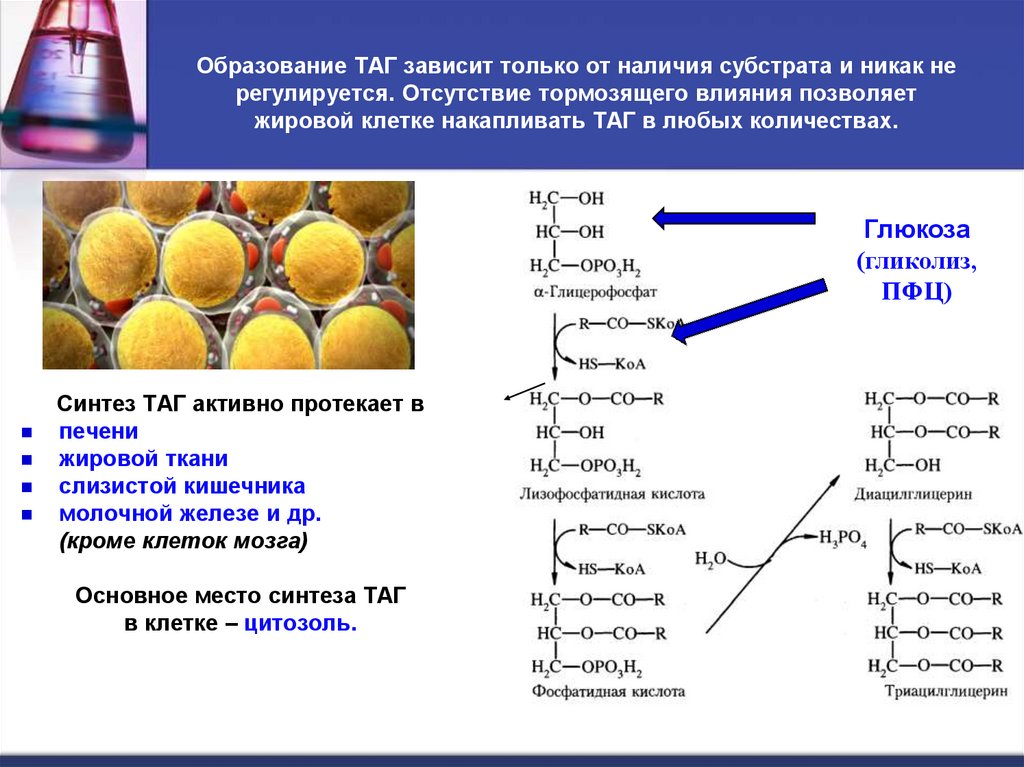
5. Образование ТАГ зависит только от наличия субстрата и никак не регулируется. Отсутствие тормозящего влияния позволяет жировой
клетке накапливать ТАГ в любых количествах.Глюкоза
(гликолиз,
ПФЦ)
Синтез ТАГ активно протекает в
печени
жировой ткани
слизистой кишечника
молочной железе и др.
(кроме клеток мозга)
Основное место синтеза ТАГ
в клетке – цитозоль.
6. Ожирение - это увеличение отложения ТАГ в адипоцитах по сравнению с нормой.
В норме у человека (масса ~70 кг )количество ТАГ в депо составляет 10-11 кг.
Важной характеристикой содержания жира в
организме является индекс массы тела (ИМТ).
Норма ИМТ – 20 - 24,9 кг/м2,
25 - 29,9 кг/м2- избыточный вес, >30 кг/м2 - ожирение.
Ожирение наблюдается у 50% людей старше 50 лет.
Постоянное переедание приводит к гиперплазии
адипоцитов и к развитию тяжелых форм ожирения.
При лечении ожирения наблюдают уменьшение
количества жиров в адипоцитах, но количество
самих адипоцитов практически не изменяется.
Первичное ожирение развивается в результате
алиментарного дисбаланса избыточной калорийности питания
по сравнению с расходами энергии.
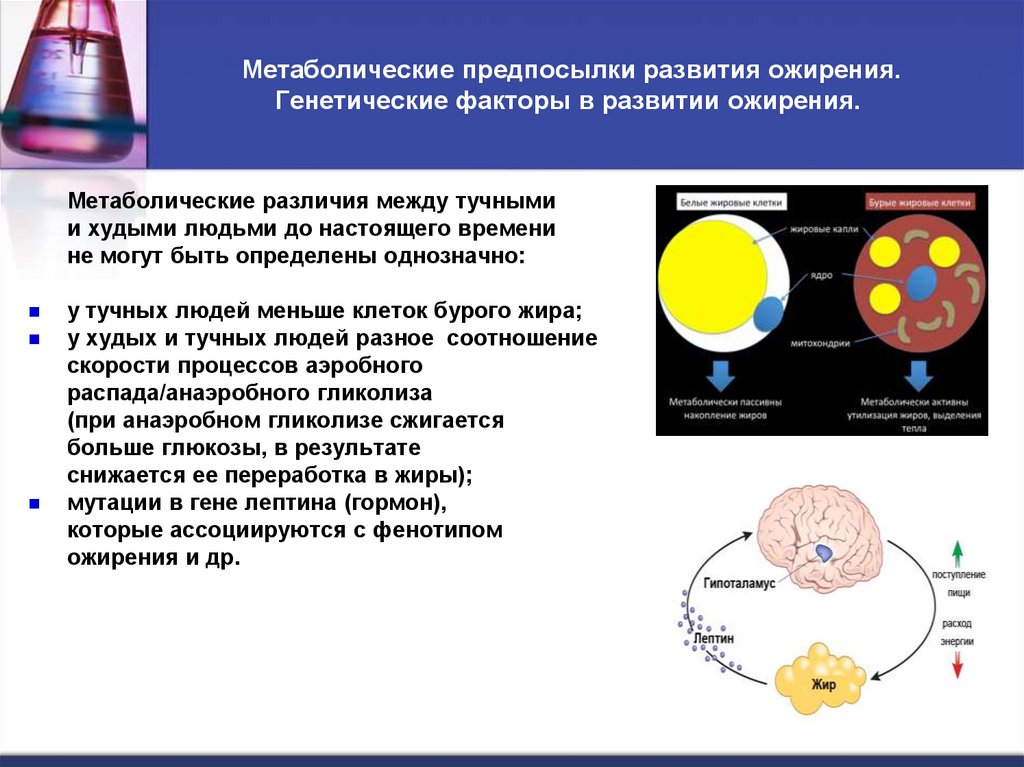
7. Метаболические предпосылки развития ожирения. Генетические факторы в развитии ожирения.
Метаболические предпосылки развития ожирения.Генетические факторы в развитии ожирения.
Метаболические различия между тучными
и худыми людьми до настоящего времени
не могут быть определены однозначно:
у тучных людей меньше клеток бурого жира;
у худых и тучных людей разное соотношение
скорости процессов аэробного
распада/анаэробного гликолиза
(при анаэробном гликолизе сжигается
больше глюкозы, в результате
снижается ее переработка в жиры);
мутации в гене лептина (гормон),
которые ассоциируются с фенотипом
ожирения и др.
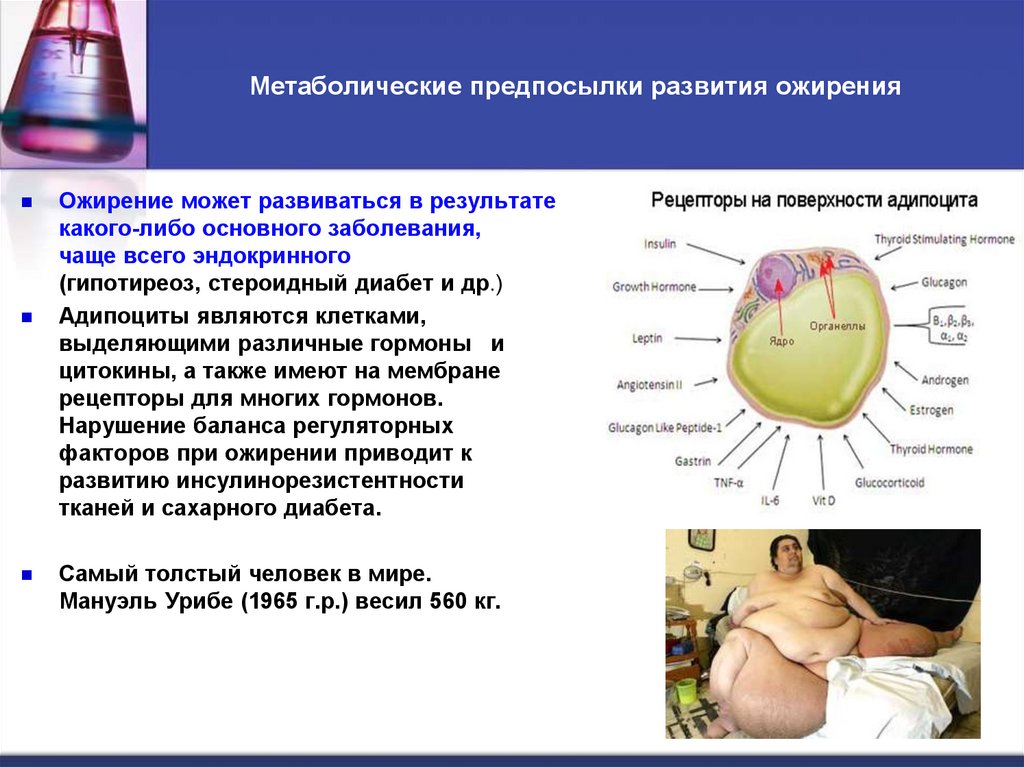
8. Метаболические предпосылки развития ожирения
Ожирение может развиваться в результатекакого-либо основного заболевания,
чаще всего эндокринного
(гипотиреоз, стероидный диабет и др.)
Адипоциты являются клетками,
выделяющими различные гормоны и
цитокины, а также имеют на мембране
рецепторы для многих гормонов.
Нарушение баланса регуляторных
факторов при ожирении приводит к
развитию инсулинорезистентности
тканей и сахарного диабета.
Самый толстый человек в мире.
Мануэль Урибе (1965 г.р.) весил 560 кг.
9.
Избыточный вес (ожирение) может оказывать значительное воздействиена здоровье и приводить к серьезным последствиям, таким как сердечнососудистые заболевания, диабет второго типа, мышечно-скелетные
повреждения (остеоартрит), онкологические заболевания. Эти состояния
становятся причиной преждевременной смерти и устойчивой инвалидности.
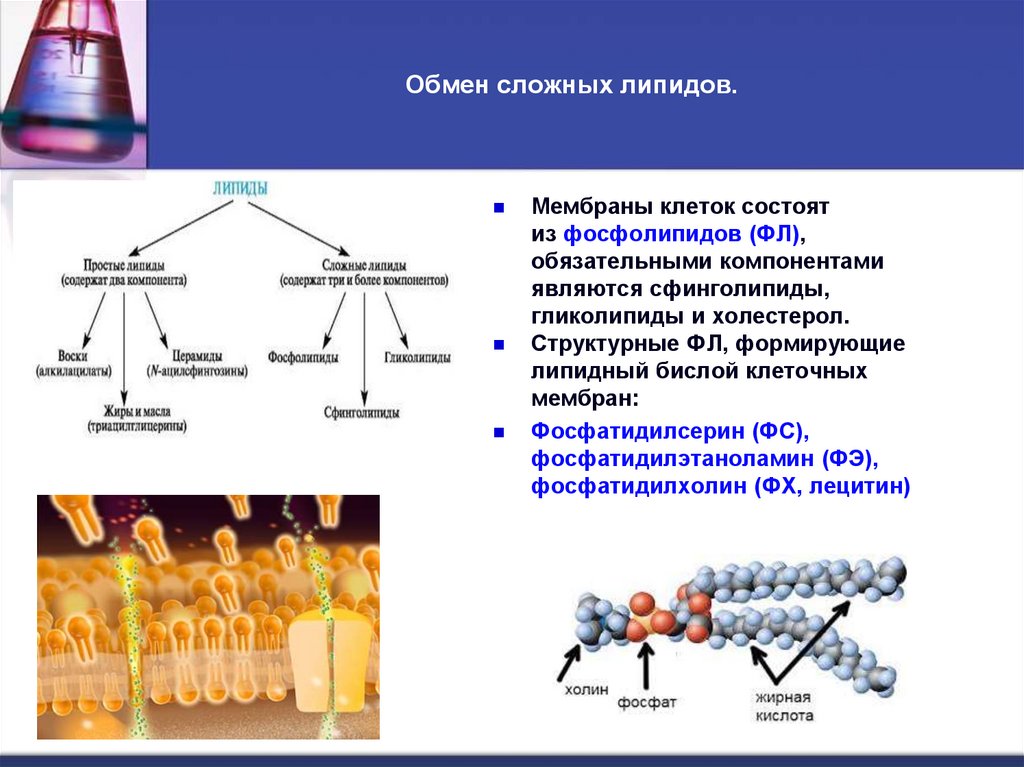
10. Обмен сложных липидов.
Мембраны клеток состоятиз фосфолипидов (ФЛ),
обязательными компонентами
являются сфинголипиды,
гликолипиды и холестерол.
Структурные ФЛ, формирующие
липидный бислой клеточных
мембран:
Фосфатидилсерин (ФС),
фосфатидилэтаноламин (ФЭ),
фосфатидилхолин (ФХ, лецитин)
11. Синтез ФЛ проходит через стадию образования фосфатидной кислоты (ФК).
Наиболее простым ФЛ является фосфатидная кислота (ФК) –
промежуточное соединение в синтезе и ТАГ и ФЛ.
В зависимости от вида жирной кислоты, фосфатидная кислота
может содержать насыщенные или ненасыщенные ЖК:
если для синтеза используются насыщенные и мононенасыщенные кислоты
(С16:0, С18:0, С16:1, С18:1), то ФК направляется на синтез ТАГ;
если для синтеза используются ПНЖК (ω6 С18:2, С20:4; ω3 С18:3, С20:5),
то ФК становится предшественником синтеза ФЛ.
12. Биосинтез фосфолипидов (ФЛ).
Процесс наиболееинтенсивно протекает
в печени, а также
в других тканях
(исключая эритроциты).
Синтез ФЛ происходит
в ЭПР клетки.
ФЛ - производные
фосфатидной кислоты и
одного из аминоспиртов
(этаноламин, холин),
аминокислоты серина,
циклического спирта
инозитола.
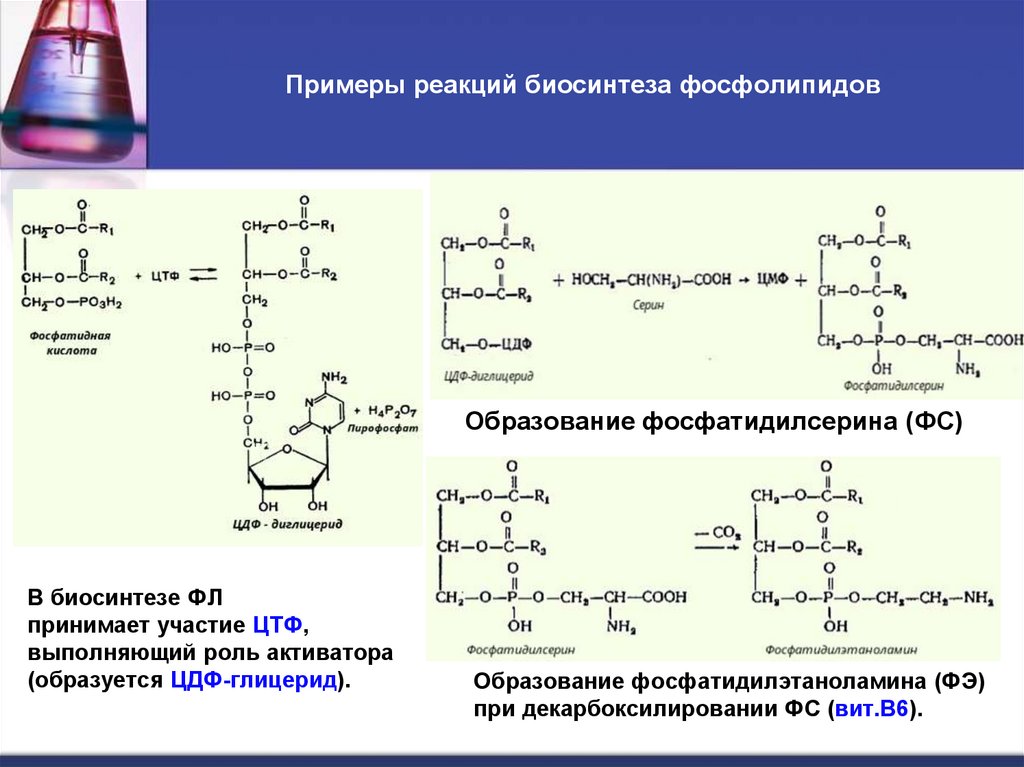
13. Примеры реакций биосинтеза фосфолипидов
Образование фосфатидилсерина (ФС)В биосинтезе ФЛ
принимает участие ЦТФ,
выполняющий роль активатора
(образуется ЦДФ-глицерид).
Образование фосфатидилэтаноламина (ФЭ)
при декарбоксилировании ФС (вит.В6).
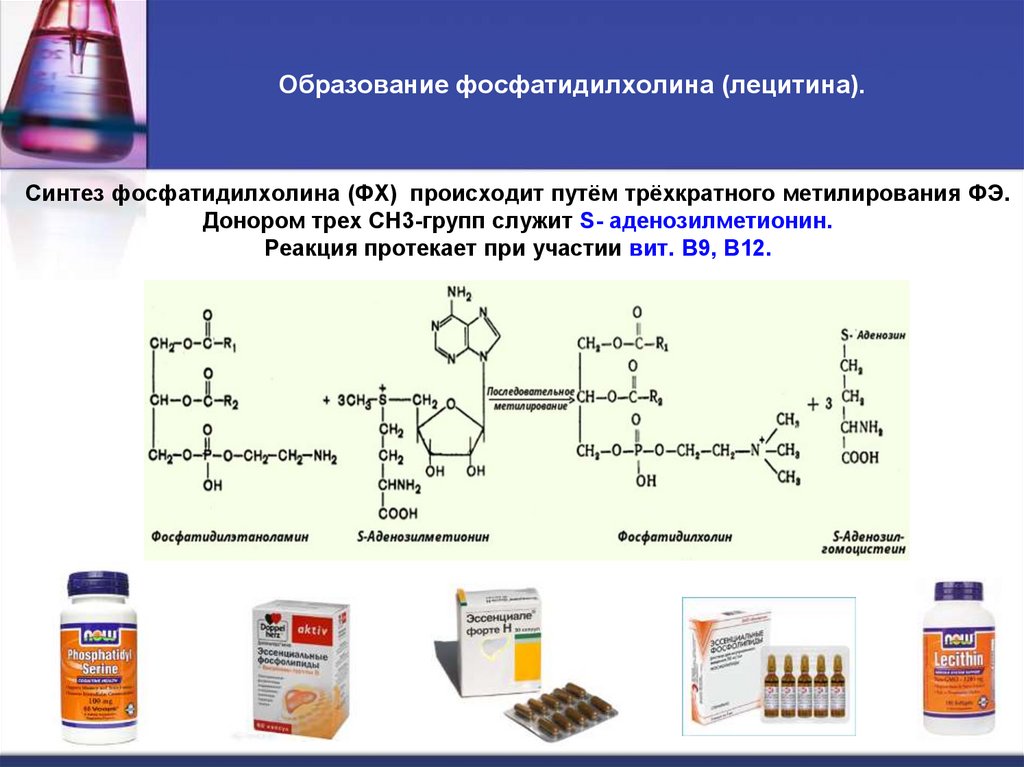
14. Образование фосфатидилхолина (лецитина).
Синтез фосфатидилхолина (ФХ) происходит путём трёхкратного метилирования ФЭ.Донором трех СН3-групп служит S- аденозилметионин.
Реакция протекает при участии вит. В9, В12.
15. Липотропные факторы – вещества, способствующие синтезу ФЛ и препятствующие отложению ТАГ в печени.
Липотропные факторы –вещества, способствующие синтезу ФЛ
и препятствующие отложению ТАГ в печени.
Липотропный эффект этих соединений обусловлен тем, что общим
предшественником ТАГ и ФЛ является фосфатидная кислота.
При недостатке липотропных факторов фосфатидная кислота используется
преимущественно для синтеза ТАГ (нерастворимы в воде и накапливаются в
гепатоцитах, способствуя их жировому перерождению).
Липотропные факторы - соединения, необходимые для синтеза ФЛ:
Метионин
Холин
ПНЖК
С18:2
С18:3
С20:4
С20:5
Витамины
В6
В9
В12
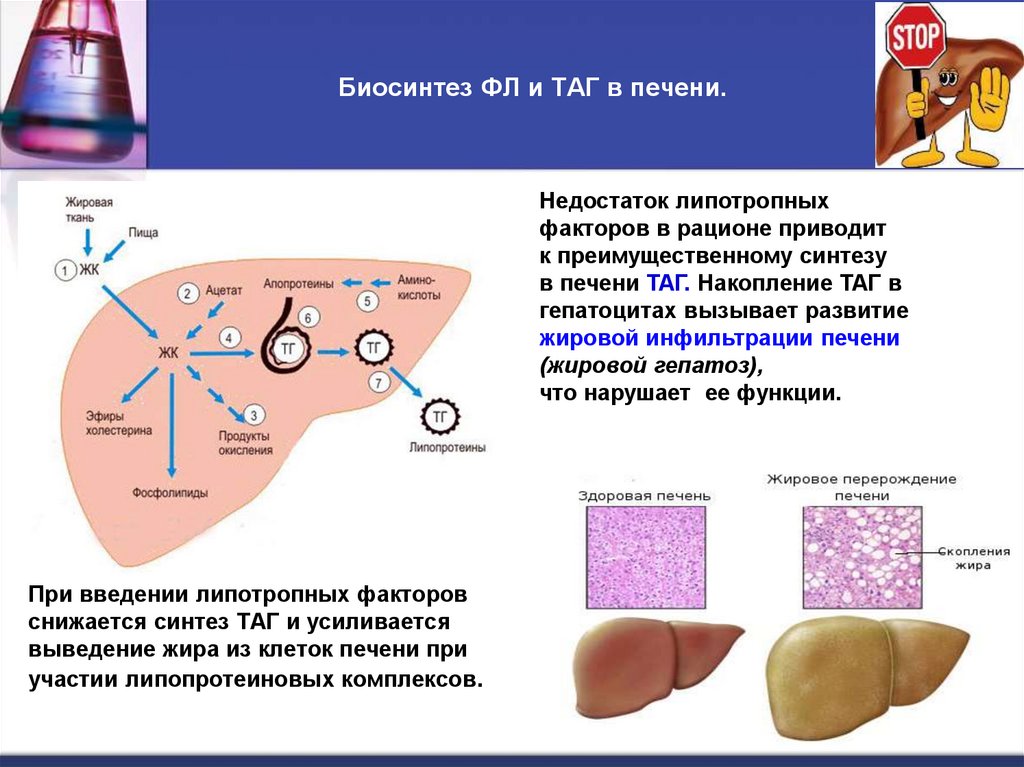
16. Биосинтез ФЛ и ТАГ в печени.
Фосфатиднаякислота
Липотропные
факторы
ТАГ
Депонирование
(резерв)
ФЛ
Построение
мембран клеток
При введении липотропных факторов
снижается синтез ТАГ и усиливается
выведение жира из клеток печени при
участии липопротеиновых комплексов.
Недостаток липотропных
факторов в рационе приводит
к преимущественному синтезу
в печени ТАГ. Накопление ТАГ в
гепатоцитах вызывает развитие
жировой инфильтрации печени
(жировой гепатоз),
что нарушает ее функции.
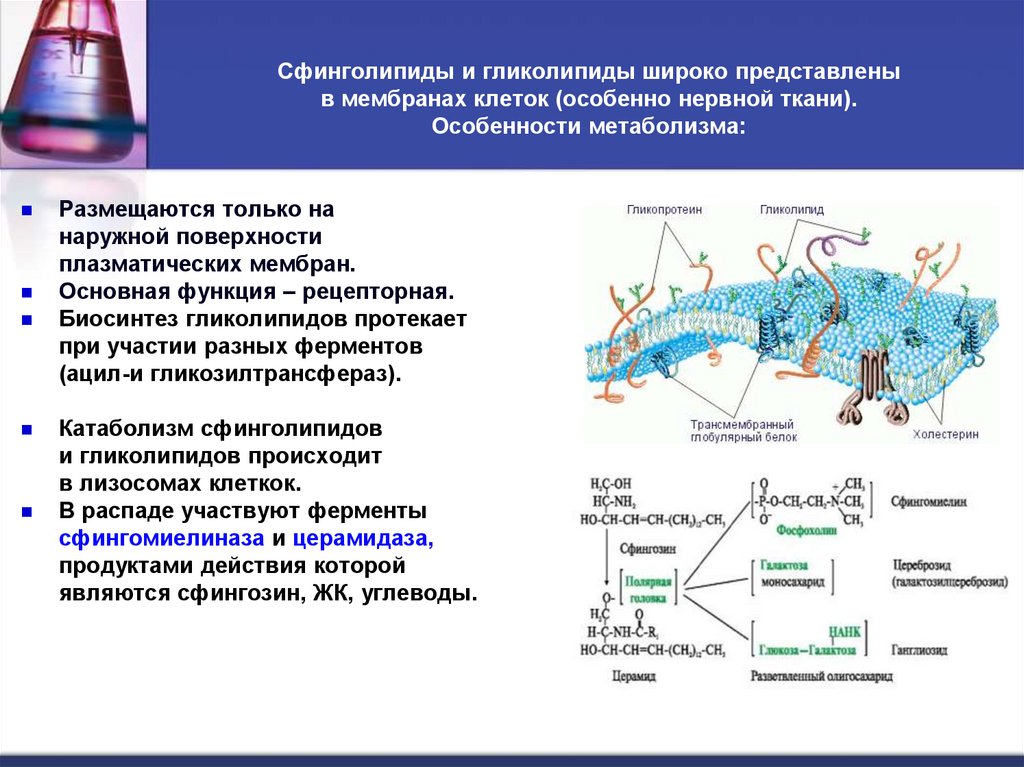
17. Сфинголипиды и гликолипиды широко представлены в мембранах клеток (особенно нервной ткани). Особенности метаболизма:
Размещаются только нанаружной поверхности
плазматических мембран.
Основная функция – рецепторная.
Биосинтез гликолипидов протекает
при участии разных ферментов
(ацил-и гликозилтрансфераз).
Катаболизм сфинголипидов
и гликолипидов происходит
в лизосомах клеткок.
В распаде участвуют ферменты
сфингомиелиназа и церамидаза,
продуктами действия которой
являются сфингозин, ЖК, углеводы.
18.
Болезни накопления сложных липидов –липидозы.
Нарушение катаболизма
сфинголипидов и гликолипидов причина наследственных
заболеваний, связанных с их
накоплением в лизосомах клеток
(снижается активность гидролаз,
локализованных в лизосомах и
участвующих в расщеплении).
Сфинголипидозы приводят
к смерти в раннем возрасте,
т. к. происходит поражение
клеток нервной ткани,
где сконцентрированы
гликосфинголипиды.
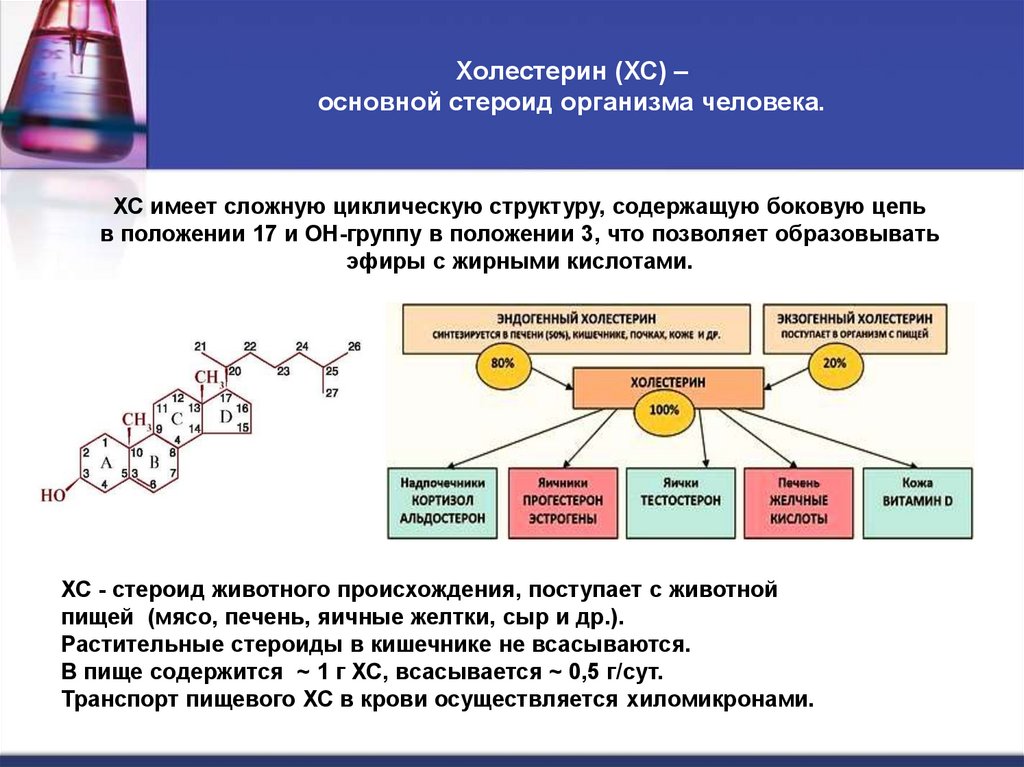
19. Холестерин (ХС) – основной стероид организма человека.
ХС имеет сложную циклическую структуру, содержащую боковую цепьв положении 17 и ОН-группу в положении 3, что позволяет образовывать
эфиры с жирными кислотами.
ХС - стероид животного происхождения, поступает с животной
пищей (мясо, печень, яичные желтки, сыр и др.).
Растительные стероиды в кишечнике не всасываются.
В пище содержится ~ 1 г ХС, всасывается ~ 0,5 г/сут.
Транспорт пищевого ХС в крови осуществляется хиломикронами.
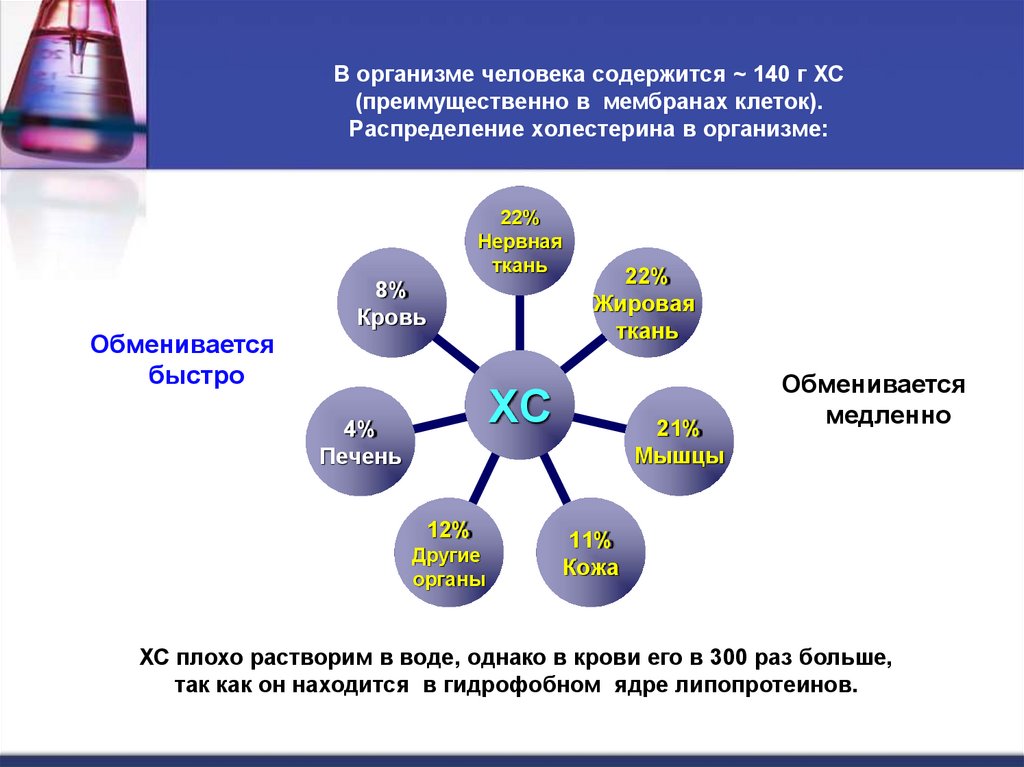
20. В организме человека содержится ~ 140 г ХС (преимущественно в мембранах клеток). Распределение холестерина в организме:
22%Нервная
ткань
Обменивается
быстро
8%
Кровь
22%
Жировая
ткань
ХС
4%
Печень
12%
Другие
органы
21%
Мышцы
Обменивается
медленно
11%
Кожа
ХС плохо растворим в воде, однако в крови его в 300 раз больше,
так как он находится в гидрофобном ядре липопротеинов.
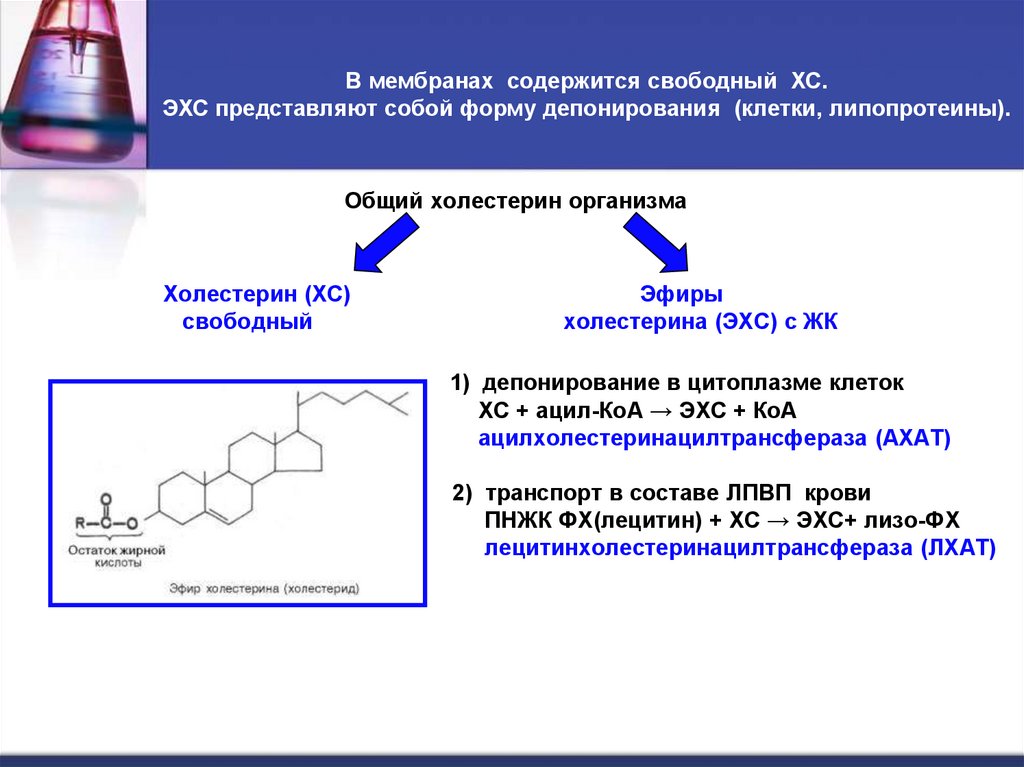
21. В мембранах содержится свободный ХС. ЭХС представляют собой форму депонирования (клетки, липопротеины).
Общий холестерин организмаХолестерин (ХС)
свободный
Эфиры
холестерина (ЭХС) с ЖК
1) депонирование в цитоплазме клеток
ХС + ацил-КоА → ЭХС + КоА
ацилхолестеринацилтрансфераза (АХАТ)
2) транспорт в составе ЛПВП крови
ПНЖК ФХ(лецитин) + ХС → ЭХС+ лизо-ФХ
лецитинхолестеринацилтрансфераза (ЛХАТ)
22. Биосинтез холестерина включает 35 реакций.
Биосинтез ХС наиболее интенсивно протекаетв печени (80%), стенке кишечника (10%),
коже (5%), коре надпочечников (5 %).
Синтез ХС происходит в цитозоле и ЭПР.
Исходным субстратом для синтеза
является ацетил-КоА.
В процессе синтеза выделяется 4 стадии:
синтез мевалоновой кислоты,
синтез изопентилдифосфата,
образование сквалена,
циклизация ХС.
Суммарная реакция синтеза холестерина:
18 ацетил-КоА + 18 НАДФН2 + 18 АТФ + О2
↓
ХС + 9 СО2 + 18 HS-КоА
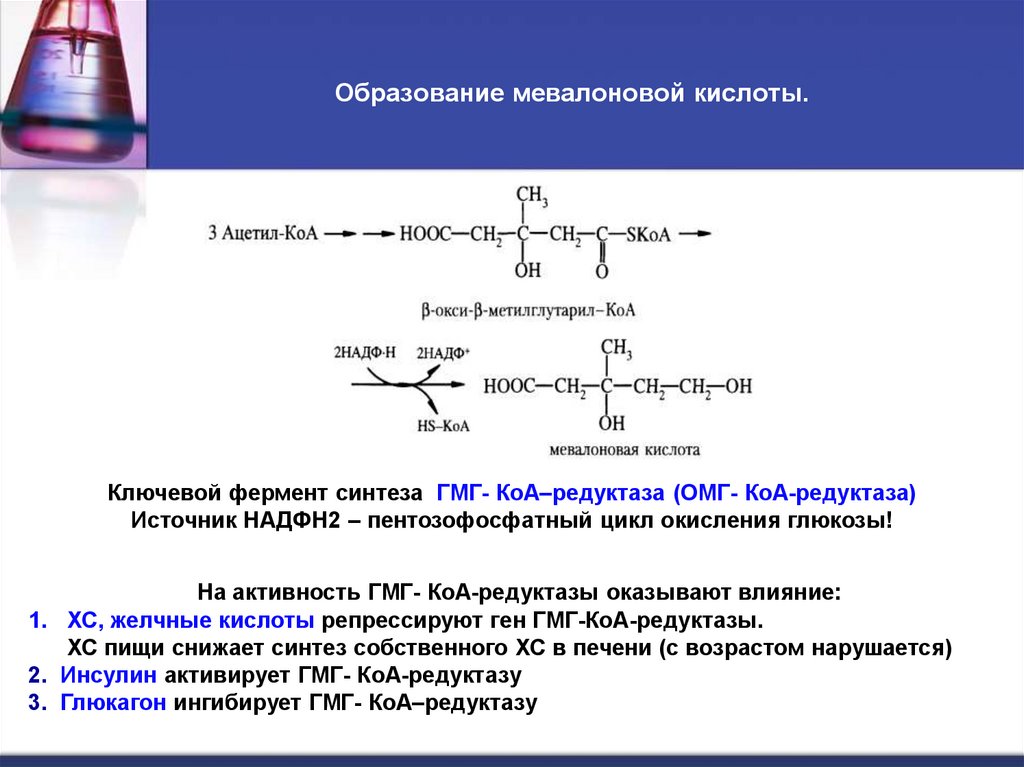
23. Образование мевалоновой кислоты.
Ключевой фермент синтеза ГМГ- КоА–редуктаза (ОМГ- КоА-редуктаза)Источник НАДФН2 – пентозофосфатный цикл окисления глюкозы!
На активность ГМГ- КоА-редуктазы оказывают влияние:
1. ХС, желчные кислоты репрессируют ген ГМГ-КоА-редуктазы.
ХС пищи снижает синтез собственного ХС в печени (с возрастом нарушается)
2. Инсулин активирует ГМГ- КоА-редуктазу
3. Глюкагон ингибирует ГМГ- КоА–редуктазу
24. Количество синтезированного в организме ХС составляет 0,5 - 1,0 г/сут и зависит от его содержания в пище.
Синтез ХС происходит в абсорбтивный период, когда в клетках печениактивируется гликолиз – источник 18 ацетил-КоА
и пентозофосфатный шунт – источник 18 НАДФН2.
В синтезе участвует ~ 35 ферментов (35 реакций),
этот метаболический путь - один из самых длинных в организме.
Большая часть синтезированного в печени ХС, превращается в ЭХС,
которые упаковываются в ЛПОНП и ЛПНП и секретируются в кровь.
Синтез ХС активируется при питании углеводами
и ингибируется при голодании.
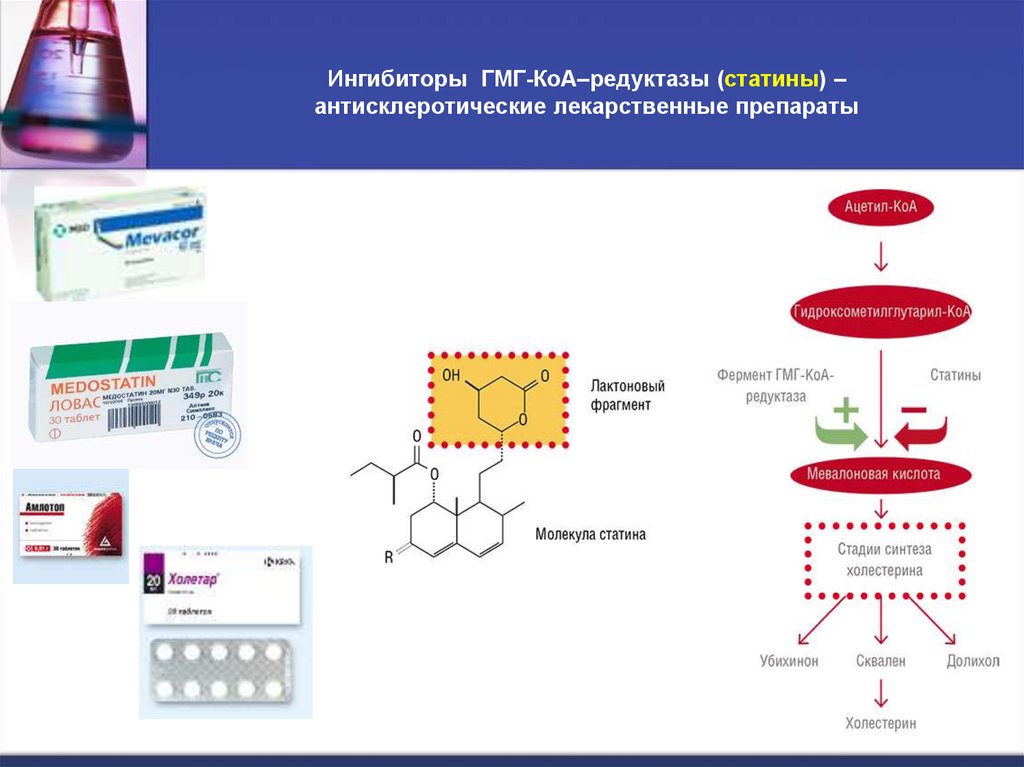
25. Ингибиторы ГМГ-КоА–редуктазы (статины) – антисклеротические лекарственные препараты
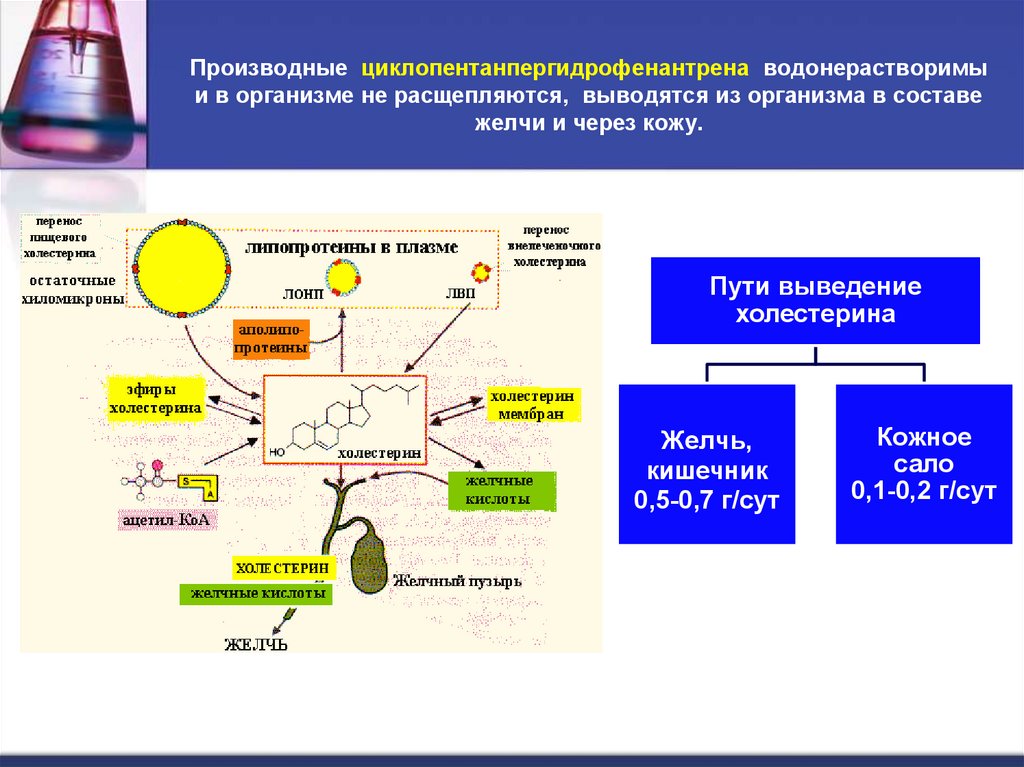
26. Производные циклопентанпергидрофенантрена водонерастворимы и в организме не расщепляются, выводятся из организма в составе
желчи и через кожу.Пути выведение
холестерина
Желчь,
кишечник
0,5-0,7 г/сут
Кожное
сало
0,1-0,2 г/сут
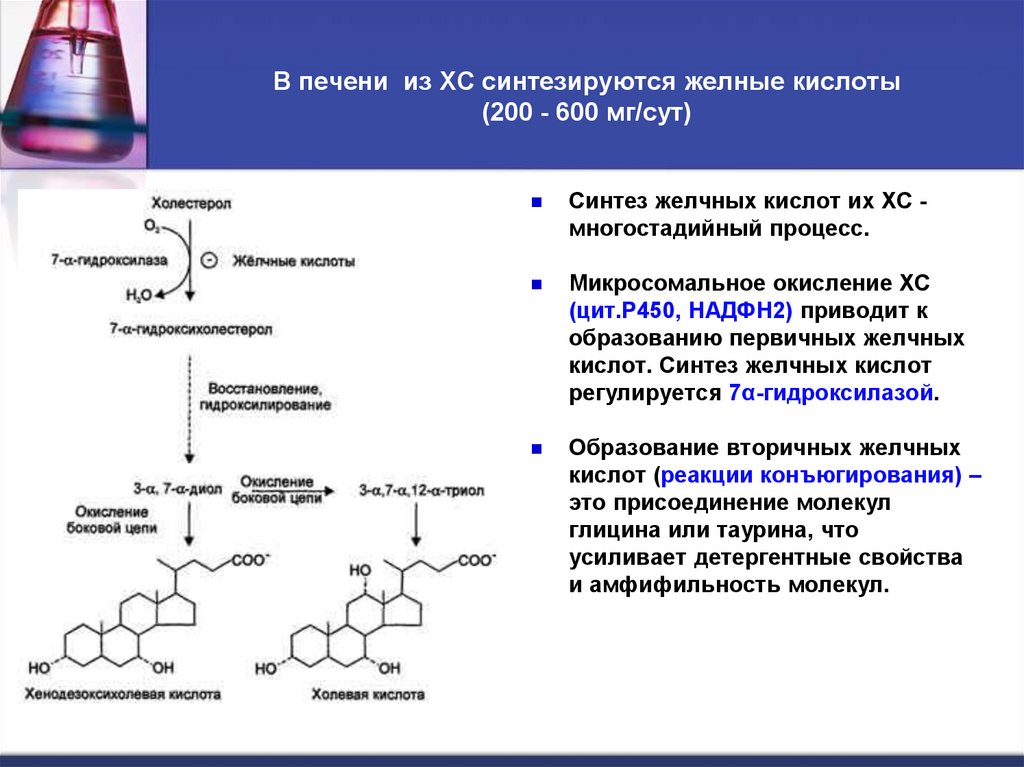
27. В печени из ХС синтезируются желные кислоты (200 - 600 мг/сут)
Синтез желчных кислот их ХС многостадийный процесс.Микросомальное окисление ХС
(цит.Р450, НАДФН2) приводит к
образованию первичных желчных
кислот. Синтез желчных кислот
регулируется 7α-гидроксилазой.
Образование вторичных желчных
кислот (реакции конъюгирования) –
это присоединение молекул
глицина или таурина, что
усиливает детергентные свойства
и амфифильность молекул.
28.
Состав желчи.Компоненты
Концентрация
(ммоль/л)
Желчные кислоты
310
Фосфатидилхолин
8
Холестерол
25
Билирубин
3,2
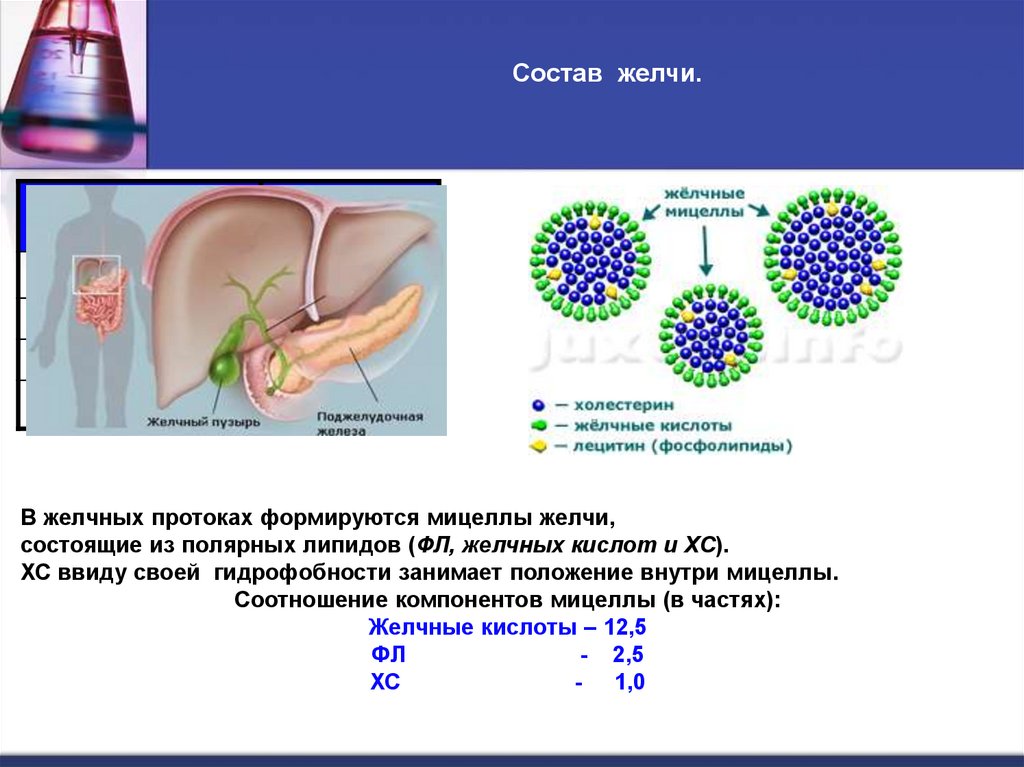
В желчных протоках формируются мицеллы желчи,
состоящие из полярных липидов (ФЛ, желчных кислот и ХС).
ХС ввиду своей гидрофобности занимает положение внутри мицеллы.
Соотношение компонентов мицеллы (в частях):
Желчные кислоты – 12,5
ФЛ
- 2,5
ХС
- 1,0
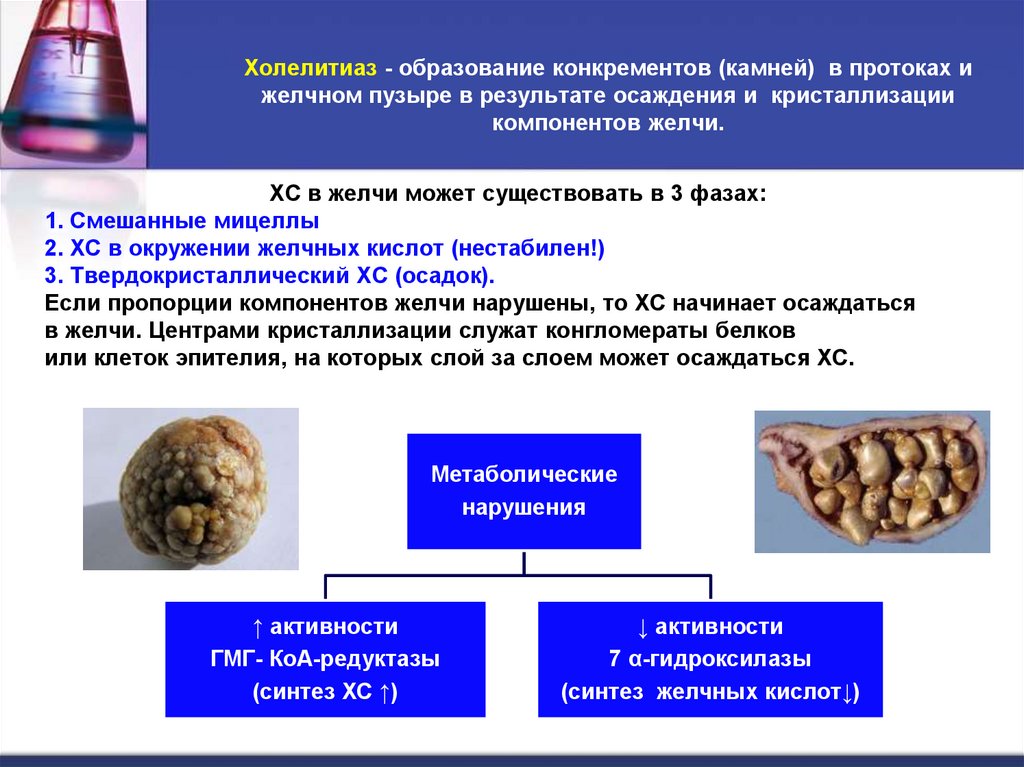
29. Холелитиаз - образование конкрементов (камней) в протоках и желчном пузыре в результате осаждения и кристаллизации компонентов
желчи.ХС в желчи может существовать в 3 фазах:
1. Смешанные мицеллы
2. ХС в окружении желчных кислот (нестабилен!)
3. Твердокристаллический ХС (осадок).
Если пропорции компонентов желчи нарушены, то ХС начинает осаждаться
в желчи. Центрами кристаллизации служат конгломераты белков
или клеток эпителия, на которых слой за слоем может осаждаться ХС.
Метаболические
нарушения
↑ активности
ГМГ- КоА-редуктазы
(синтез ХС ↑)
↓ активности
7 α-гидроксилазы
(синтез желчных кислот↓)
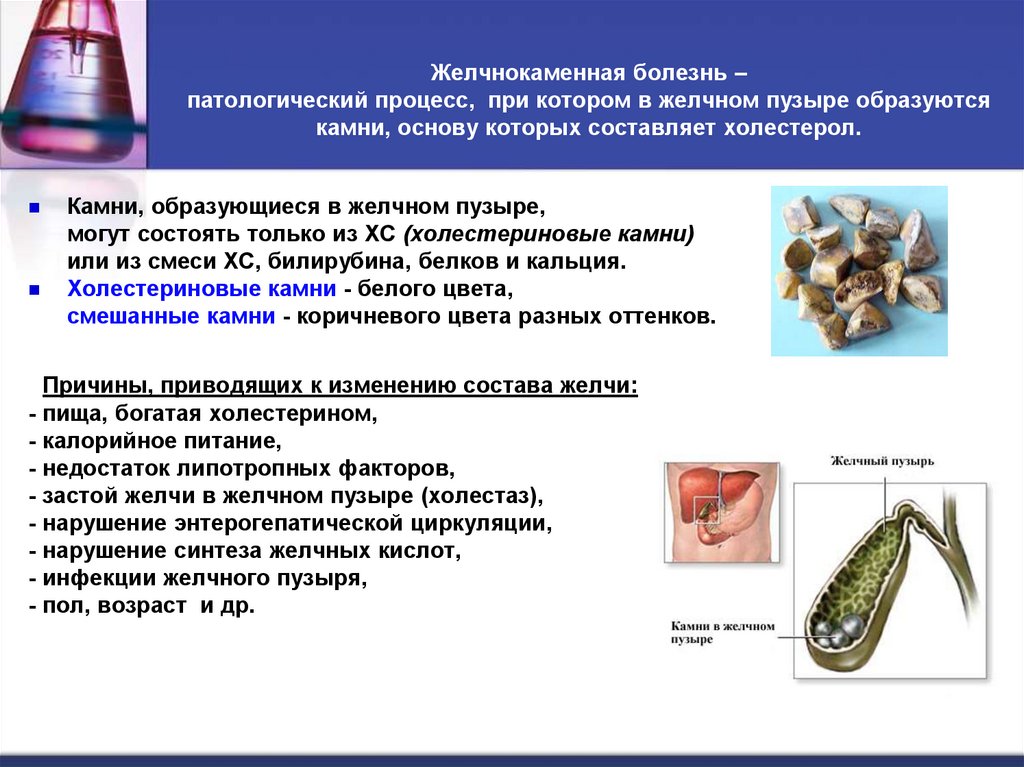
30. Желчнокаменная болезнь – патологический процесс, при котором в желчном пузыре образуются камни, основу которых составляет
холестерол.Камни, образующиеся в желчном пузыре,
могут состоять только из ХС (холестериновые камни)
или из смеси ХС, билирубина, белков и кальция.
Холестериновые камни - белого цвета,
смешанные камни - коричневого цвета разных оттенков.
Причины, приводящих к изменению состава желчи:
- пища, богатая холестерином,
- калорийное питание,
- недостаток липотропных факторов,
- застой желчи в желчном пузыре (холестаз),
- нарушение энтерогепатической циркуляции,
- нарушение синтеза желчных кислот,
- инфекции желчного пузыря,
- пол, возраст и др.
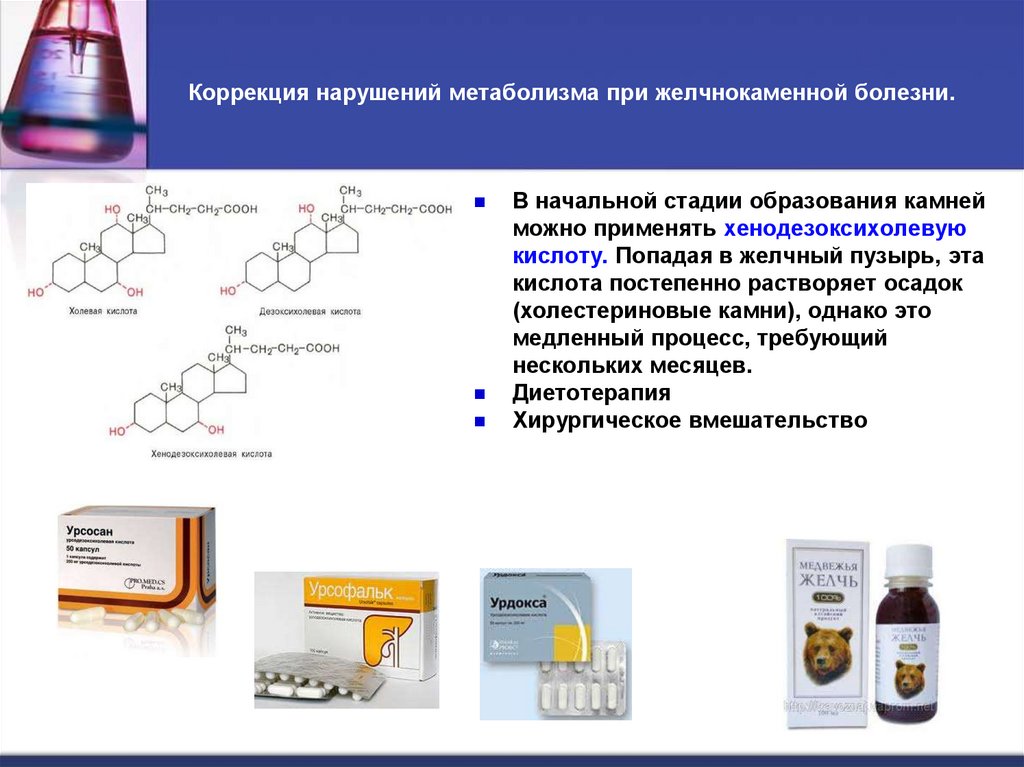
31. Коррекция нарушений метаболизма при желчнокаменной болезни.
В начальной стадии образования камнейможно применять хенодезоксихолевую
кислоту. Попадая в желчный пузырь, эта
кислота постепенно растворяет осадок
(холестериновые камни), однако это
медленный процесс, требующий
нескольких месяцев.
Диетотерапия
Хирургическое вмешательство
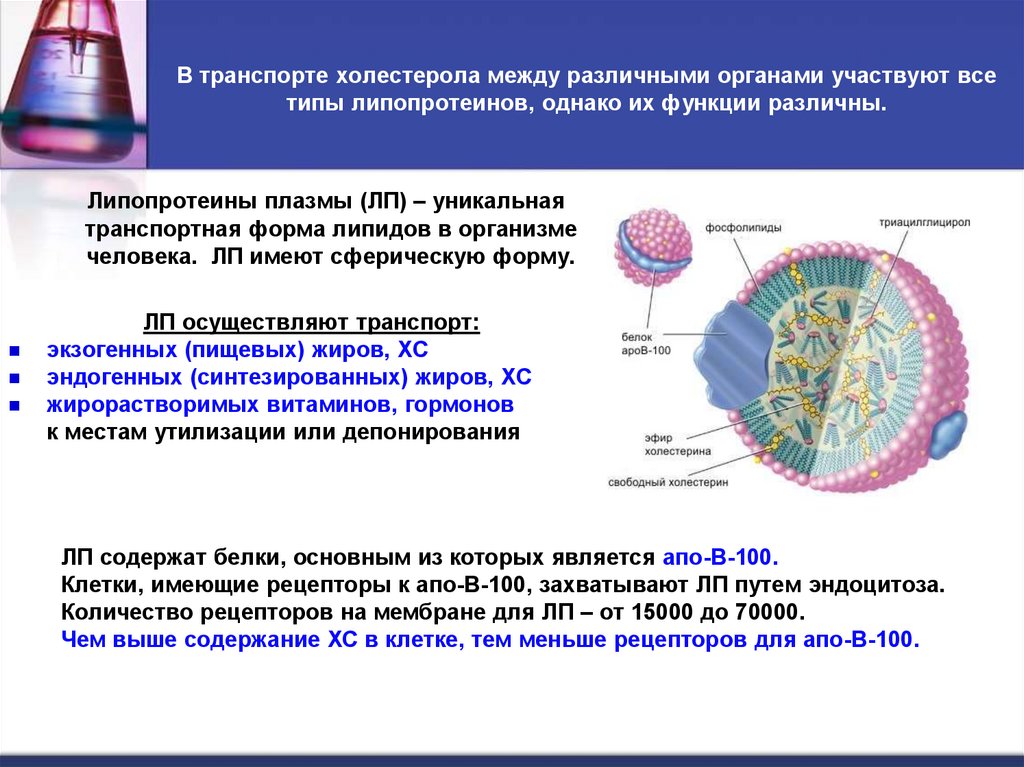
32. В транспорте холестерола между различными органами участвуют все типы липопротеинов, однако их функции различны.
Липопротеины плазмы (ЛП) – уникальнаятранспортная форма липидов в организме
человека. ЛП имеют сферическую форму.
ЛП осуществляют транспорт:
экзогенных (пищевых) жиров, ХС
эндогенных (синтезированных) жиров, ХС
жирорастворимых витаминов, гормонов
к местам утилизации или депонирования
ЛП содержат белки, основным из которых является апо-В-100.
Клетки, имеющие рецепторы к апо-В-100, захватывают ЛП путем эндоцитоза.
Количество рецепторов на мембране для ЛП – от 15000 до 70000.
Чем выше содержание ХС в клетке, тем меньше рецепторов для апо-В-100.
33. Классификация липопротеинов крови. Состав липопротеинов.
Хиломикроны (натощак нет!) ХМЛП очень низкой плотности ЛОНП
ЛП низкой плотности
ЛНП
ЛП высокой плотности
ЛВП
Классификация ЛП обусловлена методами исследования:
1. Ультрацентрифугирование (плотность, плавучесть)
2. Электрофорез (подвижность в электрическом поле)
34. Липопротеины очень низкой плотности (ЛОНП)
ОбразованиеФункции
Катаболизм
клетки стенки кишечника, печень.
транспорт эндогенных (синтезированных) ТАГ, ХС
к местам утилизации (депонирования).
Содержание ТАГ снижается с 55% до 7%,
что приводит к увеличению доли ХС и его эфиров
до 50%. Теряя ТАГ, ЛОНП трансформируются
в ЛППП и ЛПНП.
35. Липопротеины низкой плотности (ЛПНП) – атерогенный класс липопротеинов.
ОбразованиеФункции
Катаболизм
синтез в печени, трансформация ЛОНП
транспорт ХС (60-70%) из печени к тем тканям,
которые имеют на мембране клеток белки-рецепторы
к ЛПНП (апо-В100): надпочечники, кожа, селезенка и др.
проникают целиком в клетку путем эндоцитоза.
Ферменты лизосом гидролизуют содержимое ЛПНП.
ХС метаболизирует в клетке или депонируется.
У здоровых людей период
полураспада ЛПНП составляет 2-5 сут.
При избытке ХС в организме/клетке
метаболизма ЛПНП не происходит и
их уровень в крови резко возрастает.
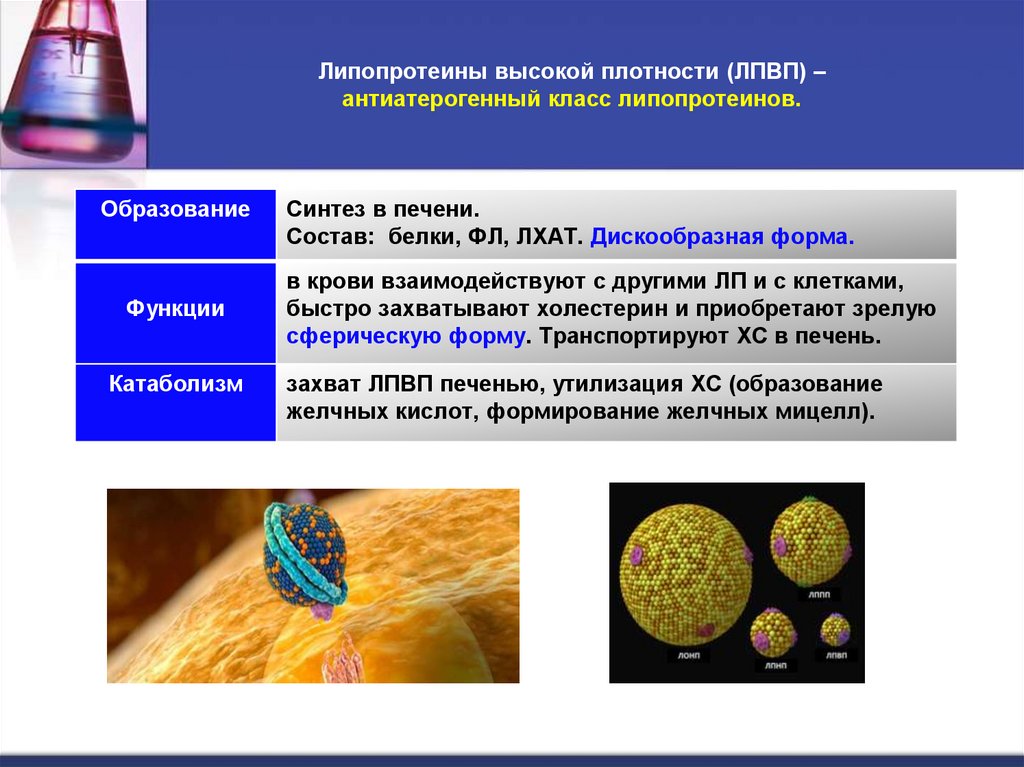
36. Липопротеины высокой плотности (ЛПВП) – антиатерогенный класс липопротеинов.
ОбразованиеФункции
Катаболизм
Синтез в печени.
Состав: белки, ФЛ, ЛХАТ. Дискообразная форма.
в крови взаимодействуют с другими ЛП и с клетками,
быстро захватывают холестерин и приобретают зрелую
сферическую форму. Транспортируют ХС в печень.
захват ЛПВП печенью, утилизация ХС (образование
желчных кислот, формирование желчных мицелл).
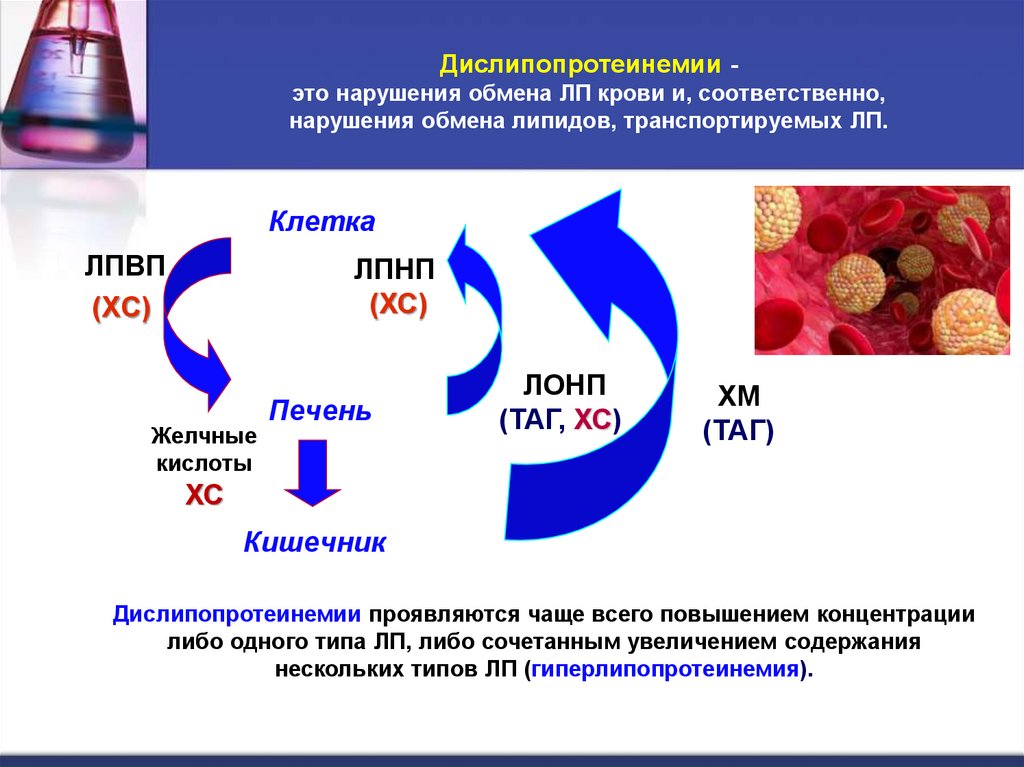
37. Дислипопротеинемии - это нарушения обмена ЛП крови и, соответственно, нарушения обмена липидов, транспортируемых ЛП.
Дислипопротеинемии это нарушения обмена ЛП крови и, соответственно,нарушения обмена липидов, транспортируемых ЛП.
Клетка
ЛПВП
(ХС)
ЛПНП
(ХС)
Желчные
кислоты
Печень
ЛОНП
(ТАГ, ХС)
ХМ
(ТАГ)
ХС
Кишечник
Дислипопротеинемии проявляются чаще всего повышением концентрации
либо одного типа ЛП, либо сочетанным увеличением содержания
нескольких типов ЛП (гиперлипопротеинемия).
38. Исследование фракций ЛП в клинической практике используют для типирования дислипопротеинемий..
Классификация дислипопротеинемий (Д.С. Фредериксон и соавт., 1967),одобрена экспертами ВОЗ и получила широкое распространение.
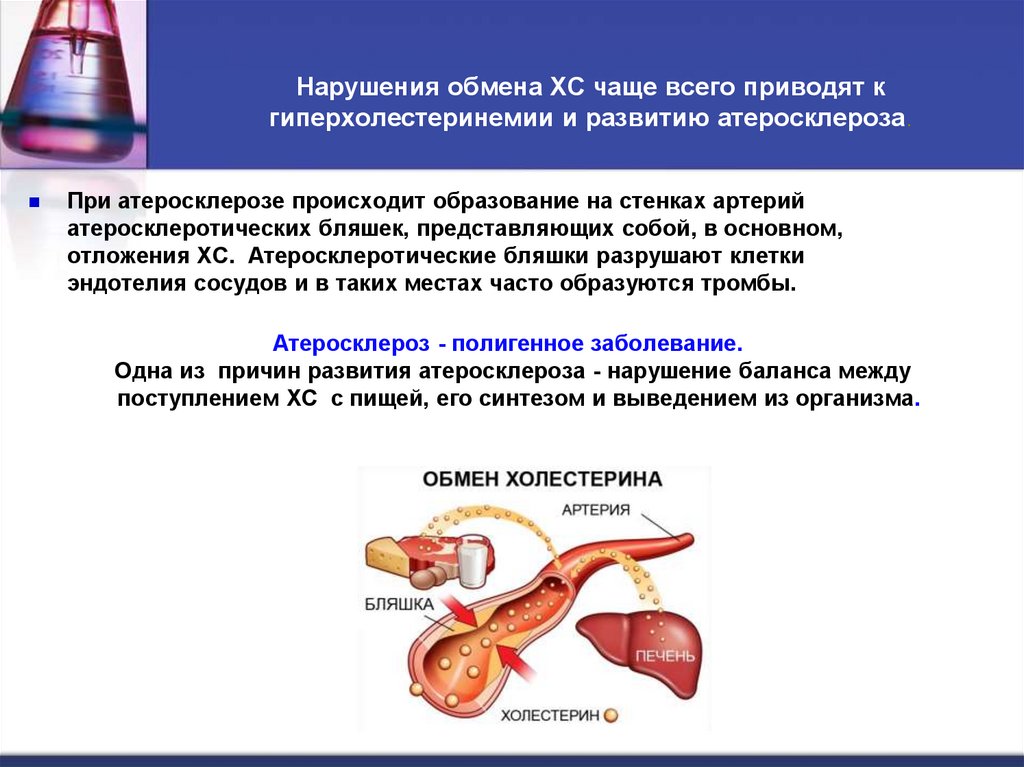
39. Нарушения обмена ХС чаще всего приводят к гиперхолестеринемии и развитию атеросклероза.
При атеросклерозе происходит образование на стенках артерийатеросклеротических бляшек, представляющих собой, в основном,
отложения ХС. Атеросклеротические бляшки разрушают клетки
эндотелия сосудов и в таких местах часто образуются тромбы.
Атеросклероз - полигенное заболевание.
Одна из причин развития атеросклероза - нарушение баланса между
поступлением ХС с пищей, его синтезом и выведением из организма.
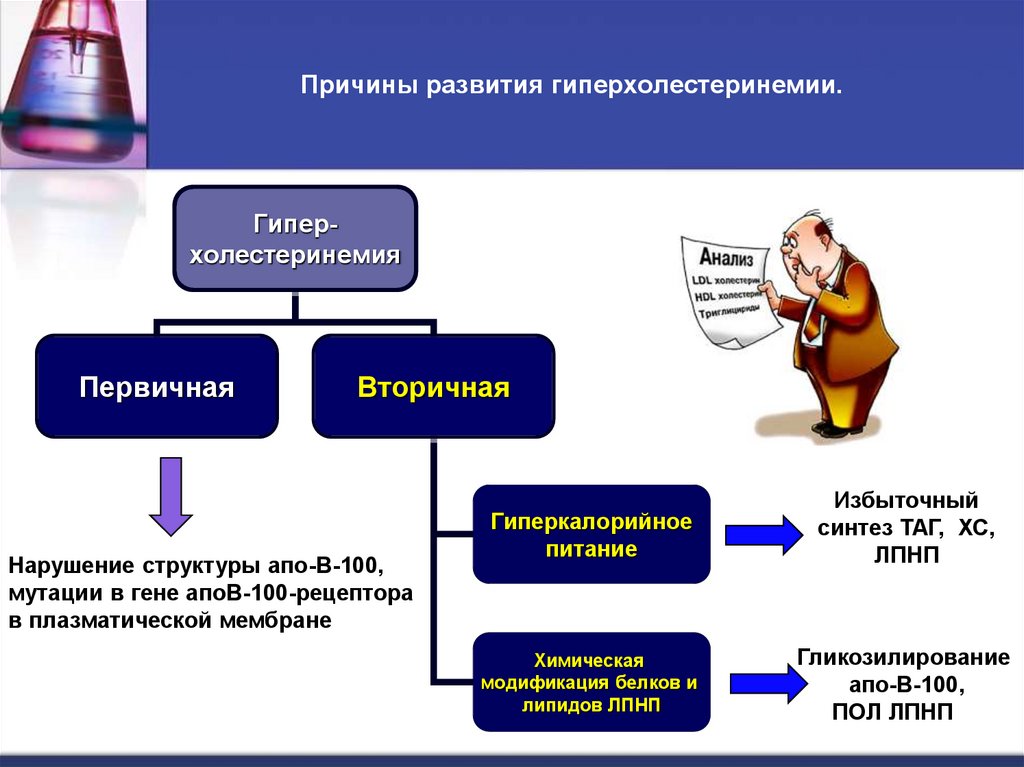
40. Причины развития гиперхолестеринемии.
ГиперхолестеринемияПервичная
Вторичная
Нарушение структуры апо-В-100,
мутации в гене апоВ-100-рецептора
в плазматической мембране
Гиперкалорийное
питание
Избыточный
синтез ТАГ, ХС,
ЛПНП
Химическая
модификация белков и
липидов ЛПНП
Гликозилирование
апо-В-100,
ПОЛ ЛПНП
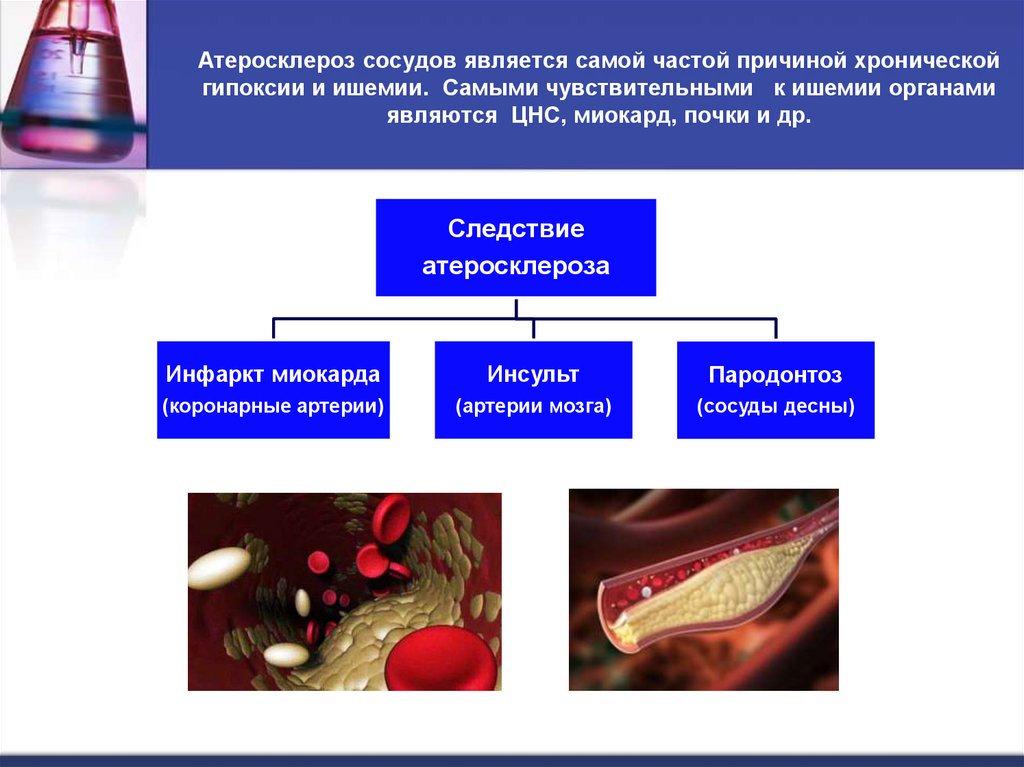
41. Атеросклероз сосудов является самой частой причиной хронической гипоксии и ишемии. Самыми чувствительными к ишемии органами
Атеросклероз сосудов является самой частой причиной хроническойгипоксии и ишемии. Самыми чувствительными к ишемии органами
являются ЦНС, миокард, почки и др.
Следствие
атеросклероза
Инфаркт миокарда
Инсульт
Пародонтоз
(коронарные артерии)
(артерии мозга)
(сосуды десны)
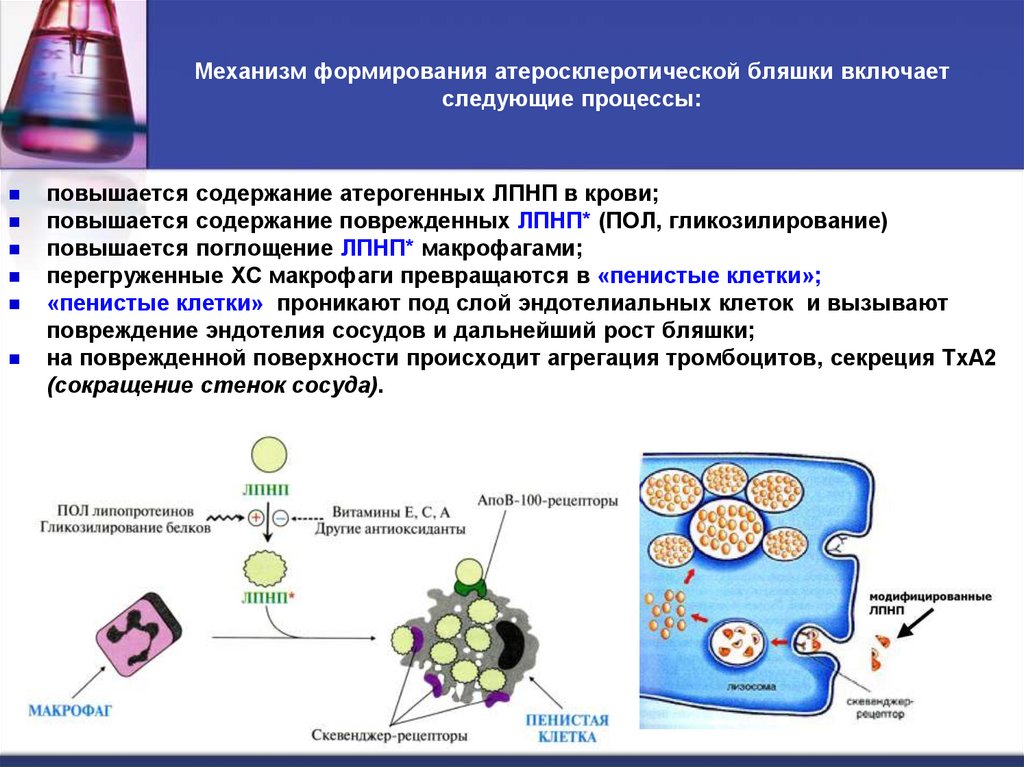
42. Механизм формирования атеросклеротической бляшки включает следующие процессы:
повышается содержание атерогенных ЛПНП в крови;повышается содержание поврежденных ЛПНП* (ПОЛ, гликозилирование)
повышается поглощение ЛПНП* макрофагами;
перегруженные ХС макрофаги превращаются в «пенистые клетки»;
«пенистые клетки» проникают под слой эндотелиальных клеток и вызывают
повреждение эндотелия сосудов и дальнейший рост бляшки;
на поврежденной поверхности происходит агрегация тромбоцитов, секреция ТхА2
(сокращение стенок сосуда).
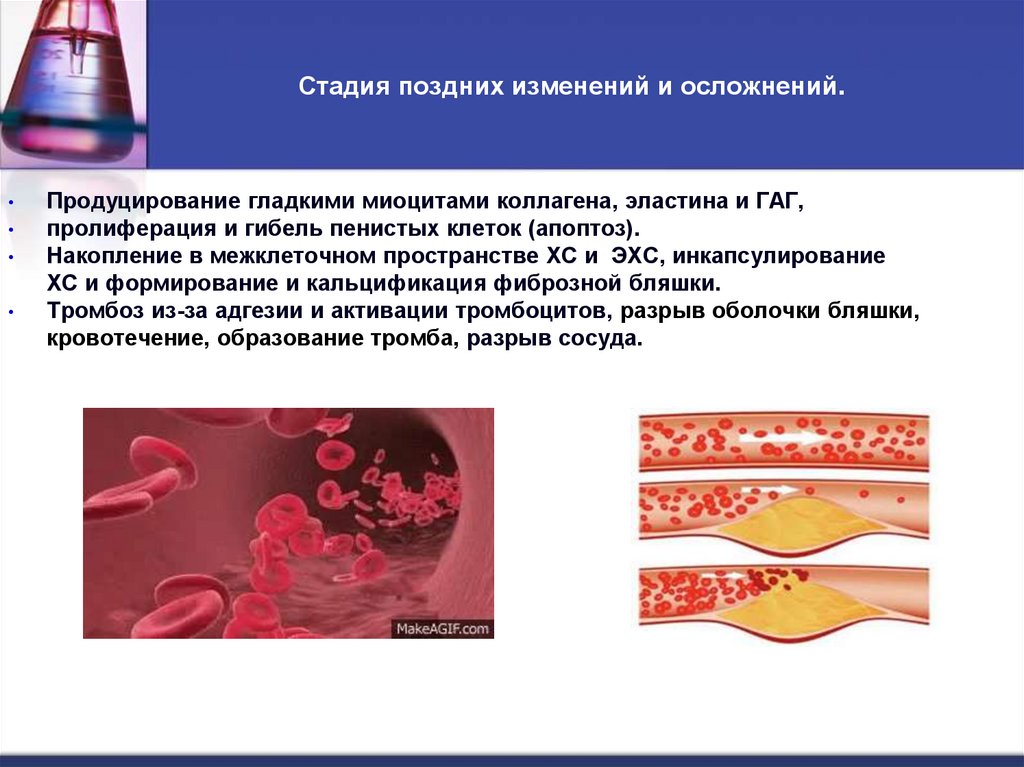
43. Стадия поздних изменений и осложнений.
Продуцирование гладкими миоцитами коллагена, эластина и ГАГ,
пролиферация и гибель пенистых клеток (апоптоз).
Накопление в межклеточном пространстве ХС и ЭХС, инкапсулирование
ХС и формирование и кальцификация фиброзной бляшки.
Тромбоз из-за адгезии и активации тромбоцитов, разрыв оболочки бляшки,
кровотечение, образование тромба, разрыв сосуда.
44.
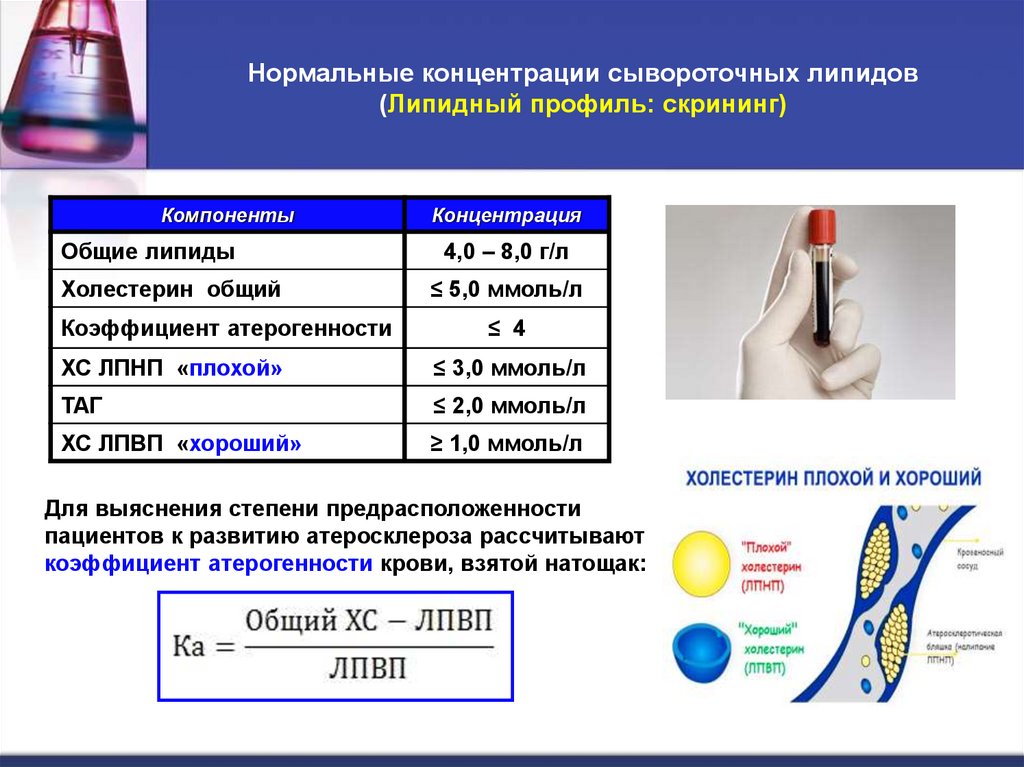
Нормальные концентрации сывороточных липидов(Липидный профиль: скрининг)
Компоненты
Концентрация
Общие липиды
4,0 – 8,0 г/л
Холестерин общий
≤ 5,0 ммоль/л
Коэффициент атерогенности
≤ 4
ХС ЛПНП «плохой»
≤ 3,0 ммоль/л
ТАГ
≤ 2,0 ммоль/л
ХС ЛПВП «хороший»
≥ 1,0 ммоль/л
Для выяснения степени предрасположенности
пациентов к развитию атеросклероза рассчитывают
коэффициент атерогенности крови, взятой натощак:
45. Биохимические основы комплексной коррекции липидного обмена при атеросклерозе.
Гипокалорийная диета (с низким содержанием ХС илегкоусвояемых углеводов - растительная пища!).
ПНЖК семейства ω-3 - из них синтезируются эйкозаноиды,
подавляющие тромбообразование и замедляющие развитие
атеросклеротической бляшки, повышают метаболизацию
холестерина.
Витамины С, Е, А и другие антиоксиданты ингибируют ПОЛ
и поддерживают структуру ЛПНП и их метаболизм.
46. Принципы лекарственной терапии нарушений липидного обмена при атеросклерозе
«Размыкание» цикла энтерогепатической циркуляции желчных кислот.- Холестирамин, холестипол (полимеры). Адсорбируют в кишечнике желчные
кислоты, выделяются с фекалиями и таким образом уменьшают их возврат в
печень и повышают скорость превращения ХС в желчные кислоты
(снижают гиперхолестеринемию).
- Энтеросорбенты (целлюлоза, пектины, хитозан и др.).
Адсорбируют в кишечнике желчные кислоты и холестерин,
уменьшают их возврат в печень и повышают скорость превращения
ХС в желчные кислоты (снижают гиперхолестеринемию).
Ингибирование синтеза ХС.
Прием ингибиторов ГМГ–КоА–редуктазы (статины)
Активация катаболизма липопротеинов.
Лекарственные препараты фибраты активируют ЛП-липазу
и ускоряют катаболизм ЛОНП, активируют окисление ЖК в печени,
уменьшают синтез ТАГ, ЭХС и секрецию ЛОНП печенью.
















 Медицина
Медицина








