Похожие презентации:
Количество вещества
1. Количество вещества
2.
Физические величины3.
Рассмотрим реакцию взаимодействияводорода и кислорода:
2Н2 + О2 = 2Н2О
Как нужно отмерить водород и кислород,
чтобы они полностью прореагировали и
образовали воду?
(Нужно взять на одну молекулу кислорода
две молекулы водорода.)
Но технически это выполнить невозможно
из-за малого размера молекул. Как быть?
4.
2Н2 + О2 = 2Н2ОА если взять столько граммов водорода, сколько
весят 2 его молекулы, т.е. массой 4 г.
Соответственно кислорода взять 32 г, т.е. какова
его молекулярная масса. Тогда поставленное
вначале условие будет соблюдено - все
молекулы водорода и все молекулы кислорода
прореагируют друг с другом и образуют воду.
5.
Потому вещество решили измеритьединицей, в которой как бы соединились
две величины - число молекул и масса
вещества.
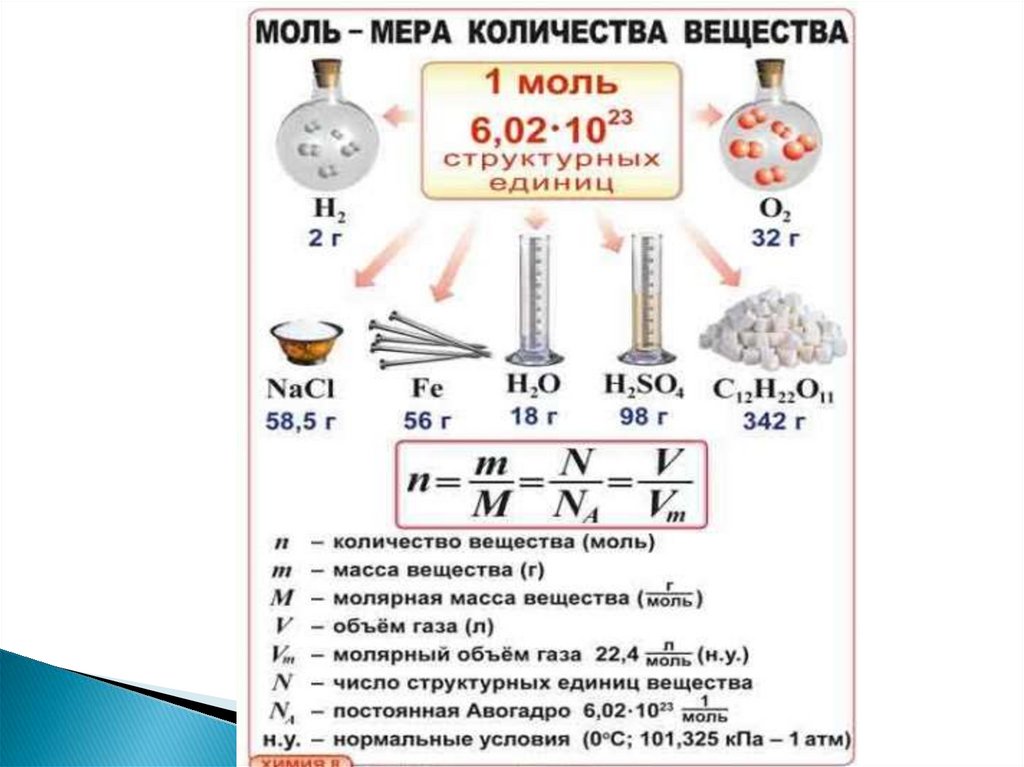
Такая единица называется моль
6.
Чтобы отмерить 1 моль вещества, нужновзять столько граммов его, какова
относительная молекулярная масса
вещества:
1 моль Н2 весит 2 г (Мr (Н2) = 2)
1 моль О2 весит 32 г (Мr (О2) = 32)
1 моль Н2О весит 18 г (Мr (Н2О) = 18)
7.
А сколько реальных частиц - молекулсодержится в 1 моле любого вещества?
1 моль Н2 весит 2 г (Мr (Н2) = 2)
1 моль О2 весит 32 г (Мr (О2) = 32)
1 моль Н2О весит 18 г (Мr (Н2О) = 18)
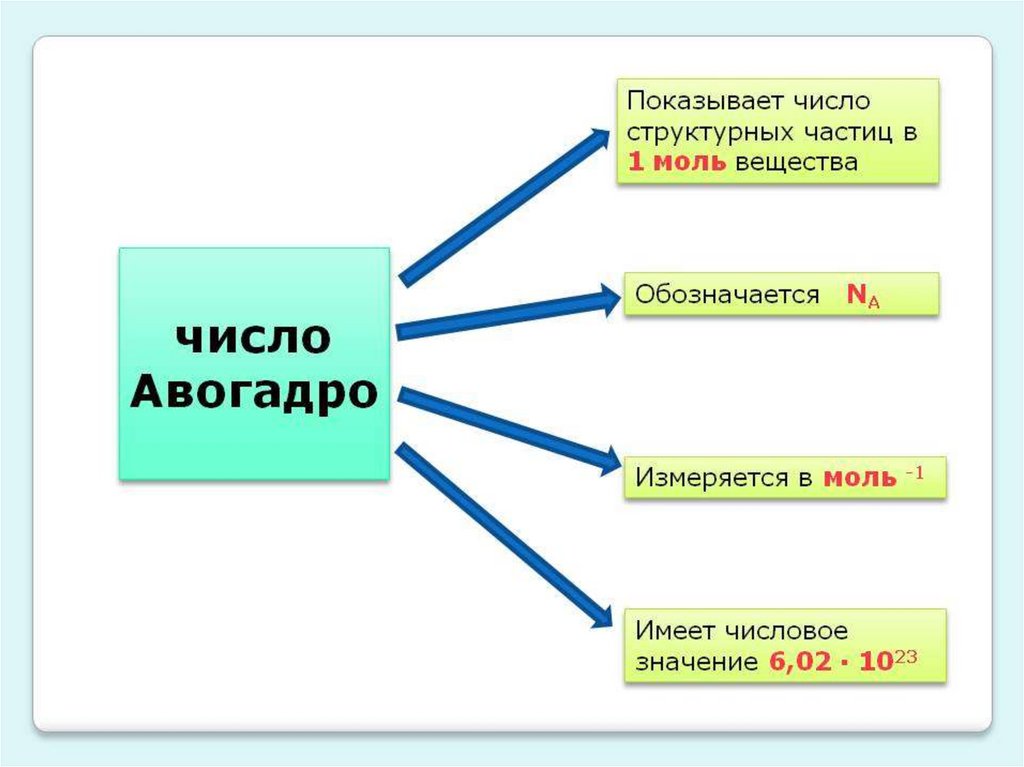
Очевидно, что одинаковое число. Оно
называется постоянной Авогадро.
Моль - количество вещества, которое
содержит число атомов или молекул,
равное числу Авогадро (NA = 6,02 · 1023).
NA = N/n, где N – число частиц, n –
количество вещества
8.
9.
Количество вещества обозначается буквойn («эн») или v («ню»)
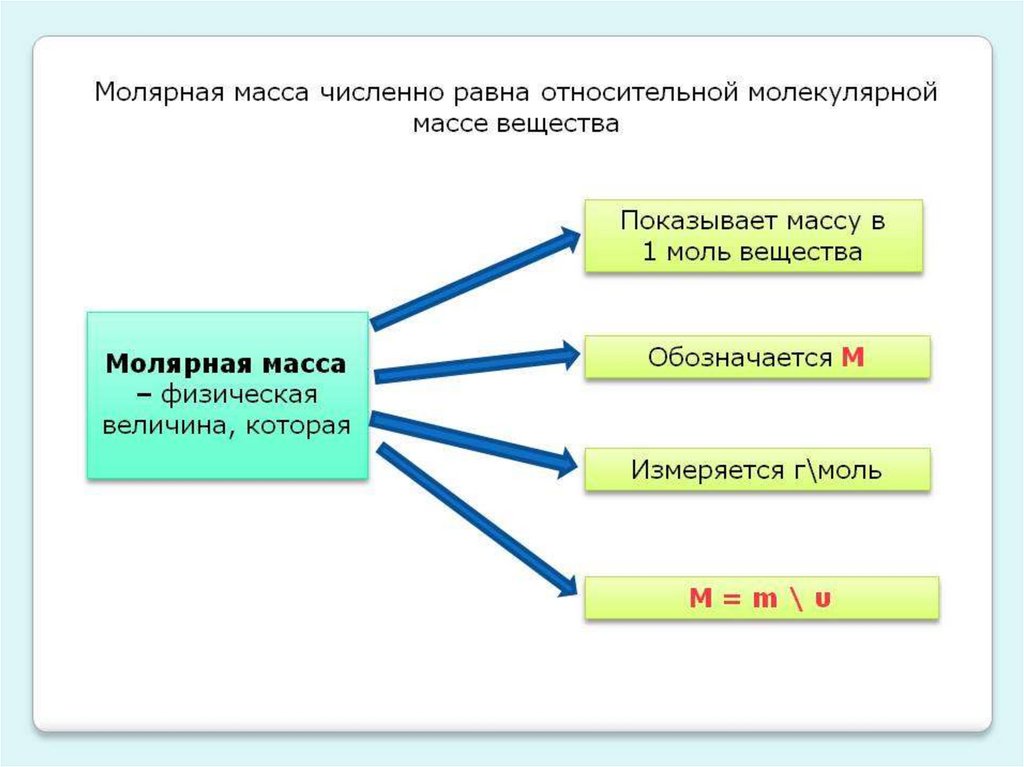
Масса 1 моль называется молярной массой,
обозначается буквой М
Молярная масса измеряется в г/моль и равна
относительной молекулярной массе
вещества, например, М (Н2О) = 18 г/моль
Если известна масса вещества (m), то,
рассчитав его молярную массу (М), можно
найти количество вещества (n):
n = m/M, следовательно, m = M · n
10.
11.
12. Закрепление
Задача 1. Какова масса 1,5 моль оксида углерода(IV) СО2?
13.
Задача 2. Какое количество серной кислоты H2SO4содержится в 294 г её?
14.
Задача.На лабораторных весах взвесили кусочек
цинка - его масса оказалась 13 г.
Вычислите:
а) количество вещества цинка в кусочке
б) число атомов цинка











 Химия
Химия








