Похожие презентации:
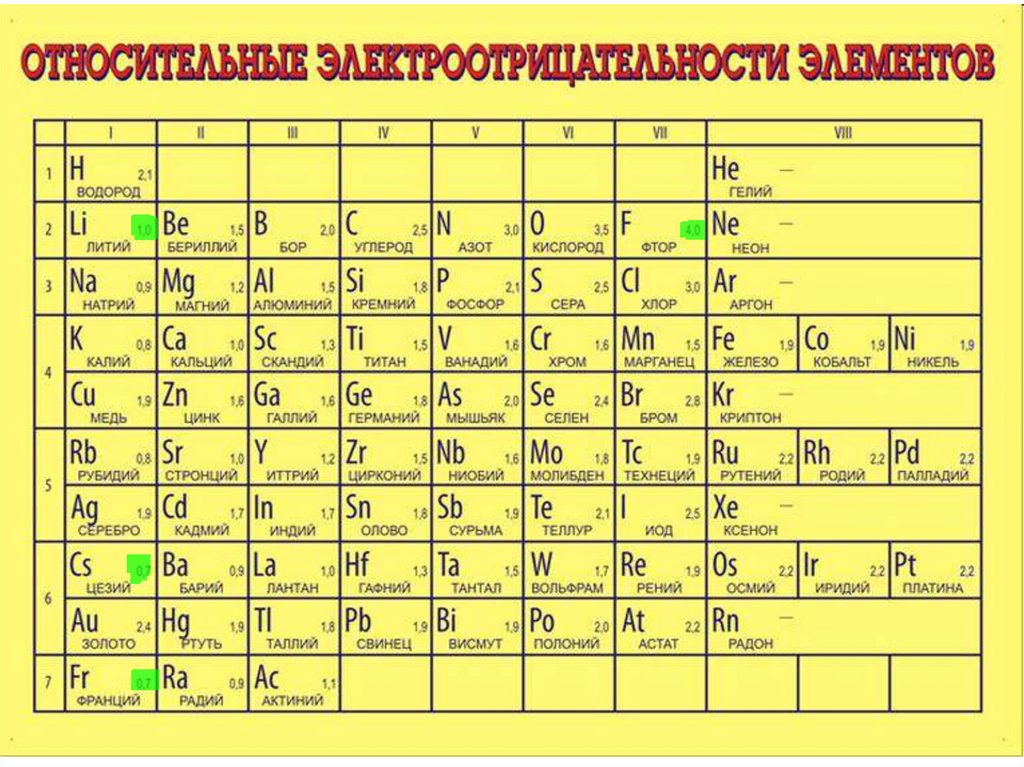
Электроотрицательность Степень окисления Валентность химических элементов
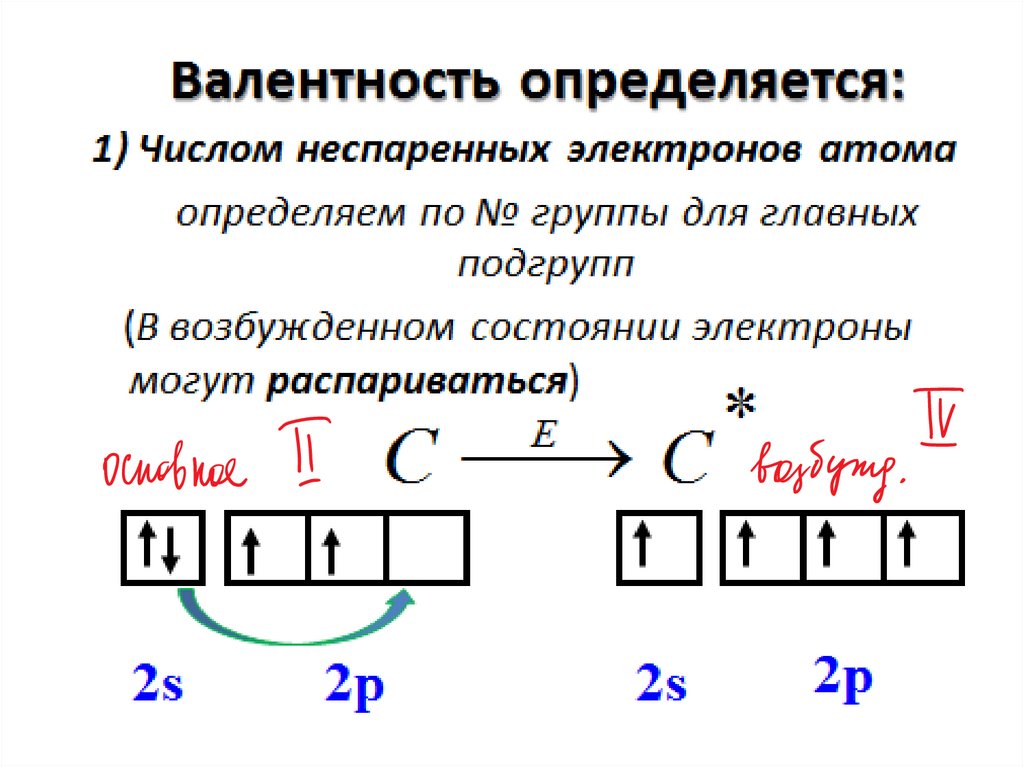
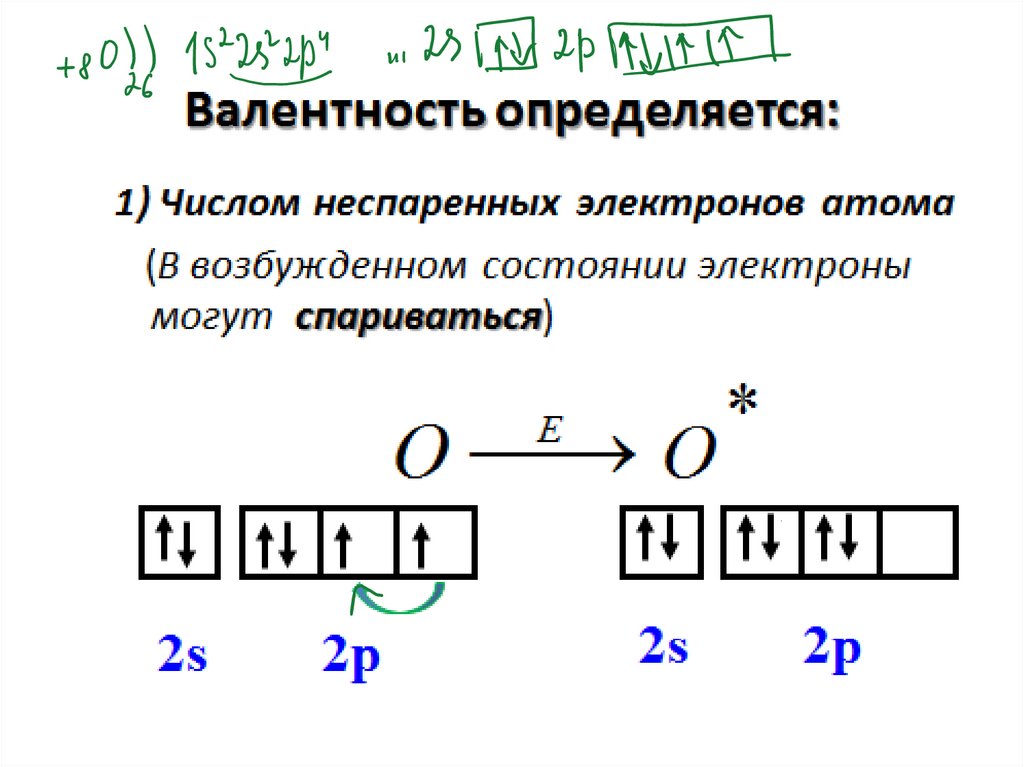
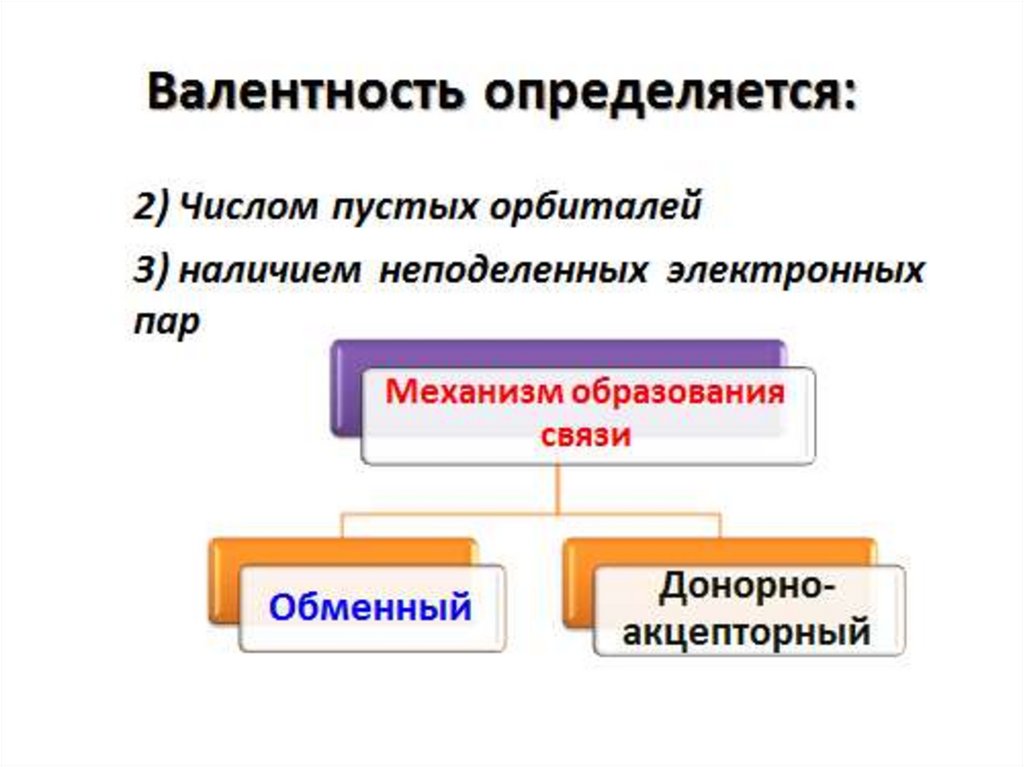
1.
ЭлектроотрицательностьСтепень окисления
Валентность химических элементов
2.
3.
4.
5.
Валентность это число химических связей, которое данныйатом образует с другими атомами.
Электроны, принимающие участие в образовании
химических связей называют валентными
Валентные электроны располагаются на внешнем
уровне (для главных подгрупп)
на внешнем s-подуровне + предвнешнем dподуровне (для побочных подгрупп)
6.
Атом водорода был выбран в качествестандарта, обладающего валентностью,
равной 1.
Валентность обозначается римскими
цифрами.
I I
I II
III I
IV I
НCl H2O
NH3
CH4
7.
Переменная и постояннаявалентность
Есть элементы, которые имеют
постоянную валентность:
H, Li, Na, К, Rb, Cs, F, Ag
I
О, Be, Mg, Ca, Sr, Ba, Zn, Cd II
B, Al
III
8.
Элементыс переменной валентностью
Cu, Hg
I,II
Fe, Co, Ni II, III
Sn, Pb, C
II, IV
P, As
III, V
S
II, IV, VI
Cr
II, III, VI
Mn
II, IV, VI, VII
Cl, Br, I
I, III, V, VII
9.
Алгоритм определения валентности элемента поформуле вещества:
1. над символами химических элементов с постоянной валентностью надписать
валентность элемента
? II
Fe2O3
2. умножить валентность на число атомов этого элемента
IIx3=6
3.разделить полученное число на число атомов элемента с неизвестной
валентностью; частное является значением валентности данного элемента
6:2=III
III II
Fe2O3
10.
Задание 1: определите валентность элементов поформулам следующих веществ
PH3
CuO
Mn2O7
SO2
SiH4
P2O5
11.
Алгоритм составления формулы вещества повалентности элементов
1. над символами элементов надписать валентности элементов
VI II
S O
2.найти НОК для чисел валентности: 6
3. разделить НОК на значение валентности этих элементов:
S (6 : VI=1);
O (6 : II=3)
4.полученные числа это индексы этих элементов в формуле:
SO3
12.
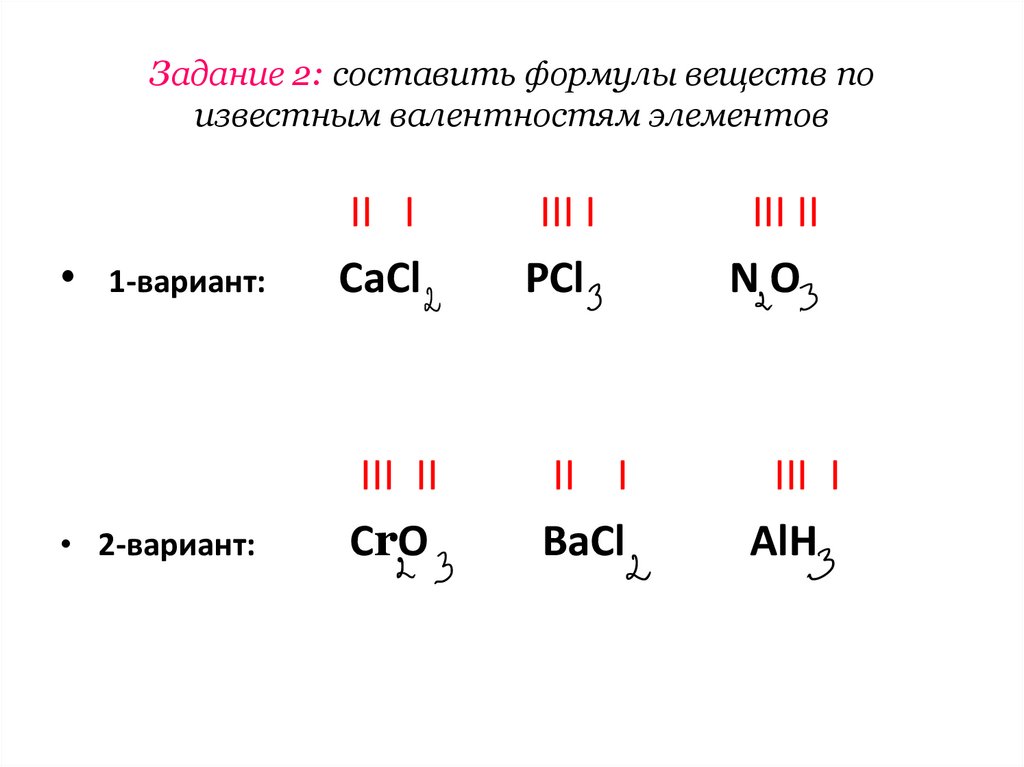
Задание 2: составить формулы веществ поизвестным валентностям элементов
1-вариант:
II I
CaCl
III I
PCl
III II
NO
• 2-вариант:
III II
СrO
II I
BaCl
III I
AlH
13.
14.
15.
16.
Структурная формула • это графическое изображениехимического строения молекулы
вещества, в котором
показывается порядок связи
атомов, их геометрическое
расположение. Кроме того, она
наглядно показывает
валентность атомов входящих в
ее состав.
17.
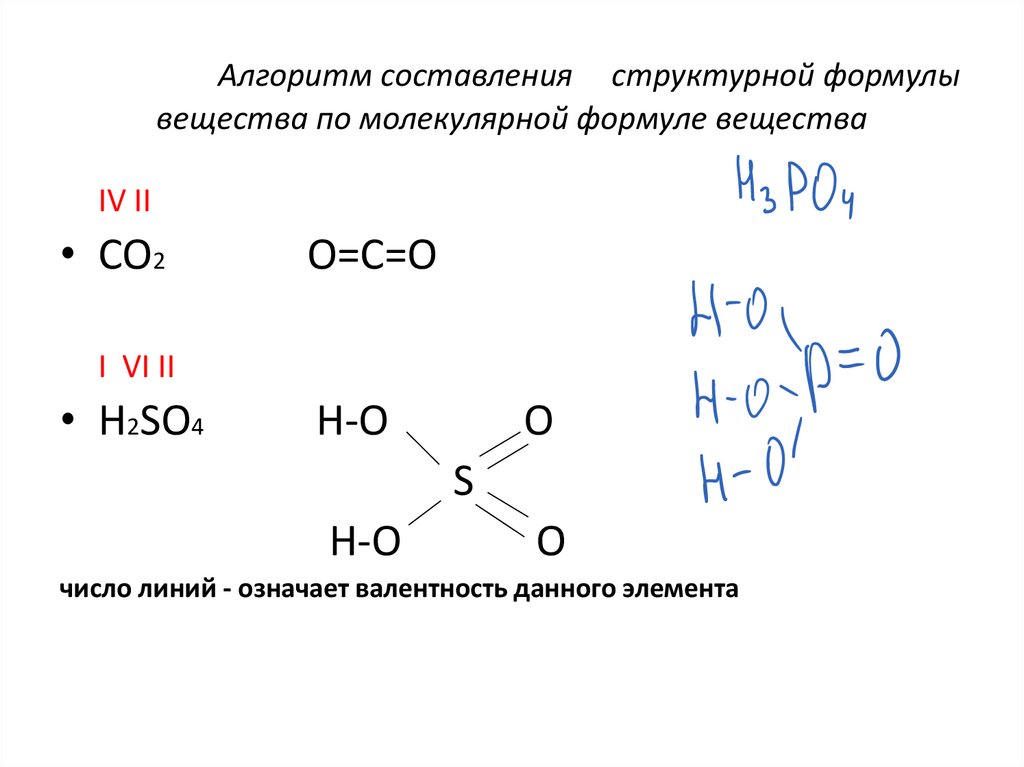
Алгоритм составления структурной формулывещества по молекулярной формуле вещества
IV II
• CO2
O=C=O
I VI II
• H2SO4
H-O
O
S
H-O
O
число линий - означает валентность данного элемента
18.
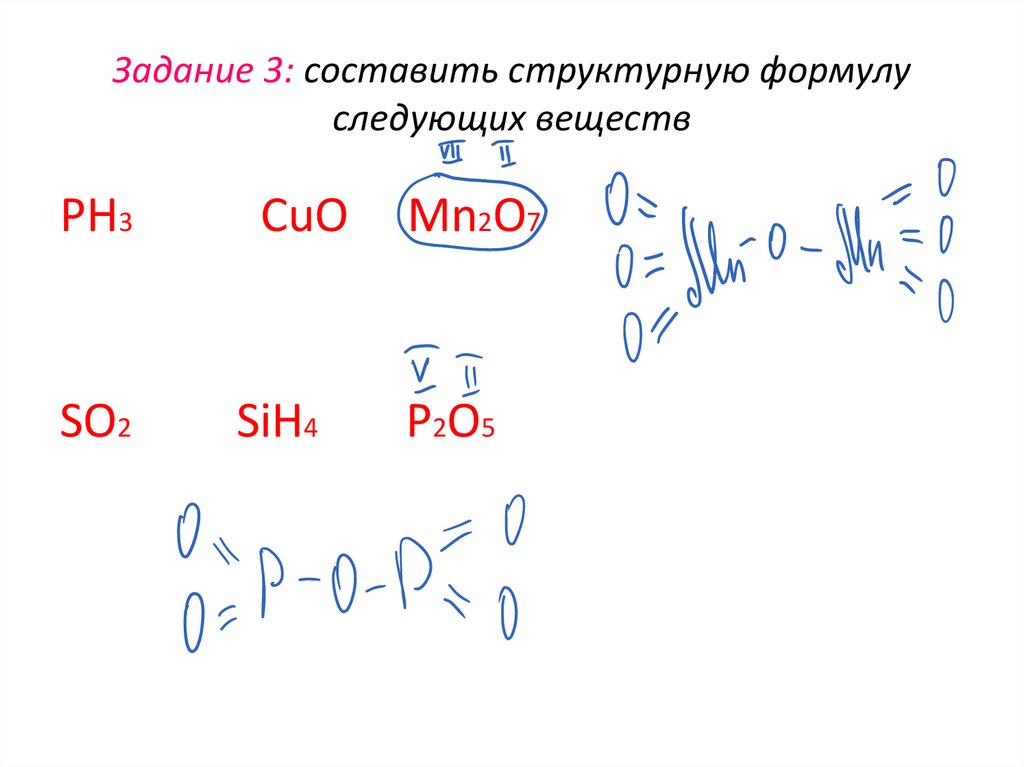
Задание 3: составить структурную формулуследующих веществ
PH3
CuO
Mn2O7
SO2
SiH4
P2O5
19.
20.
21.
22.
23.
24.
1)Степень окисления простых веществ равна нулю
Например: S0, H02, Cl02, O02, Na0.
2) Максимальная (высшая) степень окисления равна + номер
группы (элемент на первом месте)
Например: P2+5O5 , S+6F6.
Если степень окисления переменная – будет указано в скобках.
3) Минимальная степень окисления равна – ( 8 – номер группы)
(элемент на втором месте)
Например: SCl2-1 , Li3P-3.
4) Постоянные степени окисления:
* H +1 (кроме гидридов активных металлов, например:Na+1H-1)
* O-2 (кроме O+2F2, H2O2-1,пероксидов металлов)
* F-1
* металлы первой А группы–степень окисления +1
* металлы второй А группы– степень окисления +2
* металлы третьей А группы – степень окисления +3
25.
Cl+14
+7
2
O
-2
7
-14 =0
В соединениях суммарная степень окисления всегда равна
нулю. Зная это и степень одного из элементов, всегда можно
найти степень окисления другого элемента по формуле
бинарного соединения. Например, найдём степень окисления
хлора в соединении Cl2O7. Обозначим степень окисления
кислорода: Cl2O7-2.Следовательно, семь атомов кислорода
будут иметь общий отрицательный заряд(-2).7=-14. Тогда
общий заряд двух атомов хлора будет равен+14, а степень
окисления одного атома:
(+14):2=+7
26.
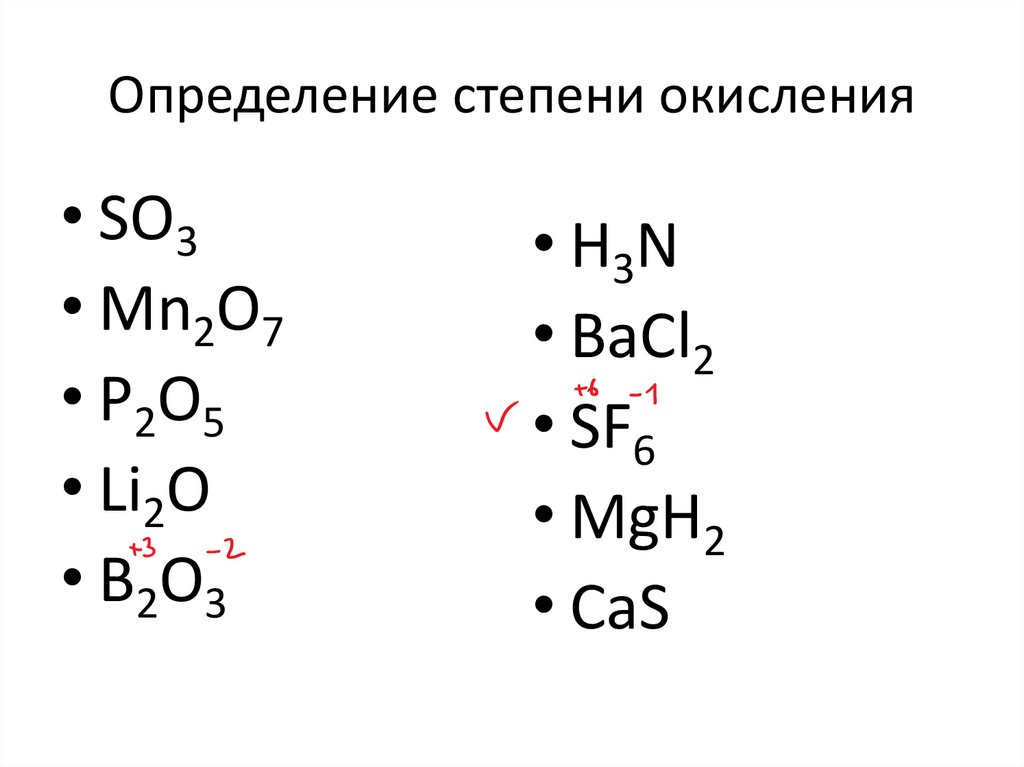
Определение степени окисления• SO3
• Mn2O7
• P2O5
• Li2O
• B2O3
• H3N
• BaCl2
• SF6
• MgH2
• CaS
27.
Правило: алгебраическая сумма степеней окисления всложном ионе равна суммарному заряду этого иона.
(S2 O3-2)2Рассмотрим пример:
+4
-6
=-2
Обозначим степень окисления кислорода-2 .Три иона
кислорода будут иметь общий отрицательный заряд
(-2).3=-6. Тогда общий заряд двух ионов серы будет
равен+4, а одного иона (+4):2=+2
(S22+O3-2)2-
28.
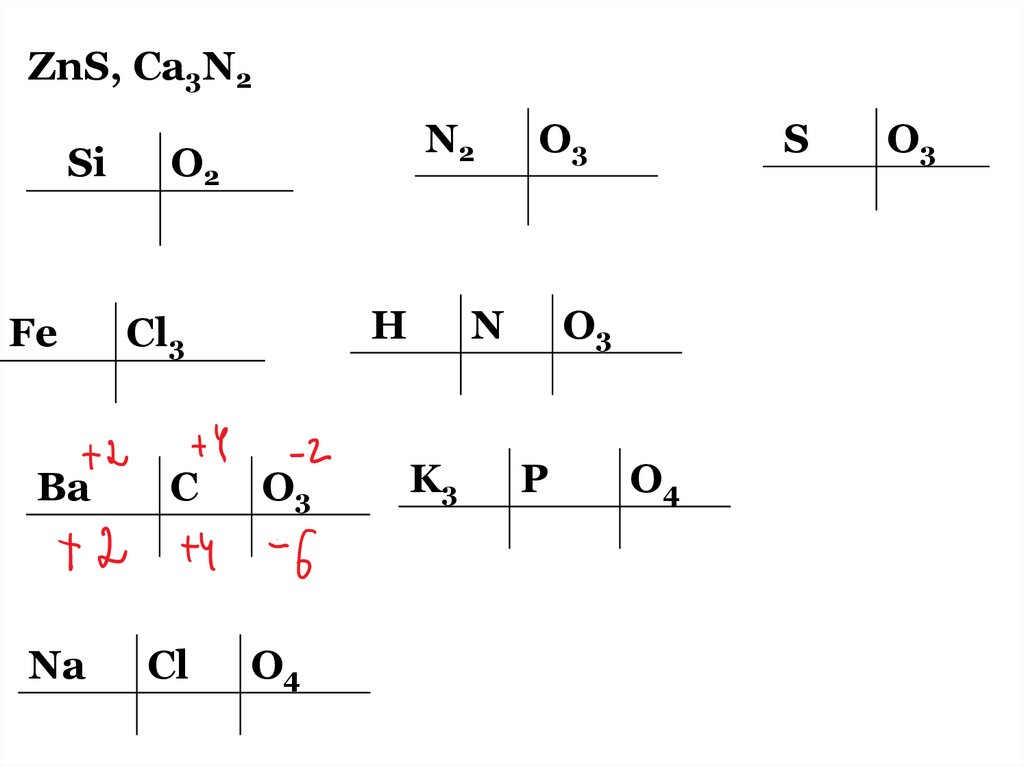
ZnS, Ca3N2Si
Fe
N2
O2
H
Cl3
Ba
C
O3
Na
Cl
O4
O3
N
K3
S
O3
P
O4
O3
29.
Составление формул по степени окисленияОксид натрия Хлорид железа (III) Нитрид магния Оксид серы (IV) -
Сульфид алюминия Гидрид магния -
30.
1)Расставьте
степени
окисления в
соединениях и в
ионах:
MgO
Zn
KNO3
HMnO4
CaSО3
Na3PO4
(CrO4)-2
(IO4)-
2) Составьте формулы
следующих соединений:
Хлорид железа(III)
Оксид серы(VI)
Гидрид калия
Нитрид бария
3) Назовите вещества,
представленные формулами:
P2O5
AgBr
CuS
NaH
31.
проверь знанияI вариант
II вариант
1) Расставьте степени окисления в соединениях и в ионах:
H2SO3 H4P2O7 ZnF2
BaCO3 O2 Na2SO4
(PO4)3-, (MnO4)-
CaBr2 KClO4 S8
Na2Cr2O7 Li2SO4 MgSiO3
(ClO2)- ,(NO3)-
2) Составьте формулы следующих соединений:
Хлорид магния
Сульфид железа (III)
Оксид бора
Нитрид кальция
Оксид азота(II)
Фторид алюминия
Гидрид бария
Оксид серы(IV)
Сульфид магния
Нитрид лития
3) Назовите вещества, представленные формулами:
LiH , CuO, FeCl3, Ag2S
FeCl2, CaH2, CO2, Al2S3
























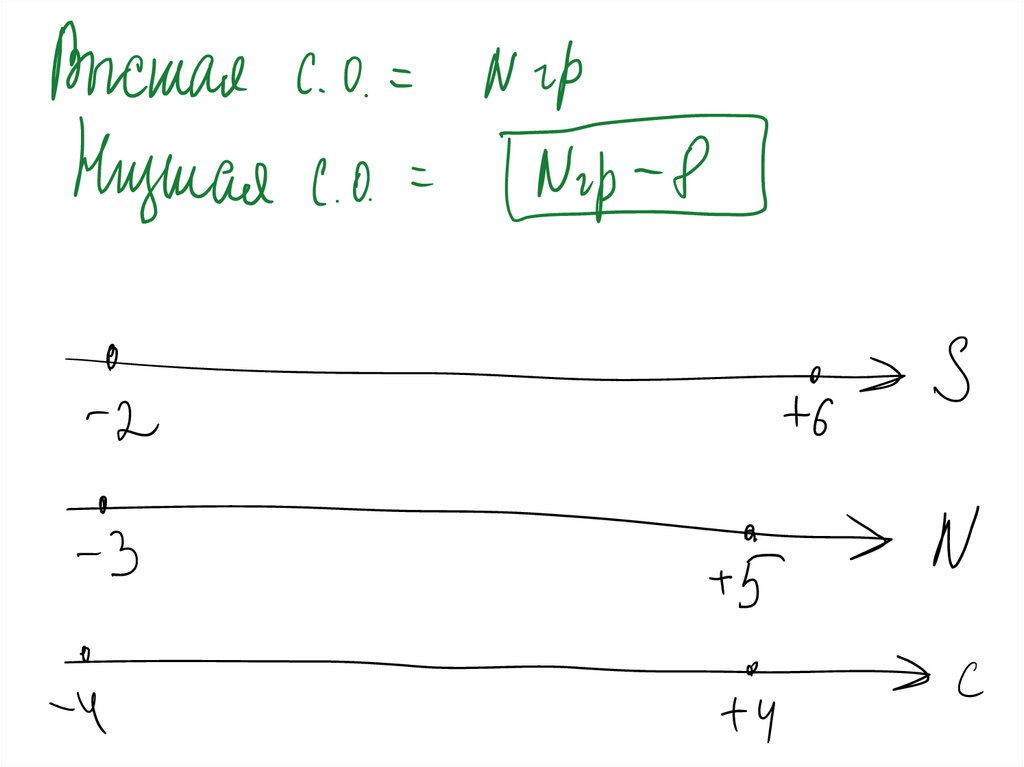

 Химия
Химия








