Похожие презентации:
Водород. Опыт Пилатра де Розьера (8 класс)
1.
Ильина И.В., руководитель ЦДОШ, учитель химииМБОУ «Средняя общеобразовательная школа №27
имени А.А. Дейнеки» г. Курска
E-mail мой: ilina.irina71@mail.ru
2.
Допиши химические реакции иукажи их тип:
1) 2H2O2 = 2Н2О + О2
2) 2HgO = 2Hg + O2
3) S + O2= SO2
4) CH4 +2O2= CO2 + 2H2O
3.
ПРОВЕРЬ СЕБЯ1. Водород открыл:
А) Д. И. Менделеев;
Б) Карл Шееле;
В) Генри Кавендиш;
Г) Антуан Лавуазье.
2. Название водороду дал:
А) Д. И. Менделеев;
Б) Карл Шееле;
В) Генри Кавендиш;
Г) Антуан Лавуазье.
3. Водород – как химический элемент во Вселенной
занимает…
А) первое место; Б) второе место; В) третье место.
4.
«Границ научному познанию ипредсказанию предвидеть
невозможно» Д.И.Менделеев.
Физические и химические
свойства водорода.
Применение водорода.
5.
Физические свойства1. Газ без цвета, вкуса и запаха.
2. t0пл. -259,10С.
3. t0кип. -2530С.
4. Легче воздуха в 14,5 раз.
5. Плохо растворим в воде.
6. Хорошо растворим в некоторых
металлах (например, Pd).
7. Самая высокая теплопроводность
среди газообразных веществ (в 7
раз выше теплопроводности
воздуха).
6.
Взаимодействиес простыми веществами
Взаимодействие с неметаллами
S + H2 = H2S
N2 + 3H2 = 2NH3
F2 + H2 = 2HF
Cl2 + H2 = 2HCl
Водород взаимодействует с активными
металлами, образуя гидриды:
2Na + H2 = 2NaH
Ca + H2 = CaH2
7.
Взаимодействиесо сложными веществами
Взаимодействует с оксидами
металлов
• CuO + H2 = Cu + H2O
• Fe2O3 + 3H2 = 2Fe + 3H2O
• WO3 + 3H2 = W + 3H2O
8.
Обычно легок и летуч,Он вдруг становится могуч:
Его нагрев, неосторожно
Взорвать в округе все возможно.
Осторожно: ВОДОРОД!
Наиболее взрывоопасная смесь,
состоящая из двух объёмов водорода
и одного объёма кислорода –
«гремучий газ»
2H2 + O2 = 2H2O + Q
Вывод: прежде чем поджигать водород,
необходимо проверить его на чистоту.
9.
Опыт Пилатра де РозьераКак-то он решил проверить, что
будет, если вдохнуть водород; до
него никто такого эксперимента не
проводил. Не заметив никакого
эффекта, ученый решил убедиться,
проник ли водород в легкие. Он еще
раз глубоко вдохнул этот газ, а затем
выдохнул его на огонь свечи, ожидая
увидеть вспышку пламени. Однако
водород в легких экспериментатора
смешался с воздухом, и произошел
сильный взрыв.
10.
Осуществите превращенияH2 → H2S → SO2 → SO3
1) H2 + S = H2S
2)2H2S +3O2 =2SO2 + 2H2O
3)2 SO2 + O2 = 2SO3
11.
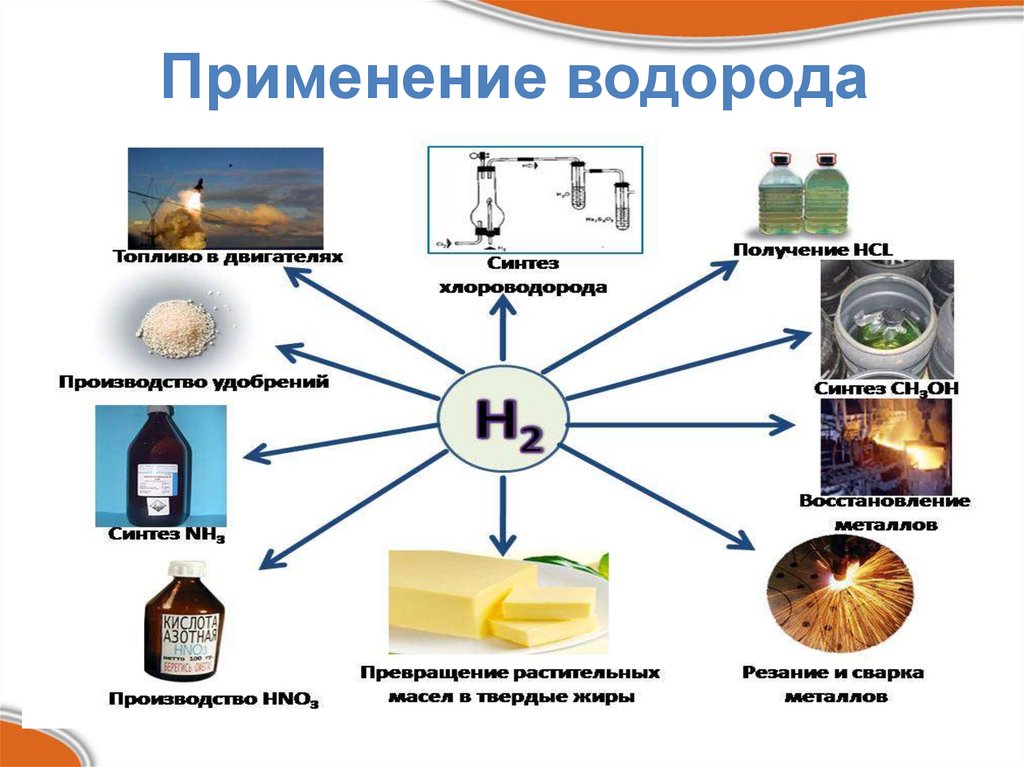
Применение водородаПрименение водорода в
металлургии. Водород как
восстановитель, для получения
металлов и неметаллов (кремния,
вольфрама)
Смесь кислорода с
водородом используют при
сварке и резке металлов.
12.
Применение водородаВодород является активным
газом и в соединениях с азотом
может использоваться в
производстве листового, полого
стекла и оптического волокна.
Превращение жидких
растительных масел в
твердые жиры – маргарин.
13.
Применение водородаВоенная промышленность
(производство
водородных бомб)
В продажу водород поступает в баллонах.
Они окрашены в тёмно-зелёный цвет и
снабжаются красной надписью "Водород"
14.
Применение водорода15.
Подумаем и ответим. (да или нет)1. Водород самый тяжелый газ.
2. Если он чистый, загорается со слабым
звуком.
3. Восстанавливает металлы из оксидов
4. Взаимодействует с водой.
5. Применяется при сварке металлов.
6. Соединяясь с серой, образует газ с запахом
тухлого яйца.
7. Распространенный элемент в воздухе.
16.
Домашнее задание1. Параграф 15
2. Задача №1 (из презентации)
3. Упражнения №1 и №2 (из презентации)
Пишите в электронный журнал или на мою почту.
E-mail мой: ilina.irina71@mail.ru
17.
Домашнее заданиеУпражнение №1. Осуществите превращения:
эл.ток
H2→ MgH2 → H2О → H2 → Н2S → SO2.
Определите тип реакции.
Упражнение №2. Составьте уравнения реакций
взаимодействия
водорода
со
следующими
веществами: F2, Ca, Al2O3, оксидом ртути (II),
оксидом вольфрама (VI).
Задача №1. По термохимическому уравнению
2 Н2 + О2 = 2 Н2О + 573 кДж рассчитайте
количество теплоты, которая выделится при
сжигании 7 литров водорода.
















 Химия
Химия








