Похожие презентации:
Диеновые углеводороды
1.
Диеновые углеводороды2.
Определение диеновых углеводородовДиеновые углеводороды (диены) — это органические соединения, содержащие две двойные связи между
атомами углерода в молекуле. Их общая формула — CₙH₂ₙ₋₂.
В зависимости от расположения двойных связей диены делятся на три типа:
Изолированные – двойные связи
Сопряжённые – двойные связи
Кумулированные – двойные связи
разделены двумя и более
чередуются с одинарной (C=C–C=C), находятся у одного атома углерода
одинарными связями (C=C–C–C=C). что придаёт им повышенную
(C=C=C).
устойчивость.
3.
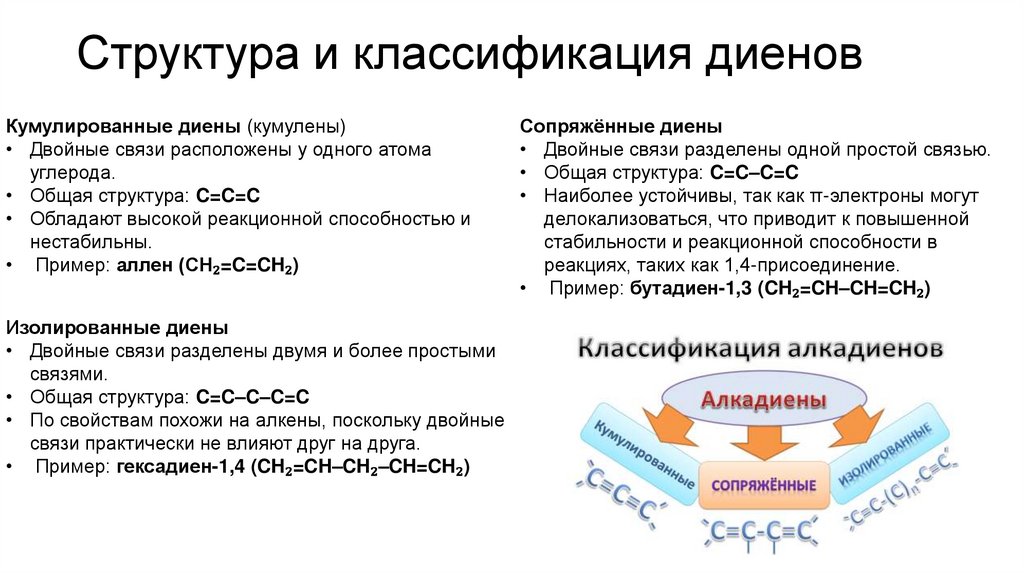
Структура и классификация диеновКумулированные диены (кумулены)
• Двойные связи расположены у одного атома
углерода.
• Общая структура: C=C=C
• Обладают высокой реакционной способностью и
нестабильны.
• Пример: аллен (СH₂=C=CH₂)
Изолированные диены
• Двойные связи разделены двумя и более простыми
связями.
• Общая структура: C=C–C–C=C
• По свойствам похожи на алкены, поскольку двойные
связи практически не влияют друг на друга.
• Пример: гексадиен-1,4 (CH₂=CH–CH₂–CH=CH₂)
Сопряжённые диены
• Двойные связи разделены одной простой связью.
• Общая структура: C=C–C=C
• Наиболее устойчивы, так как π-электроны могут
делокализоваться, что приводит к повышенной
стабильности и реакционной способности в
реакциях, таких как 1,4-присоединение.
• Пример: бутадиен-1,3 (CH₂=CH–CH=CH₂)
4.
Химические свойства диеновыхуглеводородов
1. Реакции присоединения
Присоединение электрофильных реагентов (гидрогена, галогенов, галогеноводородов) проходит по двойным
связям.
Для сопряжённых диенов возможны два типа присоединения:
1,2-присоединение (по первой двойной связи)
1,4-присоединение (по концам сопряжённой системы) – более устойчивый продукт из-за делокализации
π-электронов.
Пример: CH2 = CH − CH = CH2 + HBr → CH3 − CH = CH − CH2Br (1,2−присоединение)
CH2 = CH − CH = CH2 + HBr → CH3 − CHBr − CH = CH2 (1,4−присоединение)
Для изолированных диенов реакция протекает аналогично алкенам, без образования устойчивых
делокализованных структур.
2. Гидрирование (присоединение водорода, восстановление)
Диены можно превратить в алкены или алканы с помощью катализатора (Ni, Pt, Pd):
CH2 = CH − CH = CH2 + H2 Ni CH3 − CH = CH − CH3 При избытке водорода диены полностью насыщаются до
алканов.
5.
3. ОкислениеМягкое окисление (реакция с KMnO₄ в нейтральной среде) – образование гликолей (диолов):
CH2 = CH − CH = CH2 + [O] → CH2(OH) − CH = CH − CH2(OH)
Жёсткое окисление (реакция с KMnO₄ в кислой среде) – разрыв двойных связей с образованием
карбонильных соединений или кислот.
4. Полимеризация
Сопряжённые диены, такие как бутадиен-1,3 и изопрен, легко полимеризуются с образованием эластичных
полимеров – каучуков:
nCH2 = CH − CH = CH2 → (−CH2−CH=CH−CH2−)
Эта реакция важна для производства синтетических каучуков и пластмасс.
5. Реакция Дильса-Альдера (циклоаддиция)
Сопряжённые диены участвуют в реакции с диенофилами (алкенами, алкинами), образуя шестичленные
циклы:
CH2 = CH − CH = CH2 + C2H2 → циклогексен
Это ключевая реакция в органическом синтезе, применяемая в фармацевтике и химической промышленности.



 Химия
Химия








