Похожие презентации:
Ревматические болезни. Пороки сердца
1. Ревматические болезни. Пороки сердца.
High-Yield concepts2. Введение
• Ревматическиеболезни
—
группа
заболеваний,
характеризующихся
системным поражением соединительной
ткани
и
сосудов,
обусловленным
иммунными нарушениями.
• Аутоиммунные реакции – основной
механизм эволюции и морфогенеза
ревматических заболеваний.
3. Концепция аутоиммунных реакций
• 1. Физиологические: присутствие антител противизмененных собственных антигенов (вследствие их
повреждения);
направлено
на
защиту
от
патологических реакций, вызываемых продуктами
распада собственных антигенов.
• 2. Патологические: критерии – 1) специфические
иммунные
реакции
против
конкретных
собственных антигенов; 2) доказательство того, что
развивающаяся иммунная реакция не является
вторичной по отношению к повреждению тканей и
т.п.; 3) отсутствие других явных причин иммунного
ответа.
4. Классификация аутоиммунных заболеваний
ОрганоспецифическиеСистемные
Опосредованные антителами (гуморальные)
Аутоиммунная гемолитическая анемия
Системная красная волчанка
Аутоиммунная тромбоцитопения
Аутоиммунный атрофический гастрит
при пернициозной анемии
Миастения
Болезнь Грейвса-Базедова
Синдром Гудпасчера
Опосредованные Т-клетками (клеточные)
Сахарный диабет, тип1
Ревматоидный артрит
Рассеянный склероз
Склеродермия, синдром Сьогрена
Другие заболевания, принимаемые за аутоиммунные: ВБК, ПБЦ, Узелковые
полиартериит, воспалительные миопатии, аутоиммунный гепатит
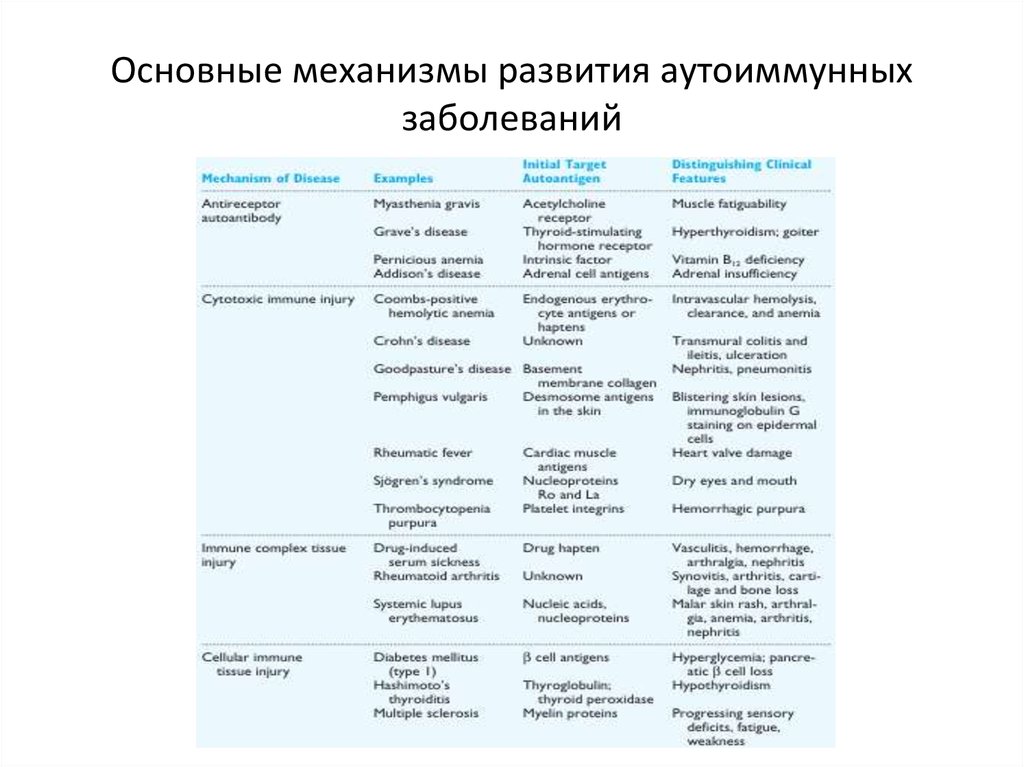
5. Основные механизмы развития аутоиммунных заболеваний
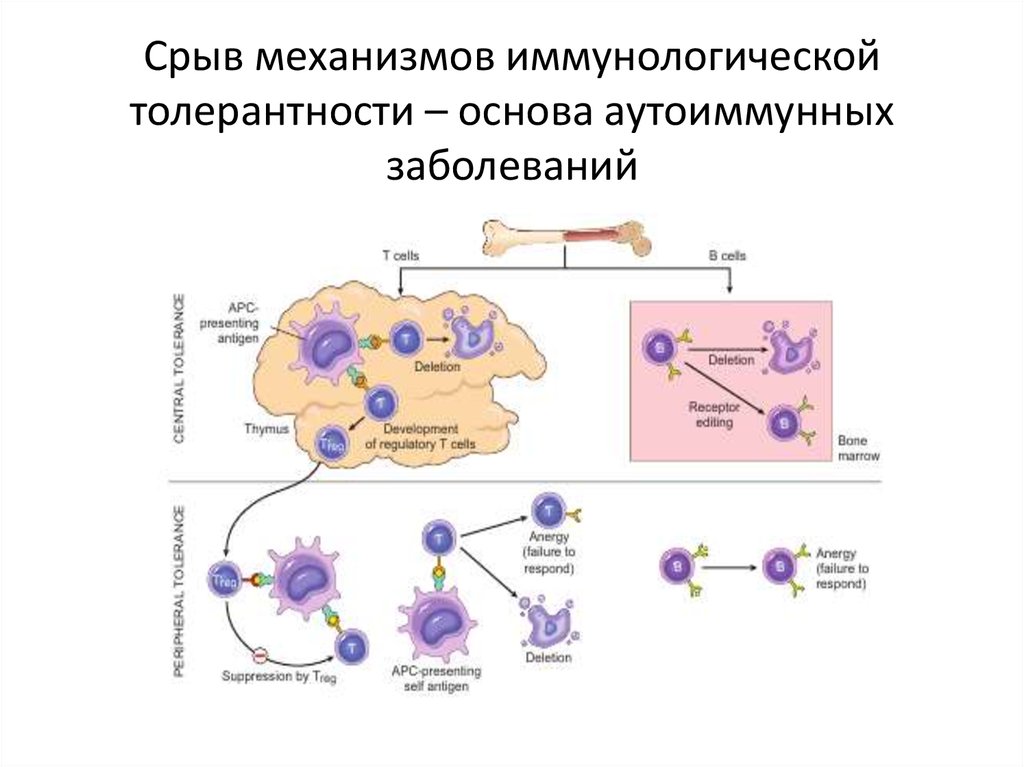
6. Срыв механизмов иммунологической толерантности – основа аутоиммунных заболеваний
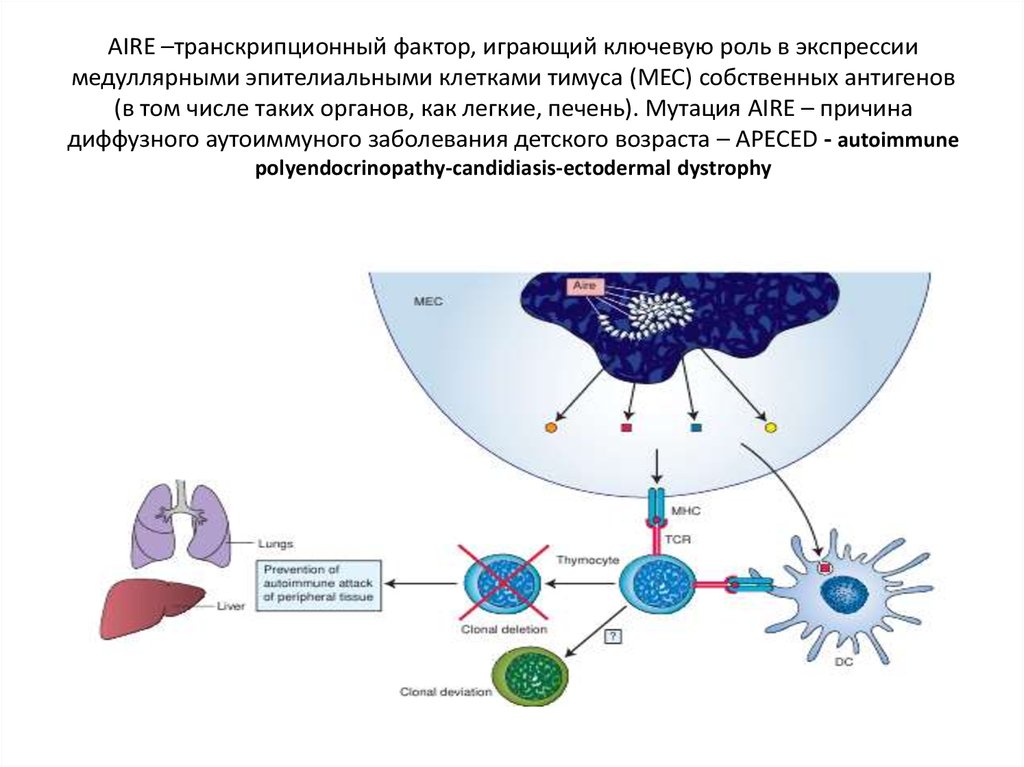
7. AIRE –транскрипционный фактор, играющий ключевую роль в экспрессии медуллярными эпителиальными клетками тимуса (MEC) собственных антигенов (
AIRE –транскрипционный фактор, играющий ключевую роль в экспрессиимедуллярными эпителиальными клетками тимуса (MEC) собственных антигенов
(в том числе таких органов, как легкие, печень). Мутация AIRE – причина
диффузного аутоиммуного заболевания детского возраста – APECED - autoimmune
polyendocrinopathy-candidiasis-ectodermal dystrophy
8. Популяция Т-регуляторных клеток предотвращает иммунные реакции против собственных антигенов
Treg представляют собой CD4+ Тсубпопуляцию,с
высокой
степенгнью экспрессии CD25, альфацепи ИЛ2-рецептора и наличием
транскрипционного фактора FOXP3,
играющего ключевую роль в
созревании
и
поддержании
функциональной активности этой
субпопуляции.
IPEX синдром - immunodysregulation
polyendocrinopathy enteropathy Xlinked syndrome – ассоциирован с
мутацией гена фактора FOXP3.
Делеция гена FOXP3 может стать
причиной
спотанных
абортов,
поскольку FOXP3+ Т-регуляторные
клетки играют ключевую роль в
развитии
иммунологической
толерантности организма матери по
отношении к плоду
9. Делеция путем апоптоза
Fas-mediated apoptosis of Tcells. Связывание FasL с Fas
вызывает
тримеризацию
Fas. Это активирует домен
смерти, ассоциированный с
Fas, FADD. Прокаспаза 8
связывается с FADD и
происходит ее активация, и
каспазный
каскадный
механизм
приводит
к
апоптозу клетки.
Мутации гена Fas – причина
аутоиммуного
лимфопролиферативного
синдрома (ALPS).
10. Общие механизмы толерантности В-клеток
Общие механизмытолерантности Вклеток
1. Делеция – незрелые
аутореактивные клоны Вклеток взаимодействуют с
мембранно-связанными
собственными антигенами.
2. Анергия –
длительная
функциональная
инактивация
аутореактивных
В-клеток
после их взаимодействия с
растворимым антигеном.
3. Редактирование
рецепторов.
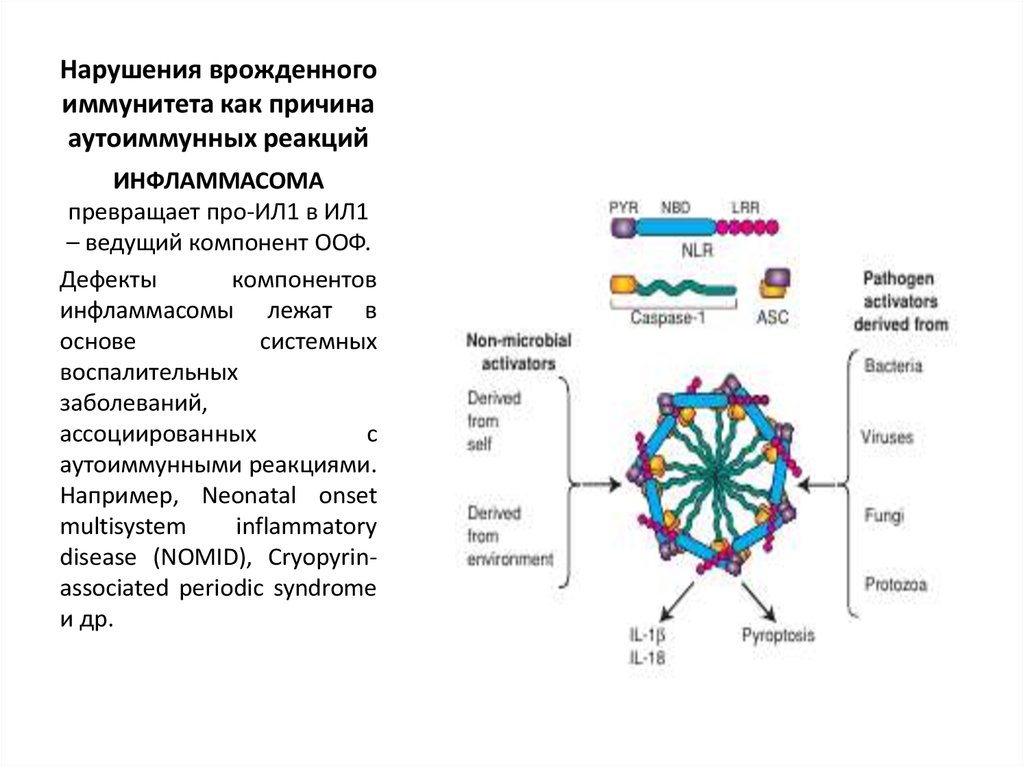
11. Нарушения врожденного иммунитета как причина аутоиммунных реакций
ИНФЛАММАСОМАпревращает про-ИЛ1 в ИЛ1
– ведущий компонент ООФ.
Дефекты
компонентов
инфламмасомы лежат в
основе
системных
воспалительных
заболеваний,
ассоциированных
с
аутоиммунными реакциями.
Например, Neonatal onset
multisystem
inflammatory
disease (NOMID), Cryopyrinassociated periodic syndrome
и др.
12. Пироптоз – тип воспалительной клеточной гибели
1.Взаимодействие
клетки
с
инфекционными и неинфекционными
агентами.
2. Инфламмасомы распознают эпитопы
через PRR, внутри инфламмасомы есть
прокаспаза 1.
3. После активации инфламмасомы в
ней образуется каспаза 1.
4. Каспаза 1 формирует поры в
мембране клетки, что сопровождается
выходом ее компонентов наружу.
5. Вслед за этим разрушается ядро
клетки.
6. Такие внутриклеточные компоненты
как
цитоскелет,
шапероны,
гликопротеины
и
каспаза
7
разрушаются вне клетки.
7. Пироптоз.
Каспаза 1 также называется ИЛ1бетта –
конвертирующим ферментом
13. Причины аутоиммунных расстройств
• Нарушения секвестрацииаутоантигенов:
иммунологическая
привилегированность тканей с
гистогематическими барьерами:
• - симпатический офтальмит;
• - симпатический эпидидимит;
• - синдром Дресслера – 3 «П» –
перикардит, пневмонит, плеврит
(через 2-4 недели после
перенесенного ОИМ).
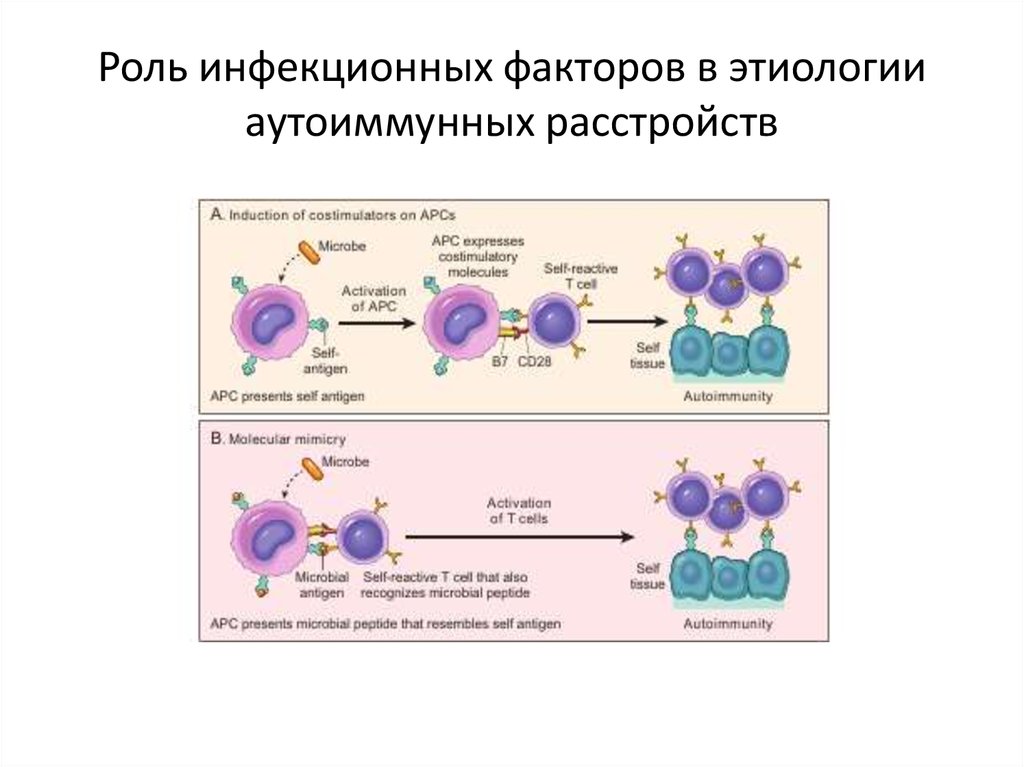
14. Роль инфекционных факторов в этиологии аутоиммунных расстройств
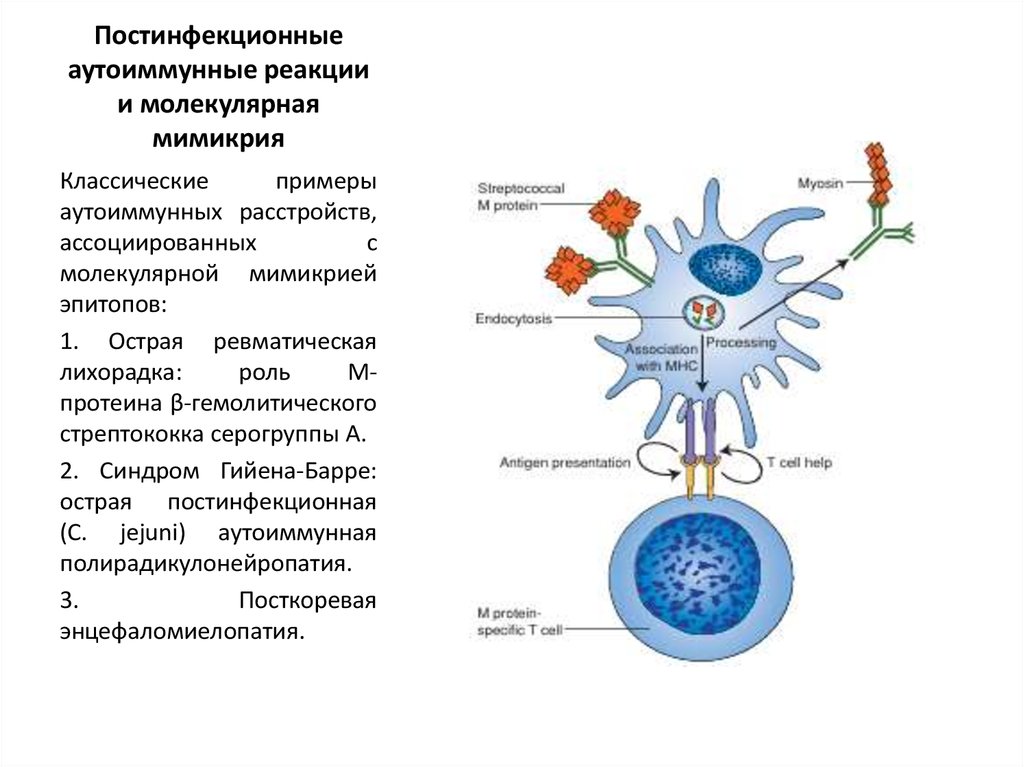
15. Постинфекционные аутоиммунные реакции и молекулярная мимикрия
Классическиепримеры
аутоиммунных расстройств,
ассоциированных
с
молекулярной мимикрией
эпитопов:
1. Острая ревматическая
лихорадка:
роль
Мпротеина β-гемолитического
стрептококка серогруппы А.
2. Синдром Гийена-Барре:
острая постинфекционная
(C. jejuni) аутоиммунная
полирадикулонейропатия.
3.
Посткоревая
энцефаломиелопатия.
16. Роль генетической предрасположенности
• Большинствоаутоиммунных
болезней
являются комплексными мультигенными и
мультифакториальными расстройствами.
Многие
менделирующие
(моногенные)
аутоиммунные болезни были упомянуты
ранее: APECED, IPEX, APLS и др.
• Генетическая предрасположенность может
быть
ассоциирована
с
носительством
определенных генов системы HLA и не-HLAполиморфизмов.
17. Роль HLA-генов в развитии аутоиммунных заболеваний
Молекулы главного комплекса гистосовместимости I класса (A, B, C)представляют пептиды из цитоплазмы на поверхности клетки (включая
вирусные пептиды при их наличии). Эти пептиды представляют собой
фрагменты белков, разрушенных в протеасомах. Длина пептидов в среднем
около 9 аминокислот. Чужеродные антигены привлекают клетки Ткиллеры (также называемые CD8 положительные или цитотоксические Тклетки), которые уничтожают клетку-носитель антигена. Молекулы этого класса
присутствуют на поверхности всех типов клеток, кроме эритроцитов и
клеток трофобласта.
Молекулы главного комплекса гистосовместимости II класса (DP, DM, DOA,
DOB, DQ, DR) представляют антигены из пространства вне клетки в неё, в
частности T-лимфоцитам. Некоторые антигены стимулируют деление клеток Тхелперов, которые затем стимулируют B-клетки для производства антител к
данному антигену. Молекулы этого класса находятся на поверхности
антигенпредставляющих клеток: дендритных клеток, макрофагов, Bлимфоцитов.
18. TAP-протеасомный путь в MHC I и роль HLA-DM в MHC II презентации антигенов
19. Роль не-HLA-генов в развитии аутоиммунных заболеваний
20. Общие морфогенетические черты ревматических болезней:
• наличие признаков хронического воспаления ангиогенез,склероз,
преобладанием
мононуклеарной круглоклеточной инфильтрации;
• нарушения иммунного гомеостаза в виде реакций
гиперчувствительности немедленного (II и III)и
замедленного типов;
• системная прогрессирующая дезорганизация
соединительной ткани;
• генерализованный васкулит;
• хроническое течение с обострениями.
21. Системная дезорганизация соединительной ткани
Поражения соединительной ткани при этихзаболеваниях заключаются в её системной
прогрессирующей дезорганизации.
Различают 4 последовательные фазы
дезорганизации:
• мукоидное набухание;
• фибриноидные изменения;
• воспалительные клеточные реакции;
• склероз.
22. Ревматическая лихорадка и ревматическая болезнь сердца
• RF–
острая,
иммунологически
опосредованная,
мультисистемная
воспалительная
болезнь,
классически
развивающаяся через несколько недель
после
перенесенного
фарингита,
вызванного
β-гемолитическим
стрептококком группы А.
• RHD – фактически единственная причина
приобретенного митрального стеноза.
23. Group A beta-hemolytic streptococcal infection (GABHS) и критерии Centor’s
Существуют 4 клиническихпризнака, в наибольшей
степени указывающих на
эмпирическую
роль
βгемолитического
S.
pyogenes
гр.
A
в
возникновении фарингита:
1. Повышение температуры
выше 38 ° C.
2. Болезненность передних
шейных
лимфатических
узлов.
3. Отсутствие кашля.
4.Фаринго-тонзиллярный
экссудат.
Наличие
3-х
из
4-х
признаков
–
90%
вероятность наличия GABHS.
24. John’s клинические критерии диагноза ревматической лихорадки (1992 г)
Основные («большие») критерии:• 1) кардит, 2) мигрирующий полиартрит крупных
суставов, 3) хорея Сиденхэма, 4) подкожные узлы,
5) кольцевидная эритема,
• «Малые» критерии: 1) лихорадка, 2) артралгии, 3)
увеличение СОЭ, С-реактивного белка,
лейкоцитоз.
• Кроме того, большое значение имеют
повышенный титр противострептококковых AT
(АСЛ-О, АСК, АСГ) и высевание из зева βгемолитического стрептококка группы А.
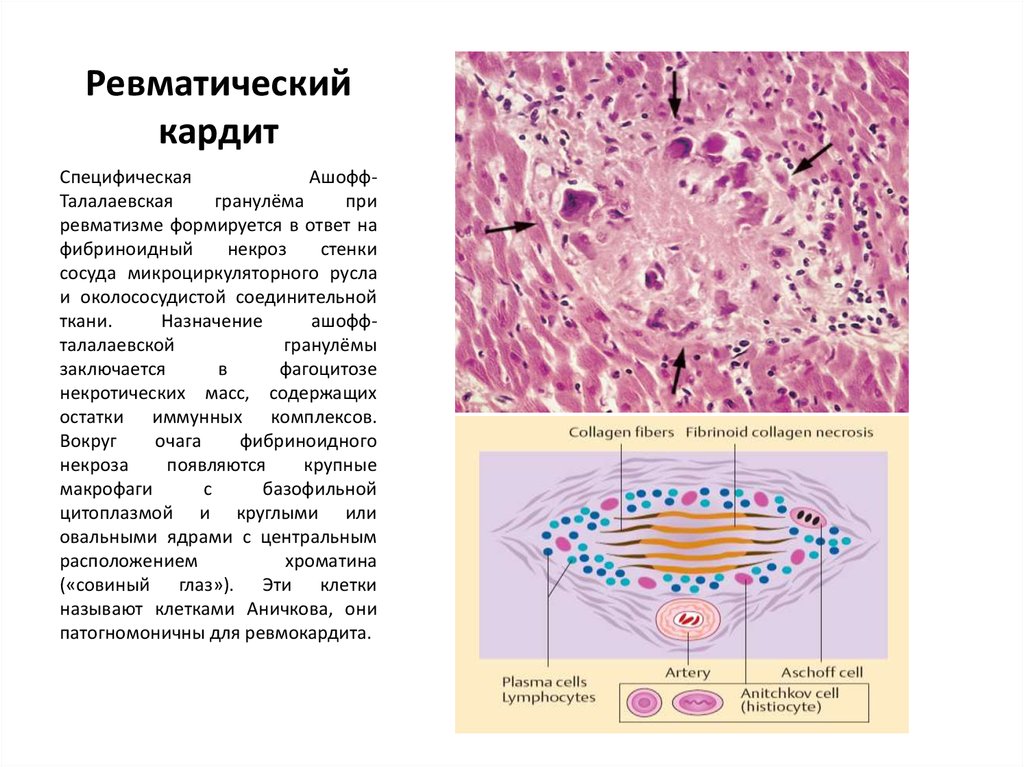
25. Ревматический кардит
СпецифическаяАшоффТалалаевская
гранулёма
при
ревматизме формируется в ответ на
фибриноидный
некроз
стенки
сосуда микроциркуляторного русла
и околососудистой соединительной
ткани.
Назначение
ашоффталалаевской
гранулёмы
заключается
в
фагоцитозе
некротических масс, содержащих
остатки иммунных комплексов.
Вокруг
очага
фибриноидного
некроза
появляются
крупные
макрофаги
с
базофильной
цитоплазмой и круглыми или
овальными ядрами с центральным
расположением
хроматина
(«совиный глаз»). Эти клетки
называют клетками Аничкова, они
патогномоничны для ревмокардита.
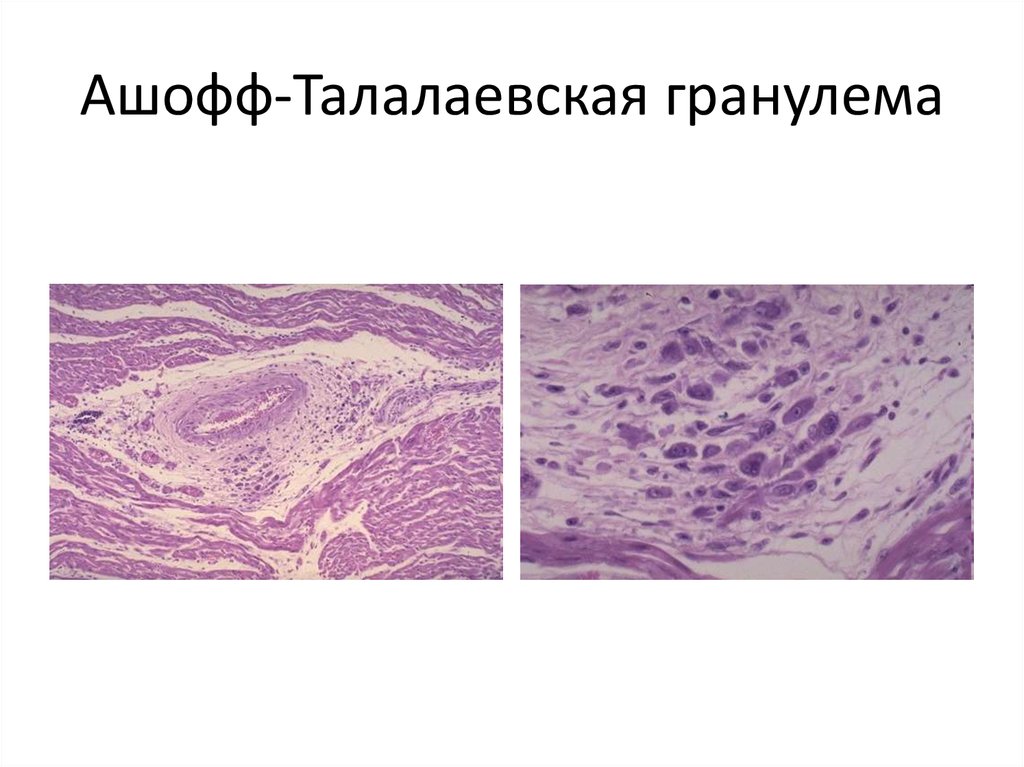
26. Ашофф-Талалаевская гранулема
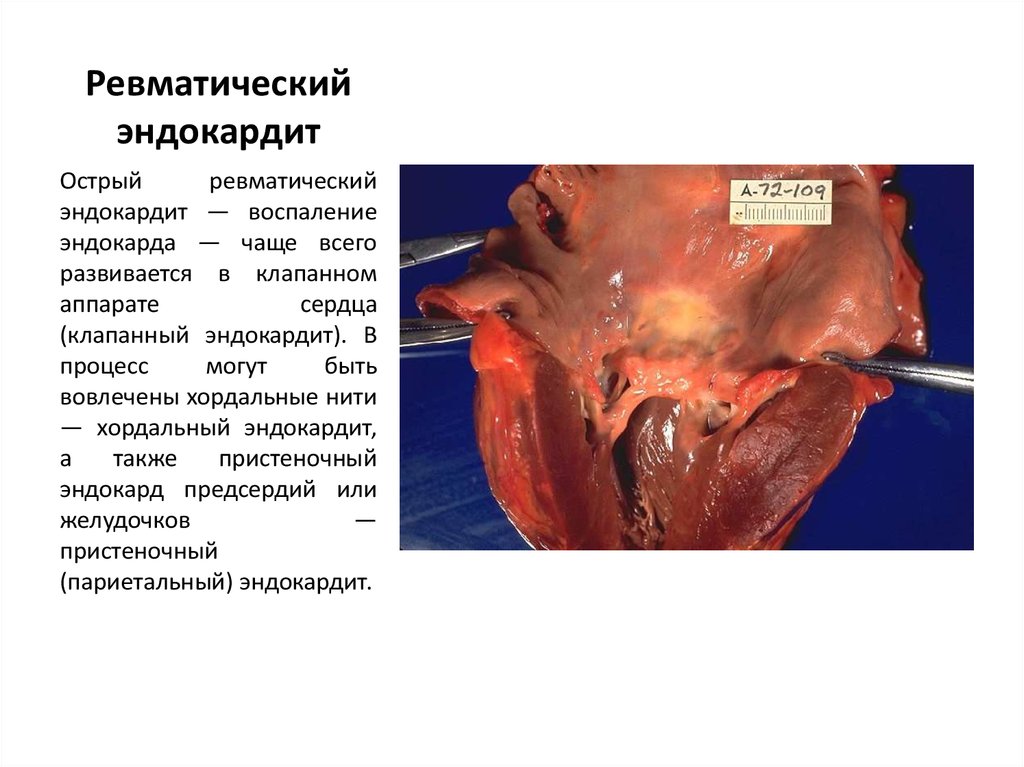
27. Ревматический эндокардит
Острыйревматический
эндокардит — воспаление
эндокарда — чаще всего
развивается в клапанном
аппарате
сердца
(клапанный эндокардит). В
процесс
могут
быть
вовлечены хордальные нити
— хордальный эндокардит,
а
также
пристеночный
эндокард предсердий или
желудочков
—
пристеночный
(париетальный) эндокардит.
28. Ревматический эндокардит
Выделяют 4 видасвязанных между собой
морфологических
изменений клапанов
сердца:
- диффузный эндокардит
(или вальвулит),
- острый бородавчатый,
- фибропластический,
- возвратнобородавчатый
эндокардиты.
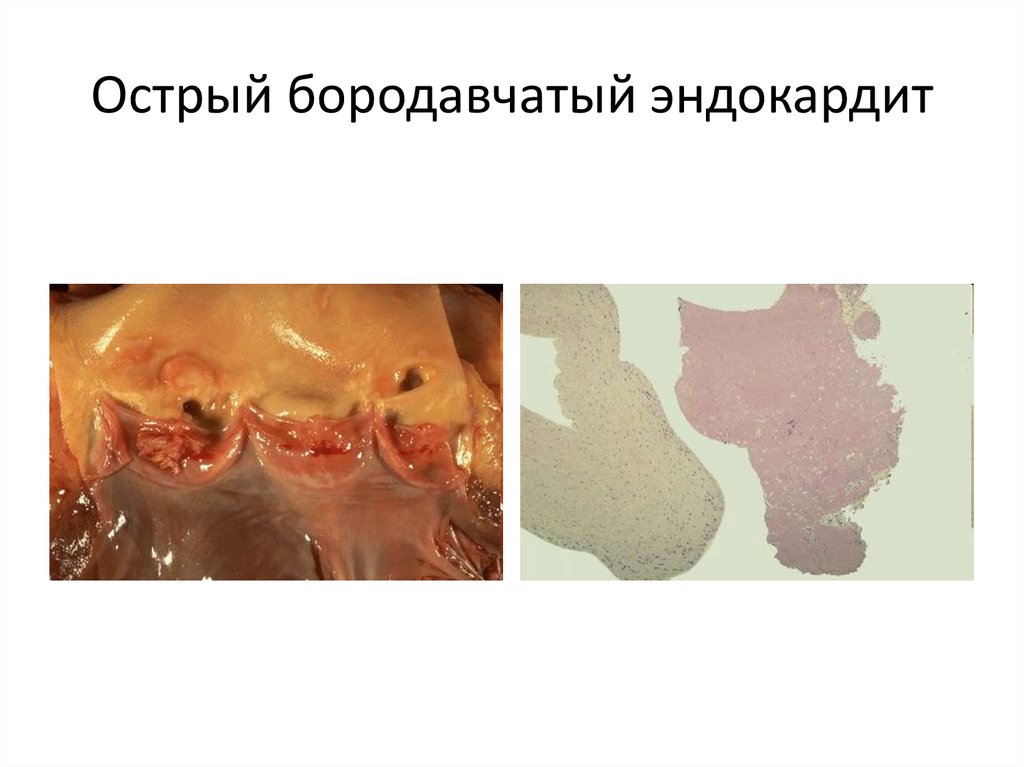
29. Острый бородавчатый эндокардит
30. Особенности ревматического и неревматического эндокардитов: 1) острая фаза РЛ характеризуется появлением мелких бородавчато-подобных вег
Особенности ревматического и неревматического эндокардитов: 1)острая фаза РЛ характеризуется появлением мелких бородавчатоподобных вегетаций по линии соединения створок клапанов; 2) при
инфекционном эндокардите определяются крупные, иррегулярные
массы вегетаций в стенках самих створок с распространением на
хордальные нити; 3) небактериальный тромбоэндокардит – круглые
оформленные вегетации по линии соединения створок; 4) эндокардит
Либмана-Сакса – мелкие и средних размеров вегетации как на
желудочковой, так и на предсердной стороне клапанных створок.
31. Эволюция клапанного эндокардита при ревматизме
Висходе
эндокардита
развиваются
склероз,
гиалиноз и деформация
клапанных заслонок.
Часто они срастаются друг с
другом,
нередко
развиваются
склероз
и
петрификация фиброзного
кольца.
Хорды
клапанов
также
утолщены, укорочены и
спаяны друг с другом.
Отверстие клапанов обычно
резко сужено, имеет вид
«рыбьего рта».
32. Возвратно-бородавчатый эндокардит
33. Повреждение эндотелия клапанов и «warty» эндокардит
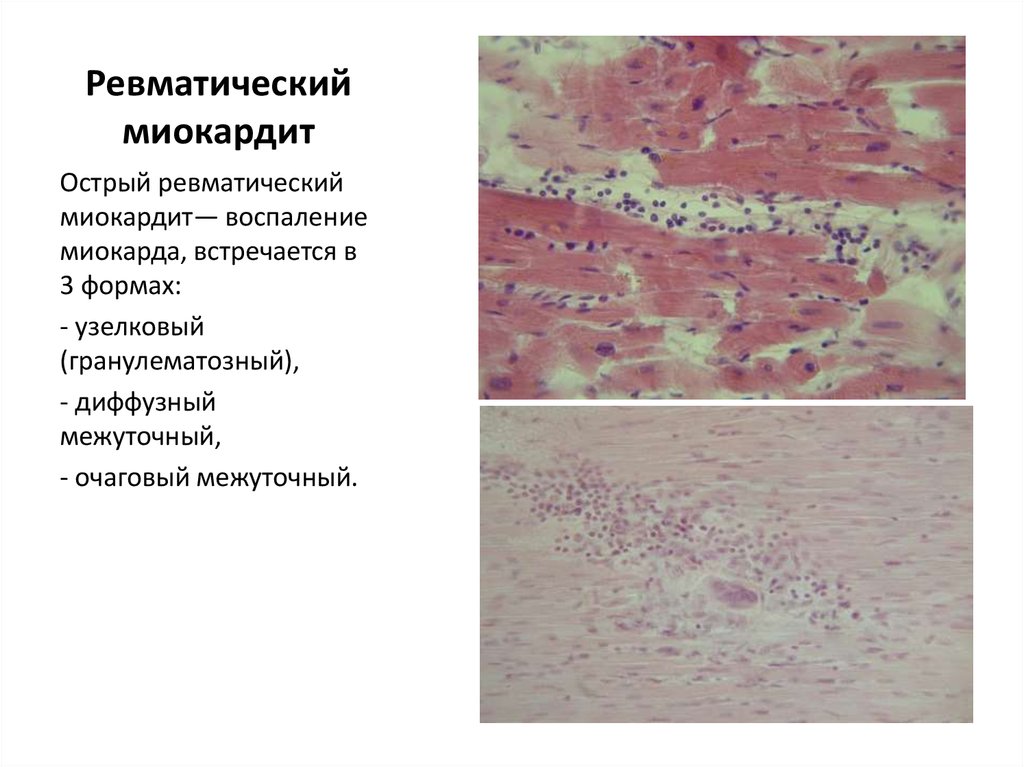
34. Ревматический миокардит
Острый ревматическиймиокардит— воспаление
миокарда, встречается в
3 формах:
- узелковый
(гранулематозный),
- диффузный
межуточный,
- очаговый межуточный.
35. Ревматический миокардит
36. Ревматический перикардит
В перикарде развиваетсясерозное,
серознофибринозное
и
фибринозное воспаление
(«волосатое
сердце»).
При
организации
фибринозного экссудата
образуются синехии и
возникает облитерация
полости
перикарда.
Иногда
происходит
обызвествление
образовавшейся
соединительной
ткани
(«панцирное сердце»).
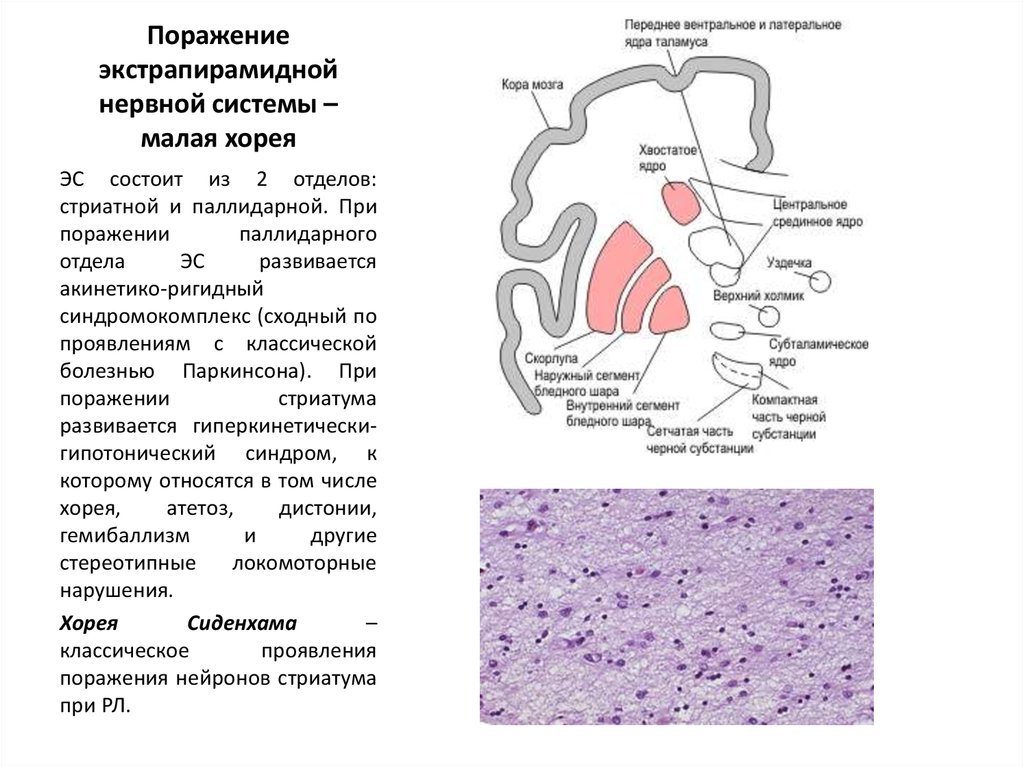
37. Поражение экстрапирамидной нервной системы – малая хорея
ЭС состоит из 2 отделов:стриатной и паллидарной. При
поражении
паллидарного
отдела
ЭС
развивается
акинетико-ригидный
синдромокомплекс (сходный по
проявлениям с классической
болезнью Паркинсона). При
поражении
стриатума
развивается гиперкинетическигипотонический синдром, к
которому относятся в том числе
хорея,
атетоз,
дистонии,
гемибаллизм
и
другие
стереотипные
локомоторные
нарушения.
Хорея
Сиденхама
–
классическое
проявления
поражения нейронов стриатума
при РЛ.
38. Полиартритическая форма RF
• характеризуется поражением крупных суставов сразвитием
очагов
дезорганизации
в
синовиальной оболочке (синовит), васкулитов с
гиперемией
сосудов,
периваскулярными
лимфоидными инфильтратами в виде муфт,
появлением серозного и серозно-фибринозного
выпота в полости сустава.
• Суставной хрящ в процесс не вовлекается,
поэтому деформации суставов при ревматизме не
происходит.
39. Системная красная волчанка
• мультисистемноеаутоиммунное
заболевание
с
широким
набором
продуцируемых аутоантител, в первую
очередь,
антинуклеарных
антител,
участвующих
в
формировании
неэлиминируемых иммунных комплексов,
поражающих различные органы и ткани.
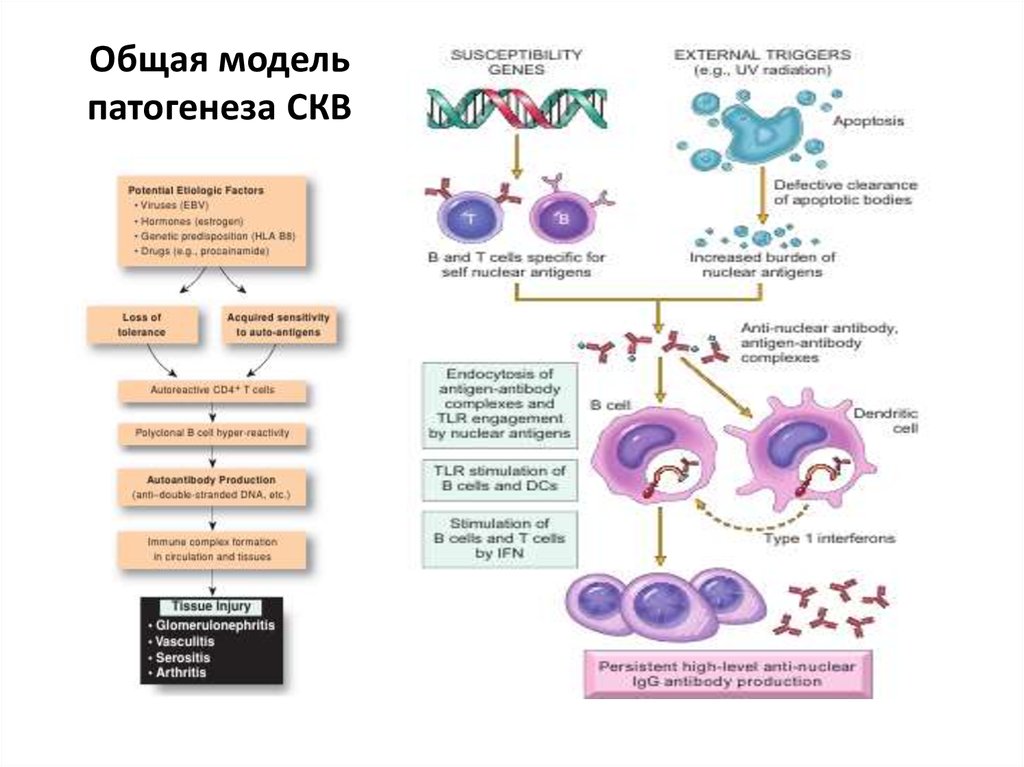
40. Общая модель патогенеза СКВ
41. Патогенез СКВ
• 1. Роль генетических факторов.• 2. Роль иммунных факторов.
• 3. Роль факторов окружающей среды и
гормонального фона.
42. Роль генетических факторов
• Существуют по крайней мере 20 независимых генетическихполиморфизмов, выявленных в качестве факторов риска СКВ.
Среди них:
• HLA-DR2,
• C2/C4,
• FcγRIIA (human platelet IgG Fc receptor),
• PDCD 1 (programmed cell death protein 1),
• PTPN 22 (protein tyrosine phosphatase, non-receptor type 22),
• IRF 5 (IRF5 является членом семейства регуляторных факторов
интерферона),
• TYK 2 (нерецепторная тирозинкиназа 2) и
• TNF-α.
43. Роль иммунологических факторов
1.Роль
В-клеток
определяется
ускользанием аутореактивных клонов от
делеции и продукцией ими аутоантител к
нескольким эпитопам, что отражает
антиген-управляемый характер иммуного
ответа при СКВ.
2.
Доказательства
роли
Т-клеток
включают: 1) ассоциацию СКВ с
некоторыми гаплотипами MHC II класса;
2) продукцией аутоантител, которая
определяется классическим Т-зависимым
ответом в виде переключения синтеза АТ и
соматического гипермутагенеза. CD4+ T
клетки
становятся
аутореактивными
вследствие гипометилирования ДНК и
усиления
экспрессии
адгезивной
молекулы LFA (CD11a), что определяет
устойчивость взаимосвязей с АПК.
44. Другие иммунные нарушения
• Плазмацитоидные дендритные клетки, имеющие провоспалительныйфенотип, способны к продукции IFN-α.
• Цитокиновая сеть с участием IL-4, IL-6, IL-10 и IFN-α отражает
системный характер воспалительного ответа при СКВ.
• ЦИК и ИК in situ – развитие ГЧ III типа, образование цитотоксических
анатител к мембранным антигенам эритроцитов и тромбоцитов - II
тип ГЧ.
• Больные СКВ имеют повышенный уровень циркулирующего
апоптотического детрита («мусора») и нарушенную способность к
фагоцитозу апоптозных телец. Комплексы ДНК / гистоны и РНК /
белки апоптотических клеток специфически связываются с
аутоантителами и активируют как дендритные клетки, так
и
аутореактивные клоны В-клеток с помощью подтипов TLR 7 и 9, что
усиливает синтез IFN-α, универсального индуктора врожденных и
адаптивных иммунных реакций.
45. Виды аутоантител, определяемых у больных СКВ
• 1. АТ к двойной спиральной ДНК – специфичны,ассоциации с нефритом.
• 2. АТ к Smith-антигену (стержневому белку мяРНП) –
специфичны, основа диагностики СКВ.
• 3. АТ к фосфолипидным комплексам мембран (отвечают
за ложно(+)реакцию Видаля, определяют развитием
вторичного АФС)
• 4. Другие АТ - ANA (антинуклеарные): к U1-RNP, гистонам,
ядерным
антигенам,
негистоновым
белкам.
Определяются
методом
непрямой
иимунофлюоресценции.
46. Характер органных поражений при СКВ
Существует несколько клиническихвариантов СКВ:
Лекарственно-индуцированная
СКВ: прокаинамид, гидралазин,
изониазид. Факторы риска –
высокие
дозы
препаратов,
«медленные ацетиляторы», HLADR 4 и 6- гаплотипы. Features that
distinguish drug-induced lupus from
SLE
include:
(1)
Antihistone
antibodies; (2) No antibodies against
native DNA; (3) No decrease in
serum complement levels; (4) A low
incidence of renal and CNS
involvement; (5) Disappearance of
symptoms and laboratory test results
when the drug is discontinued.
47. Морфология СКВ
1. Поражение сосудов - острый некротизирующий васкулит затрагивает
капилляры, малые артерии и артериолы, может присутствовать в любой
ткани. Артериит характеризуется фибриноидныхми отложениями в
сосудистых стенках. В хронической стадии сосуды подвергаются фиброзу с
утолщение стенок и сужением просветов.
2. Поражение кожи носа и щек в виде классической волчаночной
«бабочки» - приблизительно 50% пациентов, но подобная сыпь может
также располагаться на конечностях и туловище. Крапивница,
макулопапулезные поражения, изъязвления также могут иметь место при
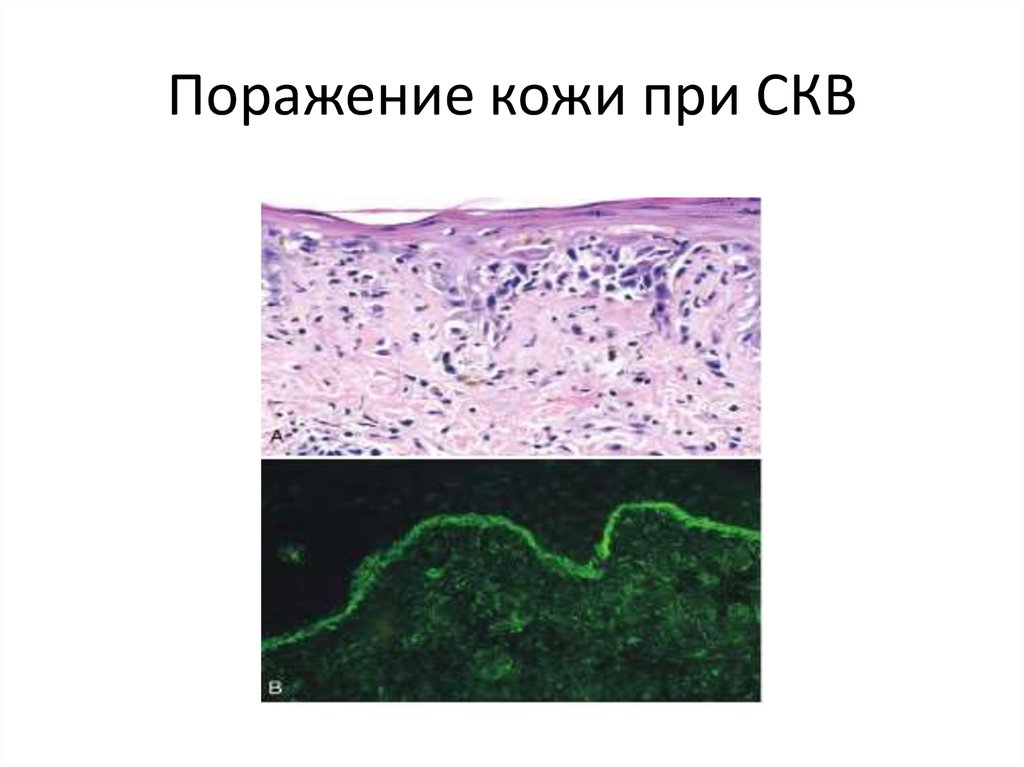
СКВ. Воздействие солнечного света усиливает эритему. Гистологически –
признаки вакуолярной дегенерации базального слоя эпидермиса В дерме
отек и периваскулярные мононуклеарные инфильтраты. Васкулит с
фибриноидным
некрозом
стенки
также
встречается.
Иммунофлуоресцентная
микроскопия
показывает
осаждение
иммуноглобулинов вдоль дермо-эпидермального соединения.
48. Поражение кожи при СКВ
49. Поражение почек при СКВ
1. Минимальный мезангиальныйлюпус-нефрит, класс 1 – отсутствие
изменений на световом уровне, ИК
при РИФ в мезангии.
2. Мезангиальный
пролиферативный люпус-нефрит,
класс 2: пролиферация
мезангиоцитов и накполение
мезангиального матрикса,
гранулярные депозиты ИГ и С без
вовлечения капилляров клубочков.
3. Фокальный люпус-нефрит, класс
3, рис. А.
4. Диффузный люпус-нефрит, класс
4, рис В, С – проволочные петли
5. Мембранозный люпус-нефрит,
класс 5.
6. Распространенный
склерозирующий люпус-нефрит,
класс 6.
50. Поражение сердца при СКВ
ЭндокардитЛибмана-Сакса
51. Гиперпластический («луковичный») склероз артериол селезенки
52. Ревматоидный артрит
53.
54. Морфология ревматоидного артрита
55. Болезнь Бехтерева
• Тип серонегативных спондилоартропатий.• Анкилозирующий спондилит приводит к разрушению
суставного хряща и костному анкилозу, особенно в крестцовоподзвдошных и межпозвоночных суставах (между отростками
позвонков). Он также известен как ревматоидный спондилит и
болезнь Мари-Штрюмпеля. Проявляется на 2-3 десятилетии
жизни в виде болей в нижней части спины и развитием
спинальной неподвижности.
• Вовлечение периферических суставов, таких как бедренный,
коленный и плечевой, происходит, по крайней мере, у одной
трети больных. Примерно 90% пациентов HLA-B27 позитивны;
ассоциации также найдены с геном рецептора IL-23.
56. Склеродермия (системный склероз)
• Аутоиммунноезаболевание
неизвестной
этиологии,
с
избыточной
продукцией
коллагенов 1 и 3 типов в коже и
многих внутренних органов.
• Семейный
случаи
ассоциированы
с
носительством
гаплотипов
HLA-DQB1.
• Пик манифестации – 40-50
лет, женщины страдают в 3-8
раз чаще.
• Формы:
ограниченная
(CREST),
диффузная
склеродермия
и
фульминантная.
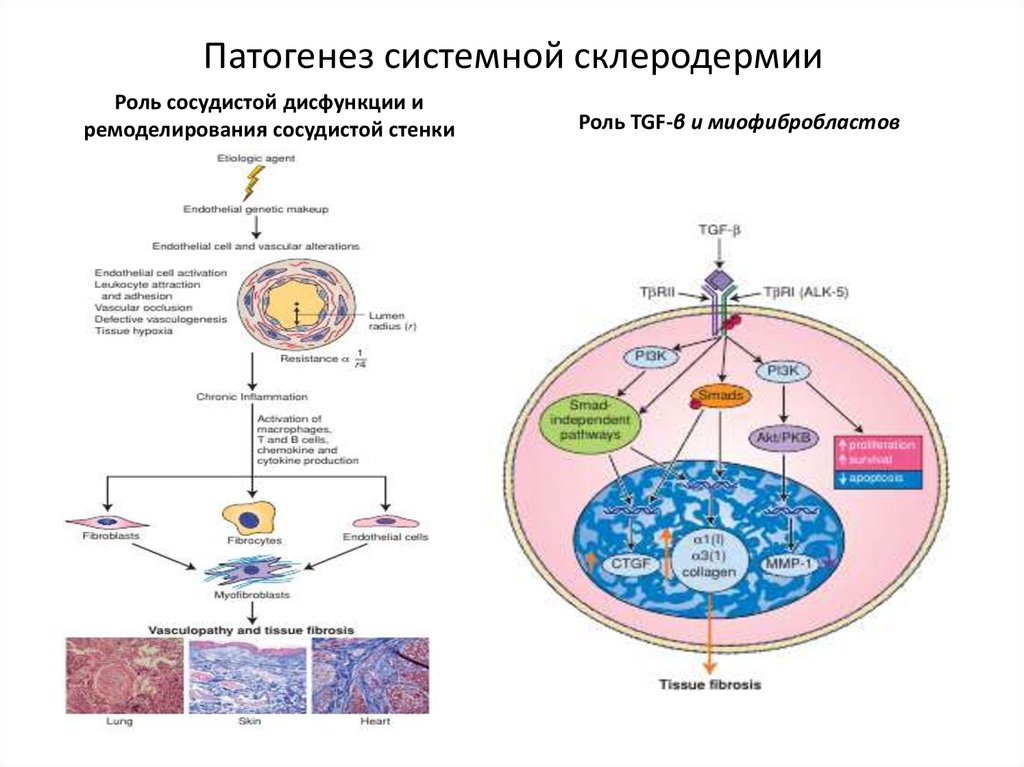
57. Патогенез системной склеродермии
Роль сосудистой дисфункции иремоделирования сосудистой стенки
Роль TGF-β и миофибробластов
58. Источники миофибробластов при системном склерозе
• 1. Фибробласты и сосудистые адвентициальные клетки.• 2. Хемокин-опосредованное привлечение предшественников
фибробластов из костного мозга.
• 3. Эпителиально-мезенхимальный переход (из эпителиальных клеток,
которые приобретают мезенхимальный фенотип с потерей Екадгеринов).
59. Патогенез системной склеродермии
1. Активация превращения наивных Т хелперов в CD4 TH2 под действием
неизвестного антигена.
2. Увеличение продукции провоспалительных цитокинов CD4 TH2 клетками.
3. Активация фибробластов и появление фиброгенных миофибробластов.
4. Увеличение продукции антител к топоизомеразе 1 ДНК и центромерами
(anti–Scl-70).
5. Под действием цитокинов и Т-клеток в мелких сосудах кожи снижается
продукция вазодилататоров (NO, PgI2) и увеличивается синтез
вазоконстриктора – эндотелина.
6. Повреждение эндотелиальных клеток сопровождается выходом PDGF и
TGF-β, которые играют ключевую роль в развитии системного фиброза в
различных органах и тканях.
60. Морфология системной склеродермии
61. Системные поражения при склеродермии
• 1. Феномен Рейно: преходящие последовательные изменения цветакожи
пальцев
кистей
(белый-синий-красный);
связаны
васкулитом/тромбозом и периваскулярным фиброзом.
• 2. Отек, утолщение кожи, симптом «кисета», кальцификаты.
• 3. Поражение ЖКТ: дисфагия, стриктуры и язвы пищевода, Барретта
пищевод; нарушения моторики желудка, тонкой кишки –
постпрандиальные дисэвакуаторные расстройства.
• 4.
Респираторные
изменения:
легочная
гипертензия
и
интерстициальный фиброз, ХЛС.
• 5. Почки: гиперпластические изменения артериол («шелуха лука»),
васкулит/тромбоз петель клубочка, фибриноидные изменения.
• 6. C—calcification, R—Raynaud phenomenon, E—Esophageal dysmotility,
S—sclerodactyly, T—telangiectasias (i.e., multiple punctate blood vessel
dilations).
62. Дерматомиозит
Некроз и регенерация мышечных волоконwww.neuro.wustl.edu/.../pathol/dermmyo.htm
www.phoenixneurology.com
63. Миозит-специфические антитела
1. Анти- Jo-1 part of ANTI SYNTHETASE Ab’sAntibodies to the antigen- Aminoacyl-tRNA
synthetase, in 20-50% of PM>>DM
2. ANTI SRP = anti signal recognition particle. In
5% of PM
3. ANTI Mi-2 in 10% of DM.
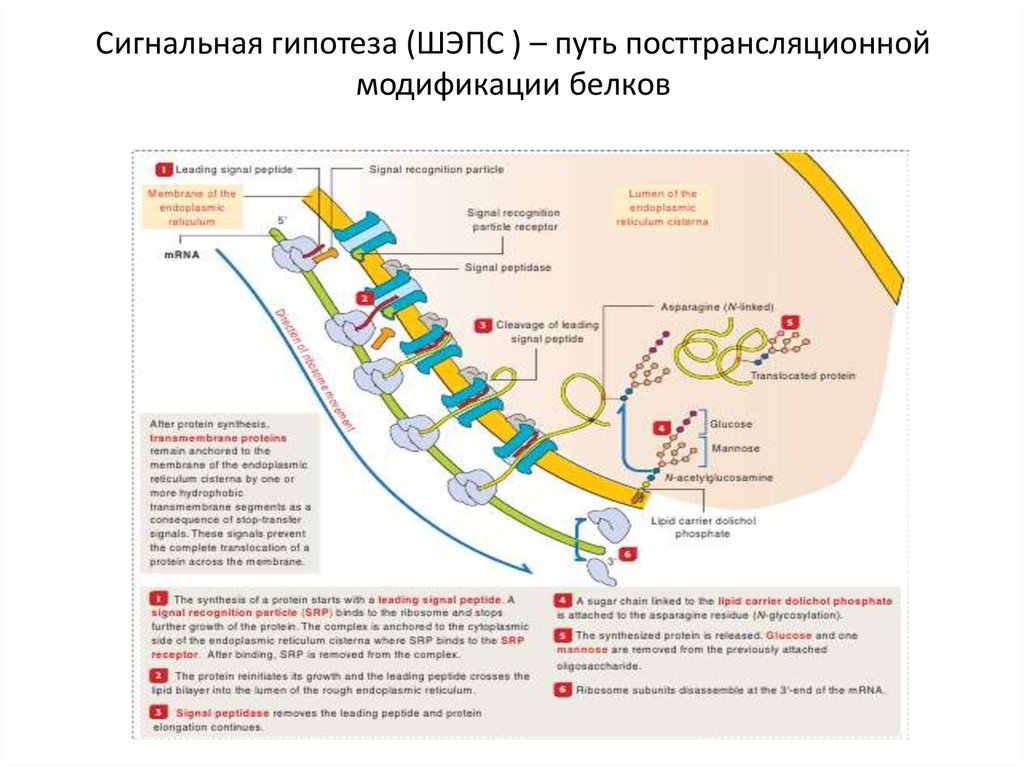
64. Сигнальная гипотеза (ШЭПС ) – путь посттрансляционной модификации белков
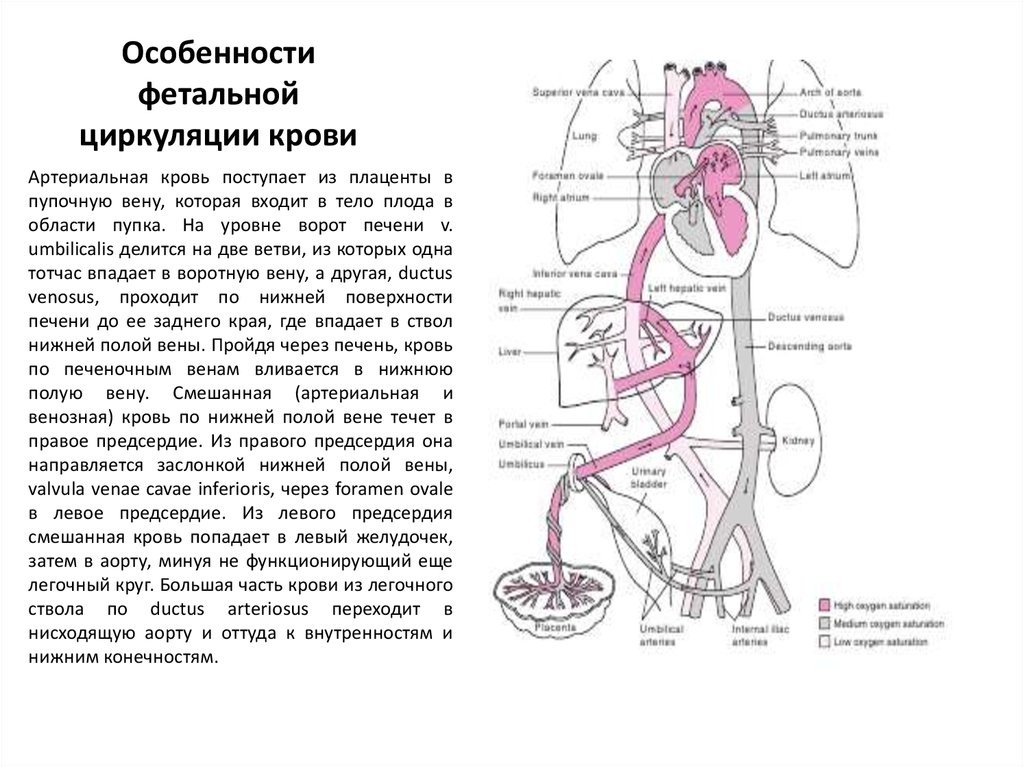
65. Особенности фетальной циркуляции крови
Артериальная кровь поступает из плаценты впупочную вену, которая входит в тело плода в
области пупка. На уровне ворот печени v.
umbilicalis делится на две ветви, из которых одна
тотчас впадает в воротную вену, а другая, ductus
venosus, проходит по нижней поверхности
печени до ее заднего края, где впадает в ствол
нижней полой вены. Пройдя через печень, кровь
по печеночным венам вливается в нижнюю
полую вену. Смешанная (артериальная и
венозная) кровь по нижней полой вене течет в
правое предсердие. Из правого предсердия она
направляется заслонкой нижней полой вены,
valvula venae cavae inferioris, через foramen ovale
в левое предсердие. Из левого предсердия
смешанная кровь попадает в левый желудочек,
затем в аорту, минуя не функционирующий еще
легочный круг. Большая часть крови из легочного
ствола по ductus arteriosus переходит в
нисходящую аорту и оттуда к внутренностям и
нижним конечностям.
66. Эмбриологические основы ВПС
67. Эмбриологические основы ВПС
68. Развитие аортико-пульмональной перегородки (АПП)
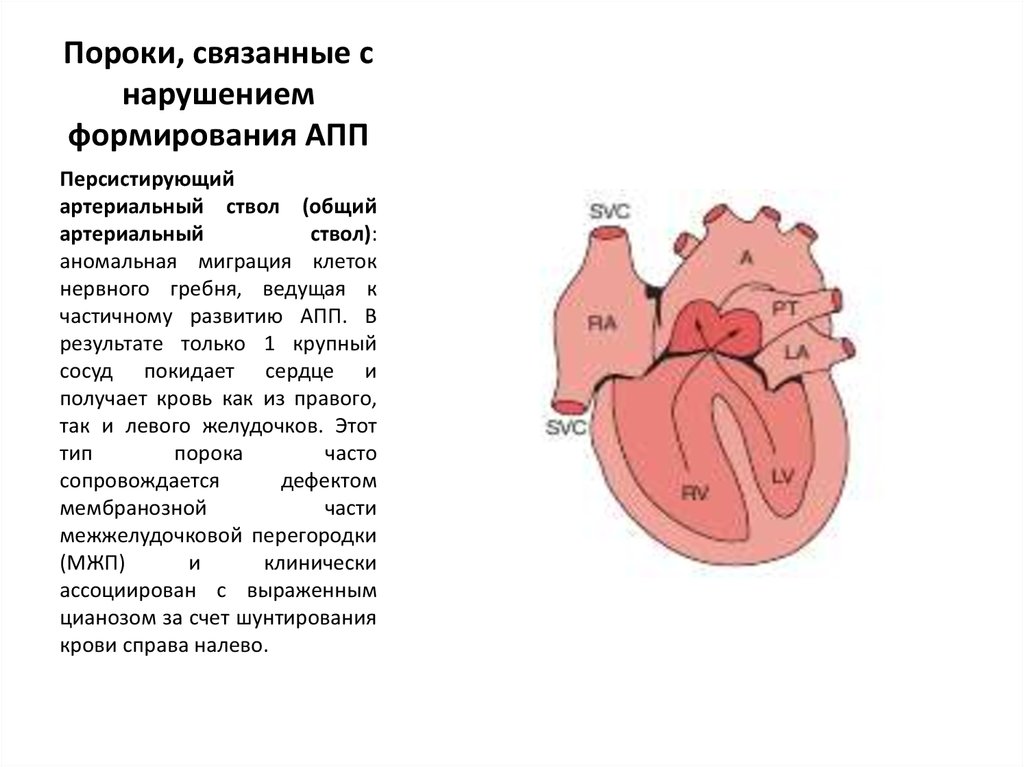
69. Пороки, связанные с нарушением формирования АПП
Персистирующийартериальный ствол (общий
артериальный
ствол):
аномальная миграция клеток
нервного гребня, ведущая к
частичному развитию АПП. В
результате только 1 крупный
сосуд покидает сердце и
получает кровь как из правого,
так и левого желудочков. Этот
тип
порока
часто
сопровождается
дефектом
мембранозной
части
межжелудочковой перегородки
(МЖП)
и
клинически
ассоциирован с выраженным
цианозом за счет шунтирования
крови справа налево.
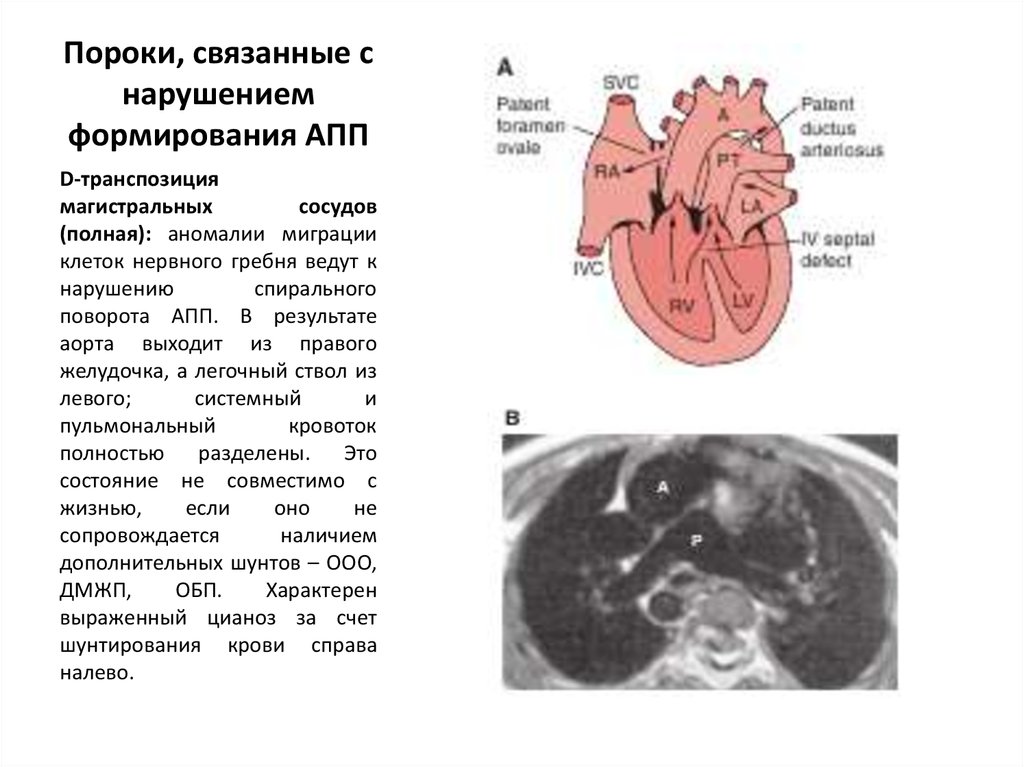
70. Пороки, связанные с нарушением формирования АПП
D-транспозициямагистральных
сосудов
(полная): аномалии миграции
клеток нервного гребня ведут к
нарушению
спирального
поворота АПП. В результате
аорта выходит из правого
желудочка, а легочный ствол из
левого;
системный
и
пульмональный
кровоток
полностью разделены. Это
состояние не совместимо с
жизнью,
если
оно
не
сопровождается
наличием
дополнительных шунтов – ООО,
ДМЖП,
ОБП.
Характерен
выраженный цианоз за счет
шунтирования крови справа
налево.
71. Пороки, связанные с нарушением формирования АПП
L-транспозиция магистральныхсосудов (корректированная):
происходит
инверсия
желудочков,
в
результате
которой анатомически правый
желудочек
оказывается
на
левой стороне и из него
выходит аорта, а анатомически
левый желудочек оказывается
на правой стороне и из него
выходит легочный ствол. Обе
девиации
–
инверсия
желудочков и вторичная по
отношению к ней транспозиция
сосудов
–
взаимно
перекрывают
друг
друга,
вследствие чего нарушений
гемодинамики не наблюдается.
72. Пороки, связанные с нарушением формирования АПП
Тетрада Фалло: аномальнаямиграция клеток нервного
гребня
веден
к
несимметричной спирализации
АПП. В результате аорта
приобретает больший диаметр,
чем легочный ствол. Тетрада
включает: стеноз легочного
ствола, гипертрофию правого
желудочка,
аномальное
расширение выходного отдела
аорты и ДМЖП. Клинически –
синий
тип
порока
с
шунтированием слева направо,
выраженность
симптомов
определяется степенью стеноза
легочного ствола.
73. Развитие межпредсердной перегородки (МПП)
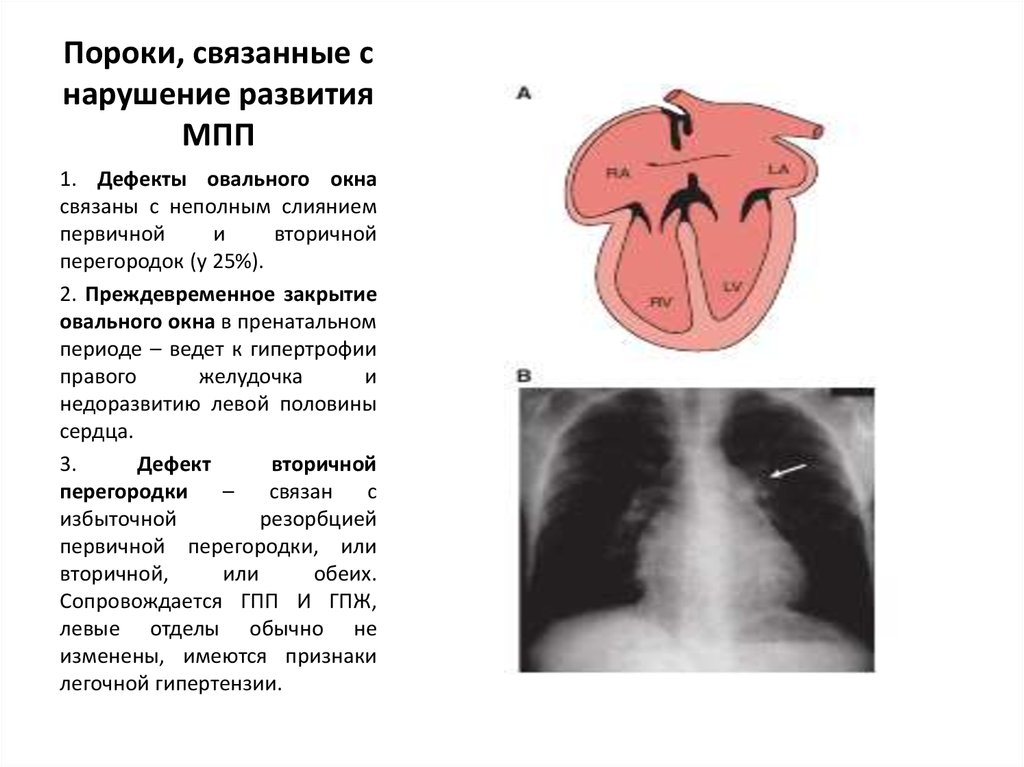
74. Пороки, связанные с нарушение развития МПП
1. Дефекты овального окнасвязаны с неполным слиянием
первичной
и
вторичной
перегородок (у 25%).
2. Преждевременное закрытие
овального окна в пренатальном
периоде – ведет к гипертрофии
правого
желудочка
и
недоразвитию левой половины
сердца.
3.
Дефект
вторичной
перегородки
–
связан
с
избыточной
резорбцией
первичной перегородки, или
вторичной,
или
обеих.
Сопровождается ГПП И ГПЖ,
левые отделы обычно не
изменены, имеются признаки
легочной гипертензии.
75. Пороки, связанные с нарушение развития МПП
Общее предсердие – cortriloculare biventriculare.
Ассоциировано с полным
недоразвитием
перегородок
–
как
первичной,
так
и
вторичной.
76. Развитие атриовентрикулярной перегородки (АВП)
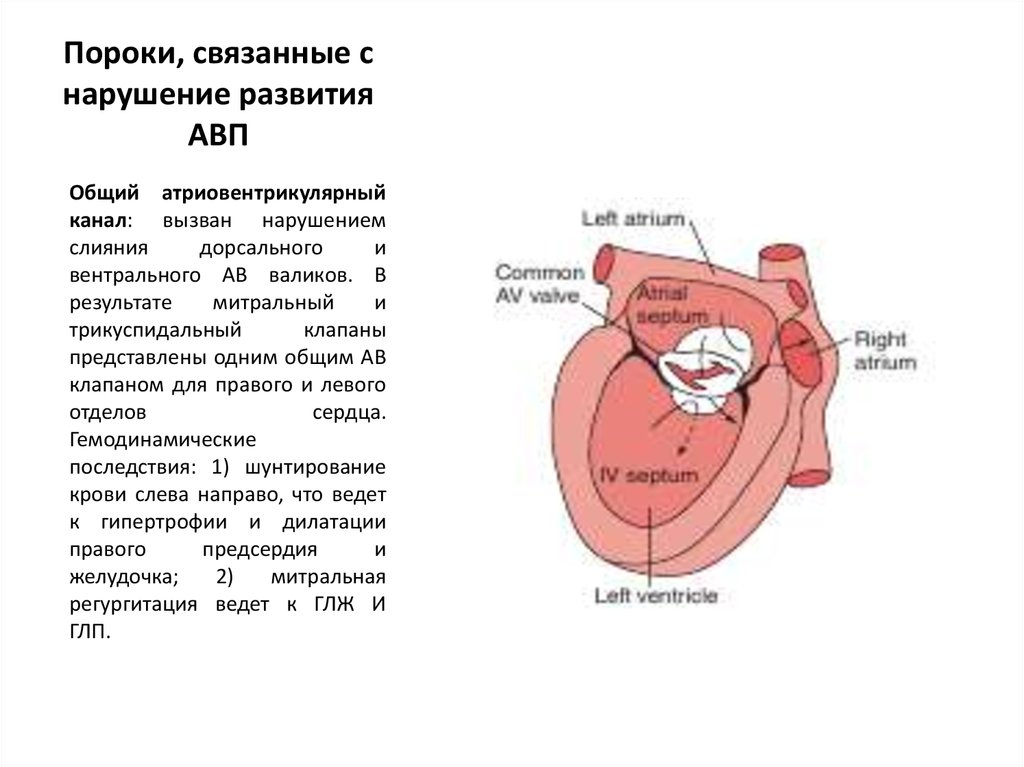
77. Пороки, связанные с нарушение развития АВП
Общий атриовентрикулярныйканал: вызван нарушением
слияния
дорсального
и
вентрального АВ валиков. В
результате
митральный
и
трикуспидальный
клапаны
представлены одним общим АВ
клапаном для правого и левого
отделов
сердца.
Гемодинамические
последствия: 1) шунтирование
крови слева направо, что ведет
к гипертрофии и дилатации
правого
предсердия
и
желудочка;
2)
митральная
регургитация ведет к ГЛЖ И
ГЛП.
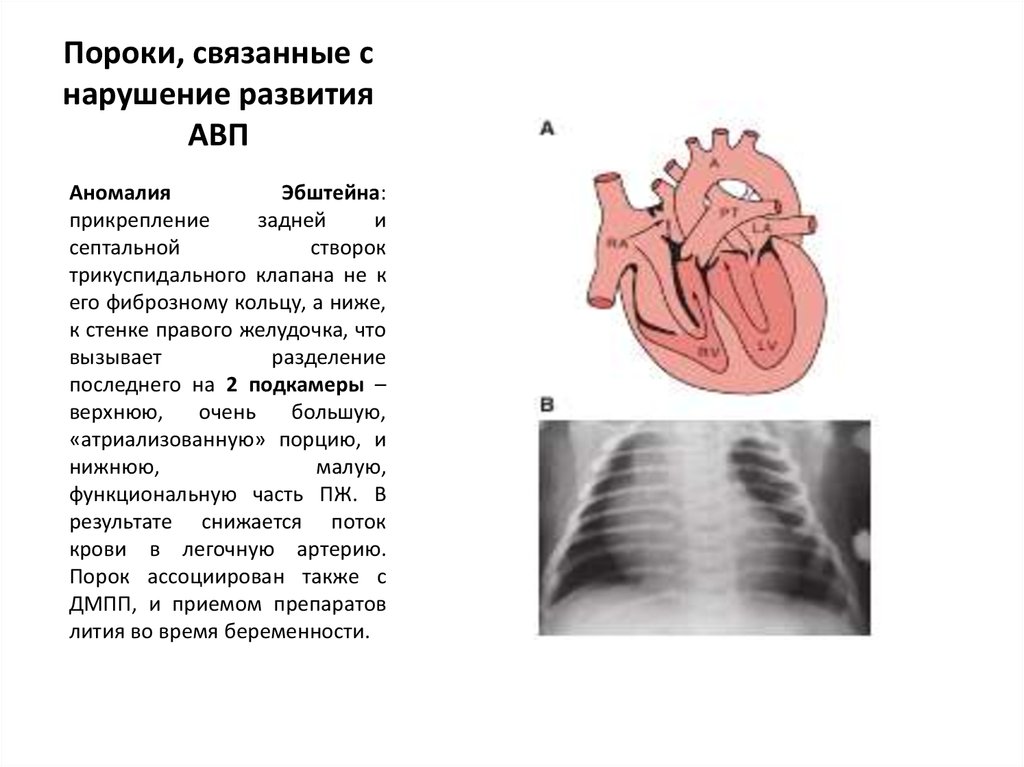
78. Пороки, связанные с нарушение развития АВП
АномалияЭбштейна:
прикрепление
задней
и
септальной
створок
трикуспидального клапана не к
его фиброзному кольцу, а ниже,
к стенке правого желудочка, что
вызывает
разделение
последнего на 2 подкамеры –
верхнюю,
очень
большую,
«атриализованную» порцию, и
нижнюю,
малую,
функциональную часть ПЖ. В
результате снижается поток
крови в легочную артерию.
Порок ассоциирован также с
ДМПП, и приемом препаратов
лития во время беременности.
79. Пороки, связанные с нарушение развития АВП
Дефект первичного окнаМПП:
связан
с
нарушением
слияния
АВП
с
первичной
межпредсердной
перегородкой.
Сочетается
также
с
дефектом митрального
клапана.
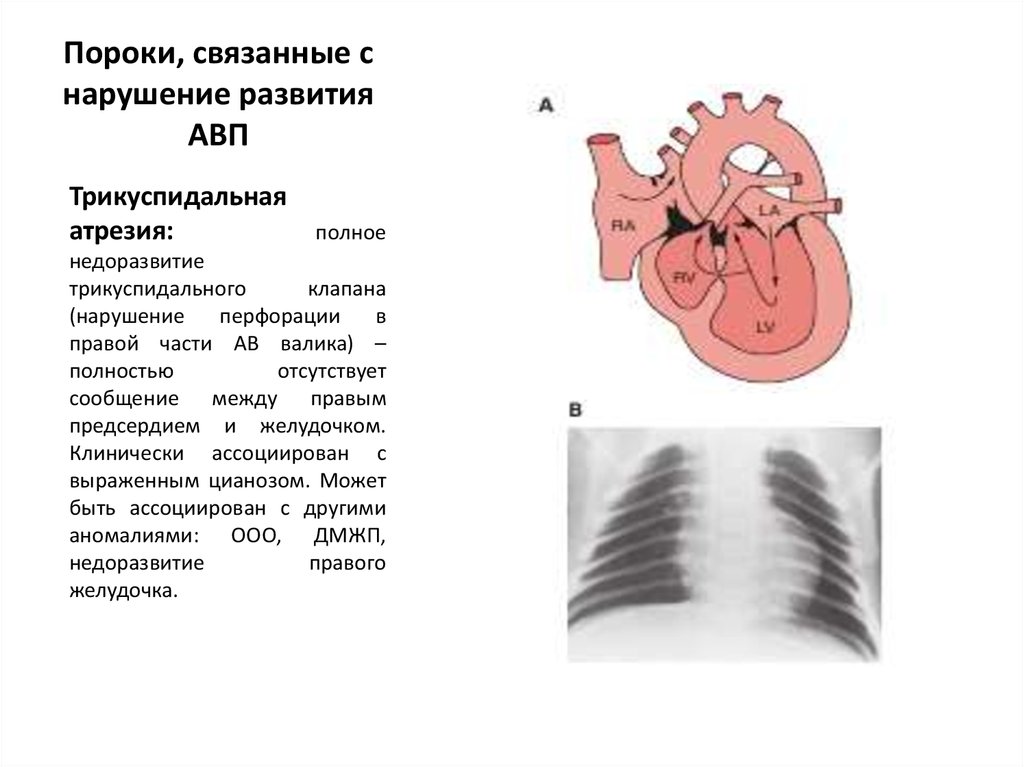
80. Пороки, связанные с нарушение развития АВП
Трикуспидальнаяатрезия:
полное
недоразвитие
трикуспидального
клапана
(нарушение
перфорации
в
правой части АВ валика) –
полностью
отсутствует
сообщение между правым
предсердием и желудочком.
Клинически ассоциирован с
выраженным цианозом. Может
быть ассоциирован с другими
аномалиями: ООО, ДМЖП,
недоразвитие
правого
желудочка.
81. Развитие межжелудочковой перегородки (МЖП)
a - правый бульбарный гребень, b - левый бульбарный гребень, с сливающиеся атриовентрикулярные валики82. Пороки, связанные с нарушение развития МЖП
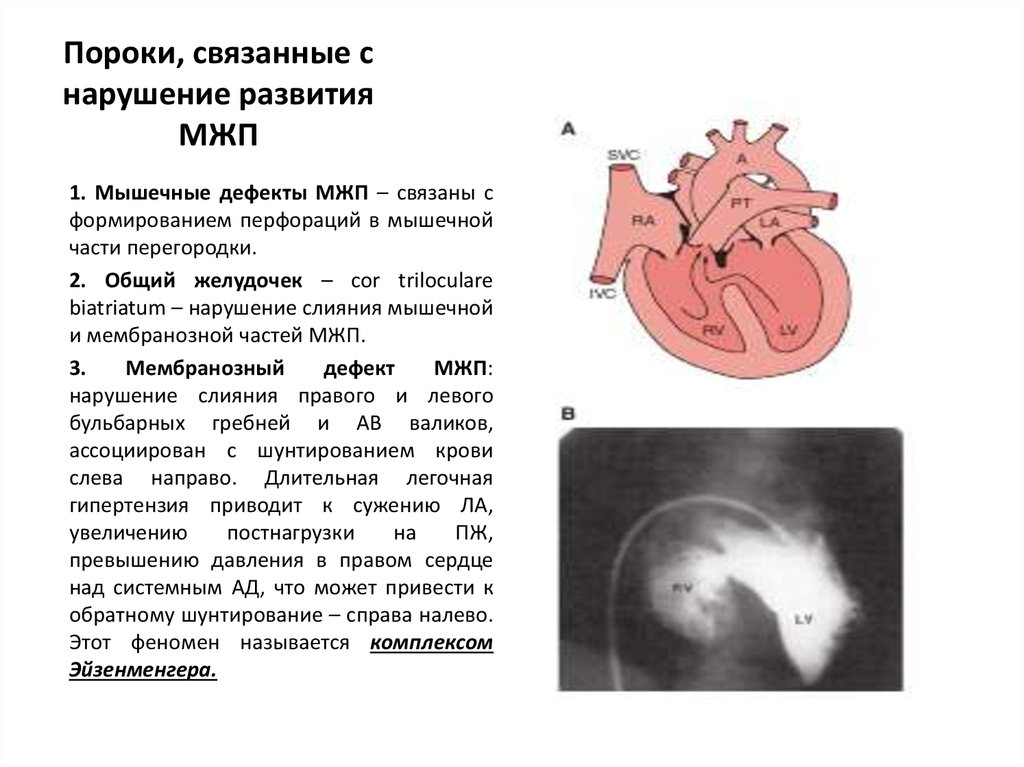
1. Мышечные дефекты МЖП – связаны сформированием перфораций в мышечной
части перегородки.
2. Общий желудочек – cor triloculare
biatriatum – нарушение слияния мышечной
и мембранозной частей МЖП.
3.
Мембранозный
дефект
МЖП:
нарушение слияния правого и левого
бульбарных гребней и АВ валиков,
ассоциирован с шунтированием крови
слева направо. Длительная легочная
гипертензия приводит к сужению ЛА,
увеличению
постнагрузки
на
ПЖ,
превышению давления в правом сердце
над системным АД, что может привести к
обратному шунтирование – справа налево.
Этот феномен называется комплексом
Эйзенменгера.
83. Некоторые пороки развития сосудов
1. Открытый артериальный (Боталлов) проток (ОБП) – между аортой и
легочным стволом, в норме его функциональное закрытие происходит в
течение нескольких часов после рождения за счет сокращения гладких мышц,
в последующем формируется ligamentum arteriosum. Поддержание открытым
реализуется во внутриутробной жизни за счет продукции простагландинов
трофобластом, а в случае нарушения его закрытия после рождения
применяют НПВС (напр., индометацин). Открытый артериальный проток
вызывает шунтирование крови слева направо, часто встречается у
недоношенных детей, рожденных от матерей, переболевших краснухой во
время беременности.
2. Постдуктальная коарктация аорты – резкое сужение просвета на
участке дистальнее артериального (Боталлова) протока и места выхода левой
подключичной артерии. Проявляется повышением АД в артериях верхней
половины тела и снижением его в артериях нижних конечностей, высоким
риском церебрального кровоизлияния и инфекционного эндокардита.
Предуктальная коарктация встречается очень редко.
84. Морфологические особенности приобретенных пороков сердца
• Виды пороков клапанов: стеноз отверстия –сужение за счет сращениястворок между собой; недостаточность- укорочение и неполное
закрытие створок; относительная недостаточность обусловлена
расширением фиброзного кольца без укорочения створок.
• Стеноз клапанов бывает по типу «диафрагмы» и «воронки». При
стенозе отверстия по типу диафрагмы происходит сращение одних
лишь створок, т.е. развиваются комиссуры. При стенозе отверстия по
типу воронки, срастаются створки клапанов, хорды, а иногда и
папиллярные мышцы.
• При стенозе митрального клапана возникает гипертрофия левого
предсердия и правого желудочка, а полость левого желудочка
уменьшается. При недостаточности двухстворчатого клапана,
гипертрофируются все отделы сердца. При пороках аортальных
клапанов сильно гипертрофируется левый желудочек.
85. Be smart!
У ребенка, родившегося в срок, выявлен выраженныйцианоз («синий» тип порока), аускультативно – сердечный
шум. На эхокардиограмме: дилатация выходного отдела
аорты, дефект межжелудочковой перегородки, гипертрофия
правого желудочка и стеноз легочного ствола.
В каком из следующих генов этот ребенок, скорее всего,
имеет унаследованную мутацию?
A. Тяжелых цепей β-миозина(β-MHC);
Б. Фибриллина 1 (FBN1);
В. KCNQ1;
Г. NOTCH2;
Д. Транстиретина (TTR).





























































 Медицина
Медицина








