Похожие презентации:
Сложные эфиры и жиры. Получение сложных эфиров реакцией этерификации. Сложные эфиры в природе, их значение
1.
Урок химииТема: Сложные эфиры и жиры. Получение сложных эфиров
реакцией этерификации. Сложные эфиры в природе, их
значение. Применение сложных эфиров на основе свойств.
Жиры как сложные эфиры. Классификация жиров. Химические
свойства жиров: гидролиз и гидрирование жидких жиров.
Применение жиров на основе свойств. Мыла.
Углеводы. Углеводы, их классификация: моносахариды
(глюкоза, фруктоза), дисахариды (сахароза), полисахариды
(крахмал и целлюлоза).
Глюкоза – вещество с двойственной функцией –
альдегидоспирт. Химические свойства глюкозы: окисление в
глюконовую кислоту, восстановление в сорбит, спиртовое
брожение. Применение глюкозы на основе свойств.
Значение углеводов в живой природе и жизни человека.
Понятие о реакциях поликонденсации и гидролиза на примере
взаимопревращений: глюкоза полисахарид.
1
2.
Сложный эфир- это продукт реакции взаимодействияспирта с кислородосодержащей кислотой, имеющий общую
формулу:
*Сложные эфиры, или эсте́ры (от др.-греч. αἰθήρ — «эфир») – это производные
кислот (как карбоновых, так и неорганических) с общей формулой СnH2nO2,
формально являющиеся продуктами замещения атомов водорода в гидроксилах
—OH кислотной функции на углеводородный остаток (алифатический,
алкенильный, ароматический или гетероароматический); рассматриваются также
как ацилпроизводные спиртов.
*о
*жирными углеводородами называются углеводороды с открытой цепью
2
*одн
алки
3.
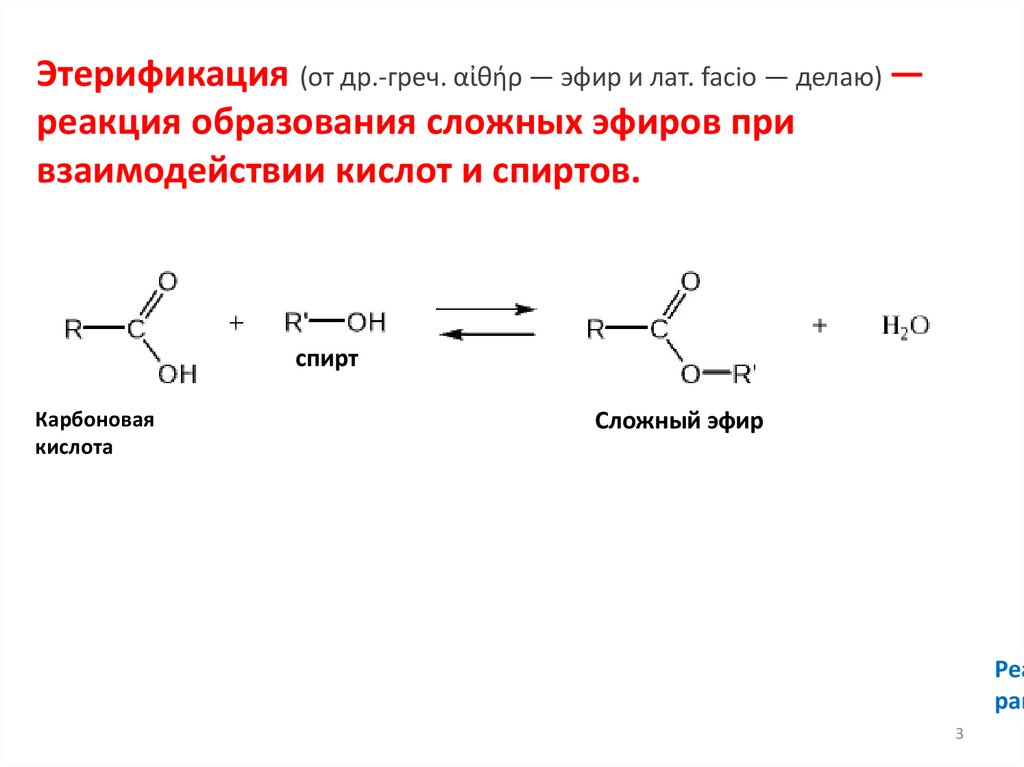
Этерификация (от др.-греч. αἰθήρ — эфир и лат. facio — делаю) —реакция образования сложных эфиров при
взаимодействии кислот и спиртов.
спирт
Карбоновая
кислота
Сложный эфир
Реа
рав
3
4.
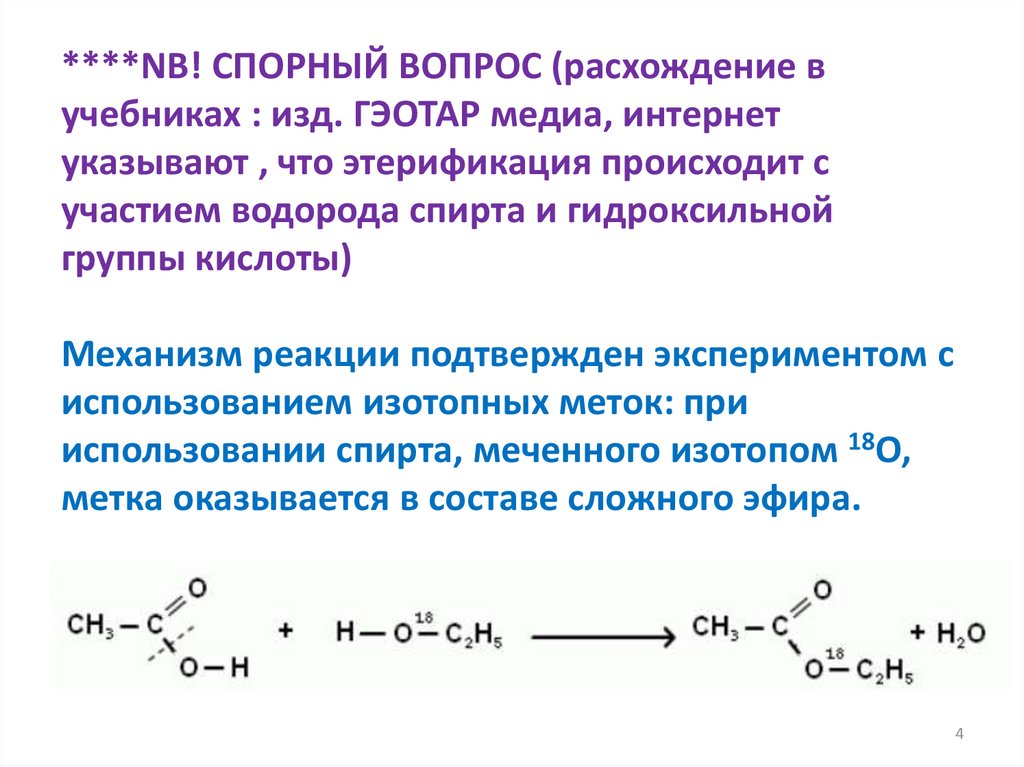
****NB! СПОРНЫЙ ВОПРОС (расхождение вучебниках : изд. ГЭОТАР медиа, интернет
указывают , что этерификация происходит с
участием водорода спирта и гидроксильной
группы кислоты)
Механизм реакции подтвержден экспериментом с
использованием изотопных меток: при
использовании спирта, меченного изотопом 18O,
метка оказывается в составе сложного эфира.
4
5.
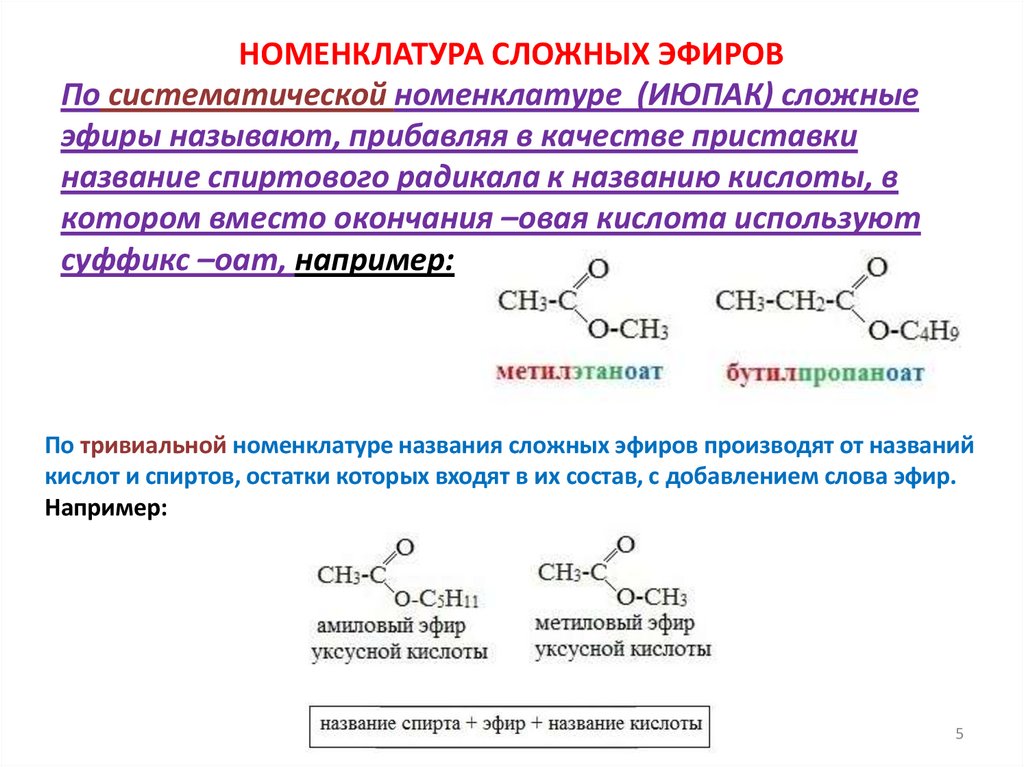
НОМЕНКЛАТУРА СЛОЖНЫХ ЭФИРОВПо систематической номенклатуре (ИЮПАК) сложные
эфиры называют, прибавляя в качестве приставки
название спиртового радикала к названию кислоты, в
котором вместо окончания –овая кислота используют
суффикс –оaт, например:
По тривиальной номенклатуре названия сложных эфиров производят от названий
кислот и спиртов, остатки которых входят в их состав, с добавлением слова эфир.
Например:
5
6.
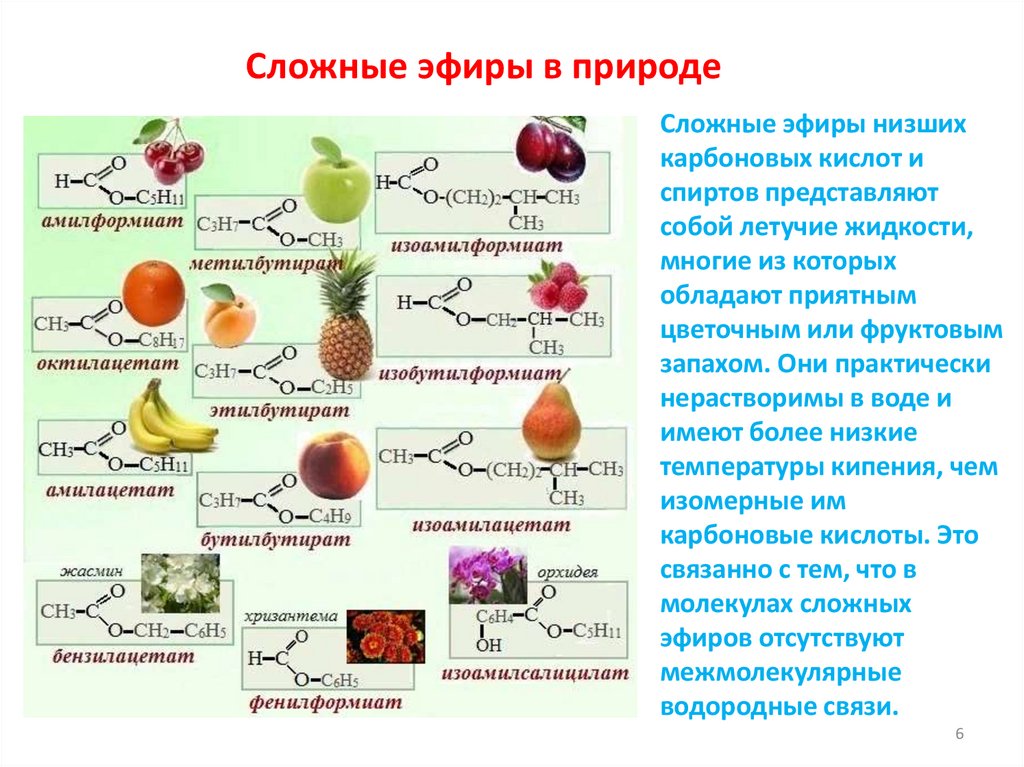
Сложные эфиры в природеСложные эфиры низших
карбоновых кислот и
спиртов представляют
собой летучие жидкости,
многие из которых
обладают приятным
цветочным или фруктовым
запахом. Они практически
нерастворимы в воде и
имеют более низкие
температуры кипения, чем
изомерные им
карбоновые кислоты. Это
связанно с тем, что в
молекулах сложных
эфиров отсутствуют
межмолекулярные
водородные связи.
6
7.
Воск — распространённая в растительном и животном мире смесь простыхлипидов (сложные эфиры высших жирных кислот и высших
высокомолекулярных спиртов). В состав молекул липидов, составляющих
воски (в отличие от жиров, имеющих сходное строение), не входит глицерин.
Воски обладают химической устойчивостью,
не подвержены окислению, водостойки,
имеют достаточную твердость и высокую
температуру плавления.
В косметике воски, чаще всего, выполняют роль
структурообразующих компонентов, влияющих на
плотность и термостойкость изделий. Отдельные виды
восков содержат биологически активные вещества, что
усиливает их полезное воздействие на кожу.
7
8.
*Воски растительного происхожденияРастения обладают способностью продуцировать восковидные вещества. Воск
создаёт защитную плёнку и покрывает ей различные части растений: стебли, листья,
цветы, плоды. Это один из видов защиты растений от неблагоприятных факторов
внешней среды, например, болезнетворных бактерий и вирусов.
Состав
Растительный воски, как и воски животные, состоят, прежде всего, из эфиров
одноатомных жирных спиртов и жирных кислот. Так же в их состав входят свободные
жирные спирты и жирные кислоты. Из жирных кислот больше всего растительные
воски содержит пальмитиновой кислоты. В меньшем количестве найдены
стеариновая, олеиновая и миристиновая.
Почти всегда растительный воск содержит небольшие количества красящих, пахучих
и смолистых веществ.
Примеры растительных восков
Карнаубский воск, Пальмовый воск , Японский воск, Воск жожоба, Воск розы
Состоят на 80% из сложных эфиров мирицилового спирта и церотовой кислоты.
Содержат также лактоны, жирные кислоты, смолистые вещества. Используются в
губной помаде, туши для ресниц, румянах, жидкой пудре, шариковых дезодорантах
как структурообразующий компонент, повышающий их твердость и температуру
плавления. “Запирают” влагу в коже, придают вязкую приятную консистенцию
косметическим средствам. Проявляют легкое бактерицидное и
противовоспалительное действие. Используются в составе губных помад и других
декоративных изделий.
8
9.
Животные и растительные воски имеют в своем составе сложные эфирыПчелиный воск наиболее известный из этого вида восков. Он содержит сложный
эфир пальмитиновой кислоты и мирицилового спирта (мирицилпальмитат,
пальмитиномирициловый эфир):
CH3(CH2)14–CO–O–(CH2)29CH3
Миристилпальмитат, локализованный в углублениях костей черепа кашалота,
является проводником звуков при эхолокации.
Шерстяной (шерстный) воск – ланолин – обильно покрывает шерсть животных.
Спермацет содержится в костных черепных углублениях некоторых видов китов,
особенно кашалотов. На 90% состоит из пальмитиноцетилового эфира.
К воскам относятся кожное сало и ушная сера.
Воск бактерий покрывает поверхность кислотоупорных бактерий, например,
туберкулезных, обеспечивая их устойчивость к внешним воздействиям.
Из пчелиного воска пчелы строят соты, шерстяной (ланолин) предохраняет шерсть
и кожу животных от влаги, засорения и высыхания.
9
10.
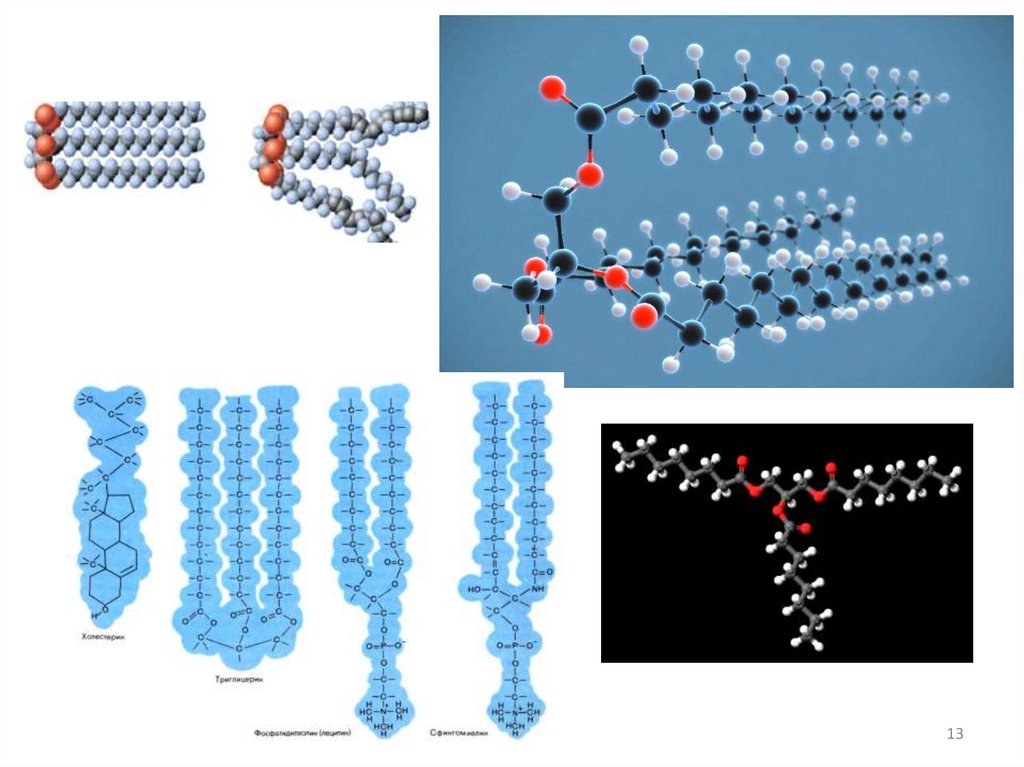
Жиры как сложные эфирыЖиры, также триглицери́ды, триацилглицериды (сокр. ТАГ)
— органические вещества, продукты этерификации
карбоновых кислот и трёхатомного спирта глицерина.
В живых организмах выполняют, прежде всего, структурную и
энергетическую функции: они являются основным компонентом
клеточной мембраны, а в жировых клетках сохраняется энергетический
запас организма.
Состав жиров определили французские ученые М. Шеврель и М. Бертло. В 1811
году М. Шеврель установил, что при нагревании смеси жира с водой в щелочной
среде образуются глицерин и карбоновые кислоты (стеариновая и олеиновая). В
1854 году химик М. Бертло осуществил обратную реакцию и впервые
синтезировал жир, нагревая смесь глицерина и карбоновых кислот.
10
11.
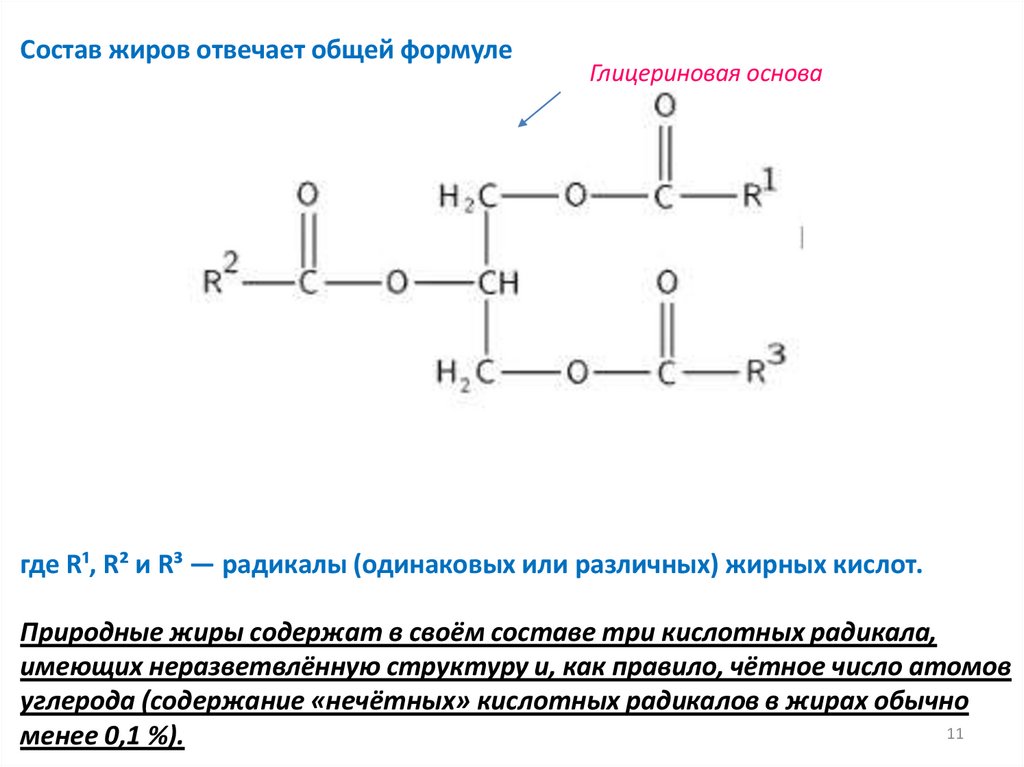
Состав жиров отвечает общей формулеГлицериновая основа
где R¹, R² и R³ — радикалы (одинаковых или различных) жирных кислот.
Природные жиры содержат в своём составе три кислотных радикала,
имеющих неразветвлённую структуру и, как правило, чётное число атомов
углерода (содержание «нечётных» кислотных радикалов в жирах обычно
11
менее 0,1 %).
12.
Природные жиры чаще всего содержат следующие жирныекислоты:
Насыщенные/Алкановые кислоты: стеариновая (C17H35COOH),
маргариновая (C16H33COOH), пальмитиновая (C15H31COOH),
капроновая (C5H11COOH),
масляная (C3H7COOH)
Ненасыщенные:
Алкеновые кислоты: пальмитолеиновая (C15H29COOH, 1
двойная связь),
олеиновая (C17H33COOH, 1 двойная связь)
Алкадиеновые кислоты: линолевая (C17H31COOH, 2 двойные
связи)
Алкатриеновые кислоты: линоленовая (C17H29COOH, 3 двойные
связи)
арахидоновая (C19H31COOH, 4 двойные связи, реже
встречается)
В состав некоторых жиров входят остатки и насыщенных, и
ненасыщенных карбоновых кислот.
12
13.
1314.
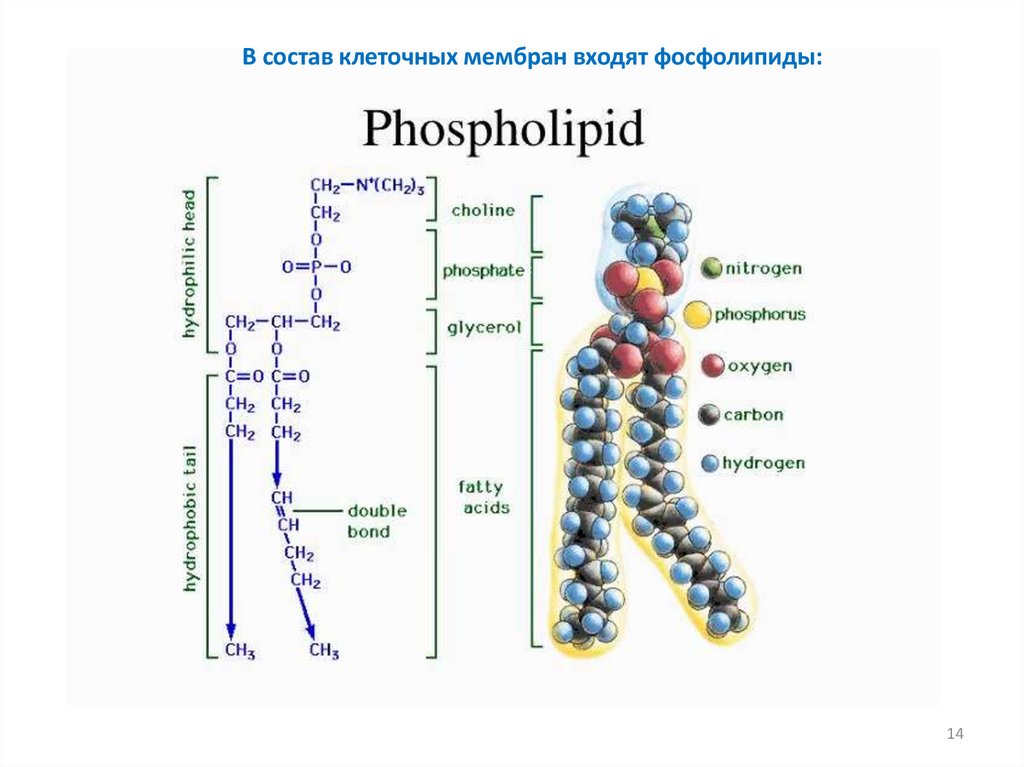
В состав клеточных мембран входят фосфолипиды:14
15.
В основе классификации жиров лежит несколько признаков:1. По происхождению
-животные (наземных животных, птиц, морских животных и рыб)
-растительные (из семян и мякоти плодов)
2. По агрегатному состоянию
-жидкие (подсолнечное, соевое и др.)
-твердые (бараний, говяжий, кокосовое масло и др.)
-полужидкие (свиной жир)
3. По химическому строению
-предельные (остатки насыщенных высших карбоновых
кислот)
-непредельные (остатки ненасыщенных высших карбоновых
кислот)
15
16.
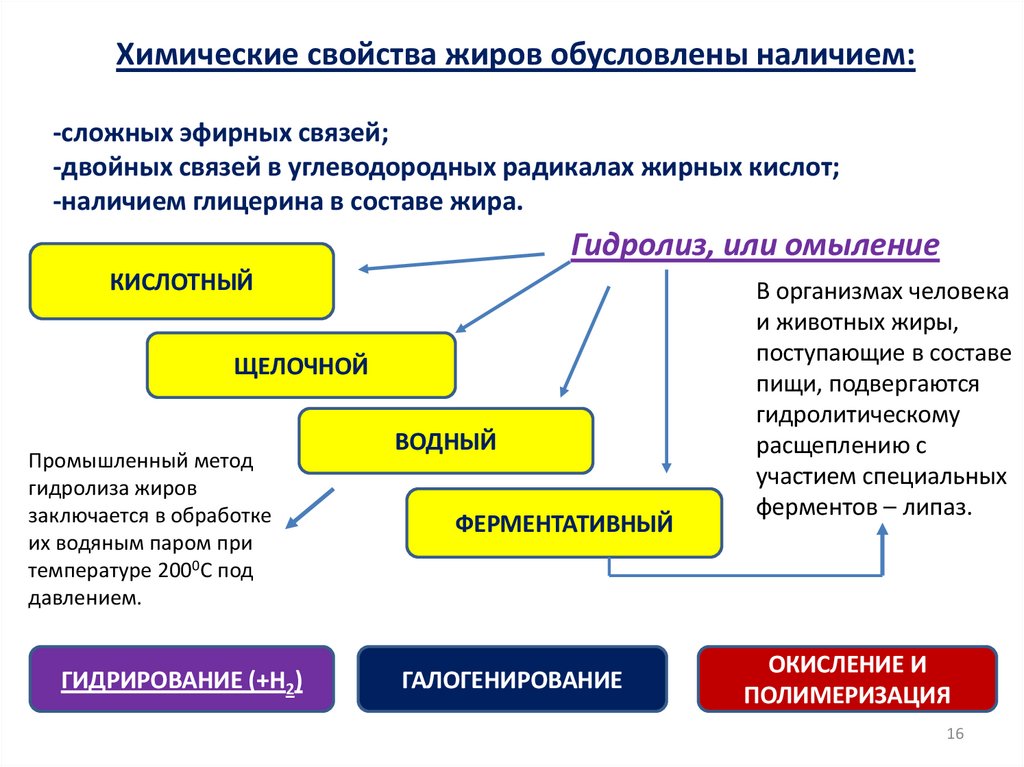
Химические свойства жиров обусловлены наличием:-сложных эфирных связей;
-двойных связей в углеводородных радикалах жирных кислот;
-наличием глицерина в составе жира.
Гидролиз, или омыление
КИСЛОТНЫЙ
ЩЕЛОЧНОЙ
Промышленный метод
гидролиза жиров
заключается в обработке
их водяным паром при
температуре 2000С под
давлением.
ГИДРИРОВАНИЕ (+Н2)
ВОДНЫЙ
ФЕРМЕНТАТИВНЫЙ
ГАЛОГЕНИРОВАНИЕ
В организмах человека
и животных жиры,
поступающие в составе
пищи, подвергаются
гидролитическому
расщеплению с
участием специальных
ферментов – липаз.
ОКИСЛЕНИЕ И
ПОЛИМЕРИЗАЦИЯ
16
17.
Жирам как сложным эфирам свойственна обратимая реакциягидролиза, катализируемая минеральными кислотами:
Щелочной гидролиз (реакция Шевреля)
При участии щелочей гидролиз жиров происходит необратимо — щелочи
превращают образующиеся кислоты в соли и тем самым устраняют возможность
взаимодействия кислот с глицерином. Продуктами в этом случае являются мыла соли высших карбоновых кислот и щелочных металлов:
17
18.
***Мы́ло — твёрдый или, реже, жидкий продукт, содержащийповерхностно-активные вещества, в соединении с водой,
используемый как косметическое и моющее средство.
Основными компонентами мыла являются растворимые соли
предельных (насыщенных) жирных кислот, например стеарат
натрия. Иногда в мыло добавляют различные масла и глицерин
для придания определённой консистенции, цвета, густоты.
.
Жир (тристеарат),
или триглицерид
стеариновой кислоты
* Натриевое мыло- твердое, калиевое- жидкое
18
19.
Синтетические моющие средства – натриевые соли синтетических кислот(сульфокислот — RSO3H), сложных эфиров высших спиртов и серной
кислоты — алкилсульфаты — ROSO2OН).
Сырье: на основе растительных жиров или нефти. Например, лаурилсульфат
натрия. Международный синоним — Sodium Laurylsulfate.
CH3-(CH2)10-CH2-(OCH2CH2)n-O-SO3Na+
Получение Синтетеческих Моющих
средств: из додеканола
Проблема Синтетических Моющих Средств: чистота ингредиентов ( при
производстве ПАВ из нефти) и промышленных примесей.
19
20.
Жидкие жиры превращают в твердые путем реакции гидрогенизации(каталитического гидрирования). При этом водород присоединяется по
двойной связи, содержащейся в углеводородном радикале молекул масел:
Продукт гидрогенизации масел — твердый жир (искусственное сало, саломас – сало
из масла). Маргарин - пищевой жир, состоит из смеси гидрогенизированных масел
(подсолнечного, кукурузного, хлопкого и др.), животных жиров, молока и вкусовых
добавок (соли, сахара, витаминов и др.).
В условиях процесса гидрогенизации масел (высокая температура, металлический
катализатор) происходит изомеризация части кислотных остатков, содержащих циссвязи С=С, в более устойчивые транс-изомеры. Повышенное содержание в
маргарине (особенно, в дешевых сортах) остатков транс-ненасыщенных кислот
увеличивает опасность атеросклероза, сердечно-сосудистых и других заболеваний.20
21.
Присоединение галогенов жидкими жирамиСвежие растительные масла обесцвечивают бромную и
йодную воду:
21
22.
Реакции окисления и полимеризации (для жидких ненасыщенных жиров)Жиры, содержащие остатки ненасыщенных кислот, под действием
кислорода воздуха окисляются и полимеризуются.
При длительном хранении жиры портятся (прогоркают). Под действием воздуха,
света и микроорганизмов происходит частичный гидролиз жиров с образованием
свободных жирных кислот и продуктов их превращения, обычно имеющих
неприятный запах и вкус.
Многие продукты окисления жиров являются токсичными для организма.
Установлено, что токсичность окисленных жиров обусловлена высокой
химической активностью продуктов их окисления, И в первую очередь
свободными радикалами, перекисями, карбонильными соединениями.
Гидроперекиси легко усваиваются организмом. В опытах на животных было
установлено, что вскоре после всасывания гидроперекиси обнаруживаются в
печени и в жировой ткани. Наиболее токсичной является гидроперекись
линолевой кислоты. Воздействие на организм продуктов окисления
губительно: они задерживают развитие растущего организма, могут
способствовать образованию злокачественных опухолей.
22
Срок
годн
23.
УглеводыУглеводы — органические вещества, содержащие
карбонильную группу и несколько гидроксильных групп.
Дословно: «гидраты углерода». Название было предложено К. Шмидтом в
1844 году. Появление такого названия связано с тем, что первые из
известных науке углеводов описывались общей формулой Cx(H2O)y,
формально являясь соединениями углерода и воды.
Классификация углеводов
Глюкоза
Фруктоза
Рибоза
Сахароза
Мальтоза
Лактоза
Крахмал
Гликоген
Целлюлоза
23
24.
Названиямоносахаридов строят в соответствии с их
классификацией с окончанием “оза” : альдопентоза,
кетогексоза и т. д.
Наиболее часто встречающиеся в природе моносахариды имеют тривиальные
названия, например, альдопентозы - рибоза, ксилоза, арабиноза, дезоксирибоза,;
альдогексозы - глюкоза, манноза; кетогексоза – фруктоза.
По номенклатуре ИЮПАК :
2,3,4,5 – тетрогидроксипентаналь (рибоза);
1,3,4,5,6-пентагидроксигексан-2-он (фруктоза) ;
2,3,4,5,6-пентагидроксигексаналь -(глюкоза )и т.д.
24
25.
Моносахариды представляют собой производныемногоатомных спиртов, содержащие карбонильную
группу — альдегидную или кетонную.
По количеству атомов углерода в цепи моносахариды подразделяют на: низшие
(диозы, триозы, тетрозы), средние (пентозы, гексозы) и высшие (гептозы, октозы и
нонозы).Природные моносахариды с углеродной цепью, содержащей более девяти
атомов углерода, не обнаружены.
Образование циклических форм
связано со способностью углеродной
цепи принимать выгодную
клешневидную конформацию и с
дальнейшим взаимодействием
внутри одной молекулы
карбонильной группы с
гидроксильной группой. Это
взаимодействие приводит к
образованию циклического
полуацеталя. Устойчивыми являются
5 — и 6 -членные циклы.
25
26.
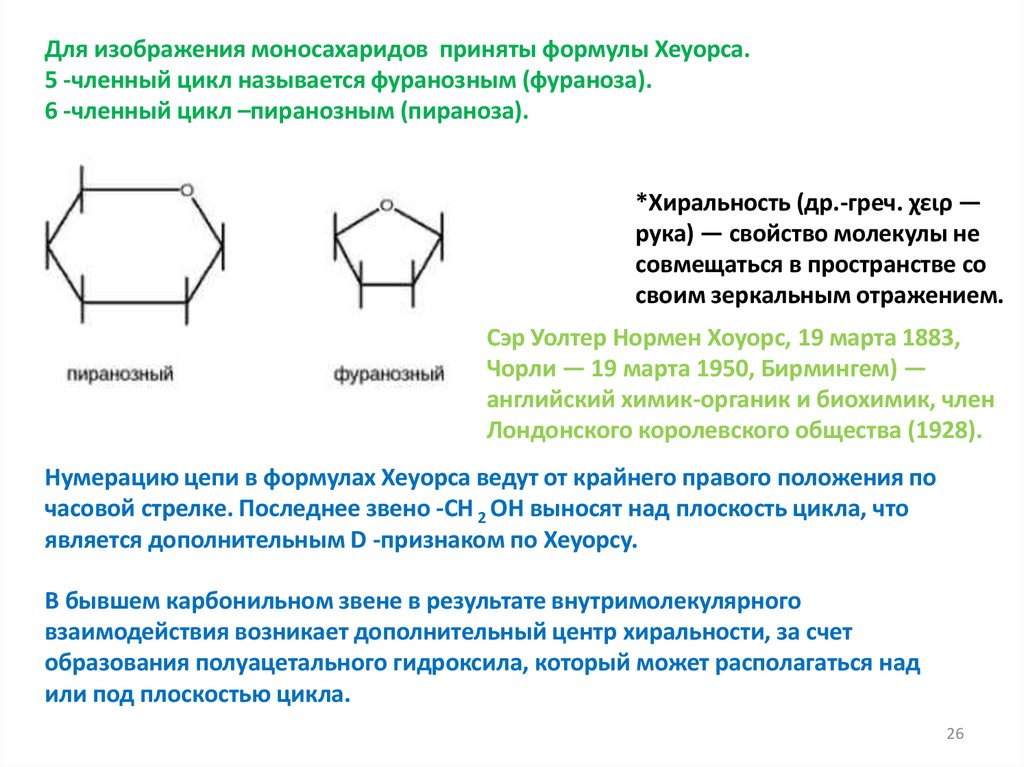
Для изображения моносахаридов приняты формулы Хеуорса.5 -членный цикл называется фуранозным (фураноза).
6 -членный цикл –пиранозным (пираноза).
*Хиральность (др.-греч. χειρ —
рука) — свойство молекулы не
совмещаться в пространстве со
своим зеркальным отражением.
Сэр Уолтер Нормен Хоуорс, 19 марта 1883,
Чорли — 19 марта 1950, Бирмингем) —
английский химик-органик и биохимик, член
Лондонского королевского общества (1928).
Нумерацию цепи в формулах Хеуорса ведут от крайнего правого положения по
часовой стрелке. Последнее звено -СН 2 ОН выносят над плоскость цикла, что
является дополнительным D -признаком по Хеуорсу.
В бывшем карбонильном звене в результате внутримолекулярного
взаимодействия возникает дополнительный центр хиральности, за счет
образования полуацетального гидроксила, который может располагаться над
или под плоскостью цикла.
26
27.
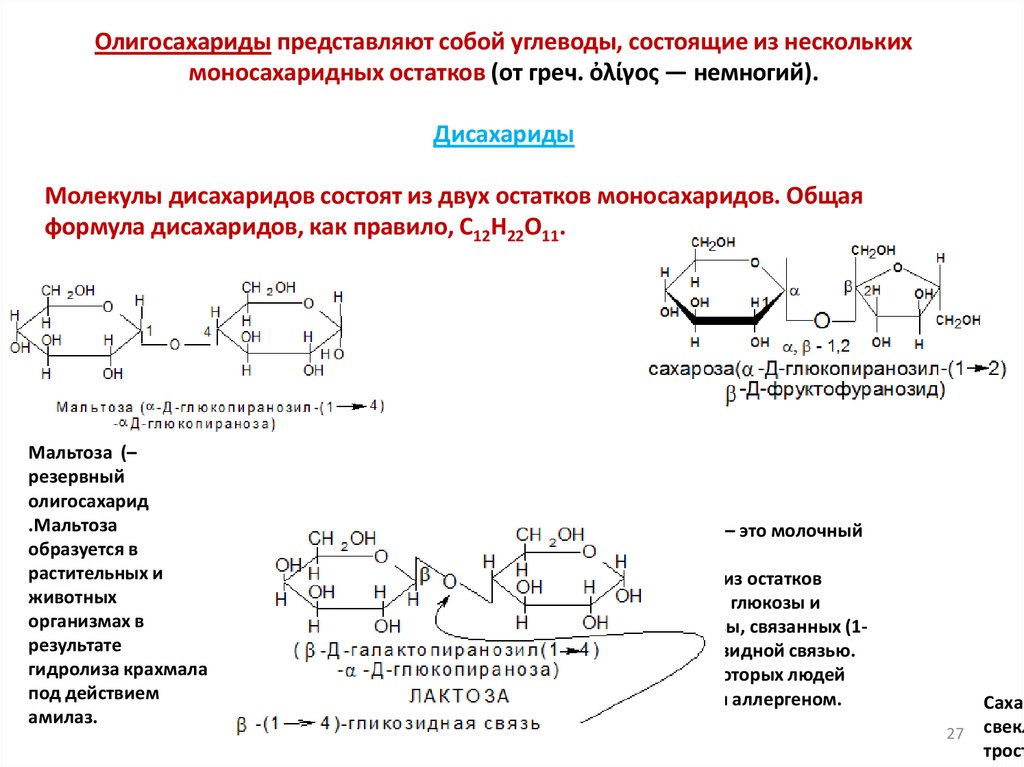
Олигосахариды представляют собой углеводы, состоящие из несколькихмоносахаридных остатков (от греч. ὀλίγος — немногий).
Дисахариды
Молекулы дисахаридов состоят из двух остатков моносахаридов. Общая
формула дисахаридов, как правило, C12H22O11.
Мальтоза (–
резервный
олигосахарид
.Мальтоза
образуется в
растительных и
животных
организмах в
результате
гидролиза крахмала
под действием
амилаз.
Лактоза – это молочный
сахар.
Состоит из остатков
молекул глюкозы и
галактозы, связанных (14) гликозидной связью.
Для некоторых людей
является аллергеном.
Сахар
27 свекл
трост
28.
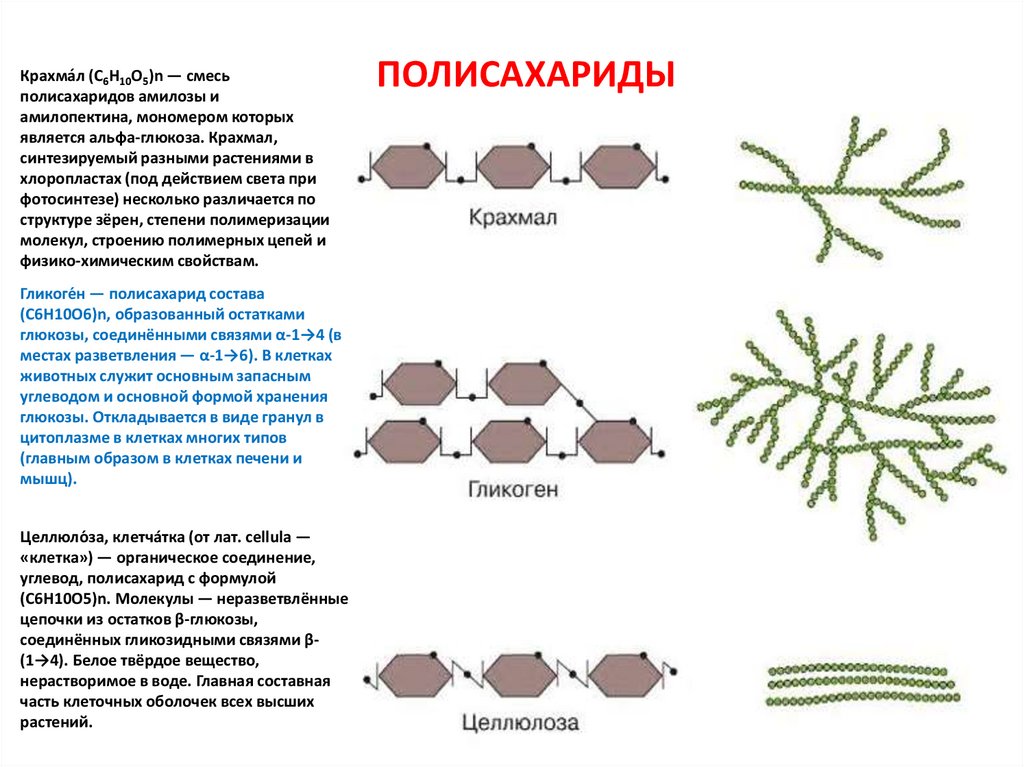
Крахма́л (C6H10O5)n — смесьполисахаридов амилозы и
амилопектина, мономером которых
является альфа-глюкоза. Крахмал,
синтезируемый разными растениями в
хлоропластах (под действием света при
фотосинтезе) несколько различается по
структуре зёрен, степени полимеризации
молекул, строению полимерных цепей и
физико-химическим свойствам.
ПОЛИСАХАРИДЫ
Гликоге́н — полисахарид состава
(C6H10O6)n, образованный остатками
глюкозы, соединёнными связями α-1→4 (в
местах разветвления — α-1→6). В клетках
животных служит основным запасным
углеводом и основной формой хранения
глюкозы. Откладывается в виде гранул в
цитоплазме в клетках многих типов
(главным образом в клетках печени и
мышц).
Целлюло́за, клетчáтка (от лат. cellula —
«клетка») — органическое соединение,
углевод, полисахарид с формулой
(C6H10O5)n. Молекулы — неразветвлённые
цепочки из остатков β-глюкозы,
соединённых гликозидными связями β(1→4). Белое твёрдое вещество,
нерастворимое в воде. Главная составная
часть клеточных оболочек всех высших
растений.
28
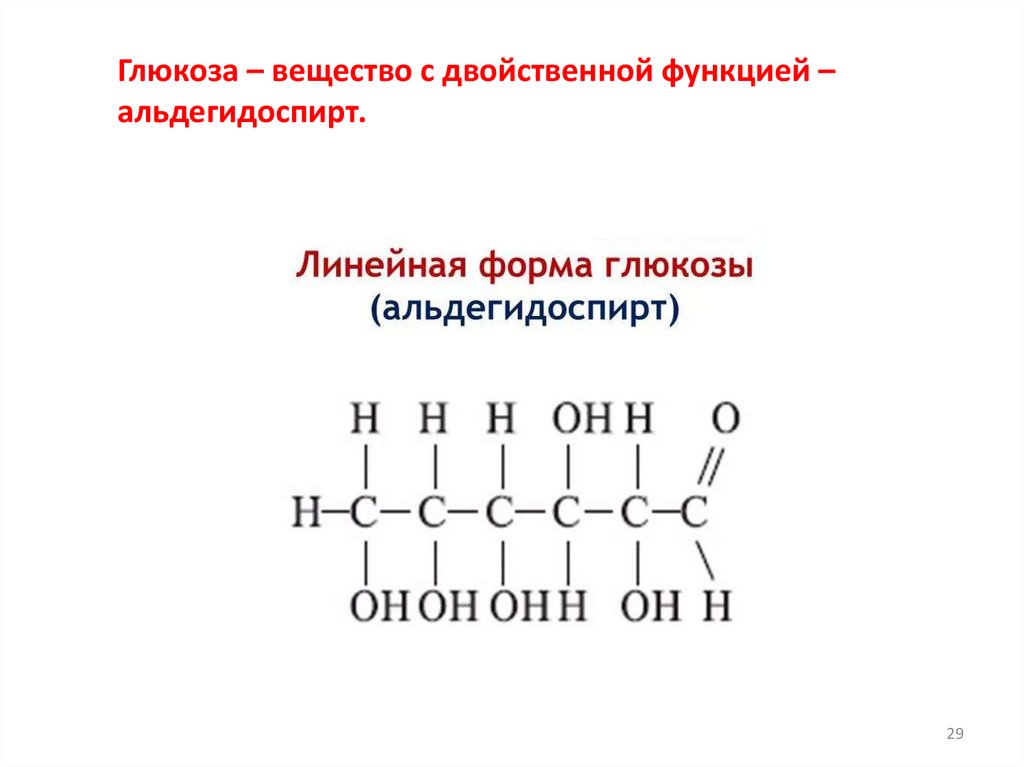
29.
Глюкоза – вещество с двойственной функцией –альдегидоспирт.
29
30.
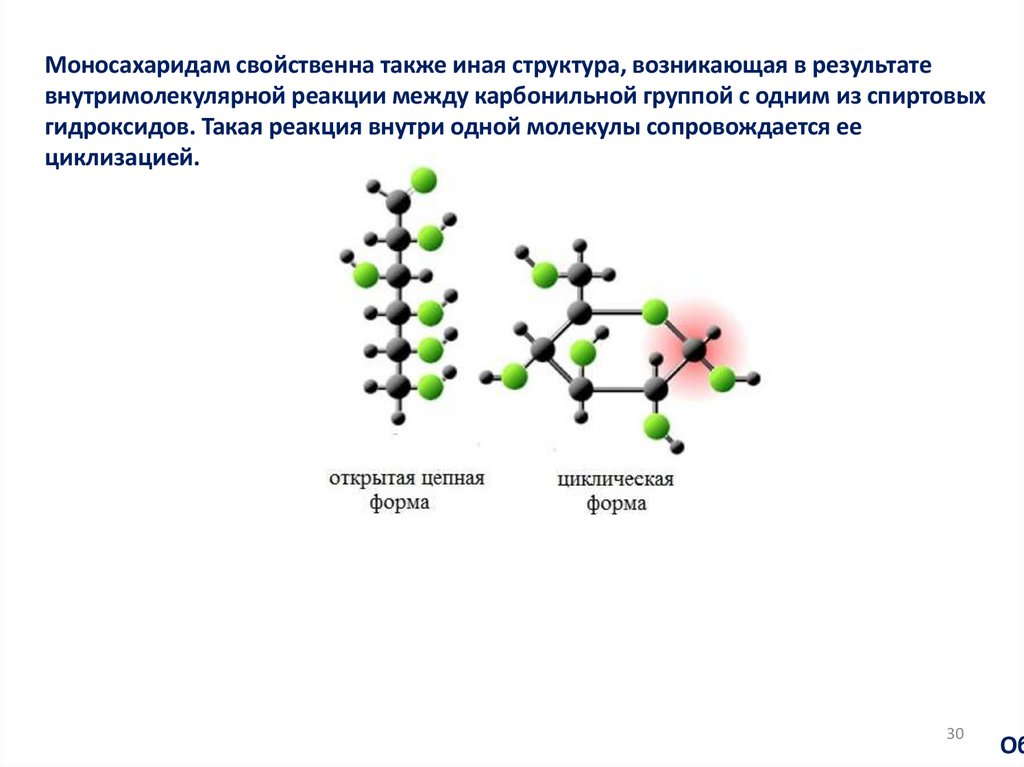
Моносахаридам свойственна также иная структура, возникающая в результатевнутримолекулярной реакции между карбонильной группой с одним из спиртовых
гидроксидов. Такая реакция внутри одной молекулы сопровождается ее
циклизацией.
30
Об
31.
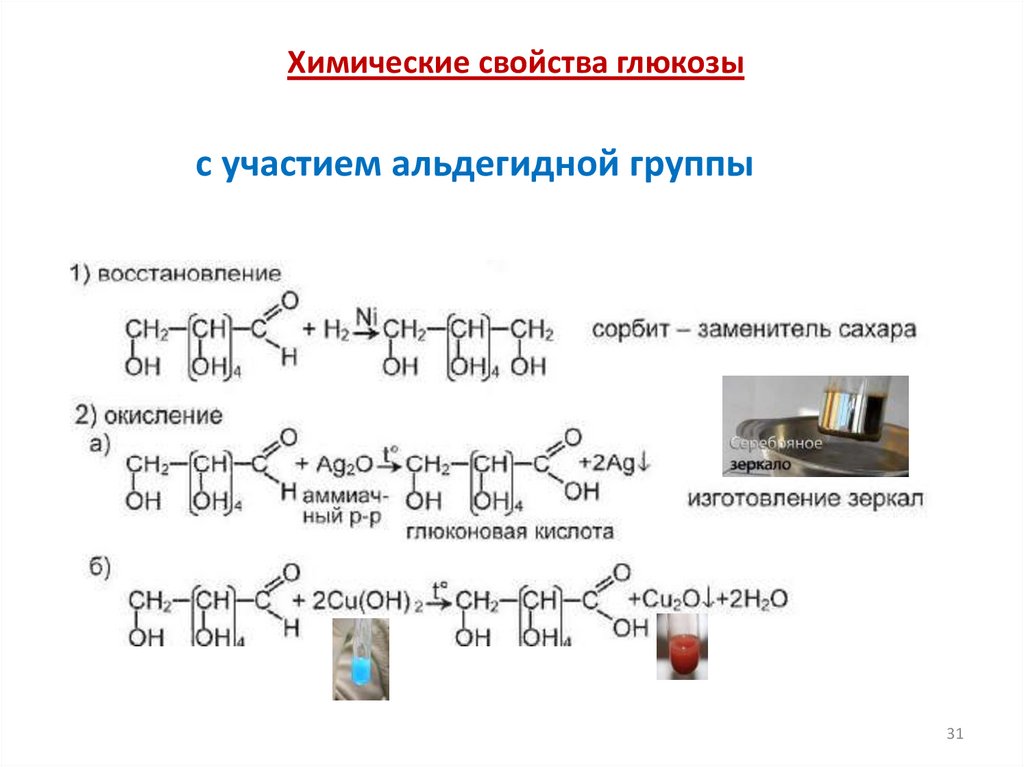
Химические свойства глюкозыс участием альдегидной группы
31
32.
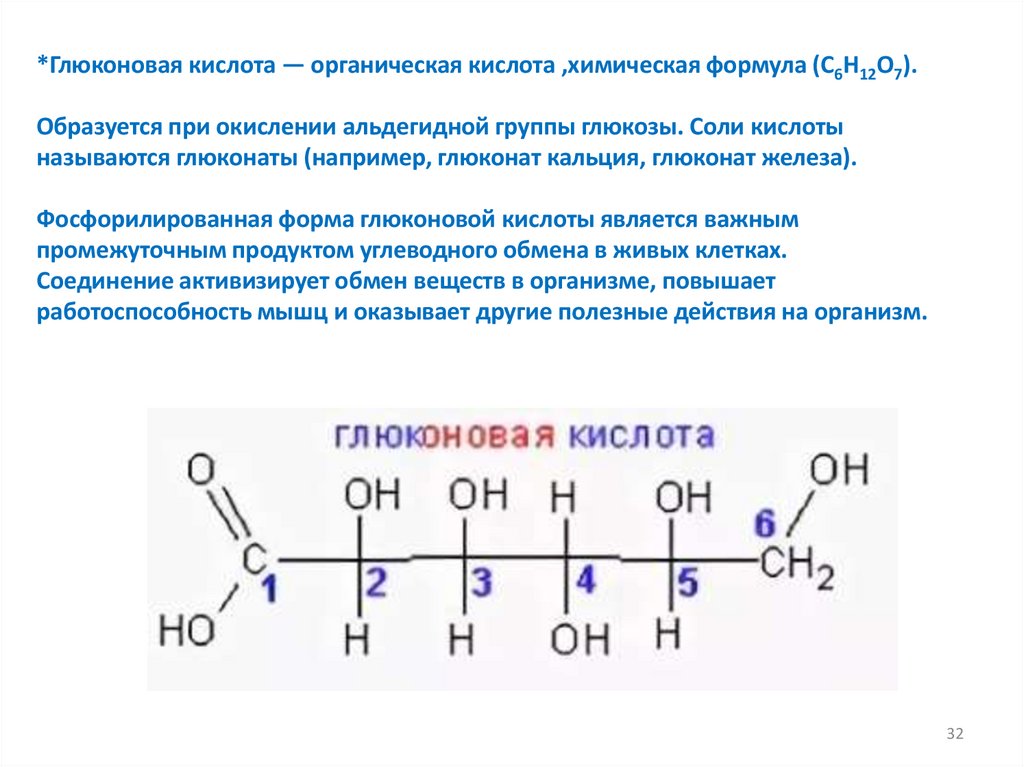
*Глюконовая кислота — органическая кислота ,химическая формула (C6H12O7).Образуется при окислении альдегидной группы глюкозы. Соли кислоты
называются глюконаты (например, глюконат кальция, глюконат железа).
Фосфорилированная форма глюконовой кислоты является важным
промежуточным продуктом углеводного обмена в живых клетках.
Соединение активизирует обмен веществ в организме, повышает
работоспособность мышц и оказывает другие полезные действия на организм.
32
33.
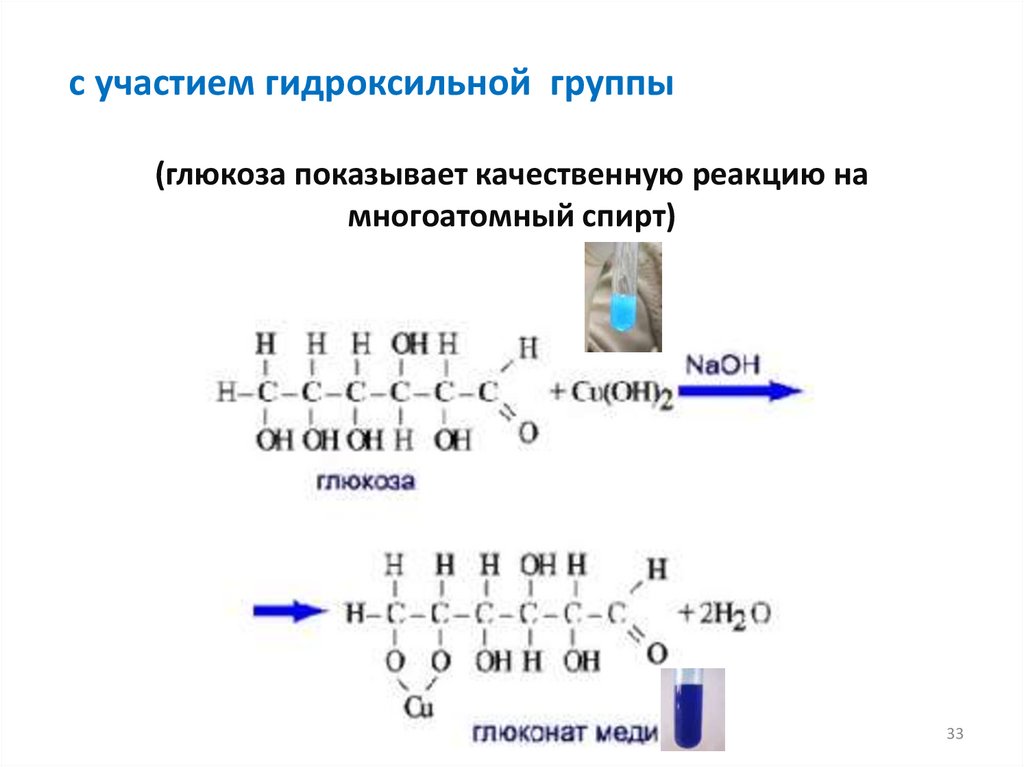
с участием гидроксильной группы(глюкоза показывает качественную реакцию на
многоатомный спирт)
33
34.
Спиртовое брожение— биохимическая реакция брожения,осуществляемая микроорганизмами, в результате которой
углеводы, преимущественно глюкоза, преобразуется в
молекулы этанола и углекислого газа. Реакция происходит в
бескислородной среде и является разновидностью
клеточного дыхания.
Этиловый спирт
34
35.
ГЛЮКОЗА НЕ ПОДВЕРГАЕТСЯ ГИДРОЛИЗУ!(не разлагается в водных растворах)
Углеводы, которые не подвергаются в водных
растворах гидролизу , т.е. не распадаются на более
простые вещества, называются моносахаридами.
35
36.
ГИДРОЛИЗ ПОЛИСАХАРИДОВВсе дисахариды способны вступать в реакцию гидролиза, катализируемую
кислотами, а также различными ферментами. В ходе такой реакции из одной
молекулы исходного дисахарида образуется две молекулы моносахарида, которые
могут быть как одинаковыми, так и различными в зависимости от состава
исходного моносахарида.
36
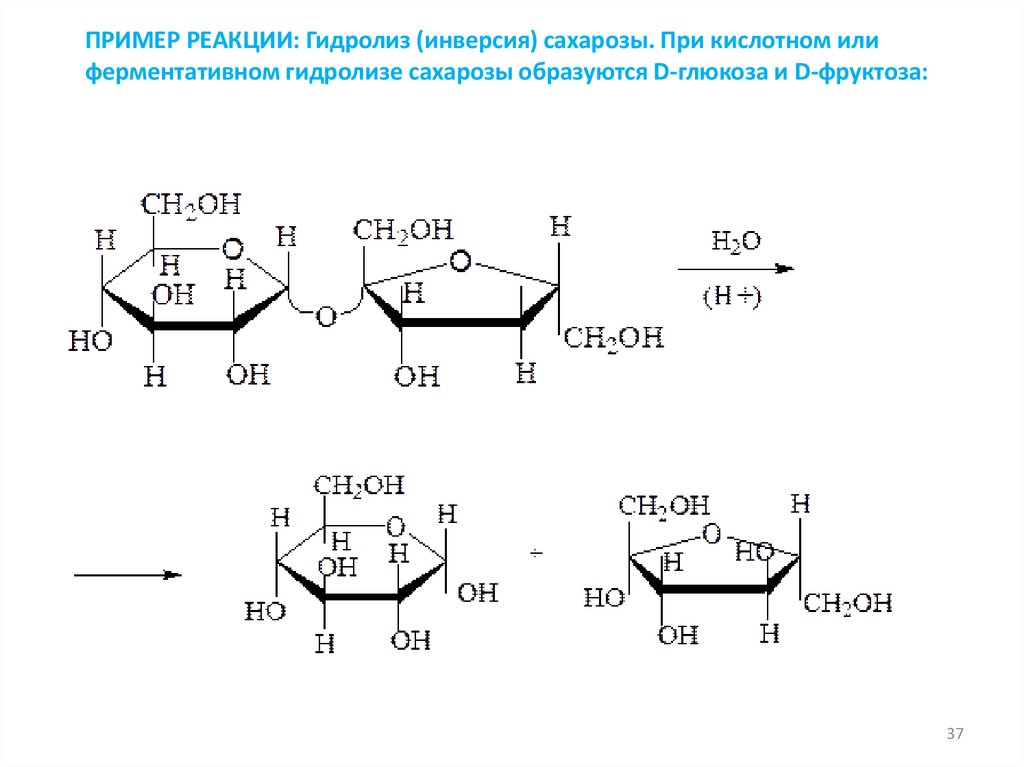
37.
ПРИМЕР РЕАКЦИИ: Гидролиз (инверсия) сахарозы. При кислотном илиферментативном гидролизе сахарозы образуются D-глюкоза и D-фруктоза:
37
38.
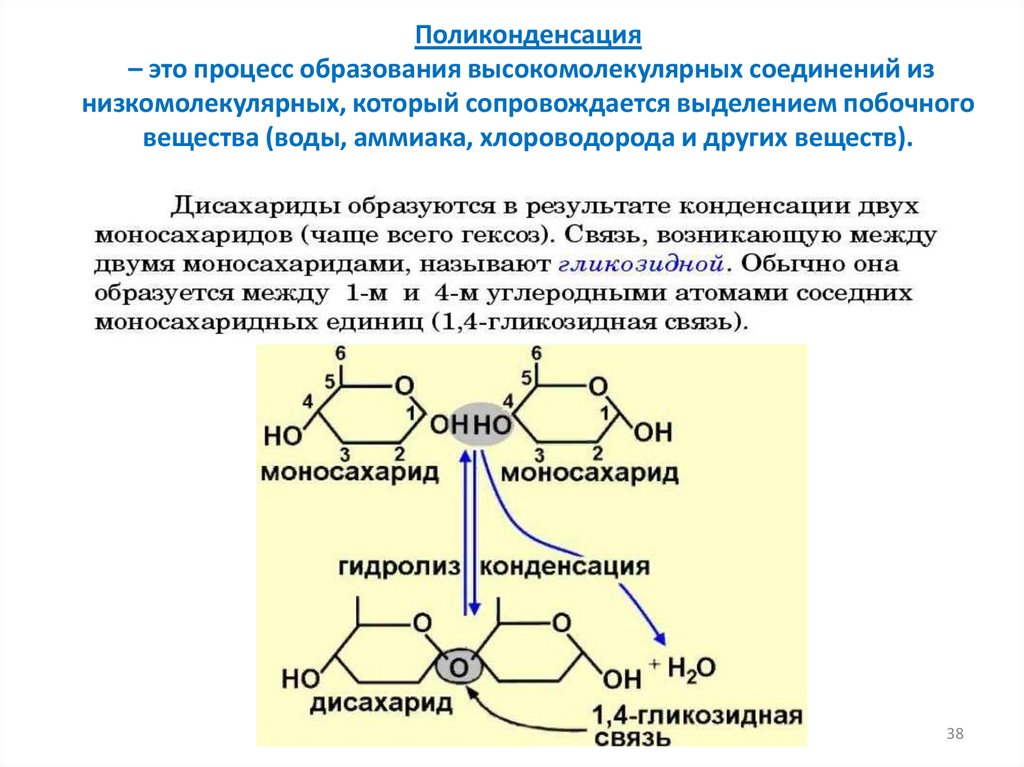
Поликонденсация– это процесс образования высокомолекулярных соединений из
низкомолекулярных, который сопровождается выделением побочного
вещества (воды, аммиака, хлороводорода и других веществ).
38
39.
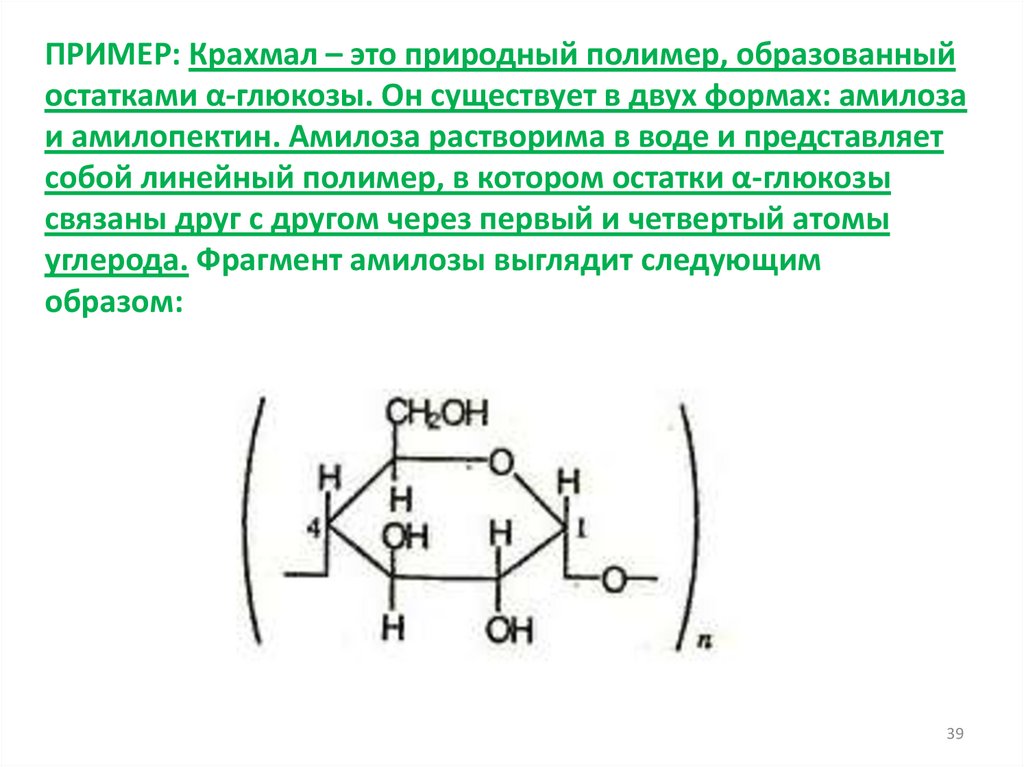
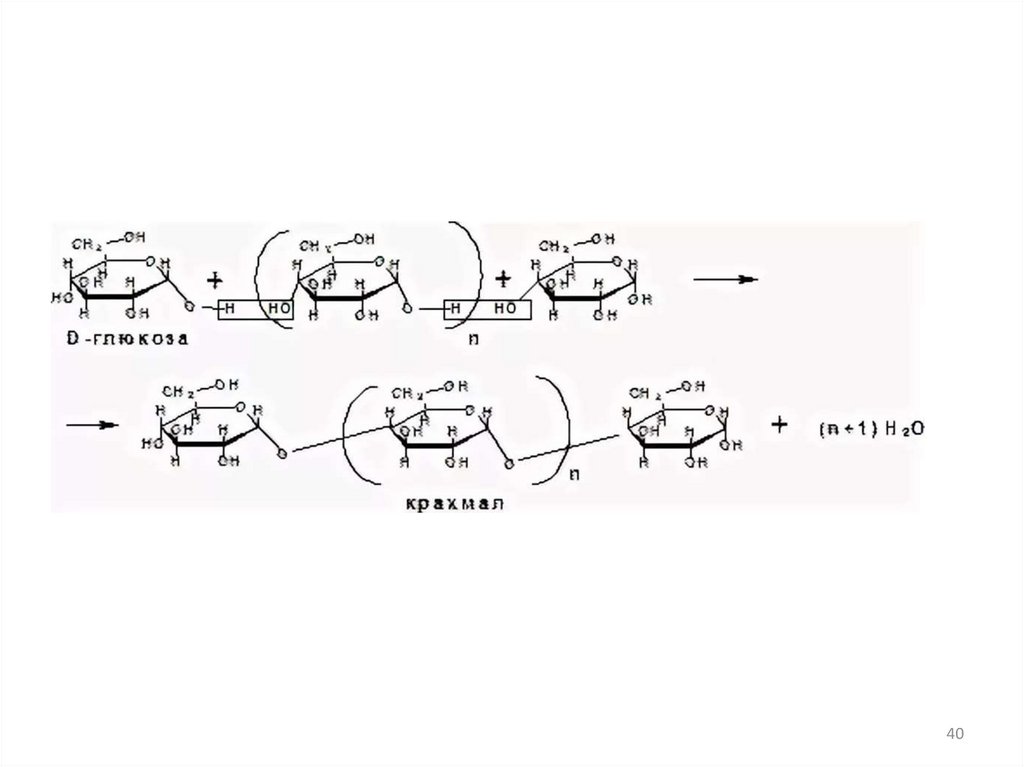
ПРИМЕР: Крахмал – это природный полимер, образованныйостатками α-глюкозы. Он существует в двух формах: амилоза
и амилопектин. Амилоза растворима в воде и представляет
собой линейный полимер, в котором остатки α-глюкозы
связаны друг с другом через первый и четвертый атомы
углерода. Фрагмент амилозы выглядит следующим
образом:
39
40.
4041.
Амилопектин (от др.-греч. ἄμυλος — «пирог из тонкой муки», πηκτς — «сбитый»,«сплочённый») — один из основных полисахаридов, составляющих крахмал.
Образован разветвлёнными цепочками остатков глюкозы, соединённых
гликозидными связями α-(1→4) и α-(1→6).
По структуре молекул подобен амилозе и гликогену, но у амилопектина цепочки
ветвятся чаще, чем у амилозы, и реже, чем у гликогена.
41
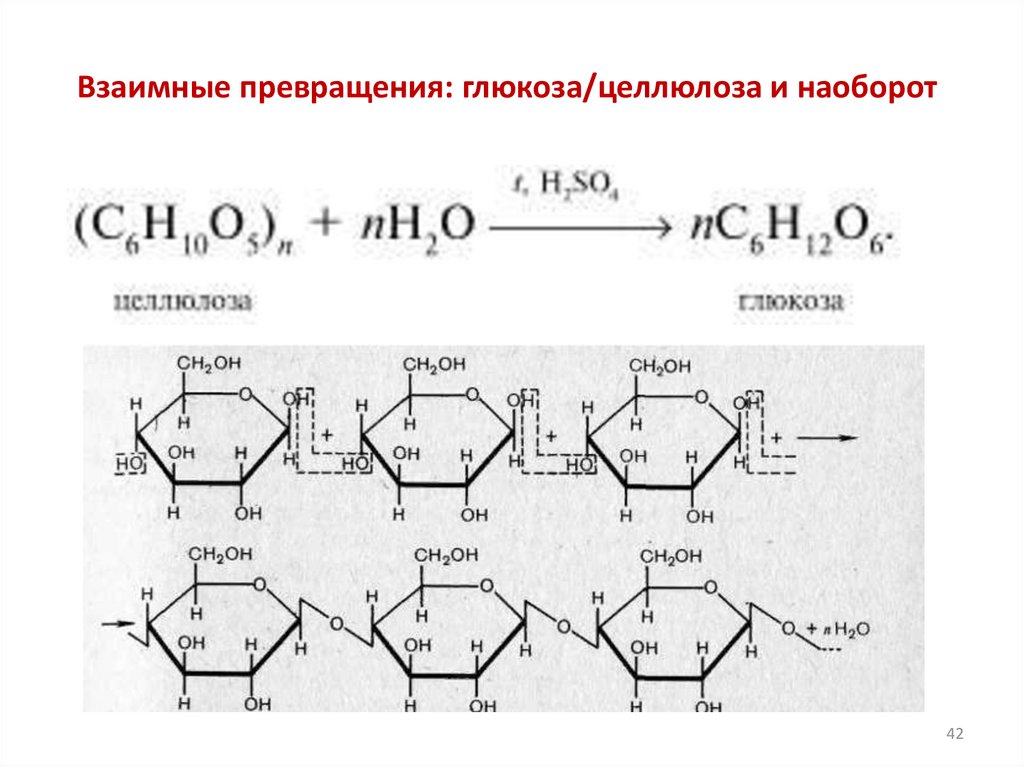
42.
Взаимные превращения: глюкоза/целлюлоза и наоборот42
43.
Образование макромолекул целлюлозы клеточных стеноквысших растений катализирует особый фермент.
У млекопитающих (как и большинства других животных) нет ферментов,
способных расщеплять целлюлозу. Однако многие травоядные животные
(например, жвачные) имеют в пищеварительном тракте бактериисимбионты, которые расщепляют и помогают хозяевам усваивать этот
полисахарид. Расщепление целлюлозы связано с действием в
расщепляющих организмах фермента целлюлазы.
43
44.
Домашнее задание:Ерохин.Ю.М. стр 351-360
Габриелян О.С. стр. 212-218
44
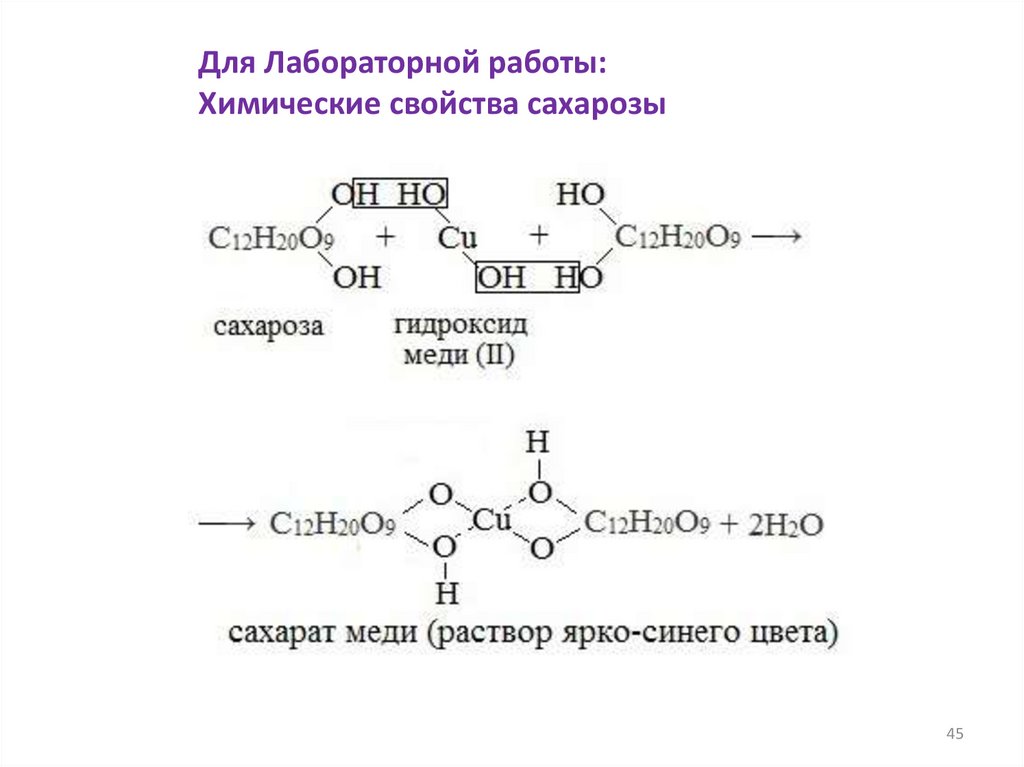
45.
Для Лабораторной работы:Химические свойства сахарозы
45
























 Биология
Биология








