Похожие презентации:
Основы биотехнологии презентации лекций для студентов заочной формы обучения
1. Основы биотехнологии презентации лекций для студентов заочной формы обучения
2.
• Биотехнология - дисциплина, изучающая возможностииспользования живых организмов, их систем или
продуктов
их
жизнедеятельности
для
решения
технологических задач, а также возможности создания
живых организмов с необходимыми свойствами методом
генной инженерии.
• Основной целью биотехнологии является получение
целевого продукта, создание рентабельного производства
необходимых людям продуктов.
• Высокоразвитые страны мира относят биотехнологию к
одной из важнейших современных отраслей, принимают
меры по стимулированию ее развития.
3.
• Историюформирования
биотехнологии
можно
разделить на ряд этапов:
• 1. Допастеровская эра (до 1865 г.).
• Биотехнология возникла в древности (примерно 6000-5000
лет до н.э.), когда люди научились, используя процесс
брожения, выпекать хлеб, готовить молочнокислые
напитки, сыр, вино, варить пиво.
• На Востоке получали ферментированные продукты
(соевый соус).
• Выращивали съедобные грибы.
• Микробиологические процессы происходили при мочке
льна, изготовлении кож.
4.
• Во второй половине XV века начинается развитиесовременного естествознания.
• На становление биологии оказали влияние успехи химии.
Химики изучали процессы брожения, которые связывали с
присутствием в среде дрожжей или ферментов.
• В XVI-XVII веках сначала во Франции, а затем
повсеместно, для разрыхления теста стали использовать
пивные, а затем спиртовые дрожжи.
• В 1674 г. Левенгук создал микроскоп.
• Лучшие его линзы увеличивали в 270 раз. Он смог
разглядеть микроскопические водоросли, простейших и
даже бактерии.
5.
ЛуиПастер
был
профессором
Страсбургском университете.
химии
в
В 1857 году Пастер доказал, что спиртовое брожение являлось
результатом
не
химического
процесса,
а
активности
микроорганизмов. Он экспериментально опроверг представление о
самопроизвольном зарождении живых существ.
Изучал порчу вина и пива. Обнаружил, что
разные виды брожения вызывают разные
виды микроорганизмов.
Предложил для сохранения вина и пива
способ стерилизации – пастеризацию.
Пастер изучал болезни животных и человека, создал научные
основы вакцинопрофилактики и вакцинотерапии.
6.
В конце XIX – начале XX вв. изучение брожения привелок развитию бродильного производства. Получали продукты
брожения - этанол, бутанол, ацетон, глицерин и др.
Изучали микробиологические процессы при получении,
хранении и созревании кисломолочных продуктов.
Промышленное производство лимонной кислоты из
гриба Aspergillus niger.
Разработан метод аэробной очистки канализационных вод.
7.
• В 1928 г. открыт первый антибиотик пенициллин, полученныйна основе продуктов жизнедеятельности микроорганизмов.
• Выделен А. Флемингом из гриба Penicillum notatum в Англии.
В 40-х г. в США Флори и Чейн занимались выделением и
очисткой пенициллина, организацией его производства.
• Флеминг, Флори и Чейн вместе получили Нобелевскую
премию по физиологии и медицине в 1945 году.
8.
• В 1960-1970 гг. - расширение спектра промышленнопроизводимых микробных продуктов.
• Производство аминокислот (глутамин и лизин).
• Получение чистых ферментов (протеазы, амилазы,
глюкозоизомеразы).
• Производство микробного белка. Микроорганизмы
выращивают на нефти, отходах спиртовой, целлюлознобумажной, деревообрабатывающей промышленности.
9.
Эра новой биотехнологии (после 1975 г.).В 1972 г. в США П. Бергом с сотрудниками создана
первая рекомбинантная ДНК, состоящая из фрагмента
ДНК вируса ОВ40 и бактериофага λ dvgal с лактозным
опероном E. coli.
С этого времени началось развитие генетической
инженерии.
Генетическая инженерия - система экспериментальных
приемов, позволяющих конструировать лабораторным путем
(в пробирке) рекомбинантные молекулы ДНК.
10.
• Первый коммерческий продукт – человеческий инсулин,продуцируемый бактерией, разрешен к применению в
1982 году.
• В результате применения методов генной инженерии:
• 1) Получают бактерии-сверхпродуценты с повышенным
уровнем синтеза нужных человеку веществ.
• 2) Получают рекомбинантные бактерии (встроены гены
других
организмов),
способные
синтезировать
несвойственные им продукты.
• 3) Получают трансгенные растения и животные.
11.
В настоящее время в биотехнологии выделяют важныенаправления:
1) Промышленная микробиология.
2) Медицинская биотехнология.
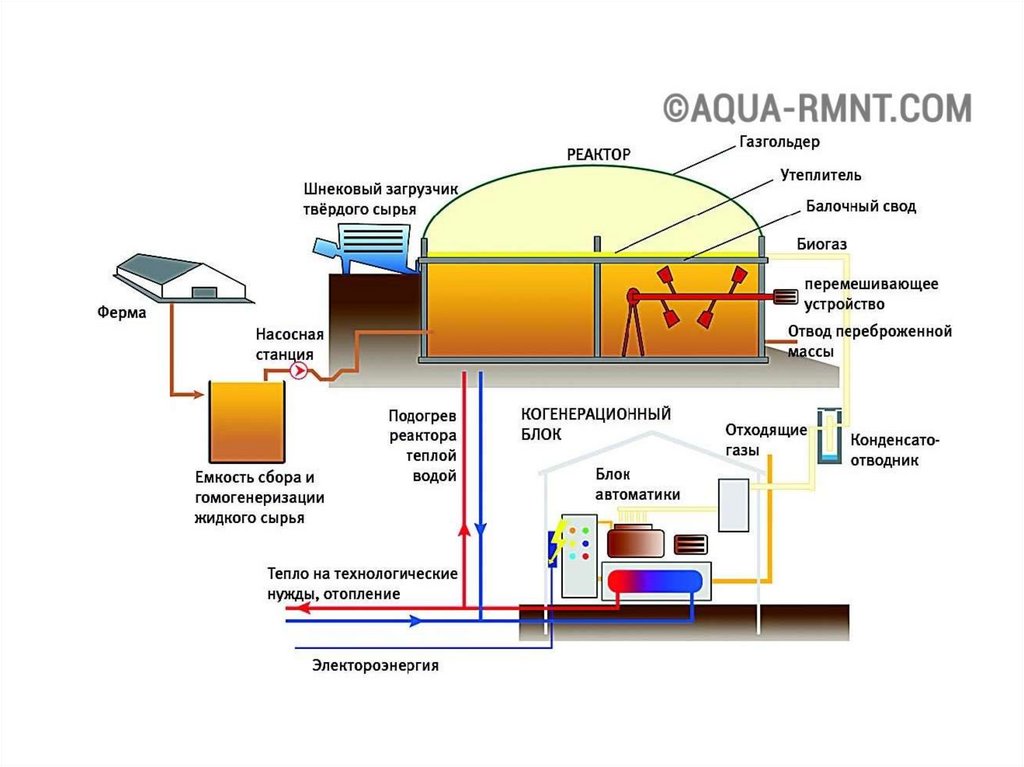
3) Технологическая биоэнергетика.
4) Сельскохозяйственная биотехнология.
5) Экологическая биотехнология.
6) Инженерная энзимология.
7) Клеточная и генетическая инженерия.
8) Биогидрометаллургия.
12.
Основными задачами биотехнологии являются:1.
Производство
биологически-активных
веществ
и
лекарственных препаратов для медицины (антибиотиков,
гормонов, вакцин, сывороток, высокоспецифичных антител);
2. Получение ветеринарных препаратов, кормовых добавок для
повышения продуктивности животноводства;
3. Получение продуктов для использования в пищевой,
химической,
микробиологической
и
других
отраслях
промышленности;
4. Разработка технологий борьбы с загрязнениями
окружающей среды;
5. Разработка микробиологических средств защиты растений
и бактериальных удобрений;
6. Создание новых полезных штаммов микроорганизмов,
сортов растений и пород животных.
13.
Объекты биотехнологии, требования к ихприменению
Биотехнологические
ступенях организации:
объекты
находятся
на
разных
а) субклеточные структуры (вирусы, плазмиды, ДНК
митохондрий и хлоропластов, ядерная ДНК);
б) бактерии и цианобактерии;
в) грибы;
г) водоросли;
д) простейшие;
е) культуры клеток растений и животных;
ж) растения.
14.
• Основойбольшинства
современных
биотехнологических производств является синтез
разнообразных биологически активных веществ с
помощью микроорганизмов.
• Микроорганизмы, микробы (от греч. micros – малый) –
микроскопически малые организмы (до 500 мкм),
преимущественно одноклеточные: бактерии,
одноклеточные грибы, водоросли, простейшие, клетки
которых нельзя увидеть невооруженным глазом.
15.
Преимущества использования микроорганизмов:1) генетическое разнообразие позволяет им
а) синтезировать большое количество веществ;
б) разлагать большое количество природных и неприродных
соединений.
2) отличаются быстрым ростом. Это позволяет за короткий
промежуток времени синтезировать большое количество
требуемого продукта в строго контролируемых условиях.
16.
Преимуществабиологических
способов
перед
химическими:
1. Химическими способами не могут быть синтезированы
многие
сложные
органические
молекулы
(белки,
антибиотики);
2. Биологические системы работают при атмосферном
давлении, невысоких температурах, близких к нейтральному
значениях рН и т. д.;
3. Каталитические биохимические реакции намного
специфичнее, чем реакции химического катализа;
4. Образуются изомеры одного типа, а не их смесей, как
это часто бывает в реакциях химического синтеза.
17.
Биологические способы в сравнении с химическимиметодами имеют недостатки:
1. Процесс нужно вести в асептических условиях, т.к.
возможно загрязнение посторонней микробиотой.
2. Целевой продукт нужно выделять из смеси веществ.
3. Требуется много воды для приготовления питательной
среды, которую нужно очищать перед сбросом в
окружающую среду.
4. Биопроцессы обычно идут медленнее в сравнении со
стандартными химическими процессами.
18.
Принципы подбора биотехнологическихобъектов
Первичным
этапом
разработки
биотехнологического процесса является:
1) получение чистых культур микроорганизмов,
2) клеток или тканей (растений или животных).
любого
Многие дальнейшие этапы работы с биотехнологическими
объектами
проводятся
с
использованием
методов,
применяемых в микробиологических производствах.
19.
• Промышленные микроорганизмы используются впромышленном производстве.
• Модельные микроорганизмы служат модельными
объектами при изучении фундаментальных жизненных
процессов.
• К их числу относятся кишечная палочка (E. coli), сенная
палочка (Bac. subtilis) и пекарские дрожжи (S. cerevisiae).
• Базовые объекты биотехнологии
• Во многих биотехнологических процессах используются
GRAS-микроорганизмы (generally recognized as safe),
которые обычно считаются безопасными.
20.
• Отбор микроорганизмов для использования вмикробиологическом производстве:
• 1) Отбор проб из естественных мест обитания
предполагаемого продуцента.
• Получение накопительной культуры. Посев проб в
элективную среду, обеспечивающую преимущественное
развитие интересующего микроорганизма.
• Выделение чистой культуры с дальнейшим изучением
изолированного микроорганизма, определением его
способности образовывать нужные вещества.
• 2) Выбор нужного вида из имеющихся коллекций
микроорганизмов.
21.
• Критерии при выборе биотехнологическогообъекта:
• 1) Способен синтезировать целевой продукт.
• 2) Имеет высокую скорость роста;
• 3) Растет на доступных и недорогих питательных
субстратах;
• 4) Устойчивость к заражению посторонней микробиотой.
• 5) Непатогенный и не токсигенный для человека и
животных, безопасный для окружающей среды.
22.
• Микроорганизмы культивируют на разнообразныхпитательных средах.
• Требования к питательной среде:
• 1) Должна содержать все необходимые для роста
питательные вещества в определенном количестве и легко
усвояемой форме;
• 2) твердая среда должна иметь оптимальную влажность;
• 3) иметь определенную кислотность, вязкость, буферную
емкость, по возможности быть прозрачной;
• 4) быть стерильной.
23.
Компонентный состав сред определяется питательнымипотребностями продуцента.
Важным критерием, определяющим выбор сырья для
биотехнологических процессов, являются:
1) стоимость,
2) наличие в достаточных количествах,
3) химический состав.
24.
• При культивировании микроорганизмов на стерильныхпитательных средах, нужно поддерживать оптимальные
или благоприятные для них условия - температуру и
рН среды.
• При выращивании аэробных микроорганизмов, особенно
в больших объемах среды, ее дополнительно аэрируют,
встряхивая, перемешивая, а при необходимости
пропускают через среду стерильный воздух.
• При культивировании строго анаэробных бактерий
создают
анаэробные
(бескислородные)
условия,
используют прокипяченные питательные среды, которыми
заполняют пробирки и колбы под пробку (без пузырьков
воздуха) и др.
25.
• Питательные среды для выращивания микроорганизмовмогут быть твердые (плотные) или жидкие.
• Микроорганизмы можно выращивать на поверхности
твердых или жидких питательных сред без
перемешивания - такой способ называется методом
поверхностного культивирования.
26.
• При глубинном культивировании микроорганизмывыращивают на жидких питательных средах при
перемешивании, как правило в колбах на качалке
(шейкере) .
• При промышленном культивировании микроорганизмов в
больших масштабах их выращивают в специальных
аппаратах – ферментерах на жидких питательных средах.
27.
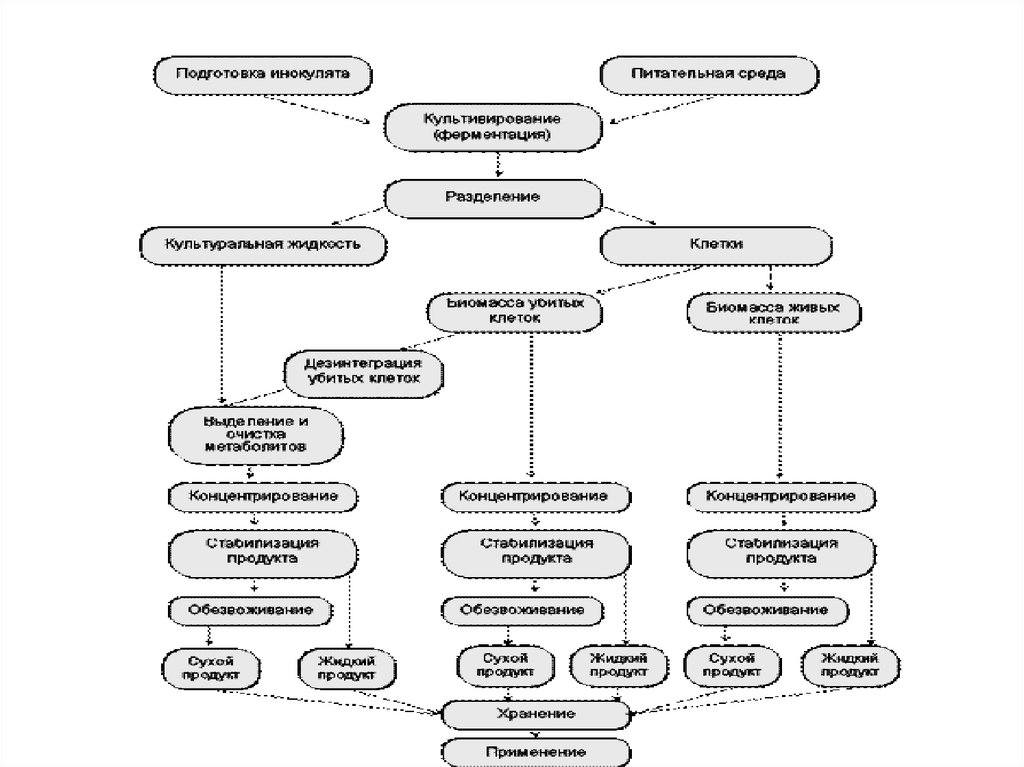
Стадии биотехнологического производства1. Подготовка сырья (питательной среды) субстрата с
заданными свойствами (рН, температура, концентрация).
2. Подготовка биообъекта: посевной культуры или
фермента ( в т.ч. иммобилизованного).
3. Ферментация - образование целевого продукта за счет
биологического превращения компонентов питательной
среды в биомассу или в целевой метаболит.
4. Выделение и очистка целевого продукта.
5. Получение товарной формы продукта
6. Переработка и утилизация отходов (биомассы,
культуральной жидкости и т.п.).
28.
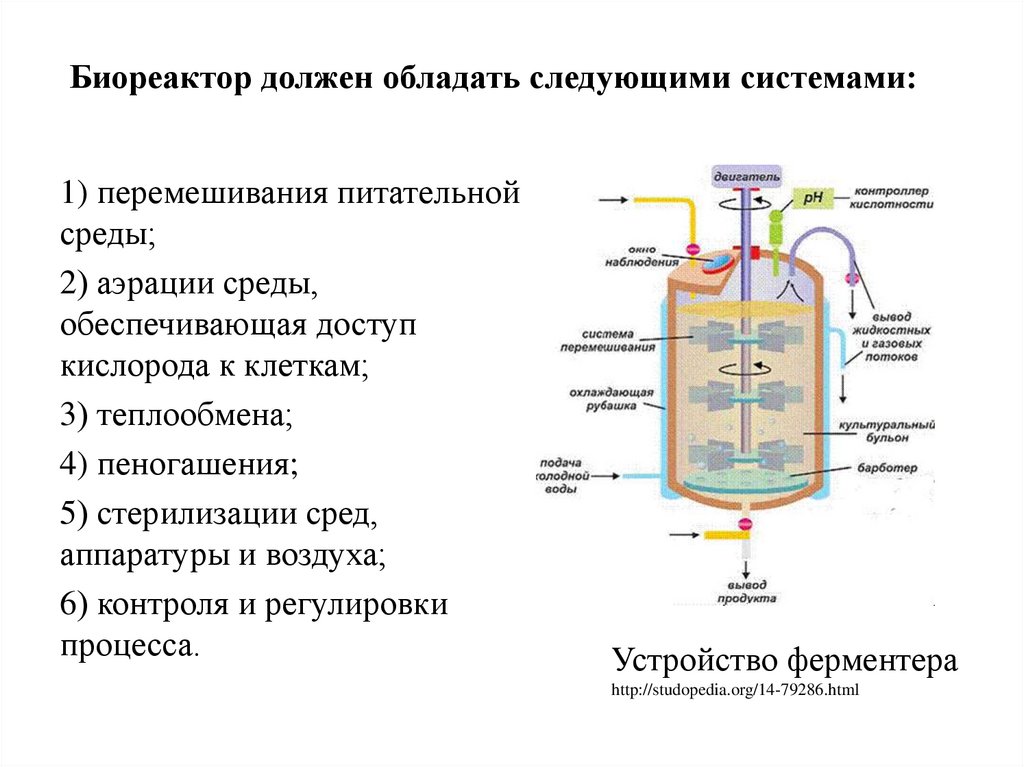
Биореактор должен обладать следующими системами:1) перемешивания питательной
среды;
2) аэрации среды,
обеспечивающая доступ
кислорода к клеткам;
3) теплообмена;
4) пеногашения;
5) стерилизации сред,
аппаратуры и воздуха;
6) контроля и регулировки
процесса.
Устройство ферментера
http://studopedia.org/14-79286.html
29.
• Требования к биореакторам:• Должны обеспечивать благоприятные условия для роста
культивируемого микроорганизма.
• Исключить попадание посторонних микроорганизмов.
• Объем культивируемой смеси должен оставаться
постоянным, чтобы не было утечки или испарения
содержимого.
• Параметры культивирования (температура, рН, уровень
аэрации и т.д.) должны постоянно контролироваться.
• Культура
при
выращивании
должна
хорошо
перемешиваться.
30.
• Для обеспечения необходимых условий протеканиябиотехнологических
процессов
используются
ферментеры или биореакторы.
• Биореакторы варьируют от простых сосудов до сложных
систем с различным уровнем компьютерного оснащения.
31.
• Лабораторные,пилотные
и
промышленные
биореакторы: проблемы масштабирования
• Технология производственного процесса отрабатывается
поэтапно:
в
лабораторных,
пилотных
(опытнопромышленных) и промышленных установках.
• Обычно встречаются следующие объемы аппаратов:
• 1) для лабораторных – 0,5 – 100 л;
• 2) для пилотных – 100 л – 5 м3;
• 3) для промышленных биореакторов – 5 – 1000 м3 и более.
• На каждом из этапов наращивания масштаба
биотехнологического
процесса
(масштабирования
процесса) – решаются свои задачи налаживания
производства и его оптимизации.
32.
• Лабораторныебиореакторы
используют
для
определения скорости роста клеток, эффективности
утилизации субстратов и образования целевого продукта,
расчет коэффициентов массопередачи (поступления в
среду О2, освобождения от газообразных продуктов);
• Пилотные установки используют для отработки
технологических параметров для производства.
• Производственные установки используют для выпуска
продукции.
33.
Автоклавируемый стеклянныйбиореактр с рабочим объёмом до
4,5 литров (общий объём 6,2
литра)
34.
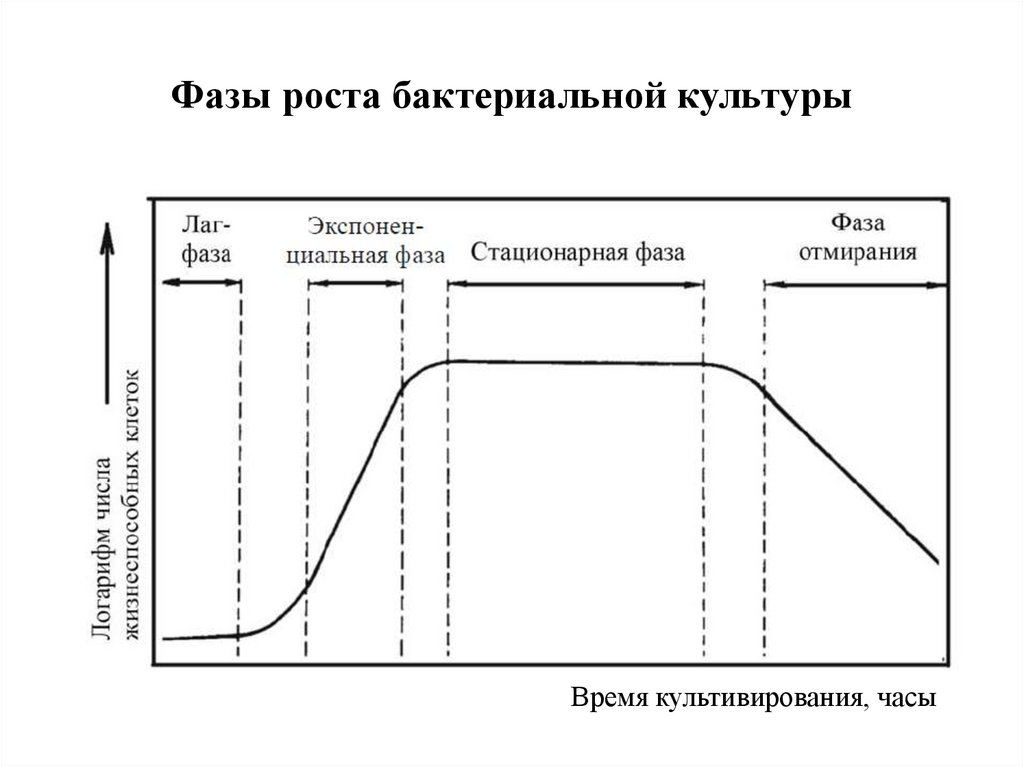
Периодические процессыПериодический процесс состоит из следующих этапов:
1) стерилизация сред, биореактора и вспомогательного
оборудования;
2) загрузка аппарата питательной средой;
3) внесение посевного материала (клеток, спор);
4) рост культуры, который может совпадать во времени со
следующим этапом или предшествовать ему;
5) синтез целевого продукта;
6) отделение и очистка готового продукта;
7) мойка биореактора и его подготовка к новому циклу.
35. Фазы роста бактериальной культуры
Время культивирования, часы36.
• Продление процесса периодического культивирования• Периодическое культивирование с подпиткой - в
процессе культивирования в аппарат через определенные
интервалы добавляют питательные вещества.
• Отъемно-доливочное
культивирование
часть
содержимого биореактора периодически изымается и
добавляется равное количество питательной среды. Такой
прием
обеспечивает
регулярное
"омолаживание"
(обновление) культуры и задерживает ее переход в фазу
отмирания.
Этот
прием
иногда
называется
полунепрерывным культивированием.
37.
Непрерывное культивирование• При
непрерывном
культивировании
в
аппарат
культивирования
непрерывно
подается
свежая
питательная среда и непрерывно удаляется выросшая
культура.
• Для
установившегося
режима
непрерывного
культивирования характерны постоянные концентрации
биомассы микроорганизмов и удельная скорость роста
популяции.
• Различают хемостатный и турбидостатный режимы
непрерывного культивирования.
38.
• Конструкция хемостата предусматривает наличие:• 1) приспособления для подачи питательной среды;
• 2) устройства, обеспечивающего отток культуральной
жидкости вместе с клетками,
• 3) системы, контролирующей концентрацию элементов
питательной среды и управляющей скоростью её подачи.
39.
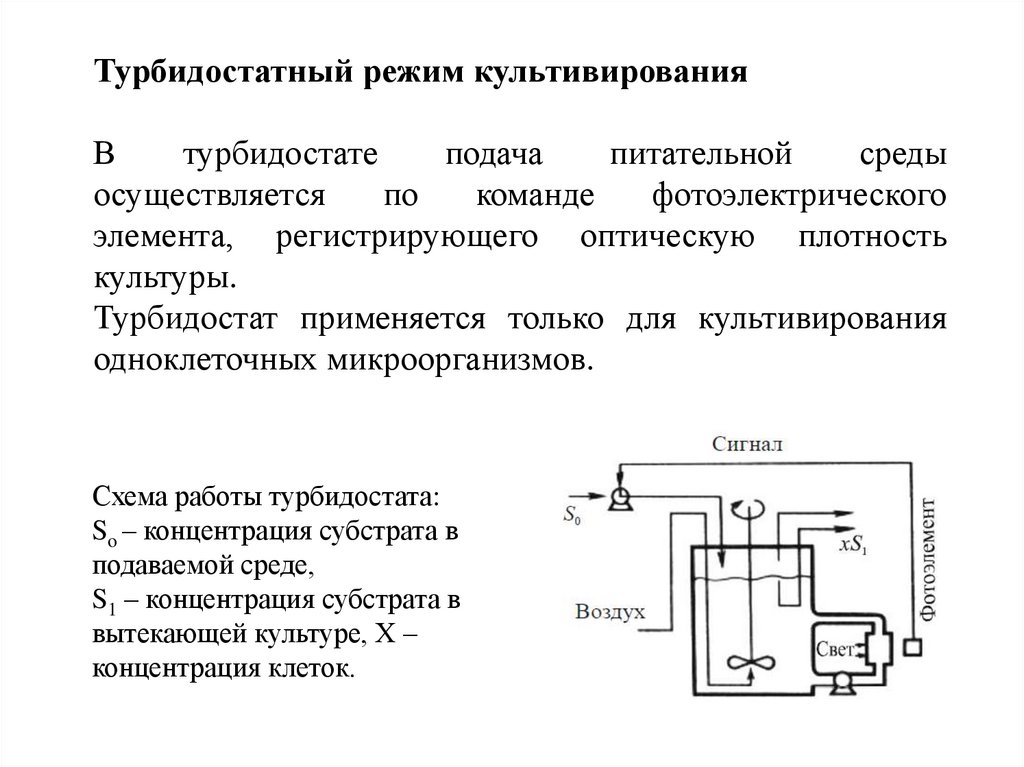
Турбидостатный режим культивированияВ
турбидостате
подача
питательной
среды
осуществляется
по
команде
фотоэлектрического
элемента, регистрирующего оптическую плотность
культуры.
Турбидостат применяется только для культивирования
одноклеточных микроорганизмов.
Схема работы турбидостата:
So – концентрация субстрата в
подаваемой среде,
S1 – концентрация субстрата в
вытекающей культуре, Х –
концентрация клеток.
40. Анаэробные процессы. Биореакторы для обеспечения анаэробных условий. Нет приспособлений для аэрирования среды.
41.
42.
• Твердофазное культивирование:• исследование биодеградации материалов;
• биоремедиация загрязненных почв промышленными
отходами, нефтепродуктами и т.п.;
• получение ферментов и биологически-активных
компонентов.
43.
• Твердофазное культивирование грибов44.
Классификация продуктов биотехнологическихпроизводств
1) Клетки микроорганизмов, которые используют для
получения биомассы.
Производство пекарских, винных, кормовых дрожжей;
вакцин, белково-витаминных концентратов, средств
защиты растений, заквасок для получения
кисломолочных продуктов и силосования кормов,
микробных удобрений и т.д.
45.
2) Продукты метаболизма живых клеток:– Первичные метаболиты необходимы для роста
клеток. (структурные единицы биополимеров —
аминокислоты, нуклеотиды, моносахариды, витамины,
коферменты, органические кислоты)
– Вторичные метаболиты (антибиотики, пигменты,
токсины), образующиеся по завершении фазы их роста.
3) получение ферментов микробного происхождения;
4) получение рекомбинантных продуктов;
5) биотрансформация веществ;
6) утилизация неприродных соединений.
46.
47.
• Получение товарных форм биопрепаратов.1. Представляют собой жизнеспособные микроорганизмы
(средства защиты растений, бактериальные удобрения,
закваски для силосования кормов, и др.).
2. Представляют собой инактивированную биомассу
клеток и продукты ее переработки (кормовые дрожжи).
3. Очищенные продукты метаболизма микроорганизмов
(витамины, аминокислоты, ферменты, антибиотики,
липиды, полисахариды и др.).
48.
• Культивирование клеток растений• Культуры клеток и тканей растений выращивают на
искусственной питательной среде в асептических
условиях.
• В основе метода культуры клеток и тканей растений лежит
уникальное
свойство
растительной
клетки
–
тотипотентность – это способность клетки реализовывать
генетическую
информацию,
обеспечивающую
ее
дифференцировку и развитие до целого организма.
49.
• Принципы культивирования растительных клеток.• 1) Создание асептических условий - стерилизация
помещения (ламинар-бокса), посуды, инструментов,
питательных сред, самих растений (диацид, перекись
водорода, сулема).
• 2) Питательные среды имеют сложный состав: углеводы
(глюкоза или сахароза), т.к. некоторые ткани не содержат
хлорофилла; макро- и микроэлементы; фитогормоны
(ауксины, цитокинины).
• 3)
Условия
культивирования:
освещенность,
температура (26° С), аэрация, влажность.
50.
• Культуры клеток высших растений.51.
• Если культивирование клеток растений происходит наповерхности агаризованной среды, то образуется
каллусная ткань.
• Каллус – неорганизованная пролиферирующая ткань,
состоящая из дедифференцированных клеток.
52.
• Каллус может образовываться на изолированных кусочкахткани (эксплантах) in vitro.
• Цвет массы может быть белым, желтоватым, зеленым,
красным. В зависимости от происхождения и условий
выращивания каллусные ткани бывают рыхлые или
плотные. В длительной культуре каллусные ткани теряют
пигментацию и становятся рыхлыми.
53.
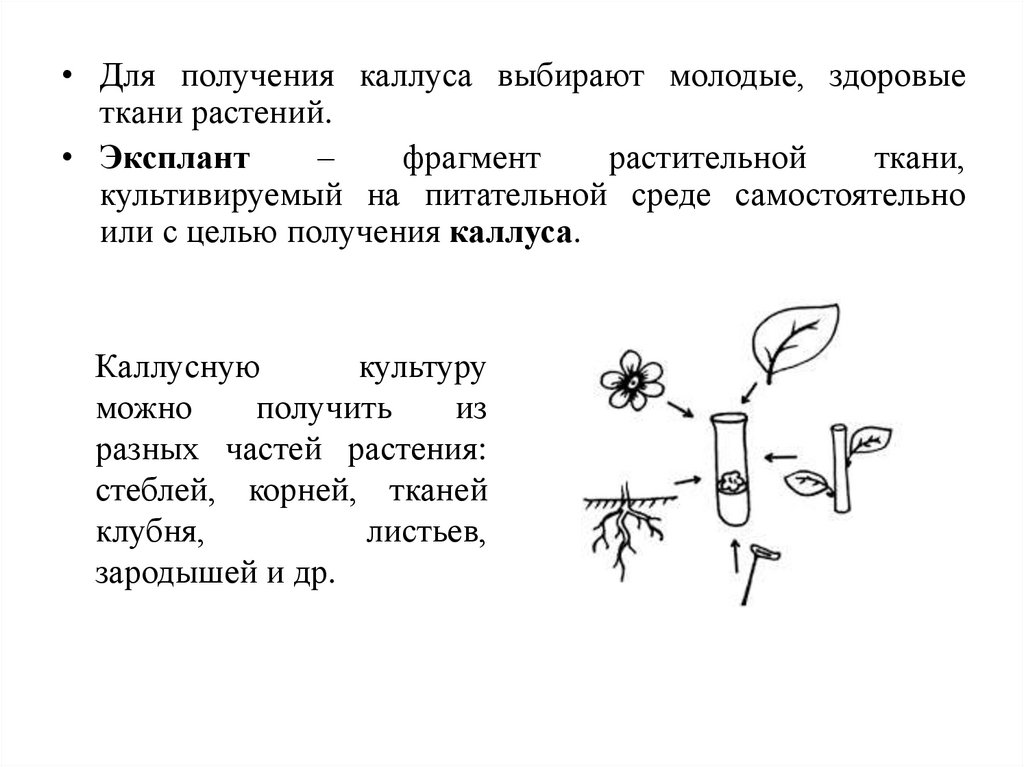
• Для получения каллуса выбирают молодые, здоровыеткани растений.
• Эксплант
–
фрагмент
растительной
ткани,
культивируемый на питательной среде самостоятельно
или с целью получения каллуса.
Каллусную
культуру
можно
получить
из
разных частей растения:
стеблей, корней, тканей
клубня,
листьев,
зародышей и др.
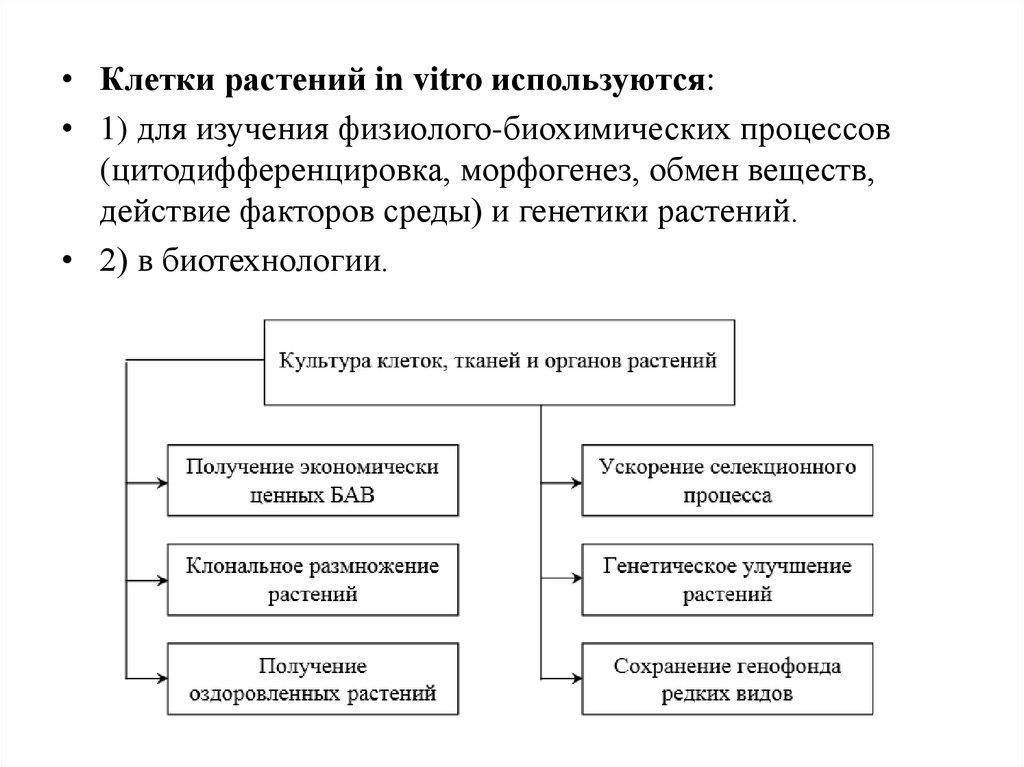
54.
• Клетки растений in vitro используются:• 1) для изучения физиолого-биохимических процессов
(цитодифференцировка, морфогенез, обмен веществ,
действие факторов среды) и генетики растений.
• 2) в биотехнологии.
55.
• Протопласты растительных клеток, их получение,методы регенерации и культивирования.
• Протопласт (от греч. Protos - первый и platos вылепленный, образованный) - клетка, лишенная
целлюлозной оболочки, окруженная цитоплазматической
мембраной,
способная
осуществлять
активный
метаболизм.
56.
• Основными этапами при получении протопластовявляются следующие:
• 1) удаление эпидермиса в стерильных условиях;
• 2) измельчение ткани;
• 3) помещение в мацерирующий раствор, состоящий их
сахара, минеральных солей, ферментов (целлюлаз,
пектиназ, гемицеллюлаз);
• 4) отделение образовавшихся протопластов путем
фильтрования, центрифугирования и др.;
• 5) промывание протопластов.
57.
• На основе метода слияния протопластов разработанметод соматической гибридизации растений.
• Изолированные
протопласты,
выделенные
из
родительских растений, могут сливаться с образованием
гибридных клеток, способных регенерировать в гибридное
растение.
• В качестве родительских используются соматические
клетки растений, из которых получают протопласты.
Слияние протопластов способствует объединению не
только ядерных, но и цитоплазматических генов
родительских клеток.
• Соматический гибрид - продукт слияния и цитоплазмы, и
ядер обоих протопластов.
• Цибрид (цитоплазматический гибрид) – содержит
цитоплазму обоих родителей, а ядро одного из них.
58.
• Стимулировать слияние протопластов можно спомощью:
• 1) полиэтиленгликоля (снижение поверхностных
зарядов, отнятие воды, разрыв мембран);
• 2) под воздействием электрического поля.
• Образующиеся
гибридные
структуры
сохраняют
способность к восстановлению клеточной стенки, в
результате появляются гибридные клетки.
59.
• Метод слияния протопластов используют для селекциипромышленно важных продуцентов.
• Увеличить количество материала для отбора можно при
помощи генетической рекомбинации в сочетании с
индуцированным мутагенезом.
• Возможно получение межвидовых и межродовых
гибридов, скрещивание филогенетически отдаленных
форм.
• Известны стерильные межвидовые гибриды картофеля и
томатов (поматы), табака и картофеля, табака и
беладонны, образующие нормальные стебли и корни.
• Удается
получать
растения,
гетерозиготные
по
внеядерным генам; гибриды, в которых от одного
родителя получено ядро, а от другого – цитоплазма.
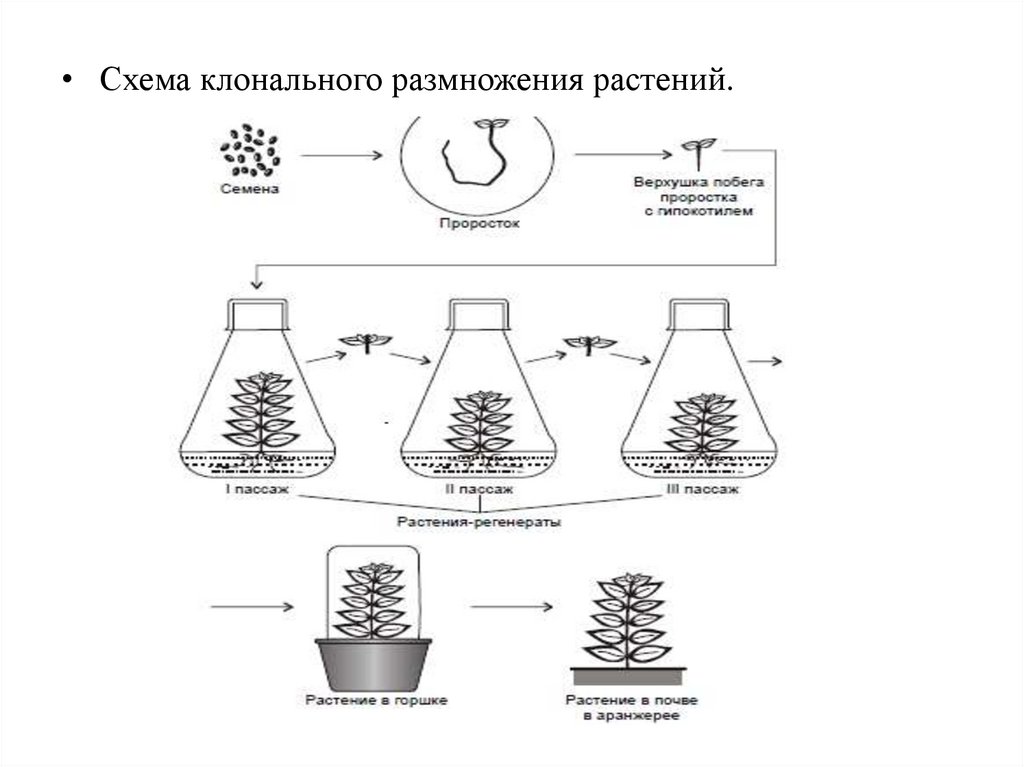
60.
• Клональноемикроразмножение
растений
размножение растений in vitro неполовым путем с
помощью метода культуры тканей, позволяющее
получать растения генетически идентичные исходному.
• В основе лежит способность соматической растительной
клетки полностью реализовать потенциал своего развития
(тотипотентность).
61.
• Клональное микроразмножение растений имеетследующие преимущества:
• 1) Высокий коэффициент размножения.
• Например, герберы при клональном размножении могут
давать до 1 млн растений в год, тогда как при обычных
способах только 100.
• 2) Получение генетически однородного материала.
• 3) Возможность оздоровления растений, освобождения их
от вирусов благодаря клонированию меристематических
тканей.
• 4) Воспроизведение посадочного материала круглый год.
• 5) Возможность размножения растений, которые в
естественных условиях трудно размножаются.
• 6) Сокращение продолжительности селекционного
периода.
62.
• При клональном используется меристематическиеткани.
• В качестве экспланта желательно использовать молодые,
слабодифференцированные ткани: кончики стеблей,
пазушные почки, зародыши, молодые листья, черенки,
соцветия, чешую луковиц.
63.
• Процесс клонального микроразмножения можноразделить на следующие стадии:
• 1. Изолирование эксплантов растения – донора,
получение хорошо растущей стерильной культуры.
Эксплант в стадии
формирования почек
Почки, прорастающие
на питательной среде
64.
• 2. Микроразмножение путем микрочеренкования.Основано на снятии апикального доминирования
(удаление
верхушечной
меристемы,
добавление
цитокининов).
• Полученные побеги отделяют от первичного экспланта и
самостоятельно культивируют на свежеприготовленной
питательной среде, стимулирующей пролиферацию
пазушных меристем и возникновение побегов более
высоких порядков. Образующиеся пучки побегов делят,
переносят на свежую питательную среду.
• 3. Укоренение размноженных побегов (добавляют в
питательную среду ауксины, затем переносят в почву).
• 4. Выращивание растений в условиях теплицы и
подготовка их к реализации или посадке в поле.




























































 Биология
Биология








