Похожие презентации:
Знаки химических элементов. Периодическая система химических элементов
1.
Знаки химических элементов.Периодическая система химических
элементов
2.
Химический элемент —определённый вид атомов.
3.
До второй половины 19 века было открытомножество химических элементов.
4.
Йёнс Якоб Берцелиус
названия на латинском
языке;
присваивание
химического символа в
соответствии с первыми
буквами латинского
названия элемента.
5.
Химические элементыкислород
водород
6.
Химические элементыгелий
кальций
7.
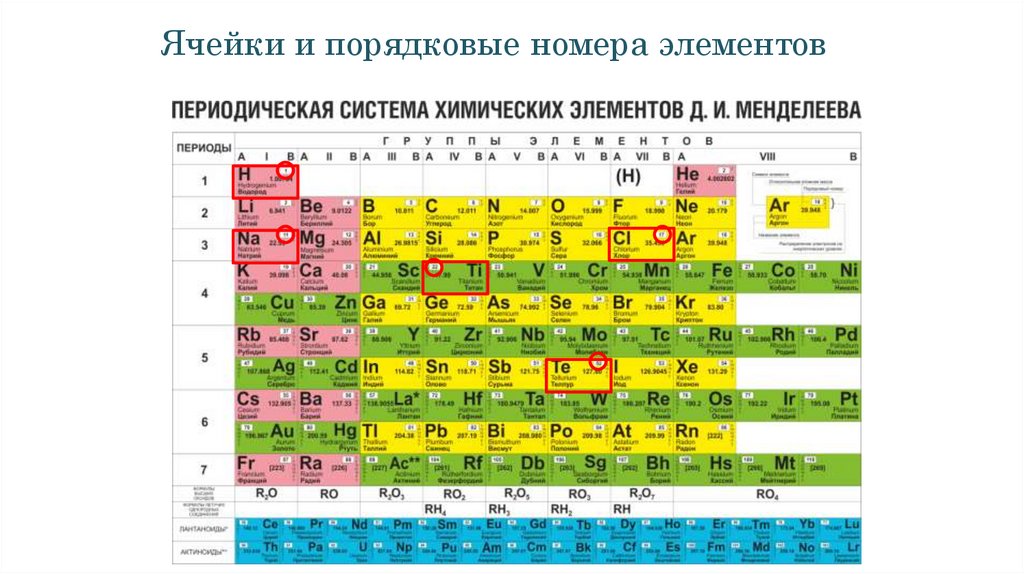
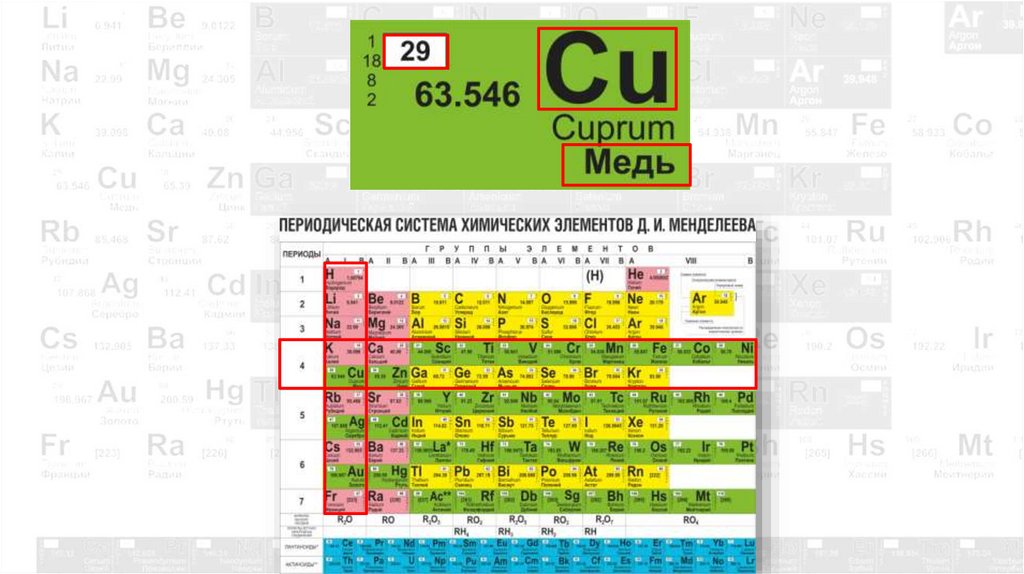
Ячейки и порядковые номера элементов8.
Периоды в таблице Менделеева9.
Период — горизонтальный рядхимических элементов, расположенный
по возрастанию их относительной
атомной массы.
10.
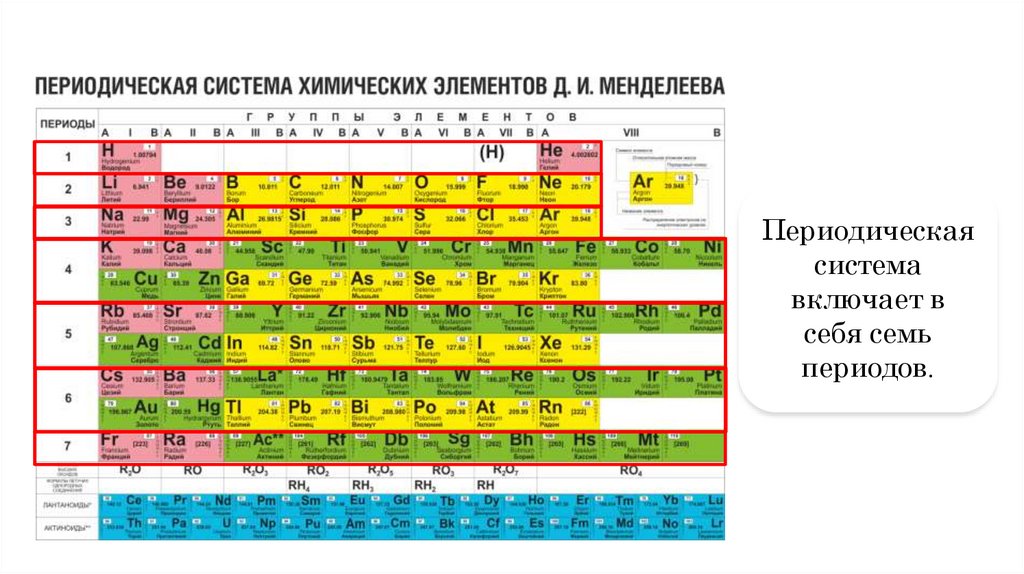
Периодическаясистема
включает в
себя семь
периодов.
11.
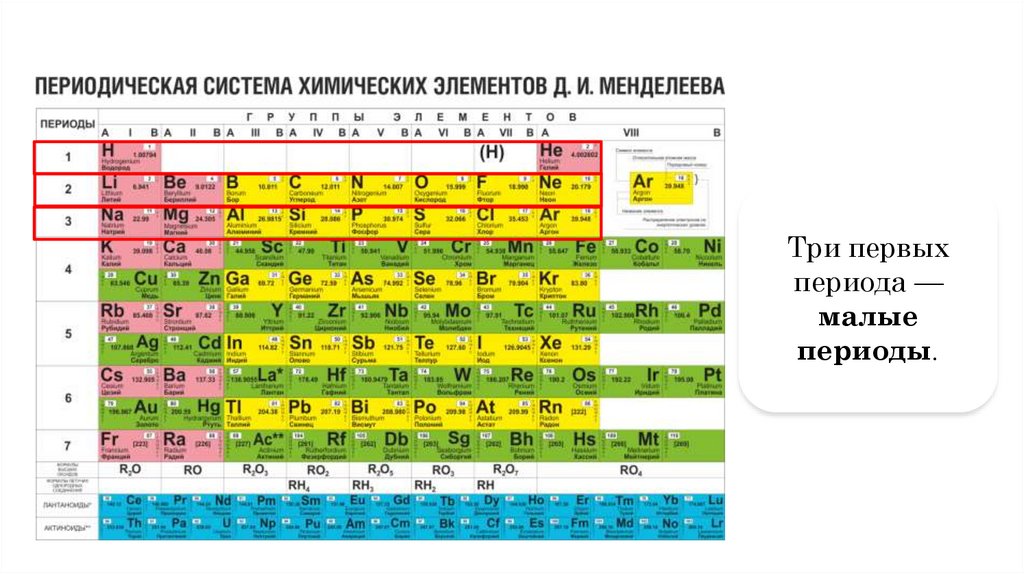
Три первыхпериода —
малые
периоды.
12.
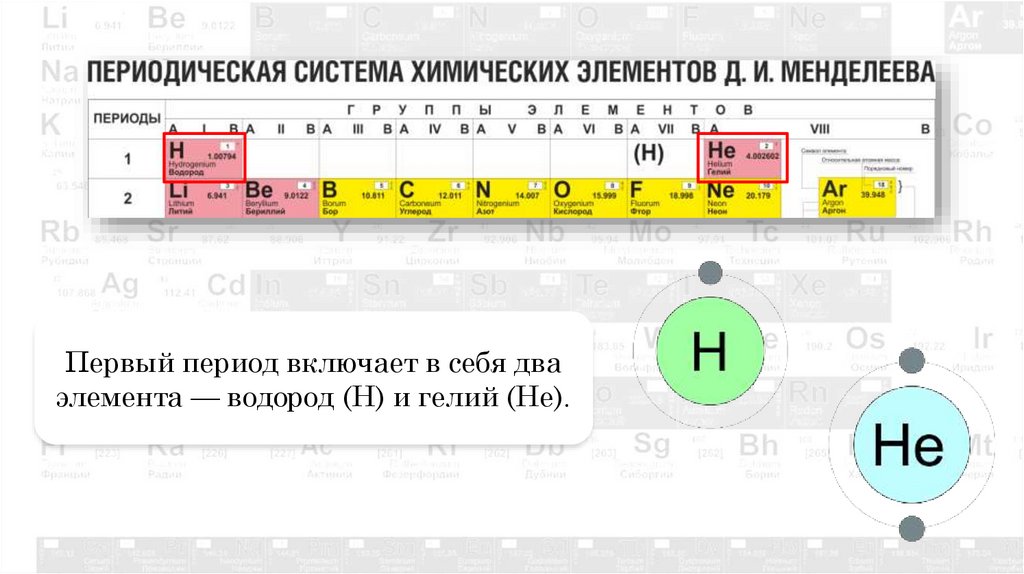
Первый период включает в себя дваэлемента — водород (Н) и гелий (Не).
13.
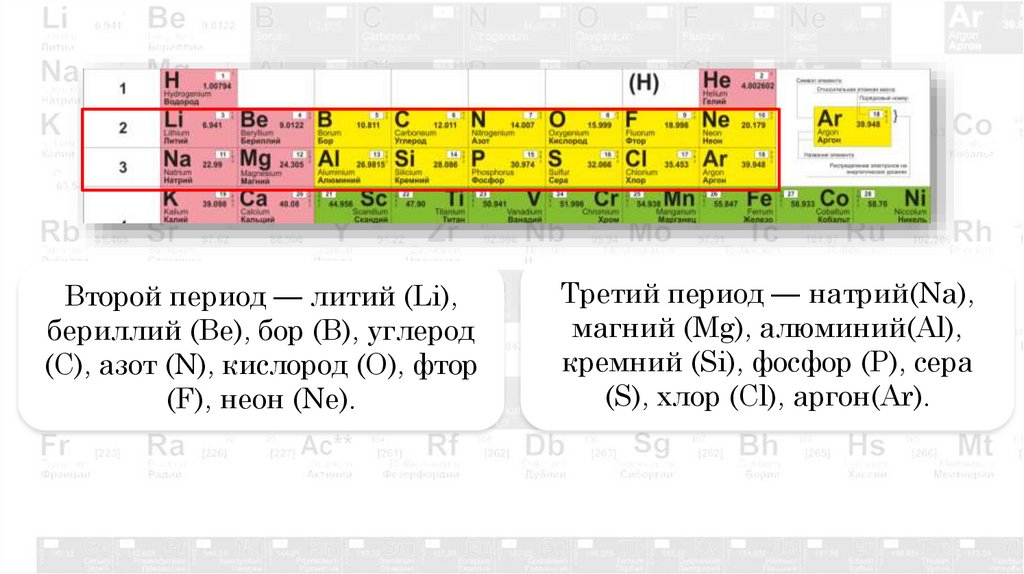
Второй период — литий (Li),бериллий (Be), бор (B), углерод
(C), азот (N), кислород (O), фтор
(F), неон (Ne).
Третий период — натрий(Na),
магний (Mg), алюминий(Al),
кремний (Si), фосфор (P), сера
(S), хлор (Cl), аргон(Ar).
14.
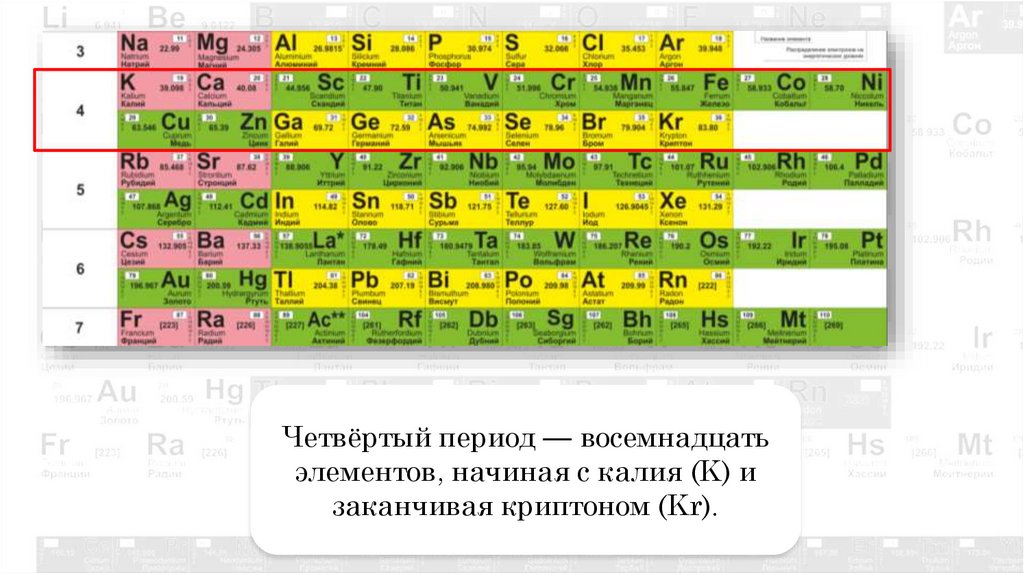
Четвёртый период — восемнадцатьэлементов, начиная с калия (K) и
заканчивая криптоном (Kr).
15.
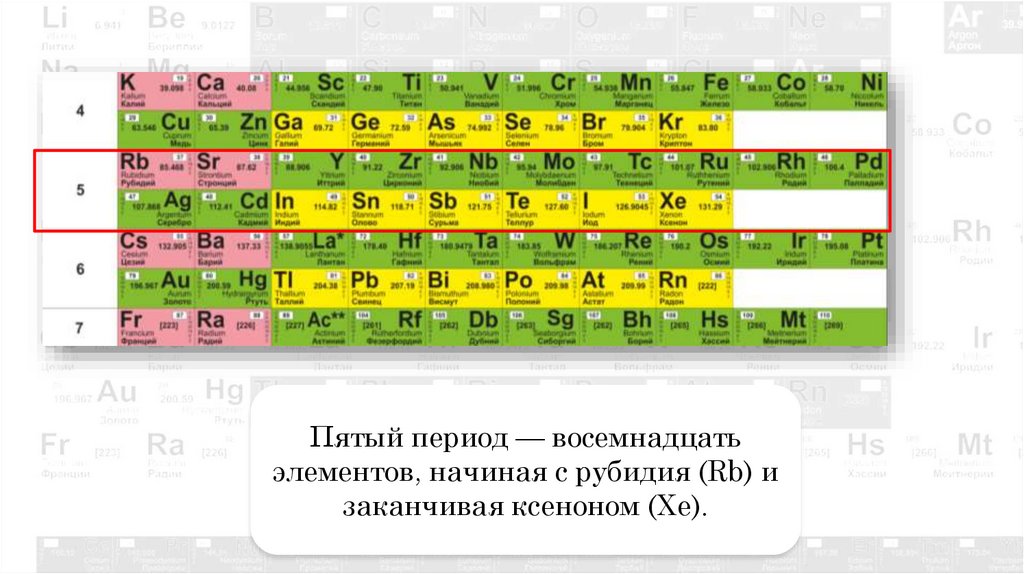
Пятый период — восемнадцатьэлементов, начиная с рубидия (Rb) и
заканчивая ксеноном (Xe).
16.
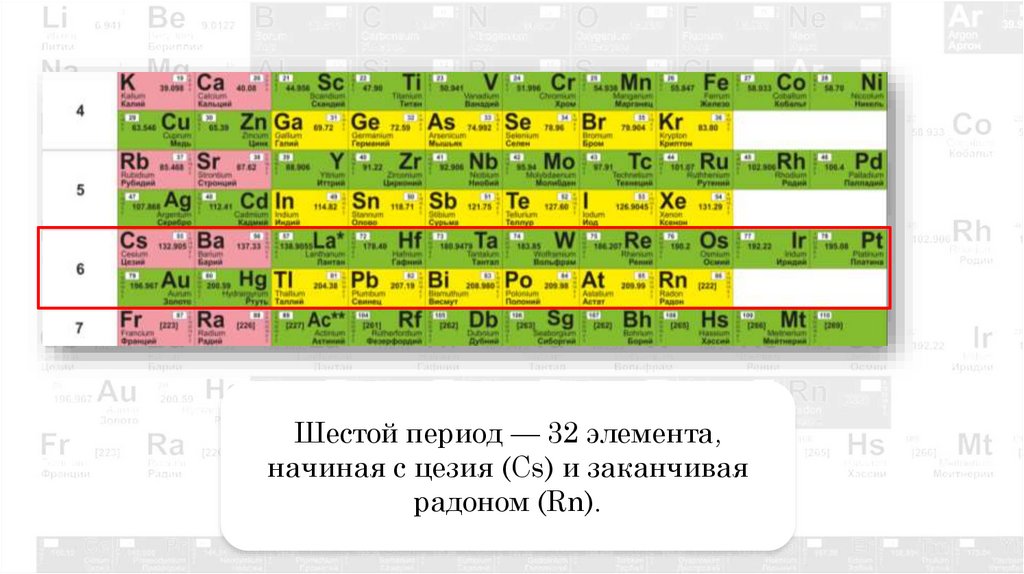
Шестой период — 32 элемента,начиная с цезия (Cs) и заканчивая
радоном (Rn).
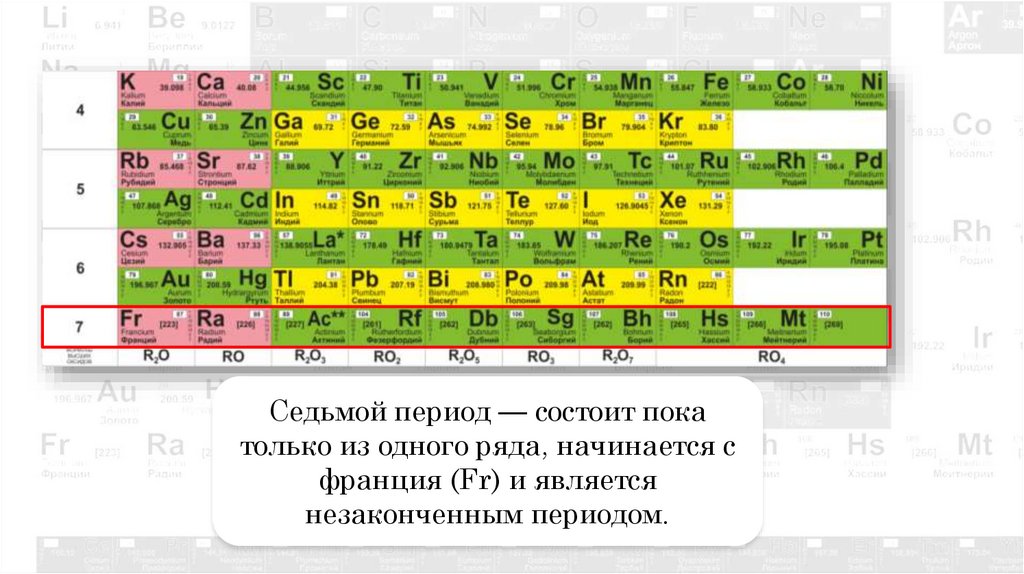
17.
Седьмой период — состоит покатолько из одного ряда, начинается с
франция (Fr) и является
незаконченным периодом.
18.
Лантаноиды и актиноиды19.
Группы элементовГруппа делится
на главную
подгруппу А и
побочную
подгруппу В.
20.
Группы элементовВ главную
подгруппу II
(второй) группы
(IIА группа) входят:
бериллий (Be),
магний (Mg),
кальций (Ca),
стронций (Sr),
барий (Ba),
радий (Ra).
21.
Группы элементовПобочная
подгруппа этой
группы (IIB группа)
включает:
цинк (Zn),
кадмий (Cd),
ртуть (Hg).
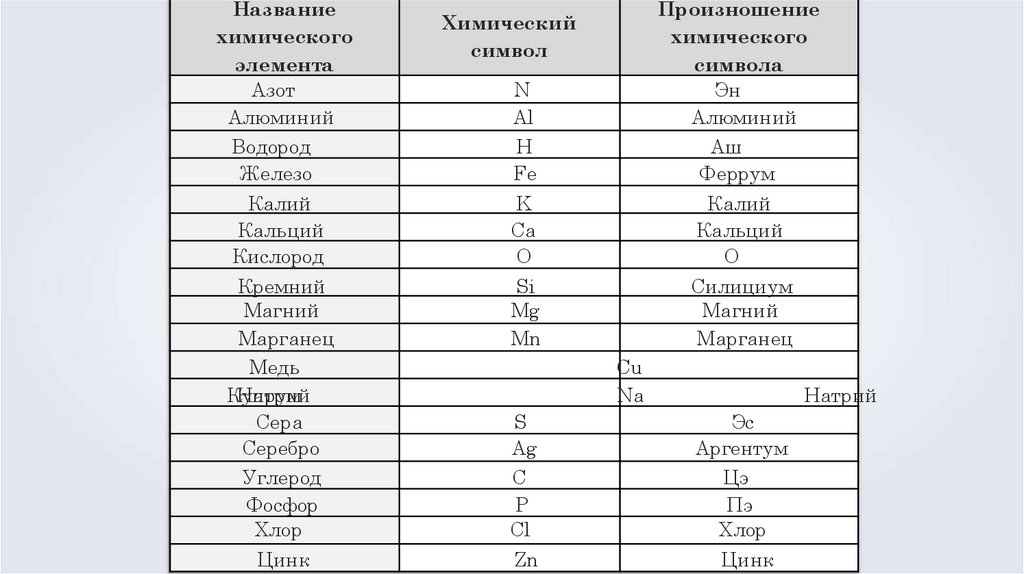
22.
Названиехимического
элемента
Азот
Алюминий
Водород
Железо
N
Al
H
Fe
Произношение
химического
символа
Эн
Алюминий
Аш
Феррум
K
Ca
O
Si
Mg
Mn
Калий
Кальций
O
Силициум
Магний
Марганец
Химический
символ
Калий
Кальций
Кислород
Кремний
Магний
Марганец
Медь
Купрум
Натрий
Сера
Сера
Серебро
Углерод
Фосфор
Хлор
SS
Ag
C
P
Cl
Эс
Эс
Аргентум
Цэ
Пэ
Хлор
Цинк
Zn
Цинк
Cu
Na
Натрий
23.
24.
25.
Относительная атомная массаАтомы элементов характеризуются
определённой (только им присущей)
массой.
Например, масса
атома Н - 1,67 · 10−23 г,
атома С −1,995 · 10−23 г,
атома О − 2,66 · 10−23 г.
26. Относительная атомная масса
• Масса молекул и атомов очень мала, поэтому ими неудобно, да иневозможно пользоваться. Невозможно взять для эксперимента 10 молекул
кислорода и взвесить их на школьных весах.
• Масса атома кислорода в кг равна 2,6667 · 10-23кг, т.е. 23 нуля после
запятой. m(H) = 0,1674 · 10-23кг. Поэтому для микромира используют особую
единицу измерения.
• Определим отношение атомных масс водорода и углерода:
1,993 10 23 г
= 12
0,1674 10 23 г
• Масса углерода в 12 раз больше массы водорода. Масса водорода составляет
1\ 12 массы углерода. И наоборот масса углерода составляет 12
относительно атомной массы водорода:
• Относительная атомная масса элемента – это величина,
показывающая, во сколько раз масса атома элемента больше 1/12
массы атома углерода.
27.
Относительная атомная массаОпределите относительные атомные массы следующих химических элементов:
Ar(H) =
Ar (N) =
Ar (Ne) =
Ar (B) =
28.
Параграф 6. упр.№4 письменно. Таблицу на странице 36 переписать втетрадь. Выучить все химические элементы, символы и их произношение диктант. Уметь определять координаты химических элементов по
Периодической системе химических элементов, а также относительную
атомную массу у элемента.
1) Определите атомную массу:
а) Ar (Li) =
б) Ar (C) =
в) Ar (O) =

















 Химия
Химия








