Похожие презентации:
Спектрофотометрические методы исследования
1.
Карагандинский медицинский университетСпектрофотометрические методы исследования.
Кафедра информатики и биостатистики
Ассистент профессор Коршуков И.В.
2.
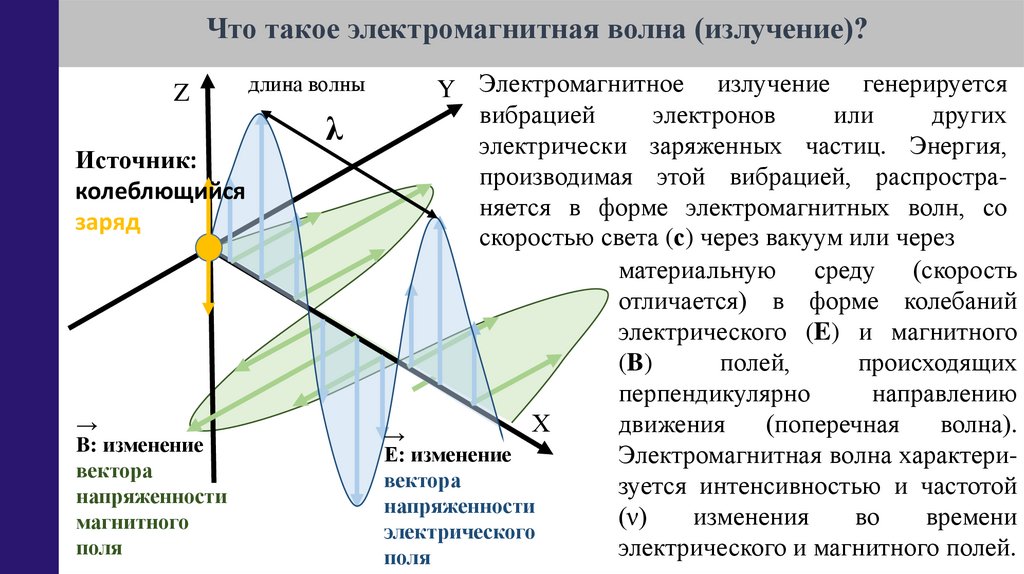
Что такое электромагнитная волна (излучение)?Z
Источник:
колеблющийся
заряд
→
B: изменение
вектора
напряженности
магнитного
поля
длина волны
λ
Y Электромагнитное излучение генерируется
вибрацией
электронов
или
других
электрически заряженных частиц. Энергия,
производимая этой вибрацией, распространяется в форме электромагнитных волн, со
скоростью света (с) через вакуум или через
материальную среду (скорость
отличается) в форме колебаний
электрического (E) и магнитного
(B)
полей,
происходящих
перпендикулярно
направлению
Х
движения
(поперечная
волна).
→
Е: изменение
Электромагнитная волна характеривектора
зуется интенсивностью и частотой
напряженности
(ν)
изменения
во
времени
электрического
электрического и магнитного полей.
поля
3.
Что такое электромагнитная волна (излучение)?Z
длина волны
Источник:
колеблющийся
заряд
λ
Y
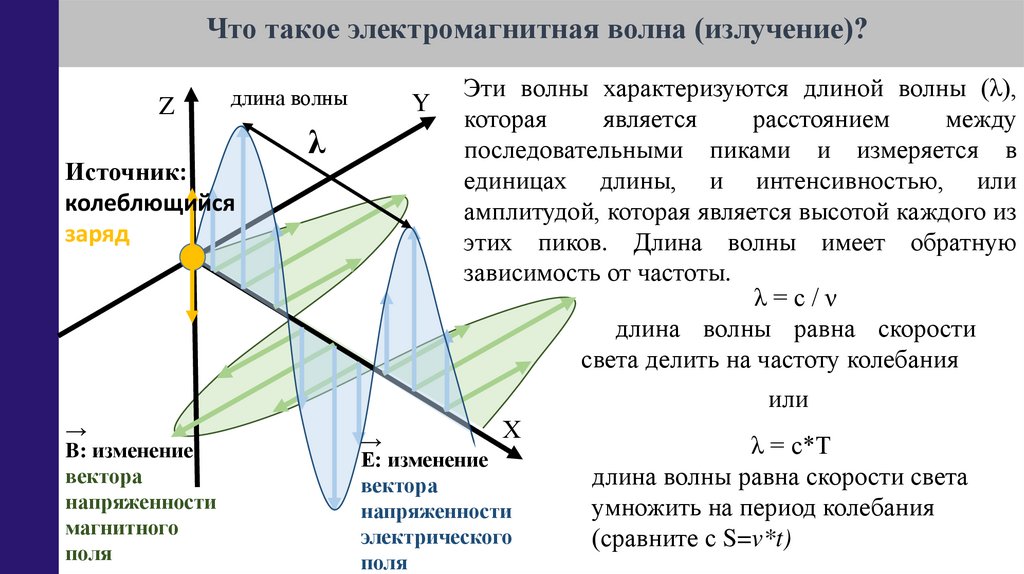
Эти волны характеризуются длиной волны (λ),
которая
является
расстоянием
между
последовательными пиками и измеряется в
единицах длины, и интенсивностью, или
амплитудой, которая является высотой каждого из
этих пиков. Длина волны имеет обратную
зависимость от частоты.
λ=с/ν
длина волны равна скорости
света делить на частоту колебания
или
→
B: изменение
вектора
напряженности
магнитного
поля
Х
→
Е: изменение
вектора
напряженности
электрического
поля
λ = с*Т
длина волны равна скорости света
умножить на период колебания
(сравните с S=v*t)
4.
Что такое электромагнитная волна (излучение)?В квантовой физике существует понятие корпускулярно-волнового дуализма:
электромагнитное излучение это:
• распространяющееся возмущение электромагнитного поля (волновая природа)
и
• поток дискретных частиц - фотонов (квантов энергии) (корпускулярная природа).
Фотоны - это пакеты энергии E=h*ν (уравнение Планка-Эйнштейна), которые
движутся со скоростью света. Фотоны с одинаковой энергией h*ν все одинаковы, и
значение их плотности соответствует интенсивности излучения. Электромагнитное
излучение взаимодействует с заряженными частицами в атомах, молекулах и более
крупных объектах материи. Эти явления, а также способы создания и наблюдения
электромагнитного излучения, и его технологические применения зависят от его
частоты ν.
5.
Некоторые характеристики и свойства электромагнитных волнОбщие свойства
Электромагнитные волны относятся множеству волн с общими свойствами,
называемого электромагнитным спектром. Все электромагнитные волны:
• являются поперечными волнами;
• могут распространяться в вакууме;
• движутся в вакууме с одинаковой скоростью (скоростью света, 300 000 000 м/с.)
Как и все волны, электромагнитные волны:
• переносят энергию из одного места в другое;
• могут отражаться;
• могут преломляться.
Различия
Каждый тип волны в электромагнитном спектре
имеет различную:
• длину волны (частоту)
Характеристики волн:
Частота ν (обратна периоду
Т)
Фаза θ
Ориентация плоскости в
которой осуществляются
колебания
Длина волны λ
Энергия кванта Е
6.
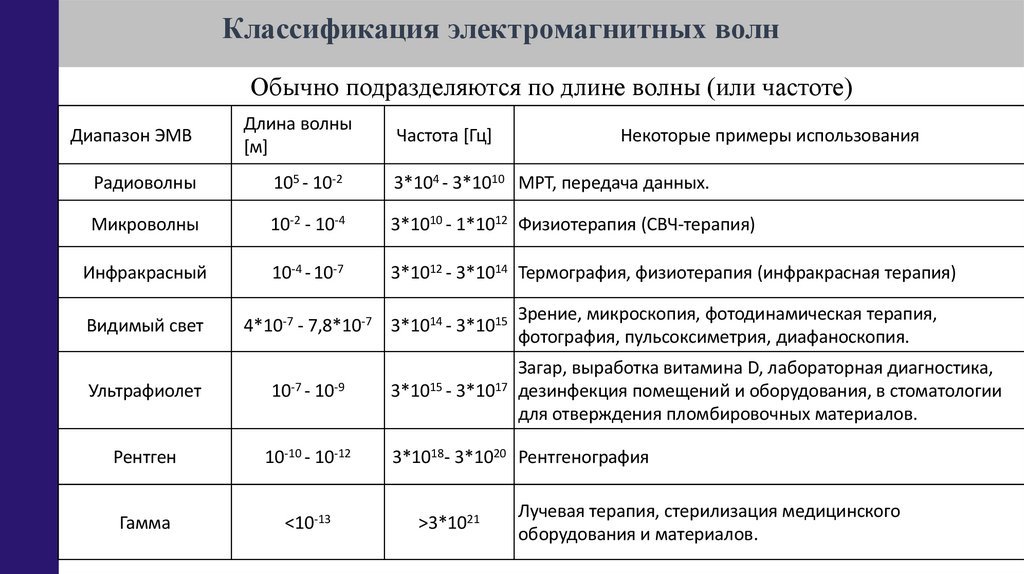
Классификация электромагнитных волнОбычно подразделяются по длине волны (или частоте)
Диапазон ЭМВ
Длина волны
[м]
Радиоволны
105 - 10-2
3*104 - 3*1010 МРТ, передача данных.
Микроволны
10-2 - 10-4
3*1010 - 1*1012 Физиотерапия (СВЧ-терапия)
Инфракрасный
10-4 - 10-7
3*1012 - 3*1014 Термография, физиотерапия (инфракрасная терапия)
Видимый свет
Частота [Гц]
4*10-7 - 7,8*10-7 3*1014 - 3*1015
Некоторые примеры использования
Зрение, микроскопия, фотодинамическая терапия,
фотография, пульсоксиметрия, диафаноскопия.
Ультрафиолет
10-7 - 10-9
Загар, выработка витамина D, лабораторная диагностика,
3*1015 - 3*1017 дезинфекция помещений и оборудования, в стоматологии
для отверждения пломбировочных материалов.
Рентген
10-10 - 10-12
3*1018- 3*1020 Рентгенография
Гамма
<10-13
>3*1021
Лучевая терапия, стерилизация медицинского
оборудования и материалов.
7.
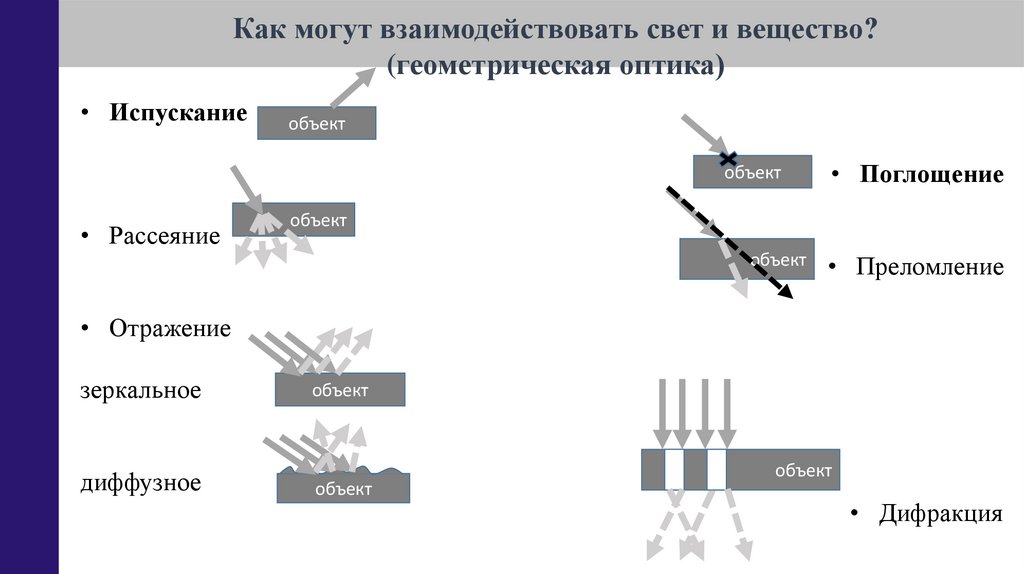
Как могут взаимодействовать свет и вещество?(геометрическая оптика)
• Испускание
объект
объект
• Рассеяние
• Поглощение
объект
объект
• Преломление
• Отражение
зеркальное
диффузное
объект
объект
объект
• Дифракция
8.
Электронные переходыПоложение каждого электрона в атоме характеризуется набором квантовых чисел.
Для каждого электрона набор этих чисел уникален.
Набор квантовых чисел определяет запас энергии электрона.
При излучении создается электромагнитная волна (фотон), которая уносит из
вещества порцию энергии (квант энергии): E=h*ν
Общий запас энергии для электрона в основном состоянии минимален и не может
быть снижен: излучение кванта невозможно, но возможно поглощение кванта.
Квант обладает свойствами: неделимость (нельзя получить половинку кванта) и
дискретностью (принимает одно из фиксированных значений).
При поглощении: электромагнитная волна передает квант энергии электрону (в
составе атома или молекулы), который переходит в возбужденное (нестабильное)
состояние (обладает избытком энергии).
9.
Энергетические уровни и электронные переходыиспускание
поглощение
испускание
поглощение
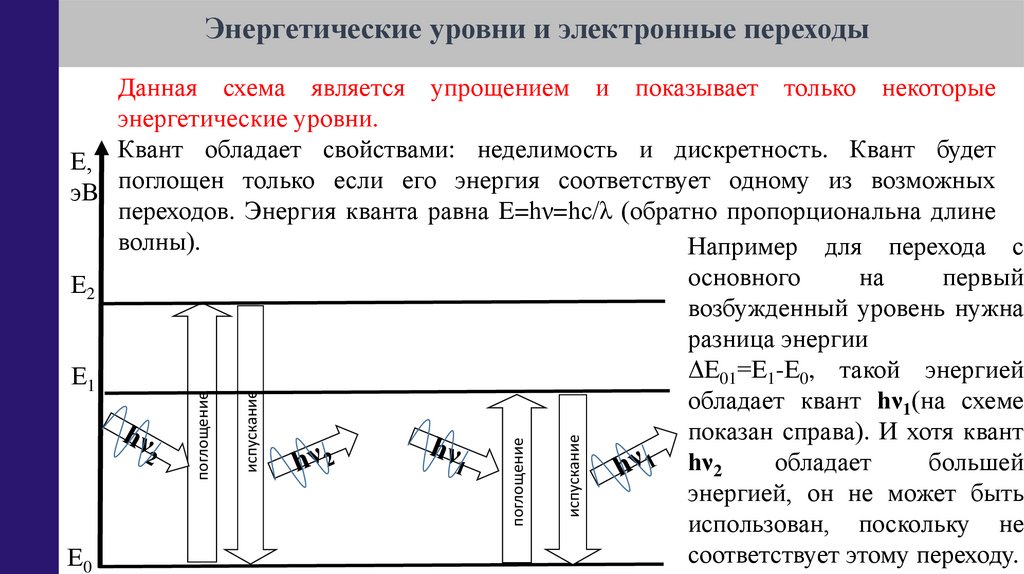
Данная схема является упрощением и показывает только некоторые
энергетические уровни.
Е, Квант обладает свойствами: неделимость и дискретность. Квант будет
эВ поглощен только если его энергия соответствует одному из возможных
переходов. Энергия кванта равна E=hν=hс/λ (обратно пропорциональна длине
волны).
Например для перехода с
основного
на
первый
Е2
возбужденный уровень нужна
разница энергии
ΔЕ01=Е1-Е0, такой энергией
Е1
обладает квант hν1(на схеме
показан справа). И хотя квант
hν2
обладает
большей
энергией, он не может быть
использован, поскольку не
соответствует этому переходу.
Е0
10.
Что такое испускание (излучение) ЭМВ??Процесс, посредством которого материя высвобождает энергию в форме
электромагнитного излучения. Это происходит, когда энергия внутри атомов, молекул или
частиц материала высвобождается после события возбуждения, вызывая излучение
электромагнитных волн в различных областях спектра,
Спонтанное излучение: когда атом, ион или молекула переходит из более высокого
энергетического состояния в более низкое (например, когда возбужденный электрон
падает на более низкую орбиталь), он спонтанно испускает фотон.
Вынужденное излучение: когда фотон определенной энергии взаимодействует с
возбужденным атомом или молекулой, он может вызвать высвобождение другого фотона
с той же фазой, направлением и энергией. Этот процесс является основой работы лазера
(усиление света путем вынужденного излучения).
Тепловое излучение: когда материал нагревается, его частицы вибрируют и колеблются,
испуская излучение. Количество и длина волны излучения зависят от температуры.
Например, объект, раскаленный докрасна или добела из-за тепла, является обычным
примером теплового излучения.
Длина волны и частота испускаемых электромагнитных волн зависят от разницы энергий
между состояниями частиц в веществе.
11.
Что такое поглощение??Процесс, посредством которого вещество (например, газы, жидкости или твердые
тела) получает энергию от электромагнитных волн (ЭМВ), проходящих через него
или взаимодействующих с ним.
Во время этого процесса энергия ЭМВ передается атомам, молекулам или частицам
внутри вещества, вызывая различные изменения, такие как:
Электронные переходы: электроны в веществе могут поглощать энергию и
переходить на более высокие энергетические уровни.
Колебательные и вращательные переходы: в молекулах поглощение энергии может
приводить к колебаниям или вращениям связей между атомами.
Тепловое возбуждение: поглощенная энергия также может увеличивать
кинетическую энергию частиц, повышая температуру материала.
Количество и способ поглощения зависят от частоты (или длины волны)
электромагнитной волны и свойств материала. Различные материалы поглощают
электромагнитные волны на разных частотах
12.
Простое (монохроматическое) и сложное излучениеЦвет это субъективное восприятие человеком ЭМВ определенной длины волны,
Монохроматическое излучение (моно–один+хромос–цвет) – ЭМИ в котором
представлены волны с одной длиной волны, также может использоваться термин
«простое излучение». Например ЭМИ с длиной волны 555 нм будет
восприниматься как зеленый цвет.
Полихроматическое излучение (поли–множество+хромос–цвет) – ЭМИ в котором
представлены волны с различными длинами волн, также может использоваться
термин «сложное излучение». Например ЭМИ в составе которого есть все длины
волн от 380 до 760 нм (границы видимого диапазона) будет восприниматься как
белый цвет. Черный цвет означает отсутствие всех длин волн видимого света.
13.
Спектральный анализ - исследование спектраПо получаемым результатам:
Спектро+скопия – наблюдение спектров глазом без фиксации результата.
Спектро+графия – получаемый спектр фиксируется, например в виде фотографии.
В настоящее время используются фотодатчики, чувствительные к длинам волн
изучаемого спектра.
По механизму получения спектра:
Эмиссионный (испускание) – подходит для простых, термостабильных веществ
Абсорбционнный (поглощение) – подходит для сложных органических молекул
14.
Спектральный анализ - исследование спектраПо целям:
Качественный – по измеренным величины поглощения (на всех длинах волн),
составить кривую (профиль) и сравнить ее с уже известными веществами для
идентификации неизвестного вещества в образце. Отвечает на вопрос – какое
именно вещество представлено в образце.
Количественный (спектрометрия) – по измеренной величине поглощения (при
данной длине волны) и известному спектру (для исследуемого вещества)
поглощения определить концентрацию вещества в растворе (закон БугераЛамберта-Бера). Отвечает на вопрос – какова концентрация данного вещества
представленного в образце.
15.
Пламенный (эмиссионный) спектроскопКлючевым событием является излучение электромагнитных волны нагретым в
пламени образцом. Поскольку требуется нагрев до высоких температур то
большинство молекул распадается на составляющие атомы, которые испускают
длины волн характерные для строения энергетических уровней соответствующего
вида атомов.
Яркость излучения (количество волн испущенных объектом) зависит не только от
количества атомов. Поэтому количественный анализ затруднен и может
выполняться лишь сравнивая исследуемый образец со стандартными образцами
(для которых известна концентрация исследуемых атомов). Применяется например
в металлургии для определения состава сплавов, в геологии для определения
состава минералов.
Преимуществом является высокая чувствительность метода, позволяющая
обнаруживать количества вещества измеряемое микрограммами. Например это
позволяет использовать метод в судебной медицине для обнаружения следовых
количеств тяжелых металлов.
16.
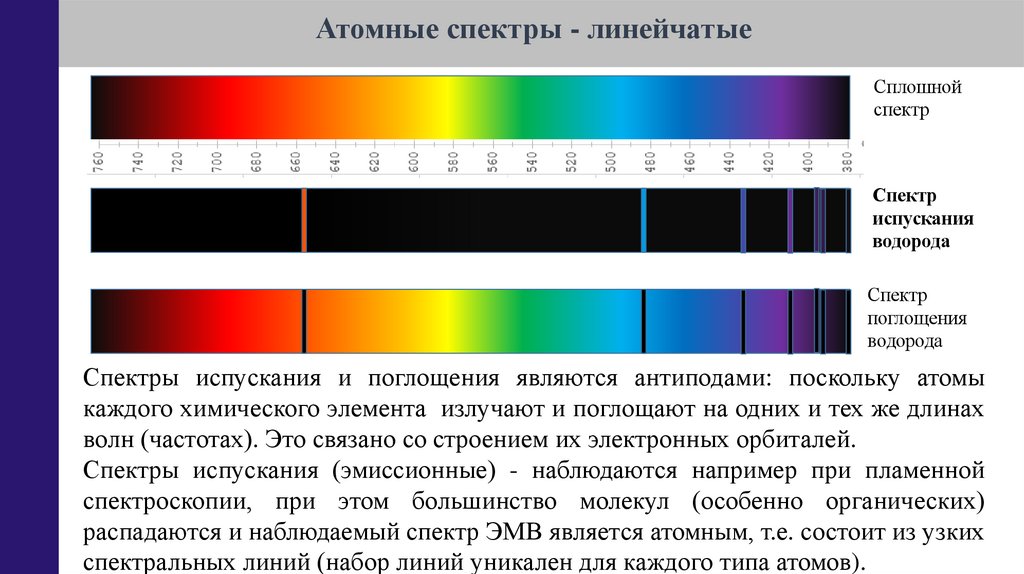
Атомные спектры - линейчатыеСплошной
спектр
Спектр
испускания
водорода
Спектр
поглощения
водорода
Спектры испускания и поглощения являются антиподами: поскольку атомы
каждого химического элемента излучают и поглощают на одних и тех же длинах
волн (частотах). Это связано со строением их электронных орбиталей.
Спектры испускания (эмиссионные) - наблюдаются например при пламенной
спектроскопии, при этом большинство молекул (особенно органических)
распадаются и наблюдаемый спектр ЭМВ является атомным, т.е. состоит из узких
спектральных линий (набор линий уникален для каждого типа атомов).
17.
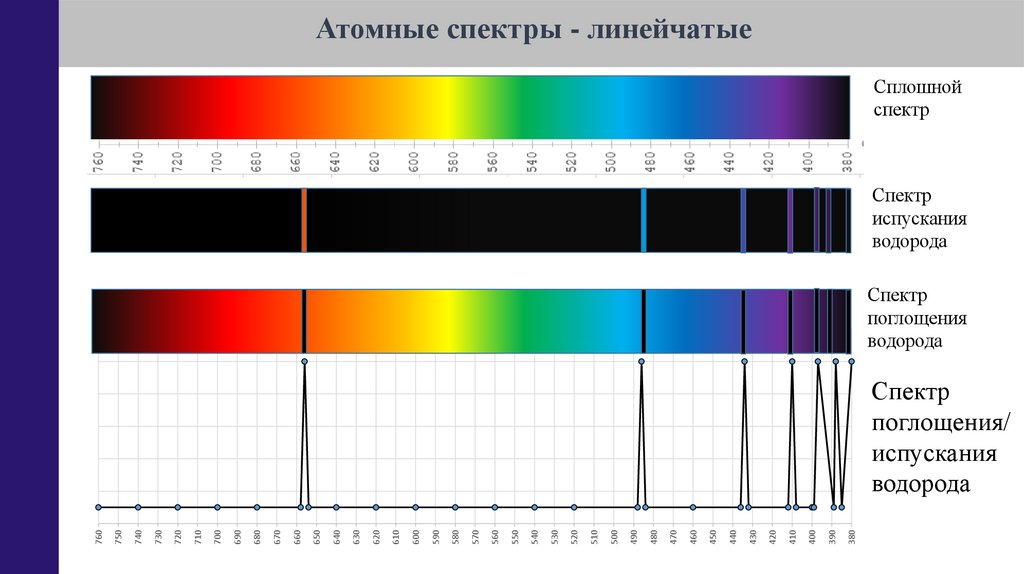
Атомные спектры - линейчатыеСплошной
спектр
Спектр
испускания
водорода
Спектр
поглощения
водорода
380
390
400
410
420
430
440
450
460
470
480
490
500
510
520
530
540
550
560
570
580
590
600
610
620
630
640
650
660
670
680
690
700
710
720
730
740
750
760
Спектр
поглощения/
испускания
водорода
18.
Пламенный (эмиссионный) спектроскопИсторически для первых опытов по наблюдению спектров (излучения)
призменный спектроскоп, состоящий из двух трубок с линзами: коллиматора и
зрительной трубки. Между ними установлена призма, которая преломляет лучи с
различной длиной волны под разными углами (дисперсия света), что позволяет
разделить их. На выходе из зрительной трубки имеется окулярная линза, в которой
можно наблюдать глазом спектральные линии. С помощью системы винтов угол
между трубками можно менять (либо положение призмы) и наблюдать различные
части спектра. Сопоставляя наблюдаемые спектральные линии с известными
спектрами атомов можно идентифицировать атомный состав образца.
https://www.spbmuseum.ru/funds/140/4933/
19.
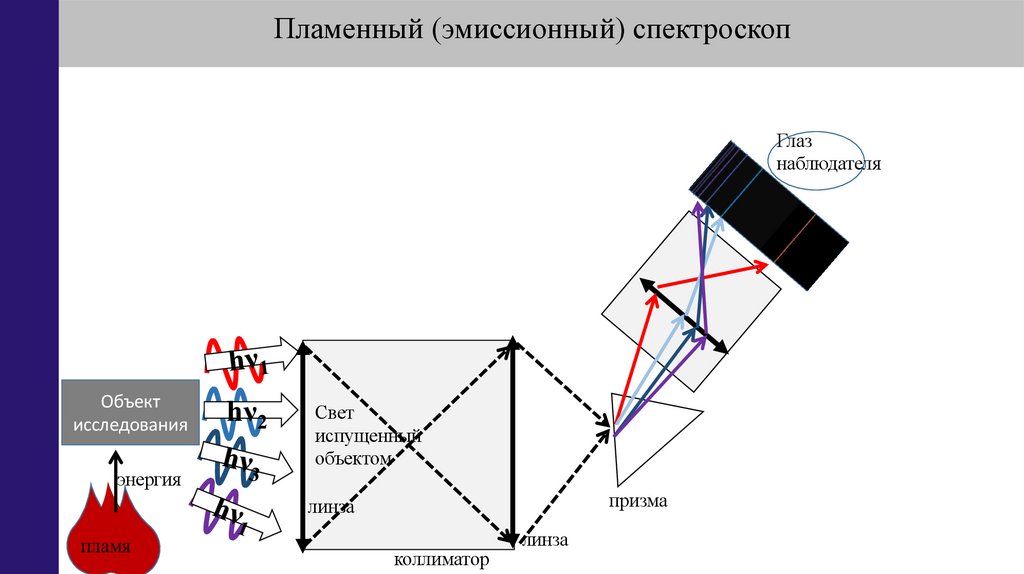
Пламенный (эмиссионный) спектроскопГлаз
наблюдателя
Объект
исследования
энергия
hν2
Свет
испущенный
объектом
призма
линза
пламя
коллиматор
линза
20.
Молекулярные спектры - полосатыеМолекулярные спектры более сложные (чем
атомные) и не являются простой комбинацией
атомных спектров атомов составляющих
молекулу.
Кроме
переходов
электронов
между
энергетическими
уровнями
в
молекуле
происходят колебания ядер атомов входящих в
молекулу, а так же вращение самой молекулы.
Общий запас энергии в молекуле складывается
из этих трех составляющих:
• электронной
• колебательной
• вращательной энергии.
(Эйдельман, Е. Д. Физика с элементами биофизики. 2023г.)
21.
Величины количественно характеризующие поглощениеИнтенсивность излучения (I) - поток энергии, переносимый излучением через
единичную площадь в единицу времени. Для монохроматического излучения можно
упростить – число волн в потоке.
Пропускание (или коэффициент пропускания T - transmittance) - доля падающего
излучения (чаще всего света) которая прошла через исследуемый образец. Доля означает
дробь, в числителе которой интенсивность излучения после образца I а в знаменателе
интенсивность до образца I0.
T= I/I0
Оптическая плотность (А – absorbance) - способность образца ослаблять (поглощать
или рассеивать) свет. Вычисляется как взятый с обратным знаком десятичный логарифм
от коэффициента пропускания.
A= -lg(T) = -lg(I/I0)
Молярный коэффициент поглощения (молярная экстинкция - extinction) ελ –
оптическая плотность образца с концентрацией 1 моль/л и толщиной слоя в 1 см. Зависит
от строения молекулы и определяется для каждой длины волны света. Чаще всего
график спектра поглощения строят по оси Y откладывая этот коэффициент, а по оси X –
длины волн.
22.
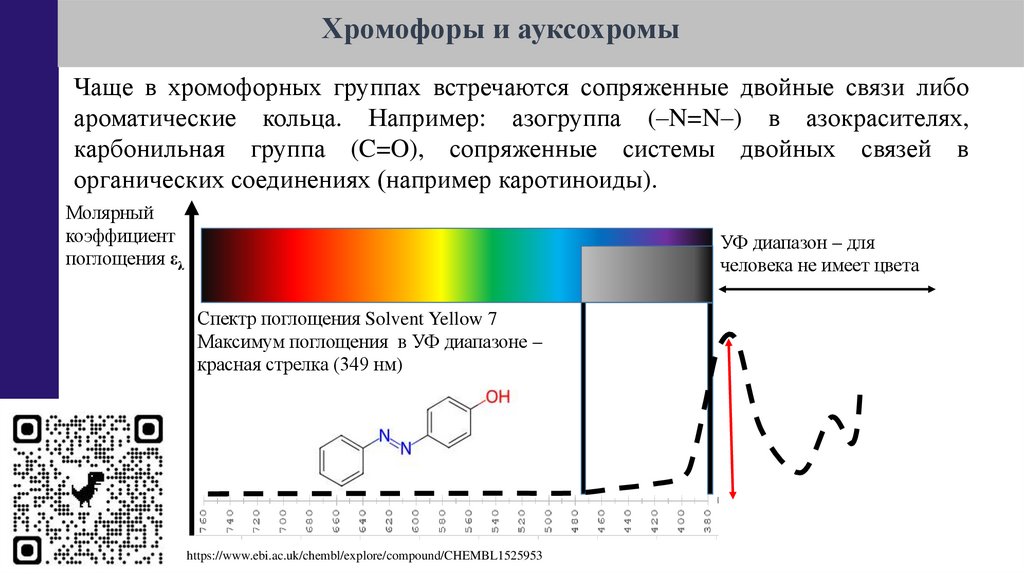
Хромофоры и ауксохромыЧаще в хромофорных группах встречаются сопряженные двойные связи либо
ароматические кольца. Например: азогруппа (–N=N–) в азокрасителях,
карбонильная группа (C=O), сопряженные системы двойных связей в
органических соединениях (например каротиноиды).
Молярный
коэффициент
поглощения ελ
УФ диапазон – для
человека не имеет цвета
Спектр поглощения Solvent Yellow 7
Максимум поглощения в УФ диапазоне –
красная стрелка (349 нм)
https://www.ebi.ac.uk/chembl/explore/compound/CHEMBL1525953
23.
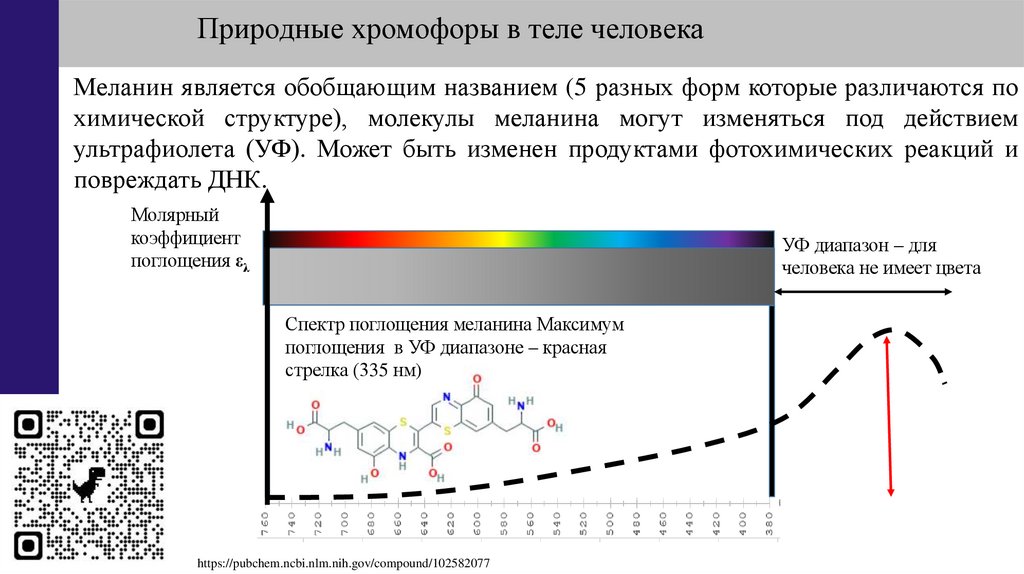
Природные хромофоры в теле человекаМеланин является обобщающим названием (5 разных форм которые различаются по
химической структуре), молекулы меланина могут изменяться под действием
ультрафиолета (УФ). Может быть изменен продуктами фотохимических реакций и
повреждать ДНК.
Молярный
коэффициент
поглощения ελ
УФ диапазон – для
человека не имеет цвета
Спектр поглощения меланина Максимум
поглощения в УФ диапазоне – красная
стрелка (335 нм)
https://pubchem.ncbi.nlm.nih.gov/compound/102582077
24.
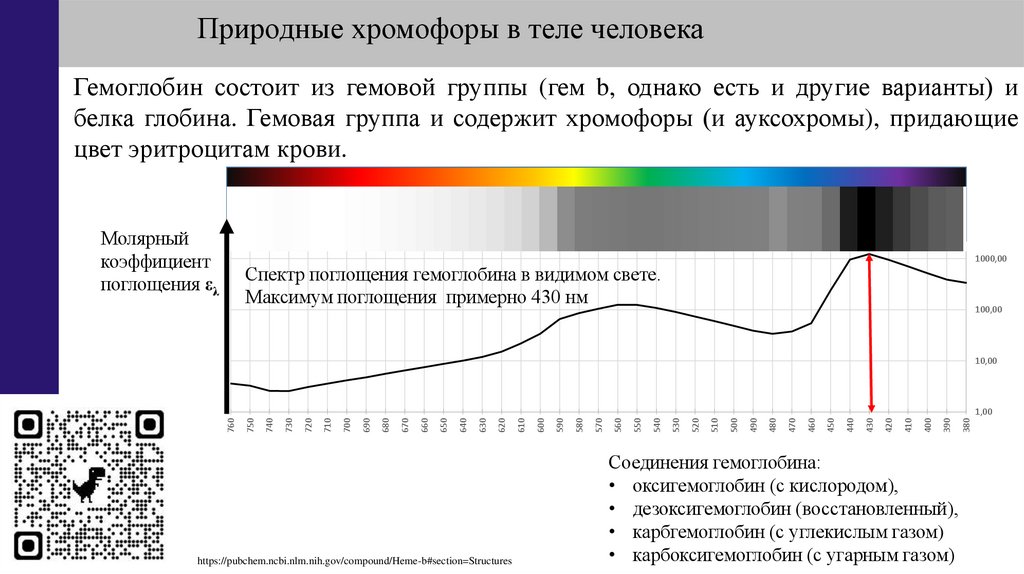
Природные хромофоры в теле человекаГемоглобин состоит из гемовой группы (гем b, однако есть и другие варианты) и
белка глобина. Гемовая группа и содержит хромофоры (и ауксохромы), придающие
цвет эритроцитам крови.
HB
Молярный
коэффициент
поглощения ελ
1000,00
Спектр поглощения гемоглобина в видимом свете.
Максимум поглощения примерно 430 нм
100,00
10,00
https://pubchem.ncbi.nlm.nih.gov/compound/Heme-b#section=Structures
Соединения гемоглобина:
• оксигемоглобин (с кислородом),
• дезоксигемоглобин (восстановленный),
• карбгемоглобин (с углекислым газом)
• карбоксигемоглобин (с угарным газом)
380
390
400
410
420
430
440
450
460
470
480
490
500
510
520
530
540
550
560
570
580
590
600
610
620
630
640
650
660
670
680
690
700
710
720
730
740
750
760
1,00
25.
Абсорбционная спектроскопияГлавное событие – это поглощение электромагнитных волн с
определёнными частотами (длинами волн, энергией кванта) молекулами
исследуемого образца. Величина энергии ЭМ волн (квантов) должна совпадать с
энергией переходов между энергетическими уровнями существующими в данной
молекуле. Набор длин волн которые данное вещество поглощает называется
спектром поглощения.
Если энергия падающей ЭМ волны (кванта) не совпадает со строением
уровней молекулы то такая ЭМ волна пройдет через молекулу вещества – это
явление пропускания. Набор длин волн которые данное вещество пропускает
называется спектром пропускания.
Состав спектров поглощения и пропускания определяется химическим строением
молекулы данного вещества и является уникальным для каждого типа молекул.
Определение спектра поглощения является одним из первых этапов исследования
вещества. К настоящему времени спектры поглощения известны и
каталогизированы для огромного числа биологических молекул, что позволяет
идентифицировать их.
26.
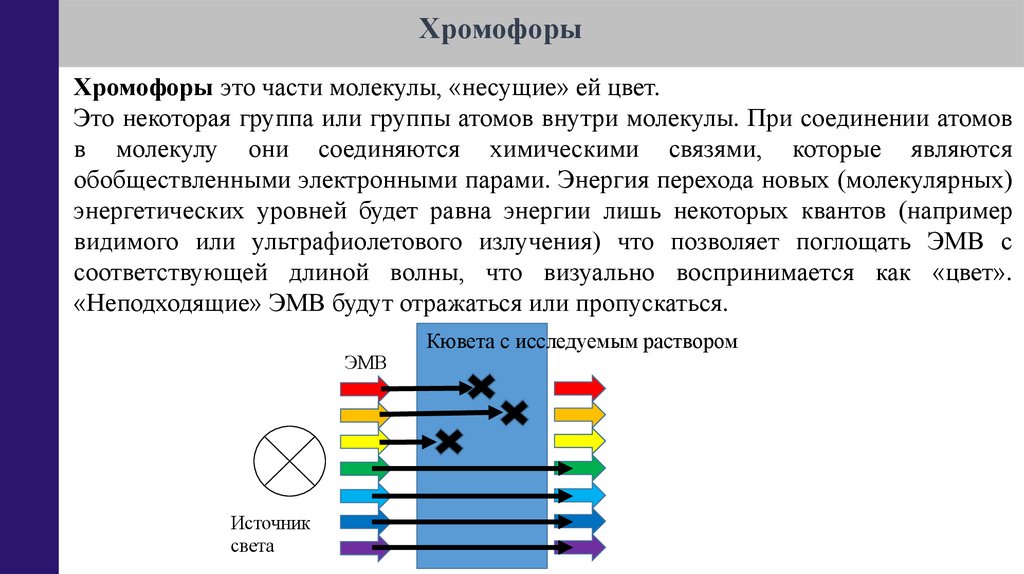
ХромофорыХромофоры это части молекулы, «несущие» ей цвет.
Это некоторая группа или группы атомов внутри молекулы. При соединении атомов
в молекулу они соединяются химическими связями, которые являются
обобществленными электронными парами. Энергия перехода новых (молекулярных)
энергетических уровней будет равна энергии лишь некоторых квантов (например
видимого или ультрафиолетового излучения) что позволяет поглощать ЭМВ с
соответствующей длиной волны, что визуально воспринимается как «цвет».
«Неподходящие» ЭМВ будут отражаться или пропускаться.
ЭМВ
Источник
света
Кювета с исследуемым раствором
27.
Абсорбционная спектрометрияНабор длин волн которые данное вещество поглощает называется спектром
поглощения. В повседневности это известно как цвет вещества.
Человеческое зрение ограничено лишь видимым диапазоном, а значит не может
представить нам полный спектр поглощения, кроме того невозможна
количественная оценка поглощения. Поэтому в научной и практической
деятельности применяются спектральные приборы спектрометры (метрео-мерять),
работающие в недоступных человеческому глазу диапазонах длин волн (обычно
используется ближний инфракрасный, видимый и ультрафиолетовый диапазоны), а
также позволяющие надежно измерять степень поглощения излучения.
Задачами абсорбционной спектрометрии являются:
Качественный анализ: измерение коэффициента поглощения исследуемого образца
на различных длинах волн, такие данные типично представляются в виде графика
(уникального для каждого вещества), на котором можно выявить максимумы
поглощения (может быть несколько).
Количественный анализ: на выбранной длине волны измерение доли поглощенного
света, зная которую можно рассчитать концентрацию вещества в образце.
28.
Величины количественно характеризующие поглощениеИнтенсивность излучения (I) - поток энергии, переносимый излучением через
единичную площадь в единицу времени. Для монохроматического излучения можно
упростить – число волн в потоке.
Пропускание (или коэффициент пропускания T - transmittance) - доля падающего
излучения (чаще всего света) которая прошла через исследуемый образец. Доля означает
дробь, в числителе которой интенсивность излучения после образца I а в знаменателе
интенсивность до образца I0.
T= I/I0
Оптическая плотность (А – absorbance) - способность образца ослаблять (поглощать
или рассеивать) свет. Вычисляется как взятый с обратным знаком десятичный логарифм
от коэффициента пропускания.
A= -lg(T) = -lg(I/I0)
Молярный коэффициент поглощения (молярная экстинкция - extinction) ελ –
оптическая плотность образца с концентрацией 1 моль/л и толщиной слоя в 1 см. Зависит
от строения молекулы и определяется для каждой длины волны света. Чаще всего
график спектра поглощения строят по оси Y откладывая этот коэффициент, а по оси X –
длины волн.
29.
Закон Бугера-Ламберта-БераИнтенсивность излучения (I) [Вт/м²]
Коэффициент пропускания (T) [безразмерная величина]
T= I/I0
Оптическая плотность (А) [безразмерная величина]
A= -lg(T) = -lg(I/I0)
ελ это молярный коэффициент поглощения [л/(моль* см]
l это толщина образца [см]
c это молярная концентрация образца [моль/л]
A= ελ *c*l
Закон Бугера-Ламберта гласит: «Слой определённой толщины поглощает некоторую
долю падающего монохроматического излучения. При этом доля пропущенного или
поглощенного излучения не зависит от интенсивности падающего излучения.»
Дополняется законом Бера - «Доля поглощенного излучения прямо пропорционально
зависит от числа частиц поглощающего вещества, т.е. концентрации.».
30.
Ограничения закона Бугера-Ламберта-БераИспользуется для
• монохроматического излучения
• растворов с малой концентрацией (малое преломление, а также зависимость
молярного коэффициента поглощения от концентрации линейная)
• истинных растворов т.к. снижение интенсивности проходящего света может
быть вызвано не только поглощением но и рассеянием
• концентрация вещества в растворе не меняется (исследуемое вещество не
распадается и не вступает в реакции под действием падающего излучения)
31.
HB100,00
10,00
1,00
262,18
270,46
285,77
276,45
228,75
149,86
137,57
173,27
211,29
252,26
283,93
313,81
325,51
337,75
390,19
519,29
706,87
947,81
1229,30
961,12
240,21
54,39
37,57
33,84
38,80
48,52
59,94
73,46
90,78
108,35
124,21
125,09
104,82
86,09
65,87
34,13
21,96
15,14
11,97
10,11
8,72
7,50
6,50
5,60
4,77
4,17
3,58
3,08
2,56
2,60
3,27
3,60
3,05
2,50
2,07
1,77
1,67
1,61
1,61
1,61
1,61
1,61
1,64
1,69
1,73
1,77
1,80
1,81
1,78
1,61
1,40
1,22
1,00
0,84
0,66
0,48
1000,00
250
260
270
280
290
300
310
320
330
340
350
360
370
380
390
400
410
420
430
440
450
460
470
480
490
500
510
520
530
540
550
560
570
580
590
600
610
620
630
640
650
660
670
680
690
700
710
720
730
740
750
760
770
780
790
800
810
820
830
840
850
860
870
880
890
900
910
920
930
940
950
960
970
980
990
1000
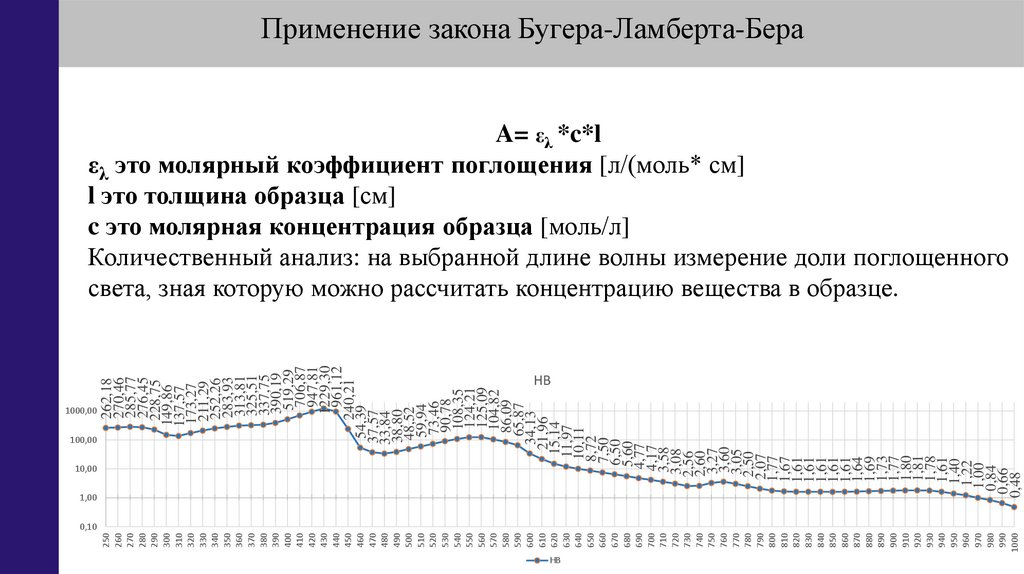
Применение закона Бугера-Ламберта-Бера
A= ελ *c*l
ελ это молярный коэффициент поглощения [л/(моль* см]
l это толщина образца [см]
c это молярная концентрация образца [моль/л]
Количественный анализ: на выбранной длине волны измерение доли поглощенного
света, зная которую можно рассчитать концентрацию вещества в образце.
0,10
HB
32.
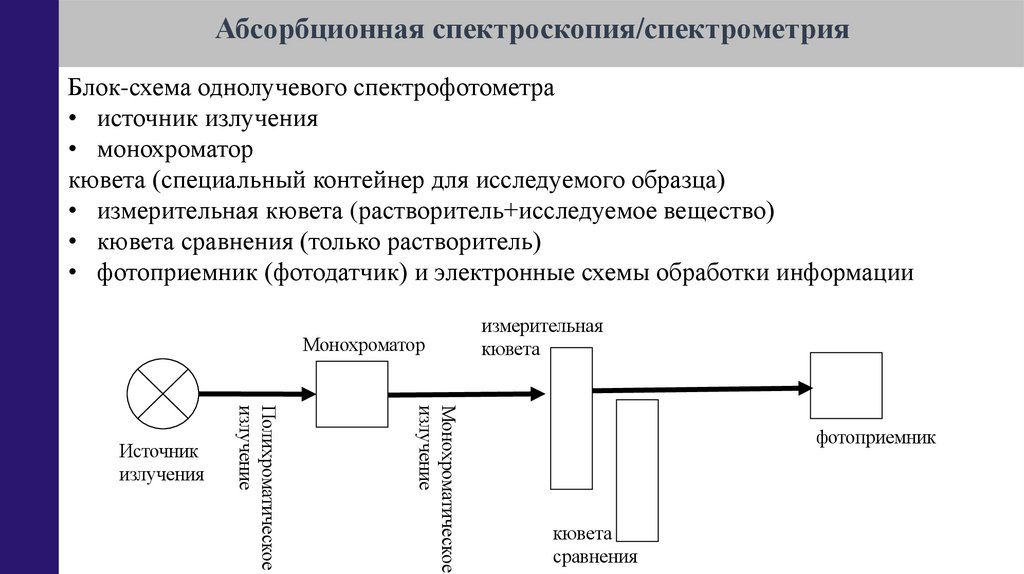
Абсорбционная спектроскопия/спектрометрияБлок-схема однолучевого спектрофотометра
• источник излучения
• монохроматор
кювета (специальный контейнер для исследуемого образца)
• измерительная кювета (растворитель+исследуемое вещество)
• кювета сравнения (только растворитель)
• фотоприемник (фотодатчик) и электронные схемы обработки информации
Монохроматор
Монохроматическое
излучение
Полихроматическое
излучение
Источник
излучения
измерительная
кювета
фотоприемник
кювета
сравнения
33.
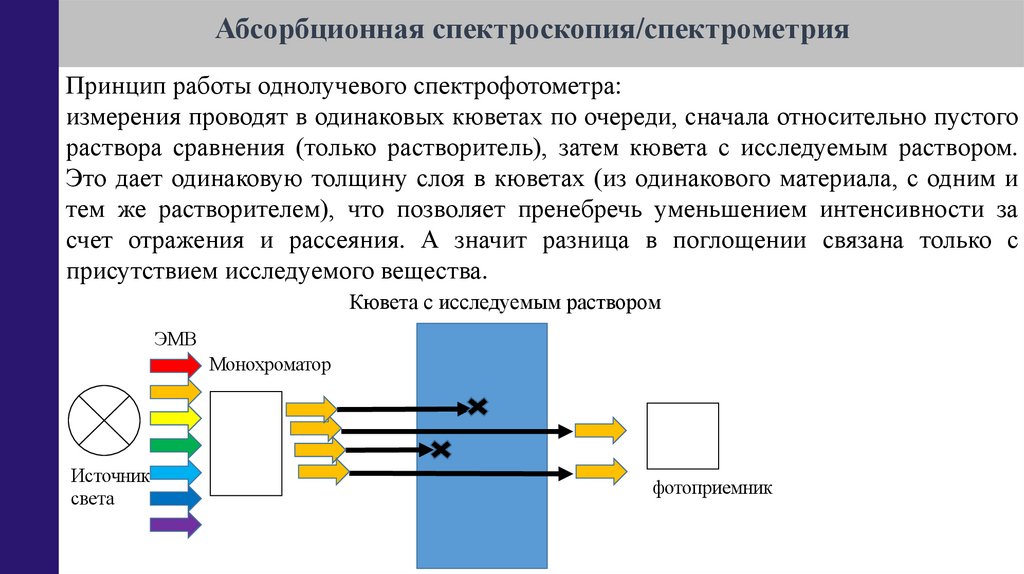
Абсорбционная спектроскопия/спектрометрияПринцип работы однолучевого спектрофотометра:
измерения проводят в одинаковых кюветах по очереди, сначала относительно пустого
раствора сравнения (только растворитель), затем кювета с исследуемым раствором.
Это дает одинаковую толщину слоя в кюветах (из одинакового материала, с одним и
тем же растворителем), что позволяет пренебречь уменьшением интенсивности за
счет отражения и рассеяния. А значит разница в поглощении связана только с
присутствием исследуемого вещества.
Кювета с исследуемым раствором
ЭМВ
Монохроматор
Источник
света
фотоприемник
34.
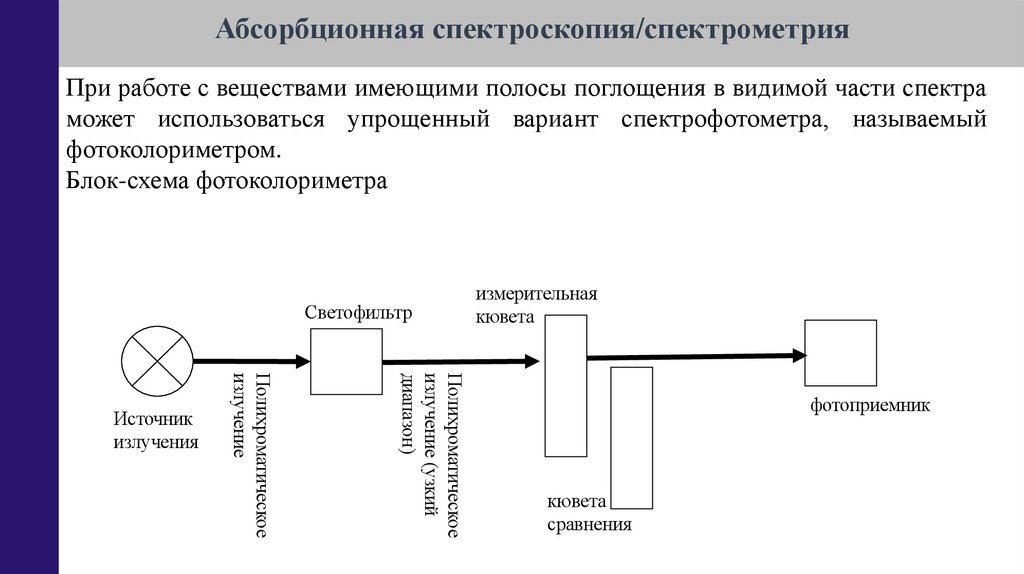
Абсорбционная спектроскопия/спектрометрияПри работе с веществами имеющими полосы поглощения в видимой части спектра
может использоваться упрощенный вариант спектрофотометра, называемый
фотоколориметром.
Блок-схема фотоколориметра
Светофильтр
Полихроматическое
излучение (узкий
диапазон)
Полихроматическое
излучение
Источник
излучения
измерительная
кювета
фотоприемник
кювета
сравнения
35.
250260
270
280
290
300
310
320
330
340
350
360
370
380
390
400
410
420
430
440
450
460
470
480
490
500
510
520
530
540
550
560
570
580
590
600
610
620
630
640
650
660
670
680
690
700
710
720
730
740
750
760
770
780
790
800
810
820
830
840
850
860
870
880
890
900
910
920
930
940
950
960
970
980
990
1000
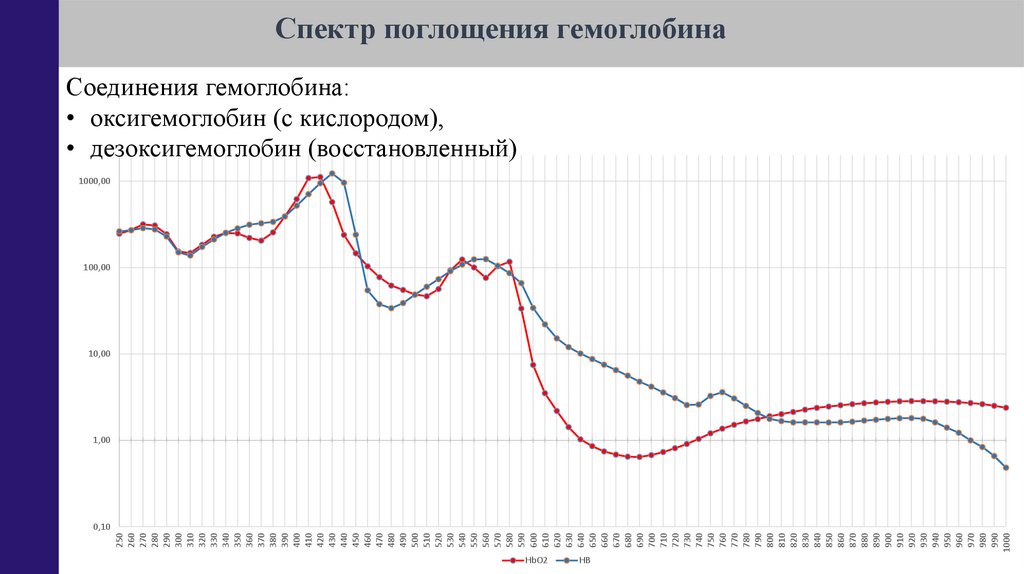
Спектр поглощения гемоглобина
Соединения гемоглобина:
• оксигемоглобин (с кислородом),
• дезоксигемоглобин (восстановленный)
1000,00
100,00
10,00
1,00
0,10
HbO2
HB
36.
250260
270
280
290
300
310
320
330
340
350
360
370
380
390
400
410
420
430
440
450
460
470
480
490
500
510
520
530
540
550
560
570
580
590
600
610
620
630
640
650
660
670
680
690
700
710
720
730
740
750
760
770
780
790
800
810
820
830
840
850
860
870
880
890
900
910
920
930
940
950
960
970
980
990
1000
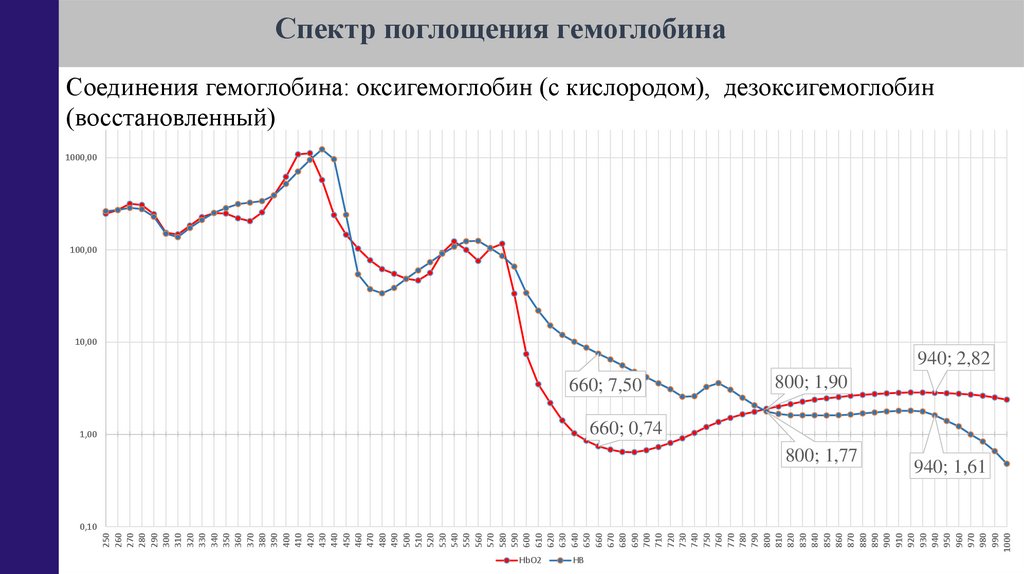
Спектр поглощения гемоглобина
Соединения гемоглобина: оксигемоглобин (с кислородом), дезоксигемоглобин
(восстановленный)
1000,00
100,00
10,00
940; 2,82
660; 7,50
1,00
HbO2
HB
800; 1,90
660; 0,74
800; 1,77
940; 1,61
0,10
37.
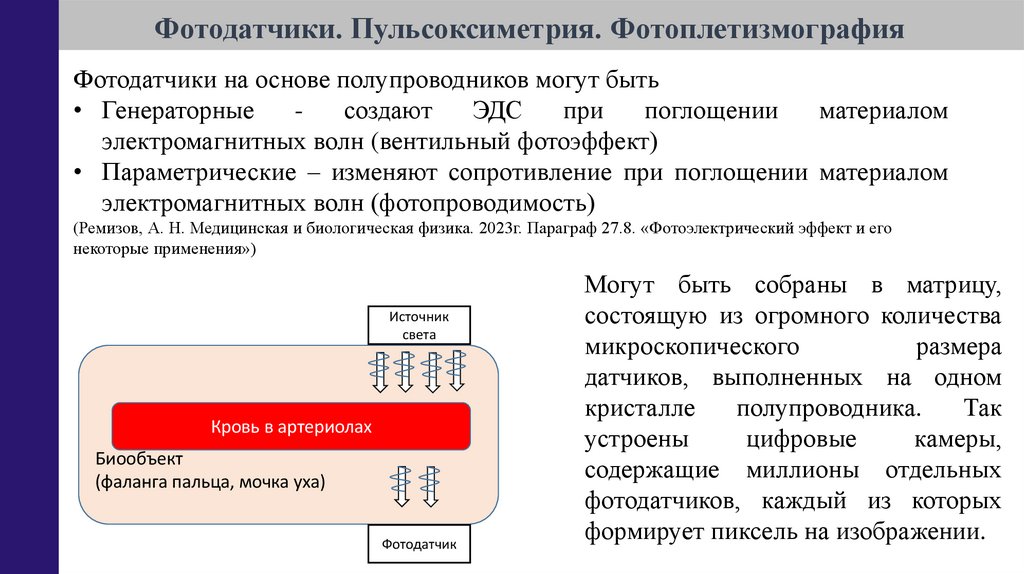
Фотодатчики. Пульсоксиметрия. ФотоплетизмографияФотодатчики на основе полупроводников могут быть
• Генераторные
создают
ЭДС
при
поглощении
материалом
электромагнитных волн (вентильный фотоэффект)
• Параметрические – изменяют сопротивление при поглощении материалом
электромагнитных волн (фотопроводимость)
(Ремизов, А. Н. Медицинская и биологическая физика. 2023г. Параграф 27.8. «Фотоэлектрический эффект и его
некоторые применения»)
Источник
света
Кровь в артериолах
Биообъект
(фаланга пальца, мочка уха)
Фотодатчик
Могут быть собраны в матрицу,
состоящую из огромного количества
микроскопического
размера
датчиков, выполненных на одном
кристалле
полупроводника.
Так
устроены
цифровые
камеры,
содержащие миллионы отдельных
фотодатчиков, каждый из которых
формирует пиксель на изображении.
38.
Литература для подготовкиОсновная литература:
Ремизов, А. Н. Медицинская и биологическая физика : учебник/А. Н. Ремизов. - 4-е изд. , испр. и
перераб. - Москва : ГЭОТАР-Медиа, 2023.
• Глава 28. «Волновые свойства частиц. Элементы квантовой механики». Параграфы: 28.8-28.9
• Глава 29. «Излучение и поглощение энергии атомами и молекулами». Параграфы: 29.1-29.5
• Глава 24. «Интерференция и дифракция света. Голография». Параграфы: 24.1, 24.2, 24.4, 24.6
• Параграф 32.4. «Биофизические основы действия ионизирующих излучений на организм»
https://www.studentlibrary.ru/book/ISBN9785970474983.html
39.
Литература для подготовкиДополнительно:
Эйдельман, Е. Д. Физика с элементами биофизики : учебник / Е. Д. Эйдельман. - 2-е изд., перераб. и
доп. - Москва : ГЭОТАР-Медиа, 2023. https://www.studentlibrary.ru/book/ISBN9785970469071.html
Глава 14. «Оптика». Параграфы: 14.1, 14.1.1, 14.1.2, 14.1.3, 14.1.5
Глава 15. «Тепловое излучение. Понятие о квантах». Параграфы: 15.1, 15.2, 15.5, 15.6
Глава 16. «Спектры атомов и молекул». Параграфы: 16.1, 16.2, 16.3, 16.5, 16.6
Глава 17. «Физические основы спектрального анализа». Параграфы: 17.1, 17.2, 17.3, 17.4, 17.5.1 17.5.4, 17.6
Антонов, В. Ф. Физика и биофизика : учебник / В. Ф. Антонов, Е. К. Козлова, А. М. Черныш. - 2-е
изд. , испр. и доп. - Москва : ГЭОТАР-Медиа, 2015.
https://www.studentlibrary.ru/book/ISBN9785970435267.html
Раздел 2. Электромагнитное излучение.
Глава 8. «Спектры излучения атомов и молекул». Параграфы: 8.1-8.2
Torp KD, Modi P, Pollard EJ, et al. Pulse Oximetry. [Updated 2023 Jul 30]. In: StatPearls [Internet]. Treasure
Island
(FL):
StatPearls
Publishing;
2025
Jan-.
Available
from:
https://www.ncbi.nlm.nih.gov/books/NBK470348/
Сергунова В.А., Манченко Е.А., and Гудкова О.Е.. "Гемоглобин: модификации, кристаллизация,
полимеризация (обзор)" Общая реаниматология, vol. 12, no. 6, 2016, pp. 49-63.
https://www.reanimatology.com/rmt/article/download/1562/1108




















 Физика
Физика








