Похожие презентации:
количество вещества задачи, 8 кл
1.
Вычисления количества,массы вещества по
уравнениям химических
реакций
2.
Количество вещества6,02*10
23
число Авогадро
Количество вещества – это порция вещества,
содержащая определённое число частиц (атомов,
молекул, ионов)
n – количество вещества. [моль]
3.
Количество вещества23
Моль – это количество вещества, содержащее 6,02*10 частиц (атомов,
молекул, ионов)
23
-1
NA = 6,02*10 моль
N
n=
NA
4.
Молярная массаМолярная масса – это отношение массы данной порции вещества к его
химическому количеству.
Молярная масса численно = относительной молекулярной массе
М = [г/моль]
m
n=
M
5.
Алгоритм решения задачи с уравнением реакцииКакое количество вещества кислорода можно получить при разложении
9 граммов воды?
Дано:
m(H2O) = 9 г
Решение:
1.Составляем уравнение реакции, исходя из условия задачи,
расставляем коэффициенты:
Найти:
2H2O = 2H2 + O2
n(O2) -?
2.Находим количество вещества воды:
n(H2O) =
m
M
=
9
18
= 0,5 моль
6.
Алгоритм решения задачи с уравнением реакцииКакое количество вещества кислорода можно получить при разложении 9
граммов воды?
Дано:
m(H2O) = 9 г
Решение:
3. Составляем пропорцию:
0,5 моль
Найти:
2H2O = 2H2 + O2
2
n(O2) -?
Х моль
n(O2) = 0,25 моль
4.Записываем ответ:
Ответ: n(O2) = 0,25 моль
1
0,5 моль
2
=
Х моль
1
7.
Алгоритм решения задачи с уравнением реакцииОпределите массу воды, образовавшуюся в результате сгорания водорода
в 3,2 г кислорода.
Дано:
m(O2) = 3,2 г
Найти:
m(H2O) -?
Решение:
1.Составляем уравнение реакции, исходя из условия задачи:
H2 + O2 = H2O
2.Расставляем коэффициенты:
2H2 + O2 = 2H2O
8.
Алгоритм решения задачи с уравнением реакцииОпределите массу воды, образовавшуюся в результате сгорания водорода в 3,2 г
кислорода.
Дано:
m(O2) = 3,2 г
Найти:
m(H2O) -?
Решение:
3.Находим количество вещества кислорода:
m
3,2
n(O2) =
=
= 0,1 моль
M
32
4.Составляем пропорцию:
0,1 моль х моль
2H2 + O2 = 2H2O
1
2
0,1 моль
х моль
=
1
2
9.
Алгоритм решения задачи с уравнением реакцииОпределите массу воды, образовавшуюся в результате сгорания водорода в 3,2 г
кислорода.
Дано:
m(O2) = 3,2 г
Решение:
5.Находим массу воды:
Найти:
m(H2O) -?
2H2 + O2 = 2H2O
m(H2O) = n*M = 0,2*18 = 3,6 г
6.Записываем ответ:
Ответ: m(H2O) = 3,6 г
10.
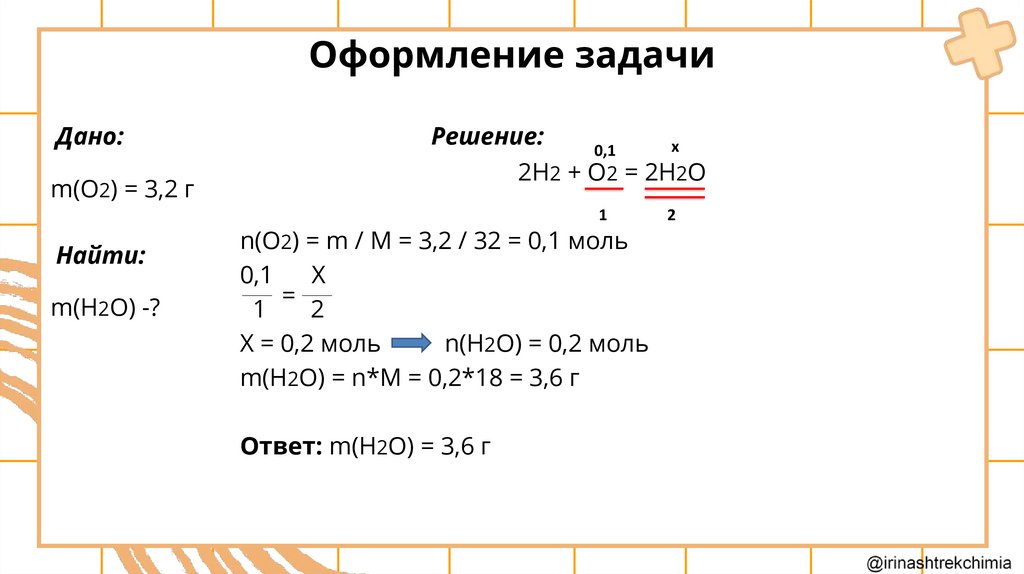
Оформление задачиДано:
m(O2) = 3,2 г
Решение:
х
0,1
2H2 + O2 = 2H2O
1
Найти:
m(H2O) -?
n(O2) = m / M = 3,2 / 32 = 0,1 моль
0,1
Х
=
1
2
Х = 0,2 моль
n(H2O) = 0,2 моль
m(H2O) = n*M = 0,2*18 = 3,6 г
Ответ: m(H2O) = 3,6 г
2
11. Решите задачи
1.Какое количество вещества водорода можно получить при разложении36 граммов воды?
2.Какое количество вещества воды можно получить из 10 граммов
водорода?
3.Определите массу водорода, необходимую для реакции с кислородом,
чтобы образовалось образования 6 граммов воды.
4.Определите массу кислорода, необходимую для сгорания 12 граммов
водорода при образовании воды










 Химия
Химия








