Похожие презентации:
вода и ее свойства
1. Вода и её свойства
2. Физические свойства воды
При нормальных условиях вода представляетсобой прозрачную жидкость, не имеющую цвета
(при малой толщине слоя),
запаха и вкуса.
При нормальном давлении кипит при температуре
100 °С, а замерзает при 0°С.
Максимальная плотность при 4°С равна 1 г/см³.
Способность расширяться при замерзании.
Лёд имеет меньшую плотность, чем жидкая вода,
поэтому он всплывает на поверхность.
3. Физические свойства воды (агрегатное состояние)
Вода в жидкомсостоянии
Вода в
газообразном
состоянии
Вода в твердом
состоянии
4. Формула воды
Молекула воды состоитиз двух атомов водорода
и одного атома кислорода,
соединённых между собой
ковалентной связью.
Химическая
формула воды
5. Химические свойства воды
1. С металлами2. С неметаллами
Вода +
3. С оксидами
4. Разложение
6. 1. Взаимодействие с Ме
А) Взаимодействие с активными металлами.При комнатной температуре вода реагирует
с активными металлами с образованием щелочей
и водорода:
2Na + 2H₂O → 2NaOH + H₂↑
гидроксид
натрия
(щелочь)
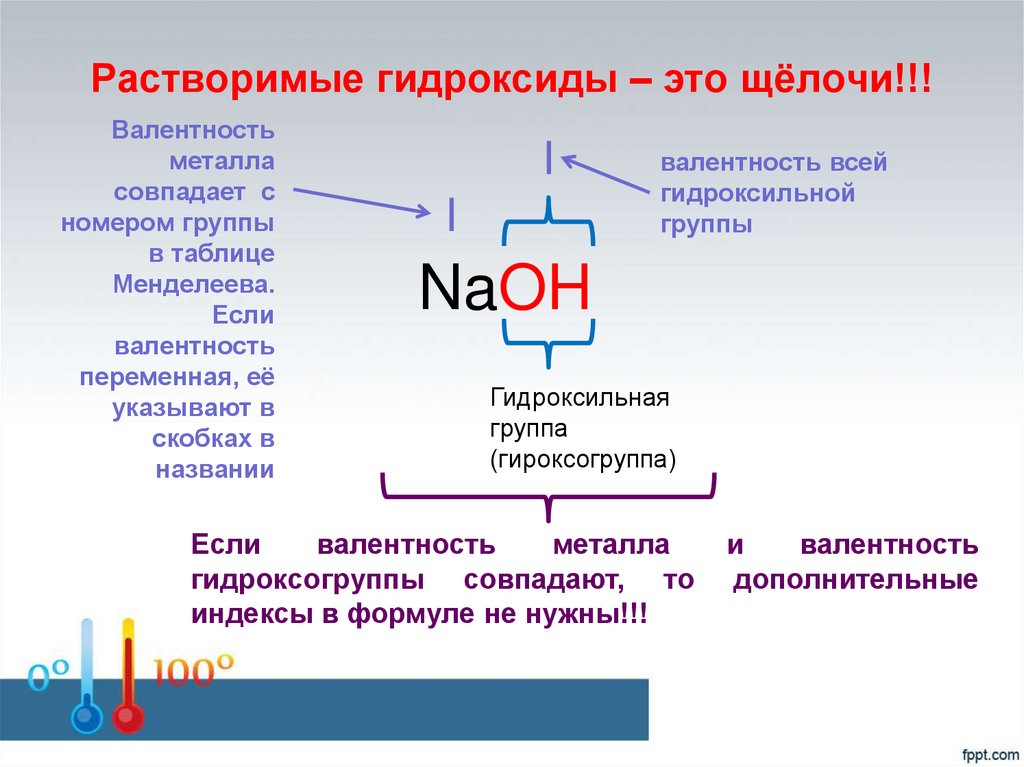
7. Растворимые гидроксиды – это щёлочи!!!
Валентностьметалла
совпадает с
номером группы
в таблице
Менделеева.
Если
валентность
переменная, её
указывают в
скобках в
названии
I
I
валентность всей
гидроксильной
группы
NaOH
Гидроксильная
группа
(гироксогруппа)
Если
валентность
металла
гидроксогруппы совпадают, то
индексы в формуле не нужны!!!
и
валентность
дополнительные
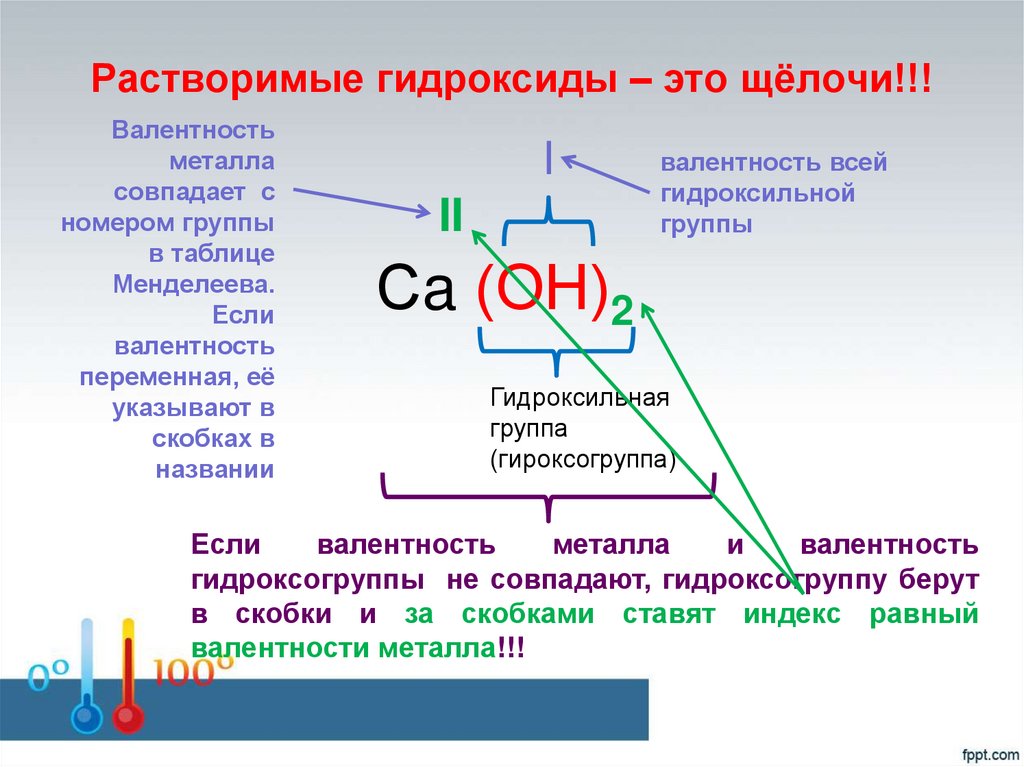
8. Растворимые гидроксиды – это щёлочи!!!
Валентностьметалла
совпадает с
номером группы
в таблице
Менделеева.
Если
валентность
переменная, её
указывают в
скобках в
названии
I
II
валентность всей
гидроксильной
группы
Сa (ОН)2
Гидроксильная
группа
(гироксогруппа)
Если
валентность
металла
и
валентность
гидроксогруппы не совпадают, гидроксогруппу берут
в скобки и за скобками ставят индекс равный
валентности металла!!!
9.
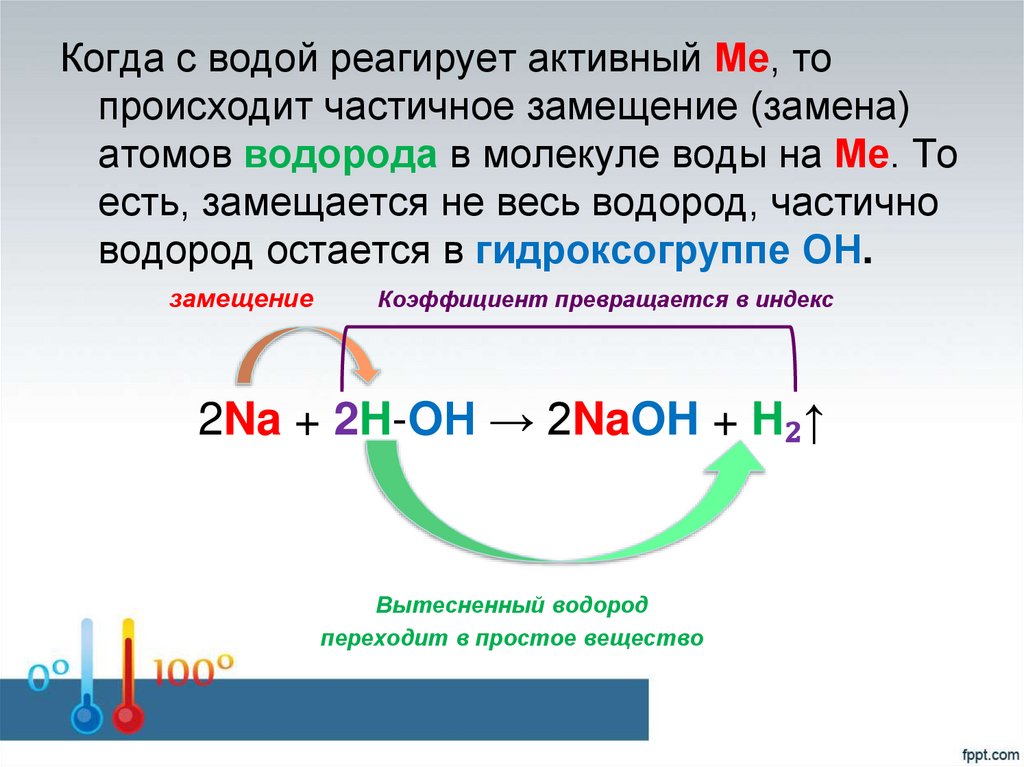
Когда с водой реагирует активный Ме, топроисходит частичное замещение (замена)
атомов водорода в молекуле воды на Ме. То
есть, замещается не весь водород, частично
водород остается в гидроксогруппе ОН.
замещение
Коэффициент превращается в индекс
2Na + 2H-OН → 2NaOH + H₂↑
Вытесненный водород
переходит в простое вещество
10. 1. Взаимодействие с Ме
Б) Взаимодействие с металлами среднейактивности.
При нагревании вода может вступать в реакцию с
металлами средней активности. Продуктами реакции
являются оксид металла и водород.:
Zn + H₂O → ZnO + H₂↑
оксид
цинка
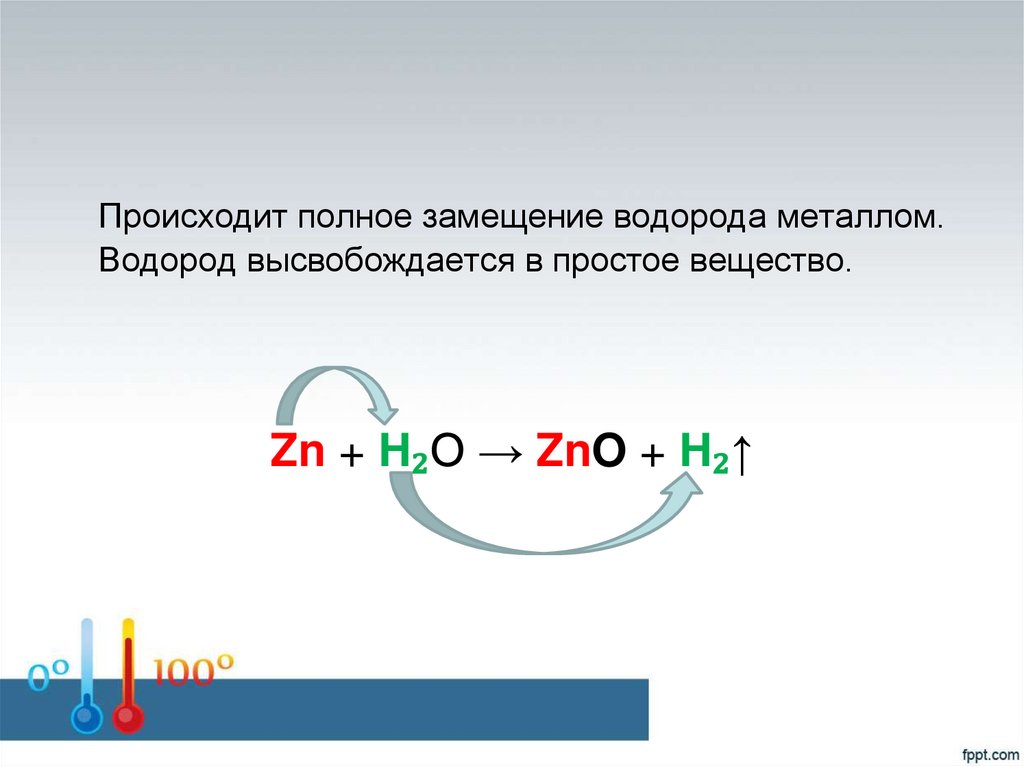
11.
Происходит полное замещение водорода металлом.Водород высвобождается в простое вещество.
Zn + H₂O → ZnO + H₂↑
12. Важное исключение из правил
Несмотря на то, что Mg металл среднейактивности, с водой он образует гидроксид
металла, а не оксид!!!
!!! Гидроксид
магния
13. 1. Взаимодействие с Ме
В) Взаимодействие с неактивными металлами.С неактивными металлами вода не реагирует
14. 2. Взаимодействие с неМе
Вода может взаимодействовать с некоторыминеметаллами, например:
С+Н2О→СО+Н2
15. 3.Взаимодействие воды с оксидами
Вода реагируетс:
А) оксидами
металлов
Б) оксидами
неметаллов
16. 3. А) взаимодействие воды с оксидами металлов
!!! Оксид – это бинарное соединение, обязательнымэлементом в нем будет кислород (он ф формуле пишется
на втором месте).
оксиды
металлов
МеО
Неметаллов
неМеО
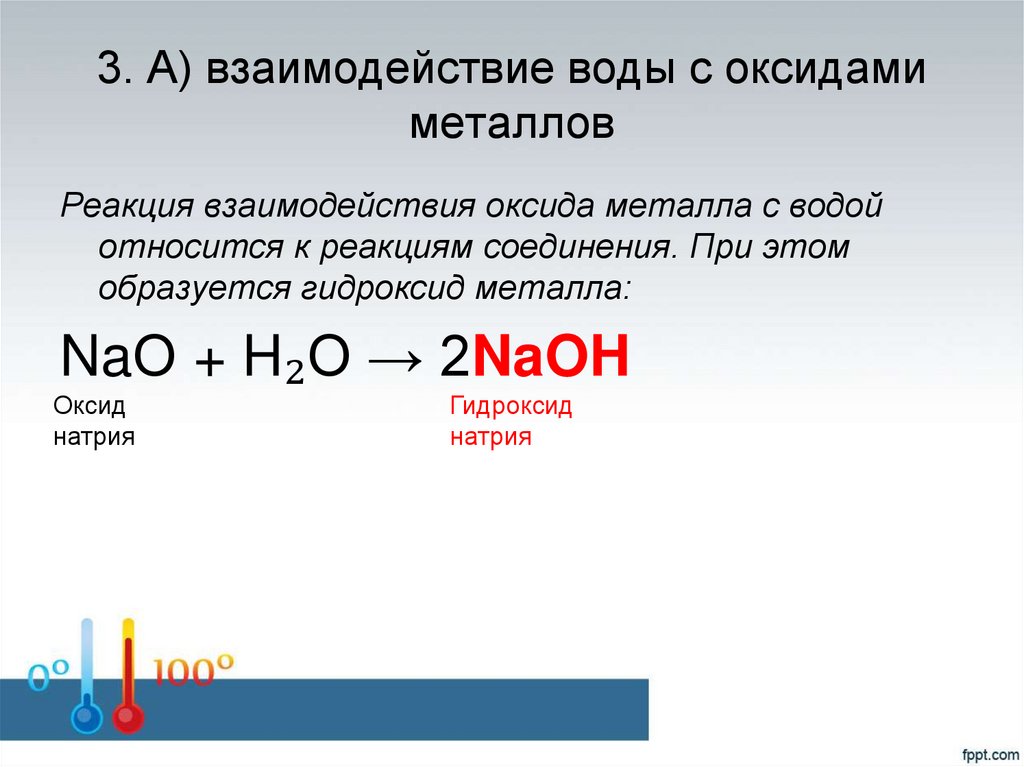
17. 3. А) взаимодействие воды с оксидами металлов
Реакция взаимодействия оксида металла с водойотносится к реакциям соединения. При этом
образуется гидроксид металла:
NaО + H₂O → 2NaOH
Оксид
натрия
Гидроксид
натрия
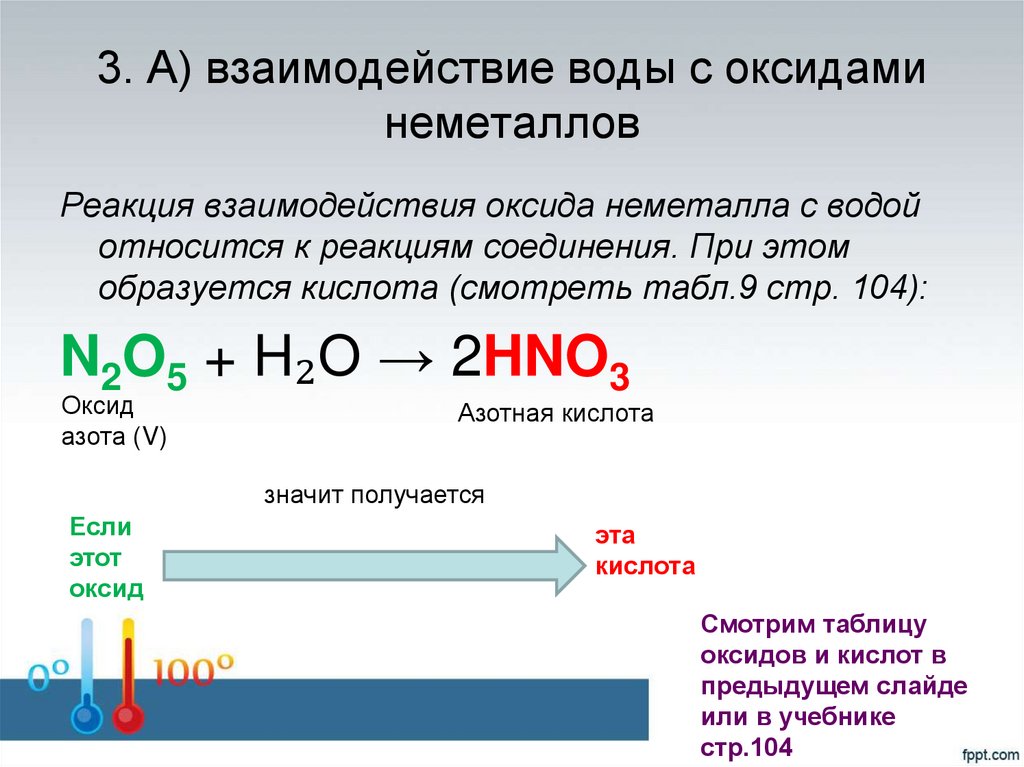
18. 3. А) взаимодействие воды с оксидами неметаллов
Реакция взаимодействия оксида неметалла с водойотносится к реакциям соединения. При этом
образуется кислота (смотреть табл.9 стр. 104):
N2O5 + H₂O → 2HNO3
Оксид
азота (V)
Азотная кислота
значит получается
Если
этот
оксид
эта
кислота
Смотрим таблицу
оксидов и кислот в
предыдущем слайде
или в учебнике
стр.104
19.
получается20. 4.Реакция разложения воды
Вода разлагается на водород и кислородпри пропускании электрического тока:
2H₂O = 2H₂ + O₂
21. Задания на закрепление материала
Задание 1:Закончите уравнения реакций,
расставьте коэффициенты:
а) Li2O + H2O →
б) Mg + H2O →
в) SO3 + H2O →
г) SiO2 + H2O →
22.
Задание 2: оставьте уравнения реакцийвзаимодействия с водой следующих
веществ:
а) натрий;
б) свинец; в) медь ;
г) литий;
д) железо; ж) серебро.
Запишите
реакции,
коэффициенты,
укажите
образующихся веществ.
расставьте
названия












 Химия
Химия








