Похожие презентации:
Работа аккумулятора_ Физика и Энергетика
1.
Работааккумулятора
2.
Основы ХИТХимические источники тока преобразуют энергию
химических связей в направленное движение
электронов.
3.
Устройство ячейкиАнод и Катод
Электролит
Электроды, выполненные из различных
Вещество, проводящее ионы между
материалов. На аноде происходит процесс
электродами, но изолирующее поток
окисления, на катоде — восстановления.
электронов внутри батареи.
4.
Процесс разрядаОкисление на аноде: Металл теряет электроны и превращается в ионы.
Внешняя цепь: Электроны устремляются от анода к катоду, создавая ток.
Восстановление на катоде: Ионы принимают электроны, завершая реакцию.
ЭДС цепи: Разность потенциалов определяется химической природой веществ.
5.
Эффективность системыМаксимальный КПД
98%
Литий-ионные технологии достигают невероятной
эффективности преобразования энергии. Потери на
нагрев (эффект Джоуля-Ленца) минимизированы за
счет низкого внутреннего сопротивления.
6.
Удельная энергоемкость (Вт·ч/кг)7.
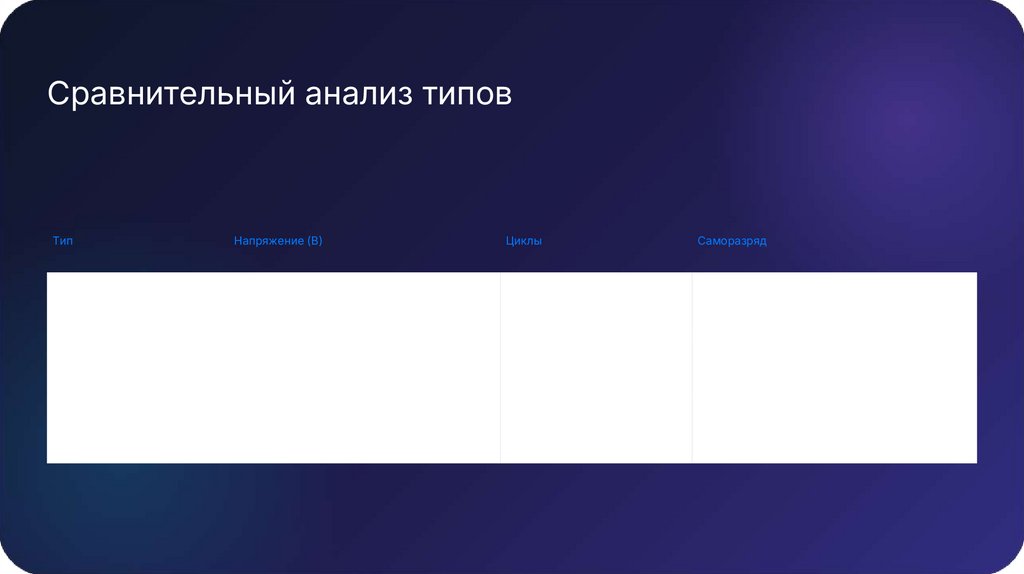
Сравнительный анализ типовТип
Напряжение (В)
Циклы
Саморазряд
Lead-Acid
2.0
300-500
Низкий (5%)
Li-Ion
3.7
1000-3000
Очень низкий (2%)
LiFePO4
3.2
5000+
Средний
8.
Деградация емкостиЗависимость емкости от количества циклов заряда-разряда (0 - 2000 циклов).
9.
История технологий1800
1859
1991
2026
Вольтов столб
Свинцово-
Коммерческий Li-
Solid State Era
кислотный
Ion
10.
Основные уравненияЗакон Ома для полной цепи
Емкость аккумулятора
Где ε — ЭДС, R — внешнее сопротивление,
Измеряется в Ампер-часах (А·ч).
r — внутреннее сопротивление.
Определяет запасенный заряд.
11.
"Электричество — это не только энергия.Это возможность хранить будущее в
маленькой ячейке."
— ЛАБОРАТОРИЯ ЭНЕРГЕТИКИ 2026










 Химия
Химия








