Похожие презентации:
№19_Основы_МКТ_Уравнение_Менделеева_Клапейрона
1.
КУРС ПОДГОТОВКИ К ЕГЭ 2026№19. Основы МКТ.
Уравнение Менделеева-Клапейрона
Преподаватель: Высотин Юрий Алексеевич
2.
2Молекулярная физика. Основные положения МКТ
Молекулярная физика (или молекулярно-кинетическая теория (МКТ)) – это раздел
физики, который изучает различные свойства тел с точки зрения их молекулярного
строения.
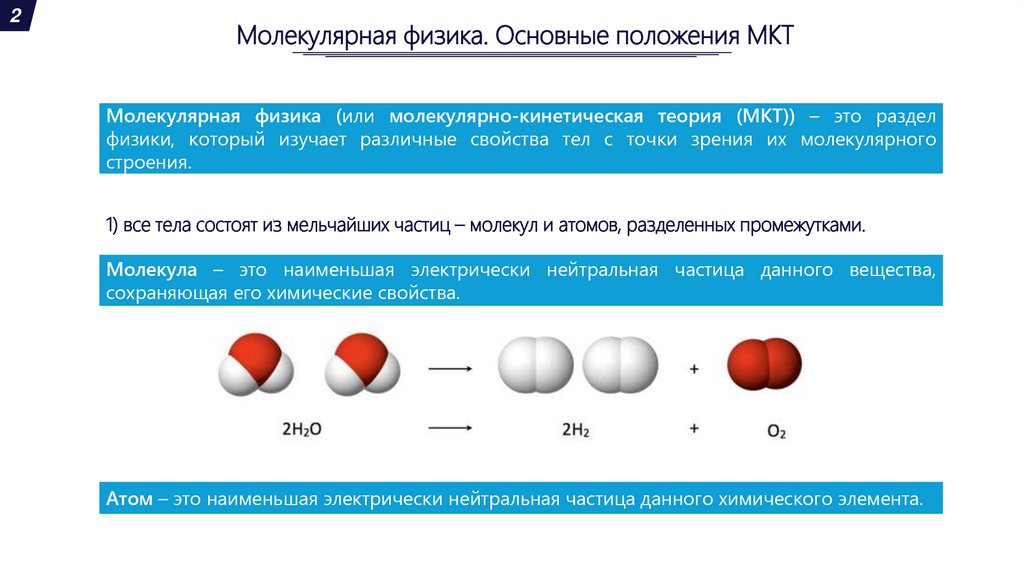
1) все тела состоят из мельчайших частиц – молекул и атомов, разделенных промежутками.
Молекула – это наименьшая электрически нейтральная частица данного вещества,
сохраняющая его химические свойства.
Атом – это наименьшая электрически нейтральная частица данного химического элемента.
3.
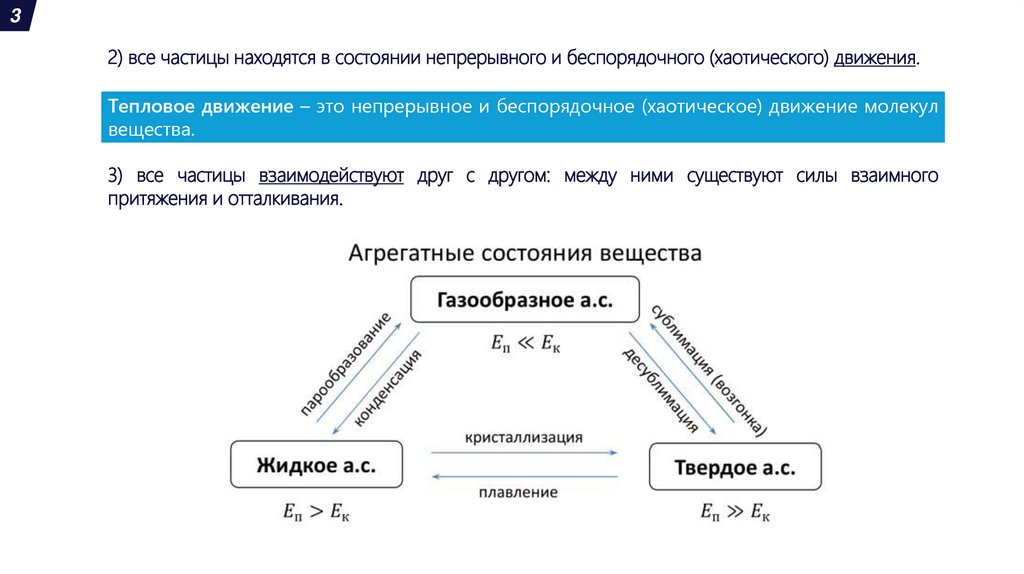
32) все частицы находятся в состоянии непрерывного и беспорядочного (хаотического) движения.
Тепловое движение – это непрерывное и беспорядочное (хаотическое) движение молекул
вещества.
3) все частицы взаимодействуют друг с другом: между ними существуют силы взаимного
притяжения и отталкивания.
4.
4Доказательства основных положений МКТ
5.
5Броуновское движение. Диффузия
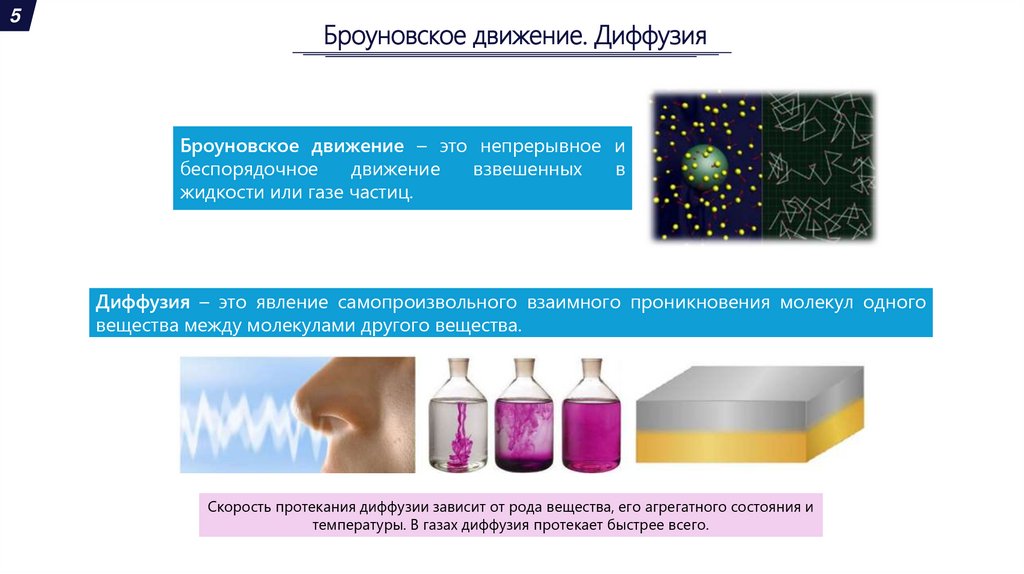
Броуновское движение – это непрерывное и
беспорядочное
движение
взвешенных
в
жидкости или газе частиц.
Диффузия – это явление самопроизвольного взаимного проникновения молекул одного
вещества между молекулами другого вещества.
Скорость протекания диффузии зависит от рода вещества, его агрегатного состояния и
температуры. В газах диффузия протекает быстрее всего.
6.
6Основные формулы молекулярной физики
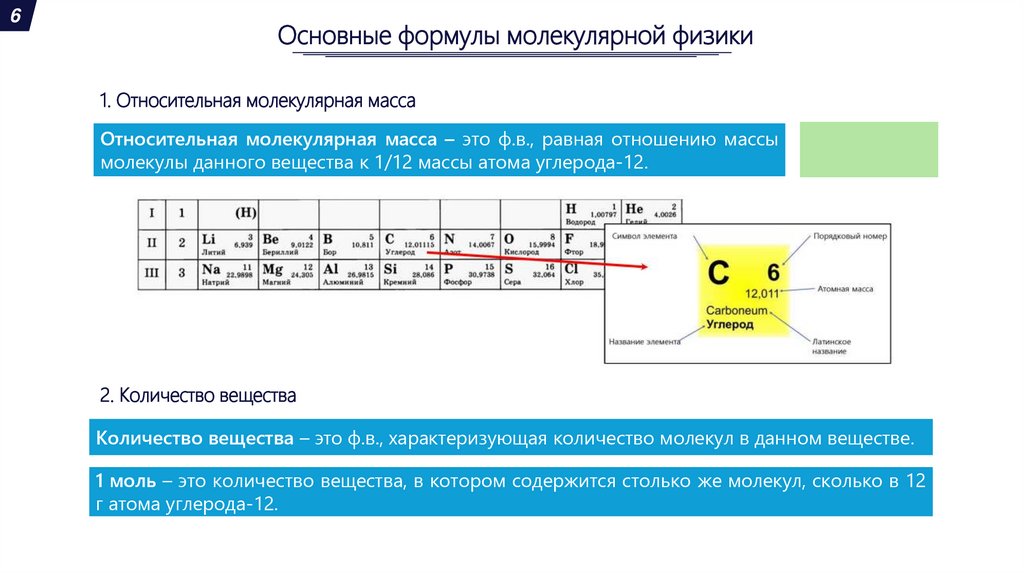
1. Относительная молекулярная масса
Относительная молекулярная масса – это ф.в., равная отношению массы
молекулы данного вещества к 1/12 массы атома углерода-12.
2. Количество вещества
Количество вещества – это ф.в., характеризующая количество молекул в данном веществе.
1 моль – это количество вещества, в котором содержится столько же молекул, сколько в 12
г атома углерода-12.
7.
7а) через число Авогадро
Число Авогадро – это число, которое численно равно
количеству молекул в 1 моль любого вещества.
б) через молярную массу
Молярная масса – это ф.в., численно равная массе 1
моль данного вещества.
- масса одной молекулы
данного вещества
8.
83. Плотность вещества
Плотность – это ф.в., равная отношению массы тела и его объема.
4. Концентрация вещества
Концентрация – это ф.в., равная отношению числа молекул вещества к объему, который
они занимают.
Плотность и концентрация вещества прямо пропорциональны друг другу.
9.
910.
10Идеальный газ
Идеальный газ – это модель реального газа, для которой выполняются следующие условия:
1) его молекулы являются материальными точками;
2) они не взаимодействуют друг с другом, а взаимодействия со стенками сосуда является
абсолютно упругим.
МКТ изучает свойства макроскопических тел (термодинамических систем)
на основе их микроскопической структуры.
11.
11Основное уравнение МКТ
12.
1213.
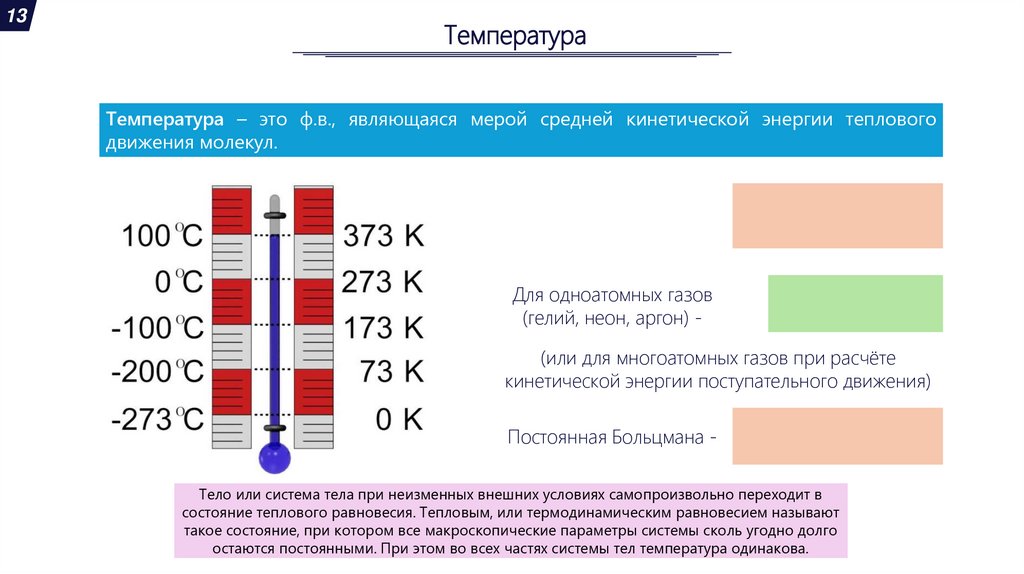
13Температура
Температура – это ф.в., являющаяся мерой средней кинетической энергии теплового
движения молекул.
Для одноатомных газов
(гелий, неон, аргон) (или для многоатомных газов при расчёте
кинетической энергии поступательного движения)
Постоянная Больцмана Тело или система тела при неизменных внешних условиях самопроизвольно переходит в
состояние теплового равновесия. Тепловым, или термодинамическим равновесием называют
такое состояние, при котором все макроскопические параметры системы сколь угодно долго
остаются постоянными. При этом во всех частях системы тел температура одинакова.
14.
1415.
15Скорость движения молекул
- универсальная газовая
постоянная
16.
16Уравнение состояния идеального газа
- уравнение
Менделеева-Клапейрона
17.
1718.
1819.
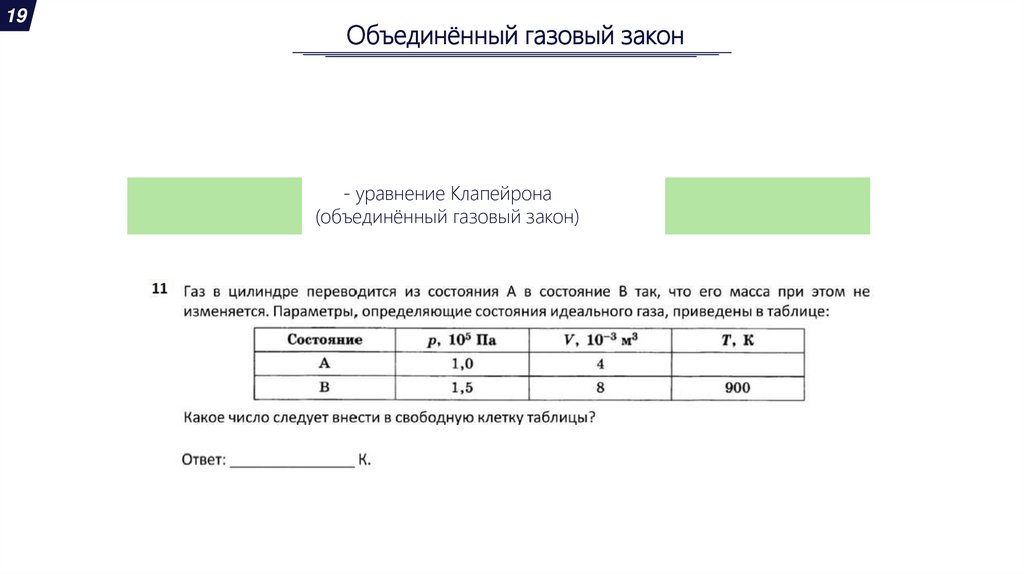
19Объединённый газовый закон
- уравнение Клапейрона
(объединённый газовый закон)
20.
2021.
21Закон Дальтона
Парциальное давление – это давление, которое производил бы газ на стенки сосуда, если
бы он в нём был один при прочих равных условиях.
Закон Дальтона: давление смеси идеальных газов равно сумме их парциальных давлений.






















 Физика
Физика








