Похожие презентации:
Биологические мембраны
1. Биологические мембраны
• До середины XX в. мембрану рассматривали какотносительно простое образование, выполняющее
лишь немногие простые стереотипные для различных
клеток функции.
• До 1960-х г.г. сведения о мембранах были сравнительно
ограничены. Было известно, что мембраны несомненно
очень тонкие (порядка 10 нм), состоят из липидного
бислоя с интегрированными белковыми молекулами.
2.
Модели мембраныМодель бислоя
В 1925 г. Гортер и Грендель предложили
модель бислоя. Они разрушали эритроциты и создавали условия для распределения их остатков по поверхности воды.
По их данным, площадь, занимаемая остатками мембран эритроцитов примерно,
вдвое превышала расчетную площадь
поверхности интактных эритроцитов.
На основании этих результатов они заключили, что мембрана клеток состоит из
двух монослоев. Более поздние исследования показали отношение поверхности монослоя к поверхности эритроцитов
1.5/1; остальная площадь приходится на
долю белков.
3.
Модели мембраныМодель Даниэлли-Давсона
Липидный бислой снаружи и изнутри клетки выстлан белковыми
молекулами. В мембранные поры также включены белки.
4. Биологические мембраны
• В покое мембраны являются электрически заряженными(поляризованными). Они имеют в своем составе водные поры,
через которые транспортируются некоторые ионы, изменяющие
заряд мембраны.
• Такие изменения заряда представляют собой различные
потенциалы, обеспечивающие межклеточную коммуникацию.
• Транспорт (ток) ионов контролируется различными мембранными
электрическими сенсорами и линганд-активируемыми
рецепторами.
• Ионные токи вызывают генерацию нервных импульсов,
градуальных потенциалов и иногда выделение медиаторов.
• Мембраны также способствуют росту и развитию дендритов и
аксонов, необходимых для локального и дистантного межклеточного
взаимодействия.
5. Биологические мембраны
Новые методологические подходы 1970-х г.г.благодаря разработке новых методов
рентгеноструктурного анализа,
электронной микроскопии,
кристаллографии,
компьютерного анализа и моделирования,
а также успехам в молекулярной биологии
привели к новому пониманию значения клеточных
мембран и открытию неизвестных прежде присущих им
механизмов синаптического контроля и
нейропластичности.
6.
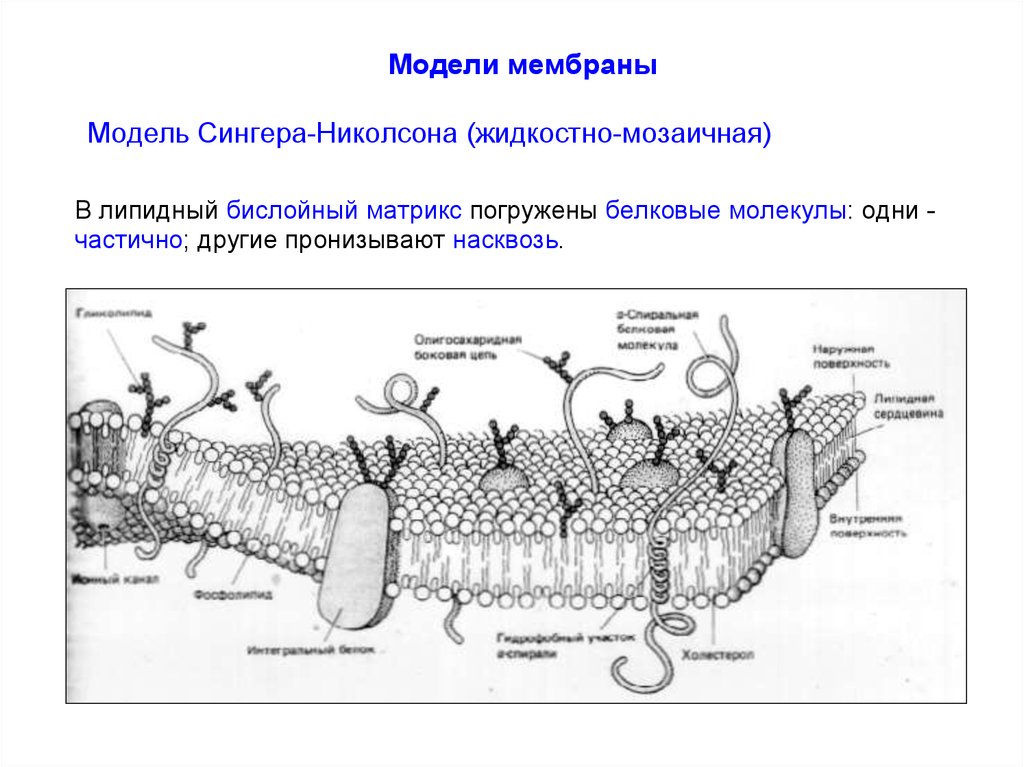
Модели мембраныМодель Сингера-Николсона (жидкостно-мозаичная)
В липидный бислойный матрикс погружены белковые молекулы: одни частично; другие пронизывают насквозь.
7.
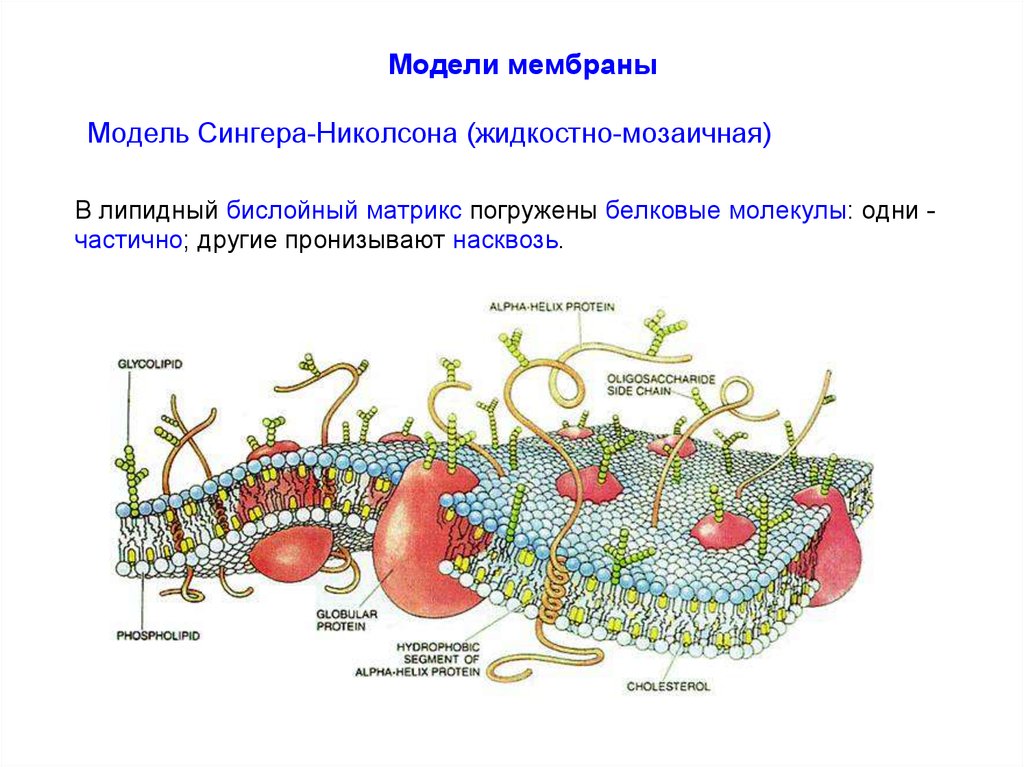
Модели мембраныМодель Сингера-Николсона (жидкостно-мозаичная)
В липидный бислойный матрикс погружены белковые молекулы: одни частично; другие пронизывают насквозь.
8.
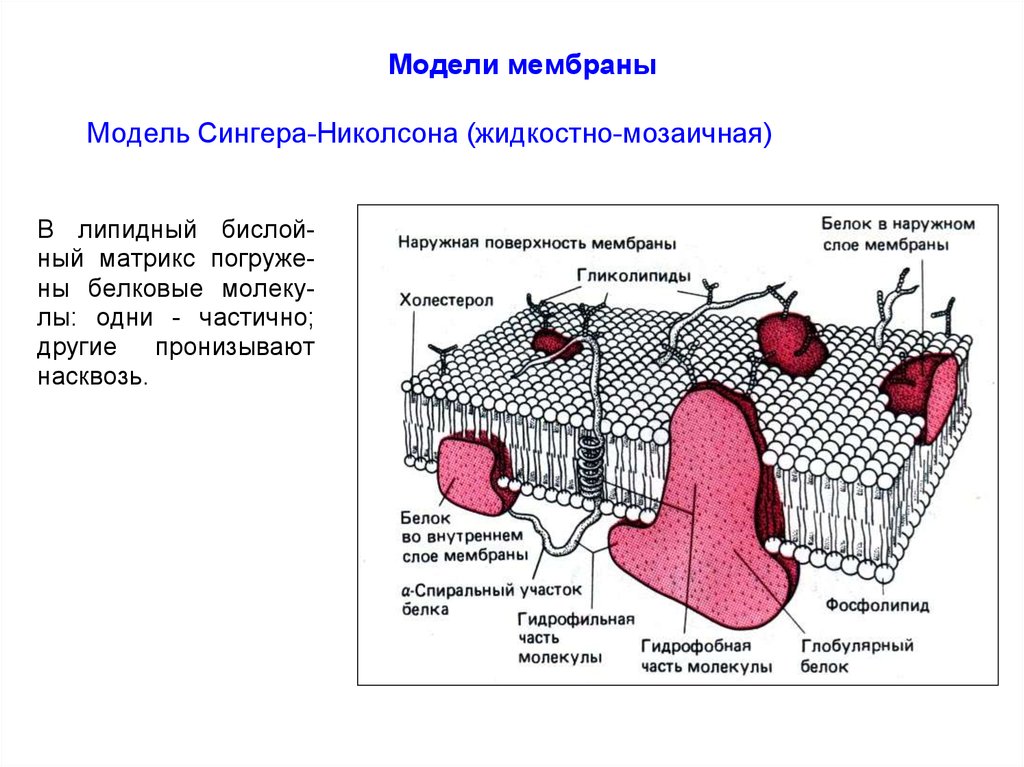
Модели мембраныМодель Сингера-Николсона (жидкостно-мозаичная)
В липидный бислойный матрикс погружены белковые молекулы: одни - частично;
другие пронизывают
насквозь.
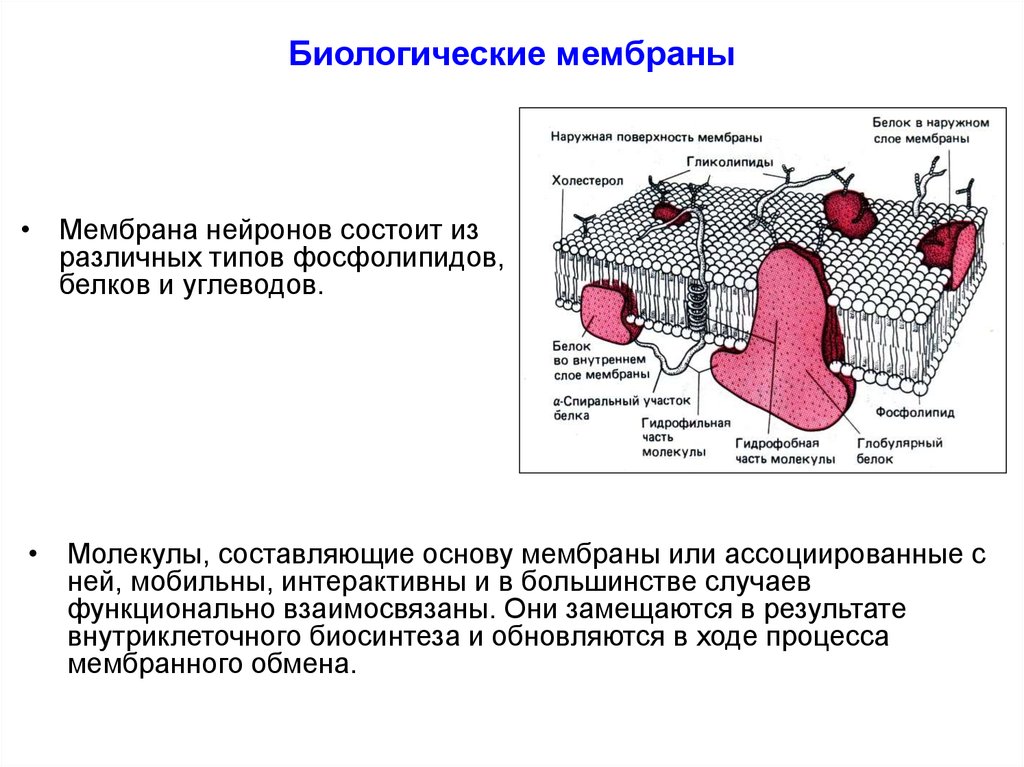
9. Биологические мембраны
• Мембрана нейронов состоит изразличных типов фосфолипидов,
белков и углеводов.
• Молекулы, составляющие основу мембраны или ассоциированные с
ней, мобильны, интерактивны и в большинстве случаев
функционально взаимосвязаны. Они замещаются в результате
внутриклеточного биосинтеза и обновляются в ходе процесса
мембранного обмена.
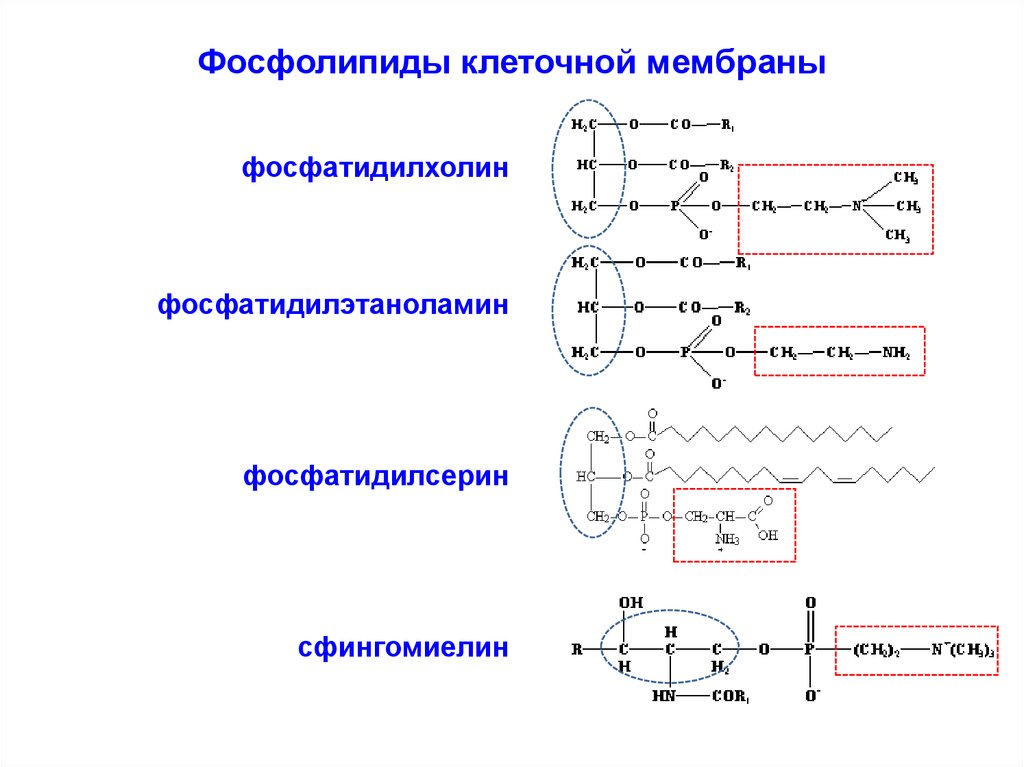
10. Фосфолипиды клеточной мембраны
Основные компоненты бислоя мембраны представляют:• фосфатидил-холин,
• сфинго-миелин,
• фосфатидил-этаноламин
• и фосфатидил-серин.
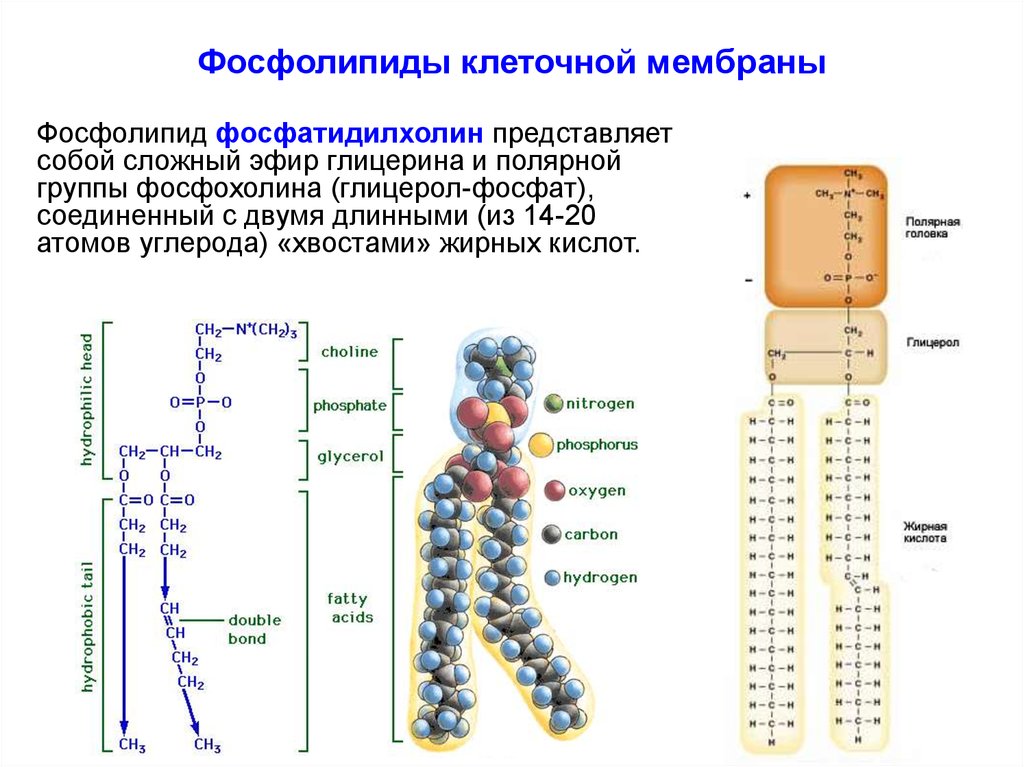
11. Фосфолипиды клеточной мембраны
Фосфолипид фосфатидилхолин представляетсобой сложный эфир глицерина и полярной
группы фосфохолина (глицерол-фосфат),
соединенный с двумя длинными (из 14-20
атомов углерода) «хвостами» жирных кислот.
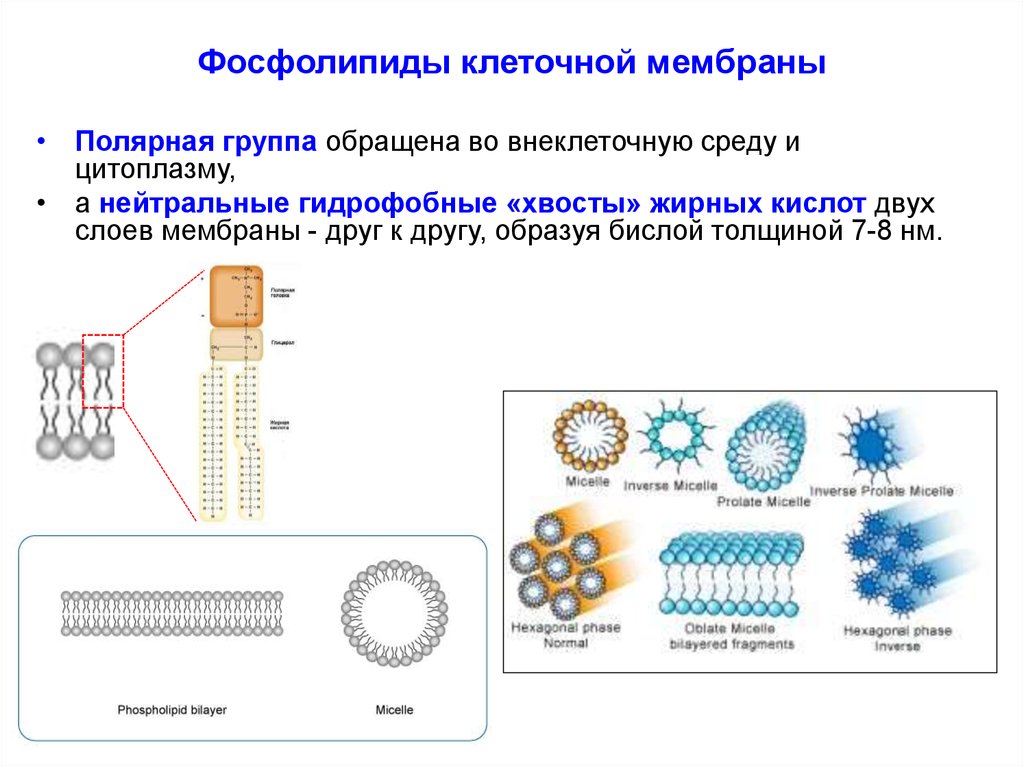
12. Фосфолипиды клеточной мембраны
• Полярная группа обращена во внеклеточную среду ицитоплазму,
• а нейтральные гидрофобные «хвосты» жирных кислот двух
слоев мембраны - друг к другу, образуя бислой толщиной 7-8 нм.
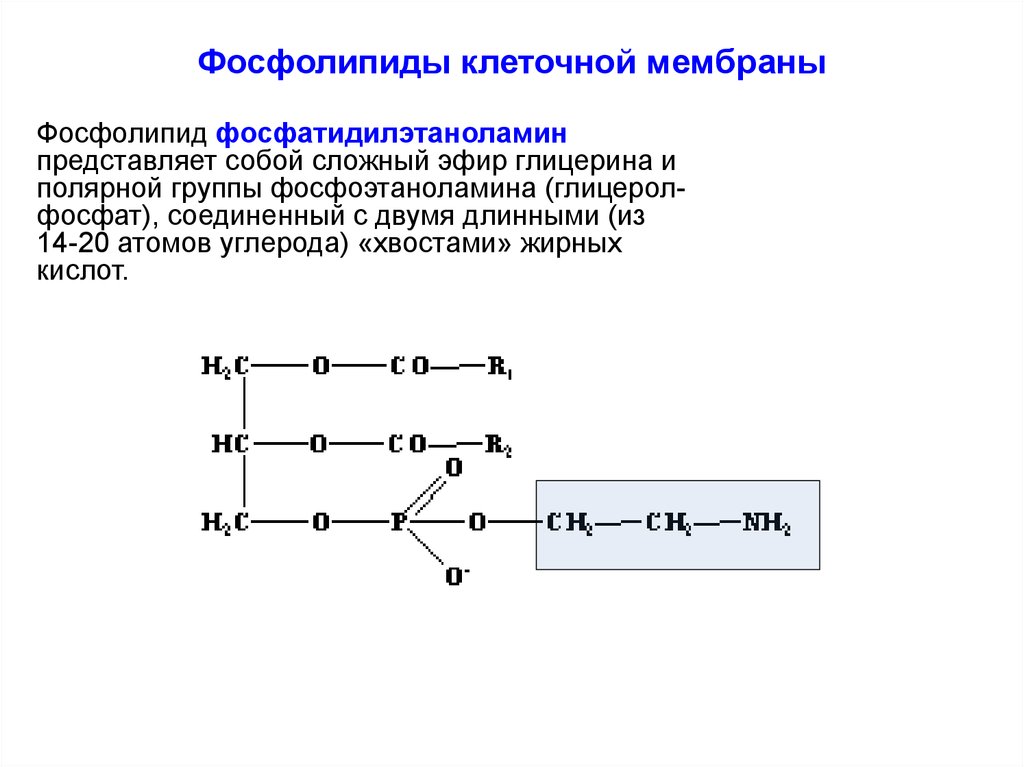
13. Фосфолипиды клеточной мембраны
Фосфолипид фосфатидилэтаноламинпредставляет собой сложный эфир глицерина и
полярной группы фосфоэтаноламина (глицеролфосфат), соединенный с двумя длинными (из
14-20 атомов углерода) «хвостами» жирных
кислот.
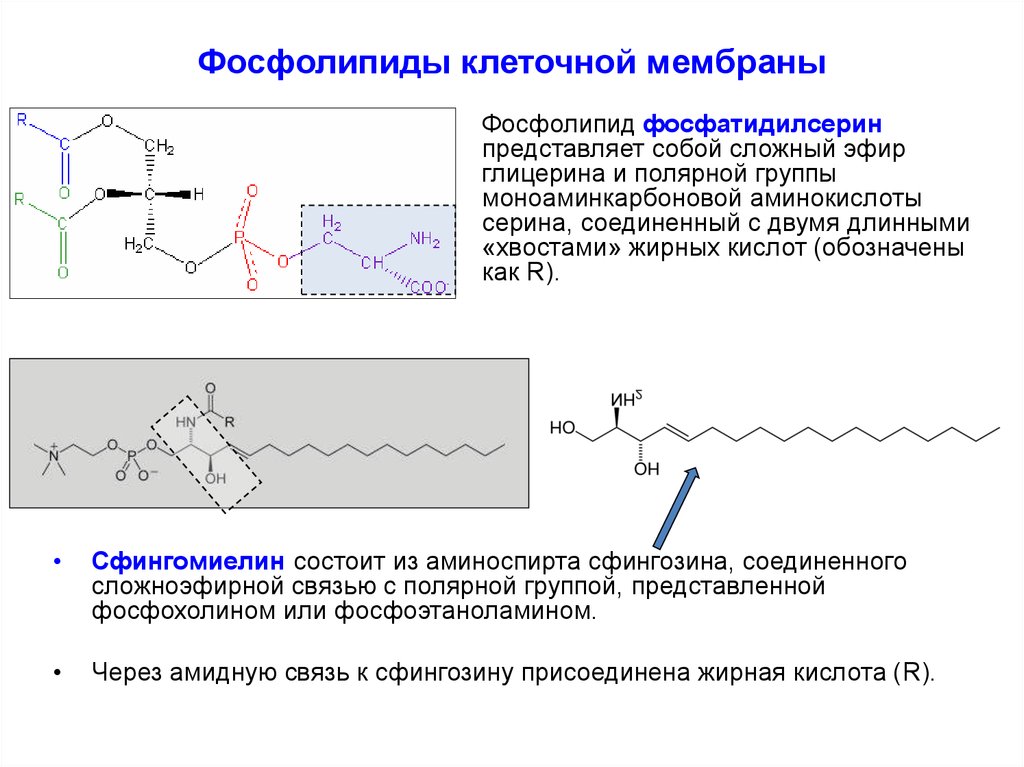
14. Фосфолипиды клеточной мембраны
Фосфолипид фосфатидилсеринпредставляет собой сложный эфир
глицерина и полярной группы
моноаминкарбоновой аминокислоты
серина, соединенный с двумя длинными
«хвостами» жирных кислот (обозначены
как R).
Сфингомиелин состоит из аминоспирта сфингозина, соединенного
сложноэфирной связью с полярной группой, представленной
фосфохолином или фосфоэтаноламином.
Через амидную связь к сфингозину присоединена жирная кислота (R).
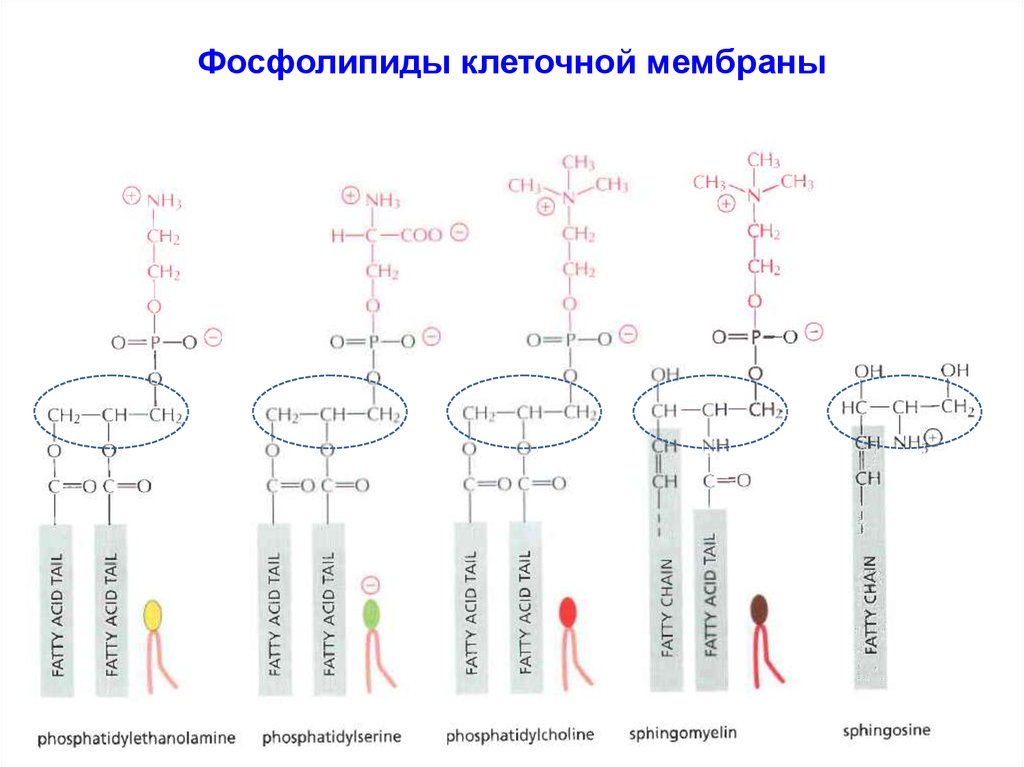
15. Фосфолипиды клеточной мембраны
фосфатидилхолинфосфатидилэтаноламин
фосфатидилсерин
сфингомиелин
16. Фосфолипиды клеточной мембраны
17. Фосфолипиды клеточной мембраны (распределение в листках бислоя)
• В малом количестве в мембране присутствуют также и другиефосфолипиды, например, инозитолфосфаты.
• Фосфолипиды по-разному распределены в клеточной мембране:
сфингомиелина и фосфатидилхолина больше во внешнем
листке бислоя,
межклеточное
пространство
цитоплазма
• в то время как фосфатидилэтаноламин и фосфатидилсерин
доминируют во внутреннем листке бислоя.
18.
Фосфолипиды клеточной мембраны(распределение в листках бислоя)
Легенда для фосфолипидов
19. Фосфолипиды в мембране выполняют три главные функции:
• Функции изолятора и барьера. Фосфолипидный бислойобразует изолированные структуры, тем самым препятствуя
проникновению в клетку полярных молекул, включая воду и
электролиты. В то время как различные газы (например, О2 и
СО2) и разнообразные растворимые в липидах вещества
(например, этиловый спирт и местные анестетики) легко
приникают через мембрану. Барьерные функции защищают
клетку от потери жизненно важных полярных
цитоплазматических компонентов и входа в клетку многих
потенциально опасных внешних веществ.
• Внутриклеточная сигнализация. Производные мембранных
фосфолипидов инозитол-1,2.3-трифосфат и диацилглицерол
выполняют роль вторичных посредников .
• Электрические свойства. Фосфолипидный бислой вместе с
открытыми каналами тока утечки в мембране демонстрирует
свойства RC-цепочки и, соответственно, фильтра низких частот, а
также и интегратора электрических входных сигналов.
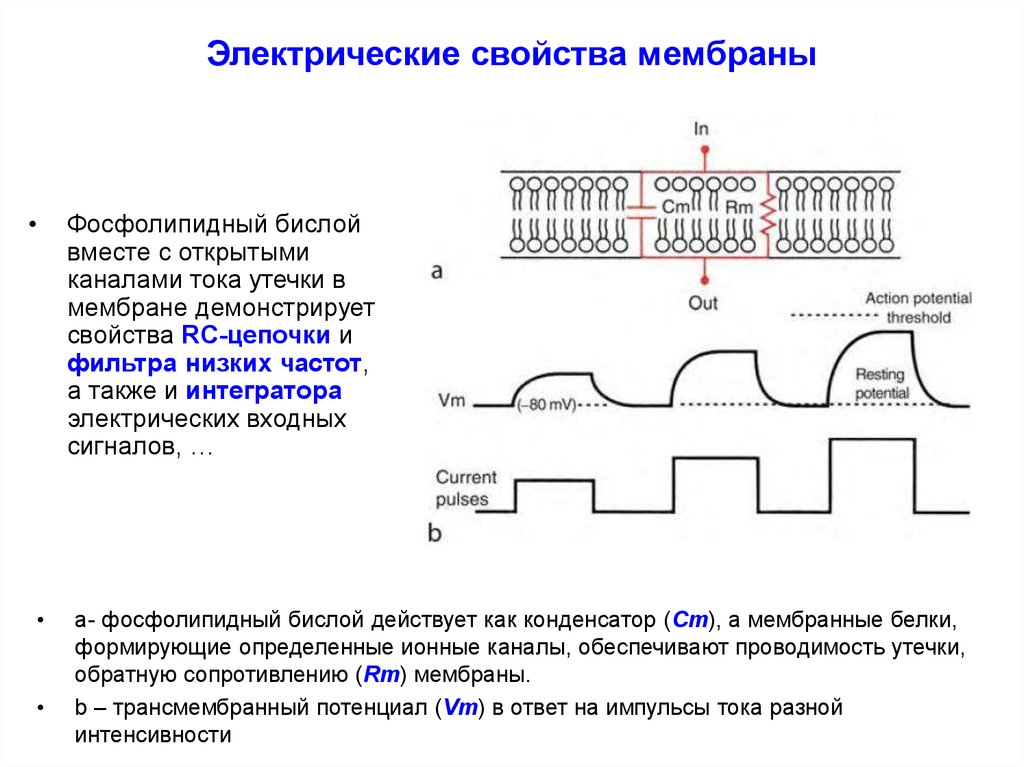
20. Электрические свойства мембраны
Фосфолипидный бислой
вместе с открытыми
каналами тока утечки в
мембране демонстрирует
свойства RC-цепочки и
фильтра низких частот,
а также и интегратора
электрических входных
сигналов, …
a- фосфолипидный бислой действует как конденсатор (Cm), а мембранные белки,
формирующие определенные ионные каналы, обеспечивают проводимость утечки,
обратную сопротивлению (Rm) мембраны.
b – трансмембранный потенциал (Vm) в ответ на импульсы тока разной
интенсивности
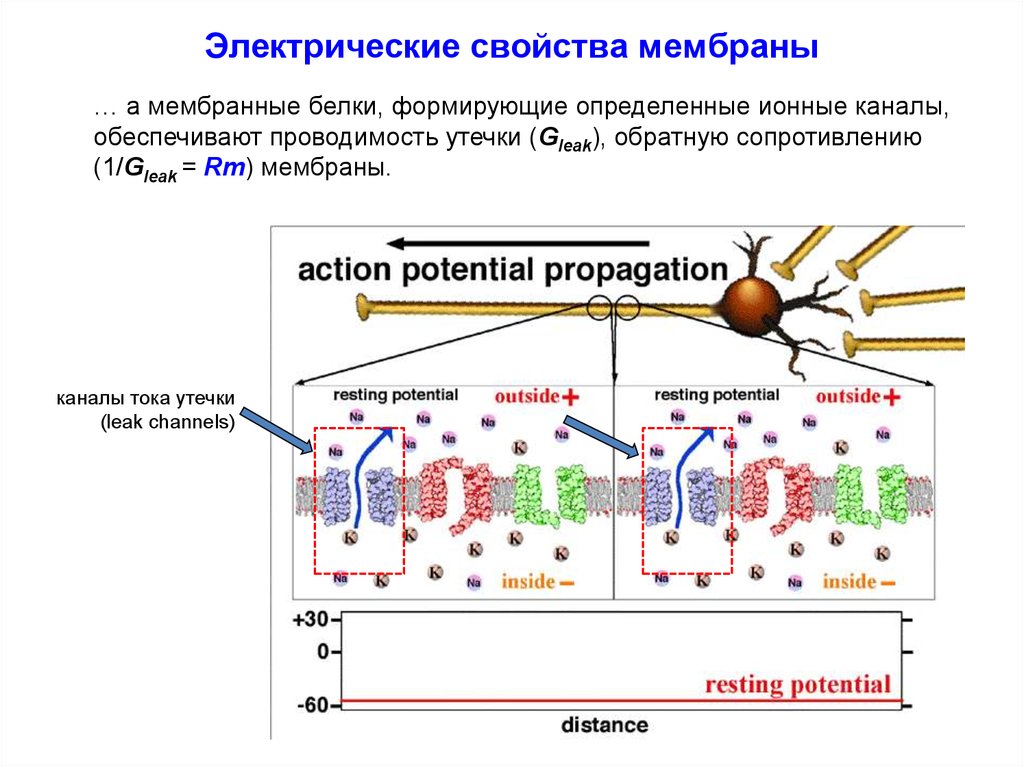
21.
Электрические свойства мембраны… а мембранные белки, формирующие определенные ионные каналы,
обеспечивают проводимость утечки (Gleak), обратную сопротивлению
(1/Gleak = Rm) мембраны.
каналы тока утечки
(leak channels)
22. Фосфолипиды клеточной мембраны
• Крайне тонкий и текучий липидный бислой клеточной мембраныхарактеризуется мембранной емкостью порядка 1 мкФ/см2,
которая обеспечивает заряд 8 10-9 кулонов/см2 при мембранном
потенциале -80 мВ, что эквивалентно заряду 5 1011
одновалентных ионов/см2.
• Даже в покое в мембране открыты каналы для ионов K+ и Na+,
поэтому мембрана демонстрирует проводимость утечки. Как
отражение свойства проводимости мембрана обладает
сопротивлением около 1000 Ом●см2.
23. Фосфолипиды клеточной мембраны
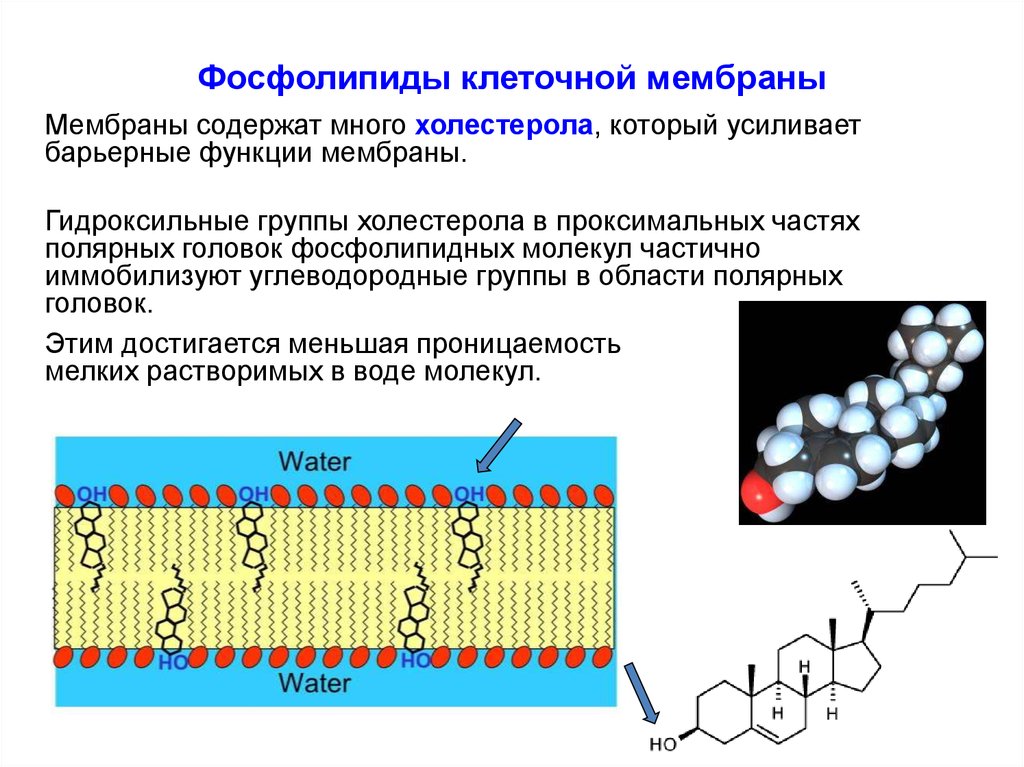
Мембраны содержат много холестерола, который усиливаетбарьерные функции мембраны.
Гидроксильные группы холестерола в проксимальных частях
полярных головок фосфолипидных молекул частично
иммобилизуют углеводородные группы в области полярных
головок.
Этим достигается меньшая проницаемость
мелких растворимых в воде молекул.
24. Фосфолипиды клеточной мембраны
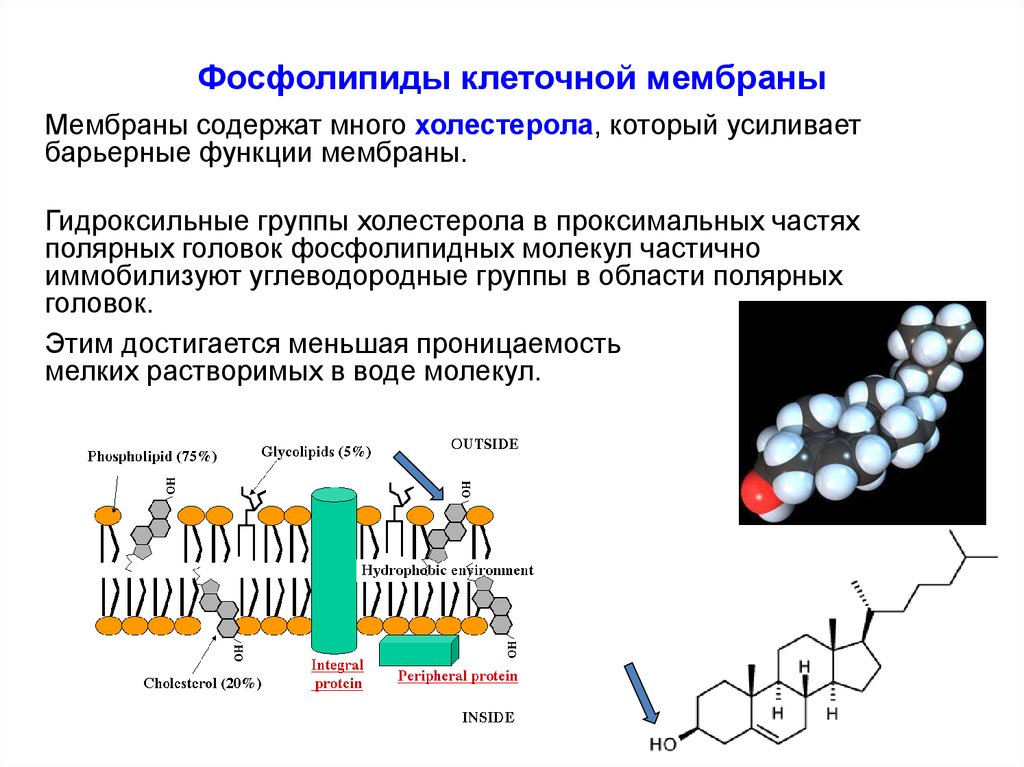
Мембраны содержат много холестерола, который усиливаетбарьерные функции мембраны.
Гидроксильные группы холестерола в проксимальных частях
полярных головок фосфолипидных молекул частично
иммобилизуют углеводородные группы в области полярных
головок.
Этим достигается меньшая проницаемость
мелких растворимых в воде молекул.
25.
26. Гликолипиды и ганглиозиды клеточной мембраны
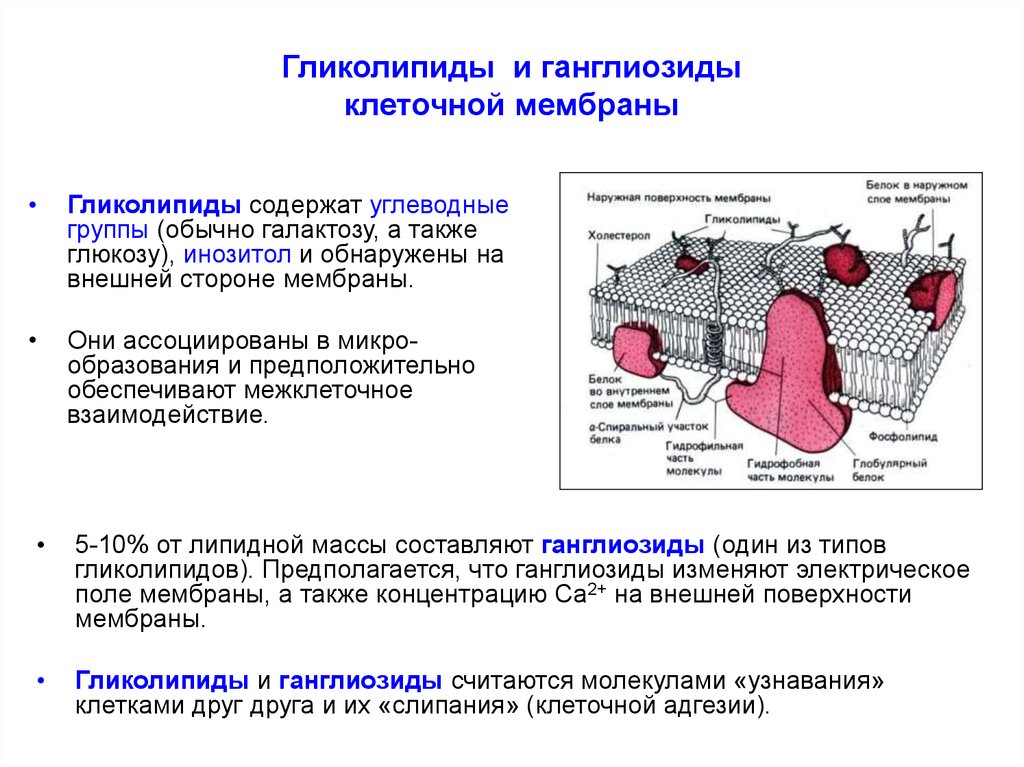
Гликолипиды содержат углеводные
группы (обычно галактозу, а также
глюкозу), инозитол и обнаружены на
внешней стороне мембраны.
Они ассоциированы в микрообразования и предположительно
обеспечивают межклеточное
взаимодействие.
5-10% от липидной массы составляют ганглиозиды (один из типов
гликолипидов). Предполагается, что ганглиозиды изменяют электрическое
поле мембраны, а также концентрацию Са2+ на внешней поверхности
мембраны.
Гликолипиды и ганглиозиды считаются молекулами «узнавания»
клетками друг друга и их «слипания» (клеточной адгезии).
27. Белки клеточной мембраны
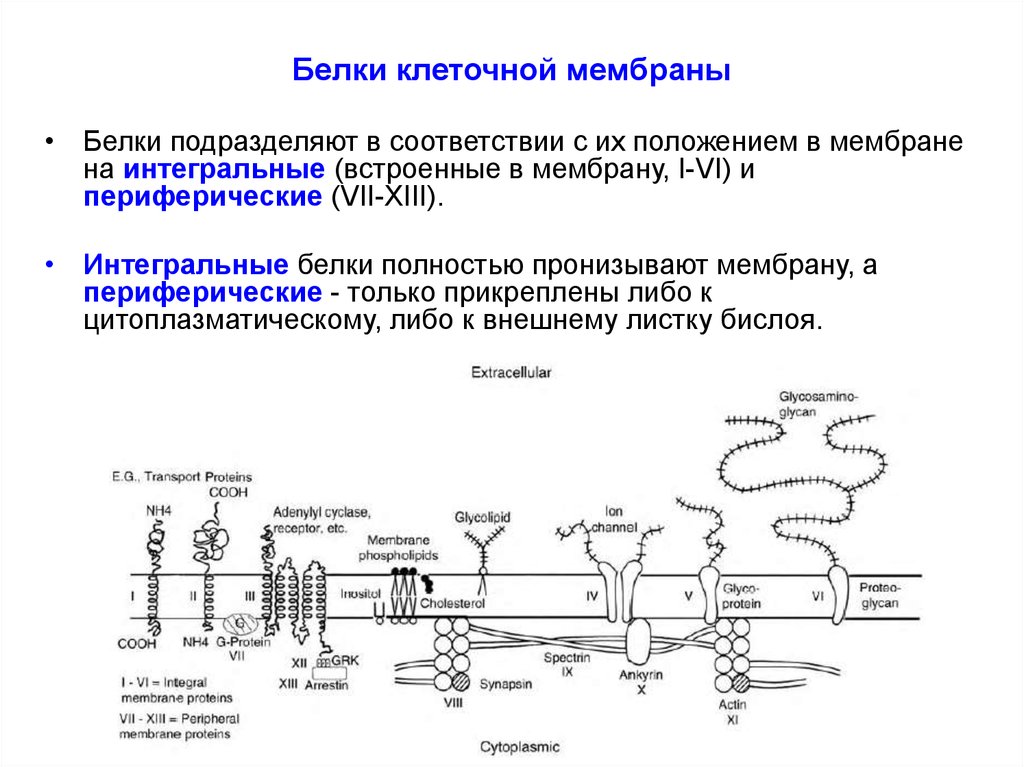
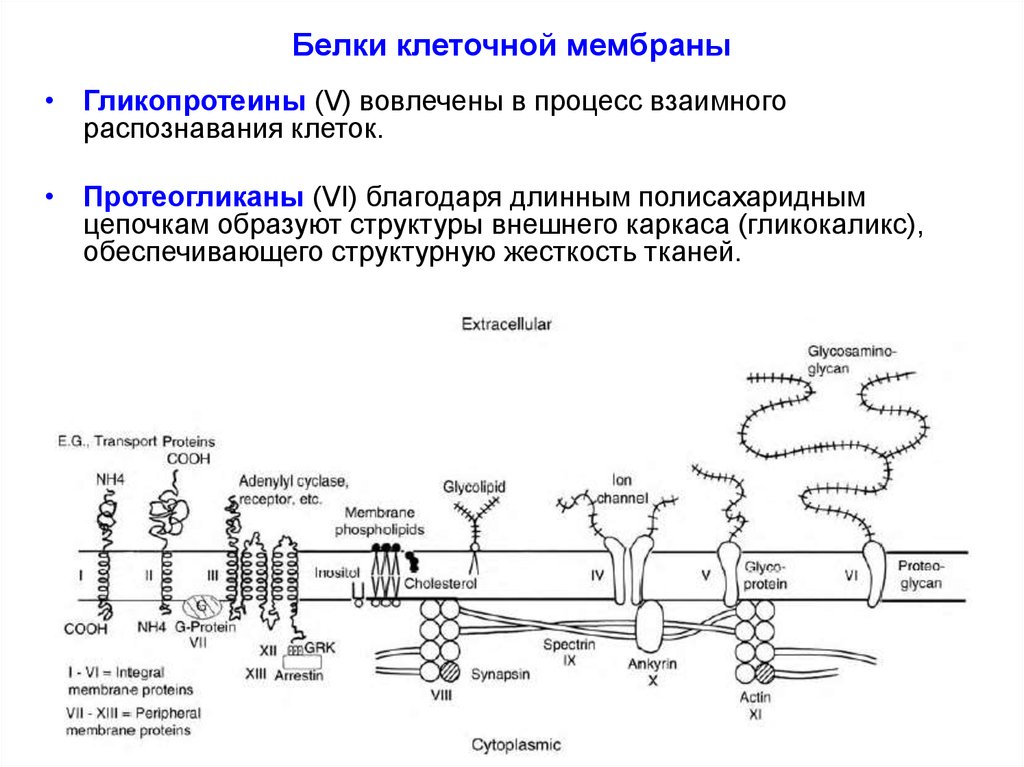
• Белки подразделяют в соответствии с их положением в мембранена интегральные (встроенные в мембрану, I-VI) и
периферические (VII-XIII).
• Интегральные белки полностью пронизывают мембрану, а
периферические - только прикреплены либо к
цитоплазматическому, либо к внешнему листку бислоя.
28. Белки клеточной мембраны
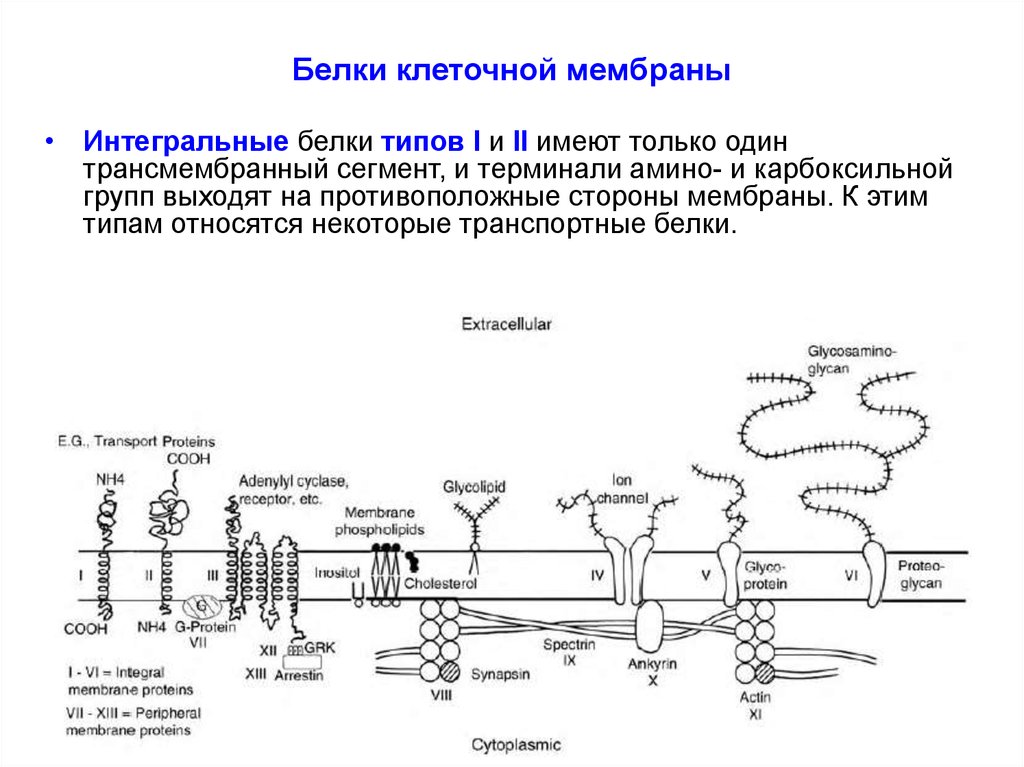
• Интегральные белки типов I и II имеют только одинтрансмембранный сегмент, и терминали амино- и карбоксильной
групп выходят на противоположные стороны мембраны. К этим
типам относятся некоторые транспортные белки.
29. Белки клеточной мембраны
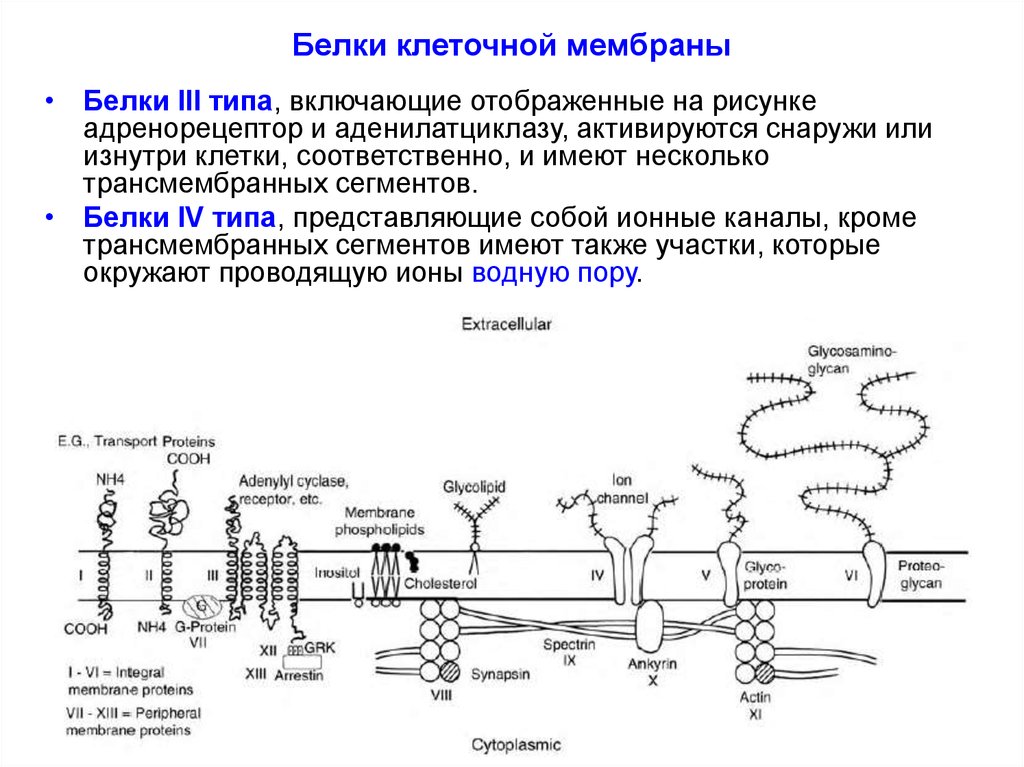
• Белки III типа, включающие отображенные на рисункеадренорецептор и аденилатциклазу, активируются снаружи или
изнутри клетки, соответственно, и имеют несколько
трансмембранных сегментов.
• Белки IV типа, представляющие собой ионные каналы, кроме
трансмембранных сегментов имеют также участки, которые
окружают проводящую ионы водную пору.
30. Белки клеточной мембраны
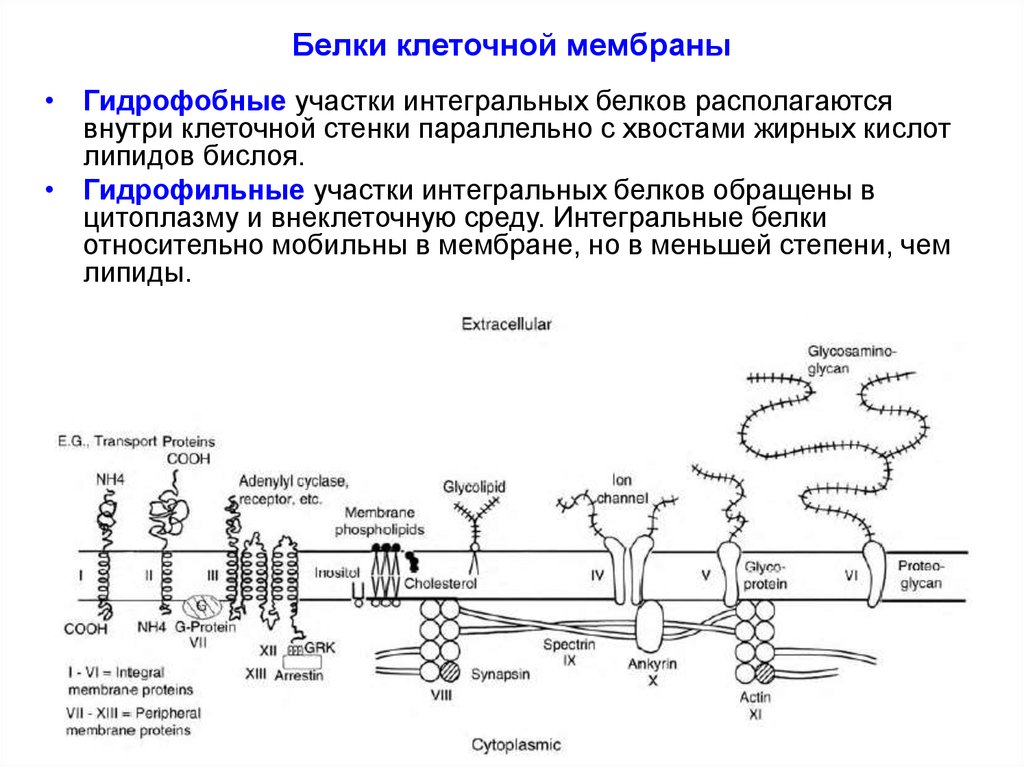
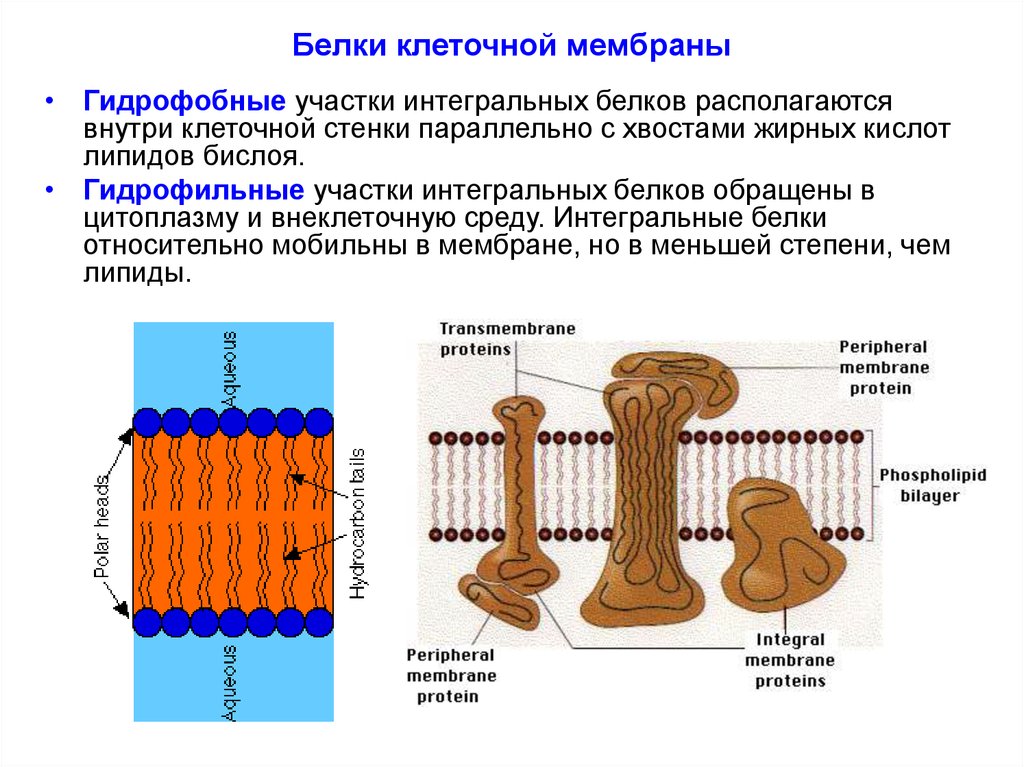
• Гидрофобные участки интегральных белков располагаютсявнутри клеточной стенки параллельно с хвостами жирных кислот
липидов бислоя.
• Гидрофильные участки интегральных белков обращены в
цитоплазму и внеклеточную среду. Интегральные белки
относительно мобильны в мембране, но в меньшей степени, чем
липиды.
31. Белки клеточной мембраны
• Гидрофобные участки интегральных белков располагаютсявнутри клеточной стенки параллельно с хвостами жирных кислот
липидов бислоя.
• Гидрофильные участки интегральных белков обращены в
цитоплазму и внеклеточную среду. Интегральные белки
относительно мобильны в мембране, но в меньшей степени, чем
липиды.
32. Интегральные белки в мембране выполняют следующие функции
Транспортная функция. Ионные помпы (системы первичного
активного транспорта) и обменники (системы вторичного активного
транспорта) транспортируют ионы против их химических градиентов
используя при этом энергию АТФ и энергию градиентов других ионов,
соответственно.
Ионные каналы обеспечивают проводимость растворенных в воде
некоторых ионов по их электрохимическим градиентам.
Транспортируют сахара и аминокислоты.
Обеспечивают распознавание клеток друг друга при образовании
клеточных агрегатов.
Рецепторы нейромедиаторов, нейромодуляторов, гормонов и других
химических передатчиков управляют проницаемостью ионов.
Роль ферментов, катализирующих внутриклеточные каскады.
Иммунореактивные элементы.
33. Белки клеточной мембраны
• Гликопротеины (V) вовлечены в процесс взаимногораспознавания клеток.
• Протеогликаны (VI) благодаря длинным полисахаридным
цепочкам образуют структуры внешнего каркаса (гликокаликс),
обеспечивающего структурную жесткость тканей.
34. Периферические белки в мембране выполняют следующие функции:
Роль ферментов, катализирующих внутриклеточные каскады
(например G-белки - VII).
Поддержание мембранной структуры (белки актин - XI, анкирин
- X, фодрин, спектрин -IX).
Связывают везикулы с элементами цитоскелета (например,
синапсин - VIII).
Посредники роста и развития дендритов и аксонов.
Обеспечивают процесс мембранного обмена – рециклирование
лиганд-активируемых рецепторов и синаптических везикул
(например, аррестин, клатрин - XIII).
Обеспечивают процесс отщепления G-белка от рецептора (Gprotein receptor kinase, GRK - XII).
35. Основные биологические процессы, происходящие с использованием ионных градиентов
• Генерация электрического сигнала за счет градиента ионов Na+или (и) Ca2+.
• Хемоосмотическое преобразование энергии - протонный градиент
в митохондриях (теория Митчела). Существует специальный
транспорт протонов (Н+), они выводятся из митохондрий в
цитоплазму. Протонный градиент (градиент РН), как источник
запасенной энергии, используется для окислительного
фосфорилирования (АДФ -> АТФ).
• Транспорт веществ против градиента концентрации.
Осуществляется за счет перемещения другого вещества по
концентрационному градиенту. Например, за счет градиента Na+
через клеточную мембрану транспортируются сахара и
аминокислоты.
36.
Потенциал покояBernstein's Hypothesis
Bernstein's hypothesis was proposed in the following article:
Bernstein, J. (1902).
Untersuchungen zur Thermodynamik der bioelektrischen Strome.
Pflfigers Arch. ges. Physiol.92: 521-562
Sir Andrew Huxley comments on Bernstein's hypothesis are as follows:
1839-1917
"The most widely accepted theory of excitation and conduction in excitable cells at that
time (from early in this century until the late 1930s, ed. note) was that of Bernstein
(1902), according to which the resting potential (inside 50-100 mV negative relative to
the external solution) was a concentration potential due to the membrane being
appreciably permeable to potassium (K+) (but not to sodium (Na+)) ions while the
concentration of potassium inside was around 50 times that in the external solution;
excitation consisted in a great increase of the permeability of the membrane to all ions
so that the membrane potential would fall nearly to zero. Current would then
flow from adjacent regions of the cell, causing a decrease in the absolute value of the
membrane potential there and this in turn was assumed to cause a similar increase of
permeability, which thus travelled along the cell as a self-propagating wave."
Huxley, Sir Andrew (1992).
Kenneth Stewart Cole
Biographical Memoirs of Fellows of the Royal Society 38: 99-110. p. 104
37.
38.
Bernstein J (1868) Über den zeitlichenVerlauf der negative Schwankung des
Nervenstroms. Pflügers Arch 1:173–207
39.
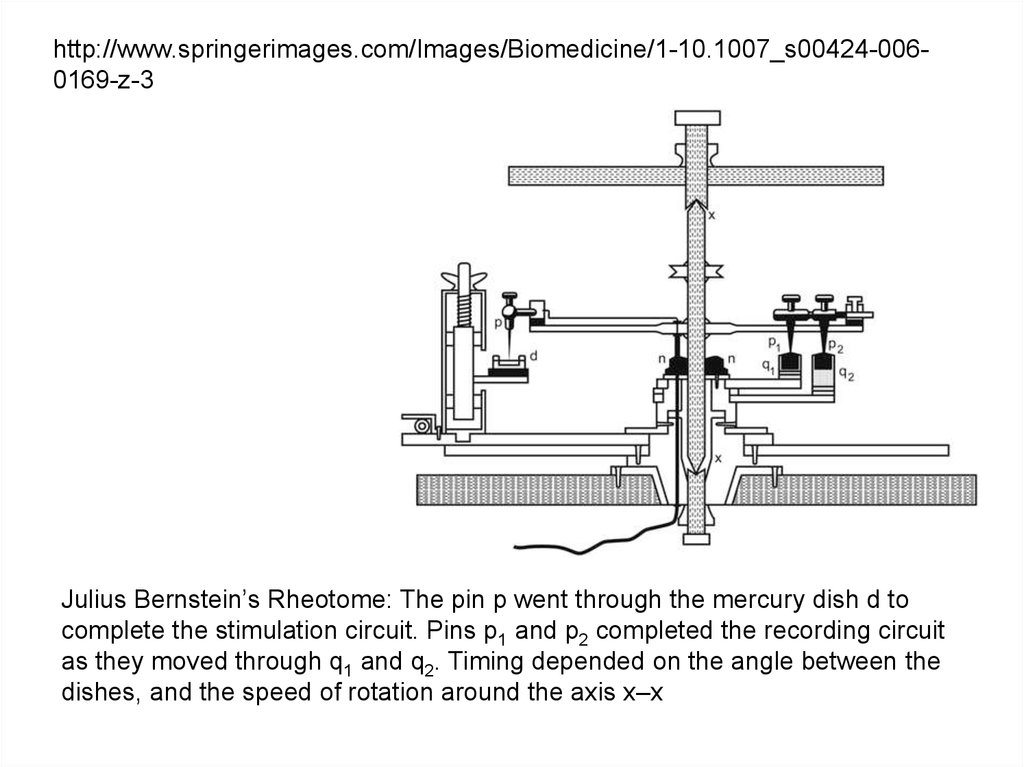
http://www.springerimages.com/Images/Biomedicine/1-10.1007_s00424-0060169-z-3Julius Bernstein’s Rheotome: The pin p went through the mercury dish d to
complete the stimulation circuit. Pins p1 and p2 completed the recording circuit
as they moved through q1 and q2. Timing depended on the angle between the
dishes, and the speed of rotation around the axis x–x
40.
First recording of action potential fromthe nerve made by Julius Bernstein;
original images were kindly provided
by Prof. Bernd Nilius, University of
Leuven.
a The Bernstein rheotome;
b the recording of an action potential.
The τ1 and τ2 indicate “sampling”
intervals of the rheotome; the duration
m–o is the duration of action potential
[“negative Schwankung”, and n is the
“sign reversal” (overshoot)]
Bernstein J (1868)
Über den zeitlichen Verlauf der negativen
Schwankung des Nervenstroms.
Pflügers Arch 1:173–207
41.
Потенциал покояПотенциал покоя – это разность потенциалов между цитоплазмой клетки и
окружающей средой.
42.
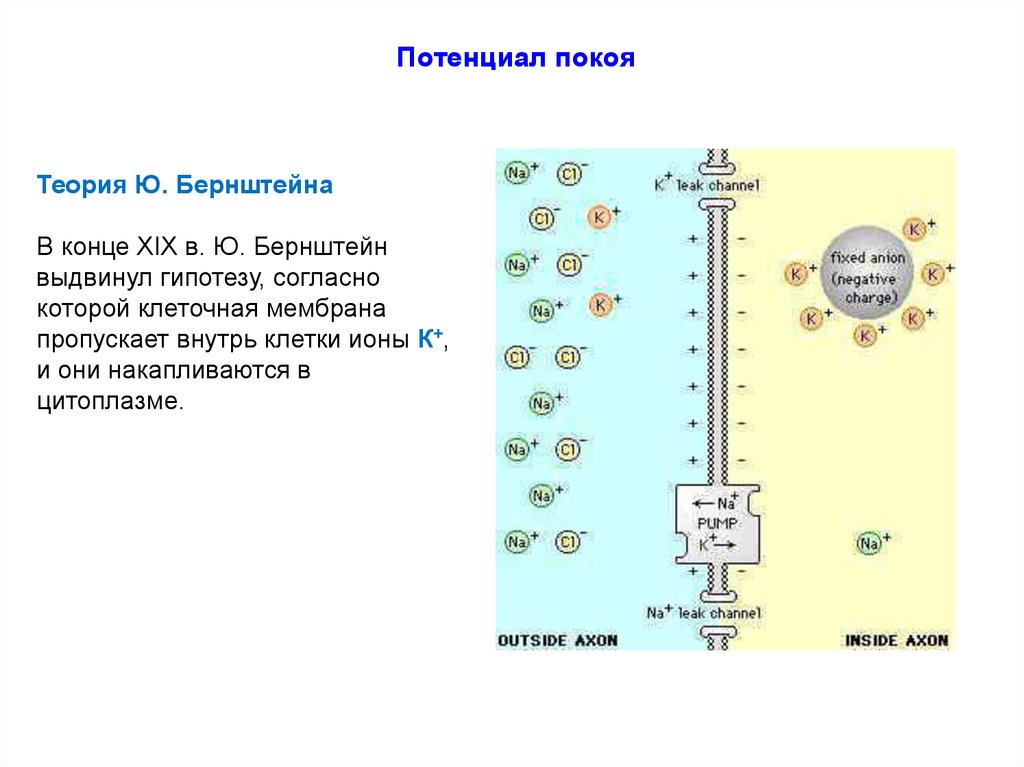
Потенциал покояТеория Ю. Бернштейна
В конце XIX в. Ю. Бернштейн
выдвинул гипотезу, согласно
которой клеточная мембрана
пропускает внутрь клетки ионы К+,
и они накапливаются в
цитоплазме.
43.
Потенциал покоя44.
Потенциал покояПотенциал покоя – это разность потенциалов между цитоплазмой клетки и
окружающей средой.
Теория Ю. Бернштейна
В конце XIX в. Ю. Бернштейн выдвинул гипотезу, согласно которой клеточная
мембрана пропускает внутрь клетки ионы К+, и они накапливаются в
цитоплазме.
В 1896 г. его ученик Василий Чаговец (1873-1941) подтвердил эту гипотезу и
применил электролитическую теорию В. Нернста к биологическим системам и
установил калиевую природу потенциала покоя.
Расчет величины потенциала покоя по уравнению Нернста для калиевого
электрода удовлетворительно совпал с измеренным потенциалом между
саркоплазмой мышцы и окружающей средой, который составлял около – 70 мВ.
[K+]in
RT
EK+ = -
ln
nF
[K+]out
45. Представления о возбуждении мышцы
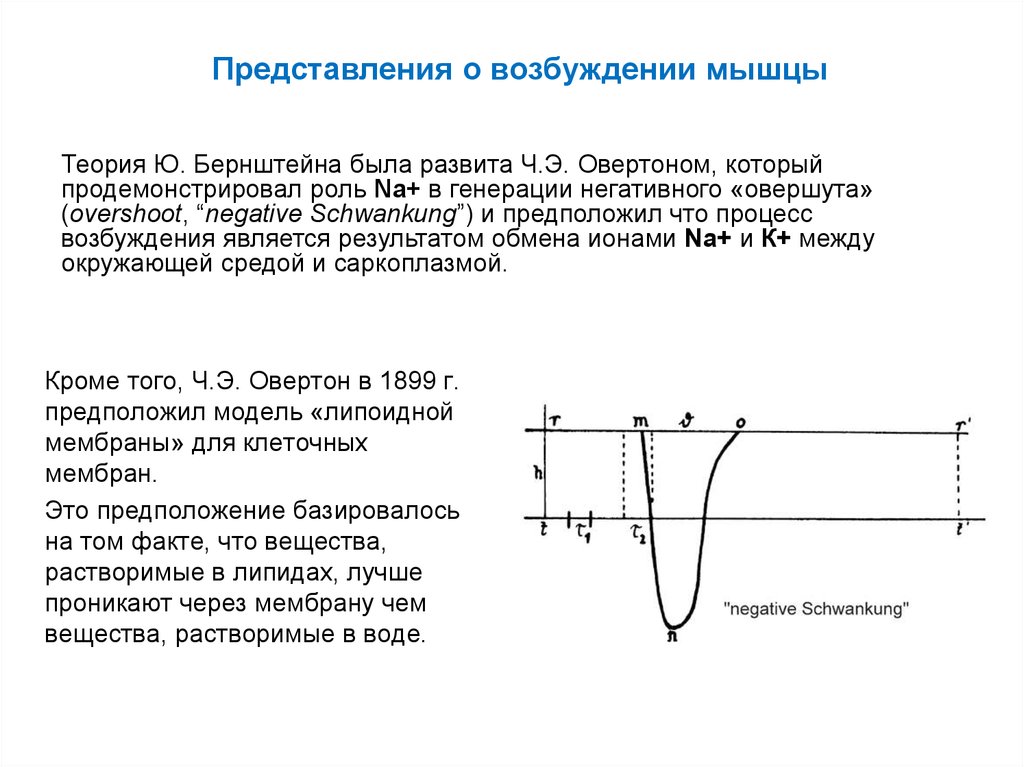
Теория Ю. Бернштейна была развита Ч.Э. Овертоном, которыйпродемонстрировал роль Na+ в генерации негативного «овершута»
(overshoot, “negative Schwankung”) и предположил что процесс
возбуждения является результатом обмена ионами Na+ и К+ между
окружающей средой и саркоплазмой.
Кроме того, Ч.Э. Овертон в 1899 г.
предположил модель «липоидной
мембраны» для клеточных
мембран.
Это предположение базировалось
на том факте, что вещества,
растворимые в липидах, лучше
проникают через мембрану чем
вещества, растворимые в воде.
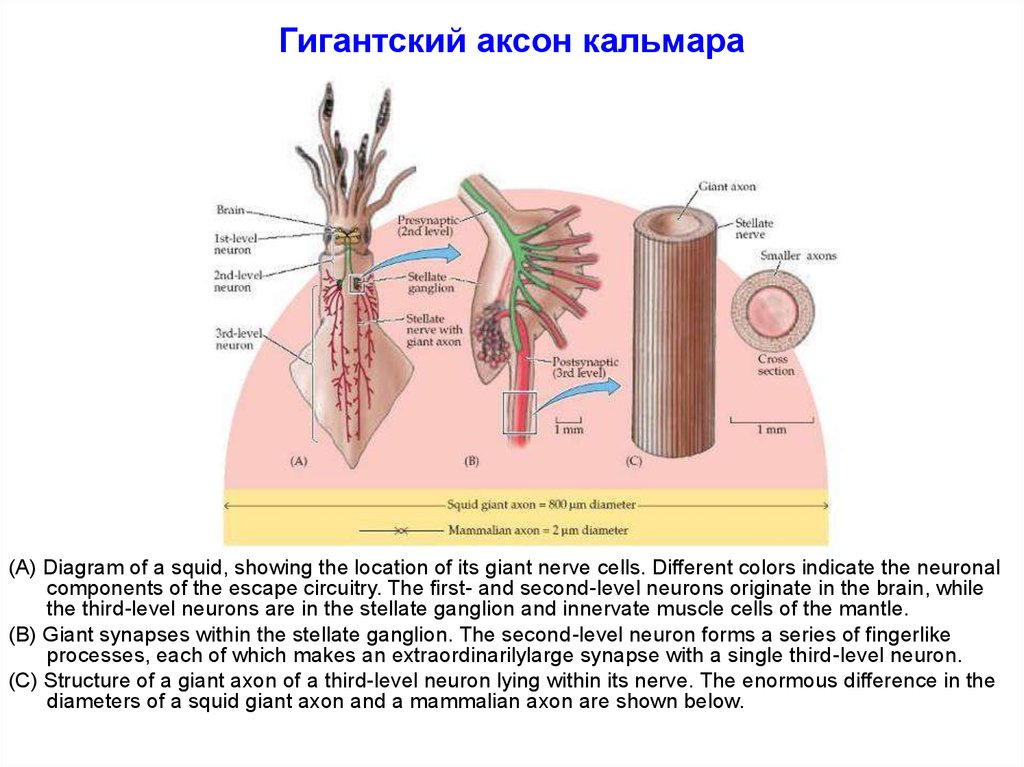
46. Гигантский аксон кальмара
(A) Diagram of a squid, showing the location of its giant nerve cells. Different colors indicate the neuronalcomponents of the escape circuitry. The first- and second-level neurons originate in the brain, while
the third-level neurons are in the stellate ganglion and innervate muscle cells of the mantle.
(B) Giant synapses within the stellate ganglion. The second-level neuron forms a series of fingerlike
processes, each of which makes an extraordinarilylarge synapse with a single third-level neuron.
(C) Structure of a giant axon of a third-level neuron lying within its nerve. The enormous difference in the
diameters of a squid giant axon and a mammalian axon are shown below.
47.
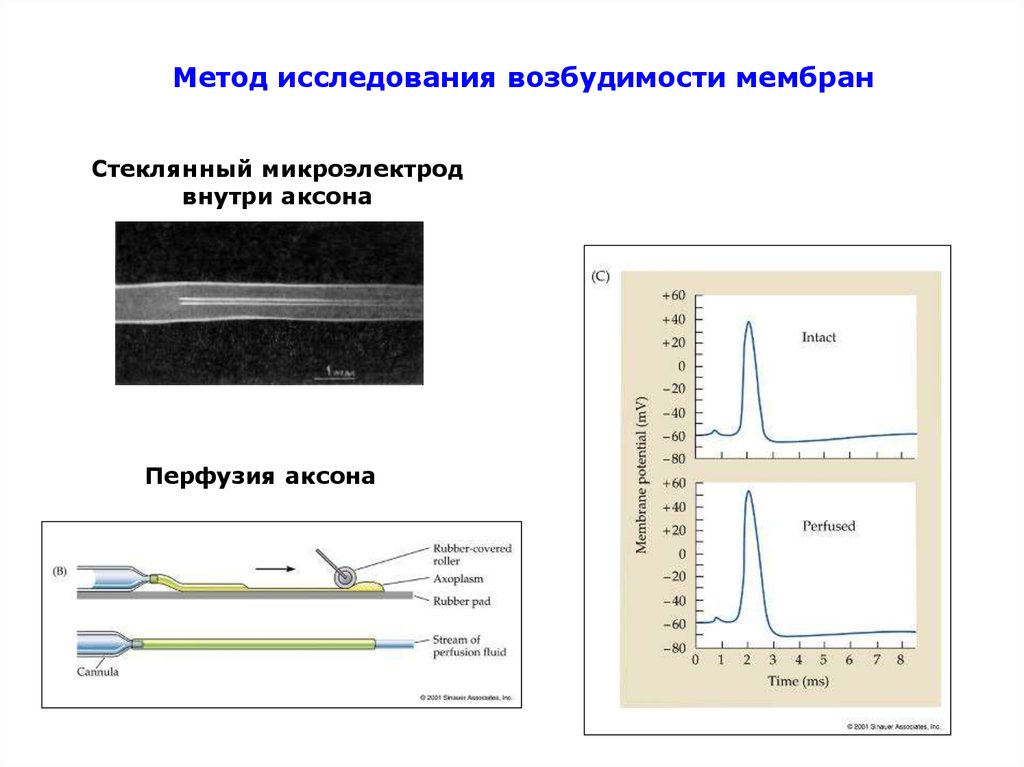
Метод исследования возбудимости мембранСтеклянный микроэлектрод
внутри аксона
Перфузия аксона
48.
Подтверждение теории Ю. Берштейна для нейроновKenneth Stewart Cole (July 10,1900 - April 18, 1984) was
affectionately known as "Kacy" by his colleagues and
friends. Others, hearing this nickname, assumed that this
stood for his initials and refer to him as K. C. Cole. Here
is a photo of Kacy on his 65th birthday (a present to one
of the authors, JWM, who worked with Kacy).
Kacy's most famous illustration shows
simultaneous records of the action potential
and the associated impedance change in a
squid axon (with Curtis in 1939, J. Gen.
Physiol. 22: 649). This elegant figure is
known internationally and is widely used.
With an electrode inserted along the axis of a
squid giant axon, Cole and Curtis demonstrated
with this famous figure a dramatic conductance
increase during a nerve impulse. A resistance
of about 1000 ohm/cm2 at rest dropped
during the action potential to the very low
value of about 25 ohm/cm2.
49.
Подтверждение теории Ю. Берштейна для нейроновFor example, it is the logo for the Membrane
Biophysics Group of the Biophysical Society and
is on its K. S. Cole Award medal.
And Kacy loved to brag that it appeared,
rotated 90 degrees as below, in Swedish
apartments as modern art!
50.
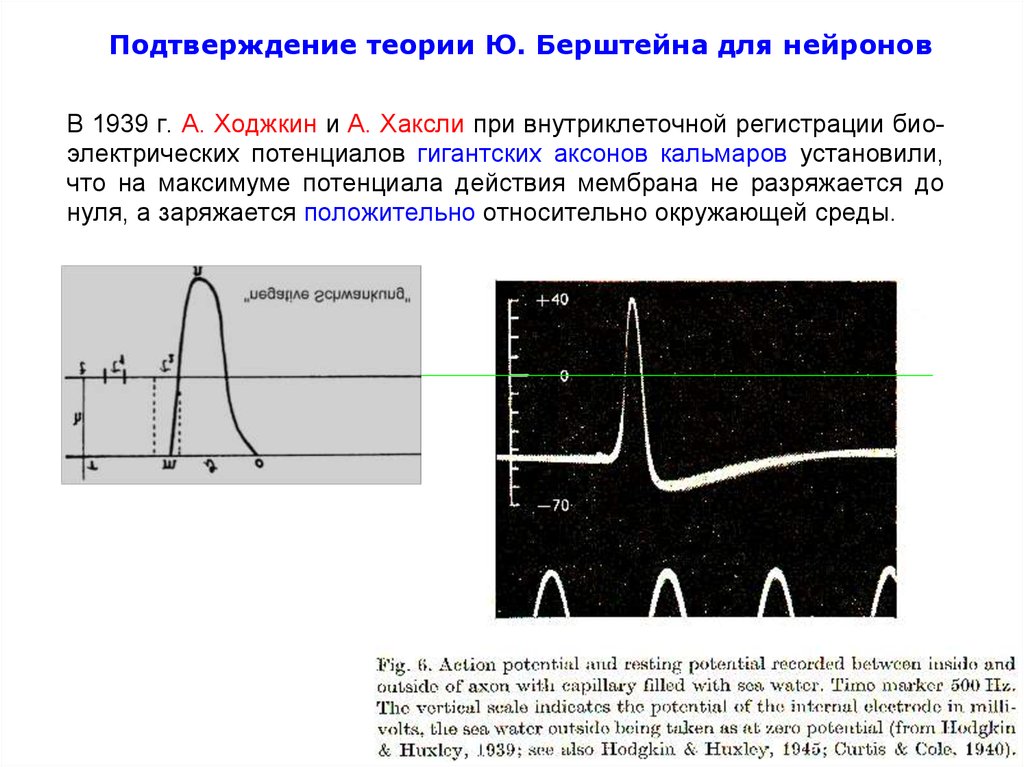
аПодтверждение теории Ю. Берштейна для нейронов
В 1939 г. А. Ходжкин и А. Хаксли при внутриклеточной регистрации биоэлектрических потенциалов гигантских аксонов кальмаров установили,
что на максимуме потенциала действия мембрана не разряжается до
нуля, а заряжается положительно относительно окружающей среды.
51.
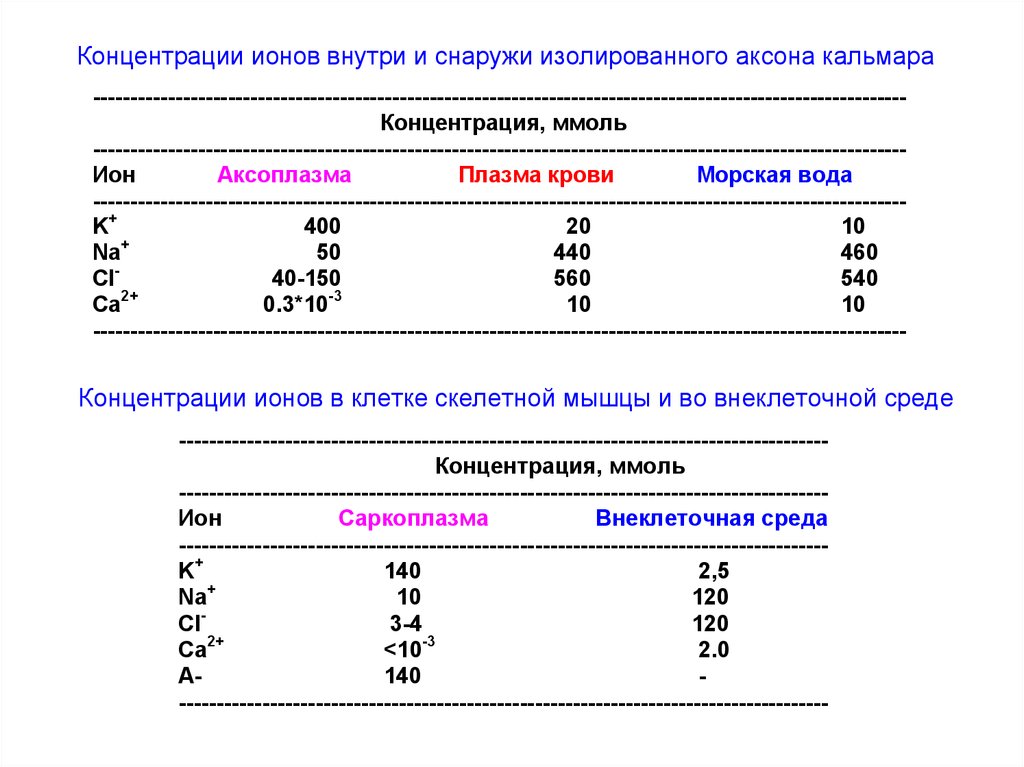
Концентрации ионов внутри и снаружи изолированного аксона кальмара------------------------------------------------------------------------------------------------------------Концентрация, ммоль
------------------------------------------------------------------------------------------------------------Ион
Аксоплазма
Плазма крови
Морская вода
------------------------------------------------------------------------------------------------------------K+
400
20
10
+
Na
50
440
460
Cl
40-150
560
540
2+
-3
Ca
0.3*10
10
10
-------------------------------------------------------------------------------------------------------------
Концентрации ионов в клетке скелетной мышцы и во внеклеточной среде
-------------------------------------------------------------------------------------Концентрация, ммоль
-------------------------------------------------------------------------------------Ион
Саркоплазма
Внеклеточная среда
-------------------------------------------------------------------------------------K+
140
2,5
+
Na
10
120
Cl
3-4
120
2+
-3
Ca
<10
2.0
A140
--------------------------------------------------------------------------------------
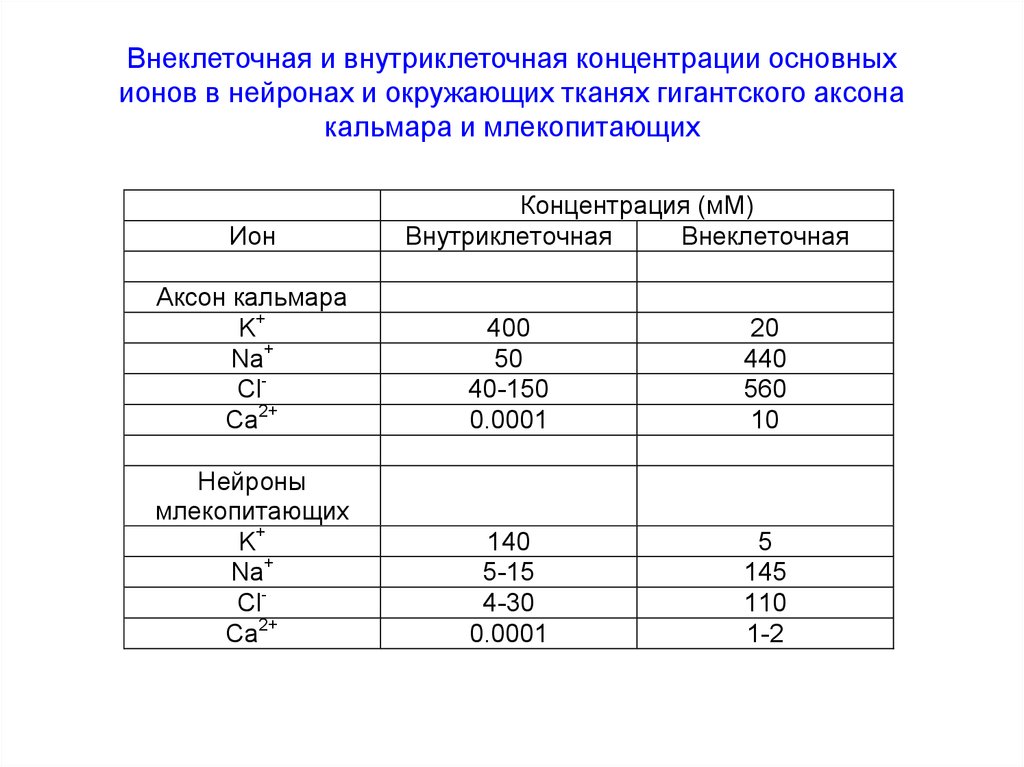
52. Внеклеточная и внутриклеточная концентрации основных ионов в нейронах и окружающих тканях гигантского аксона кальмара и млекопитающих
ИонКонцентрация (мМ)
Внутриклеточная
Внеклеточная
Аксон кальмара
K+
Na+
ClCa2+
400
50
40-150
0.0001
20
440
560
10
Нейроны
млекопитающих
K+
Na+
ClCa2+
140
5-15
4-30
0.0001
5
145
110
1-2
53.
Концентрации ионов внутри и снаружинейронов млекопитающих
Концентрация ионов (в мМ) приведена в
скобках (для Са2+ внутриклеточная
концентрация указана в мкМ).
Концентрации ионов внутри и снаружи
изолированного аксона кальмара
(повторяется для сравнения)
------------------------------------------------------------------------------------------------------------Концентрация, ммоль
------------------------------------------------------------------------------------------------------------Ион
Аксоплазма
Плазма крови
Морская вода
------------------------------------------------------------------------------------------------------------K+
400
20
10
Na+
50
440
460
Cl40-150
560
540
Ca2+
0.3*10-3
10
10
-------------------------------------------------------------------------------------------------------------
RT
Ec = -
Cin
ln
nF
Cout
Cin/out – концентрация какого-либо иона
внутри (in) и снаружи (out) нейрона.
54.
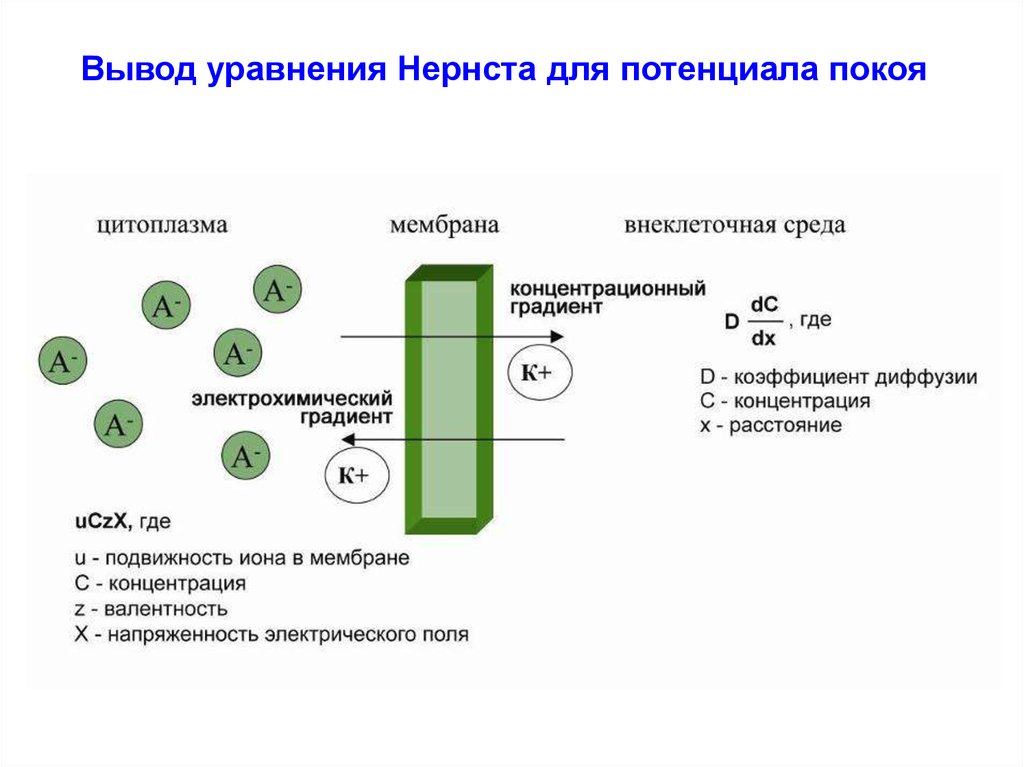
Распределение ионов по обе стороны мембраны55. Вывод уравнения Нернста для потенциала покоя
56.
Сила электрического поля уравновешивается силой диффузии ионов:dC
D
= - uCzX
dx
D = ukT, где
Соотношение А. Энштейна:
k – постоянная Больцмана;
T – абсолютная температура
dC
ukT
kT dC
= - uCzX /u
Xdx = -
dx
Cin
EK+ =
Xdx
Cout
z
Cin kT dC
= -
Cout z
kT
=-
C
C
Cin
ln C
z
EK+ = -
Cin
ln
z
(ln Cin – ln Cout)
= Cout
kT
kT
Cout
z
57.
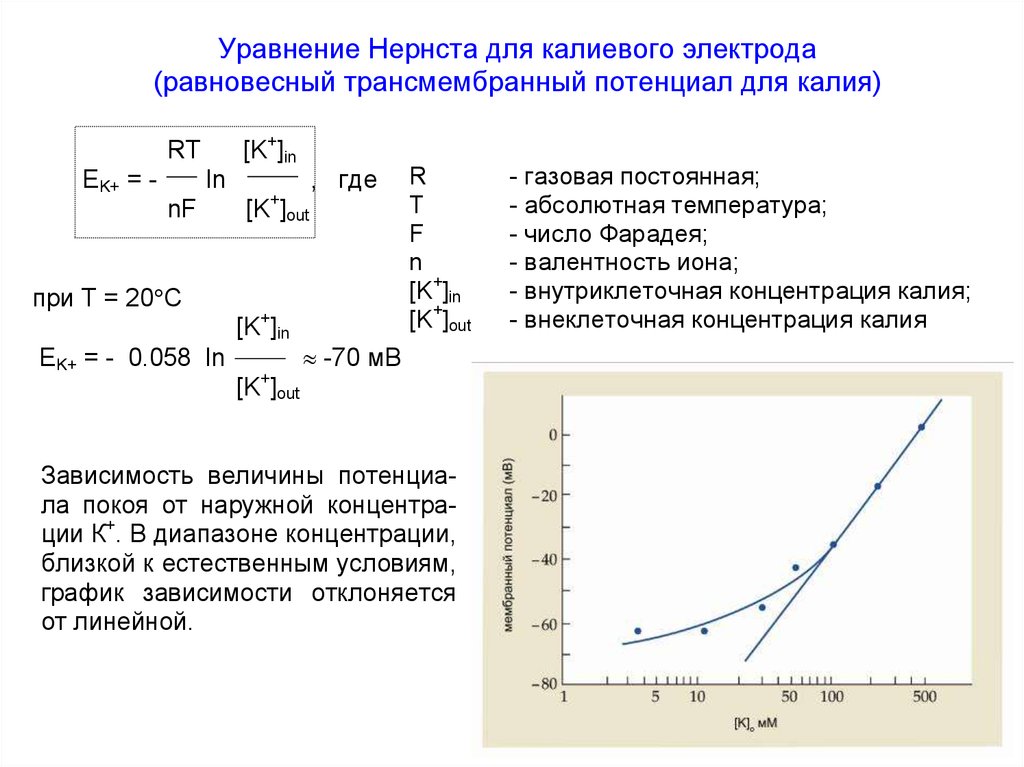
Уравнение Нернста для калиевого электрода(равновесный трансмембранный потенциал для калия)
[K+]in
RT
EK+ = -
, где
ln
nF
[K+]out
при Т = 20 С
[K+]in
EK+ = - 0.058 ln
R
T
F
n
[K+]in
[K+]out
-70 мВ
+
[K ]out
Зависимость величины потенциала покоя от наружной концентрации К+. В диапазоне концентрации,
близкой к естественным условиям,
график зависимости отклоняется
от линейной.
- газовая постоянная;
- абсолютная температура;
- число Фарадея;
- валентность иона;
- внутриклеточная концентрация калия;
- внеклеточная концентрация калия
58. Зависимость величины потенциала покоя от логарифма наружной концентрации ионов К+ ([K]out)
В соответствии с уравнением Нернста десятикратное
увеличение внеклеточной
концентрации ионов К+
(например, от 50 до 500 мМ)
приводит к снижению абсолютного значения ПП на 58
мВ.
Прямая линия на рисунке
отражает эту теоретическую
зависимость.
В действительности в
диапазоне концентраций
ионов К+, близких к естественным условиям (менее 50
мМ), график зависимости
отклоняется от линейной
функции из-за вклада в ПП
ионов Na+ и Cl-.
59.
Потенциал покоя нервной клетки определяется не только калиевым, но и натриевым и хлорным равновесными потенциалами:PK [K+]in + PNa [Na+]in
RT
EK+ = -
[ ]in
[ ]out
PCl [Cl-]out
ln
nF
P
+
,
+
+
PK [K ]out + PNa [Na ]out +
где
-
PCl [Cl ]in
- проницаемость (см/с) соответствующего иона через
клеточную мембрану;
- внутренняя
- и наружная концентрация соответствующего иона.
Расчетные проницаемости ионов соотносятся:
PK / PNa / PCl = 1.0 / 0.04 / 0.15
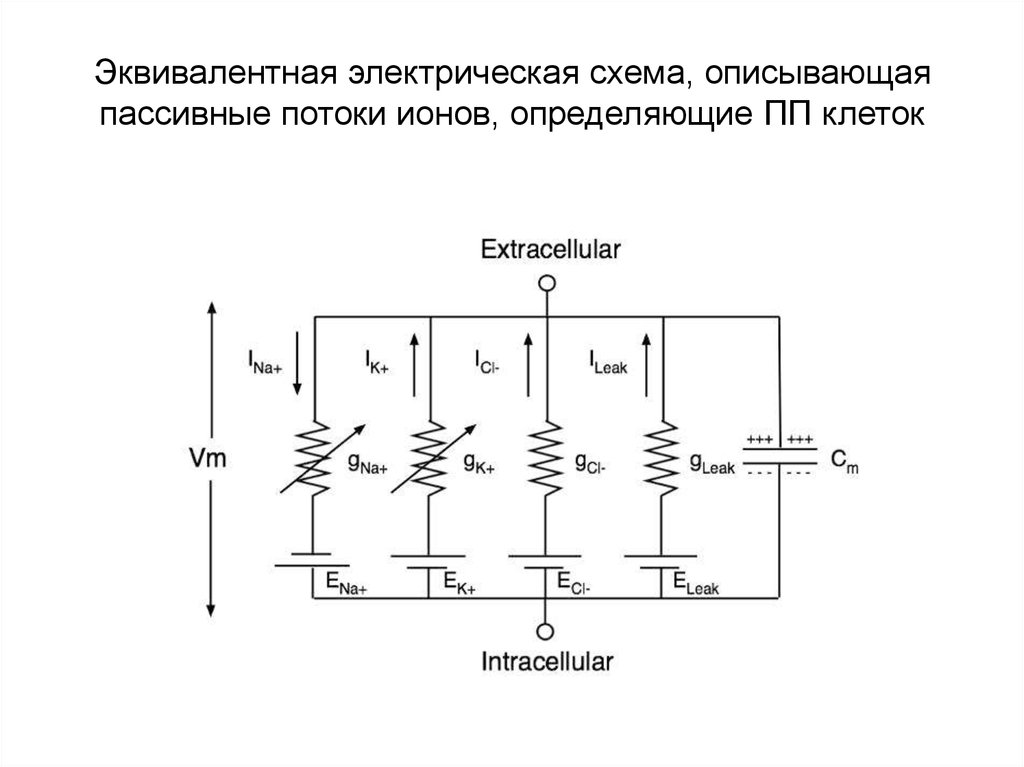
60. Эквивалентная электрическая схема, описывающая пассивные потоки ионов, определяющие ПП клеток
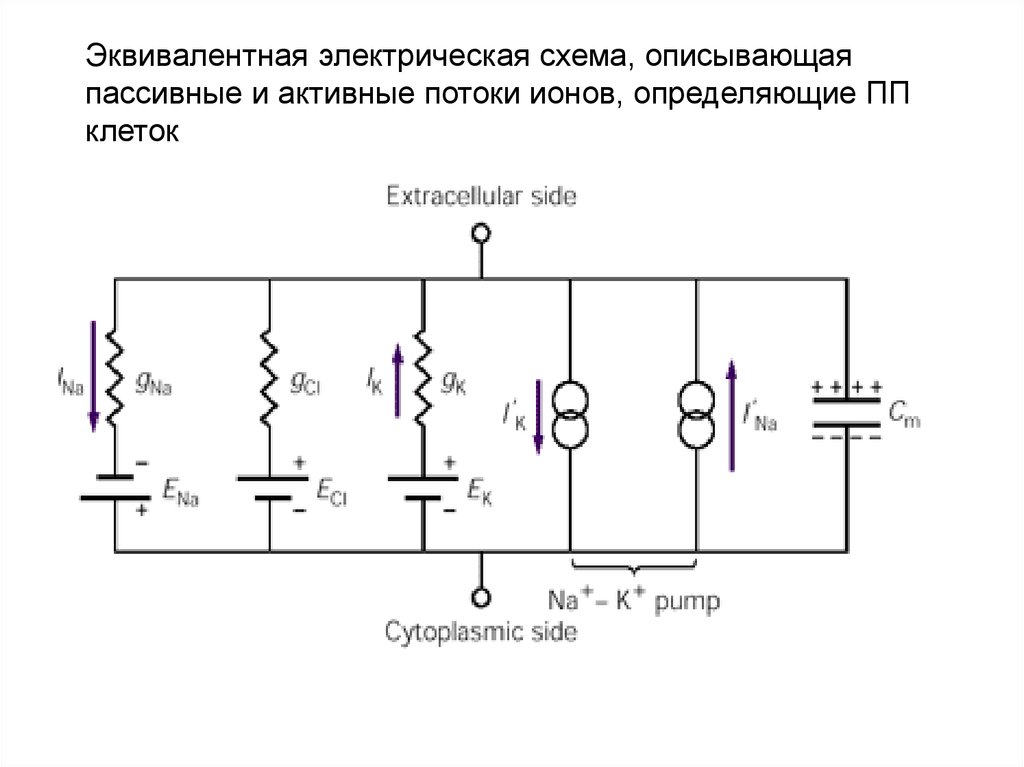
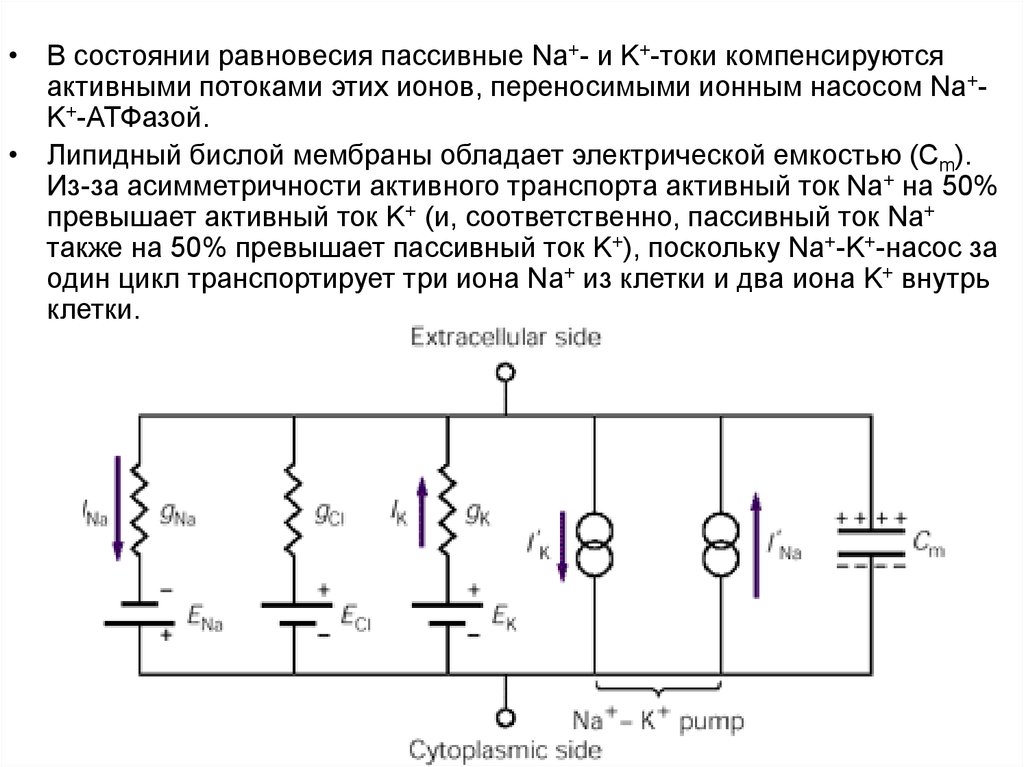
61. Эквивалентная электрическая схема, описывающая пассивные и активные потоки ионов, определяющие ПП клеток
62.
• В состоянии равновесия пассивные Na+- и K+-токи компенсируютсяактивными потоками этих ионов, переносимыми ионным насосом Na+K+-АТФазой.
• Липидный бислой мембраны обладает электрической емкостью (Cm).
Из-за асимметричности активного транспорта активный ток Na+ на 50%
превышает активный ток K+ (и, соответственно, пассивный ток Na+
также на 50% превышает пассивный ток K+), поскольку Na+-K+-насос за
один цикл транспортирует три иона Na+ из клетки и два иона K+ внутрь
клетки.


























![Зависимость величины потенциала покоя от логарифма наружной концентрации ионов К+ ([K]out) Зависимость величины потенциала покоя от логарифма наружной концентрации ионов К+ ([K]out)](https://cf.ppt-online.org/files/slide/o/OWDzHljhr5wyaMiQ9U3q87JYL2G0RPIe1Cmtvg/slide-57.jpg)

 Биология
Биология








