Похожие презентации:
Углеводороды. Арены (ароматические углеводороды)
1. Основы органической химии
E-mail: irkrav66@gmail.comОсновы
органической
химии
Семинар-10.
Углеводороды.Арены
(ароматические углеводороды)
лектор:
проф. Рохин Александр
Валерьевич
2. АРЕНЫ (ароматические углеводороды)
соединения, молекулы которыхсодержат устойчивые
циклические группы атомов
(бензольные ядра) с особым
характером химических связей.
Общая формула аренов:
2
27.07.2017
3. Простейшие представители
Одноядерные арены:С6Н6 – бензол
С7Н8 – толуол (метилбензол).
3
27.07.2017
4. Простейшие представители
Многоядерные арены:С10Н8 – нафталин
С14Н10 – антрацен и др.
4
27.07.2017
5. Арены
Ароматичность молекулы означаетее повышенную устойчивость,
обусловленную делокализацией pэлектронов в циклической системе.
Термин "ароматические соединения" возник
давно в связи с тем, что некоторые
представители этого ряда веществ имеют
приятный запах.
5
27.07.2017
6. Критерии ароматичности аренов:
Атомы углерода в sp2-гибридизованномсостоянии образуют циклическую
систему.
Атомы углерода располагаются в одной
плоскости (цикл имеет плоское
строение).
Замкнутая система сопряженных связей
содержит 4n+2π-электронов (n – целое
число)
6
27.07.2017
7. Строение бензола
Бензол С6Н6 – родоначальникароматических углеводородов.
Каждый из шести атомов углерода в его
молекуле находится в состоянии sp2гибридизации.
7
27.07.2017
8. Строение бензола
Валентные углы между каждой парой sсвязей равны 120°.скелет σ-связей представляет собой
правильный шестиугольник, в котором
все атомы углерода и все σ-связи С-С и
С-Н лежат в одной плоскости:
8
27.07.2017
9. Строение бензола
р-Электроны всех атомов углеродавзаимодействуют между собой путем
бокового перекрывания соседних 2р-АО,
расположенных перпендикулярно
плоскости σ-скелета бензольного
кольца.
9
27.07.2017
10. Строение бензола
Они образуют единое циклическое πэлектронное облако, сосредоточенноенад и под плоскостью кольца:
10
27.07.2017
11. Строение бензола
Все связи С-С в бензоле равноценны, ихдлина равна 0,140 нм, что
соответствует промежуточному значению
между длиной простой связи (0,154 нм)
и двойной (0,134 нм):
11
27.07.2017
12. Номенклатура аренов
Гомологи бензола – соединения,образованные заменой одного или
нескольких атомов водорода в
молекуле бензола на углеводородные
радикалы (R).
12
27.07.2017
13. Номенклатура аренов
Широко используются тривиальныеназвания (толуол, ксилол, кумол и
т.п.).
Систематические названия строят из
названия углеводородного радикала
(приставка) и слова бензол (корень):
13
27.07.2017
14. Номенклатура аренов
Если радикалов два или более, ихположение указывается номерами
атомов углерода в кольце, с которыми
они связаны.
Нумерацию кольца проводят так, чтобы
номера радикалов были наименьшими.
Например:
14
27.07.2017
15. Номенклатура аренов
Для дизамещенных бензолов R-C6H4-Rиспользуется также и другой способ
построения названий, при котором
положение заместителей указывают
перед тривиальным названием
соединения приставками:
орто- (о-);
мета- (м-);
пара- (п-)
15
27.07.2017
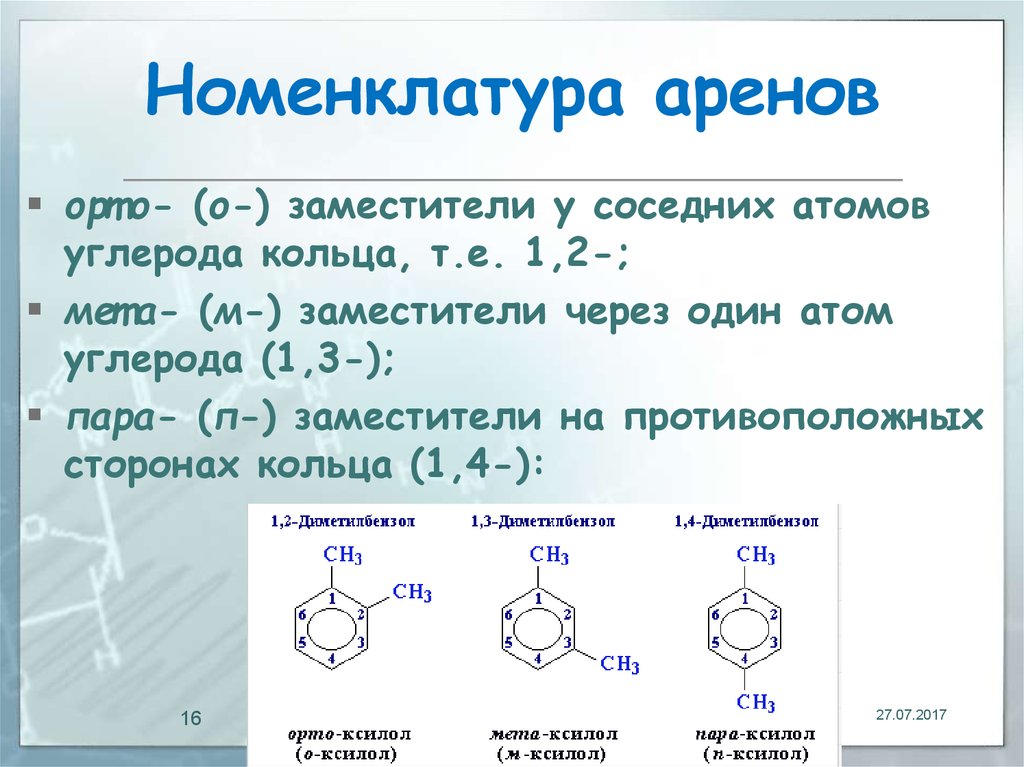
16. Номенклатура аренов
орт о- (о-) заместители у соседних атомовуглерода кольца, т.е. 1,2-;
мет а- (м-) заместители через один атом
углерода (1,3-);
пара- (п-) заместители на противоположных
сторонах кольца (1,4-):
16
27.07.2017
17. Номенклатура аренов
Ароматические одновалентные радикалыимеют общее название "арил".
Из них наиболее распространены в
номенклатуре органических соединений два:
C6H5- (фенил)
C6H5CH2- (бензил)
17
27.07.2017
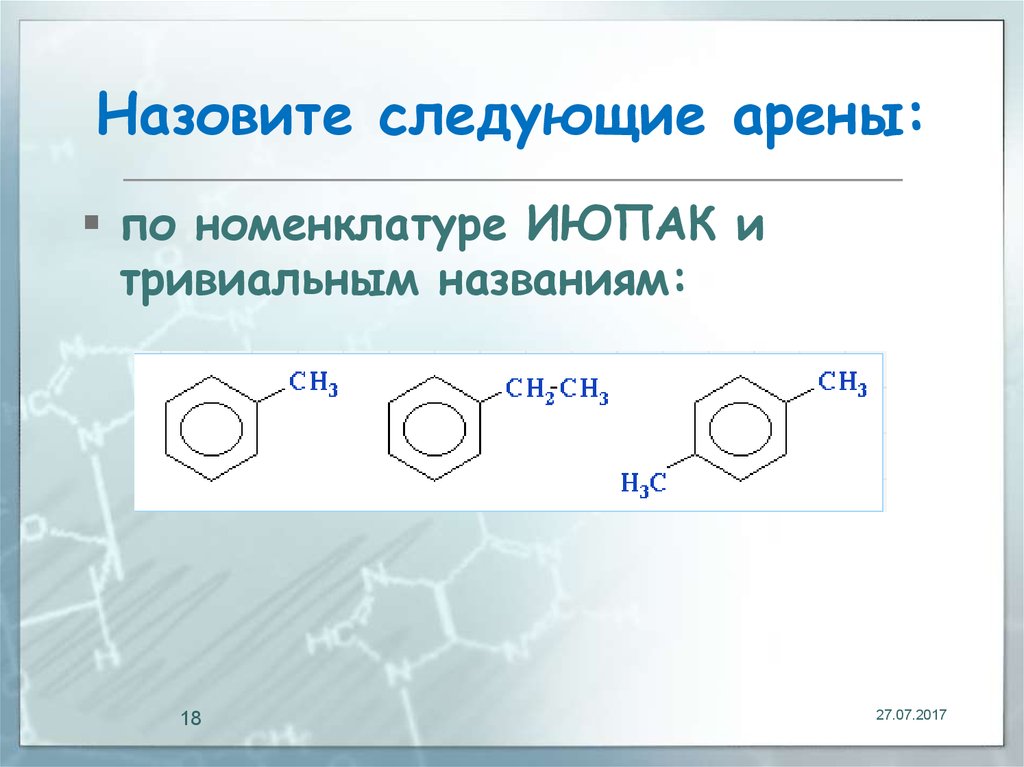
18. Назовите следующие арены:
по номенклатуре ИЮПАК итривиальным названиям:
18
27.07.2017
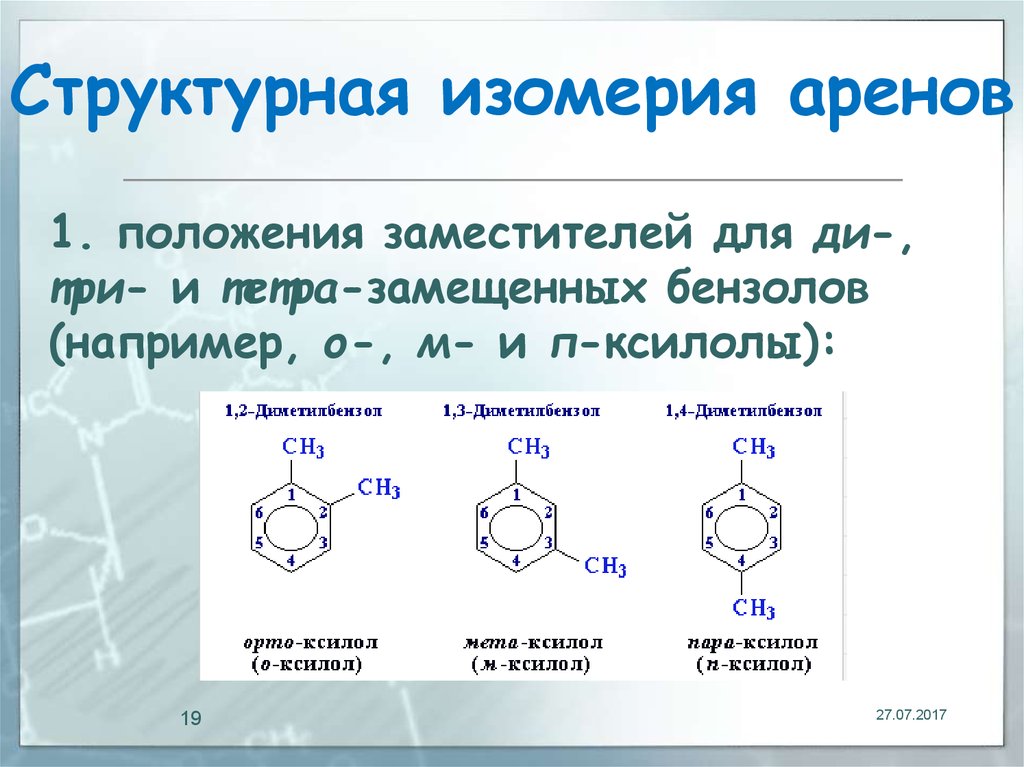
19. Структурная изомерия аренов
1. положения заместителей для ди-,три- и тетра-замещенных бензолов
(например, о-, м- и п-ксилолы):
19
27.07.2017
20. Структурная изомерия аренов
2. углеродного скелета в боковойцепи, содержащей не менее 3-х
атомов углерода:
20
27.07.2017
21. Структурная изомерия аренов
3. изомерия заместителей R, начинаяс R = С2Н5.
Например, молекулярной формуле
С8Н10 соответствует 4 изомера:
три ксилола CH3-C6H4-CH3 (о-, м-,
п-) и этилбензол C6H5-C2H5.
21
27.07.2017
22. Структурная изомерия аренов
4. Межклассовая изомерия снепредельными соединениями:
формуле С6Н6 соответствует сразу
несколько соединений:
22
27.07.2017
23. Пространственная изомерия аренов
Пространственная изомерияотносительно бензольного
кольца в алкилбензолах
отсутствует
23
27.07.2017
24. Физические свойства аренов
Бензол и его ближайшие гомологи –бесцветные жидкие вещества,
нерастворимые в воде, но хорошо
растворяющиеся во многих органических
жидкостях.
Легче воды.
Огнеопасны.
Бензол токсичен (вызывает заболевание
крови24 – лейкемию).
27.07.2017
25. Физические свойства аренов
Температуры кипения и плавления :25
27.07.2017
26. Химические свойства аренов
Отличаются от предельных инепредельных углеводородов. Это
объясняется особенностями строения
бензольного кольца.
Делокализация шести p-электронов в
циклической системе понижает энергию
молекулы, что обусловливает
повышенную устойчивость
(ароматичность) бензола и его
26
гомологов.
27.07.2017
27. Химические свойства аренов
арены не склонны вступать в реакцииприсоединения или окисления, которые
ведут к нарушению ароматичности.
наиболее характерны реакции, идущие с
сохранением ароматической системы, а
именно, реакции замещения атомов
водорода, связанных с циклом.
27
27.07.2017
28. Химические свойства аренов
Наличие областей повышенной pэлектронной плотности с двух сторонплоского ароматического цикла ведет к
тому, что бензольное кольцо является
нуклеофилом и в связи с этим склонно
подвергаться атаке электрофильным
реагентом.
28
27.07.2017
29. Химические свойства аренов
для ароматических соединенийнаиболее типичны реакции
электрофильного замещения:
Другие реакции (присоединение,
окисление) идут с трудом.
29
27.07.2017
30. Химические свойства аренов
Механизм электрофильного замещенияобозначается символом SЕ
(по первым буквам английских
терминов:
S – substitution [замещение],
E – electrophil [электрофил]).
30
27.07.2017
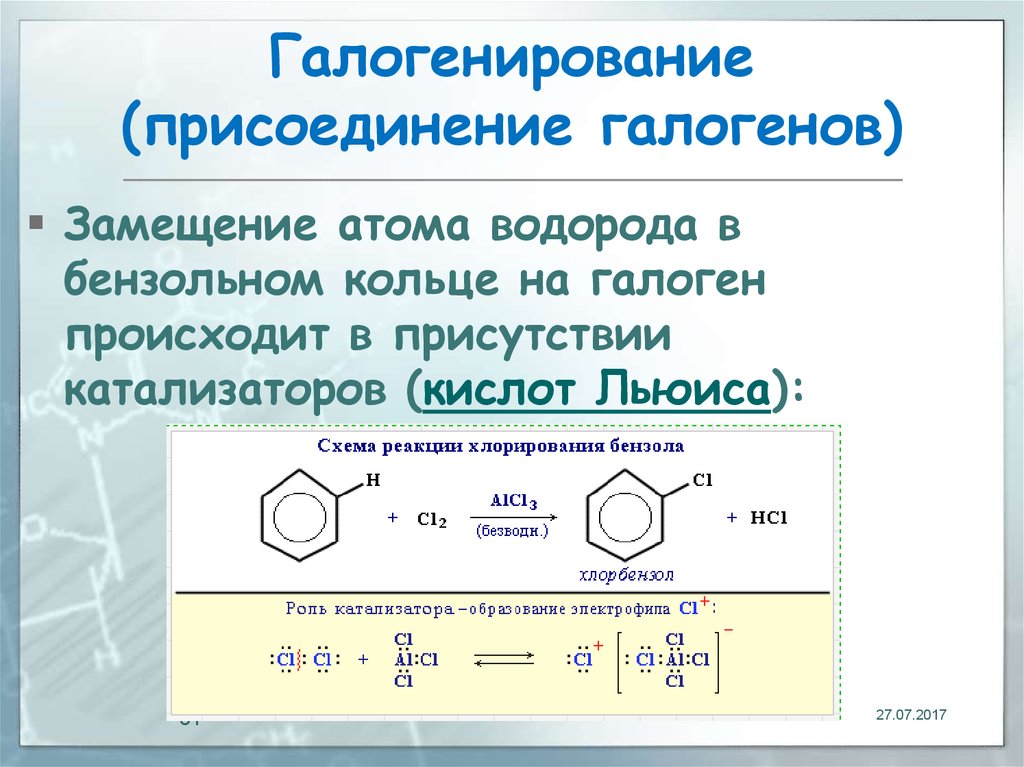
31. Галогенирование (присоединение галогенов)
Замещение атома водорода вбензольном кольце на галоген
происходит в присутствии
катализаторов (кислот Льюиса):
31
27.07.2017
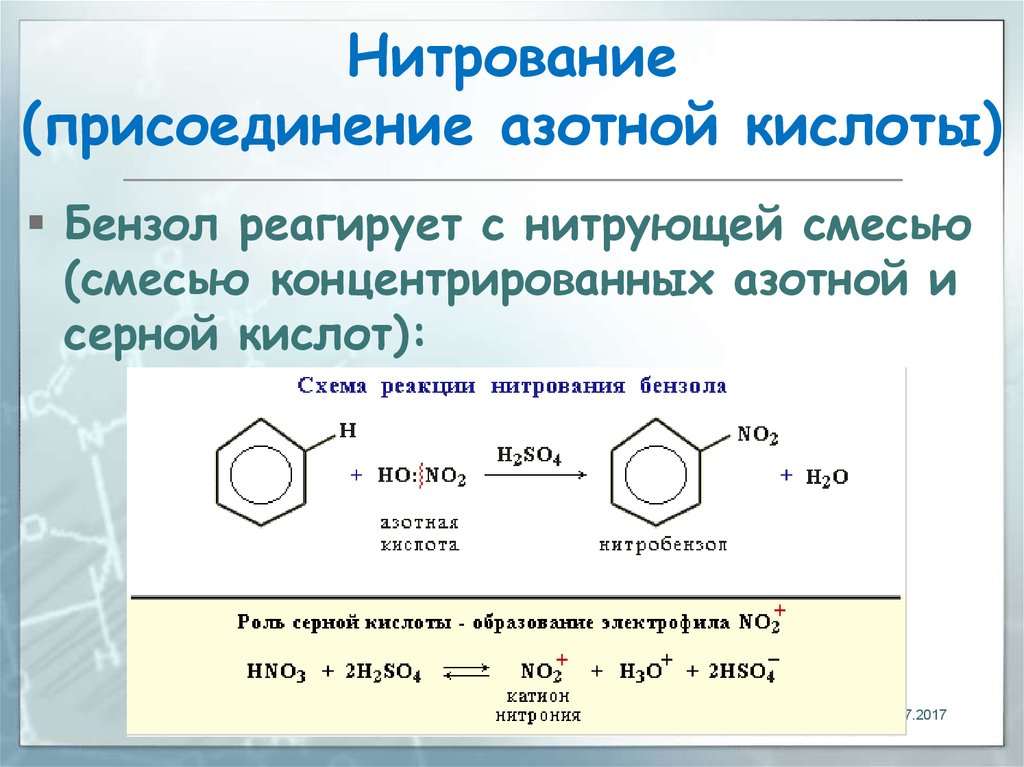
32. Нитрование (присоединение азотной кислоты)
Бензол реагирует с нитрующей смесью(смесью концентрированных азотной и
серной кислот):
32
27.07.2017
33. Алкилирование
Замещение атома водорода вбензольном кольце на алкильную
группу (алкилирование) происходит
под действием алкилгалогенидов или
алкенов в присутствии катализаторов
(кислот Льюиса) или алкенов тремя
путями.
33
27.07.2017
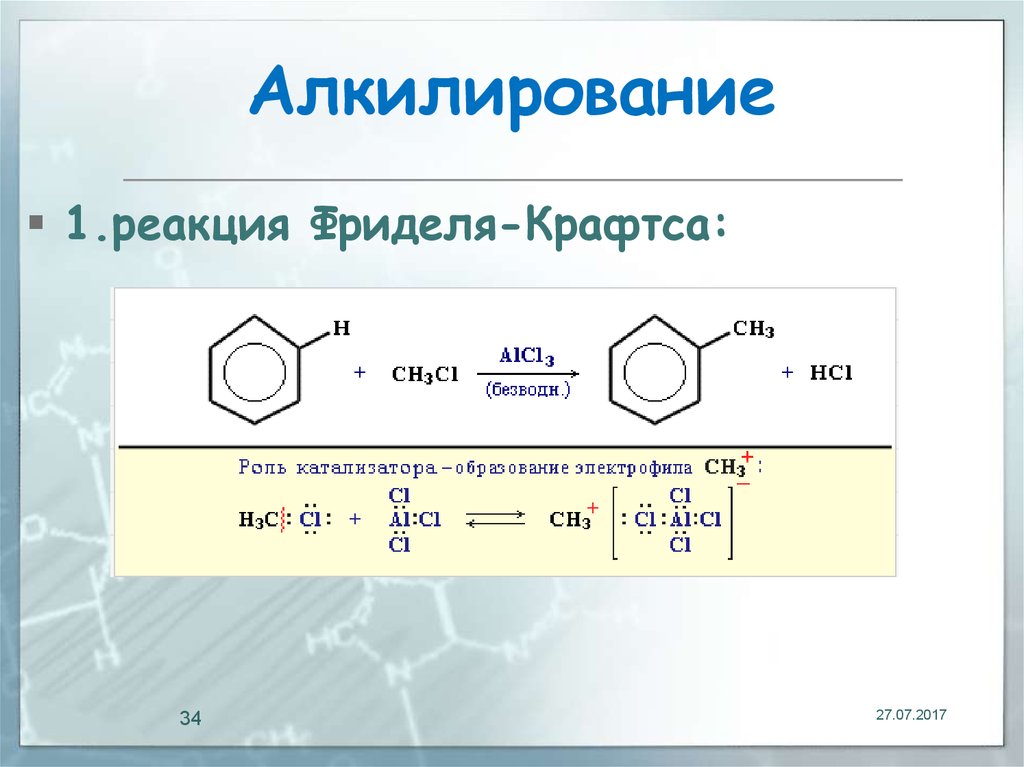
34. Алкилирование
1.реакция Фриделя-Крафтса:34
27.07.2017
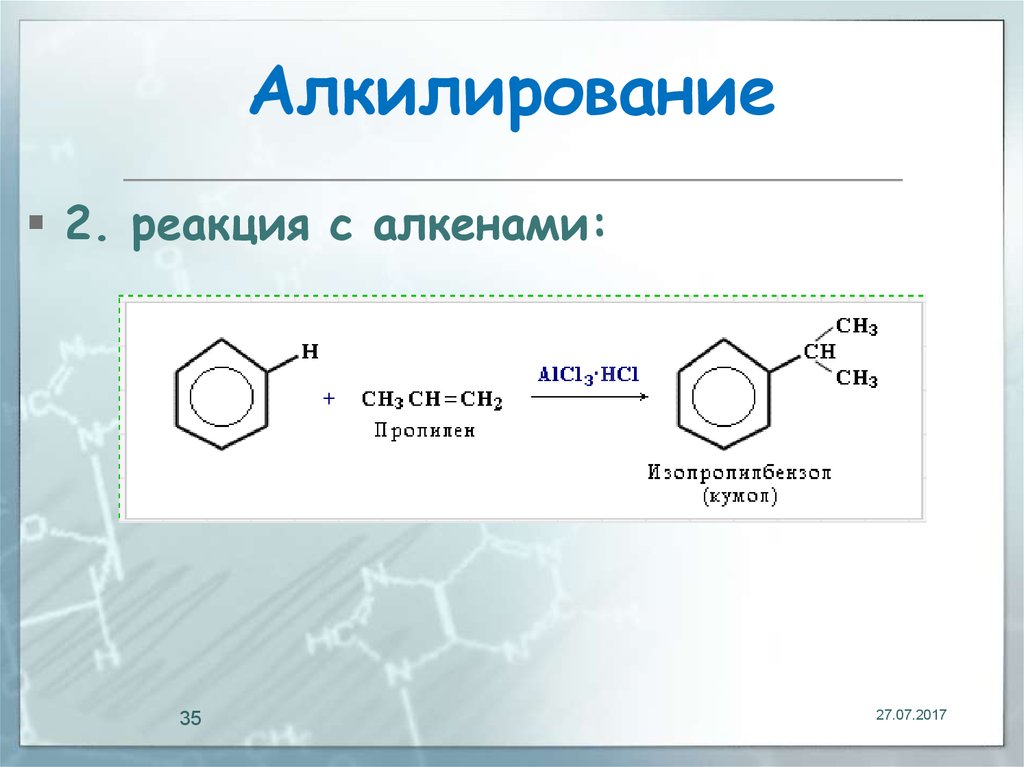
35. Алкилирование
2. реакция с алкенами:35
27.07.2017
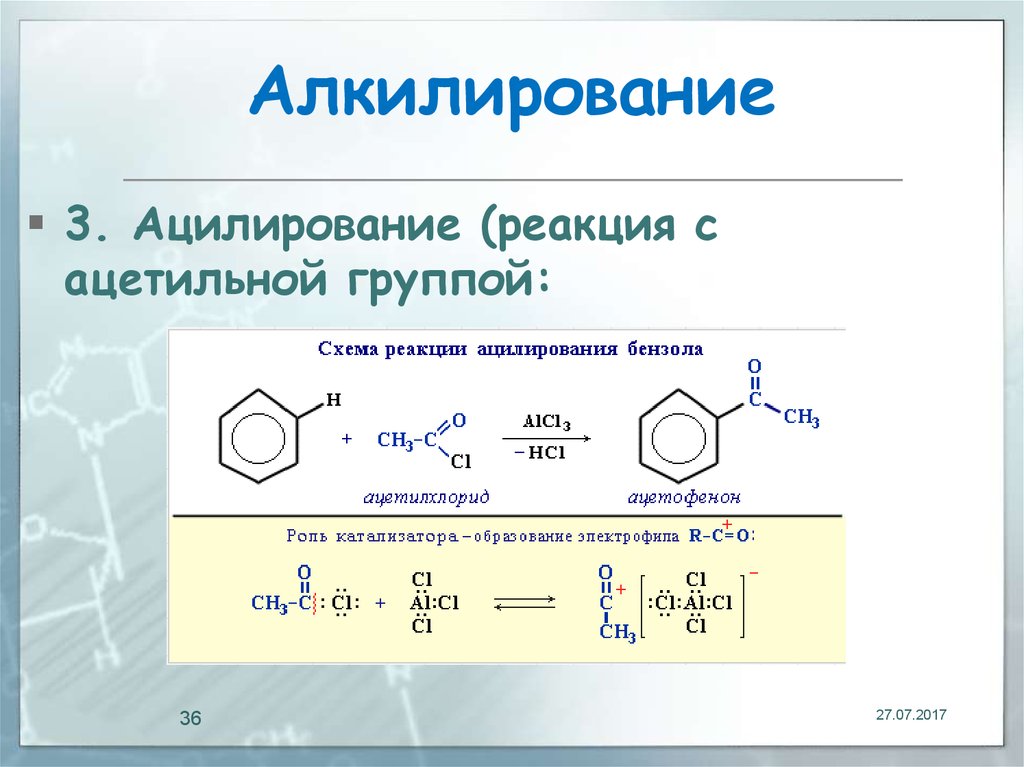
36. Алкилирование
3. Ацилирование (реакция сацетильной группой:
36
27.07.2017
37. Замещение в алкилбензолах
Получение тринитротолуола (принитровании толуола С6Н5CH3 (70°С)
происходит замещение не одного, а
трех атомов водорода с образованием
2,4,6-тринитротолуола):
37
27.07.2017
38. Реакции присоединения
В реакции присоединения, приводящиек разрушению ароматической структуры
бензольного кольца, арены могут
вступать с большим трудом:
реакции гидрирования
реакции хлорирования
38
27.07.2017
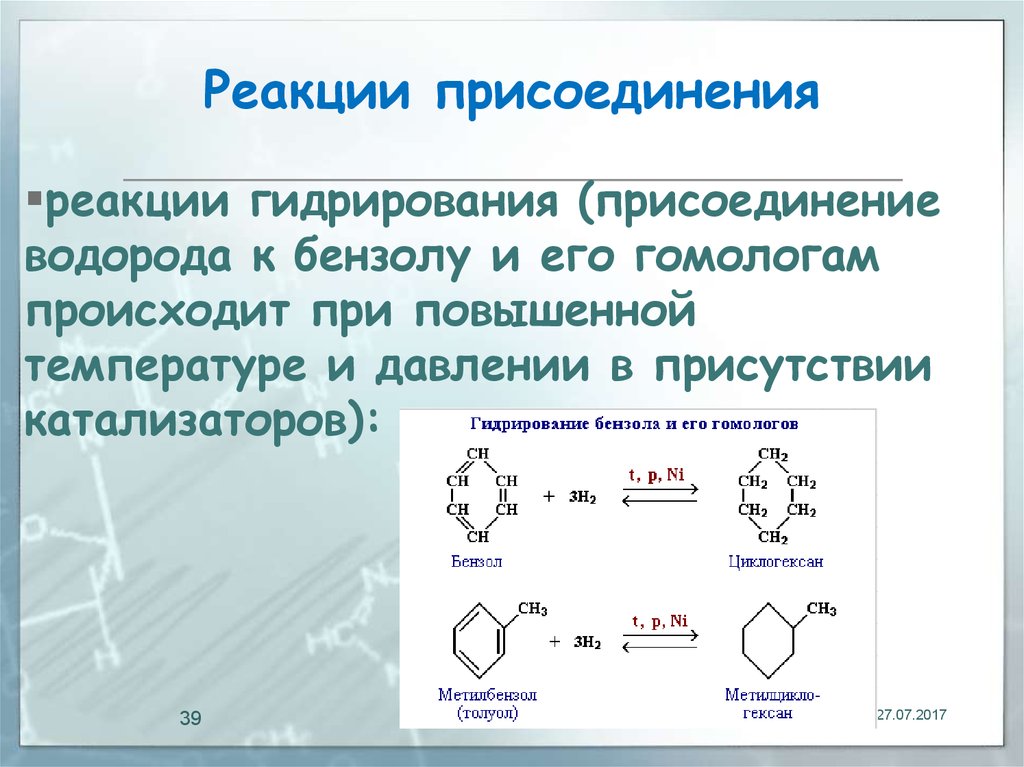
39. Реакции присоединения
реакции гидрирования (присоединениеводорода к бензолу и его гомологам
происходит при повышенной
температуре и давлении в присутствии
катализаторов):
39
27.07.2017
40. Реакции присоединения
реакции хлорирования:Практическое значение имеет
радикальное хлорирование бензола для
получения "гексахлорана" (средство
борьбы с вредными насекомыми)
40
27.07.2017
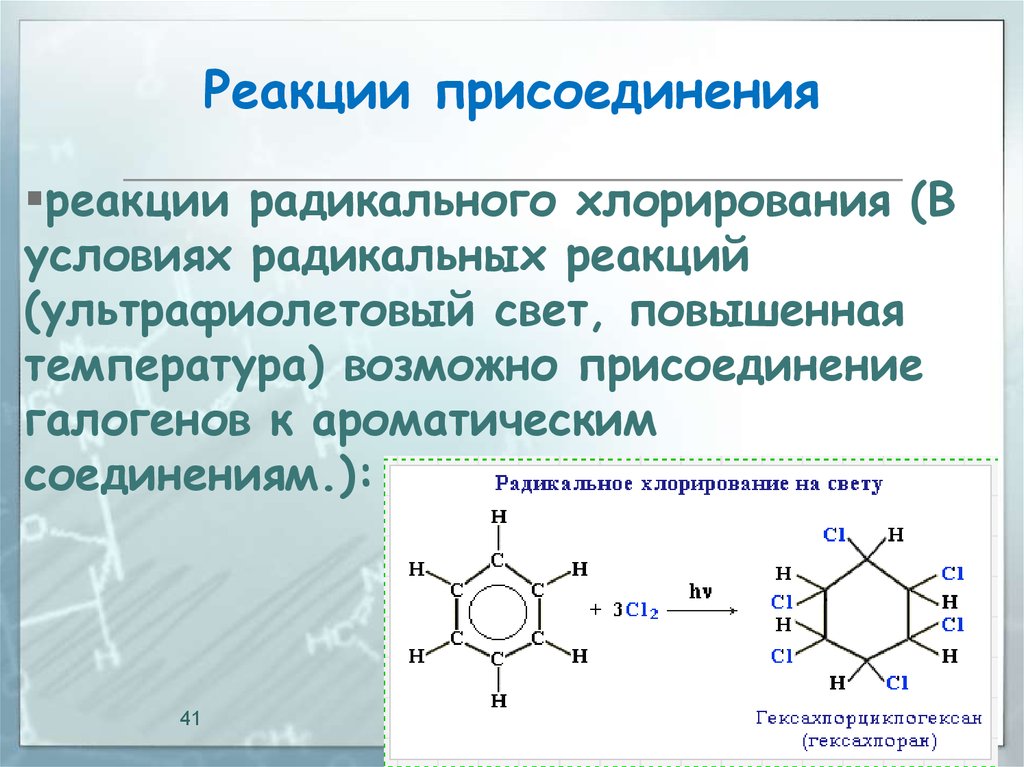
41. Реакции присоединения
реакции радикального хлорирования (Вусловиях радикальных реакций
(ультрафиолетовый свет, повышенная
температура) возможно присоединение
галогенов к ароматическим
соединениям.):
41
27.07.2017
42. Окисление аренов
Бензол не окисляется даже поддействием сильных окислителей
(KMnO4, K2Cr2O7 и т.п.).
Поэтому он часто используется как
инертный растворитель при проведении
реакций окисления других
органических соединений.
В отличие от бензола его гомологи
окисляются довольно легко.
42
27.07.2017
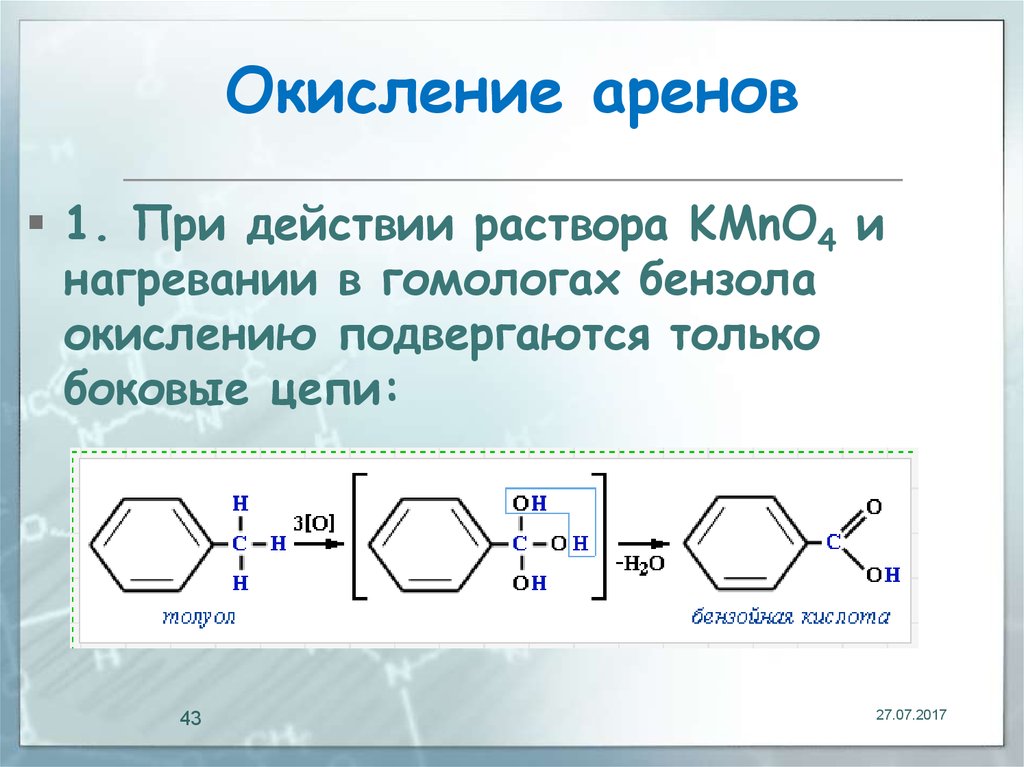
43. Окисление аренов
1. При действии раствора KMnO4 инагревании в гомологах бензола
окислению подвергаются только
боковые цепи:
43
27.07.2017
44. Окисление аренов
Окисление других гомологов(этилбензол, пропилбензол и т.д.)
также приводит к образованию
бензойной кислоты.
Разрыв связи при этом происходит
между двумя ближайшими к кольцу
атомами углерода в боковой цепи:
44
27.07.2017
45. Окисление аренов
2. Бензол и его гомологи на воздухегорят коптящим пламенем, что
обусловлено высоким содержанием
углерода в их молекулах:
Бензол и его летучие гомологи
образуют с воздухом и кислородом
взрывоопасные
смеси
45
27.07.2017
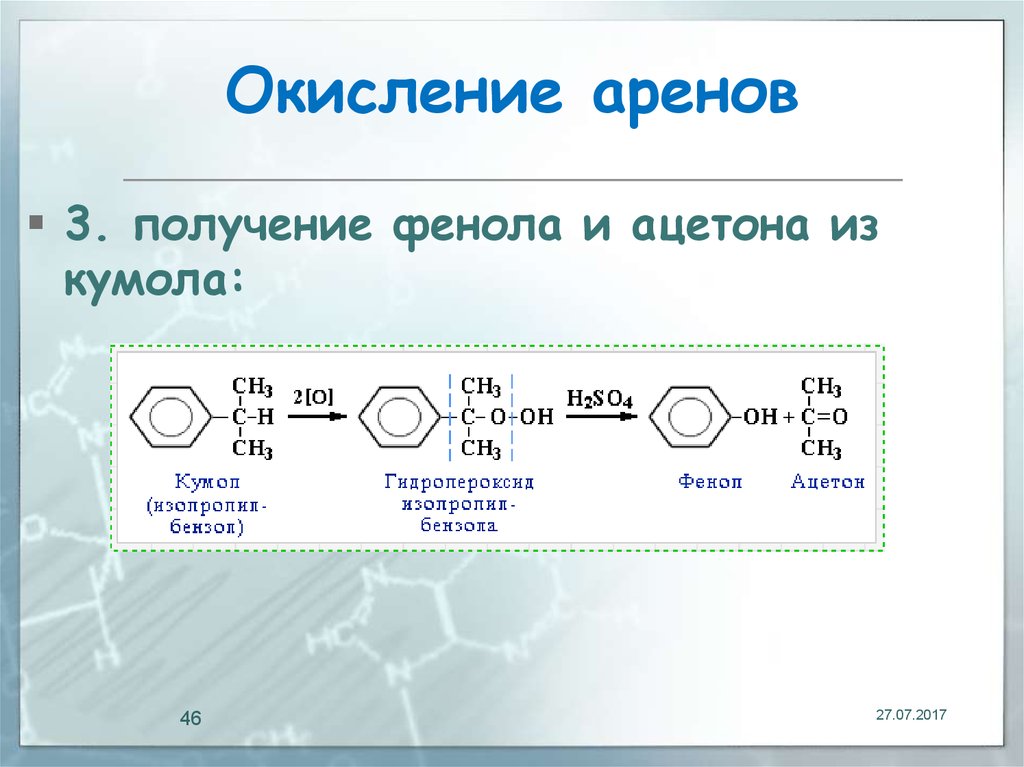
46. Окисление аренов
3. получение фенола и ацетона изкумола:
46
27.07.2017
47. Получение ароматических углеводородов
I. При коксовании каменного угляобразуется каменноугольная смола, из
которой выделяют бензол, толуол,
ксилолы, нафталин и многие другие
органические соединения.
47
27.07.2017
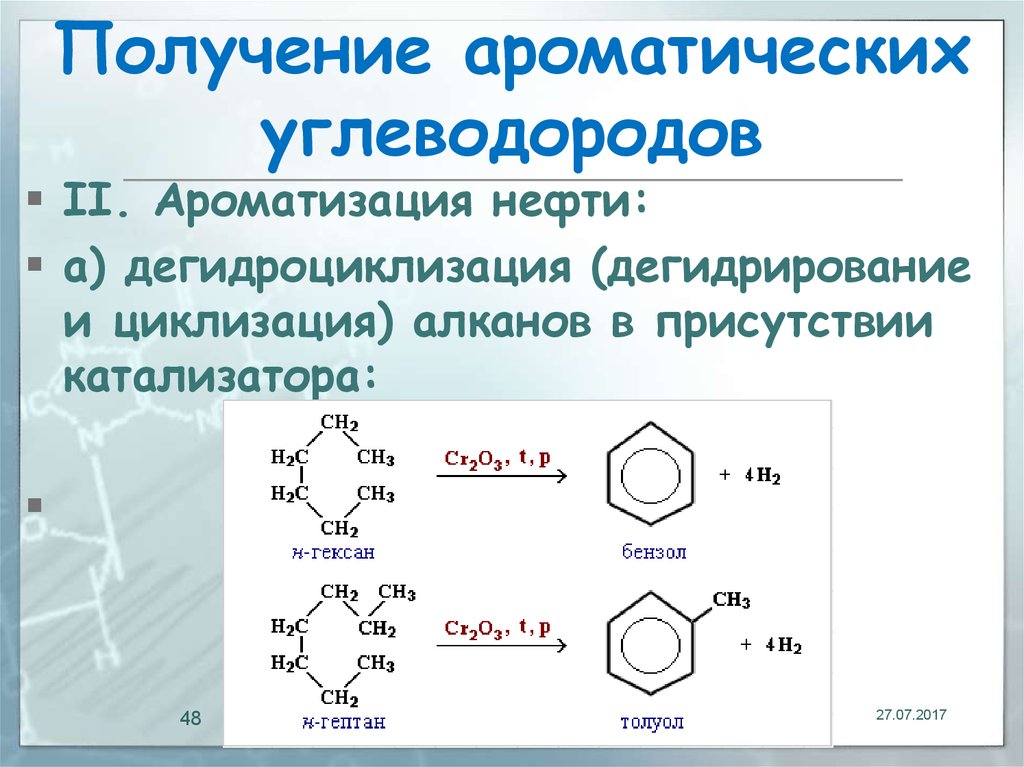
48. Получение ароматических углеводородов
II. Ароматизация нефти:а) дегидроциклизация (дегидрирование
и циклизация) алканов в присутствии
катализатора:
48
27.07.2017
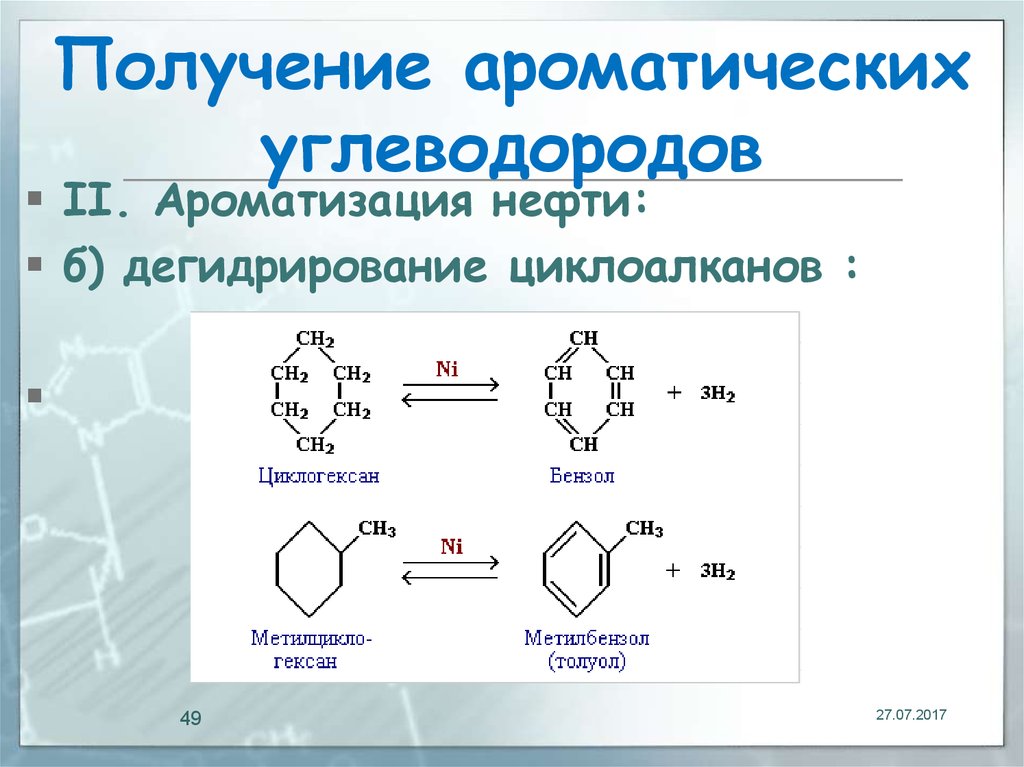
49. Получение ароматических углеводородов
II. Ароматизация нефти:б) дегидрирование циклоалканов :
49
27.07.2017
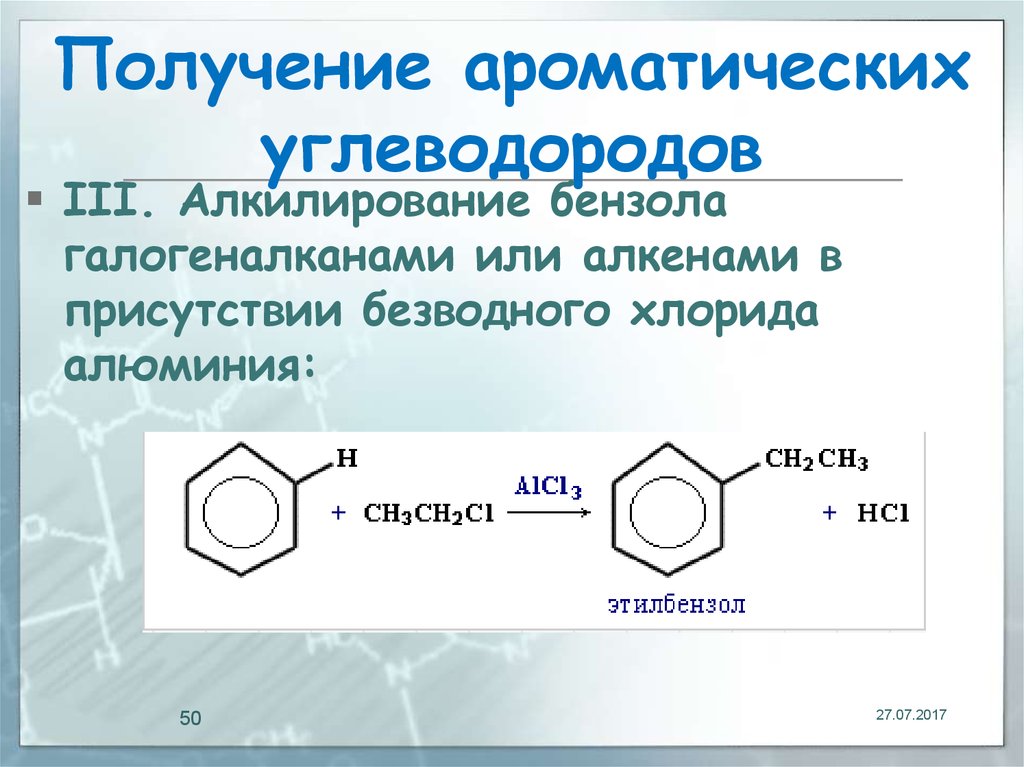
50. Получение ароматических углеводородов
III. Алкилирование бензолагалогеналканами или алкенами в
присутствии безводного хлорида
алюминия:
50
27.07.2017
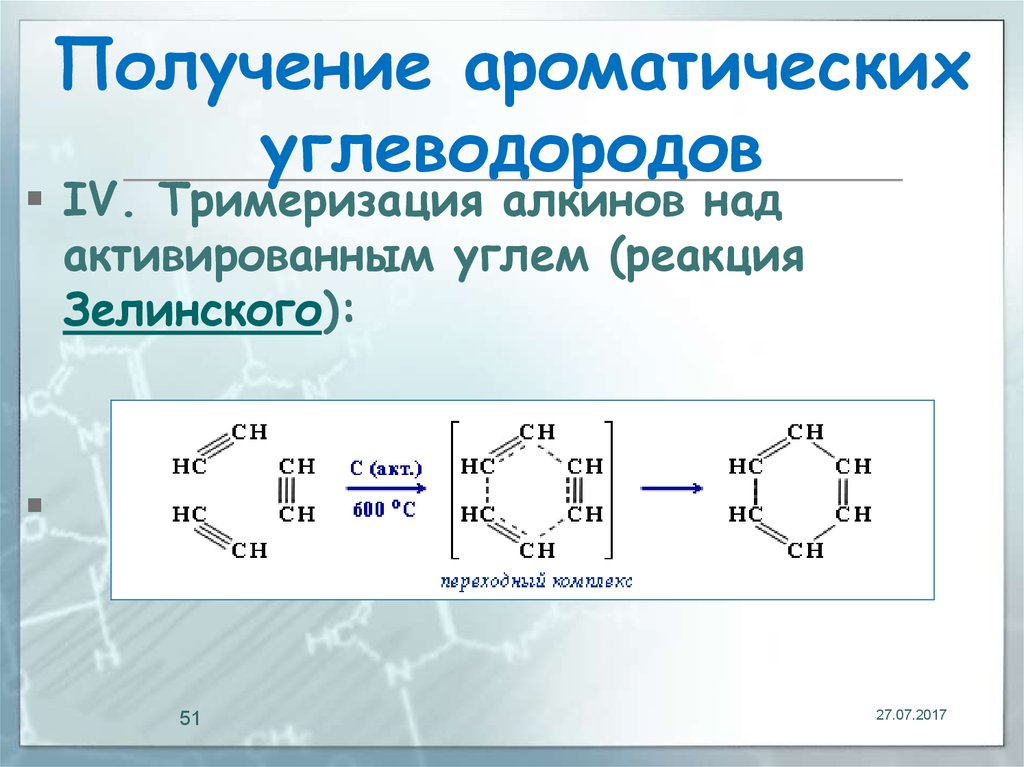
51. Получение ароматических углеводородов
IV. Тримеризация алкинов надактивированным углем (реакция
Зелинского):
51
27.07.2017
52. Получение ароматических углеводородов
V. Сплавление солей ароматическихкарбоновых кислот со щёлочью
(лабораторный метод):
52
27.07.2017
53. Применение аренов
Бензол С6Н6 используется как исходныйпродукт для получения различных
ароматических соединений –
нитробензола, хлорбензола, анилина,
фенола, стирола и т.д., применяемых
в производстве лекарств, пластмасс,
красителей, ядохимикатов и многих
других органических веществ.
53
27.07.2017
54. Применение аренов
Наибольшее практическое значениеимеет бензол:
54
27.07.2017
55. Применение аренов
Толуол С6Н5-СН3 применяется впроизводстве красителей,
лекарственных и взрывчатых веществ
(тротил, тол).
Ксилолы С6Н4(СН3)2 в виде смеси трех
изомеров – технический ксилол –
применяется как растворитель и
исходный продукт для синтеза многих
органических соединений.
55
27.07.2017
56. Применение аренов
Изопропилбензол (кумол) С6Н4СН(СН3)2 – исходное вещество дляполучения фенола и ацетона.
Винилбензол (стирол) C6H5-CН=СН2
используется для получения ценного
полимерного материала полистирола
56
27.07.2017
57. 1.Контрольная работа
1. Какие из приведенных на рисункеструктур соответствуют бензолу?
57
27.07.2017
58. 2. Контрольная работа
Дайте названия следующихароматических углеводородов:
58
27.07.2017
59. 3.Контрольная работа
Какой тип гибридизации характерендля атомов углерода в молекуле
бензола?
Ответ
Ответ
Ответ
Ответ
1:
2:
3:
4:
59
sp3
sp
sp3d
sp2
27.07.2017
60. 4. Контрольная работа
Какие арены изомерны друг другу:а) орт о-ксилол;
б) этилбензол;
в) метилбензол;
г) 1-метил-3-этилбензол;
д) мет а-ксилол;
е) изопропилбензол ?
Ответ 1:
Ответ 2:
Ответ 3:
Ответ 604:
а,
а,
б,
а,
б,
г,
в,
в,
д
е
г
е
27.07.2017
61. 5. Контрольная работа
Нарисуйте структурную формулубензола и:
61
27.07.2017
62. 6. Контрольная работа
Нарисуйте следующие соединения:62
27.07.2017
63. 7. Контрольная работа
Массовая доля выхода бензола притримеризации ацетилена составляет 42%.
Чему равна масса ацетилена, необходимого
для получения бензола количеством вещества
1 моль? Напишите уравнение реакции.
Ответ
Ответ
Ответ
Ответ
1:
2:
3:
4:
63
120,3
202,4
185,7
360,5
г
г
г
г
27.07.2017
64. 8. Контрольная работа
Какое вещество из образующихся вприведенной схеме превращений (X, Y или Z)
используется как средство борьбы с вредными
насекомыми?
Назовите это соединение.
Ответ
Ответ
Ответ
Ответ
1:
2:
3:
4:
64
X
Y
Z
Z
–
–
–
–
уксусная кислота
бензол
гексахлорциклогексан
гексахлорбензол
27.07.2017
65.
Напишите уравнения реакций,проанализировав видеоролики из папки
«Лабораторные опыты».
65
27.07.2017
66. Получение аренов
Получение и свойства бензола.Напишите уравнение реакции:
(видеоролик exp6.exe в папке лабораторные
опыты)
66
27.07.2017
67. Свойства аренов
Напишите уравнение реакции:(видеоролик exp7.exe в папке лабораторные
опыты)
67
27.07.2017
68. Свойства аренов
Напишите уравнение реакции:(видеоролик exp8.exe в папке лабораторные
опыты)
68
27.07.2017
69. Горение аренов
Напишите уравнение реакции:С6Н6 +О2 →
С6Н5-СН3 +О2 →
69
27.07.2017





















































 Химия
Химия








