Похожие презентации:
Инертные газы
1.
LOGOwww.themegallery.com
2.
Инертныегазы
3.
Название«Инертные газы»
отражает
химическую
инертность
элементов
этой подгруппы
Внешняя
электронная
оболочка устойчива:
у Не находится 2
внешних электрона,
а у остальных - по 8
внешних
электронов.
4.
Благородные газы бесцветны иодноатомны
Инертные
газы
Не имеют цвета и запаха
При прохождении через них
тока ярко светятся: гелий ярко-жёлтым светом, неон огненно красным светом,
аргон - сине-голубое свечение
5.
Гелийвыделяют
из
природных
гелионосных
газов
Гелий
содержится
в минералах:
монацит,
торианит
Химических соединений гелий не образует
6.
Единственное вещество – жидкостьвплоть до 0 К
Самая низкая из всех веществ
температура кипения
Самая интересное свойство сверхтекучесть
7.
Сварка, резка и плавкаметаллов
Составная
часть
искусственного
воздуха
Уникальный
хладагент в
экспериментальной
физике
Компонент
среды
гелиевых
лазеров
8.
Нахождение в природе:в атмосфере, земной
коре, в морской воде
Получение в
промышленности:
разделением жидкого
воздуха
9.
Наполнениегазоразрядных
трубок
В технике при
низких
температурах
Неоновые трубки
В газовых
лазерах
10.
В морской воде(больше всех
инертных газов)
В атмосферном
воздухе
(больше всех
инертных газов)
В земной коре
(больше всех
инертных газов)
11.
Создание инертнойи защитной атмосферы
Светящаяся
реклама
Заполнение
электрических
лампочек
Получение
сверхчистых
материалов
12.
Нахождение в природе:в атмосферном воздухе
Получение: побочный
продукт разделения
воздуха
13.
Газоразрядныеи рентгеновские
трубки
Для контроля
износа деталей
Изотопный
индикатор при
исследованиях
коррозии
Источник
излучения в
медицине
14.
1962 год Нил Бартлетт (Канада) –первое химическое
соединение ксенона
15.
+2+6
+8
Xe + F2
свет
2XeF2 + 4KOH
XeF2
2Xe + 4KF + O2 + 2H2O
Xe + 2F2
400С0
XeF4 + 2H2O
Xe + 3F2
XeF6 + 6KI
XeF4
4HF + Xe + O2
60 атм
XeF6
3I2 + Xe + 6KF
16.
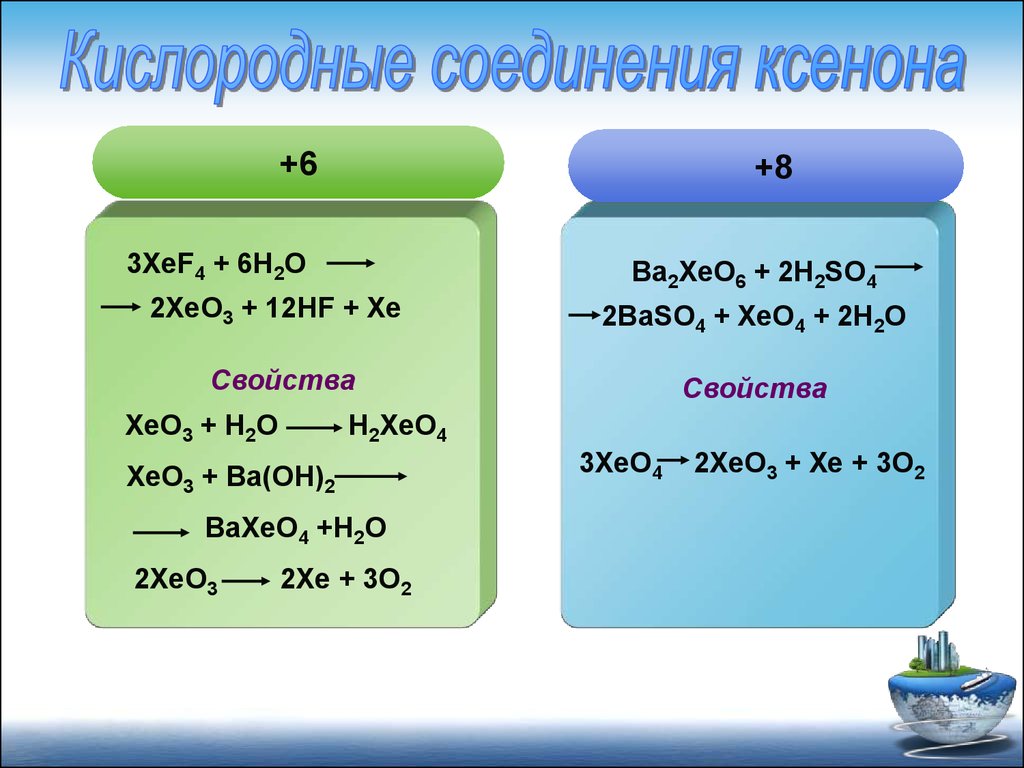
+6+8
3XeF4 + 6H2O
Ba2XeO6 + 2H2SO4
2XeO3 + 12HF + Xe
2BaSO4 + XeO4 + 2H2O
Свойства
Свойства
XeO3 + H2O
H2XeO4
XeO3 + Ba(OH)2
BaXeO4 +H2O
2XeO3
2Xe + 3O2
3XeO4
2XeO3 + Xe + 3O2
17.
Наполнениеламп накаливания
Фториды
ксенона
используют
для пассивации
металлов
Для диагностики
в медицине
В
радиографии
18.
Нахождение в природе:Содержание в земной
коре 7·10-16 % по массе.
Получение: водный
раствор любой соли
радона
19.
В медицине дляприготовления
«радоновых ванн»
Поиск
радиоактивных
элементов в
природе
Индикатор газовых
потоков в доменных
печах
Для
активации
кормов
домашних
животных
20.
LOGOwww.themegallery.com











 Химия
Химия








