Похожие презентации:
Хлорофиллы. Общие принципы организации молекулы. Основные этапы биосинтеза
1.
1.Хлорофиллы. Общие принципы организации молекулы. Основные этапы биосинтеза. Спектр
поглощения хлорофиллов. Понятие о нативных формах. Энергетические переходы в молекуле хлорофилла.
Белковые комплексы, содержащий хлорофилл. Миграция энергии. Окислительно-восстановительные реакции
с участием хлорофилла. Продукция активных форм кислорода.
2.
Каротиноиды. Общее представление о биосинтезе. Протекторная роль каротиноидов в
фотосистемах. Виолаксантиновый цикл и его роль в регуляции распределения энергии. Защитная функция
каротиноидов. Каротиноиды как предшественники АБК. Экологическая роль каротиноидов.
3.
Продукция активных форм кислорода с участием возбужденного хлорофилла. Экологические
факторы, способствующие образованию синглетного кислорода. Защитные механизмы. Роль
виолаксантинового (ксантофиллового) цикла в регуляции распределения энергии квантов света.
4.
Антенные комплексы. Подвижные и неподвижные комплексы. Фикобилисомы. Фикобилины как
дополнительные ферменты фотосинтеза у водорослей и цианобактерий. Нативные формы хлорофиллов в
антенных комплексах. Понятие о фотосинтической единице. Факторы, влияющие на ассоциацию
светособирающего комплекса с ФС II и ФС I.
5.
Строение и функционирование ФС I. Ассоциация и диссоциация с подвижным светособирающим
комплексом. Кооперация работы ФС I и ФС II. Локализация ФС I в мембране тилакоидов.
6.
Строение и функционирование фотосистемы II. Водоокисляющий комплекс и реакции образования
кислорода. Работа реакционного центра. Участие ФС II в нециклическом потоке ē. Работа ФС II в циклическом
режиме. Локализация ФС II и взаимодействие со светособирающим комплексом.
7.
Нециклический, циклический и псевдоциклический транспорт электрона. Последовательность
переносчиков. Цикл вокруг фотосистемы II. Реакция хлородыхания как регуляция редокс-статуса пула
пластохинонов. Подвижные переносчики в составе комплексов. Одно- и двухэлектронные переносчики.
8.
Взаимосвязь между фотосинтетической функцией и ультраструктурой хлоропластов. Локализация
белковых комплексов на мембранах тилакоидов (ССК, ФСII, ФСI, цитохром-b/f-комплекс, АТФ-синтаза).
Переключение с нециклического на циклический поток электронов по ЭТЦ фотосинтеза и связанное с ним
изменение локализации комплексов.
2.
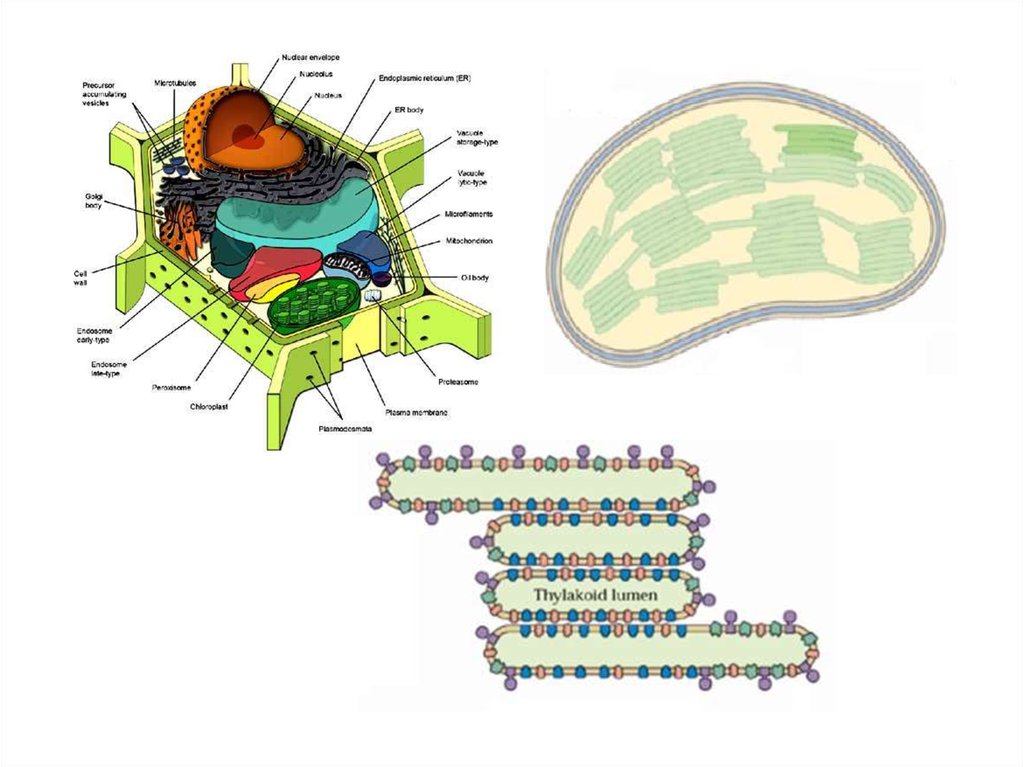
3. Функции пластид
• Фотосинтез – NB• Синтез: все жирные кислоты, многие аминокислоты, синтез
пуринов и пиримидинов, альтернативный путь синтеза
изопреноидов (в том числе в спецпластидах – лейкопластах),
шикиматный путь (параллельно цитозолю)
• Восстановление нитритов, сульфатов
• Запас (крахмал) – временный (хлоропласты), долгосрочный
(амилопласты)
• Экологические – окраска плодов, цветков (хромопласты –
каротиноиды).
Пластиды – «фабрика горячих и вредных производств»
растительной клетки
4. Взаимопревращения пластид контролируются ядерным геномом
5.
6.
ФС1ФС1
ФС1
ФС2
ССКI
ФС2
ССКII
ФС2
ФС1
ФС2
ФС1
ФС2
ССКII
ФС1
Р
ССКII
ССКII
ФС1
ФС1
ФС2
ФС1
ФС1
ФС1
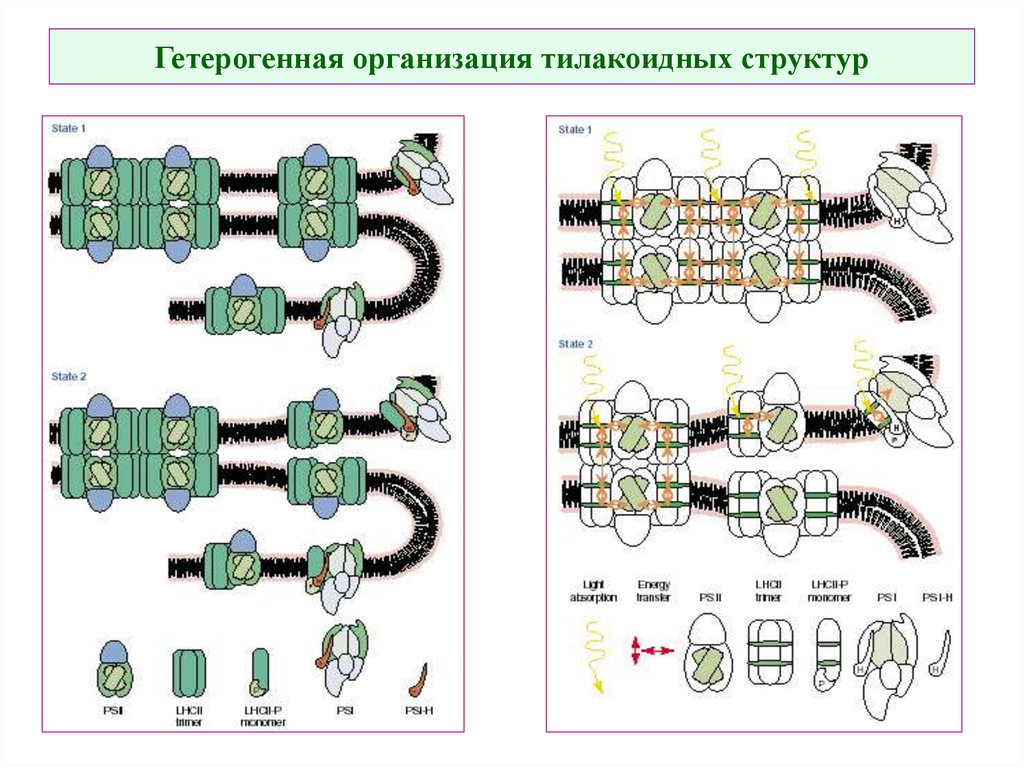
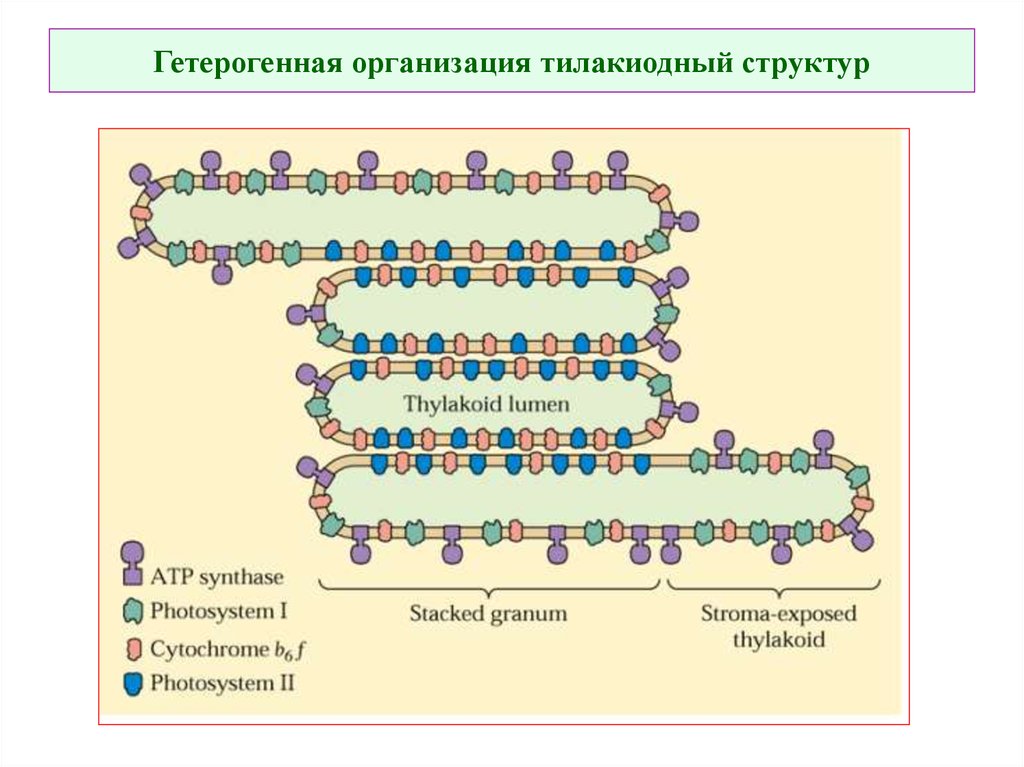
7. Гетерогенная организация тилакоидных структур
8. Гены хлоропластов
1. Транскрипция. 4 гена субъединиц пластидной РНК-полимеразы (rpo)2. Синтез белка. - 4 гена рРНК (оперон rrn)
- около 20 генов белков пластидных рибосом (rpl/rps)
- около 30 генов тРНК (trn)
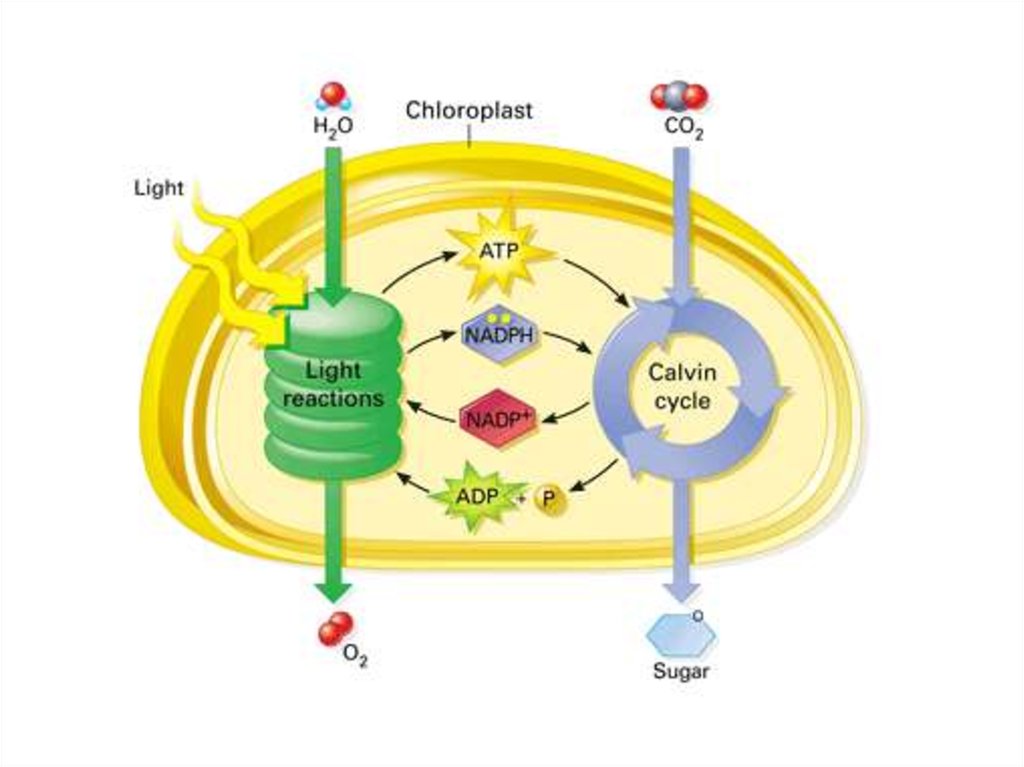
3. Фотосинтез.
- 6 генов белков фотосистемы I (psa)
- 14 генов белков фотосистемы II (psb)
- 6 генов ЭТЦ фотосинтеза (pet)
- 6 генов пластидной АТФ-зы (atp)
- ген большой субъединицы Рубиско (rbcL)
4. Около 20 генов с другими функциями
- гены пластидной НАД Н-дегидрогеназа,
- гены биосинтеза жирных кислот и др.
Всего: 110 - 120 генов, из них около 40 – «рабочих»
и около 60 – «домашнего хозяйства».
9.
Фоторецепторная система фотосинтеза строится на основедвух основных химических структур:
1.- тетрапирролы, образующие циклическую структуру
хлорофилла (магний-порфирины), а также открытую
тетрапиррольную структуру другой группы пигментов –
фикобилинов;
2. – полиизопреноиды, которые являются структурной
основой большого и разнообразного класса пигментов –
каротиноидов.
10.
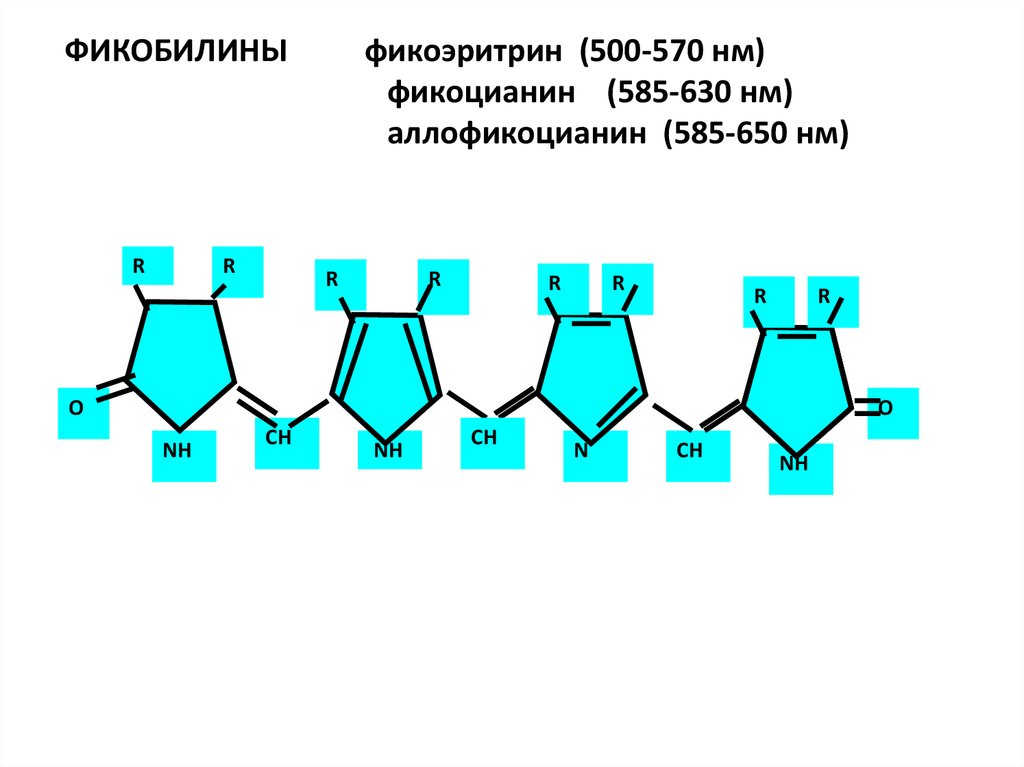
ФИКОБИЛИНЫR
R
фикоэритрин (500-570 нм)
фикоцианин (585-630 нм)
аллофикоцианин (585-650 нм)
R
R
R
R
R
R
O
O
NH
CH
NH
CH
N
CH
NH
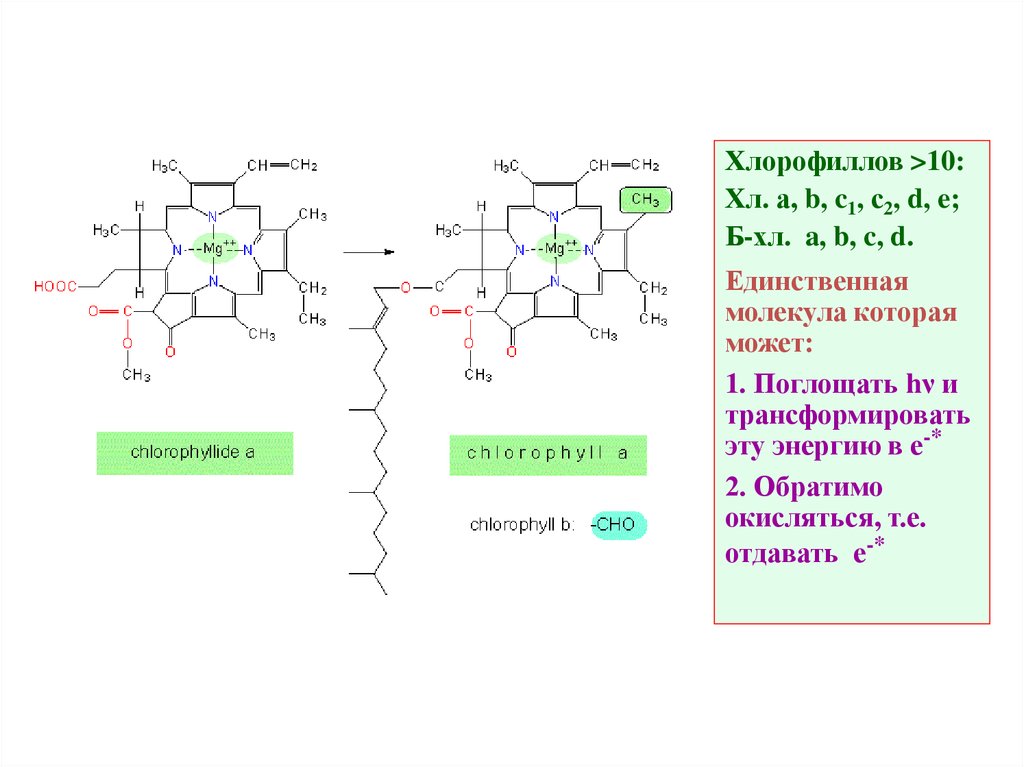
11. Основные структурные особенности молекулы хлорофилла
• Конъюгированная система двойных связей: основная 18-членнаяπ-система + дополнительные в I, II, V кольцах.
• Mg – минимум электроотрицательности; изменяет симметрию
молекулы хлорофилла; «активирует» электроны пиррольных
азотов
• V-кольцо – «форбиновая структура»: две важных группы:
карбонильная при С9 (участвует в n – π переходах) и кетоэфирная
при С10 – транс- (хл-л а) или цис- (хл-л а’).
• Гидрофобный «хвост» (обычно С20 – фитол). Структурная роль.
12.
Хлорофиллов >10:Хл. а, b, c1, с2, d, e;
Б-хл. a, b, c, d.
Единственная
молекула которая
может:
1. Поглощать hν и
трансформировать
эту энергию в е-*
2. Обратимо
окисляться, т.е.
отдавать е-*
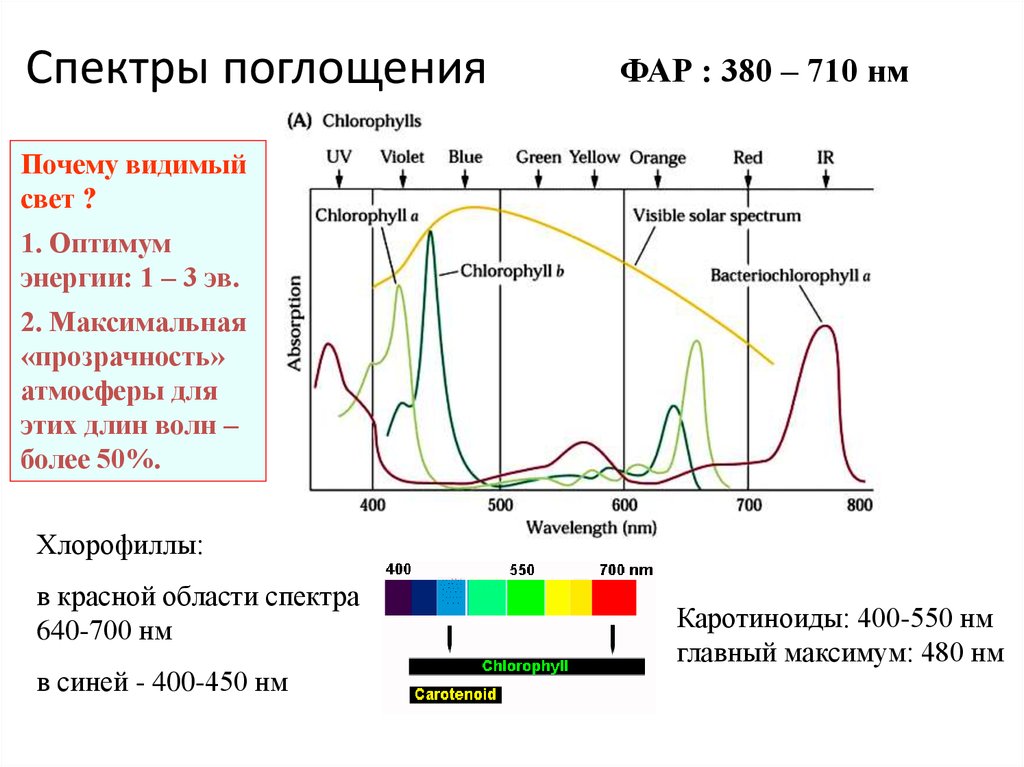
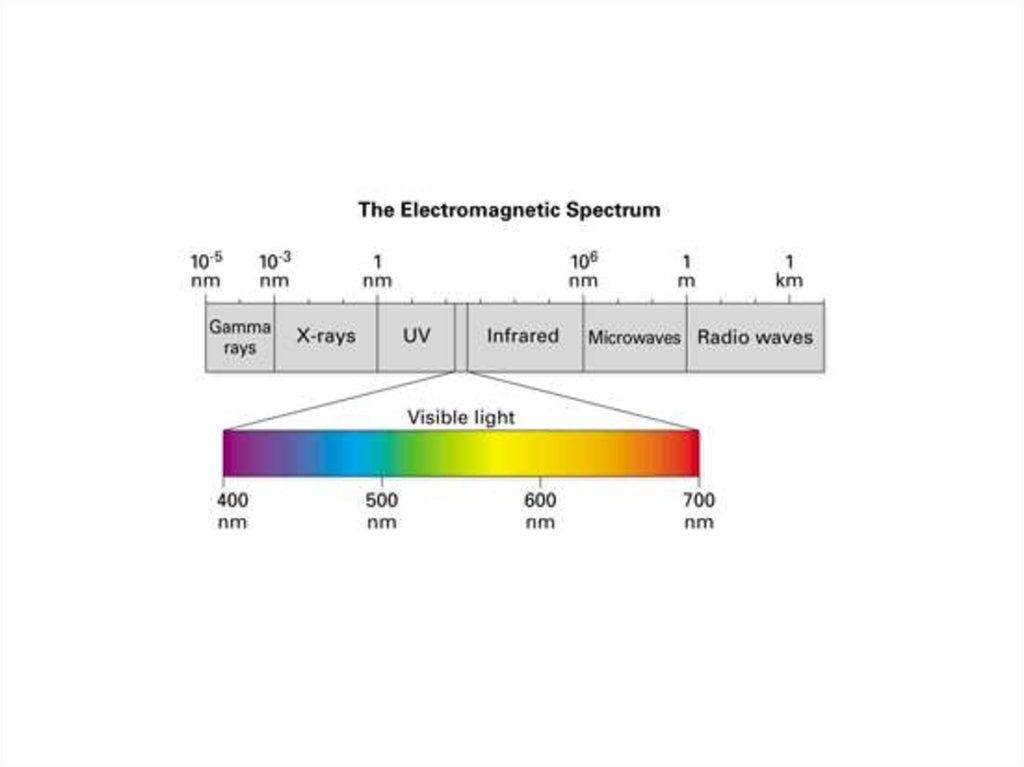
13. Спектры поглощения
ФАР : 380 – 710 нмПочему видимый
свет ?
1. Оптимум
энергии: 1 – 3 эв.
2. Максимальная
«прозрачность»
атмосферы для
этих длин волн –
более 50%.
Хлорофиллы:
в красной области спектра
640-700 нм
в синей - 400-450 нм
Каротиноиды: 400-550 нм
главный максимум: 480 нм
14.
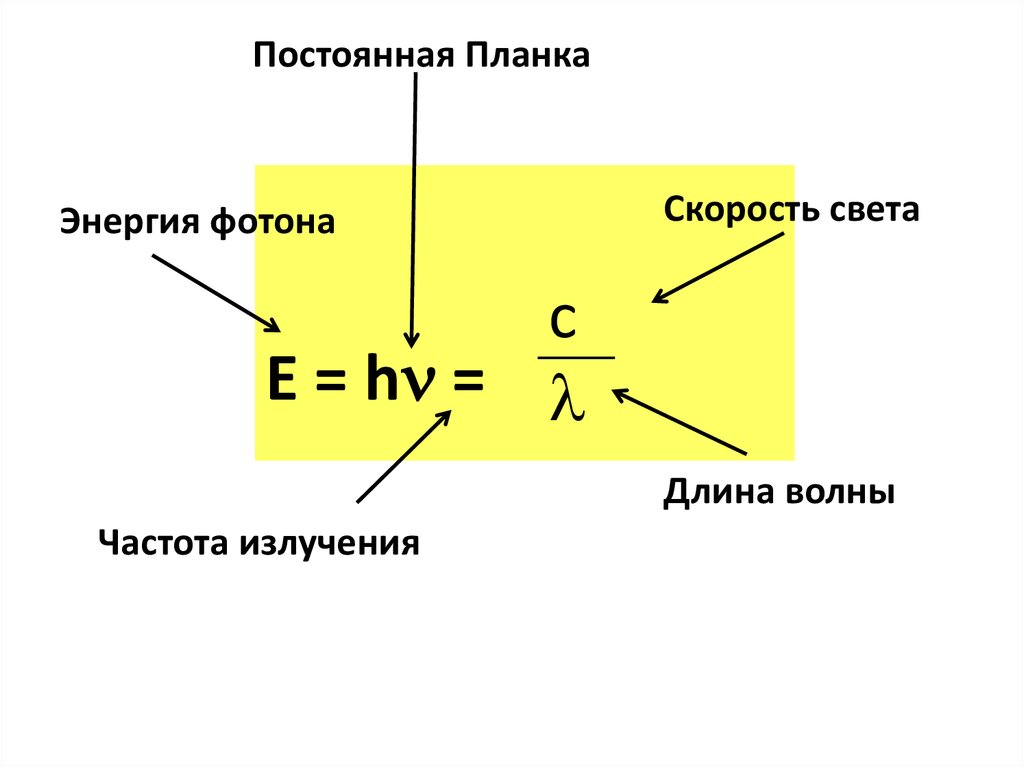
Постоянная ПланкаЭнергия фотона
Скорость света
c
E = h =
Длина волны
Частота излучения
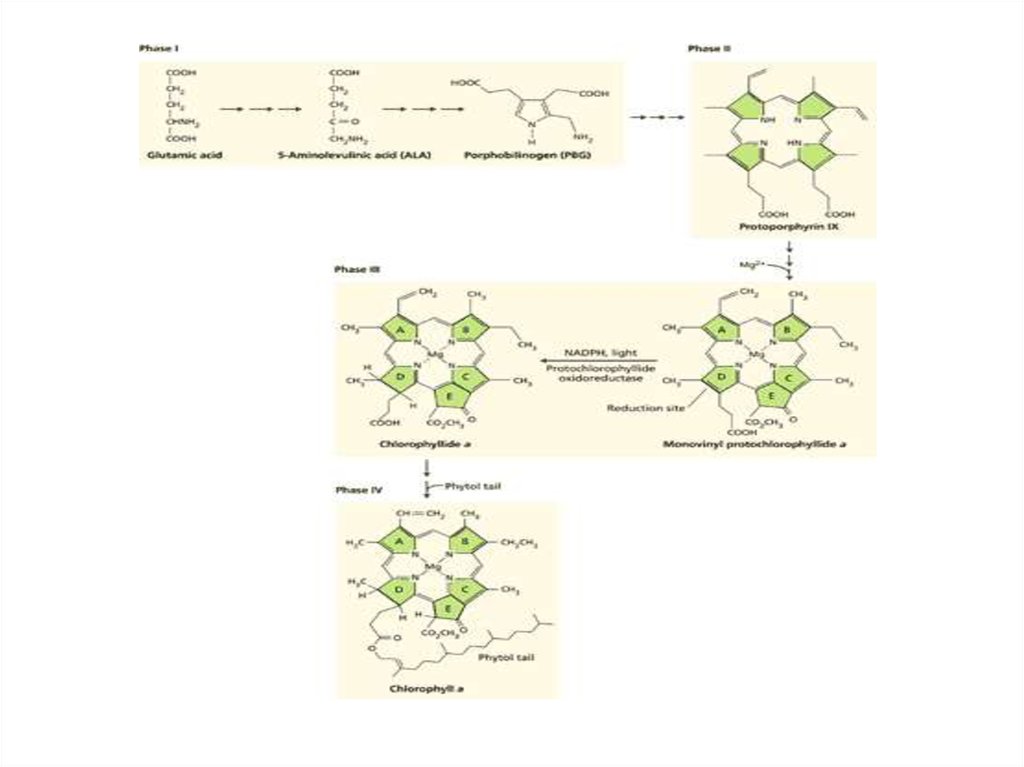
15. Биосинтез хлорофилла
• Глутамат → Глутамил-тРНК →Глутамат-1семиальдегид →δ-Аминолевулиновая кислота
• δ-Аминолевулиновая кислота →Порфобилиноген
→Гидроксиметилбилан →УропорфириногенIII
→КопропорфироногенIII →ПротопирфириногенIX
→Протопорфирин IX
• Mg-хелатаза
• Mg-протопорфирин → Mgпротопорфиринмонометиловый эфир
→Дивинилпротохлорофиллид а
→Моновинилпротохлорофиллид а
• Протохлорофиллид →СВЕТ! →Хлорофиллид а
→Хлорофилл а →Хлорофилл b
16.
17. Основные структурные особенности молекулы хлорофилла
• Конъюгированная система двойных связей: основная 18-членнаяπ-система + дополнительные в I, II, V кольцах.
• Mg – минимум электроотрицательности; изменяет симметрию
молекулы хлорофилла; «активирует» электроны пиррольных
азотов
• V-кольцо – «форбиновая структура»: две важных группы:
карбонильная при С9 (участвует в n – π переходах) и кетоэфирная
при С10 – транс- (хл-л а) или цис- (хл-л а’).
• Гидрофобный «хвост» (обычно С20 – фитол). Структурная роль.
18. Хлорофилл способен к окислительно-восстановительным превращениям. «Реакция Красновского»
Д - (Хл-Хл)680* - АД - (Хл-Хл) 680+ - АД+ - (Хл-Хл) 680 - А-
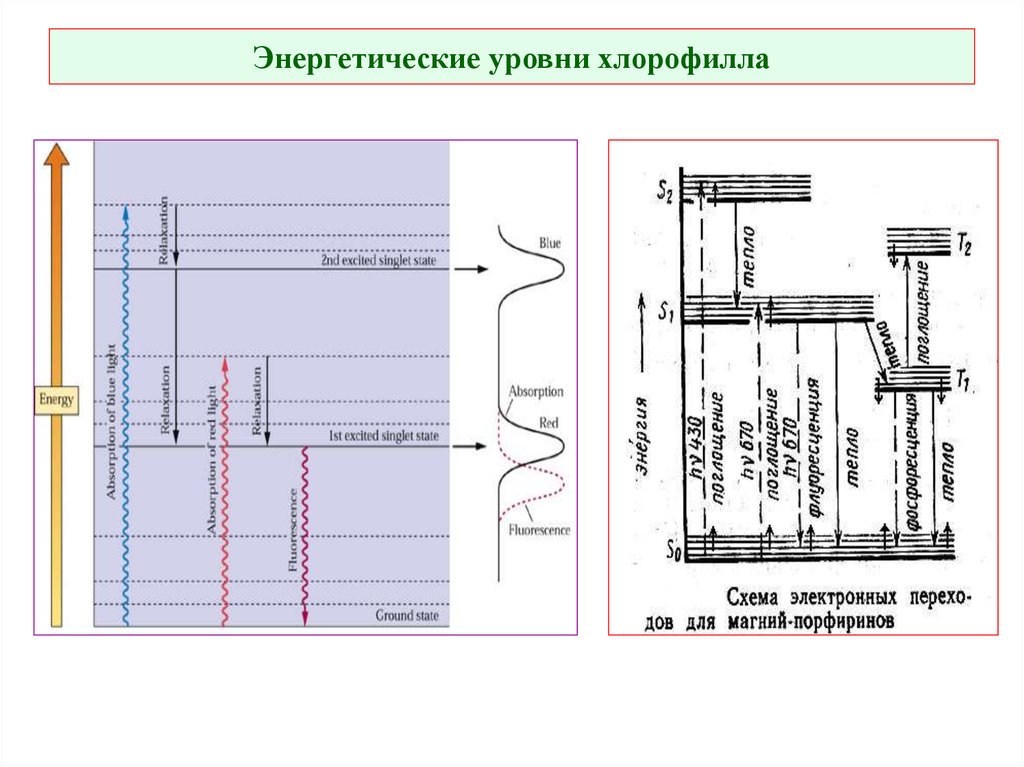
19. Энергетические состояния молекулы хлорофилла
S0 – основное синглетное состояниеS*2 , S*1 – синглетные возбужденные
состояния
Т* - триплетное возбужденное состояние
20. Энергетические уровни хлорофилла
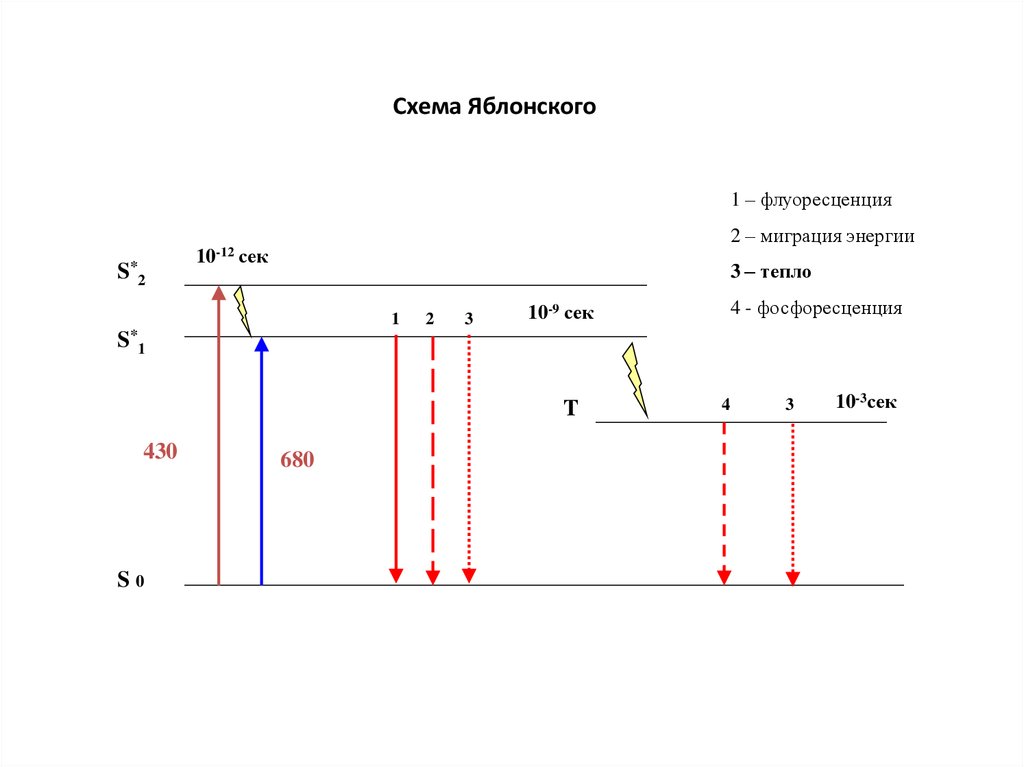
21. Схема Яблонского
1 – флуоресценцияS* 2
10-12
2 – миграция энергии
сек
3 – тепло
1
2
3
4 - фосфоресценция
10-9 сек
S* 1
T
430
S0
680
4
3
10-3сек
22.
СН3СН3
СН3
СН3
СН3
СН3
R
СН3
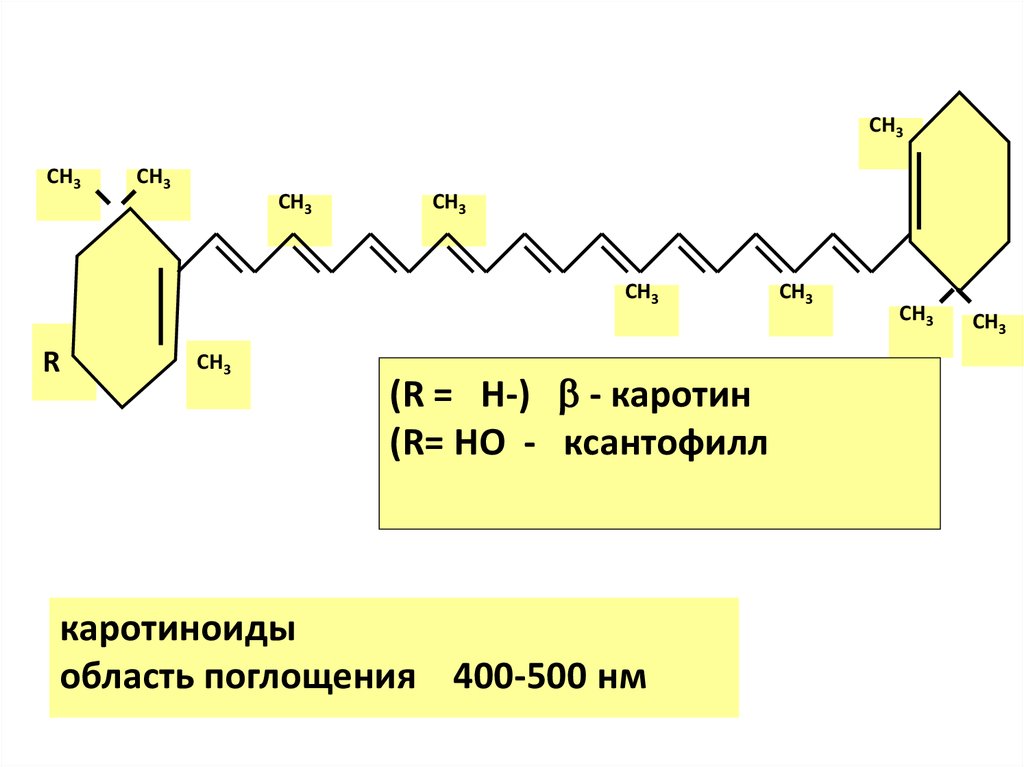
(R = H-) - каротин
(R= HO - ксантофилл
каротиноиды
область поглощения 400-500 нм
СН3
СН3
СН3
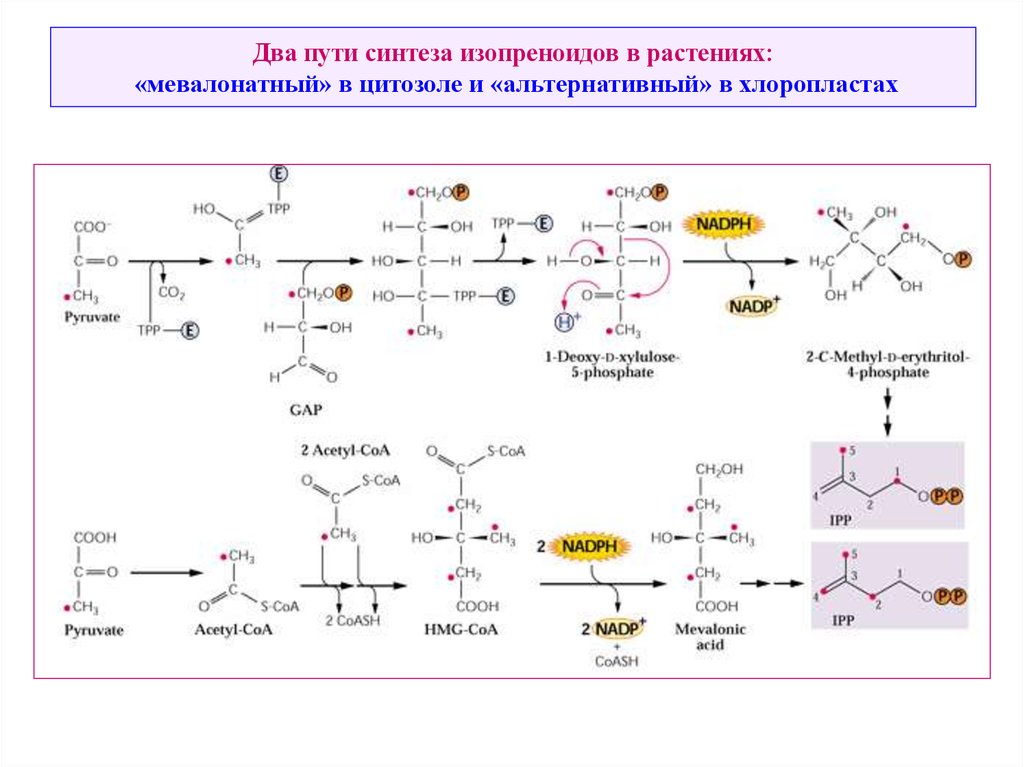
23. Два пути синтеза изопреноидов в растениях: «мевалонатный» в цитозоле и «альтернативный» в хлоропластах
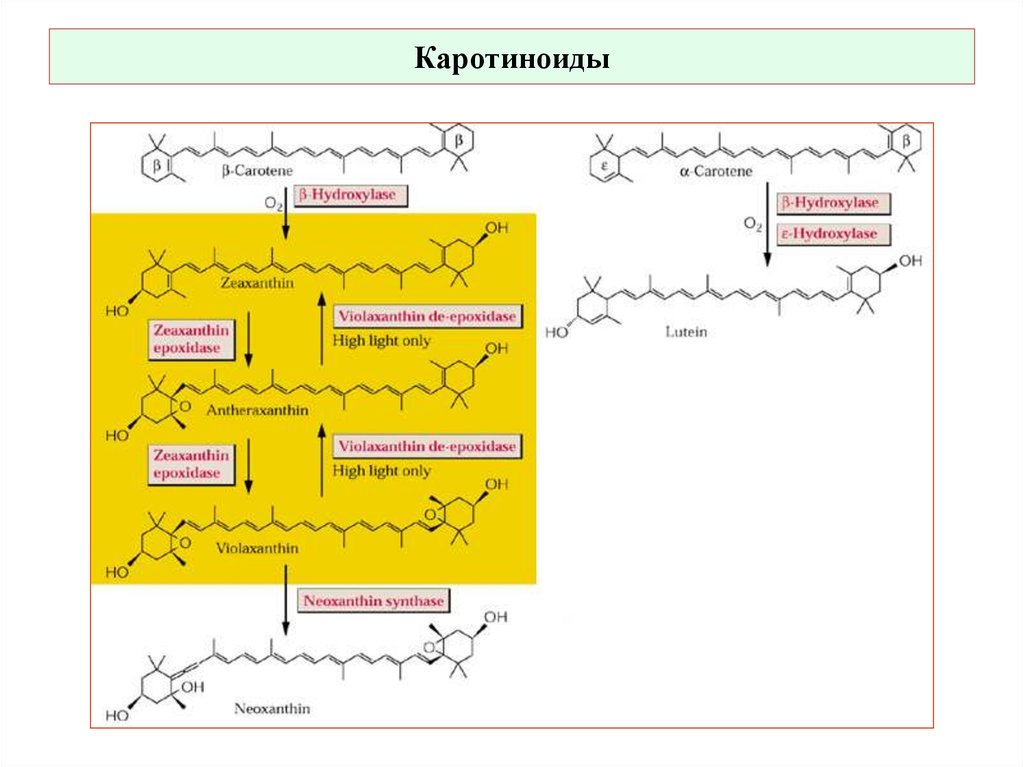
24. Каротиноиды
25. Другие важные изопреноиды
1. Фитольный хвост хлорофилов2. Убихиноны и пластохиноны, филлохинон
3. Стероидные соединения
4. Некоторые растительные гормоны
(гибереллины, брассиностероиды,
абсцизовая кислота)
5. Каучук и гуттаперча
Гиббереллин А1 (GA1)
Абсцизовая кислота (АБК)
Брассинолид
26.
ФОТОСИНТЕЗО2*
Фотоингибирование :
повреждение
белка Д1
РЦ ФС 2
разрушение
хлорофилла
О2.-
Н2О2
перекисное
окисление
липидов
мембран
27. Функции каротиноидов
1. Антенны (400 – 500 нм)2. Структурная (организация ССК)
3. Фотопротекторная (виолаксантиновый цикл)
4. Защита от УФ и высоких интенсивностей света
a/
R˚
RН
hν
RH
carо car
1Р
PРЦ
3car
1car
3Р
P + 1O2
3car
1car
3O
2
car + P+680
car+ + P680
5. Биосинтез сигнальных молекул (Абсцизовая кислота, АБК)
b/
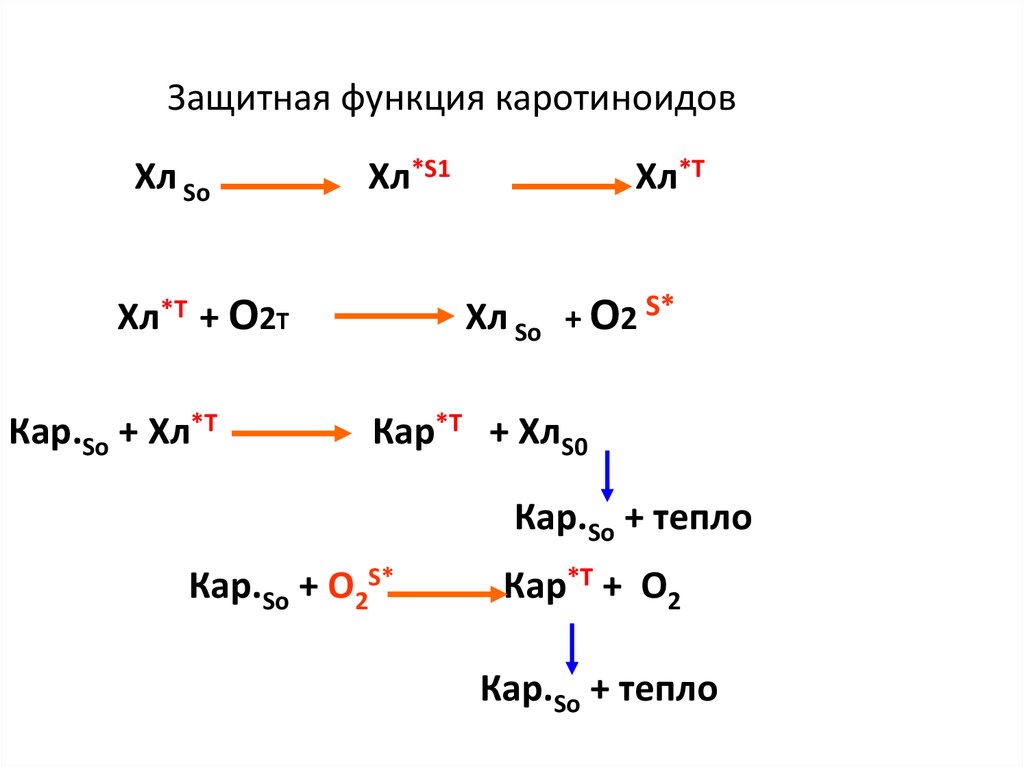
28. Защитная функция каротиноидов
Хл SoХл*S1
Хл So + O2 S*
Хл*Т + O2T
Кар.So + Хл*Т
Хл*Т
Кар*Т + ХлS0
Кар.So + тепло
Кар.So + O2S*
Кар*Т + О2
Кар.So + тепло
29.
Виолаксантиновый цикл1.Зеаксантин
2. Антераксантин
3. Виолаксантин
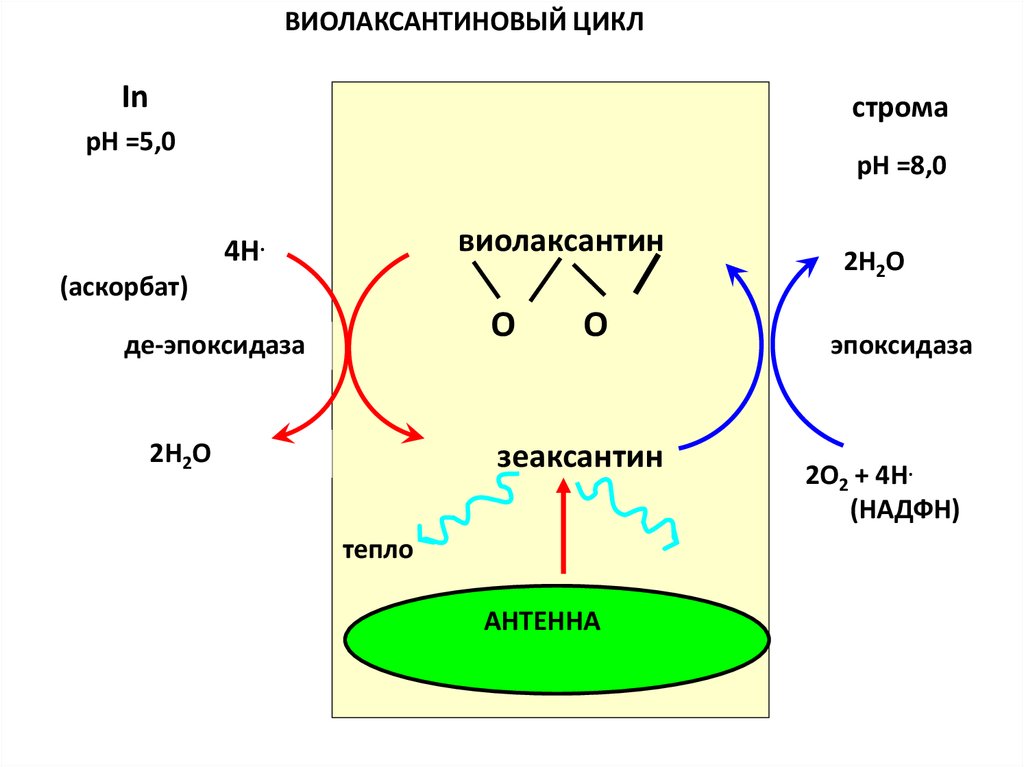
30.
ВИОЛАКСАНТИНОВЫЙ ЦИКЛIn
строма
рН =5,0
рН =8,0
виолаксантин
4Н.
(аскорбат)
О
де-эпоксидаза
2Н2О
О
зеаксантин
тепло
АНТЕННА
2Н2О
эпоксидаза
2О2 + 4Н.
(НАДФН)
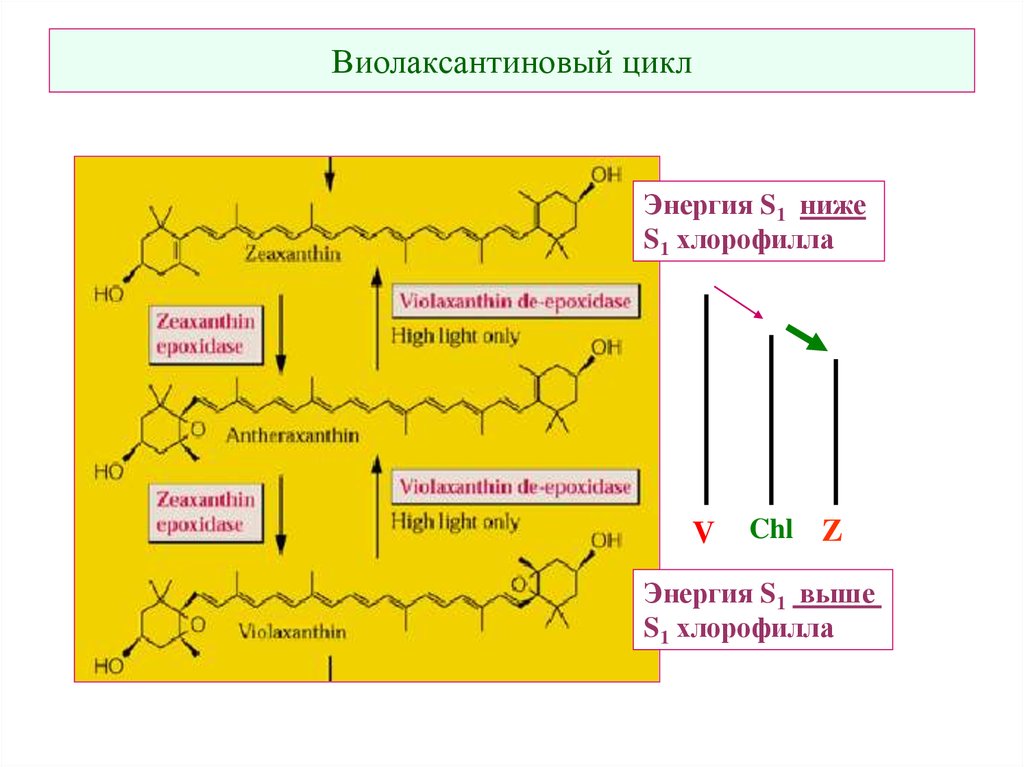
31. Виолаксантиновый цикл
Энергия S1 нижеS1 хлорофилла
V
Chl Z
Энергия S1 выше
S1 хлорофилла
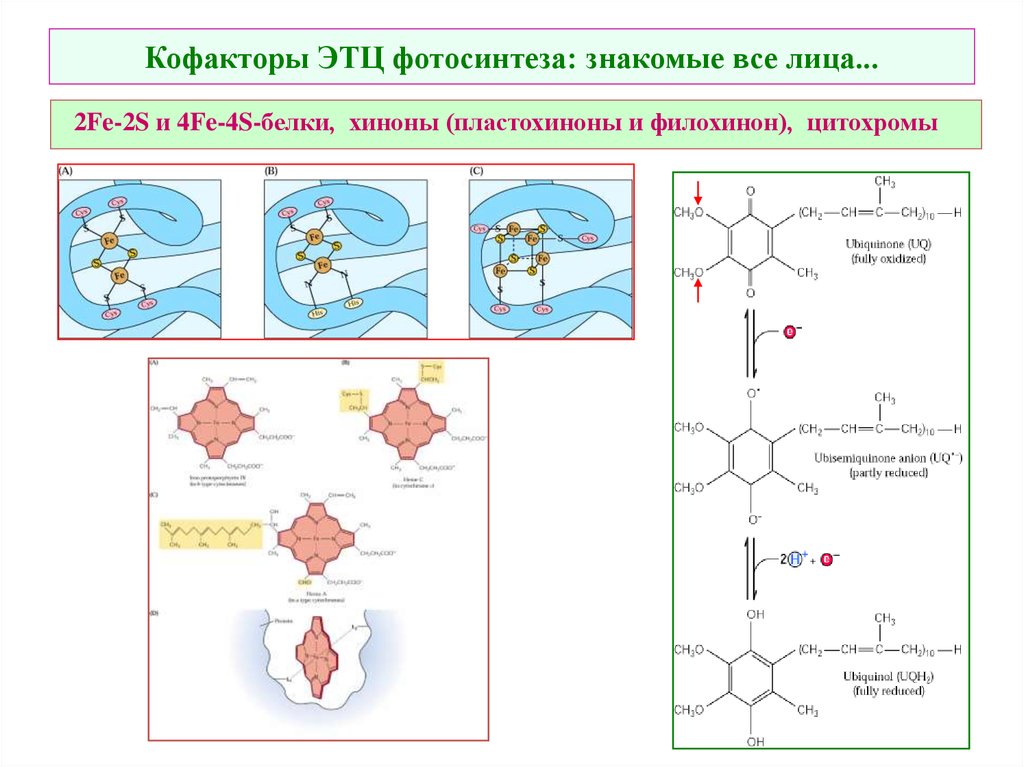
32. Кофакторы ЭТЦ фотосинтеза: знакомые все лица...
2Fe-2S и 4Fe-4S-белки, хиноны (пластохиноны и филохинон), цитохромы33.
Строение хиноновO
||
CH3O
CH3
CH3
|
[CH2-CH = C –CH2] 10-H
CH3
||
O
34.
Редокс превращения вмолекулах хинонов
O
||
O
|
е- + 2Н+
е-
||
O
|
O-
пластохинон
семихинон
Q + 1e-
OH
|
Q•– + 1e- + 2H+
|
OH
пластохинол
QH2
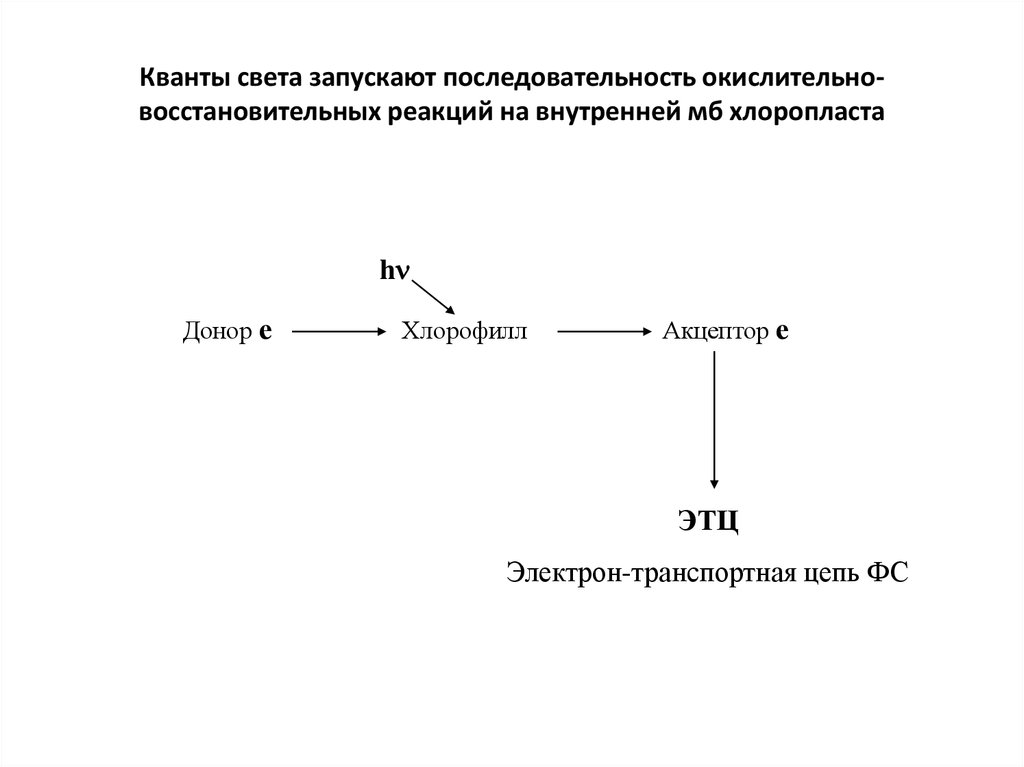
35. Кванты света запускают последовательность окислительно-восстановительных реакций на внутренней мб хлоропласта
Кванты света запускают последовательность окислительновосстановительных реакций на внутренней мб хлоропластаh
Донор е
Хлорофилл
Акцептор е
ЭТЦ
Электрон-транспортная цепь ФС
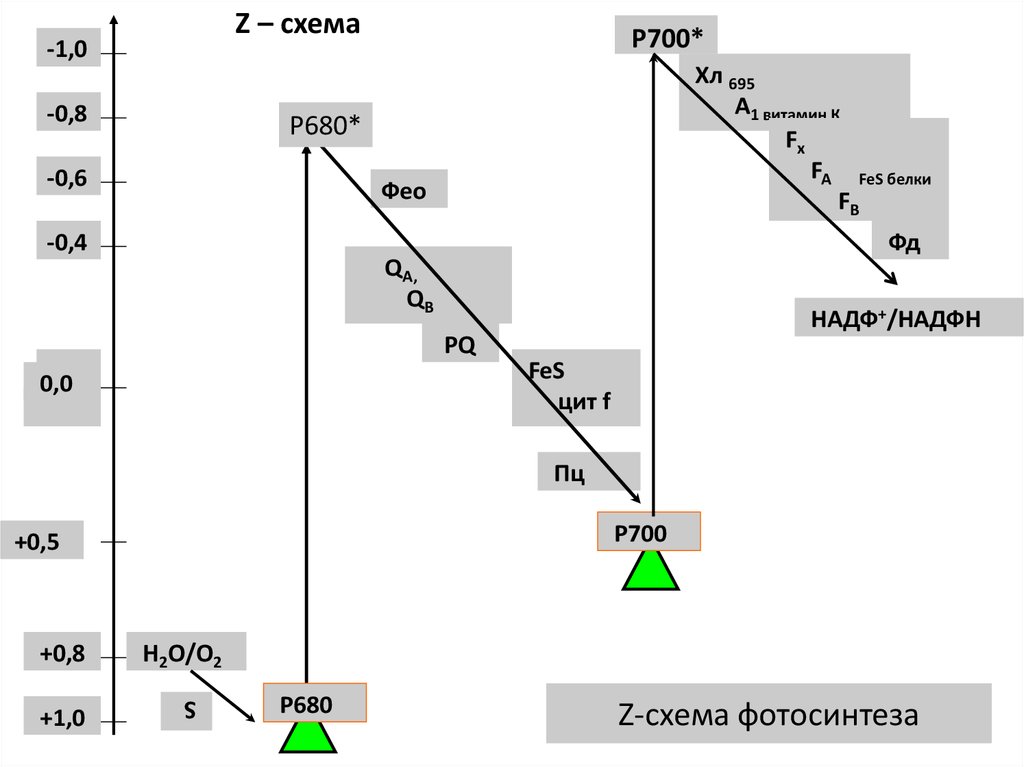
36. Z-схема
37. Z-схема фотосинтеза
Z – схема-1,0
-0,8
Р700*
Хл 695
А1 витамин К
Fx
FA FeS белки
FB
Р680*
-0,6
Фео
-0,4
Фд
QA,
QB
НАДФ+/НАДФН
PQ
FeS
цит f
0,0
Пц
Р700
+0,5
+1,0
Н2О/O2
S
+0,8
Р680
Z-схема фотосинтеза
38.
39. Гетерогенная организация тилакиодный структур
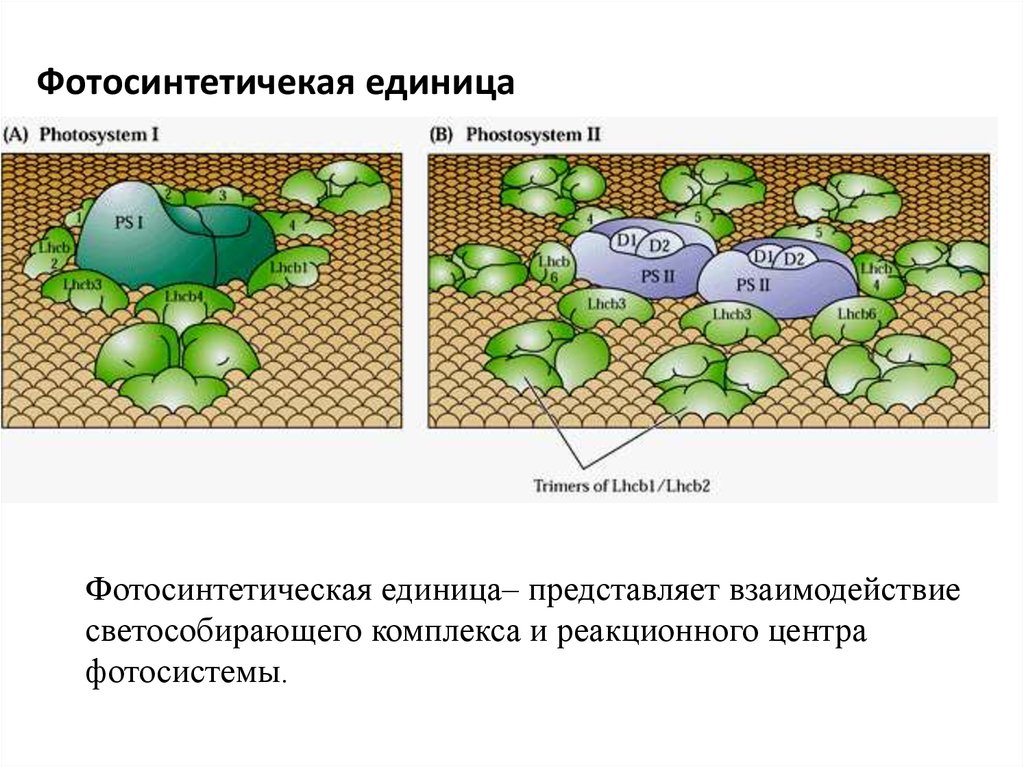
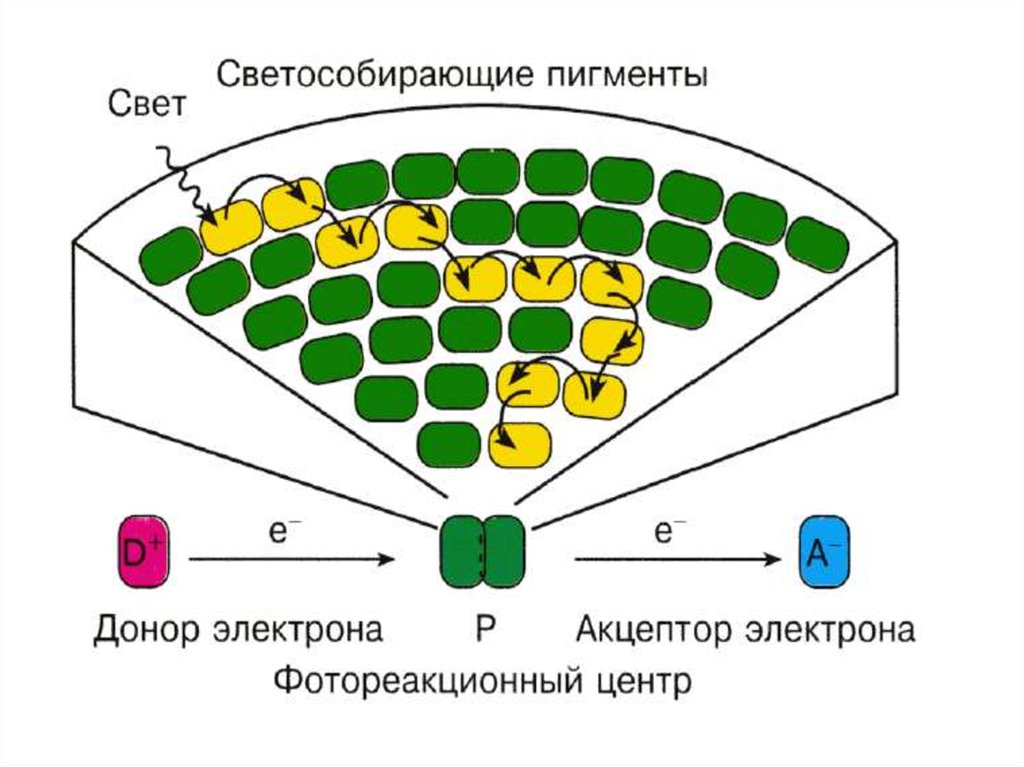
40. Фотосинтетичекая единица
Фотосинтетическая единица– представляет взаимодействиесветособирающего комплекса и реакционного центра
фотосистемы.
41. Фотосистема 2
АНТЕННА ФС2Белки -СР 24, СР26,
СР29
ССК (II)
Белки - 25,27 и 28 кДа
Хл а ~ 150
Хл b ~ 100
Каротиноиды ~ 50
СР43
ФОКУСНАЯ АНТЕННА НА
БЕЛКАХ СР43 и СР47
Хл а 30; -каротин - 2
Хл а
Хл b
ксантофиллы
РЦ
СР47
Реакционный центр
Фотосистема 2
42.
ССК IБелки 17-24 кДа
Хл а 80-120
Хл b ?
каротиноиды 50
РЦ
Кор-комплекс
Хл а 90-100
каротин 20
РЕАКЦИОННЫЙ
ЦЕНТР
43.
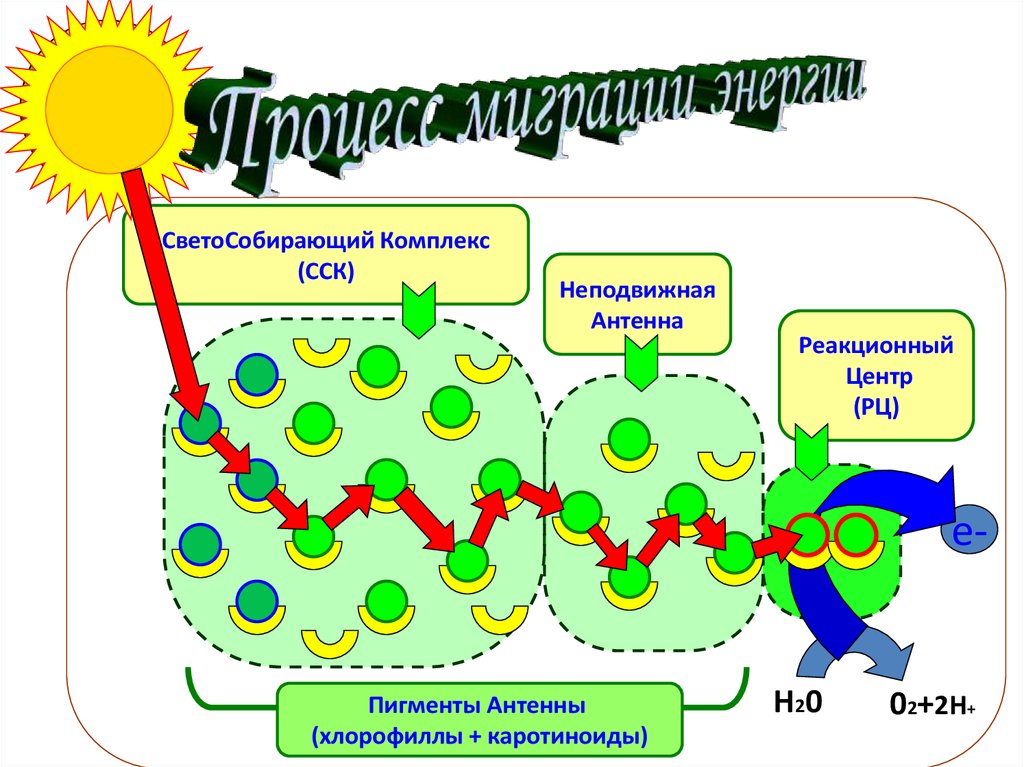
СветоСобирающий Комплекс(ССК)
Неподвижная
Антенна
Реакционный
Центр
(РЦ)
е-
Пигменты Антенны
(хлорофиллы + каротиноиды)
Н20
02+2Н+
44.
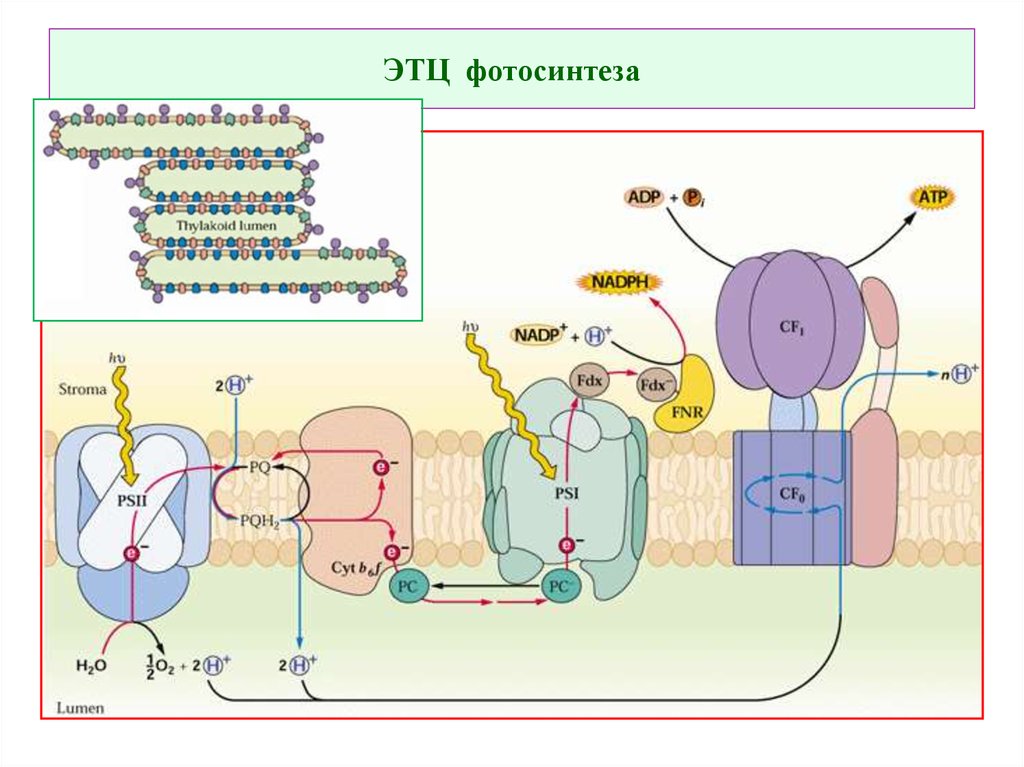
45. ЭТЦ фотосинтеза
46. Структура фотосистемы II
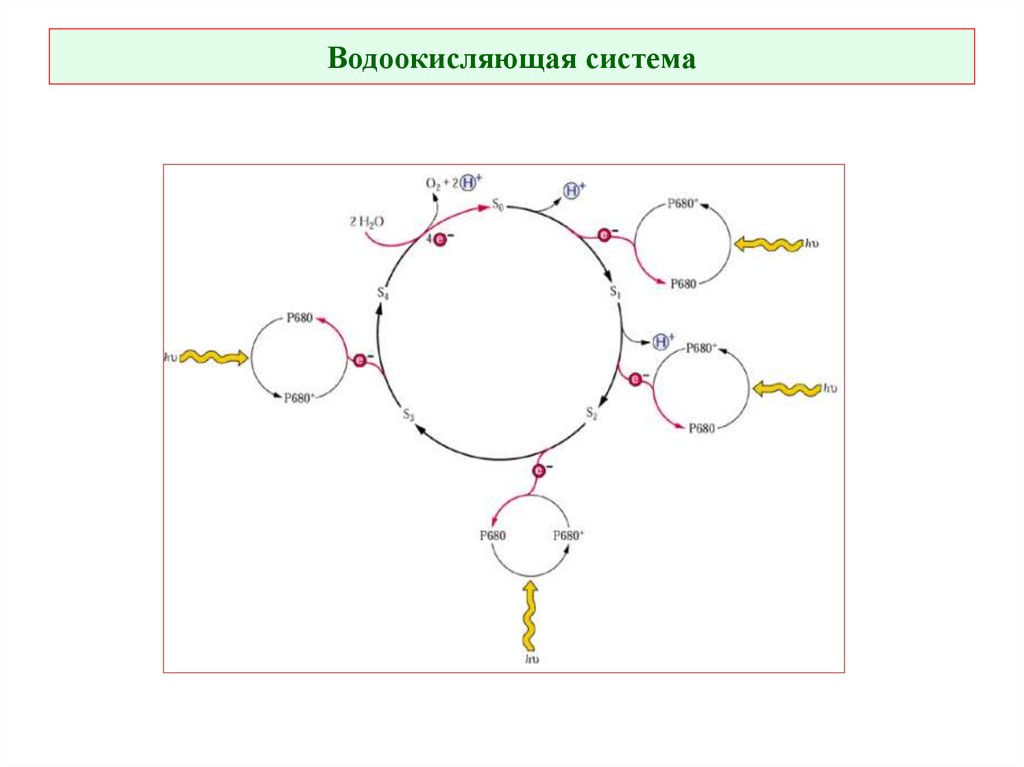
Феофитин47. Водоокисляющая система
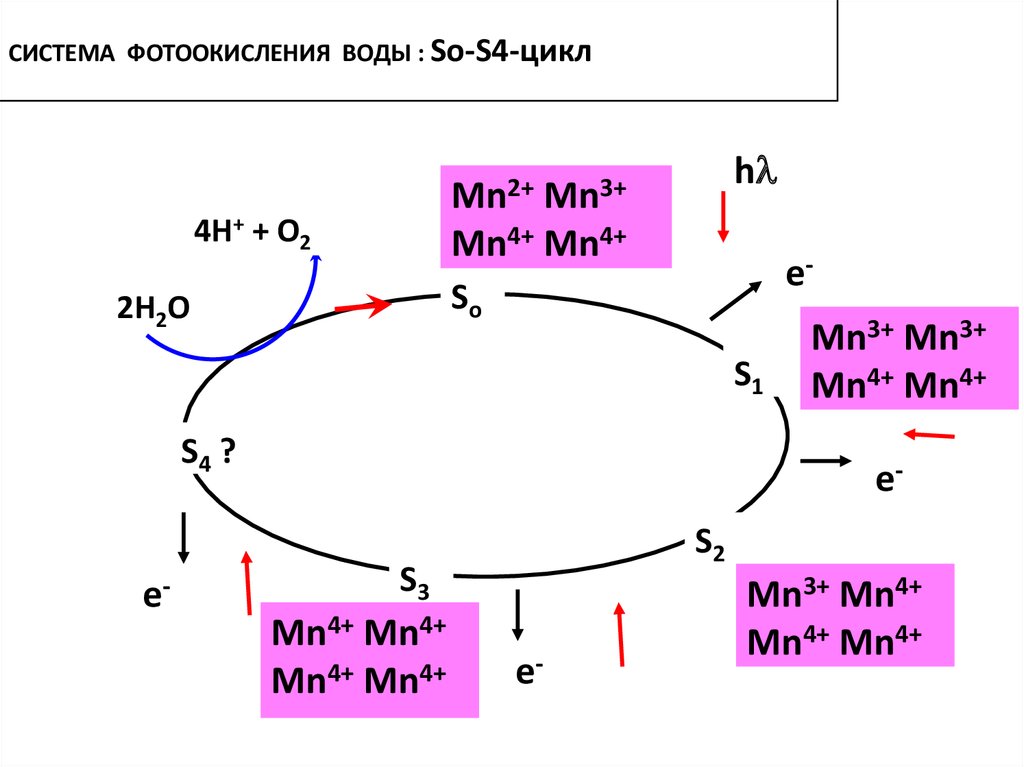
48. СИСТЕМА ФОТООКИСЛЕНИЯ ВОДЫ : So-S4-цикл
Mn2+4Н+ + О2
h
Mn3+
Mn4+ Mn4+
e-
So
2Н2О
S1
S4 ?
e-
Mn3+ Mn3+
Mn4+ Mn4+
e-
S2
S3
Mn4+ Mn4+
Mn4+ Mn4+
e-
Mn3+ Mn4+
Mn4+ Mn4+
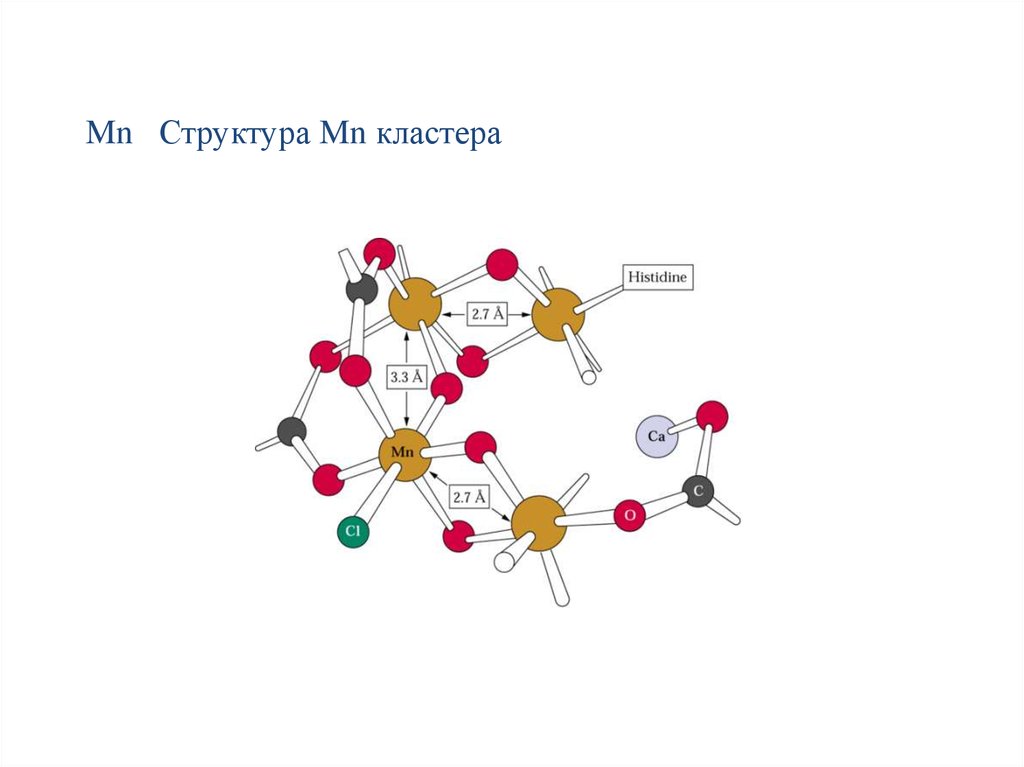
49.
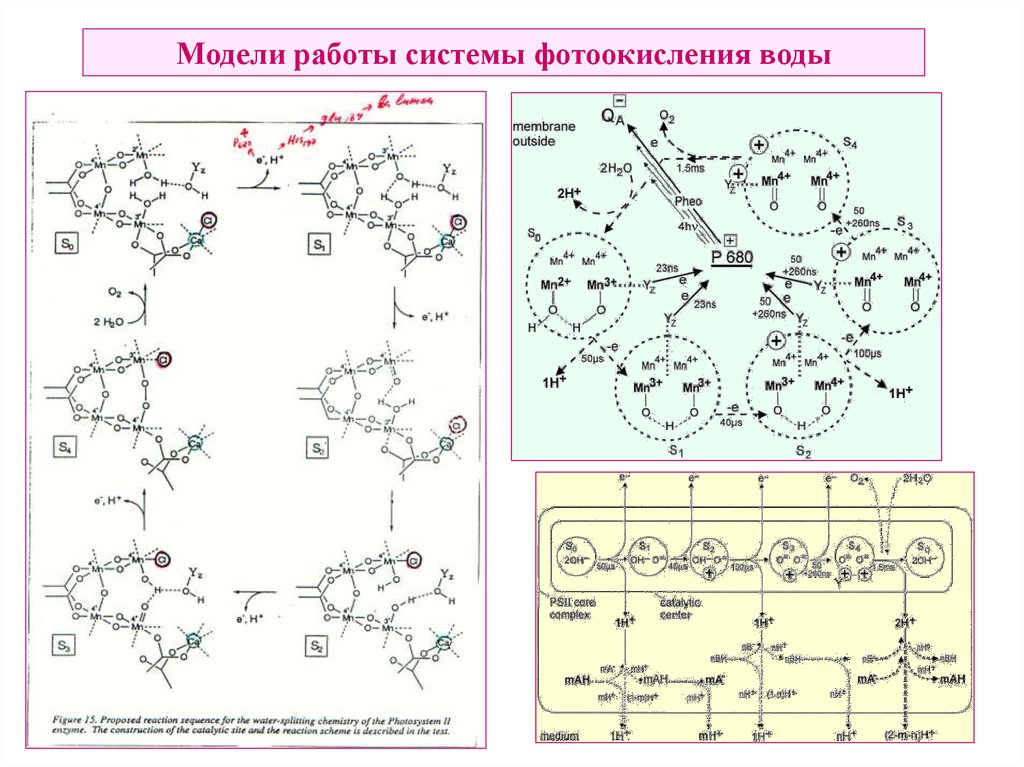
Mn Структура Mn кластера50. Модели работы системы фотоокисления воды
51. Организация ЭТЦ фотосинтетического аппарата
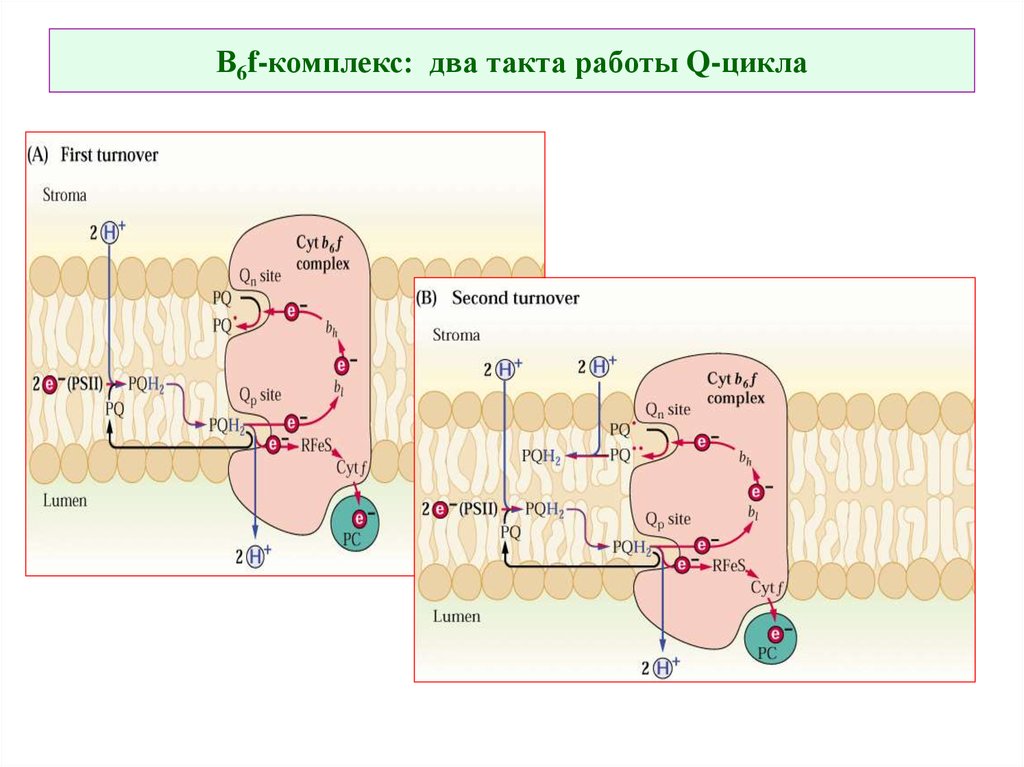
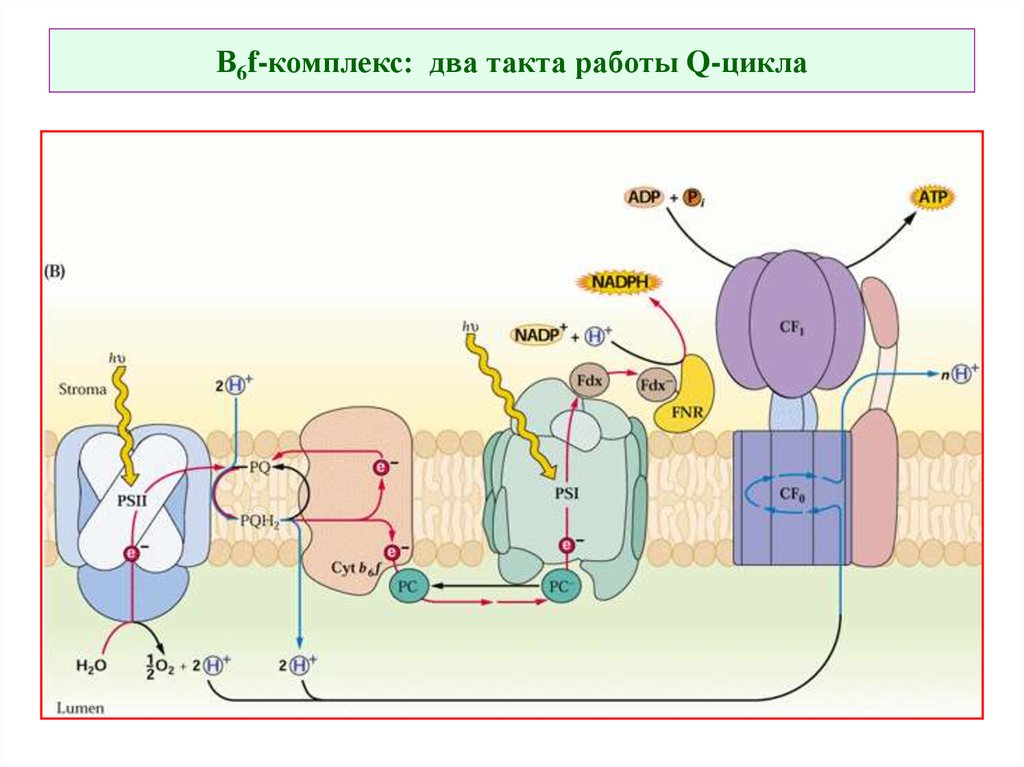
52. В6f-комплекс: два такта работы Q-цикла
53. В6f-комплекс: два такта работы Q-цикла
54. Структура RC фотосистемы I
13 белков:А – 83 kDa, 751 a-к
В - 82,5 kDa, 735 a-к
Гетеродимер, на нем:
Р700, А0, А1, Fx
С – 8,9 kDa, - FA, FB
D (19 kDa),
E – связь с Fd
F (19 kDa) - связь с Pc
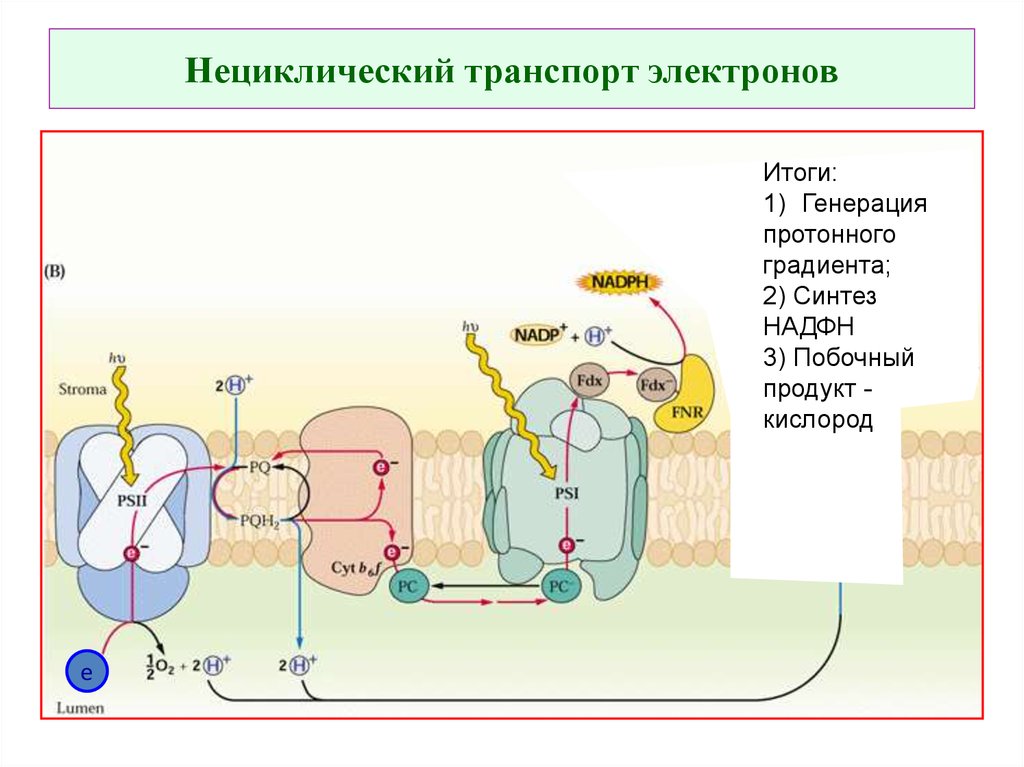
55. Нециклический транспорт электронов
Итоги:1) Генерация
протонного
градиента;
2) Синтез
НАДФН
3) Побочный
продукт кислород
е
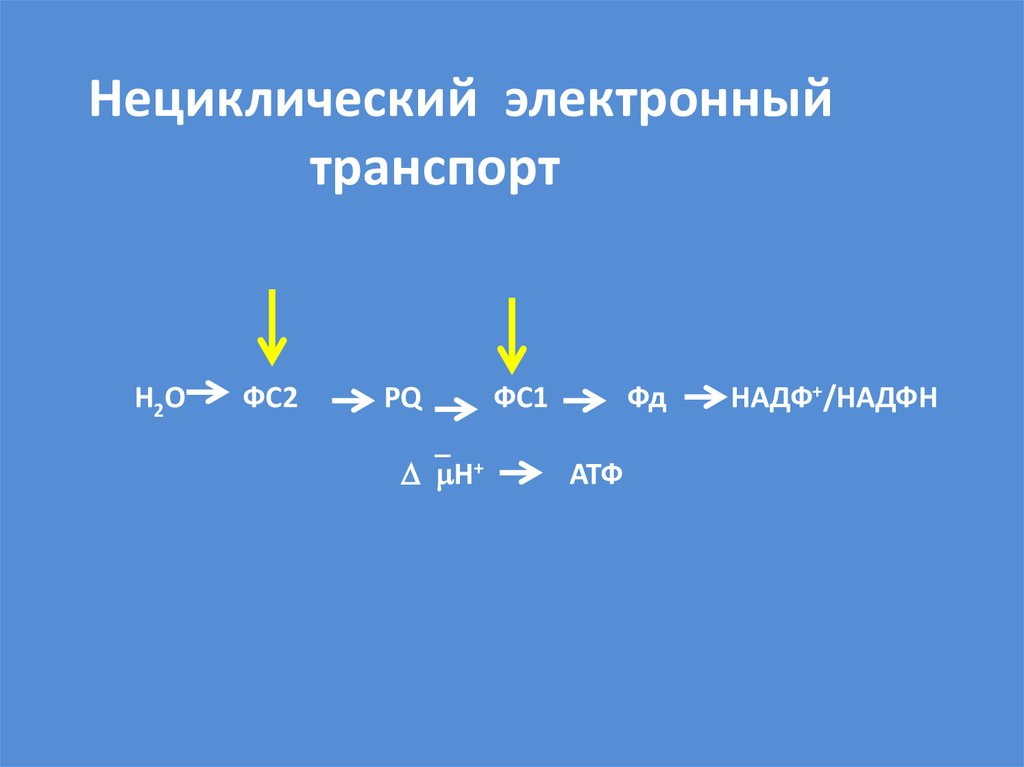
56. Нециклический электронный транспорт
H2ОФС2
PQ
Н+
ФС1
Фд
АТФ
НАДФ+/НАДФН
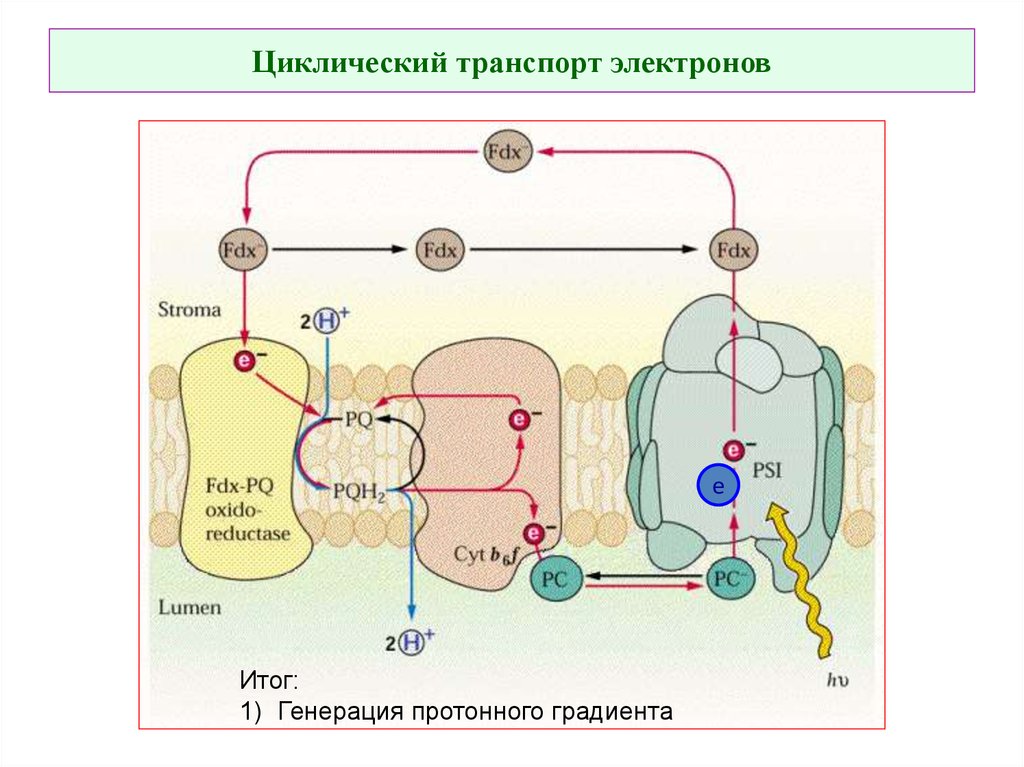
57. Циклический транспорт электронов
еИтог:
1) Генерация протонного градиента
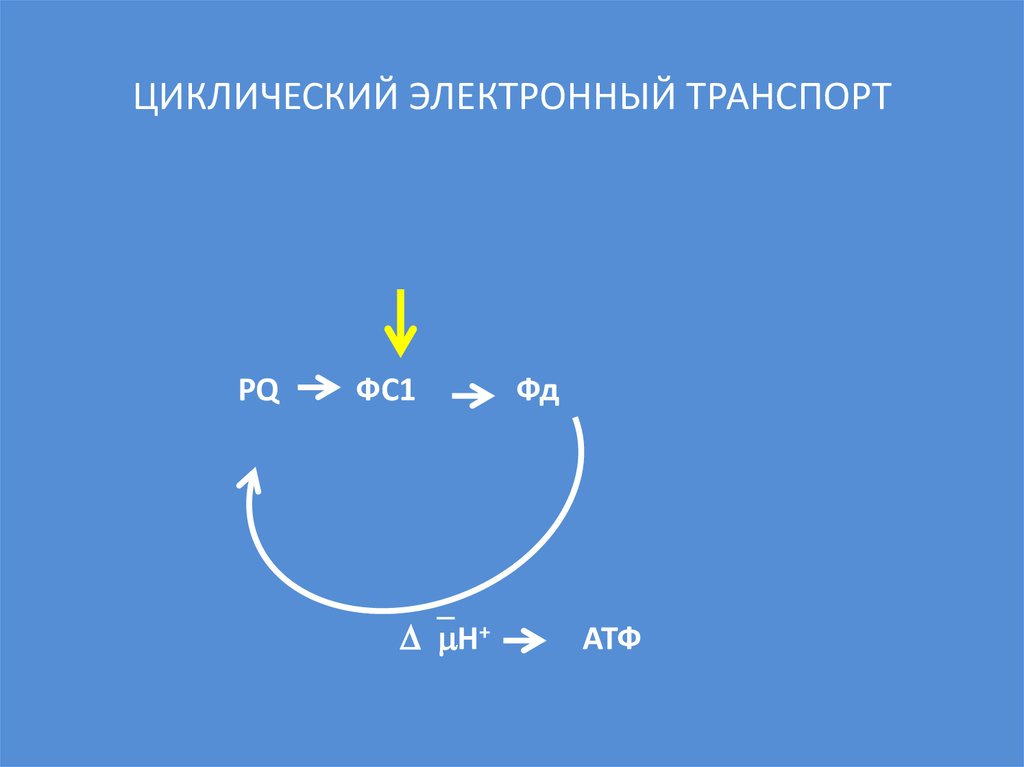
58. ЦИКЛИЧЕСКИЙ ЭЛЕКТРОННЫЙ ТРАНСПОРТ
PQФС1
Н+
Фд
АТФ
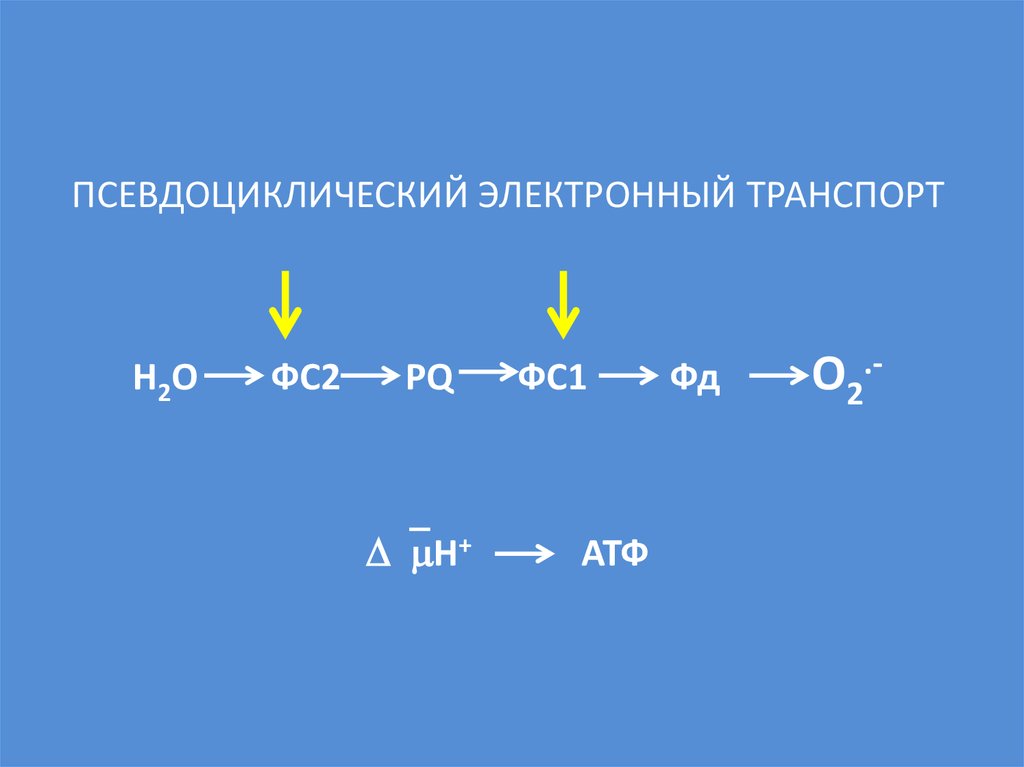
59. ПСЕВДОЦИКЛИЧЕСКИЙ ЭЛЕКТРОННЫЙ ТРАНСПОРТ Н2О ФС2 PQ ФС1 Фд O2.- Н+ АТФ
ПСЕВДОЦИКЛИЧЕСКИЙ ЭЛЕКТРОННЫЙ ТРАНСПОРТН2О
ФС2
PQ
Н+
ФС1
АТФ
Фд
O2.-
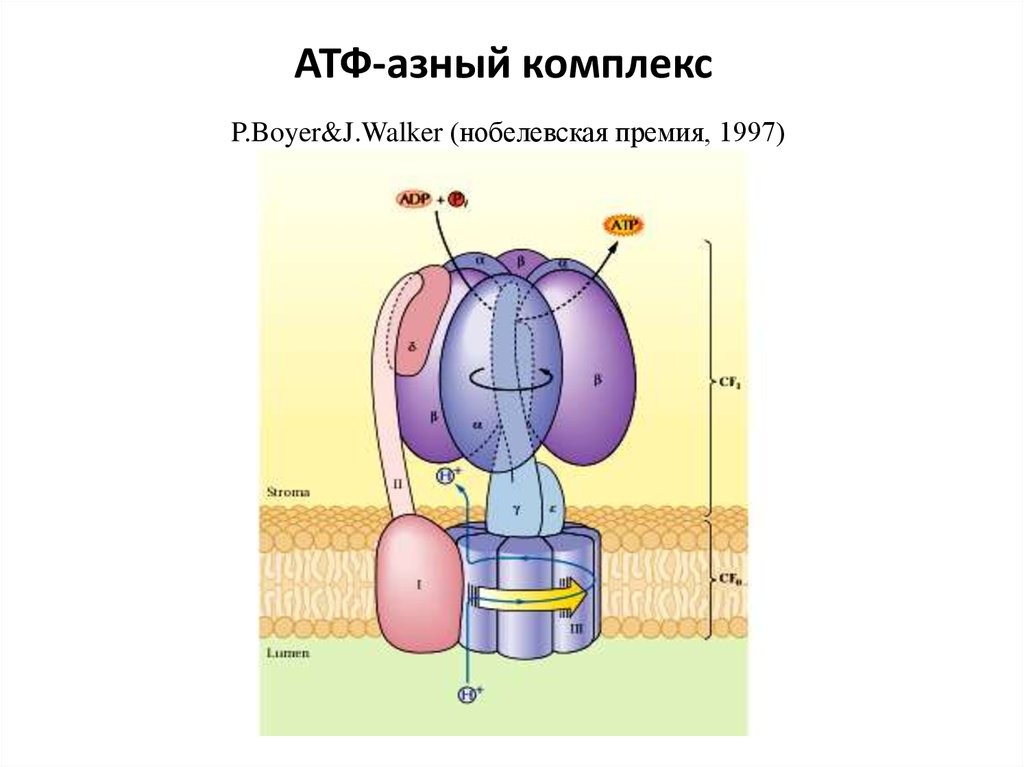
60. АТФ-азный комплекс
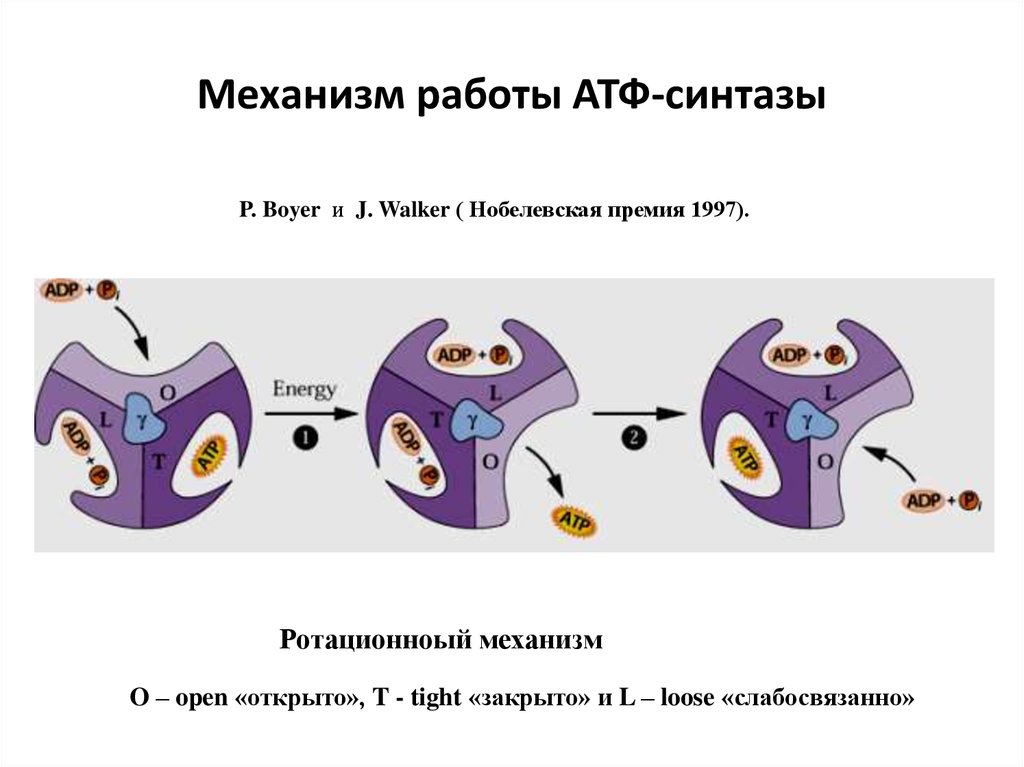
P.Boyer&J.Walker (нобелевская премия, 1997)61. Механизм работы АТФ-синтазы
P. Boyer и J. Walker ( Нобелевская премия 1997).Ротационноый механизм
O – open «открыто», T - tight «закрыто» и L – loose «слабосвязанно»
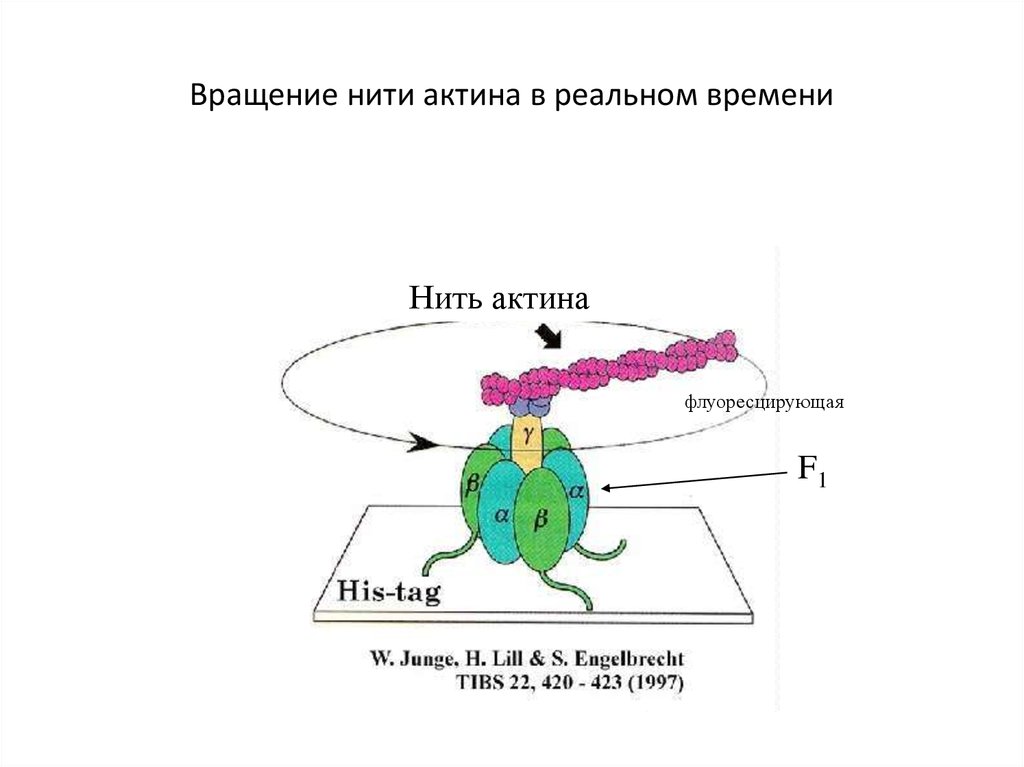
62. Вращение нити актина в реальном времени
Нить актинафлуоресцирующая
F1






















 Биология
Биология








