Похожие презентации:
Алканы (предельные углеводороды)
1. Алканы (предельные углеводороды)
ЭлХимикЭля Теп
2. Строение алканов
Алканы имеют два типа связей С-С и С-НС-С ковалентная неполярная, С-Н ковалентная
слабополярная
Все связи одинарные (σ-связи ли сигма-связи)
Валентный угол Н-С-Н равен 109º28´
Эти углеводороды называют предельными , так
как они не имеют кратных связей
3. Гомологический ряд
Метан СН4Этан С2Н6
Пропан С3Н8
Бутан С4Н10
Пентан С5Н12
Гексан С6Н14
Гептан С7Н16
Октан С8Н18
Нонан С9Н20
Декан С10Н22
Из этого следует , что
общая формула
алканов СnH2n+2
4. Изомерия
Изомеры – это вещества одинакового качественногои количественного состава, но разные по строению.
Алканам присуща структурная изомерия, то есть
изменение положения радикалов.
Радикалом называют частицу с формулой CnH2n+1
(для алканов), или еще она называется алкил
Изомерия впервые в гомологическом ряду алканов
встречается у бутана: н-бутан (нормальный бутан) ,
изобутан (2-метилпропан), то есть радикал метил
СН3 соединен со вторым атомом углеродной
цепочки, состоящей из трех атомов углерода (
вспоминаем формулу пропана С3Н8)
5. Физические свойства
Алканы с количеством атомов углерода до 4включительно – газы
С количеством 5-10 атомов углерода – жидкости
Далее – твердые вещества
6. Химические свойства
1) Крекинг – процесс термического разложенияуглеводорода, при котором происходит разрыв
связей С-С , и образуются вещества с более
короткой цепочкой углеродных атомов
Пример: СН3-СН2-СН2-СН2-СН2-СН3
СН3-СН3 + СН3-СН2-СН2-СН3
7. Химические свойства
2) Изомеризация – это процесс , при которомалканы нормального строения превращаются в
алканы с разветвленной цепочкой под действием
температур или катализаторов.
Пример: СН3-СН2-СН2-СН3
СН3-СН-СН3
СН3
8. Химические свойства
3) Дегидрирование – это процесс отщепленияводорода под действием катализаторов.
Пример: СН3-СН3
СН2 СН2 + Н2
9. Химические свойства
4) Окисление.Пример: СН4 + 2О2 = СО2 + 2Н2О
10. Химические свойства
5) Замещение :Галогенирование – реакция замещения одного и
более атомов водорода в молекуле алкана на
атом галогена. С хлором и бромом идет на свету
и при нагревании.
Пример: СН4 + Сl2
CH3Cl + HCl (
- это
квант света)
Реакция идет и дальше, пока все атомы водорода
не заменятся на атомы хлора.
11. Получение
1) Крекинг нефти2) Гидрирование непредельных углеводородов
3) Из синтез-газа ( СО+Н2)
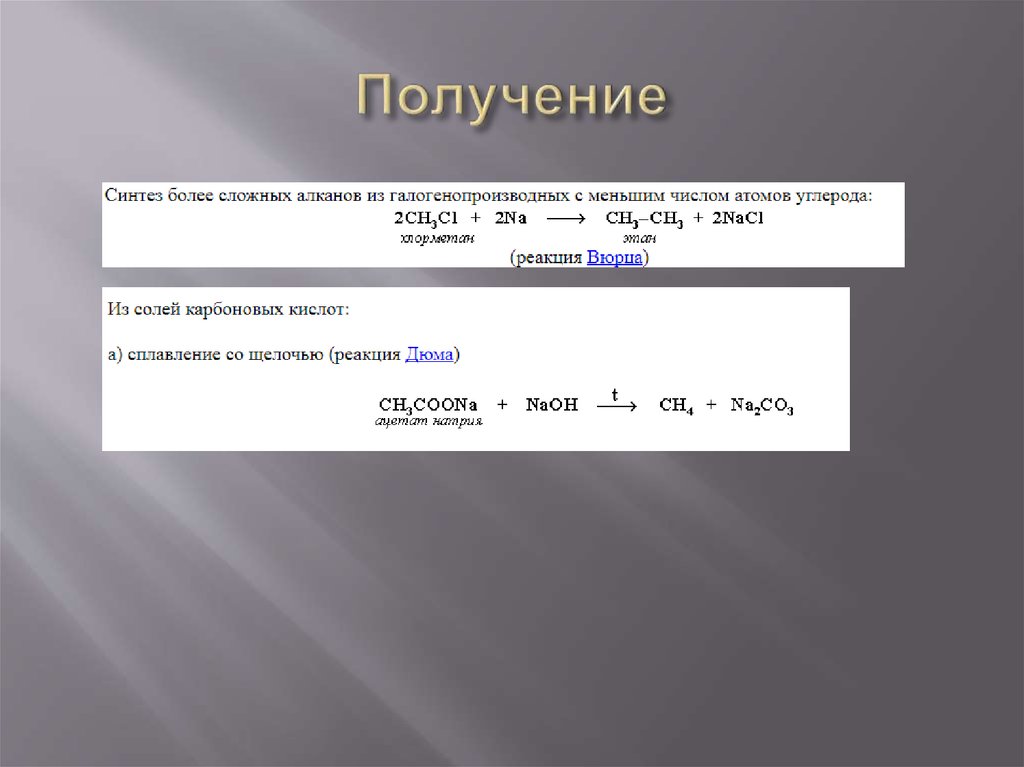
4) Синтез более сложных алканов из
галогенопроизводных с меньшим числом атомов
углерода
5) Из солей карбоновых кислот
6) Разложение карбидов металлов водой














 Химия
Химия








