Похожие презентации:
Ренин-Ангиотензин-Альдостероновая Система (РААС). Краткий анатомо-физиологический обзор
1.
РенинАнгиотензинАльдостероновая Система(РААС)
Краткий анатомофизиологически
й обзор
2.
Историческая справка1836 – R.Bright: предположение о связи гипертонии с
заболеваниями почек
1897 – R.Tigersteld: открытие ренина
1939 – I.Page: открытие ангиотензина
1954 – L.Skeggs: ангиотензин I и ангиотензин II и
предположение о существовании АПФ
1959 – обнаружена связь ЮГА почек с секрецией ренина
1971 – первый ИАПФ, выделенный из яда змеи Bothros
jararca
1975 – идентификация АПФ и coздание первого
синтетического ИАПФ – каптоприла.
3.
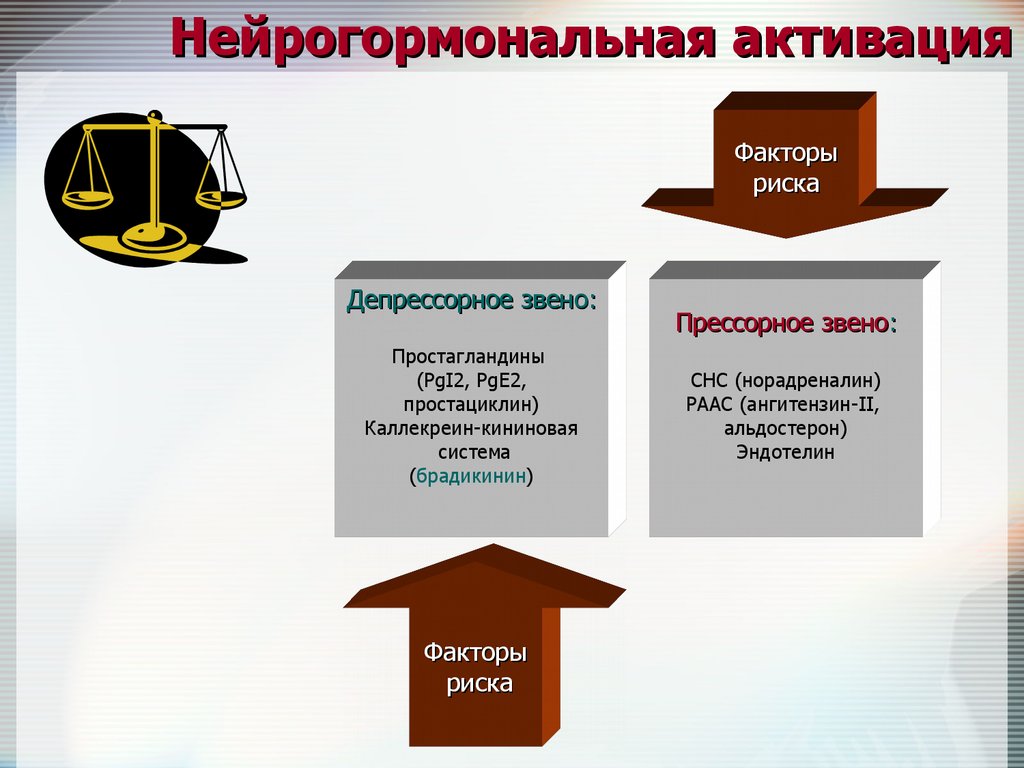
Нейрогормональная активацияФакторы
риска
Депрессорное звено:
Простагландины
(PgI2, PgE2,
простациклин)
Каллекреин-кининовая
система
(брадикинин)
Факторы
риска
Прессорное звено:
СНС (норадреналин)
РААС (ангитензин-II,
альдостерон)
Эндотелин
4.
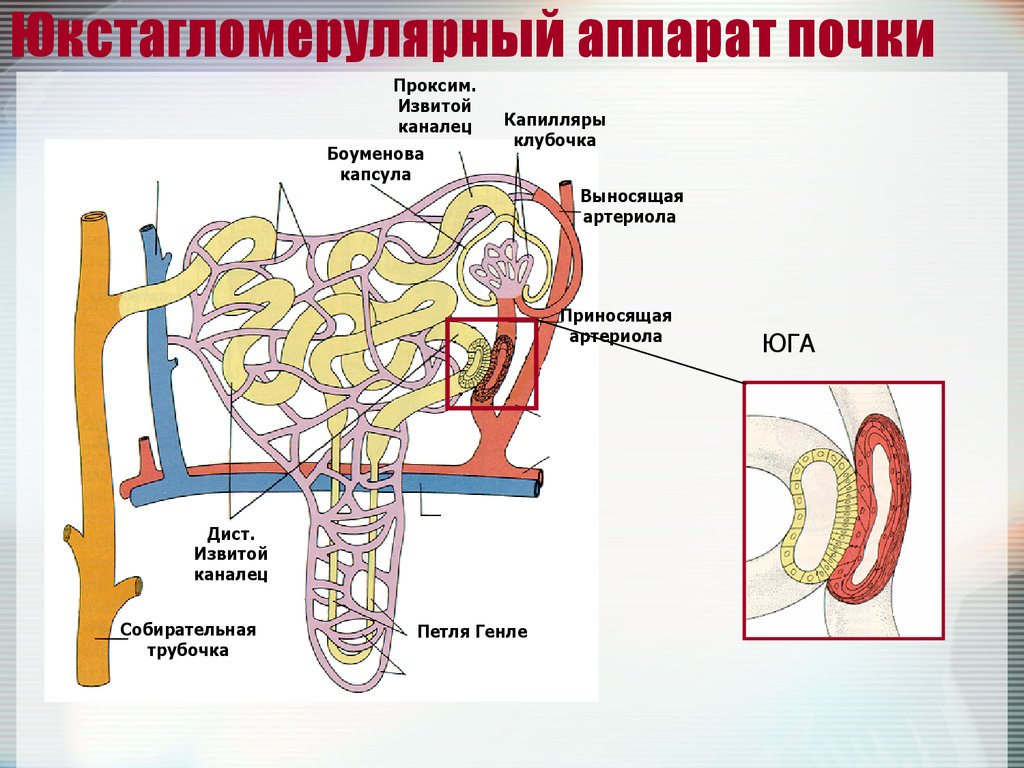
Юкстагломерулярный аппарат почкиПроксим.
Извитой
каналец
Боуменова
капсула
Капилляры
клубочка
Выносящая
артериола
Приносящая
артериола
Дист.
Извитой
каналец
Собирательная
трубочка
Петля Генле
ЮГА
5.
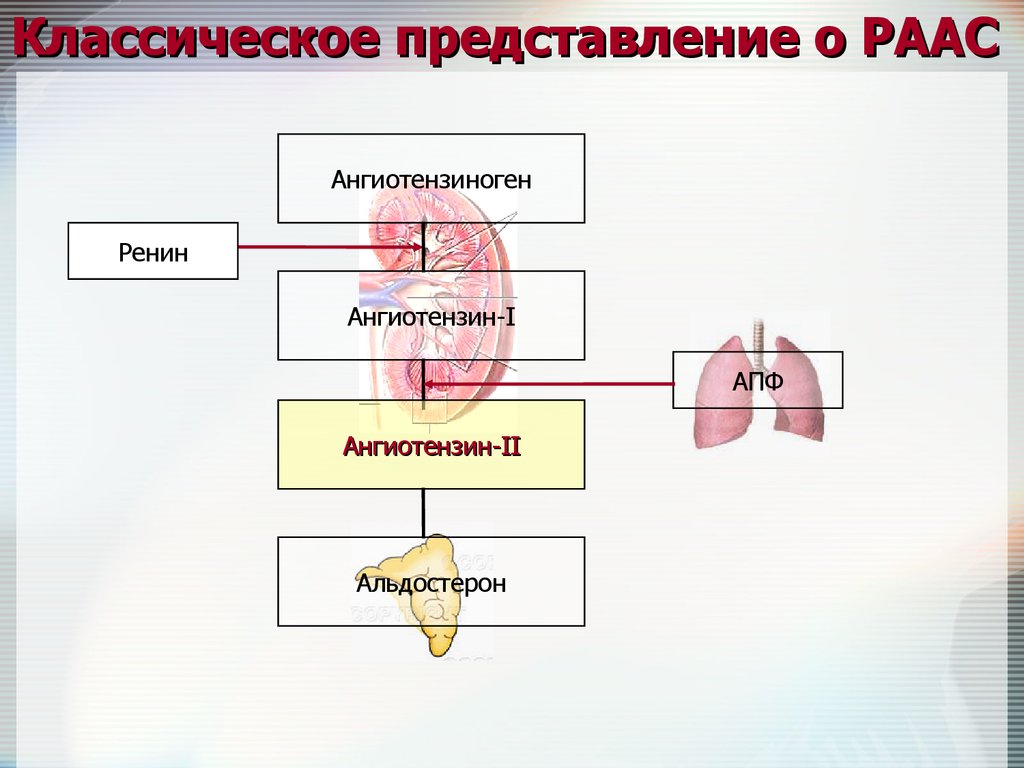
Классическое представление о РААСАнгиотензиноген
Ренин
Ангиотензин-I
АПФ
Ангиотензин-II
Альдостерон
6.
Физиологические эффекты А-IIСистемная вазоконстрикция
Синтез и секреция альдостерона
Реабсорбция натрия и воды в
проксимальных почечных канальцах
Гипертрофия кардиомиоцитов
Кардиофиброз
Пролиферация и миграция эндотелиальных
и гладкомышечных клеток, фибробластов в
сосудистой стенке и в почечных клубочках
7.
Физиологические эффекты А-IIВысвобождение эндотелина и ингибитора
активации плазминогена (РАI-1)
Высвобождение норадленалина из
окончаний симпатических нервов
Высвобождение адреналина мозговым
слоем надпочечников
Повышение активности СНС
Кардиотоксичность (повышение синтеза
свободных радикалов)
8.
Физиологические эффекты альдостеронаЗадержка натрия
Выведение калия, магния
Пролиферация фибробластов (кардио-,
ангиофиброз)
Гипертрофия кардиомиоцитов и гладких
мышц сосудов
Нарушение барорефлекторной регуляции
крообращения
Аритмогенное действие
Высвобождение ингибитора активации
плазминогена (PAI-1)
9.
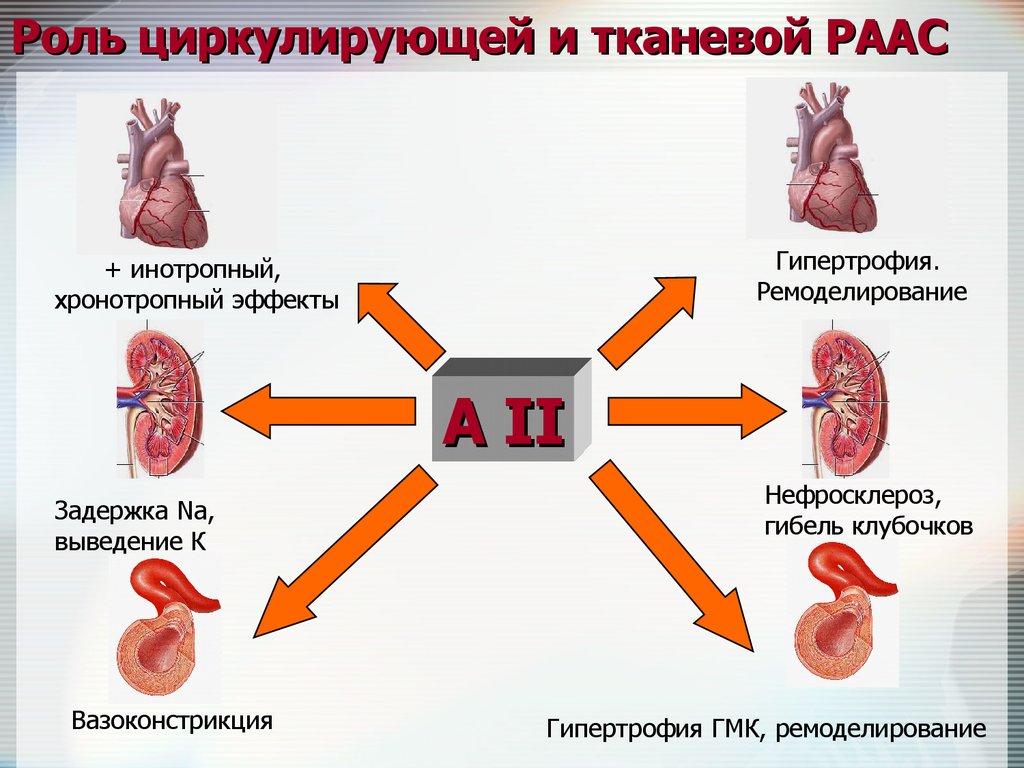
Роль циркулирующей и тканевой РААСГипертрофия.
Ремоделирование
+ инотропный,
хронотропный эффекты
А II
Задержка Na,
выведение К
Вазоконстрикция
Нефросклероз,
гибель клубочков
Гипертрофия ГМК, ремоделирование
10.
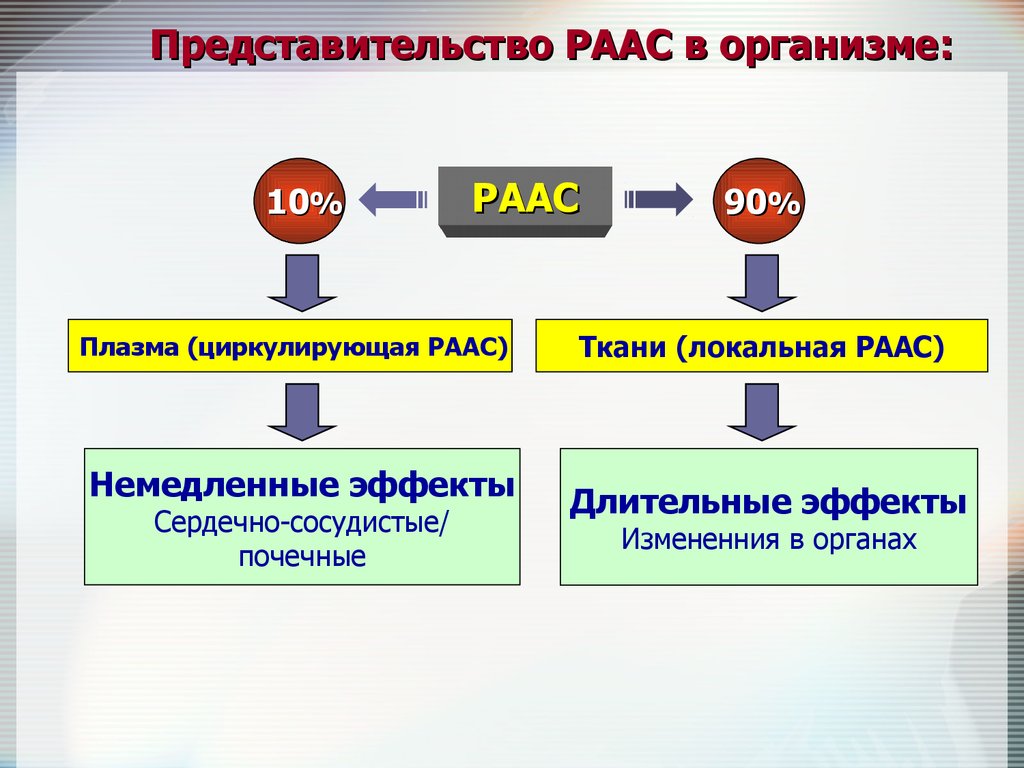
Представительство РААС в организме:10%
РААС
Плазма (циркулирующая РААС)
Немедленные эффекты
Сердечно-сосудистые/
почечные
90%
Ткани (локальная РААС)
Длительные эффекты
Измененния в органах
11.
Локальная РААСОрганы и ткани способные продуцировать А- II
Органы и ткани
Сердце
Мозг
Почки
Сосуды
Атероск. бляшки
Надпочечники
Клеточный уровень
Миоциты
нейроны
Мезангий клубочков
Эндотелий
Макрофаги
Гладкие мышцы
12.
Брадикинин: физиологические эффектыВазодилатация, в том числе
коронарных артерий, эфферентных
артериол почечных клубочков
Усиление натрийуреза
Кардиопротективное действие:
увеличение коронарного кровотока
увеличение коронарного резерва
ограничение размеров инфаркта
Ослабление оглушенности и гибернации
миокарда
13.
Брадикинин: физиологические эффектыЦитопротекция в условиях гипоксии
Стимуляция роста капилляров
Стимуляция синтеза и высвобождения NO
эндотелием
Торможение высвобождения
норадреналина из нервных окончаний СНС
Торможение секреции катехоламинов
надпочечниками
Стимуляция чувствительных нервных
волокон (в частности кашлевых)
14.
Брадикинин: метаболизм глюкозыУменьшение высвобождение глюкозы
из печени
усиление захвата глюкозы тканями
Ускорение окисления глюкозы
15.
Брадикинин:Антитрофические эффекты:
Антипролиферативные
Антифибротические
Увеличение фибринолитической
активности плазмы крови:
Усиление высвобождения тканевого
активатора плазминогена (tPA)
16.
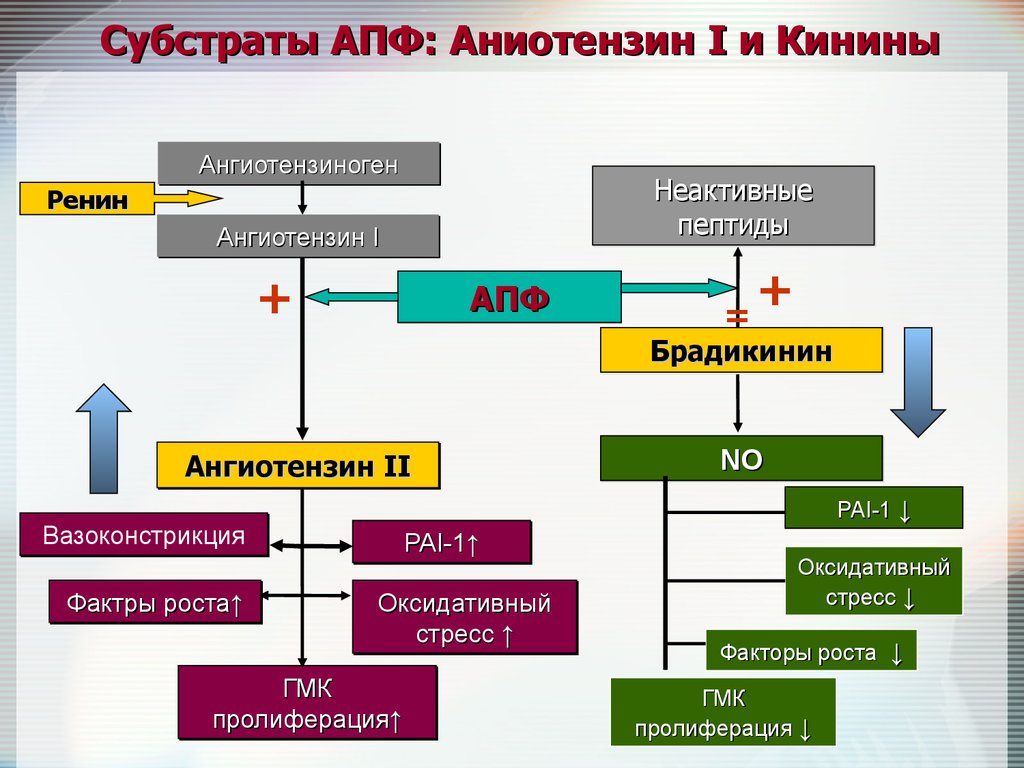
Субстраты АПФ: Аниотензин I и КининыАнгиотензиноген
Неактивные
Неактивные
пептиды
пептиды
Ренин
Ангиотензин
Ангиотензин I
+
АПФ
+
=
Брадикинин
Брадикинин
Ангиотензин II
II
Вазоконстрикция
Фактры
Фактры роста
роста↑
NO
PAI-1 ↓
PAI-1↑↑
Оксидативный
Оксидативный
стресс ↑↑
ГМК
ГМК
пролиферация
пролиферация↑↑
Оксидативный
стресс ↓
Факторы роста ↓
ГМК
пролиферация ↓
17.
БрадикининИз
Из всего
всего множества
множества медиаторов,
медиаторов,
взаимодействующих
взаимодействующих сс эндотелием
эндотелием
брадикинин
брадикинин является
является самым
самым
мощным
мощным стимулятором
стимулятором синтеза
синтеза ии
высвобождение
высвобождение NO
NO
18.
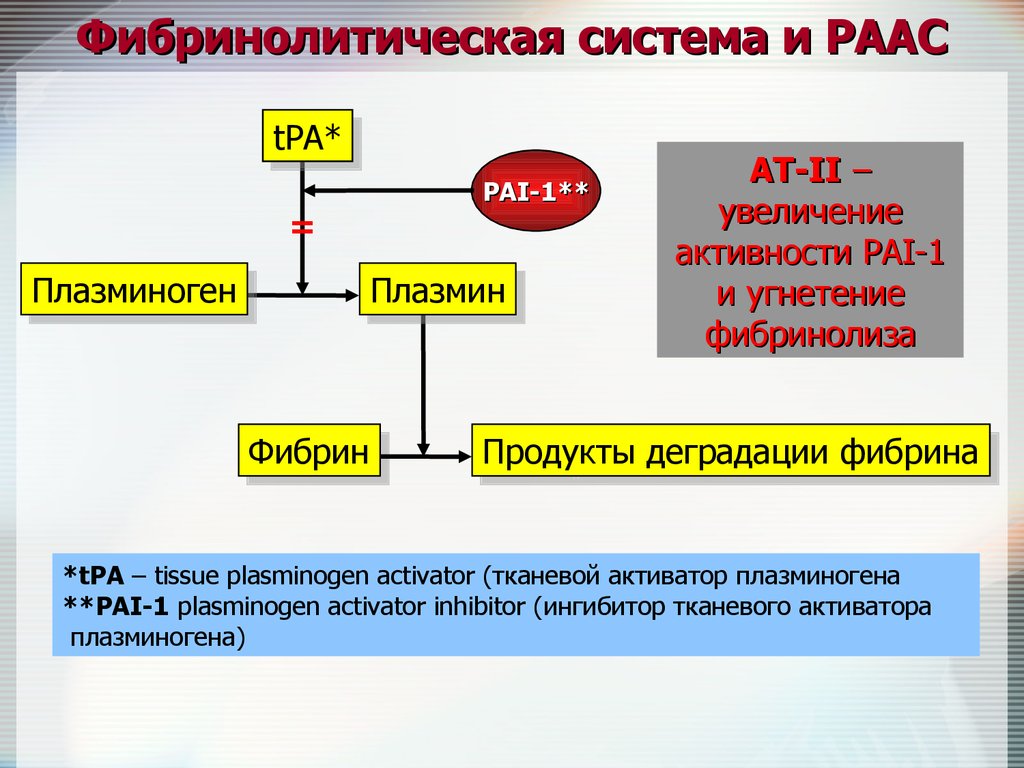
Фибринолитическая система и РААСtPA*
tPA*
PAI-1**
=
Плазминоген
Плазминоген
Плазмин
Плазмин
Фибрин
Фибрин
АТ-II –
увеличение
активности PAI-1
и угнетение
фибринолиза
Продукты
Продукты деградации
деградации фибрина
фибрина
*tPA – tissue plasminogen activator (тканевой активатор плазминогена
**PAI-1 plasminogen activator inhibitor (ингибитор тканевого активатора
плазминогена)
19.
Резюме:Активация
Активация РААС,
РААС, наряду
наряду сс СНС,
СНС, играет
играет
ключевую
ключевую роль
роль вв развитии
развитии сердечносердечнососудистых
сосудистых заболеваний
заболеваний
Наибольший
Наибольший вклад
вклад вв риск
риск развития
развития
сердечно-сосудистых
сердечно-сосудистых заболеваний
заболеваний ии их
их
осложнений
осложнений (инфаркта,
(инфаркта, инсульта,
инсульта, ХСН,
ХСН,
ХПН)
ХПН) вносит
вносит локальная
локальная или
или тканевая
тканевая РААС
РААС
20.
Роль РААСв развитии
сердечно-сосудистых заболеваний
Эндотелиальная дисфункция и
атеросклероз
21.
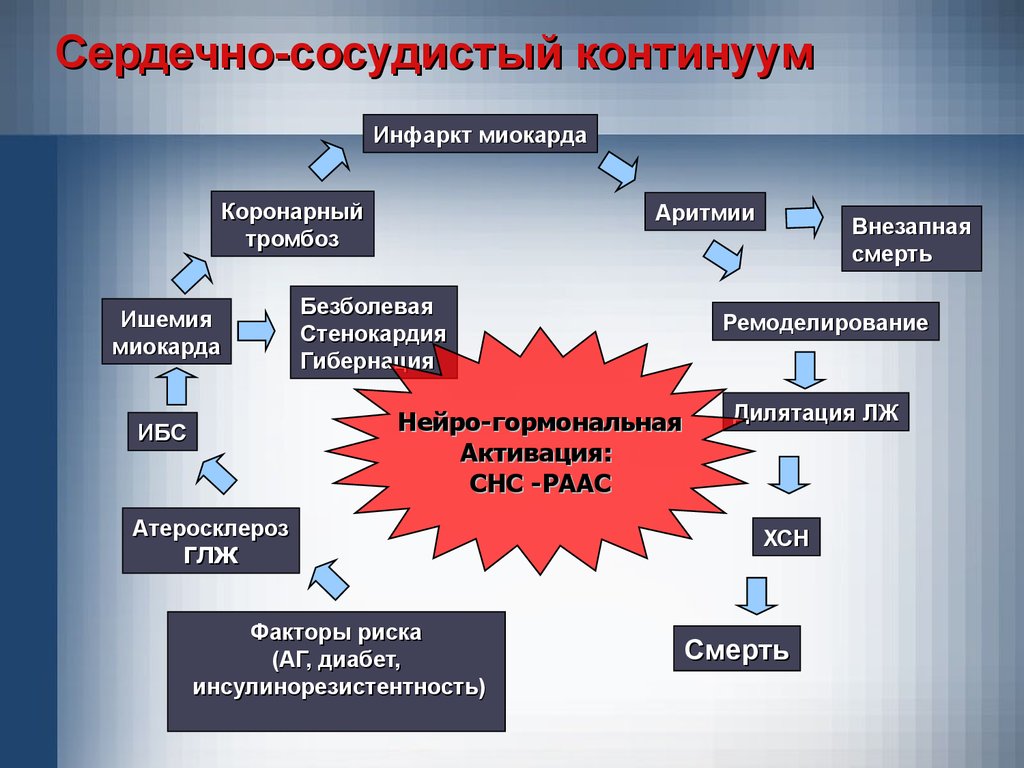
Сердечно-сосудистый континуумИнфаркт миокарда
Коронарный
тромбоз
Ишемия
миокарда
Аритмии
Безболевая
Стенокардия
Гибернация
Нейро-гормональная
Активация:
СНС -РААС
ИБС
Атеросклероз
ГЛЖ
Факторы риска
(АГ, диабет,
инсулинорезистентность)
Внезапная
смерть
Ремоделирование
Дилятация ЛЖ
ХСН
Смерть
22.
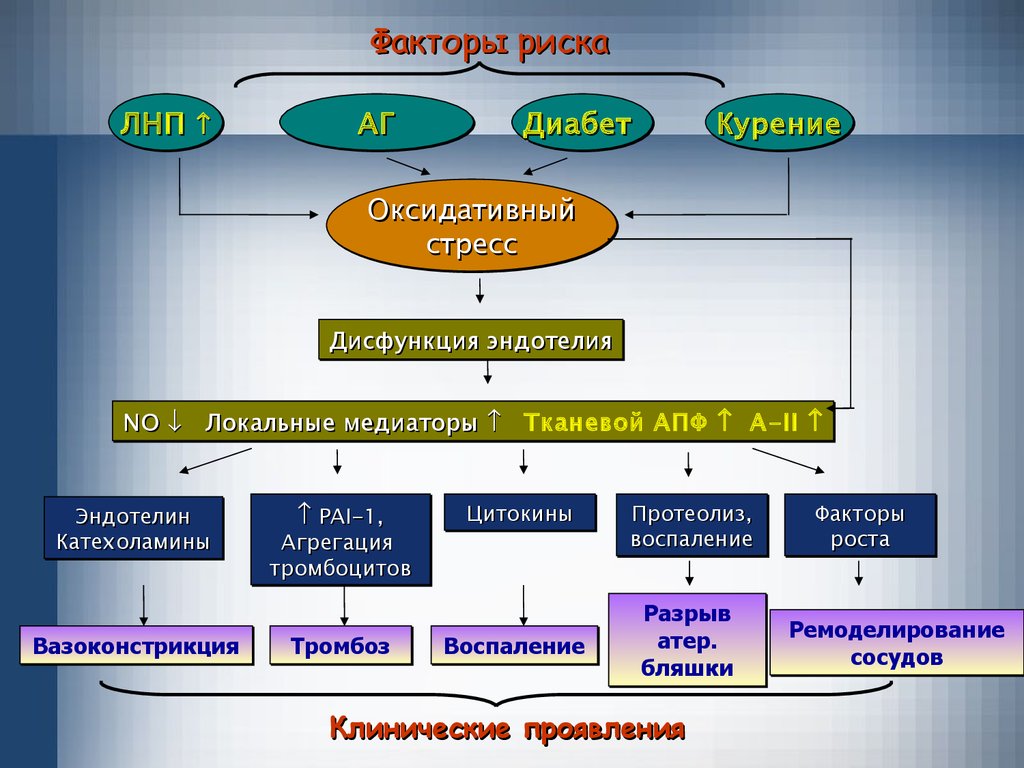
Факторы рискаЛНП
ЛНП
АГ
АГ
Диабет
Диабет
Курение
Курение
Оксидативный
Оксидативный
стресс
стресс
Дисфункция
Дисфункция эндотелия
эндотелия
NO
NO Локальные
Локальные медиаторы
медиаторы Тканевой АПФ А-II
Эндотелин
Эндотелин
Катехоламины
Катехоламины
Вазоконстрикция
PAI-1,
PAI-1,
Агрегация
Агрегация
тромбоцитов
тромбоцитов
Тромбоз
Цитокины
Цитокины
Воспаление
Протеолиз,
Протеолиз,
воспаление
воспаление
Разрыв
атер.
бляшки
Клинические проявления
Факторы
Факторы
роста
роста
Ремоделирование
сосудов
23.
Активация РААС (А-II)Атеросклероз
Атеросклероз
АПФ
А
АII
II
фильтрации
фильтрации
альдостерона
альдостерона
Протеинурия
Протеинурия
Клубочковая
Клубочковая
гипертензия
гипертензия
ИНСУЛЬТ
ХПН
Гипертрофия
Гипертрофия
Фиброз
Фиброз
Апоптоз
Апоптоз
Ремоделирование
Ремоделирование
ОИМ
ХСН
Гипертрофия
Гипертрофия
Вазоконстрикция
Вазоконстрикция
АГ
24.
Участие АII в атерогенезеМост сердечно-сосудистого континуума: атеросклероз
Факторы
риска
Circulation 2001;103;448-454
Инфаркт
миокарда
25.
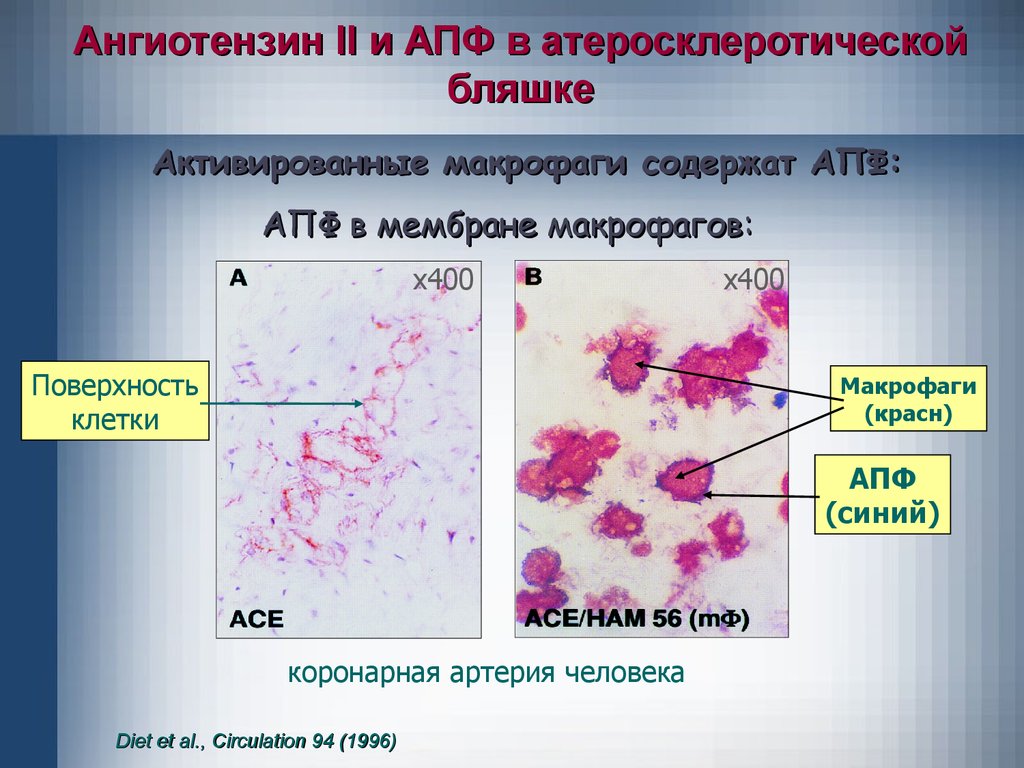
Ангиотензин ll и АПФ в атеросклеротическойбляшке
Активированные макрофаги содержат АПФ:
АПФ в мембране макрофагов:
x400
Поверхность
клетки
x400
Макрофаги
(красн)
АПФ
(синий)
коронарная артерия человека
Diet et al., Circulation 94 (1996)
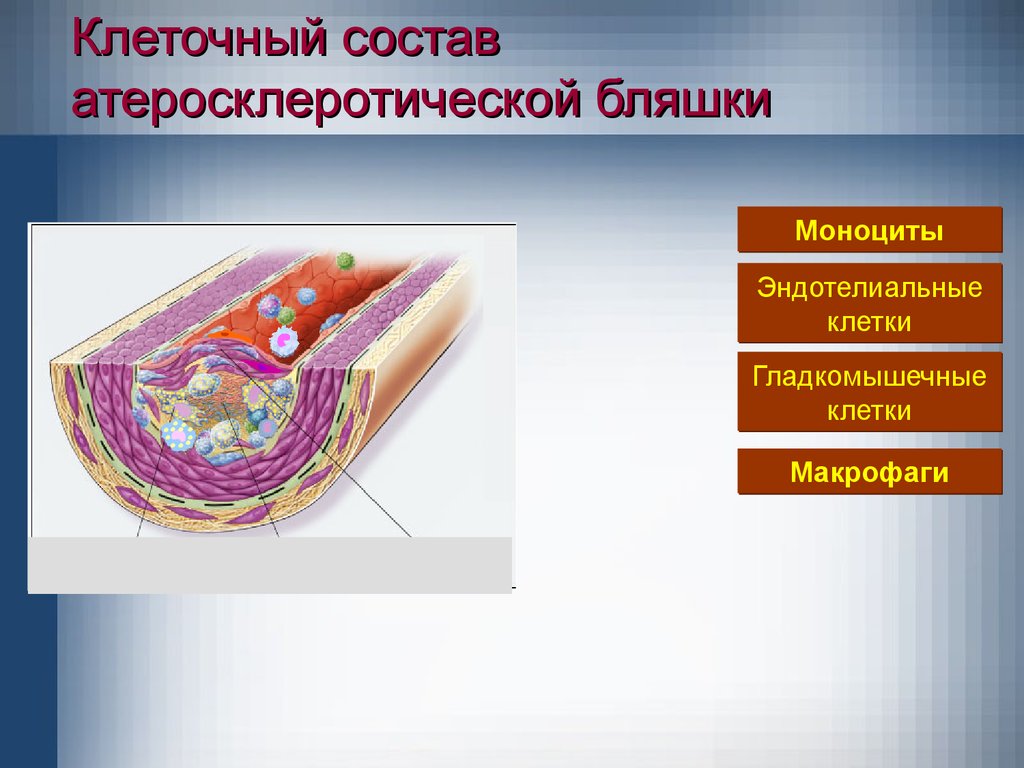
26.
Клеточный составатеросклеротической бляшки
Моноциты
Эндотелиальные
клетки
Гладкомышечные
клетки
Макрофаги
27.
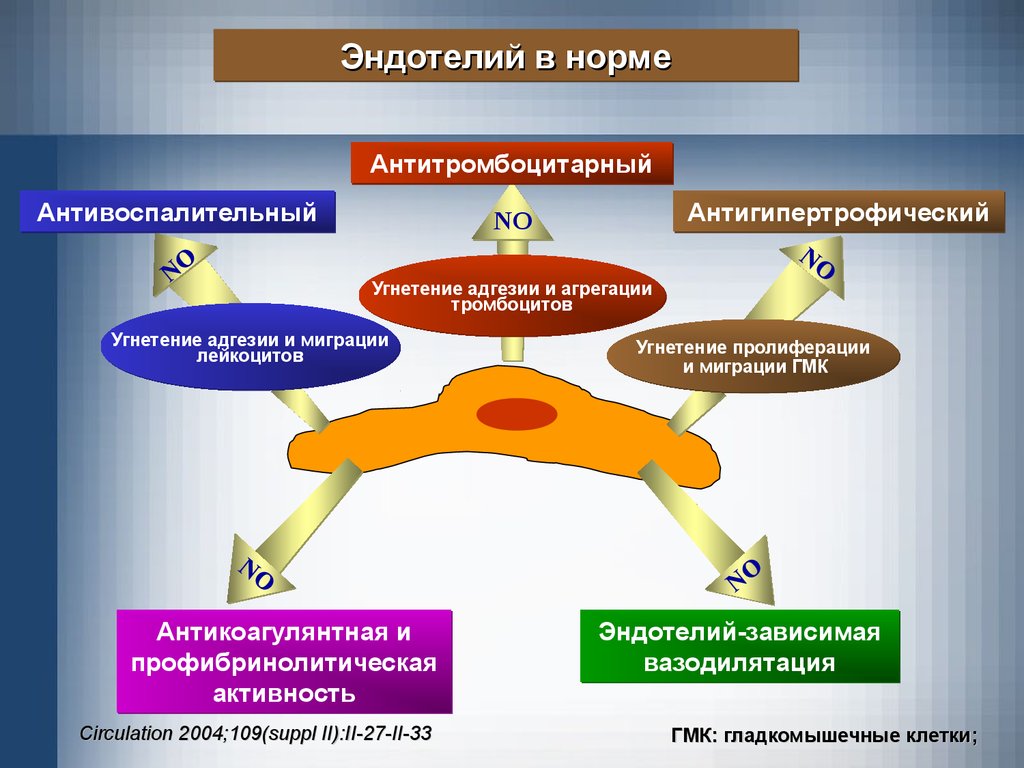
Эндотелий в нормеАнтитромбоцитарный
Антивоспалительный
NO
Антигипертрофический
NO
NO
Угнетение адгезии и агрегации
тромбоцитов
Угнетение адгезии и миграции
лейкоцитов
NO
Антикоагулянтная и
профибринолитическая
активность
Circulation 2004;109(suppl II):II-27-II-33
Угнетение пролиферации
и миграции ГМК
NO
Эндотелий-зависимая
вазодилятация
ГМК: гладкомышечные клетки;
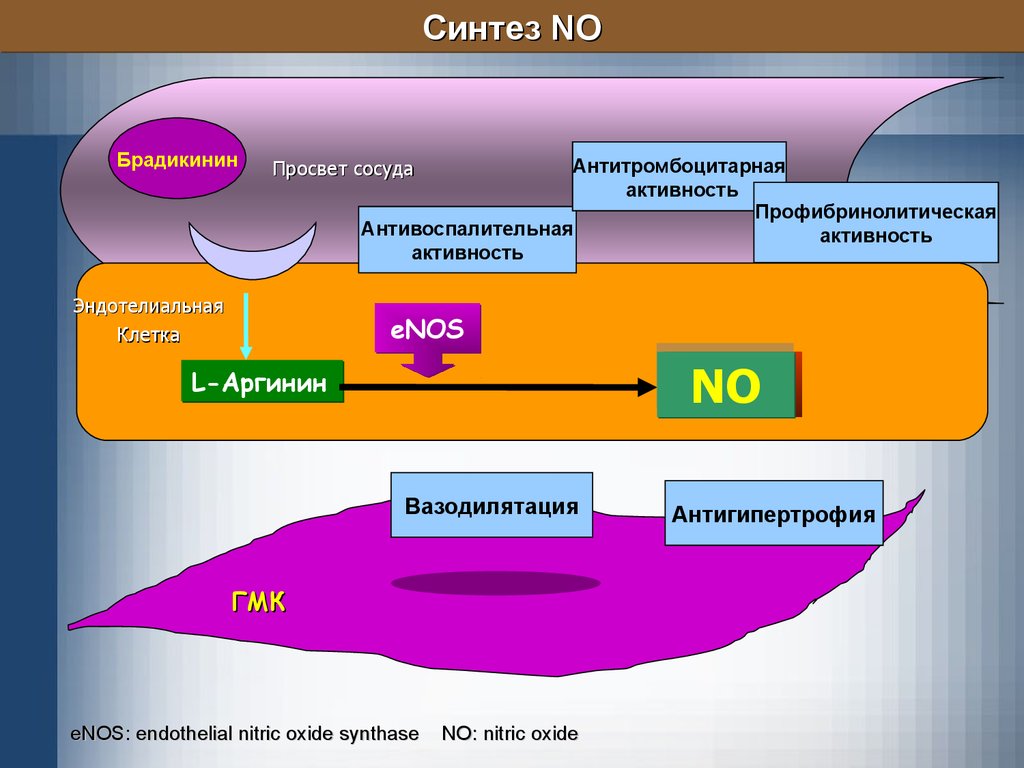
28.
Синтез NOБрадикинин
Антитромбоцитарная
активность
Профибринолитическая
Антивоспалительная
активность
активность
Просвет сосуда
Эндотелиальная
Клетка
eNOS
NO
NO
NO
L-Аргинин
Вазодилятация
ГМК
eNOS: endothelial nitric oxide synthase
NO: nitric oxide
Антигипертрофия
29.
Роль АПФ иангиотензина – II
в развитии
эндотелиальной дисфункции
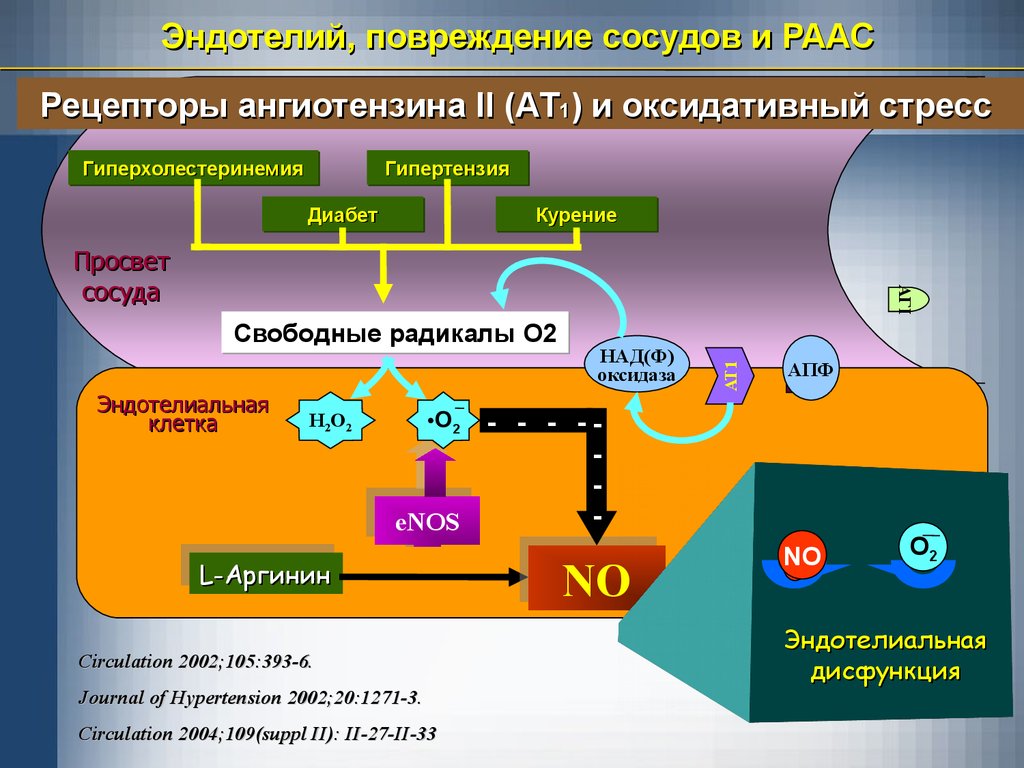
30.
Эндотелий, повреждение сосудов и РААСРецепторы ангиотензина II (АТ1) и оксидативный стресс
Гиперхолестеринемия
Гиперхолестеринемия
Гипертензия
Гипертензия
Диабет
Диабет
Курение
Курение
Эндотелиальная
клетка
•O2
H2O2
eNOS
eNOS
LL-Аргинин
Аргинин
Circulation 2002;105:393-6.
Journal of Hypertension 2002;20:1271-3.
Circulation 2004;109(suppl II): II-27-II-33
НАД(Ф)
оксидаза
AgII
Свободные радикалы О2
AT1
АГI
Просвет
сосуда
АПФ
- - - --
NO
NO
NO
NO
O2
Эндотелиальная
дисфункция
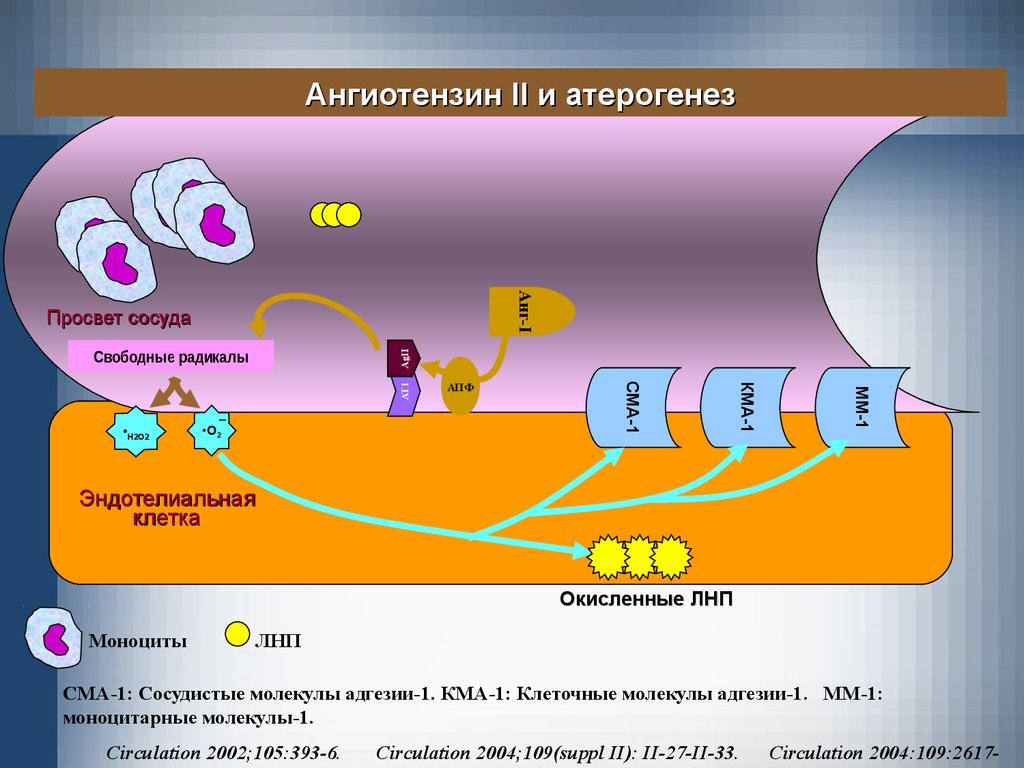
31.
Ангиотензин II и атерогенезАнг-I
Просвет сосуда
ММ-1
•O2
КМА-1
•H2O2
АПФ
СМА-1
AT1
AgII
Свободные радикалы
Эндотелиальная
клетка
Окисленные ЛНП
Моноциты
ЛНП
СМА-1: Сосудистые молекулы адгезии-1. КМА-1: Клеточные молекулы адгезии-1. ММ-1:
моноцитарные молекулы-1.
Circulation 2002;105:393-6.
Circulation 2004;109(suppl II): II-27-II-33.
Circulation 2004:109:2617-
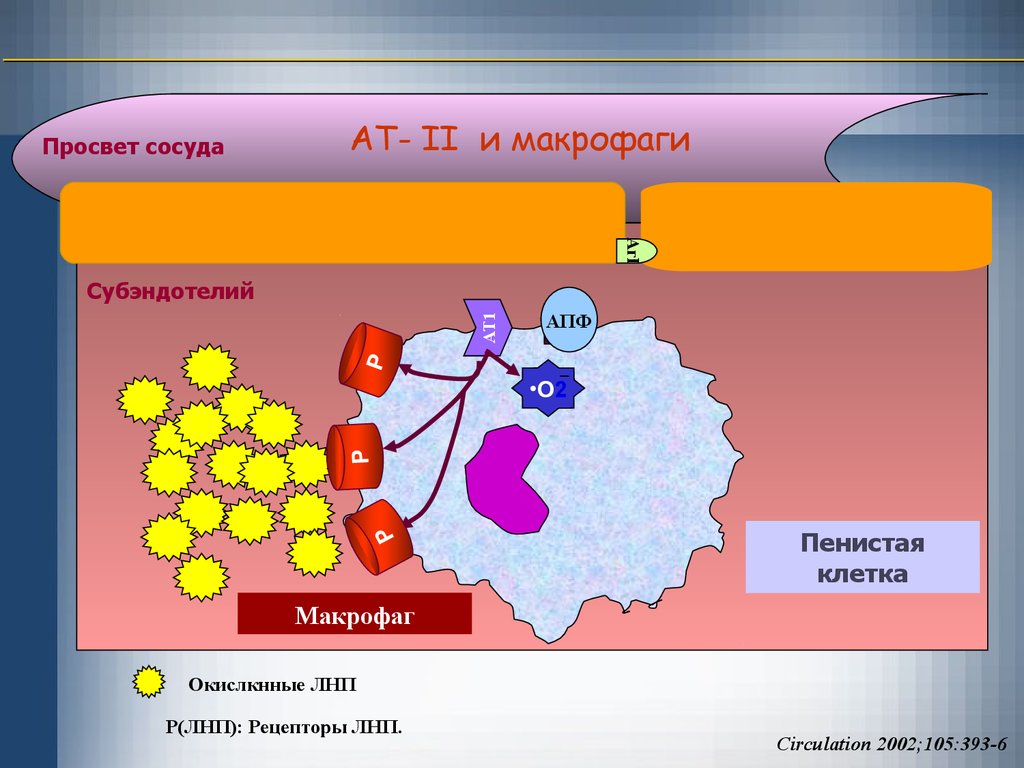
32.
Просвет сосудаАТ- II и макрофаги
АгI
AgII
АПФ
Р
AT1
Субэндотелий
Р
Р
•O2
Пенистая
клетка
Макрофаг
Окислкнные ЛНП
Р(ЛНП): Рецепторы ЛНП.
Circulation 2002;105:393-6
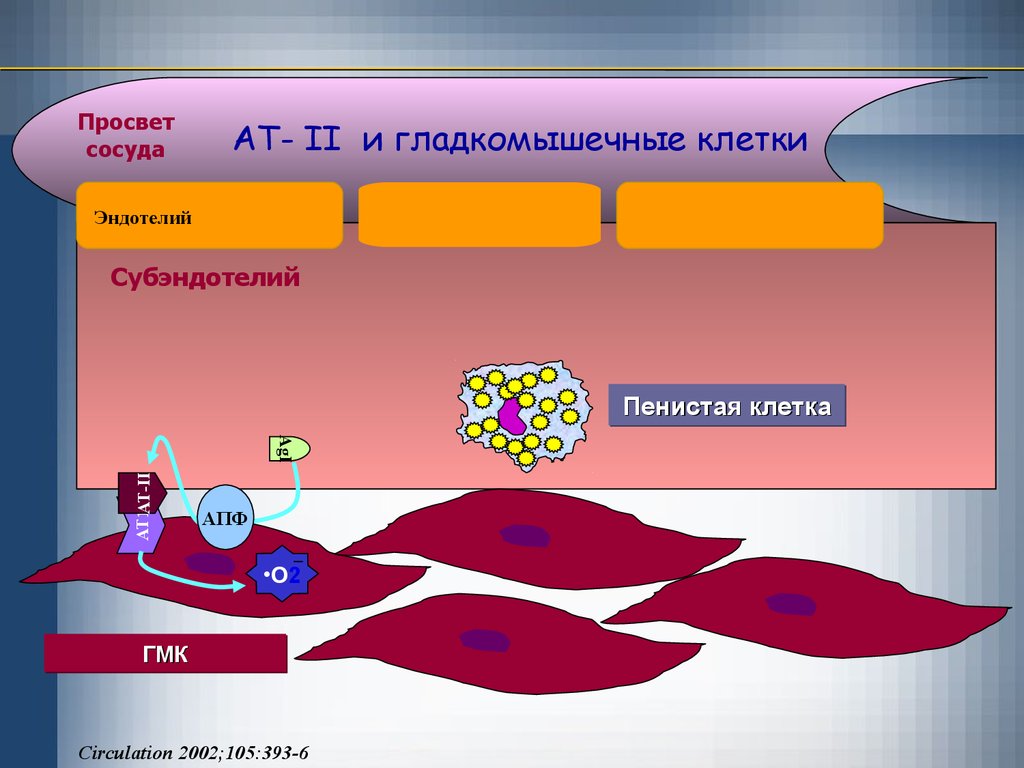
33.
Просветсосуда
АТ- II и гладкомышечные клетки
Эндотелий
Субэндотелий
Пенистая клетка
AT1АТ-II
AgI
АПФ
•O2
ГМК
ГМК
Circulation 2002;105:393-6
34.
PAI-1PAI-1
Просвет
сосуда
AT1AgII
AT1AgII
tPA
tPA
AT1AgII
АТ- II и повреждение атеросклеротической
бляшки
Circulation 2002;105:393-6
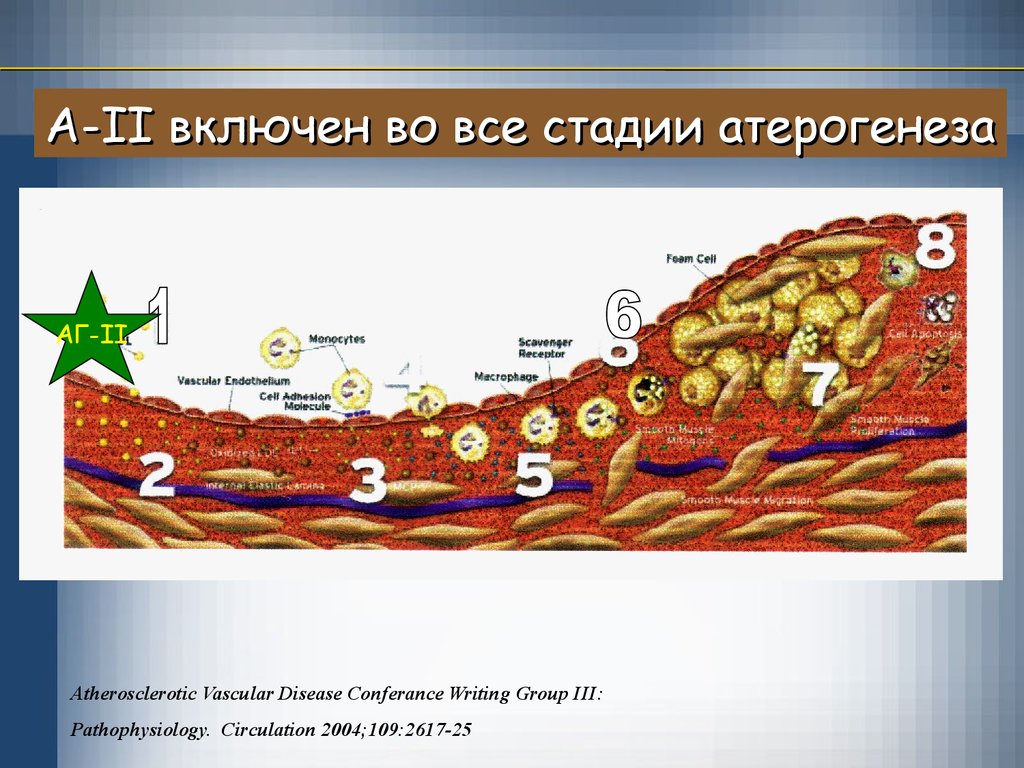
35.
А-II включен во все стадии атерогенезаАГ-II
Atherosclerotic Vascular Disease Conferance Writing Group III:
Pathophysiology. Circulation 2004;109:2617-25
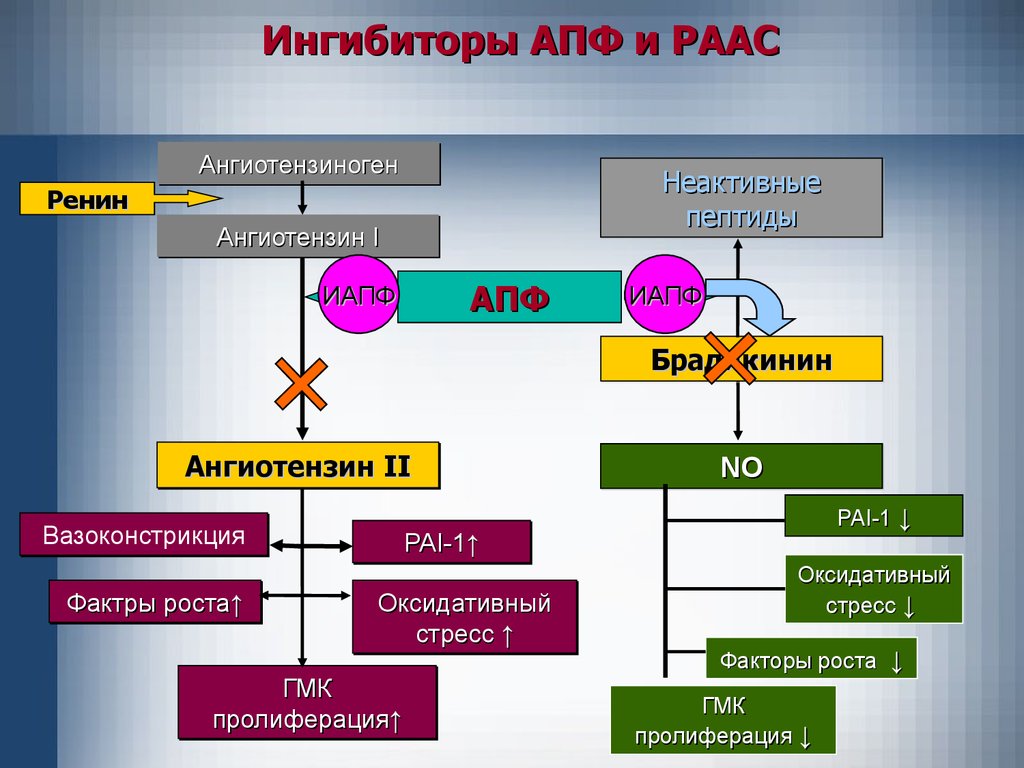
36.
Ингибиторы АПФ и РААСАнгиотензиноген
Неактивные
Неактивные
пептиды
пептиды
Ренин
Ангиотензин
Ангиотензин I
АПФ
ИАПФ
ИАПФ
Брадикинин
Брадикинин
Ангиотензин II
II
Вазоконстрикция
Фактры
Фактры роста
роста↑
NO
PAI-1 ↓
PAI-1↑↑
Оксидативный
Оксидативный
стресс ↑↑
ГМК
ГМК
пролиферация
пролиферация↑↑
Оксидативный
стресс ↓
Факторы роста ↓
ГМК
пролиферация ↓
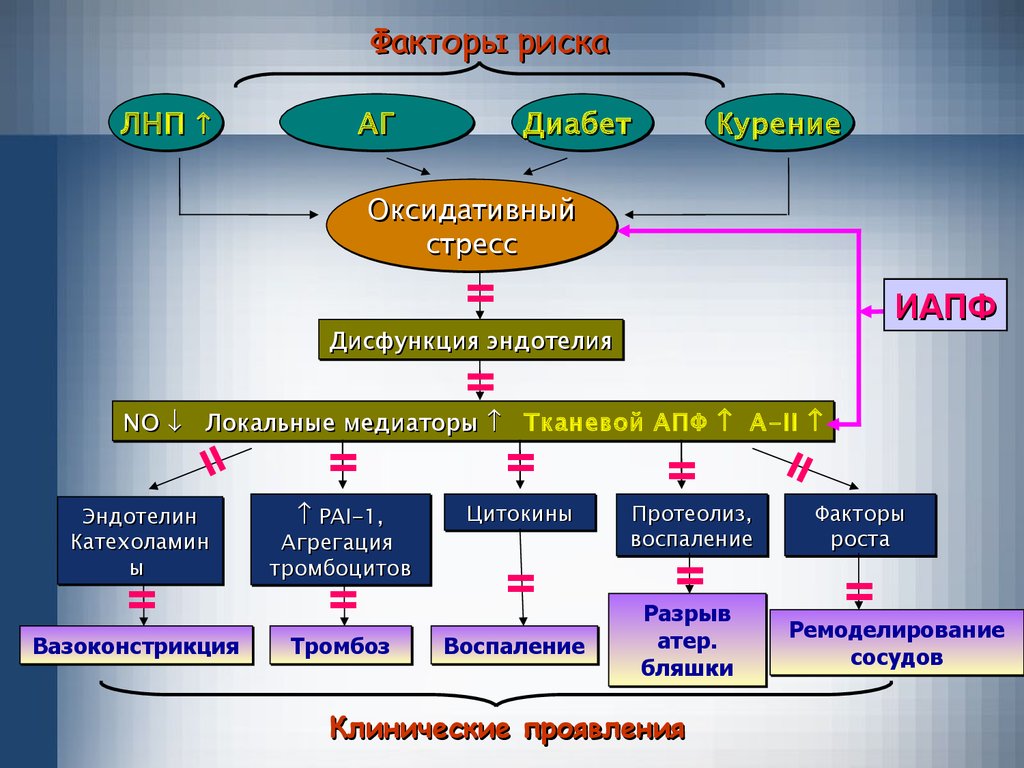
37.
Факторы рискаЛНП
ЛНП
АГ
АГ
Диабет
Диабет
Курение
Курение
Оксидативный
Оксидативный
стресс
стресс
=
ИАПФ
Дисфункция
Дисфункция эндотелия
эндотелия
=
=
Эндотелин
Эндотелин
Катехоламин
Катехоламин
ы
ы
=
Вазоконстрикция
=
=
PAI-1,
PAI-1,
Цитокины
Цитокины
Агрегация
Агрегация
тромбоцитов
тромбоцитов
=
Тромбоз
=
Воспаление
=
Протеолиз,
Протеолиз,
воспаление
воспаление
=
Разрыв
атер.
бляшки
Клинические проявления
=
NO
NO Локальные
Локальные медиаторы
медиаторы Тканевой АПФ А-II
Факторы
Факторы
роста
роста
=
Ремоделирование
сосудов
38.
Сахарный диабет – независимыйфактор сердечно-сосудистого риска
Распространенность СД в мире -2-6% в
популяции (=150.000.000)
Число больных СД удваивается каждые 25
лет
80% пациентов СД умирает от сердечнососудистых причин
СД 2 типа – заболевание сосудов
39.
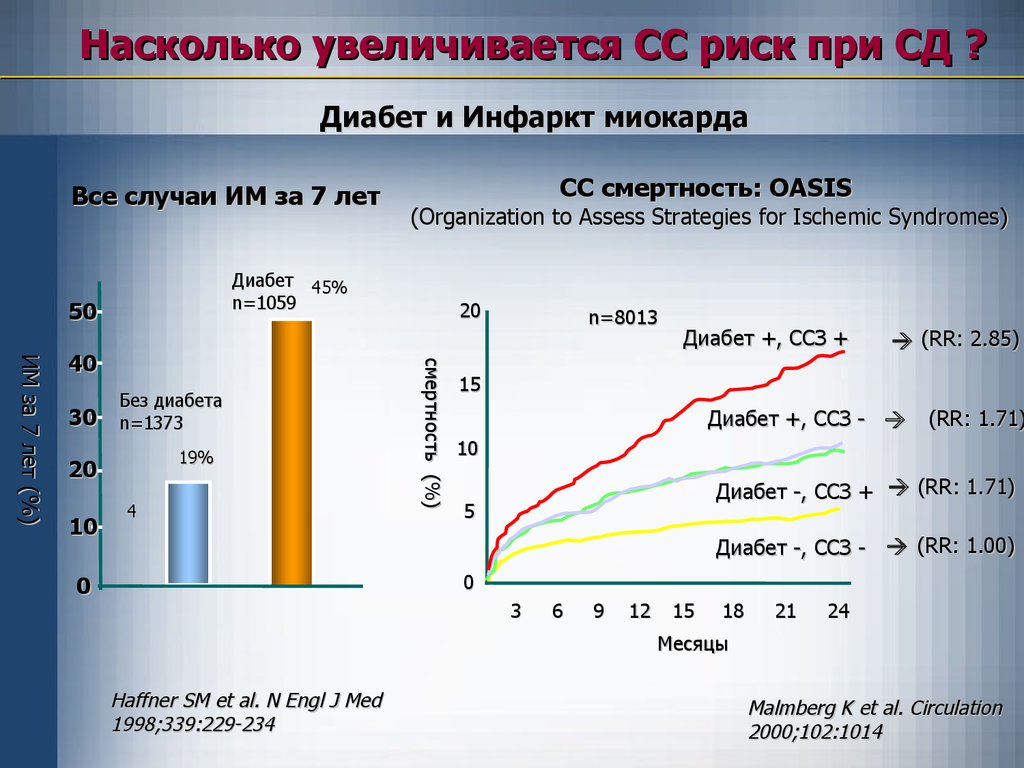
Насколько увеличивается СС риск при СД ?Диабет и Инфаркт миокарда
Все случаи ИМ за 7 лет
Без диабета
n=1373
19%
20
4
20
смертность (%)
ИМ за 7 лет (%)
40
10
(Organization to Assess Strategies for Ischemic Syndromes)
Диабет 45%
n=1059
50
30
СС смертность: OASIS
n=8013
Диабет +, ССЗ +
(RR: 2.85)
15
Диабет +, ССЗ - (RR: 1.71)
10
Диабет -, ССЗ + (RR: 1.71)
5
Диабет -, ССЗ - (RR: 1.00)
0
0
3
6
9
12
15
18
21
24
Месяцы
Haffner SM et al. N Engl J Med
1998;339:229-234
Malmberg K et al. Circulation
2000;102:1014
40.
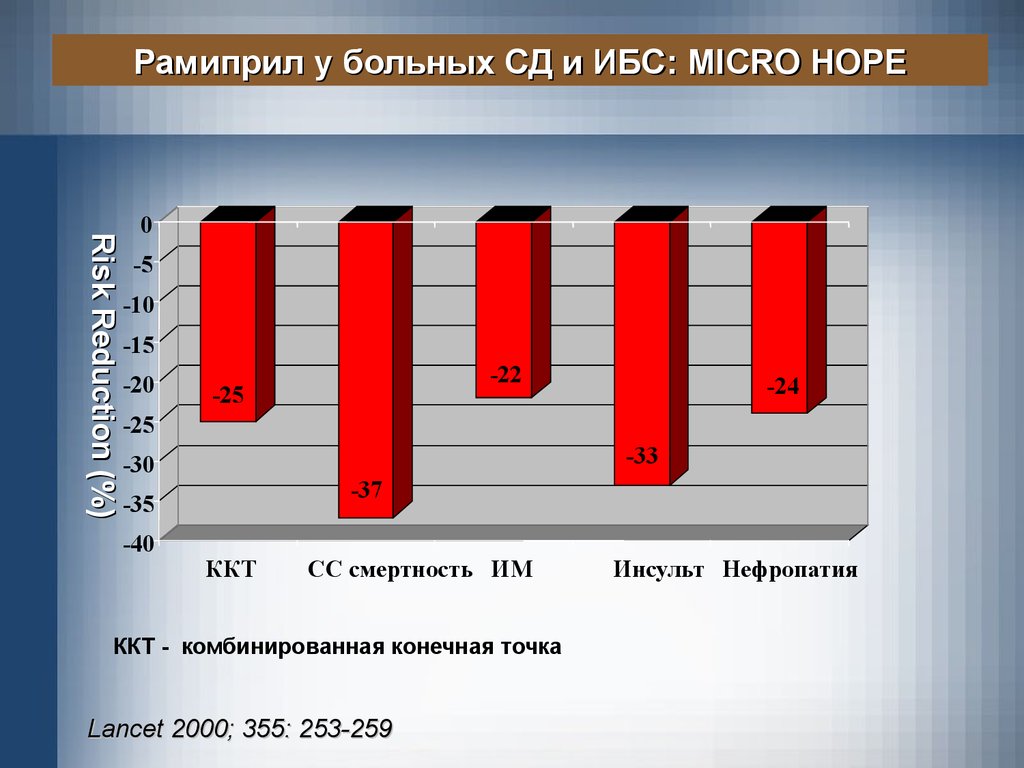
Рамиприл у больных СД и ИБС: MICRO HOPERisk Reduction (%)
0
-5
-10
-15
-20
-22
-25
-24
-25
-33
-30
-37
-35
-40
ККТ
СС смертность ИМ
ККТ - комбинированная конечная точка
Lancet 2000; 355: 253-259
Инсульт Нефропатия
41.
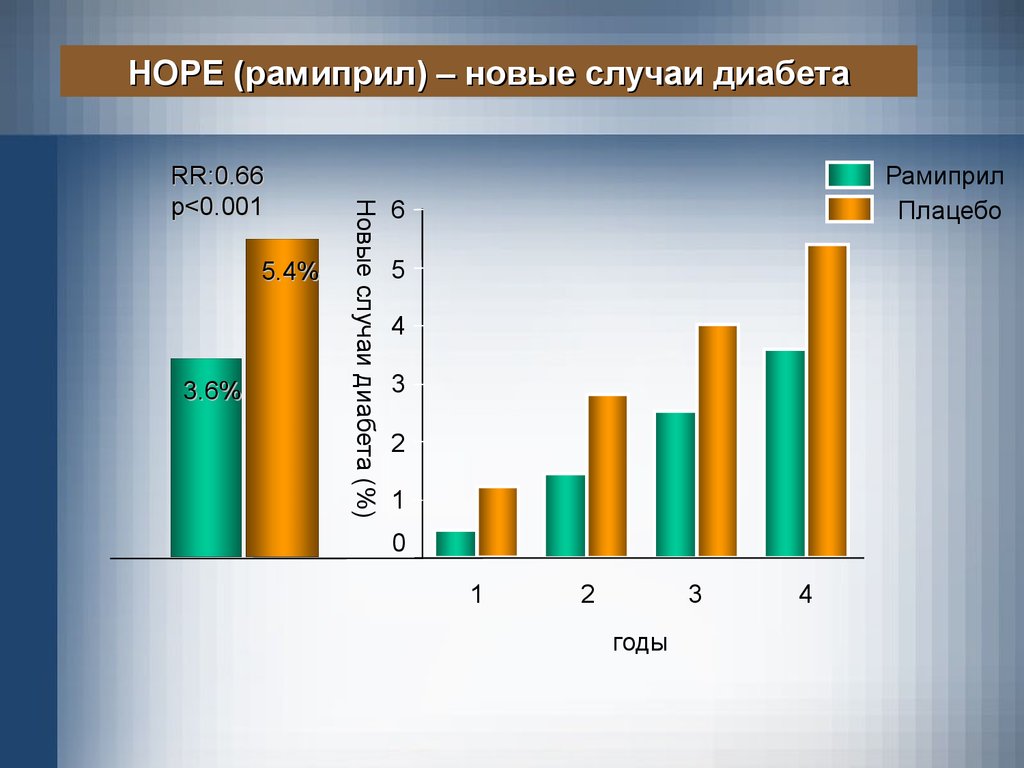
HOPE (рамиприл) – новые случаи диабета5.4%
3.6%
Новые случаи диабета (%)
RR:0.66
p<0.001
Рамиприл
Плацебо
6
5
4
3
2
1
0
1
2
3
годы
4
42.
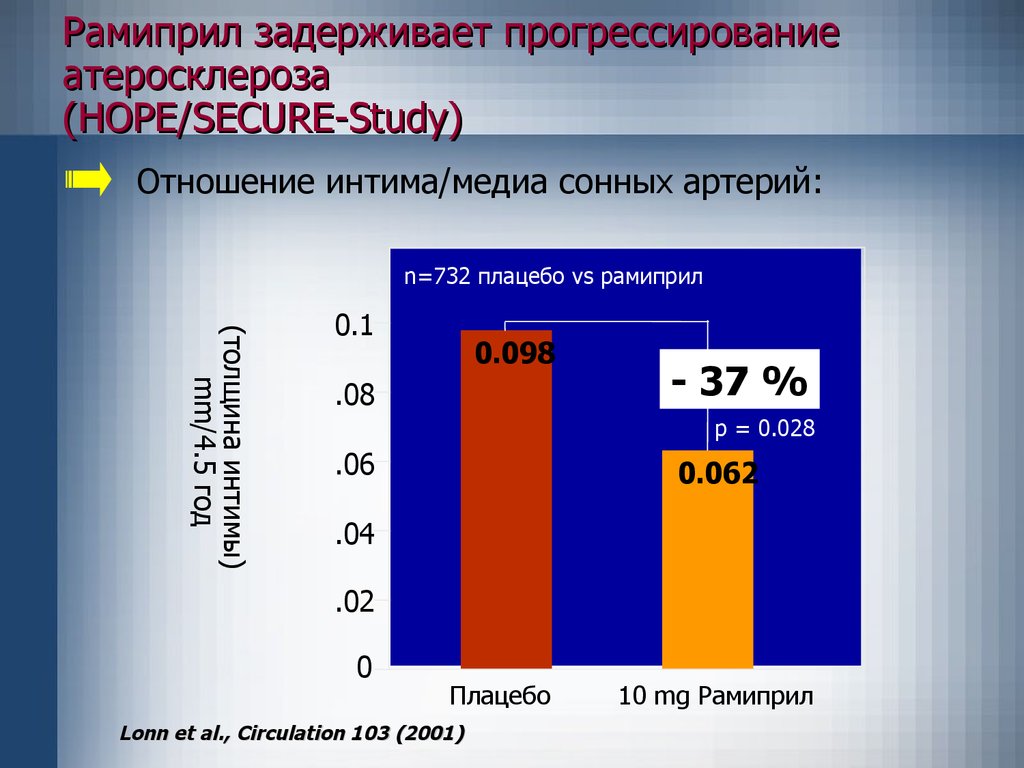
Рамиприл задерживает прогрессированиеатеросклероза
(HOPE/SECURE-Study)
Отношение интима/медиа сонных артерий:
n=732 плацебо vs рамиприл
(толщина интимы)
mm/4.5 год
0.1
0.098
.08
- 37 %
p = 0.028
.06
0.062
.04
.02
0
Плацебо
Lonn et al., Circulation 103 (2001)
10 mg Рамиприл
43.
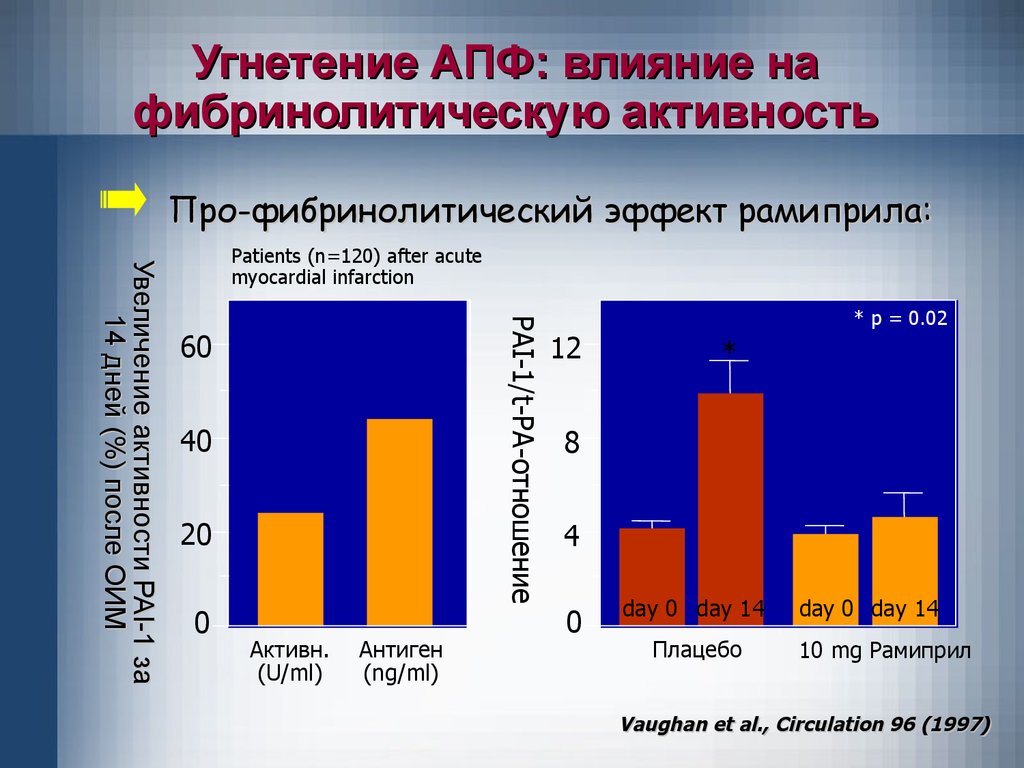
Угнетение АПФ: влияние нафибринолитическую активность
Про-фибринолитический эффект рамиприла:
PAI-1/t-PA-отношение
Увеличение активности PAI-1 за
14 дней (%) после ОИМ
Patients (n=120) after acute
myocardial infarction
60
40
20
0
Активн.
(U/ml)
Антиген
(ng/ml)
* p = 0.02
12
*
8
4
0
day 0 day 14
Плацебо
day 0 day 14
10 mg Рамиприл
Vaughan et al., Circulation 96 (1997)
44.
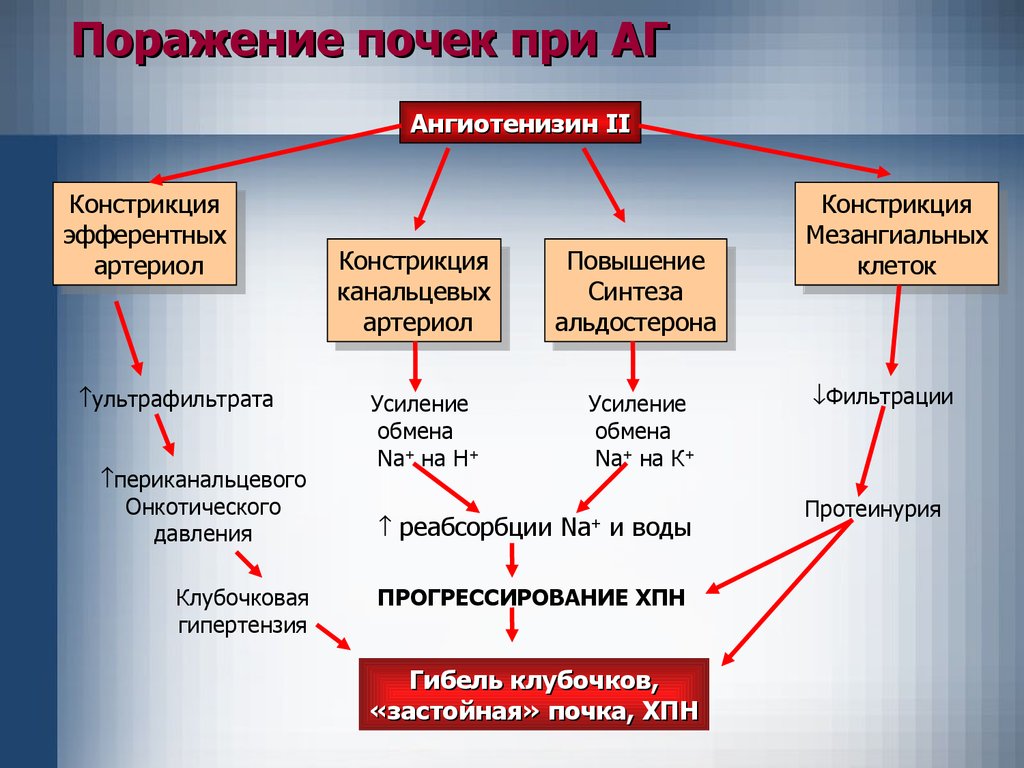
Поражение почек при АГАнгиотенизин II
Констрикция
Констрикция
эфферентных
эфферентных
артериол
артериол
ультрафильтрата
периканальцевого
Онкотического
давления
Клубочковая
гипертензия
Констрикция
Констрикция
канальцевых
канальцевых
артериол
артериол
Повышение
Повышение
Синтеза
Синтеза
альдостерона
альдостерона
Усиление
обмена
Na+ на Н+
Усиление
обмена
Na+ на К+
реабсорбции Na и воды
+
ПРОГРЕССИРОВАНИЕ ХПН
Гибель клубочков,
«застойная» почка, ХПН
Констрикция
Констрикция
Мезангиальных
Мезангиальных
клеток
клеток
Фильтрации
Протеинурия
45.
Поражение почек при АГРазвитие почечной патологии при АГ
зависит от активности тканевой РААС
Ангиотензин II действует как фактор
роста:
Пролиферация мезангиальных,
канальцевых, интерстициальных клеток
почек, повышение синтеза коллагена с
исходом в нефросклероз
46.
MICRO-HOPEEvents per patient group (%)
18
16
14
RR=17%
P=0.03
RR=24%
P=0.004
Placebo
Ramipril
NS
12
RR=24%
P=0.03
10
8
6
NS
4
2
0
Total
mortality
Revascularization
RR=Relative risk reduction
Overt
nephropathy*
NS 0.05
HOPE Study Investigators. Lancet. 2000;355:253-259.
Heart
failure†
Unstable
angina†
47.
Являются ли все эти эффектыклассовыми эффектами ИАПФ
48.
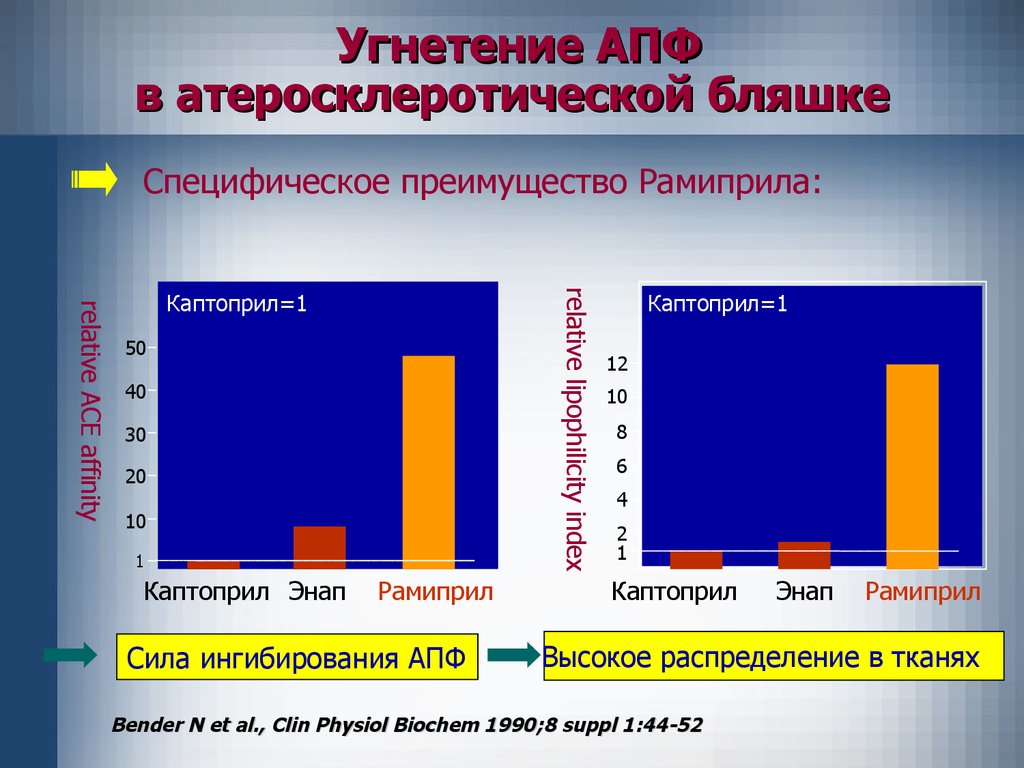
Угнетение АПФв атеросклеротической бляшке
Специфическое преимущество Рамиприла:
relative lipophilicity index
relative ACE affinity
Каптоприл=1
50
40
30
20
10
1
Каптоприл Энап
Рамиприл
Сила ингибирования АПФ
Каптоприл=1
12
10
8
6
4
2
1
Каптоприл
Энап
Рамиприл
Высокое распределение в тканях
Bender N et al., Clin Physiol Biochem 1990;8 suppl 1:44-52
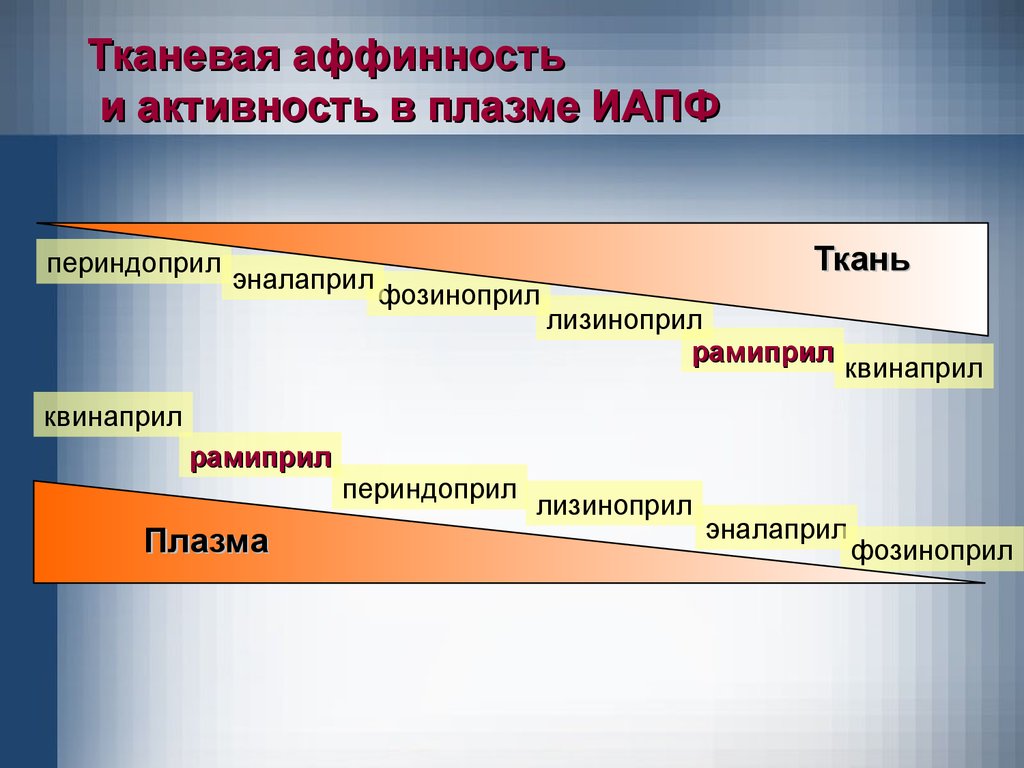
49.
Тканевая аффинностьи активность в плазме ИАПФ
периндоприл
эналаприл
Ткань
фозиноприл
лизиноприл
рамиприл
квинаприл
квинаприл
рамиприл
Плазма
периндоприл
лизиноприл
эналаприл
фозиноприл
50.
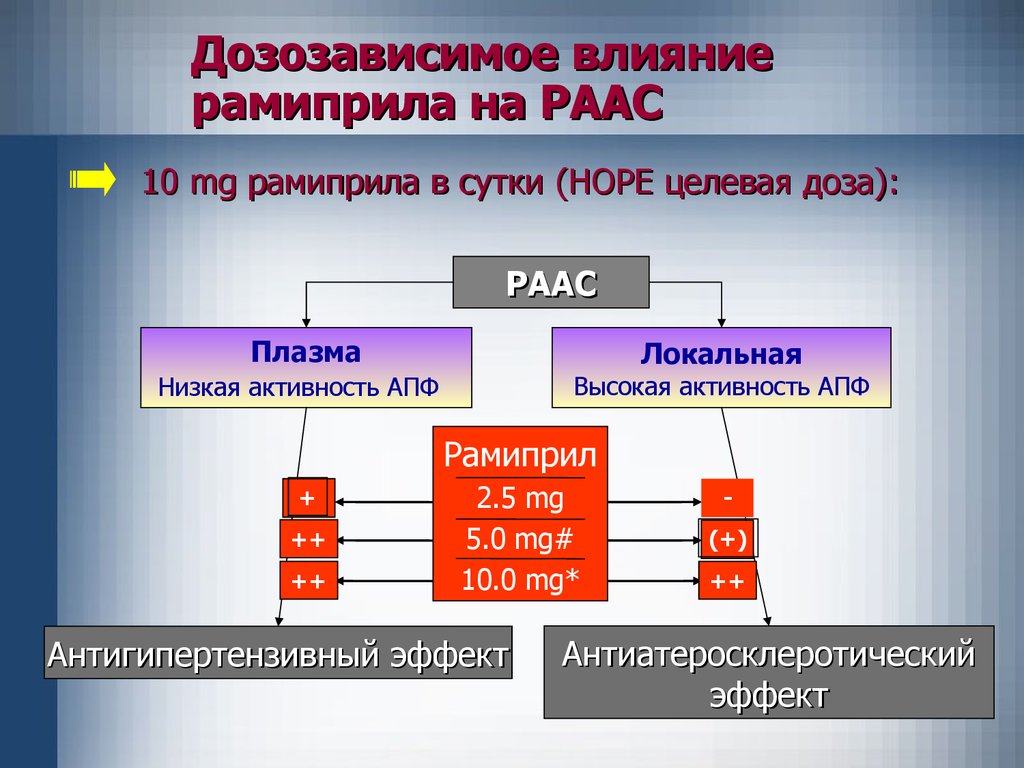
Дозозависимое влияниерамиприла на РААС
10 mg рамиприла в сутки (HOPE целевая доза):
РААС
Плазма
Локальная
Высокая активность АПФ
Низкая активность АПФ
Рамиприл
+
++
++
2.5 mg
5.0 mg#
10.0 mg*
Антигипертензивный эффект
(+)
++
Антиатеросклеротический
эффект
51.
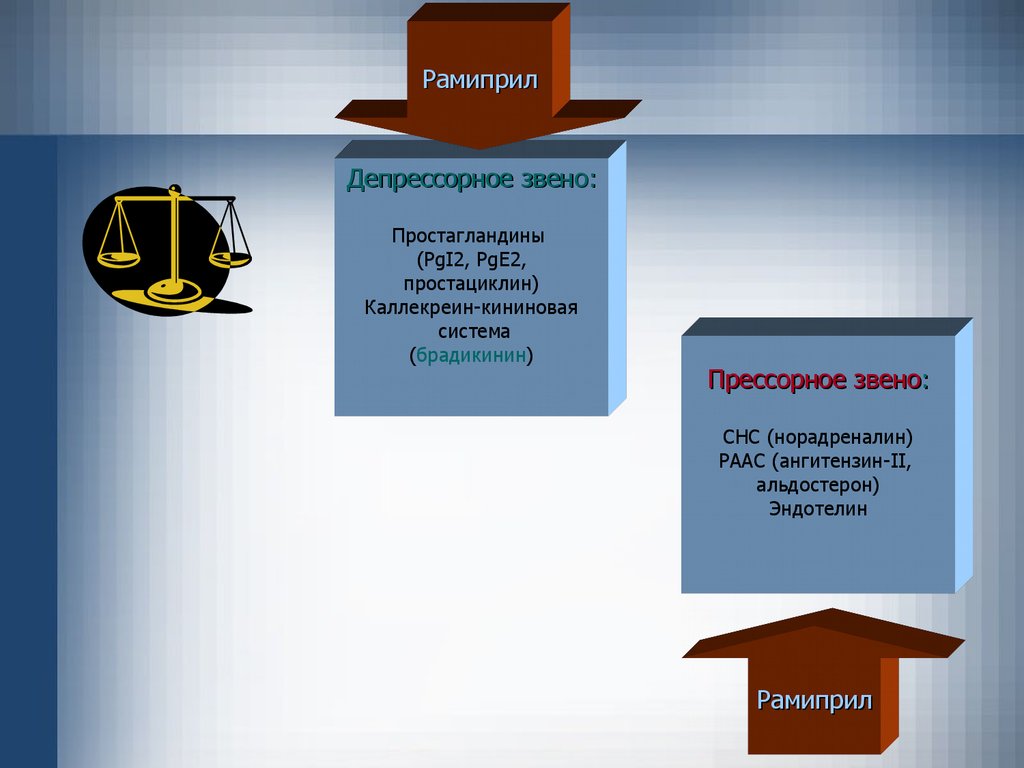
РамиприлДепрессорное звено:
Простагландины
(PgI2, PgE2,
простациклин)
Каллекреин-кининовая
система
(брадикинин)
Прессорное звено:
СНС (норадреналин)
РААС (ангитензин-II,
альдостерон)
Эндотелин
Рамиприл





















 Медицина
Медицина








