Похожие презентации:
Атомная физика. Строение атома
1.
Лекция 276. Атомная физика
6.1. Строение атома
Строение атома. Опыт Резерфорда. Планетарная
модель атома. Закономерности атомных спектров.
Постулаты Бора. Квантование орбит. Теория атома
водорода. Опыт Франка и Герца. Волновые свойства
вещества. Гипотеза де Бройля. Опыты Дэвиссона и
Джермера, Томсона-Тартаковского, Фабриканта.
Принцип неопределенности. Волновая функция,
ее статистический смысл. Уравнение Шредингера.
2.
Модель атома Томсона (1903)Первую модель атома (Plum pudding model) предложил
Дж. Дж. Томсон после открытия им же электрона (1897).
Атом имеет форму шара радиусом 10–10 м, причем
положительный заряд распределен равномерно по
всему объему, а отрицательно заряженные электроны
находятся внутри него, так что их суммарный
Сэр Джозеф
отрицательный заряд равен положительному заряду
Джон Томсон
1856-1940
шара, и в целом атом электрически нейтрален. При
Ноб. лаур.
отклонении электрона от положения равновесия
1906
возникают силы по закону Кулона, стремящиеся
возвратить его в исходное положение, что порождает
колебания электронов и обуславливает
излучение атомов.
3.
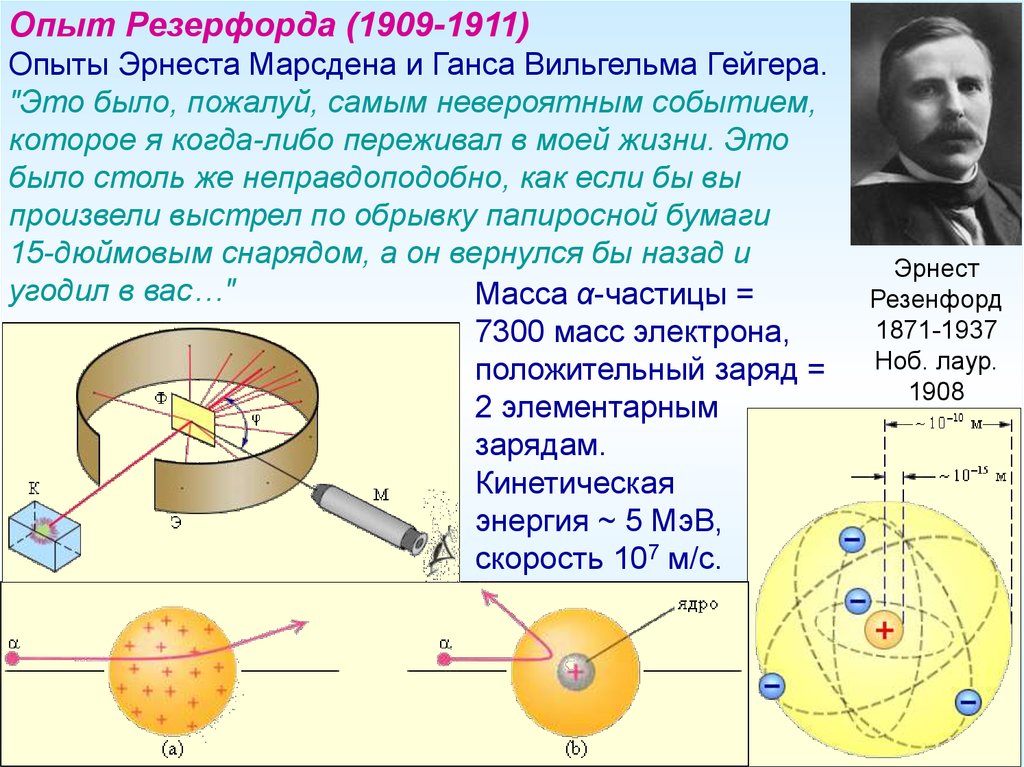
Опыт Резерфорда (1909-1911)Опыты Эрнеста Марсдена и Ганса Вильгельма Гейгера.
"Это было, пожалуй, самым невероятным событием,
которое я когда-либо переживал в моей жизни. Это
было столь же неправдоподобно, как если бы вы
произвели выстрел по обрывку папиросной бумаги
15-дюймовым снарядом, а он вернулся бы назад и
угодил в вас…"
Масса α-частицы =
7300 масс электрона,
положительный заряд =
2 элементарным
зарядам.
Кинетическая
энергия ~ 5 МэВ,
скорость 107 м/с.
Эрнест
Резенфорд
1871-1937
Ноб. лаур.
1908
4.
5.
Модель атома Резерфорда (1911)Планетарная (ядерная) модель атома – положительный
заряд не распределен равномерно по всему объему, а
весь сосредоточен в чрезвычайно малом объеме (ядре),
вокруг которого по замкнутым орбитам вращаются
электроны, причем их суммарный заряд равен заряду
ядра, так что атом в целом электрически нейтрален.
Эрнест
Радиус самой дальней орбиты равен размеру атома.
Резенфорд
Противоречия модели Резерфорда
1) Электрон, двигающийся по круговой орбите,
обладает центростремительным ускорением,
поэтому согласно теории Максвелла должен
непрерывно излучать электромагнитные волны,
т.е. терять энергию, в результате чего за время
~10–8 сек упасть на ядро.
2) Частота излучаемого электроном света должна
быть равна частоте колебаний электрона – числу
оборотов в 1 сек. Если по мере приближения к
ядру частота непрерывно меняется, то спектр
излучаемого света должен быть сплошным.
1871-1937
Ноб. лаур.
1908
6.
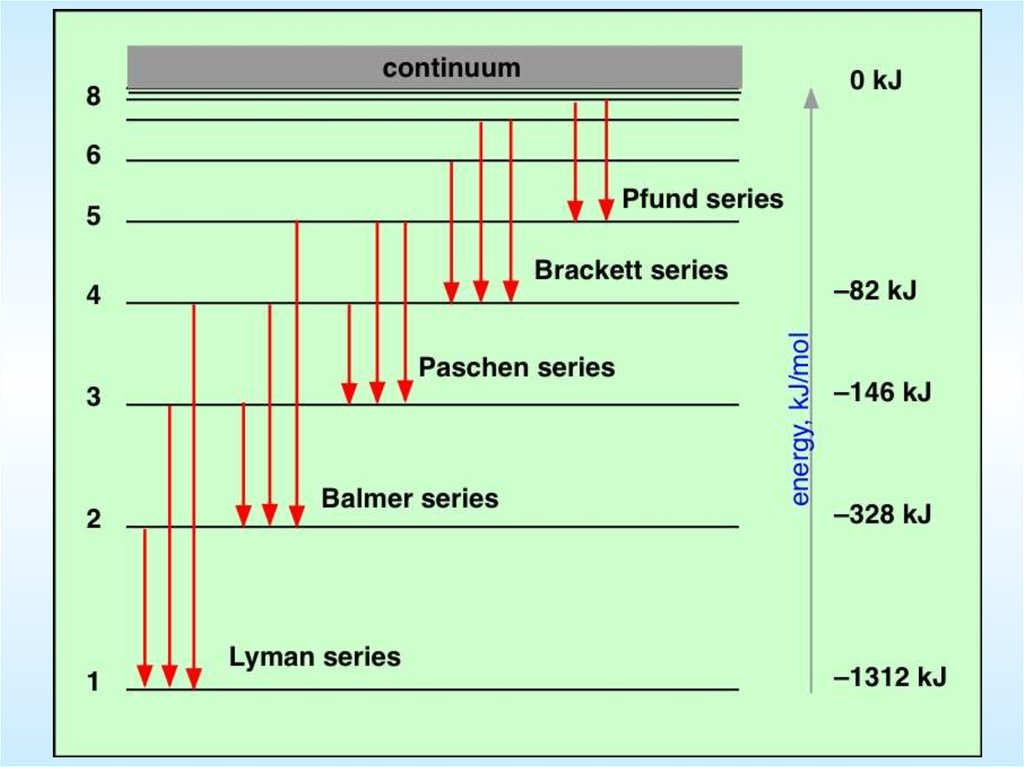
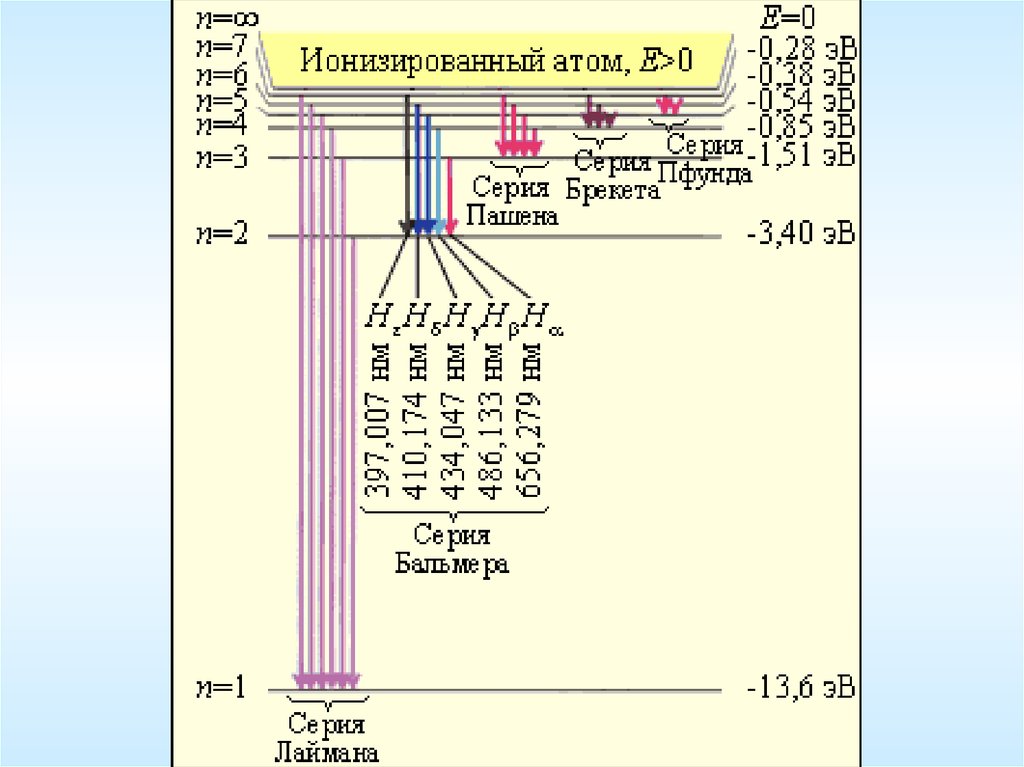
Спектр атома водорода1) Серия Лаймана (Теодор Лайман, 1906) — УФ
2) Серия Бальмера (Иоганн Якоб Бальмер, 1885)
3) Серия Пашена (Фридрих Пашен, 1908)
4) Серия Брэккета (Фредерик Брэккет, 1922)
— ИК
5) Серия Пфунда (Август Пфунд, 1924)
6) Серия Хемпфри (Кёртис Хемпфри, 1953)
Йозеф
Фраунгофер
1787-1826
Иоганн Якоб
Бальмер
1825-1898
7.
Формула Бальмера (1885)1 1
R 2 2
2 n
1
n 3, 4, 5,
Обобщенная формула Бальмера (Ридберг 1890)
1
1
R 2 2
m n
1
Йоханнес
Роберт
Ридберг
1854-1919
1
1
Rс 2 2
n
m
R = 109 737,309 см–1 – постоянная Ридберга.
Спектральные серии атома водорода
1) Серия Лаймана
m 1 n 2, 3, 4,
m 2 n 3, 4, 5,
2) Серия Бальмера
m 3 n 4, 5, 6,
3) Серия Пашена
4) Серия Брэккета
m 4 n 5, 6, 7,
m 5 n 6, 7, 8,
5) Серия Пфунда
6) Серия Хемпфри
m 6 n 7, 8, 9,
При n
1
0
2
n
1
R
1
m2
– граница серии
8.
Постулаты Бора (1913)Построена для атома водорода или водородо-подобных
ионов (с зарядом +Ze и одним только электроном).
1) Первый постулат (правило квантования орбит):
Электрон может вращаться вокруг ядра не по любой
орбите, а только по такой, на которой момент
количества движения (импульса) равен целому кратному Нильс Хенрик
некоторой величины (постоянной Планка).
Давид Бор
h
Ln me v n rn n
nh
2
h
h
2
1885-1962
Ноб. лаур.
1922
h = 1,054 10–34 Дж сек – рационализированная постоянная Планка.
2) Второй постулат (правило стационарных состояний):
Электрон, вращающийся по любой из разрешенных орбит, энергии
не излучает (атом находится в стационарном состоянии).
3) Третий постулат (правило частот):
При переходе электрона из одного стационарного состояния в
другое (с одной разрешенной орбиты на другую) испускается или
поглощается один фотон , энергия которого равна
h nm Wn Wm
разности энергий этих двух стационарных уровней.
9.
Боровская теория водородо-подобного атомаНа электрон со стороны ядра действует притягивающая сила
Кулона, которая создает центростремительное ускорение.
me v 2n
1 Ze 2
rn
4 0 rn2
h
Ln me v n rn n
2
0h2 2
2
rn
n
r
n
1
2
m
Ze
e
Для водорода
Z=1
me n 2 h 2
1 Ze 2
2 2 2
4 me rn rn 4 0 rn2
0h2
r1
0,0528 нм
2
me e
Полная энергия электрона в атоме складывается из кинетической
энергии и потенциальной энергии в электростатическом поле ядра.
me v 2n
Ze 2
Ze 2
Ze 2
Ze 2
Wn
2
8 0 rn
4 0 rn 8 0 rn 4 0 rn
me Z 2e 4 1
Ze 2 me Ze 2 1
1
W1 2
Wn
2
2
2 2 2
8 0 0 h n
n
8 0 h n
Целое число n, определяющее энергетические уровни атома,
называется главным квантовым числом.
10.
me Z 2e 4 1Ze 2 me Ze 2 1
1
W1 2
Wn
2
2
2 2 2
8 0 0 h n
n
8 0 h n
Энергетическое состояние (уровень) с n = 1 является основным
(нормальным) состоянием, все остальные уровни с n > 1 являются
возбужденными. Для атома водорода (Z = 1)
me e 4
Ze 2 me Ze 2 1
W1
2 2 13,55 эВ
2
2
8 0 0 h n
8 0 h
Отрицательное значение энергии электрона в атоме показывает,
что он находится в связанном состоянии, т.е. принадлежит данному
атому. Энергия атома с водорода увеличением n возрастает, а
энергетические уровни сближаются. В пределе при n
энергия атома стремится к нулю:
lim Wn 0
n
Нулевая энергия атома соответствует его ионизации, т.е. отрыву от
него электрона. Таким образом, энергия ионизации атома водорода
(которую нужно сообщить ему для высвобождения электрона):
Wi W1 13,55 эВ
11.
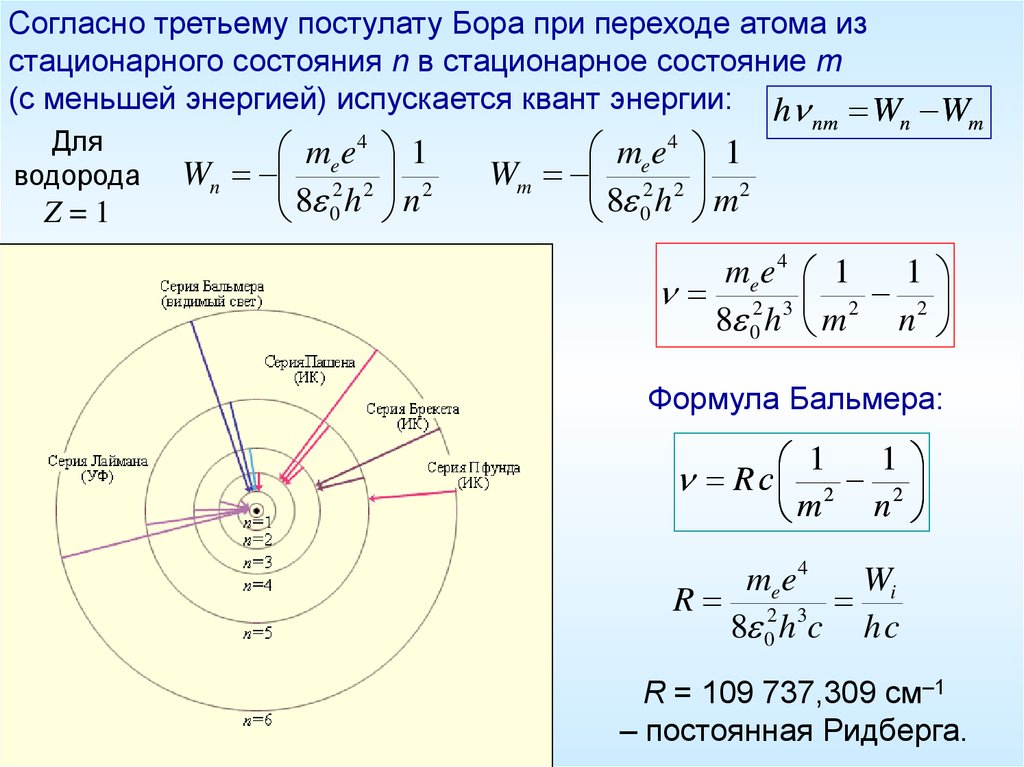
Согласно третьему постулату Бора при переходе атома изстационарного состояния n в стационарное состояние m
(c меньшей энергией) испускается квант энергии: h W W
nm
n
m
Для
водорода
Z=1
me e 4 1
Wn 2 2 2
8 0 h n
me e 4 1
Wm 2 2 2
8 0 h m
me e 4 1
1
2 3 2 2
8 0 h m n
Формула Бальмера:
1
1
Rс 2 2
n
m
me e 4
Wi
R 2 3
8 0 h c h c
R = 109 737,309 см–1
– постоянная Ридберга.
12.
13.
14.
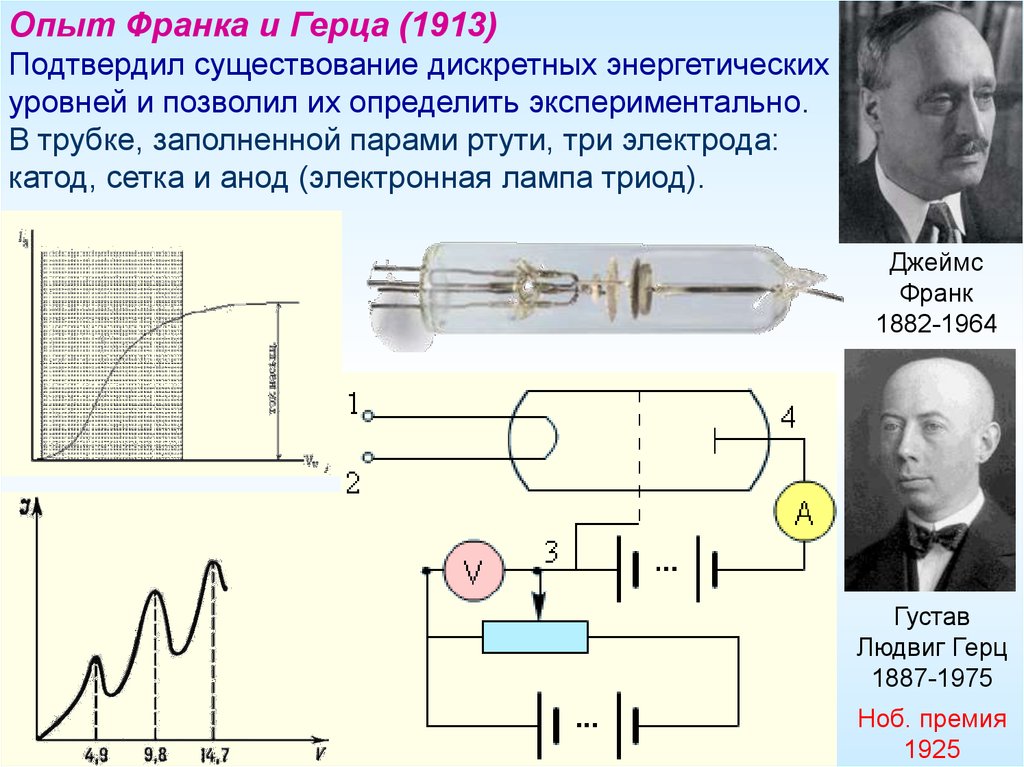
Опыт Франка и Герца (1913)Подтвердил существование дискретных энергетических
уровней и позволил их определить экспериментально.
В трубке, заполненной парами ртути, три электрода:
катод, сетка и анод (электронная лампа триод).
Джеймс
Франк
1882-1964
Густав
Людвиг Герц
1887-1975
Ноб. премия
1925
15.
Прохождение электронов через одну и две щелиПоток электронов, разогнанный до определенной скорости в
электрическом поле, проходит сквозь щель, за которой помещена
фотопленка, позволяющая по степени ее почернения судить о
распределении электронов в пространстве.
16.
Гипотеза Луи де Бройля (1924)Движение частицы можно представить как волновой
процесс с длиной волны де Бройля:
W h
p h / c h /
h
h
p me v
При обычных скоростях λ лежит в пределах 0,1-10 А,
Луис Виктор
т.е. в том же диапазоне, что и рентгеновские лучи.
Пьер Раймон,
Де Бройль предложил, что каждая орбита в атоме
7-й герцог
водорода соответствует волне, распространяющейся
де Бройли
по окружности около ядра атома. Стационарная орбита 1892-1987
Ноб. лаур.
возникает в том случае, когда волна непрерывно
1929
повторяет себя после каждого оборота вокруг
ядра (возникает круговая стоячая волна).
Возможны только такие орбиты, на которых
укладывается целое число волн де Бройля.
2 rn n n
h
me v n
h
Ln me v n rn n
2
– получили правило квантования орбит Бора.
17.
Опыт Дэвиссона и Джермера (1927)Пучок электронов, отражающийся от кристалла никеля,
(естественной дифракционной решетки), дал
отчетливую дифракционную картину, подобную
наблюдаемой для рентгеновского излучения.
По положению дифракционных максимумов была
определена длина волны электронного пучка,
Клинтон Джозеф
совпавшая с рассчитанной по формуле де Бройля.
Дэвиссон
1881-1958
Ноб. лаур. 1937
Лестер
Хэлберт
Джермер
1896-1971
18.
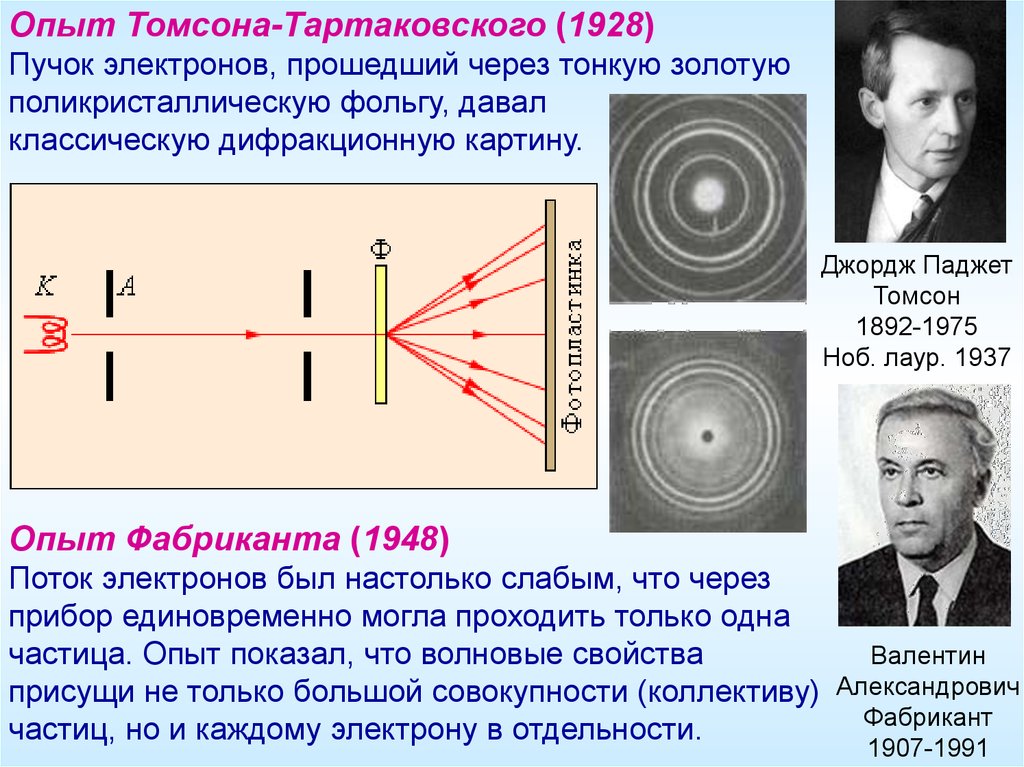
Опыт Томсона-Тартаковского (1928)Пучок электронов, прошедший через тонкую золотую
поликристаллическую фольгу, давал
классическую дифракционную картину.
Джордж Паджет
Томсон
1892-1975
Ноб. лаур. 1937
Опыт Фабриканта (1948)
Поток электронов был настолько слабым, что через
прибор единовременно могла проходить только одна
частица. Опыт показал, что волновые свойства
Валентин
присущи не только большой совокупности (коллективу) Александрович
Фабрикант
частиц, но и каждому электрону в отдельности.
1907-1991
19.
Принцип неопределенности Гейзенберга (1913)Микрочастица не может иметь одновременно и
определенную координату (х, у, z), и определенную
соответствующую проекцию импульса (рх, ру, pz), причем
неопределенности этих величин удовлетворяют
условиям: p x h
p y h
p z h
y
x
z
0
x
x 0
p h / c
p h/
До прохождения щели: x px 0
x 0
После прохождения щели:
px p sin
p x p sin p
k 1
x
sin
x
px x p h
Вернер Карл
Гейзенберг
1901-1976
Ноб. лаур.
1932
20.
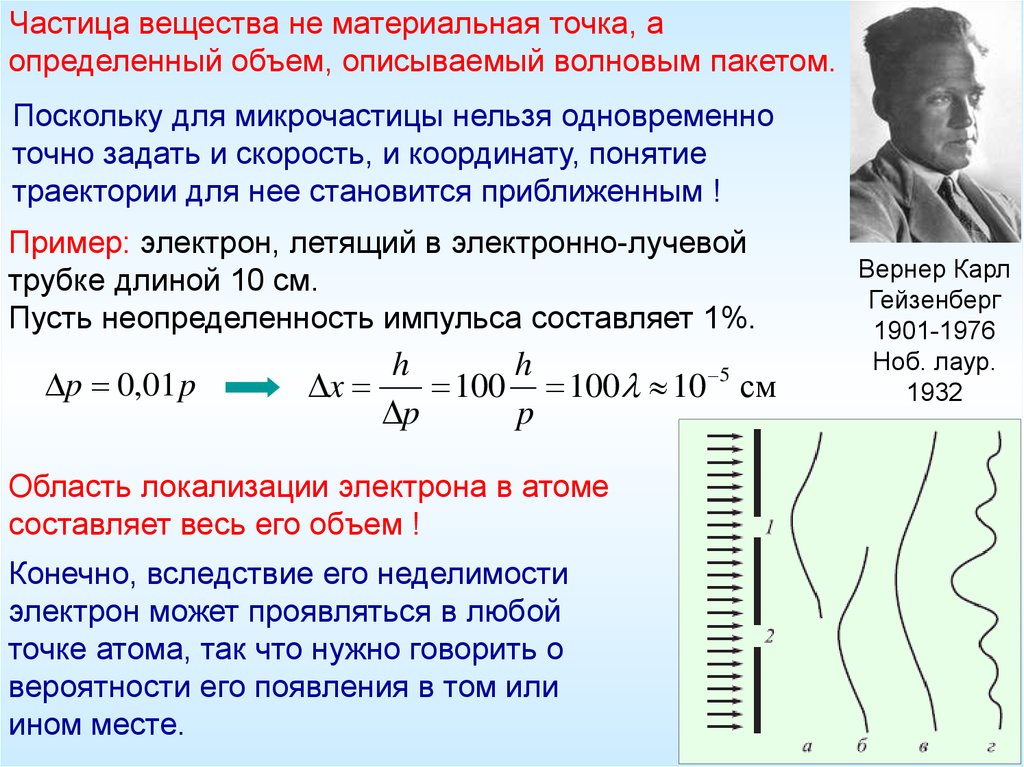
Частица вещества не материальная точка, аопределенный объем, описываемый волновым пакетом.
Поскольку для микрочастицы нельзя одновременно
точно задать и скорость, и координату, понятие
траектории для нее становится приближенным !
Пример: электрон, летящий в электронно-лучевой
трубке длиной 10 см.
Пусть неопределенность импульса составляет 1%.
p 0,01 p
x
h
h
100 100 10 – 5 см
p
p
Область локализации электрона в атоме
составляет весь его объем !
Конечно, вследствие его неделимости
электрон может проявляться в любой
точке атома, так что нужно говорить о
вероятности его появления в том или
ином месте.
Вернер Карл
Гейзенберг
1901-1976
Ноб. лаур.
1932
21.
Волновая функция (Борн, 1926)Для описания движения микрочастицы, обладающей
волновыми свойствами, не может быть использован
способ классической механики, когда состояние частицы
определяется заданием в любой момент времени ее
пространственных координат и скорости (импульса).
Состояние частицы в квантовой механике описывается
Макс Борн
волновой функцией, зависящей от пространственных
1882-1970
Ноб. лаур.
координат и времени.
Ψ ( x, у , z , t )
1954
С помощью математических
операций над волновой функцией, находятся значения
физических параметров частицы (энергия, импульс).
Вероятностный смысл волновой функции
Квадрат модуля волновой функции имеет смысл плотности
вероятности, т.е. определяет вероятность нахождения частицы
в данный момент времени в единичном объеме dV dx dy dz
в окрестности точки с координатами x, y, z .
Состояние микрочастицы полностью определяется волновой
функцией. Частица может быть обнаружена в любой точке
пространства, в которой волновая функция отлична от нуля.
22.
dP Ψ dV2
P Ψ dV
P
2
Ψ
2
dV 1
V
V
Уравнение Шредингера (1926)
Если силовые поля на частицу не действуют (т.е. ее
потенциальная энергия остается постоянной во
времени), то волновую функцию можно разложить на
две части, зависящие только от времени или координат.
Ψ ( x, у, z, t ) f (t ) Ψ ( x, у, z )
Применительно к таким стационарным состояниям
уравнение Шредингера имеет вид:
2Ψ 2Ψ 2Ψ 8 2 m
2 2 2 ( E U )Ψ 0
2
x
y
z
h
Эрвин
Рудольф
Йозеф
Александр
Шрёдингер
1887-1961
Ноб. лаур.
1933
Здесь m – масса частицы, U – потенциальная энергия, E – полная
энергия частицы.
2
2
В одномерном случае:
Ψ 8 m
2 ( E U )Ψ 0
2
x
h
23.
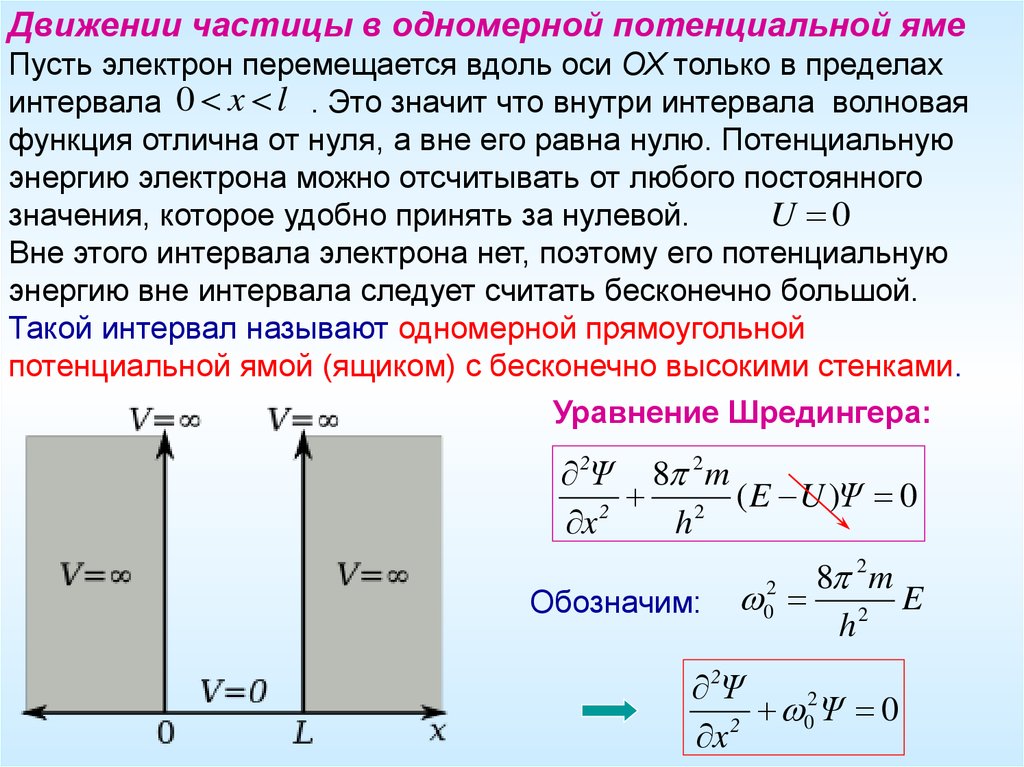
Движении частицы в одномерной потенциальной ямеПусть электрон перемещается вдоль оси ОХ только в пределах
интервала 0 x l . Это значит что внутри интервала волновая
функция отлична от нуля, а вне его равна нулю. Потенциальную
энергию электрона можно отсчитывать от любого постоянного
U 0
значения, которое удобно принять за нулевой.
Вне этого интервала электрона нет, поэтому его потенциальную
энергию вне интервала следует считать бесконечно большой.
Такой интервал называют одномерной прямоугольной
потенциальной ямой (ящиком) с бесконечно высокими стенками.
Уравнение Шредингера:
2Ψ 8 2 m
2 ( E U )Ψ 0
2
x
h
Обозначим:
2
8
m
2
0 2 E
h
2Ψ
2
0Ψ 0
2
x
24.
Решение уравнения – гармоническая функция по координате:Ψ Ψ 0 cos( 0 x 0 )
Значения Ψ 0 , 0 , 0 , E
1) При x 0 Ψ 0
находятся из граничных условий:
:
0 Ψ 0 cos(0 0 ) Ψ 0 cos 0
cos 0 0
0 / 2
0 Ψ 0 cos( 0 l / 2)
n
cos( 0 l ) 0
0 l (2n 1)
0
2
2
2
l
n 1, 2, 3, n 0
Здесь n – целое число
иначе Ψ 0 при любых x , т.е. электрон в ящике отсутствует !
2 2
2
2 2
2
2
2
h
n
h
n
h
8
m
2
0
E
E
2
2
Вспомним: 0
2
2
2
8 m
l 8 m l 8m
h
2) При
x l Ψ 0
h2 2
n
En
2
8ml
:
1
n
n
Ψ Ψ 0 cos
x Ψ 0 cos x
2
2
l
l
25.
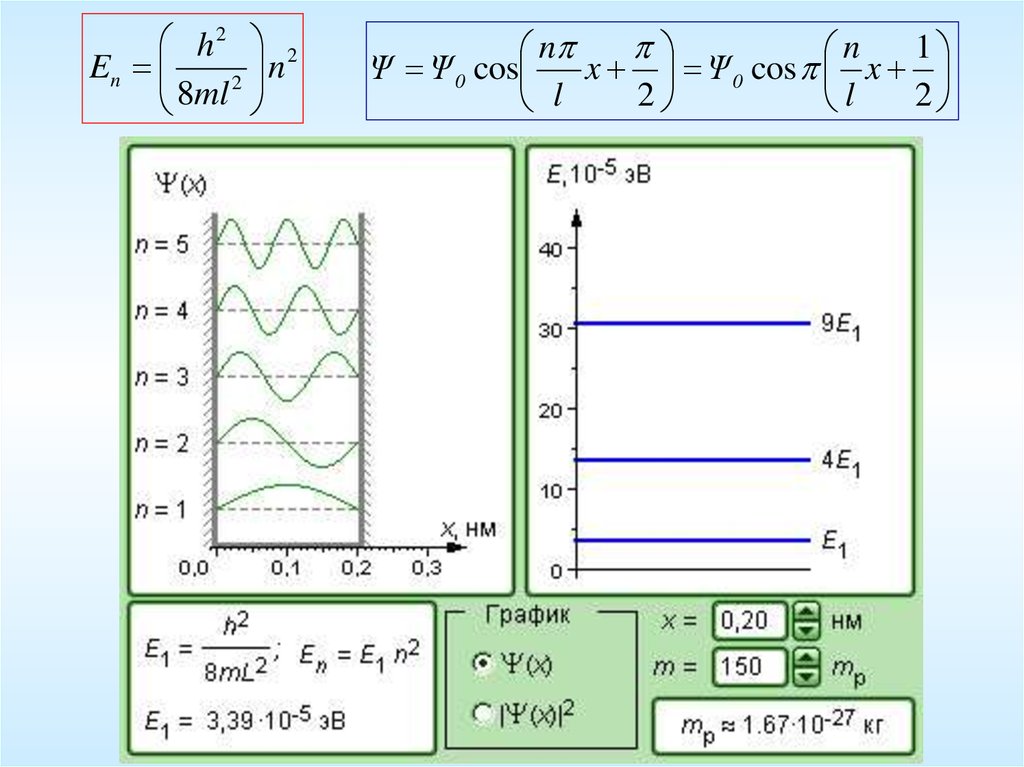
h2 2n
En
2
8ml
1
n
n
Ψ Ψ 0 cos
x Ψ 0 cos x
2
2
l
l
26.
Электрон в атоме водородаВ атоме потенциальная энергия:
Уравнение Шредингера:
Z e2
U
r
2Ψ 8 2 m
Z e2
2 (E
)Ψ 0
2
x
h
r
me Z 2e 4 1
En
2 2 2
8 0 h n

















 Физика
Физика








