Похожие презентации:
Гидрогенизационные процессы переработки нефти и газа
1.
Гидрогенизационные процессы переработкинефти и газа
Гидрокрекинг
Гидроочистка
Риформинг
Причины возрастающеего значения этих процессов:
1. Задача углубленной переработки нефти
65% (в наст. Время)
Для повышения выхода «светлых» необходимо насыщение
водородом кратных связей (ароматика, смолы) и расщепление тяжелых
компонентов нефти
Достигается в процессе гидрокрекинга
2.
2. В процессах Гидрорекинга и Каталитического РиформингаИспользование Н2 продляет срок службы катализатора, препятствует
коксообразованию и отравлению кат.
3. В процессах Гидроочистки нефтей удаляются
серосодержащие и др. гетероатомные соединения
Гидроочистке подвергаются также мазуты и сырье для процессов
кат. Крекинга и риформинга
Гидрокрекинг
Сырье:
тяжелые нефтяные дистилляты,
нефтяные остатки(мазут, гудрон),
тяжелые и высокосернистые нефти
3.
Продуктыгидрокрекинга:
( в завис.
от условий
и сырья)
высокооктановый бензин
реактивное или дизельное топливо
смазочные масла
котельное топливо
Гидрокрекинг
Одноступенчатый
Двуступенчатый
В одной стадии
гидрирование, крекинг
и гидроочистка
А) Стадия гидроочистки
и частичного гидрирования
Б) стадия гидрокрекинга
4.
Гидрокрекинг. Сырье гудрон и тяж.нефтяныеостатки
Одностадийный
Условия:
Продукты:
400-500оС, 7.0-20 МПа
катализатор бифункциональные, оксидные
Удаляется до 98% серы
Газ (3-5%)
бензиновая фракция 30-175оС (12-22%)
фракция 170-370оС (30-60%)
газойлевая фракция 370-450оС (20-10%)
Остаток Т более 540оС (40-5%) –
котельное топливо
5.
ГидрокрекингСырье:тяж.нефтяные фракции (вакуумный газойль)
(Одностадийный либо двуступенчатый)
Условия:
370-450оС, 10.0-24 МПа (проц. высокого давления)
катализатор бифункциональные, оксидные
Продукты:
Газ
бензиновая фракция
газойлевая фракция (легкие или тяжелые)
остаток с Т более380оС (мазуты)- котельное
топливо либо сырье для кат. рекинга
6.
Реакции протекающие в условиях гидрокрекинга1. Гидрирование алифатических двойных связей
RCH=CHR
H2
RCH2CH2R
2. Частичное Гидрирование полициклической ароматики
R
H2
R
7.
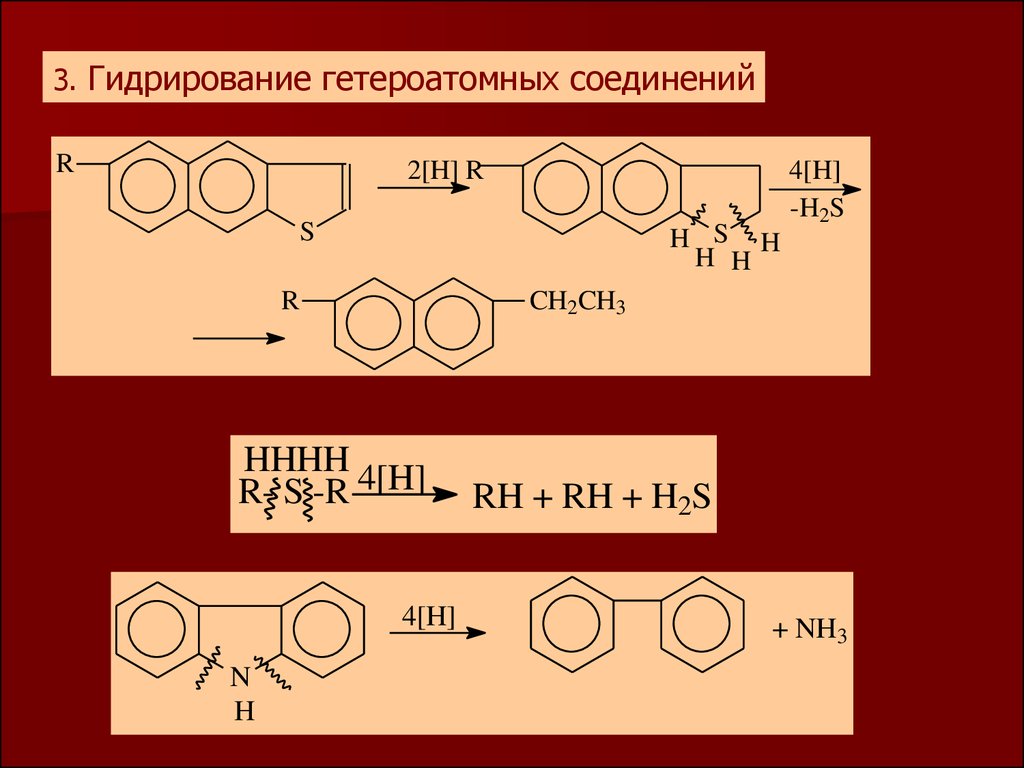
3. Гидрирование гетероатомных соединенийR
2[H] R
S
H S H
H H
R
CH2CH3
HHHH
R- S -R 4[H]
4[H]
N
H
4[H]
-H2S
RH + RH + H2S
+ NH3
8.
4[H]+ H2O
O
R
R`
H
CH R`
4[H] R
CH3
O H
H H
+ H2O
R
R
2[H]
R
OH
R
+ H2O
9.
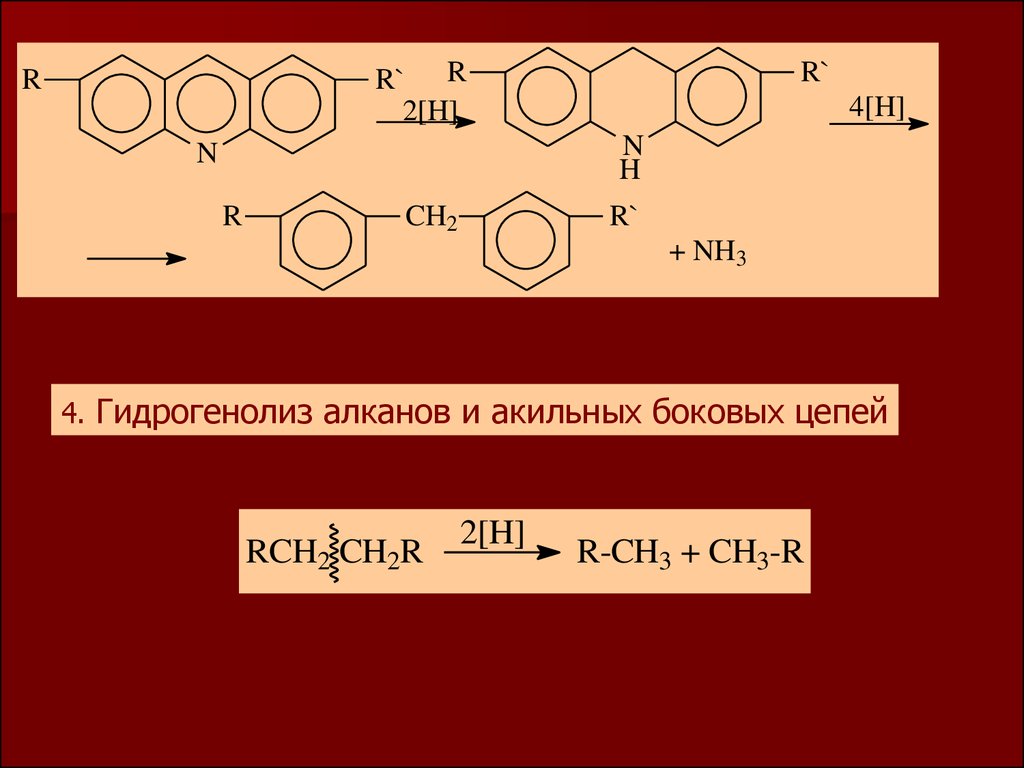
R` R2[H]
R
R`
4[H]
N
H
N
R
CH2
R`
+ NH3
4. Гидрогенолиз алканов и акильных боковых цепей
RCH2 CH2R
2[H]
R-CH3 + CH3-R
10.
В одноступенчатом гидрокрекинге и на 2 стадии двуступенчатогоприменяются бифункциональные катализаторы:
WO3, MoO3, NiO, Со2О3, WS3, MoS3, NiS, Со2S3,
Металлы (Pt, Ni) на кислом носителе
(Al2O3, цеолиты, алюмосиликаты)
Содержат Каталитические центры двух типов
Гидрирующие
Например: кат:
Pt, Ni на носителе
Крекирующие,
Изомеризующие
Атомы металла –
гидрирующие активные центры
Кислотные центры носителя (протон и апротон) –
центры изомеризации и расщепления
11.
Природа активных центровоксидов и сульфидов металлов
WO3, MoO3, NiO, Со2О3, WS3, MoS3, NiS, Со2S3
- полупроводники
В полупроводниках
переход из валентной зоны
в зону проводимости
требует преодоления эн. Барьера
(Энергия активации
электропроводности Еа)
Еа
Свободная зона,
проводимости
Запрещенная зона
Валентная зона
Поэтому оксиды Ме начинают проводить только при нагревании
12.
При нагревании:Zn
Zn
2+
Zn
+
e
+
Zn
+
e
+
Ионизация атомов цинка
Электрон блуждает по
кристаллической решетке
оксида
Вспомним: полупроводники бывают
n-полупроводники (электронные) и р-полупроводники (дырочные)
Большинство пром. Окисных Катализаторов гидрокрекинга являются
n-полупроводниками Fe2O3, WO3, MoO3
13.
На поверхности катализаторов есть свободные электроныПри взаимодействии с ними молекулы УВ подвергаются
гомолитическому распаду
Механизм гидрокрекинга над окисными катализаторами
РАДИКАЛЬНЫЙ
R
Н
H
+ +
R
. .
+ +
e
Блуждающий электрон
Продолжение цепного
процесса гидрокрекинга
14.
Большинство пром. Сульфидных Катализаторов гидрокрекингаявляются р-полупроводниками
Избыточная сера в сульфидах обусловливает образование дырок
Под влиянием которых происходит гетеролитический разрыв связей
Механизм гидрокрекинга над сульфидными катализаторами
ИОННЫЙ
Однако неспаренные электроны на поверхности сульфидных кат.
Обусловливают радикальные процессы (гидрирования)
Следовательно сульфидные кат. -бифункциональные
15.
R..
H
+++
H
:H
+++
H
..
R
+
+++
H
..
+++
Карбкатионы и протоны продолжают цепной процесс
превращения углеводородов
+
H
16.
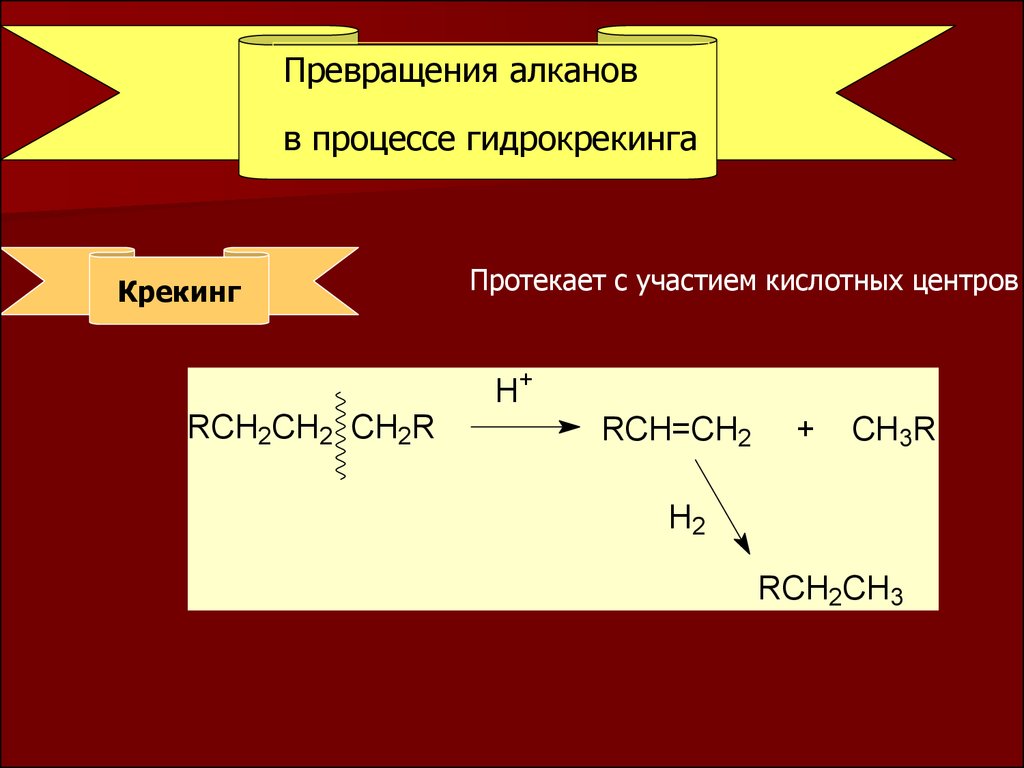
Превращения алкановв процессе гидрокрекинга
Крекинг
Протекает с участием кислотных центров
H+
RCH2CH2 CH2R
RCH=CH2
+
CH3R
H2
RCH2CH3
17.
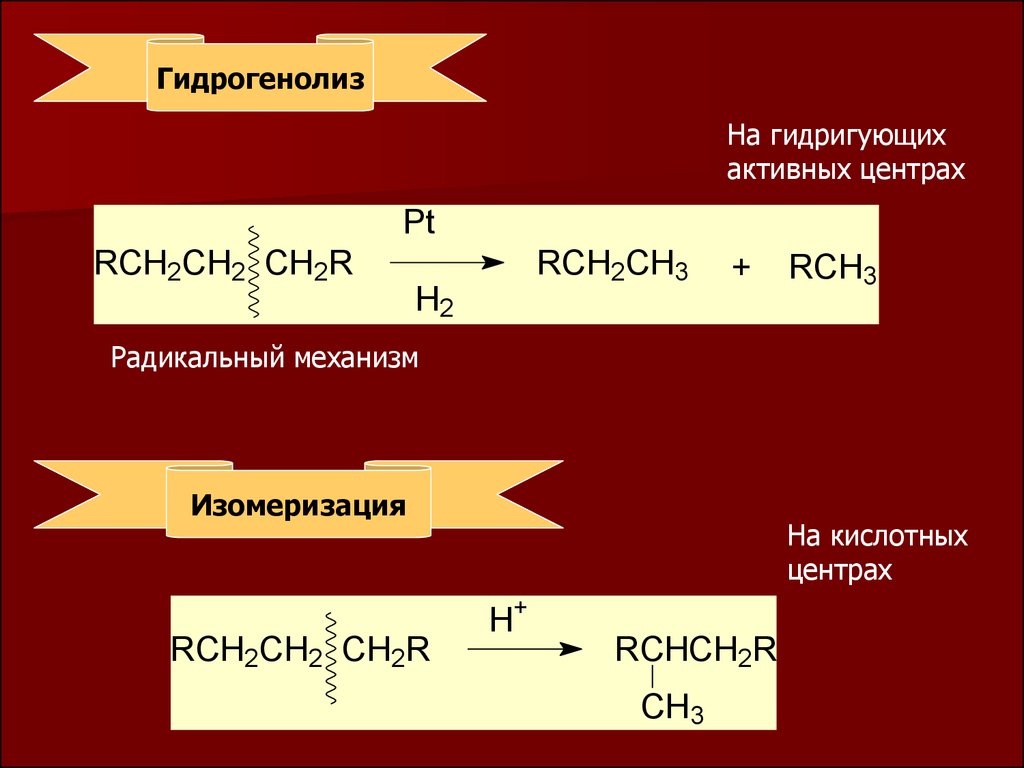
ГидрогенолизНа гидригующих
активных центрах
Pt
RCH2CH2 CH2R
RCH2CH3
+
H2
RCH3
Радикальный механизм
Изомеризация
RCH2CH2 CH2R
На кислотных
центрах
H+
RCHCH2R
CH3
18.
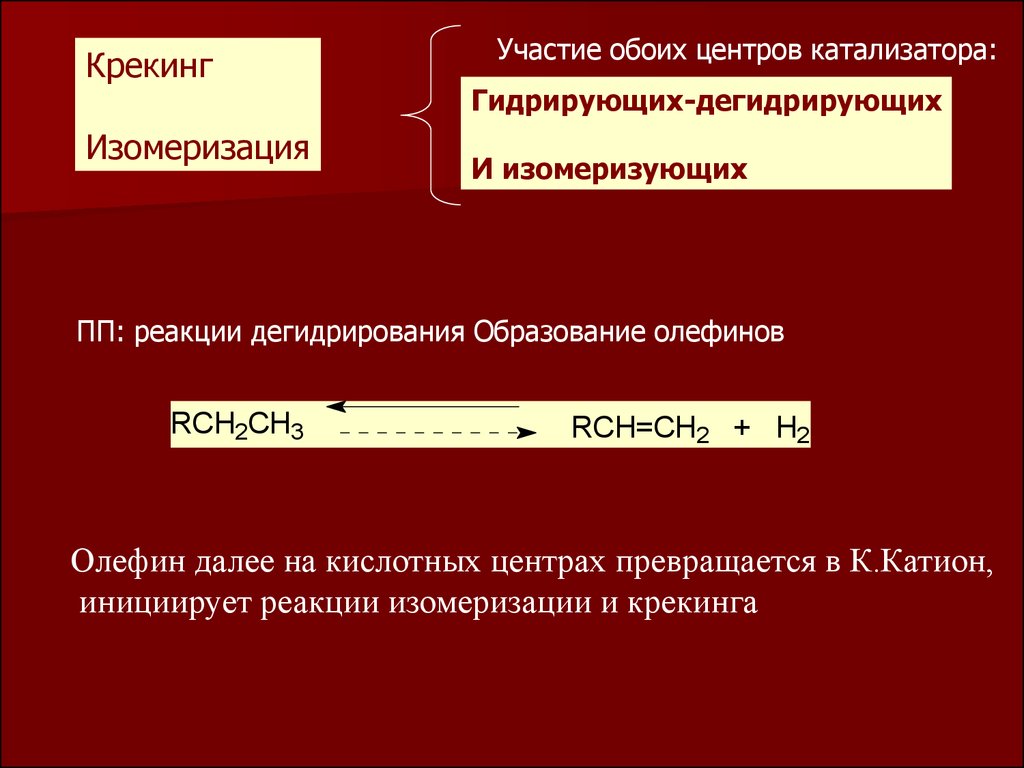
КрекингИзомеризация
Участие обоих центров катализатора:
Гидрирующих-дегидрирующих
И изомеризующих
ПП: реакции дегидрирования Образование олефинов
RCH2CH3
RCH=CH2 + H2
Олефин далее на кислотных центрах превращается в К.Катион,
инициирует реакции изомеризации и крекинга
19.
Соотношение междуКрекингом
Изомеризацией
гидрогенолизом
Определяется
а) соотношением между кислотной и
гидрирующей-дегидрирующей функцией кат.
б) давлением Н2 и Т
20.
Превращения нафтеновв процессе гидрокрекинга
1.
Крекинг боковых цепей
Происходит на кислотных центрах
Крекинг и Гидрогенолиз
колец
Происходит в случае кат.,
имеющих активные гидрирующие центры Pt,Pd,Ni
CH3
2[H]
CH3-CH2-CH-CH2-CH12-CH3
CH3
21.
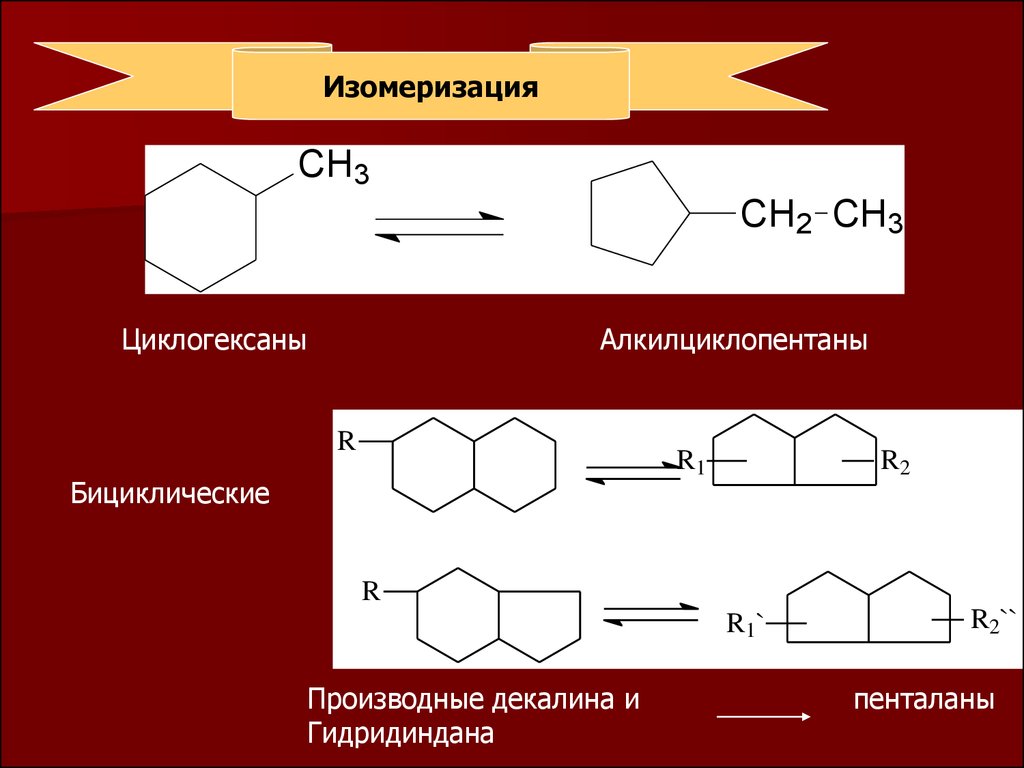
ИзомеризацияCH3
CH2 CH3
Циклогексаны
Алкилциклопентаны
R
R1
Бициклические
R2
R
R1`
Производные декалина и
Гидридиндана
R2``
пенталаны
22.
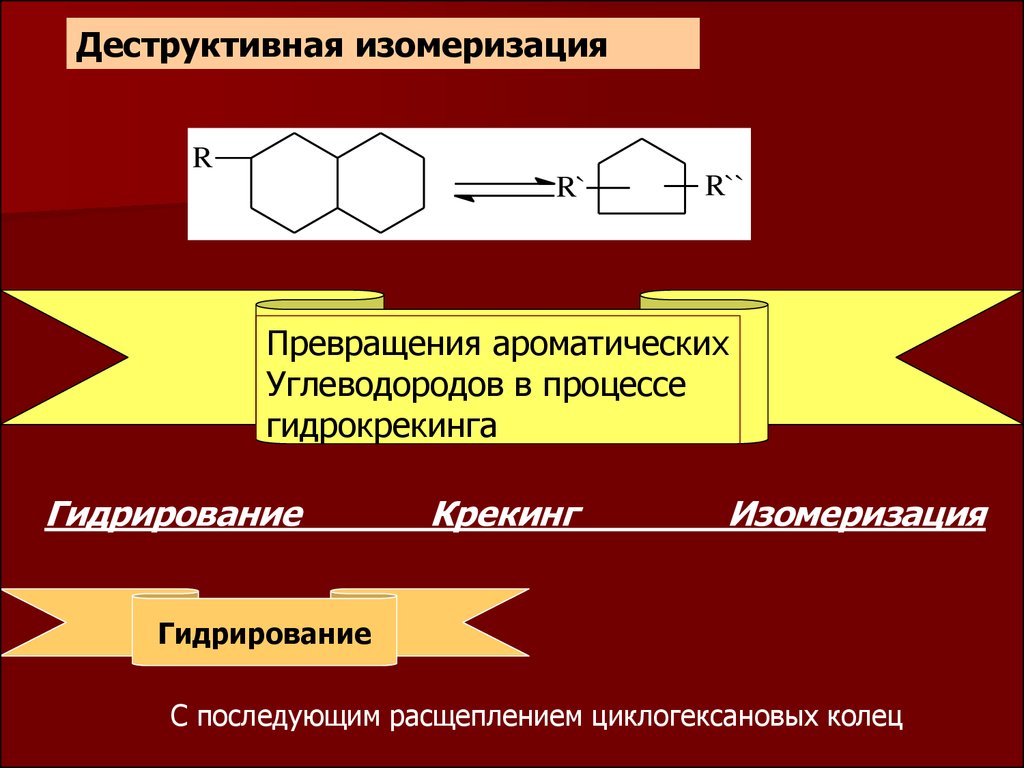
Деструктивная изомеризацияR
R`
R``
Превращения ароматических
Углеводородов в процессе
гидрокрекинга
Гидрирование
Крекинг
Изомеризация
Гидрирование
С последующим расщеплением циклогексановых колец
23.
H5C22H2
H5C2
H5C2
H2
C2H5
+ C4H10
C4H9
Закономерности гидрирования АУ в процессе Гидрокрекинга:
1. В основном гидрируются полициклические АУ
2. Незамещенные АУ гидрируются в первую очередь
3. Конечные продукты- алкилбензолы
4. Дальнейшее гидрирование алкилбензолов нежелательно,
т.к. приводит к снижению октанового числа бензина
24.
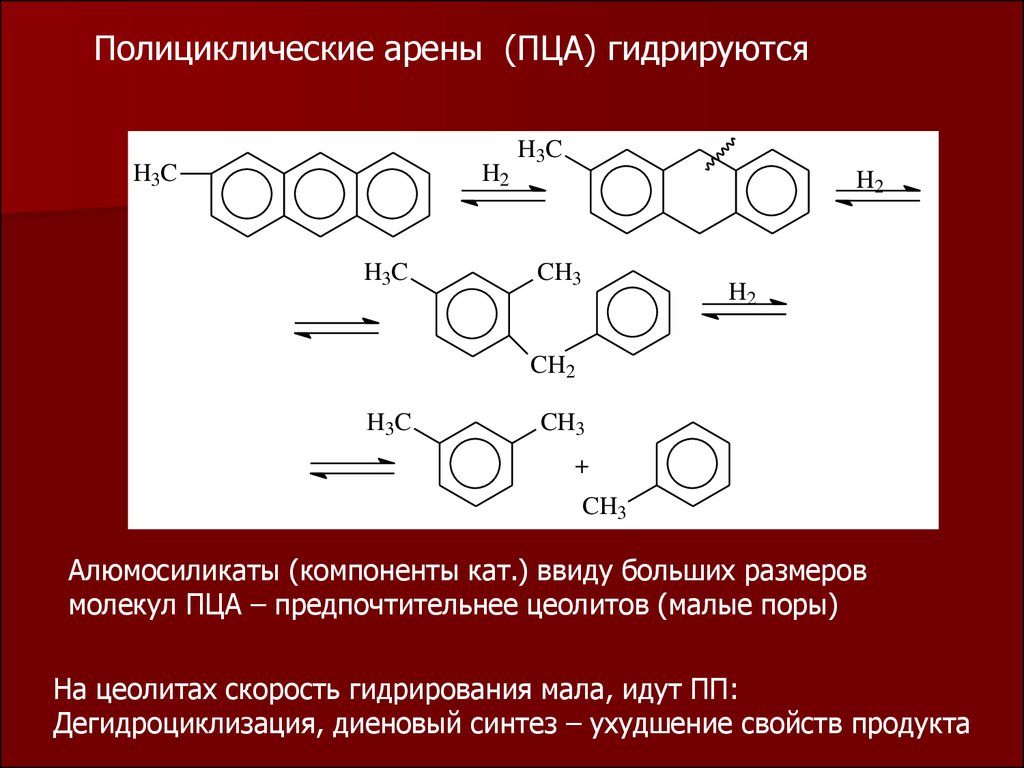
Полициклические арены (ПЦА) гидрируютсяH3C
H2
H3C
H3C
H2
CH3
H2
CH2
H3C
CH3
+
CH3
Алюмосиликаты (компоненты кат.) ввиду больших размеров
молекул ПЦА – предпочтительнее цеолитов (малые поры)
На цеолитах скорость гидрирования мала, идут ПП:
Дегидроциклизация, диеновый синтез – ухудшение свойств продукта
25.
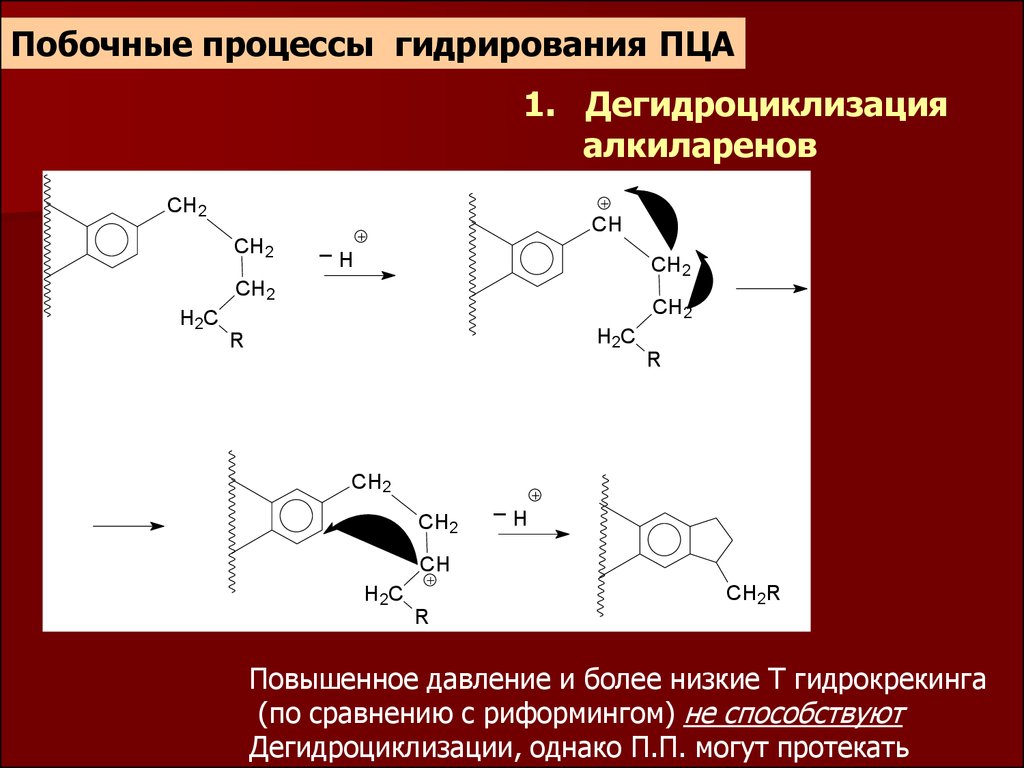
Побочные процессы гидрирования ПЦА1. Дегидроциклизация
алкиларенов
CH2
CH
CH2
_
H
CH2
CH2
CH2
H 2C
H2C
R
R
CH2
CH2
_
H
CH
CH2R
H 2C
R
Повышенное давление и более низкие Т гидрокрекинга
(по сравнению с риформингом) не способствуют
Дегидроциклизации, однако П.П. могут протекать
26.
2. Реакция диенового синтезаСпособствует повышенное давление в процессе гидрокрекинга
C=C C=C
-
äèåí î ô èë
C=C
-
2H2
äèåí
H2
27.
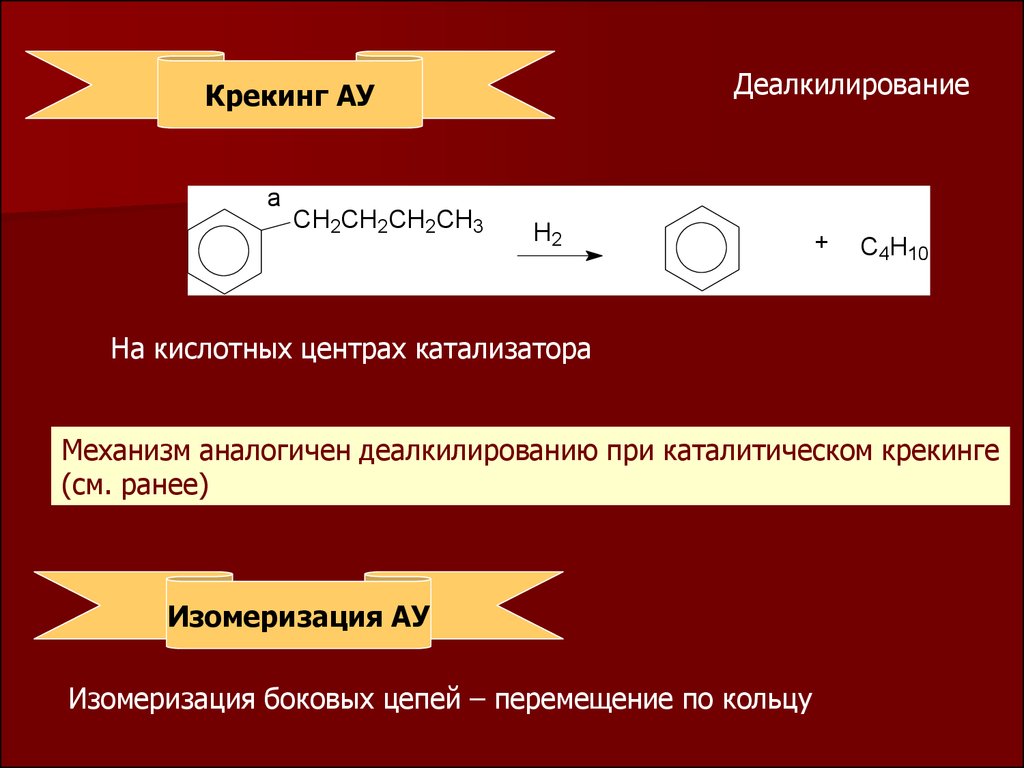
ДеалкилированиеКрекинг АУ
a
CH2CH2CH2CH3
H2
+
C4H10
На кислотных центрах катализатора
Механизм аналогичен деалкилированию при каталитическом крекинге
(см. ранее)
Изомеризация АУ
Изомеризация боковых цепей – перемещение по кольцу
28.
Гидрогенизационныепроцессы
переработки
нефти и газа
Гидроочистка


















 Химия
Химия Промышленность
Промышленность