Похожие презентации:
Гистогематические барьеры. Депонирование. Метаболизм. Фармакогенетика
1.
Лекция №4Общая фармакология
• Гистогематические барьеры
• Депонирование
• Метаболизм
• Фармакогенетика
Старший преподаватель, к.м.н.
Фатихов И.М.
2.
ЛВ быстро попадают вте органы и ткани,
которые
интенсивно
снабжаются
кровью
(сердце, печень, почки).
Переход лекарственных
веществ
в
мышцы,
слизистые
оболочки,
кожу, жировую ткань
происходит медленнее,
так
как
скорость
кровотока в них ниже.
Круги
циркуляции
3.
Биологические (гисто-гематические)барьеры - это стенки капилляров.
Они играют существенную роль в распределении лекарственных
веществ.
«забарьерные»
ткани:
мозг, плацента,
половые железы,
глаза, щитовидная
железа и др.
4.
Гематоэнцефалический барьер - состоит измембран эндотелия сосудов головного мозга и
глиальных нервных клеток.
Он отделяет ткань мозга и спинномозговую
жидкость от крови (исключение - триггерная
зона рвотного центра).
Эндотелий прилегает ПЛОТНО 1. Пассивная диффузия липофильных ЛВ
2. Нет фильтрации гидрофильных ЛВ
5.
Через ГЭБ лекарственные вещества частопереходят по механизму простой диффузии со
скоростью пропорциональной из растворимости в
липидах.
Хорошо проходят неионизированные соединения.
Гидрофильные и полярные соединения переходят
через этот барьер путем активного транспорта.
При некоторых патологических состояниях
(воспалении мозговых оболочек) проницаемость
гематоэнцефалического
барьера
для
лекарственных веществ повышается.
6.
Плацентарный барьер - между матерью иплодом.
Через плаценту путем простой диффузии переходят
липидорастворимые и неионизированные соединения.
Известно, что многие лекарственные средства (снотворные,
анальгетики,
сердечные
гликозиды,
кортикостсроиды,
гипотензивные средства, антибиотики, сульфаниламиды и др.)
хорошо проникают через плацентарный барьер.
Четвертичные аммониевые соединения тубокурарин,
ганглиоблокаторы, а также малорастворимые в жирах вещества
(инсулин и декстран) не проникают через плацентарный барьер.
7.
РАСПРЕДЕЛЕНИЕ ЛВВ одних органах концентрация ЛВ может быть высокой, в
других - ничтожно малой.
Накопление ЛВ в органах и тканях зависит от состава этих
тканей. Основную роль в депонировании ЛВ принадлежит
липидам, белкам, мукополисахаридам.
Липофильные ЛВ накапливаются НЕРАВНОМЕРНО - в
мозге, жировой ткани и меньше в мышечной ткани. Так, при
наркозе в головном мозге содержание наркозных средств
значительно больше, чем в скелетных мышцах.
Водорастворимые ЛВ накапливаются РАВНОМЕРНО - в
межклеточной жидкости, в органах выделения (почках).
Многие ЛВ имеют свойство избирательно накапливаться в
местах специфического действия. Йод накапливается в
щитовидной железе,
сердечные гликозиды в сердечной
мышце, женские половые гормоны в матке и влагалище.
8. Влияние фитопрепаратов на активность изоферментов цитохрома Р-450.
ВЛИЯНИЕ ФИТОПРЕПАРАТОВ НА АКТИВНОСТЬ ИЗОФЕРМЕНТОВЦИТОХРОМА Р-450.
Система цитохромов - большое
семейство
железосодержащих
ферментов. В организме человека
цитохромы
являются
необходимыми ферментами для
синтеза
таких
веществ,
как:
холестерин,
кортикостероиды,
жирные
кислоты.
Главной
особенностью
ферментов
цитохромов является их уникальная
способность активировать молекулу
кислорода и впоследствии, вводить
один атом кислорода в различные
соединения по месту инертных
химических связей
Индукторы изоферментов цитохрома Р-450 ускоряют биотрансформацию многих
ЛВ и в результате снижают их концентрацию и ослабляют
фармакологические эффекты. Ингибиторы изоферментов цитохрома Р-450,
наоборот, замедляют биотрансформацию лекарственных средств и таким образом
способствуют увеличению их концентрации и повышению риска развития
нежелательных лекарственных реакций.
9. Ингибиторы цитохромов
ИНГИБИТОРЫ ЦИТОХРОМОВ• Сок грейпфрута ингибирует изофермент CYP3A4
• Экстракт чеснока за счет диаллилсульфида ингибирует CYP2E1 и
снижает его активность более чем на 30 %.
• Экстракта эхинацеи пурпурной ингибирует CYP1А2 и CYP2C9 печени,
CYP3A4 кишечника и при этом индуцирует CYP3А4 в печени
• Ингибитором CYP3A4 является флавоноид красного вина
ресвератрол.
10. Влияние препаратов на активность транспортера гликопротеина-Р
ВЛИЯНИЕ ПРЕПАРАТОВ НА АКТИВНОСТЬ ТРАНСПОРТЕРАГЛИКОПРОТЕИНА-Р
Р-гликопротеин
лекарственный
транспортер
–
гликопротеин,
выполняющий
функции
трансмембранного
переносчика
веществ, который выводит ЛВ из
клетки.
Р-гликопротеин
обнаруживается во многих тканях,
особенно в органах, ответственных
за всасывание или выведение
лекарственных средств, такие как
кишечник, печень и почки.
Субстратами гликопротеина-Р являются сердечные гликозиды, бл
кальциевых каналов, макролиды, фторхинолоны, ингибиторы
ВИЧ-протеазы, статины, многие противоопухолевые средства. В ки
гликопротеин-Р препятствует всасыванию лекарств, а в почках и в
способствует активной секреции в мочу и желчь, соответственно.
11.
12.
Фармакогенетика(др.-греч. φάρμακον — лекарство
и генетика) — раздел медицинской
генетики и фармакологии, изучающий
характер реакций организма на
лекарственные средства в зависимости
от наследственных факторов.
13.
Термин фармакогенетика:Vogel F. (1959) или Motulsky AG (1957).
I этап- накопление фармакогенетических феноменов
(1932- начало 1960-х);
II этап- становление фармакогенетики как
фундаментальной науки (начало 1960-х −1990-е годы);
III этап- становление фармакогенетики как прикладной
клинической науки, переход от фармакогенетики
к фармакогеномике (начало 2000-х годов).
14.
Арно Мотульски (Arno G. Motulsky)«… идиосинкразия по
отношению к
лекарственным средствам
может быть вызвана
генетическими
особенностями и
дефицитом ферментов,
ничем другим себя не
проявляющими…»
15.
Фридрих Фогель (Friedrich Vogel)ввел термин
«фармакогеномика»
для деятельности по
изучению клинически
значимых
наследственных
особенностей
16.
Ксенобиотики – чужеродные (несинтезированные организмом человека)
химические соединения.
Метаболизм (биотрансформация)
ксенобиотиков находится под генетическим
контролем
Гены детоксикации ксенобиотиков получили
название генов «внешней среды»
17.
Роль ферментов нормального обмена веществ вдеградации ксенобиотиков
Система цитохрома Р-450: холестерин=>желчные кислоты, стероидные
гормоны; активация витамина D; окисление липидов
Глутатионтрансферазы: метаболизм лейкотриенов и простаноидов,
обезвреживание продуктов окисления липидов и пероксидов ДНК.
УДФ-глюкоронил-трансферазы: обезвреживание билирубина, метаболизм
желчных кислот, токоферолов, стероидов.
Сульфатрансферазы: метаболизм желчных кислот и гликолипидов
Ацетилтрансферазы: метаболизм гексозаминов, синтез ацетилхолина.
Метилтрансферазы: метилирование ДНК, обмен котехоламинов.
18.
Промежуточные токсичные метаболиты КБОт входа до выхода ксенобиотика из организма клетки, как правило, должны сделать его
доступным для для соответствующих систем, что требует химической модификации
исходного КБ,
то есть его метаболизма
Метаболиты, образуемые в организме из ксенобиотиков,
чем исходный КБ, и потому часто
более реакционно способны,
1) более биологически эффективны (образование активной действующей формы лекарств
в организме)
2) более опасны (образование токсинов, мутагенов и канцерогенов из слаботоксичных
предшествеников).
ТОКСИФИКАЦИЯ КСЕНОБИОТИКОВ
СИСТЕМОЙ ЦИТОХРОМОВ Р - 450
Хлороформ CHCl3
Фосген Cl2C=O
Парацетамол
метаболит,
повреждающий печень и
почки
Бензпирен
Дигидроксиэпоксид
(канцероген)
19.
Индукция ферментов метаболизма КБМитридат систематически принимал небольшие дозы ядов, чтобы избежать острого
отравления. «Эффект Митридата» основан на индукции определенных защитных систем
ЗАЩИТНАЯ
СИСТЕМА
ФЕНОБАРБИ
-ТАЛ
СИСТЕМА
ЦИТОХРОМА
+
ДИБУНОЛ,
БУТИЛГИДРОКСИАНИЗОЛ
МЕТАЛЛЫ
ПРОТИВОРАКОВЫЕ
ЛЕКАРСТВА
+
+
P-450
ЭПОКСИДРИДРОЛАЗЫ
ГЛУТАТИОН- И
УДФ-ГЛЮКУРОНИЛТРАНСФЕРАЗЫ
СИНТЕЗ GSH
МЕТАЛЛОТИОНЕИНЫ
Р-ГЛИКОПРОТЕИН
+
+
+
+
+
+
ФЕНОБАРБИТАЛ ИНДУЦИРУЕТ СИСТЕМУ ЦИТОХРОМА Р450
устойчивость клеток к ФБ возрастает и снотворное действие ФБ снижается
20.
Принципиальная схема матаболизмаОСНОВНЫЕ ФАЗЫ
ИМПОРТ
ДЕТОКСИКАЦИИ КСЕНБИОТИКОВ
АКТИВАЦИЯ
КСЕНОБИОТИКОВ
ФАЗА I
ИСХОДНЫЙ
КСЕНОБИОТИК
ДЕТОКСИКАЦИЯ
АКТИВНЫХ
ПРОМЕЖУТОЧНЫХ
МЕТАБОЛИТОВ
ФАЗА II
ЭВАКУАЦИЯ
ВЫВЕДЕНИЕ
ВОДОРАСТВОРИМЫХ
НЕТОКСИЧНЫХ
КОМПОНЕНТОВ
ФАЗА III
АКТИВНЫЕ ВОДОРАСТВОРИМЫЕ
ПРОМЕЖДУТОЧНЫЕ
НЕТОКСИЧНЫЕ
ЭЛЕКТРОФИЛЬНЫЕ
КОМПОНЕНТЫ
МЕТАБОЛИТЫ
ЦИТОХРОМЫ Р450
ЭПОКСИДГИДРОЛАЗЫ
ДЕГИДРОГЕНАЗЫ
ГЛЮТАТИОНТРАНСФЕРАЗЫ
N-АЦЕТИЛТРАНСФЕРАЗЫ
UDPГЛЮКУРОНСУЛЬФОТРАНСФЕРАЗЫ
Токсическое действие на клетку,
оксидативный стресс , мутации, рак
21.
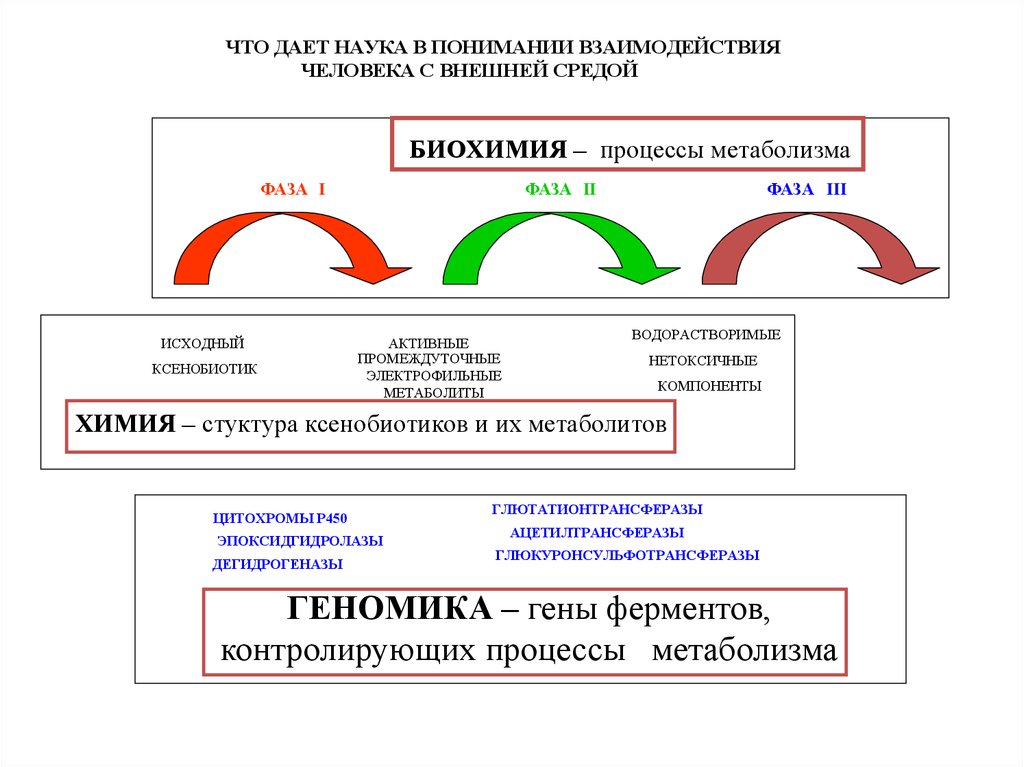
ЧТО ДАЕТ НАУКА В ПОНИМАНИИ ВЗАИМОДЕЙСТВИЯЧЕЛОВЕКА С ВНЕШНЕЙ СРЕДОЙ
БИОХИМИЯ – процессы метаболизма
ФАЗА I
ИСХОДНЫЙ
КСЕНОБИОТИК
ФАЗА II
АКТИВНЫЕ
ПРОМЕЖДУТОЧНЫЕ
ЭЛЕКТРОФИЛЬНЫЕ
МЕТАБОЛИТЫ
ФАЗА III
ВОДОРАСТВОРИМЫЕ
НЕТОКСИЧНЫЕ
КОМПОНЕНТЫ
ХИМИЯ – стуктура ксенобиотиков и их метаболитов
ЦИТОХРОМЫ Р450
ЭПОКСИДГИДРОЛАЗЫ
ДЕГИДРОГЕНАЗЫ
ГЛЮТАТИОНТРАНСФЕРАЗЫ
АЦЕТИЛТРАНСФЕРАЗЫ
ГЛЮКУРОНСУЛЬФОТРАНСФЕРАЗЫ
ГЕНОМИКА – гены ферментов,
контролирующих процессы метаболизма
22.
ФАЗЫ ДЕТОКСИКАЦИИ КСЕНОБИОТИКОВФАЗА I
активация
Образование или модификация функциональных
групп
Гидроксилирование ароматического кольца,
алифатических цепей, аминов или амидов
Эпоксидация ароматического кольца или
ненасыщенных олефинов
S-, N- и P-окисление
O-, N- и S-деалкилирование
Гидролиз эфиров или амидов
Оксилительное дезаминирование
ФАЗА II
детоксикация
Реакции конъюгирования
конъюгация с:
восстановленный
глутатион
глюкуронат
сульфат
ацетат
метил
Редукция эпоксидов, гидроксиламинов,
нитрозосоединений, N- и S- оксидов
N- и C-трансоксигенирование
Ферменты:
цитохромы Р450
алькогольдегидрогеназа
альдегиддегидрогеназаоксида-зы
пептидазы
эстеразы
гликозидазы
Ферменты:
глутатионтрансфераза
ацетилтрансферазы
метилтрансферазы
эпоксигидролазы
Общее число ферментов трансформации ксенобиотиков > 200
23.
СКОРОСТЬ ПРОЦЕССОВ ДЕТОКСИКАЦИИ КСЕНОБИОТИКОВГЕНЕТИЧЕСКИ ДЕТЕРМИНИРОВАНА
ФАЗА I
ФАЗА II
активация
детоксикация
ВЫСОКАЯ
Риск развития
патологии
НИЗКАЯ
ВЫСОКАЯ
НИЗКАЯ
НИЗКАЯ
ВЫСОКАЯ
ФАЗА I
высокая мощность ферментов Фазы I на главных путях
поступления ксенобиотиков в организм:
пищевом – печень, желудочно-кишечный тракт
дыхательном – легкие
Изоферменты тканеспецифичны
24.
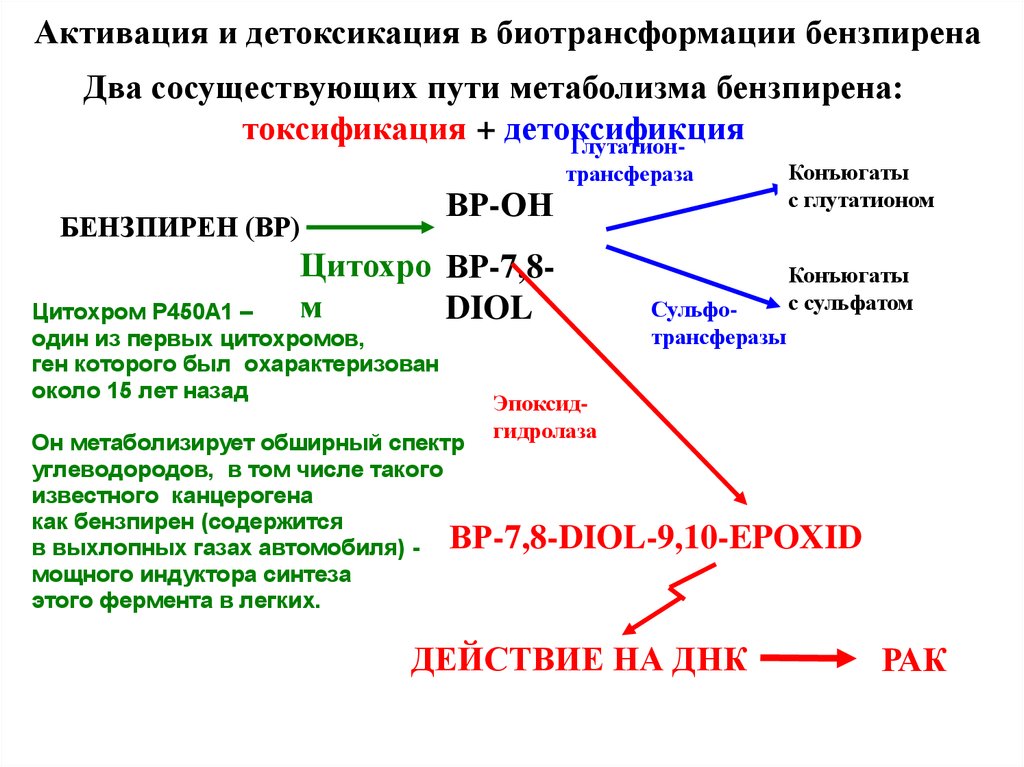
Активация и детоксикация в биотрансформации бензпиренаДва сосуществующих пути метаболизма бензпирена:
токсификация + детоксификция
Глутатион-
ВР-ОН
БЕНЗПИРЕН (ВР)
трансфераза
Цитохро ВР-7,8м
DIOL
Цитохром Р450А1 –
один из первых цитохромов,
ген которого был охарактеризован
около 15 лет назад
Сульфотрансферазы
Конъюгаты
с глутатионом
Конъюгаты
с сульфатом
Эпоксидгидролаза
Он метаболизирует обширный спектр
углеводородов, в том числе такого
известного канцерогена
как бензпирен (содержится
в выхлопных газах автомобиля) - ВР-7,8-DIOL-9,10-EPOXID
мощного индуктора синтеза
этого фермента в легких.
ДЕЙСТВИЕ НА ДНК
РАК
25.
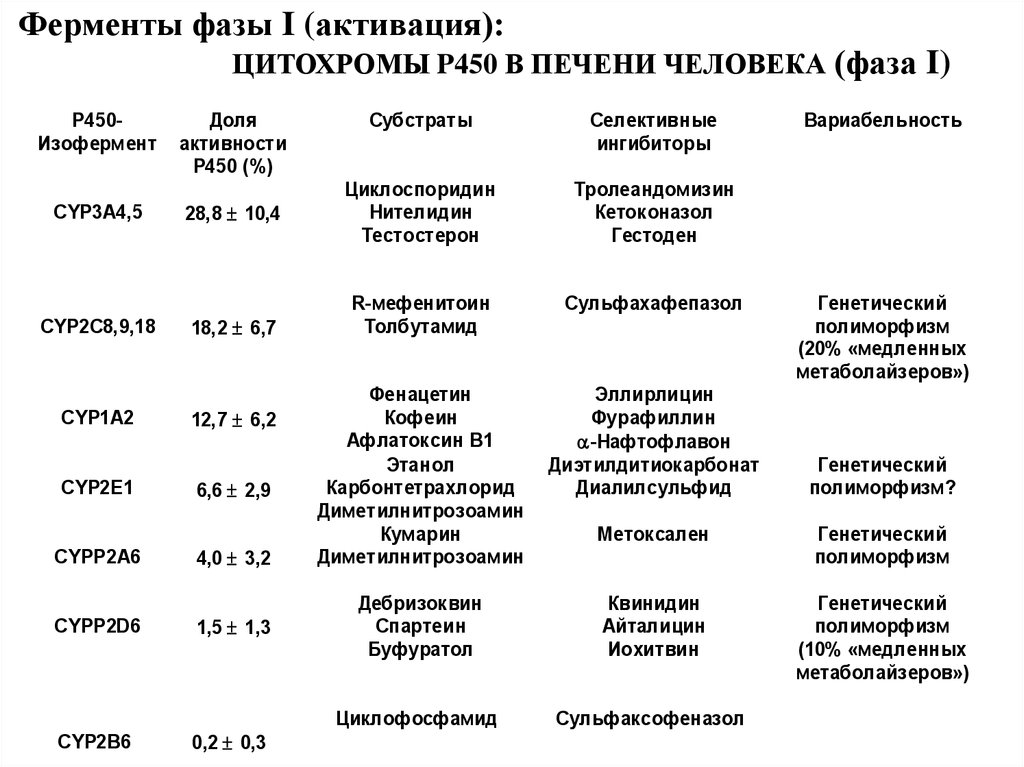
Ферменты фазы I (активация):ЦИТОХРОМЫ P450 В ПЕЧЕНИ ЧЕЛОВЕКА (фаза I)
P450Изофермент
CYP3A4,5
CYP2C8,9,18
CYP1A2
CYP2E1
CYPP2A6
CYPP2D6
CYP2B6
Доля
активности
P450 (%)
28,8 10,4
18,2 6,7
12,7 6,2
6,6 2,9
4,0 3,2
1,5 1,3
0,2 0,3
Субстраты
Селективные
ингибиторы
Вариабельность
Циклоспоридин
Нителидин
Тестостерон
Тролеандомизин
Кетоконазол
Гестоден
R-мефенитоин
Толбутамид
Сульфахафепазол
Фенацетин
Кофеин
Афлатоксин B1
Этанол
Карбонтетрахлорид
Диметилнитрозоамин
Кумарин
Диметилнитрозоамин
Эллирлицин
Фурафиллин
-Нафтофлавон
Диэтилдитиокарбонат
Диалилсульфид
Метоксален
Генетический
полиморфизм
Дебризоквин
Спартеин
Буфуратол
Квинидин
Айталицин
Иохитвин
Генетический
полиморфизм
(10% «медленных
метаболайзеров»)
Циклофосфамид
Сульфаксофеназол
Генетический
полиморфизм
(20% «медленных
метаболайзеров»)
Генетический
полиморфизм?
26.
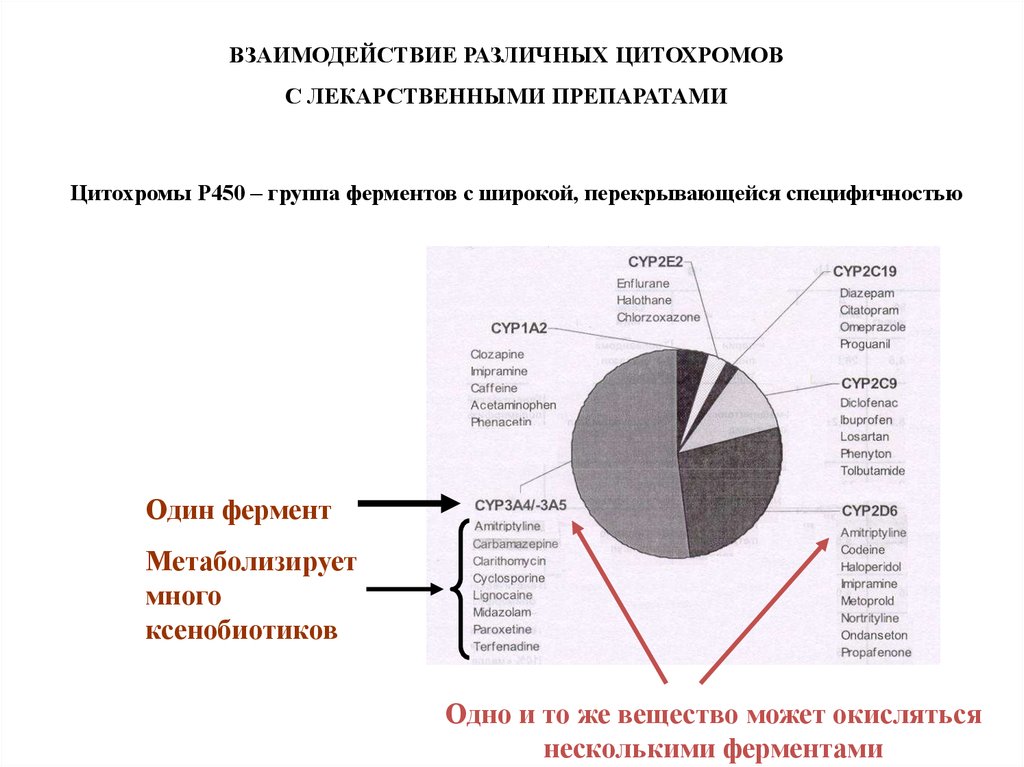
ВЗАИМОДЕЙСТВИЕ РАЗЛИЧНЫХ ЦИТОХРОМОВС ЛЕКАРСТВЕННЫМИ ПРЕПАРАТАМИ
Цитохромы Р450 – группа ферментов с широкой, перекрывающейся специфичностью
Один фермент
Метаболизирует
много
ксенобиотиков
Одно и то же вещество может окисляться
несколькими ферментами
27.
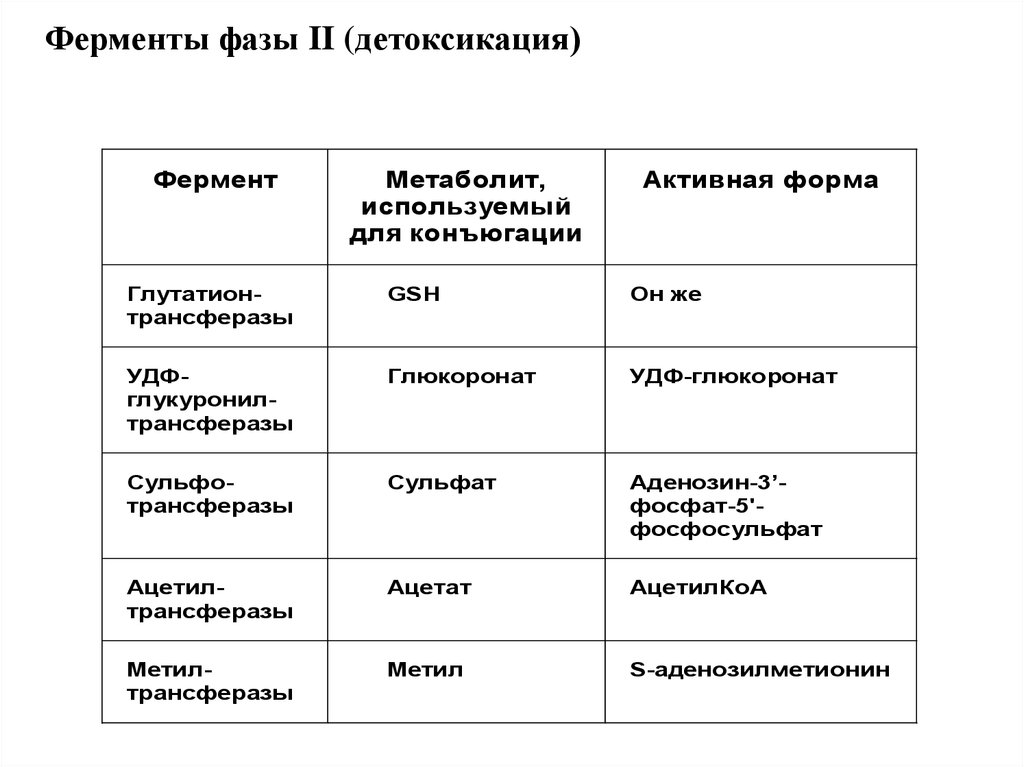
Ферменты фазы II (детоксикация)Фермент
Метаболит,
используемый
для конъюгации
Активная форма
Глутатионтрансферазы
GSH
Он же
УДФглукуронилтрансферазы
Глюкоронат
УДФ-глюкоронат
Сульфотрансферазы
Сульфат
Аденозин-3’фосфат-5'фосфосульфат
Ацетилтрансферазы
Ацетат
АцетилКоА
Метилтрансферазы
Метил
S-аденозилметионин
28.
Гены фазы II (детоксикация): глутатион-S-трансферазыГлутатион-S-трансферазы катализируют взаимодействие глутамата с
электрофильными атомами C, N, S, O широкого спектра соединений. Они
осуществляют ферментную конъюгацию сульфгидрильной группы SH2 c
органическими электрофильными молекулами ксенобиотиков.
Детоксикация ксенобиотиков глутатионтранс-феразами играет ключевую
роль в предотвращении деструкции ДНК. Особенно высока их
концентрация в плаценте, печени, почках, легких, мозге и кишечнике.
Пять классов глутатионтрансфераз и их хромосомная локализация
КЛАСС
A (
M
P
T
Локализация
6p12
1q13
11q13
22q11.23
Микросомальная
12
29.
Гены фазы II (детоксикация): глутатион-S-трансферазы (2/4)Глутатионтрансферазы класса М подразделяются на 5 групп:
GSTM1 – экспрессируется в печени и клетках крови
GSTM2 – только в мышцах
GSTM3, GSTM4, GSTM5 – выявляеются в тканях мозга.
Все эти формы синтезируются с одного гена GSTM, находящегося на длинном
плече хромосомы 1 (1q13), и являются результатом альтернативного сплайсинга
первичного РНК-транскрипта.
GSTM1 – существует в трех аллелях: А, В и 0 (отсутствие фермента)
У людей с генотипом GSTM1 0/0 при курении мутагенный и канцерогенный эффект
выражены особенно сильно.
Наличие /отсутствие гена GSTM1 в обеих хромосомах по ПЦР
- наличие
гена
- контроль
работы метода
Риск осложнений возрастает при сочетании нулевго
функционально неполноценными NAT-2 или CYP450
генотипа
GSTM1
с
30.
Гены фазы II (детоксикация): глутатион-S-трансферазы (3/4)Среди пациентов с опухолевыми заболеваниями с 40% до 80%
повышена частота нефункциональных копий обоих генов GSM1
Норма
40
Рак легкого
52
Базальноклеточная карцинома
57
Аденома гипофиза
61
Рак легкого, адекарцинома
63
Рак толстого кишечника и желудка
67
Аденома гипофиза, пролактинемия
67
Злокачественная мелонома
69
Множественные раки
71
Хронический бронхит
71
Эндометриоз
79
0
10
20
30
40
50
60
70
80
Риск болезни еще более возрастает при одновременой утрате функций
генов GSTM1 и гена NAT2 или CYP450
90
31.
Гены фазы II (детоксикация): ариламин-N-ацетилтрансферазыФермент детоксикации ФАЗЫ II
Ариламин-N-ацетилтрансфераза (NAT)
ацетилирует многие ксенобиотики:
- лекарства, содержащие ароматические аминные или гидразиновые
группы (сульфаниламиды, изониазид, клонозепам, кофеин)
- нитрозамин сигаретного дыма, оксидантов и пестицидов
У человека две формы фермента NAT 1 и NAT 2. Оба гена находятся на
хромосоме 8p21-8p23.
Ген NAT 2 представлен несколькими аллелями – "быстрым" и
"медленными". "Быстрый" аллель является исходной формой и
одинаков воу сех расах, тогда как "медленные" аллели европеоидов и
монголоидов различны.
У "медленных" ацетиляторов - гомозигот по "медленным" аллелям –
скорость работы ферментов снижена на 20%.
Среди европеоидов около 50% - "медленные" ацетиляторы.
Курящие женщины в постменопаузе имеют выраженную
предрасположенность к раку молочной железы, если они "медленные"
ацетиляторы, тогда как "быстрые" ацетиляторы такой ассоциации не
имеют.
У "быстрых" ацетиляторов повышен риск рака толстой кишки, который
снижен у "медленных" ацетиляторов.
32.
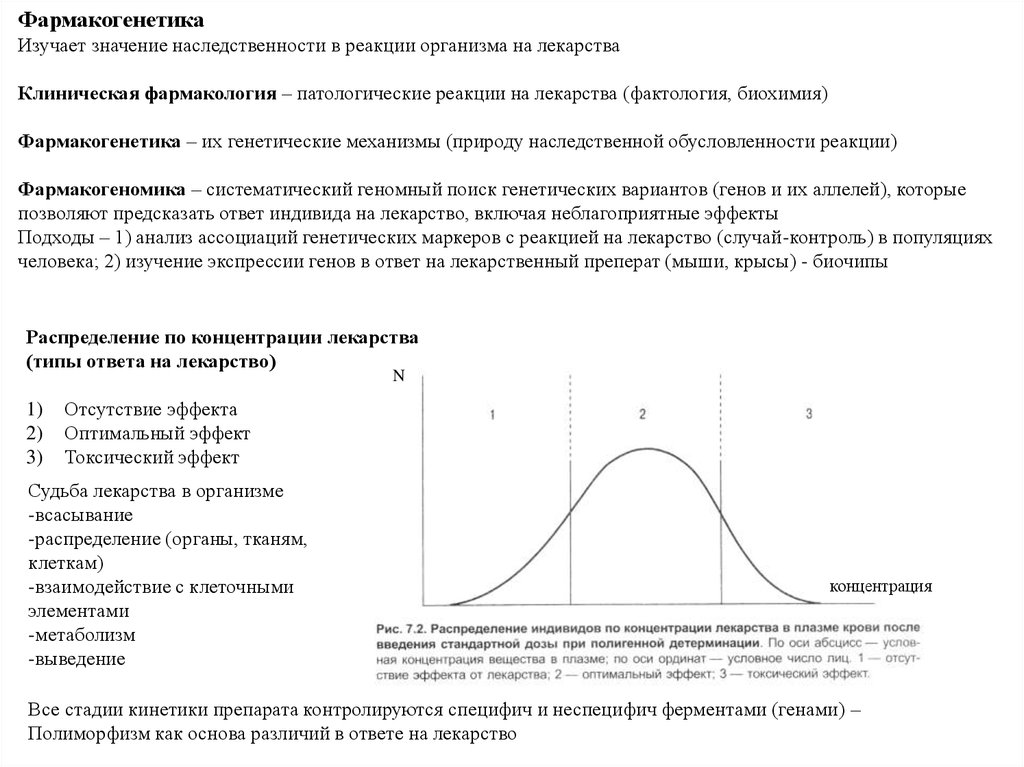
ФармакогенетикаИзучает значение наследственности в реакции организма на лекарства
Клиническая фармакология – патологические реакции на лекарства (фактология, биохимия)
Фармакогенетика – их генетические механизмы (природу наследственной обусловленности реакции)
Фармакогеномика – систематический геномный поиск генетических вариантов (генов и их аллелей), которые
позволяют предсказать ответ индивида на лекарство, включая неблагоприятные эффекты
Подходы – 1) анализ ассоциаций генетических маркеров с реакцией на лекарство (случай-контроль) в популяциях
человека; 2) изучение экспрессии генов в ответ на лекарственный преперат (мыши, крысы) - биочипы
Распределение по концентрации лекарства
(типы ответа на лекарство)
N
1)
2)
3)
Отсутствие эффекта
Оптимальный эффект
Токсический эффект
Судьба лекарства в организме
-всасывание
-распределение (органы, тканям,
клеткам)
-взаимодействие с клеточными
элементами
-метаболизм
-выведение
концентрация
Все стадии кинетики препарата контролируются специфич и неспецифич ферментами (генами) –
Полиморфизм как основа различий в ответе на лекарство
33.
Осложнения лекарственной терапии (патлогическая реакция на лекарства)1)
2)
3)
Толерантность (отсутствие эффекта несмотря на увеличение дозы)
Повышенная чувствительность (эффект передозировки при нормальной дозе) – токсический эффект
Парадоксальная (нетипичная) реакция – неожиданные исходя из мех-ма действия препарата эффекты
(осложнения)
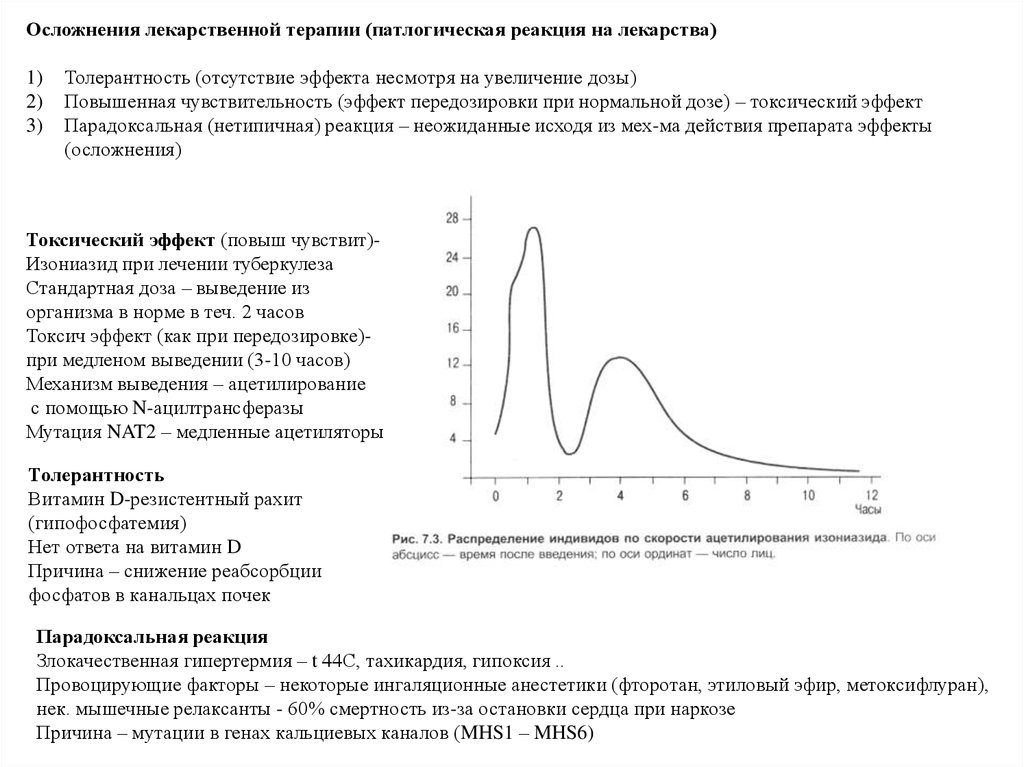
Токсический эффект (повыш чувствит)Изониазид при лечении туберкулеза
Стандартная доза – выведение из
организма в норме в теч. 2 часов
Токсич эффект (как при передозировке)при медленом выведении (3-10 часов)
Механизм выведения – ацетилирование
с помощью N-ацилтрансферазы
Мутация NAT2 – медленные ацетиляторы
Толерантность
Витамин D-резистентный рахит
(гипофосфатемия)
Нет ответа на витамин D
Причина – снижение реабсорбции
фосфатов в канальцах почек
Парадоксальная реакция
Злокачественная гипертермия – t 44С, тахикардия, гипоксия ..
Провоцирующие факторы – некоторые ингаляционные анестетики (фторотан, этиловый эфир, метоксифлуран),
нек. мышечные релаксанты - 60% смертность из-за остановки сердца при наркозе
Причина – мутации в генах кальциевых каналов (MHS1 – MHS6)
34.
Частота патологических реакций на лекарства• Депрессия
62%
• Мигрень
52%
• Астма
60%
• Болезнь Альцгеймера
30%
Нет
ответа
Токсический
ответ
Ответ без
побочных
эффектов
35.
Некоторые примеры генетического полиморфизма, ассоциированного с варьирующимиответами на лекарства
Белок (ген)
Лекарство
Проявление полиморфизма
Белок-переносчик эфиров
холестерина (CETP)
Правастатин
Эффективность правастатина при коронарном
атеросклерозе (миссенс-мутации)
Белок-переносчик эфиров
холестерина (CETP)
Правастатин
Скорость рестеноза при КАС (полиморфизм
промотора)
Рецептор активации и
пролиферации пероксисом
(PRAP2)
Инсулин
Разная чувствительность к инсулину (SNP)
Дофаминовый рецептор D3
(DD3R)
Типичные
нейролептики
Развитие поздней дискенизии у больных
шизофренией (миссенс-мутации)
Аддуцин (ADD)
Гидрохлортиаз
ид
Эффективность лечения АГ (миссенс, SNP)
Переносчик серотонина
(HTT5)
Флувоксамин
Эффективность при галлюциноторной
депрессии (полиморфизм промотора)
Калиевый канал (MIRP1)
Кларитромицин
Индуцированный кларитромицином синдром
LQT (миссенс-мутации)
2-адренергический рецептор
(ADBR2)
Сальбутамол
Эффективность при бронхиальной астме
(Миссенс, SNP)
36.
Фармакогеномика и фармакологическая промышленностьНаиболее многообещающие лекарства часто не могут пройти фазу III клинических испытаний (на людях)
Из-за побочных эффектов у небольшого числа тестируемых
- Можно ли предсказать эти эффекты?
Лекарства, уже продающиеся на рынке иногда изымаются из продажи из-за отдельных случаев
Токсических эффектов (17 препаратов в США за последние 8 лет)
- Можно ли этого избежать?
Проект по полногеномному поиску вариабельности (SNP) в связи с МФЗ и ответом на лекарства
10 млн SNP тысячи обследуемых
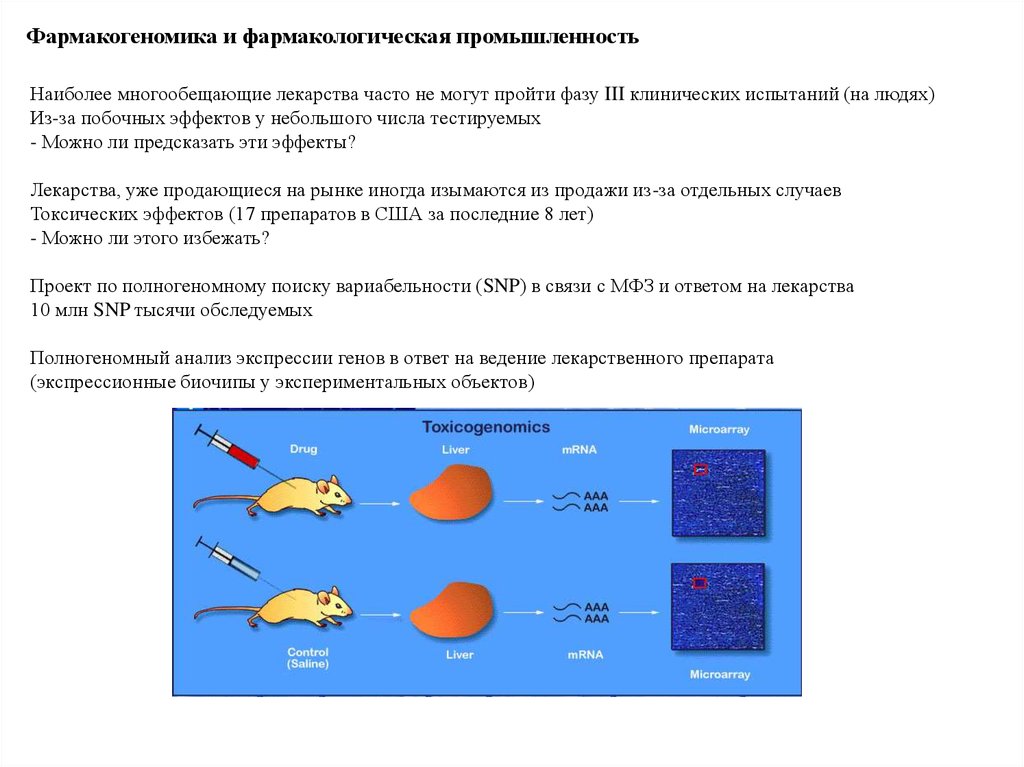
Полногеномный анализ экспрессии генов в ответ на ведение лекарственного препарата
(экспрессионные биочипы у экспериментальных объектов)


























 Медицина
Медицина








